Технология производства ортофосфатов натрия на основе экстракционной фосфорной кислоты из фосфоритов центральных кызылкумов
АКАДЕМИЯ НАУК РЕСПУБЛИКИ УЗБЕКИСТАН
ИНСТИТУТ ОБЩЕЙ И НЕОРГАНИЧЕСКОЙ ХИМИИ
УДК 661.635.12
На правах рукописи
МИРМУСАЕВА КАМОЛА САЙФУЛЛАЕВНА
ТЕХНОЛОГИЯ ПРОИЗВОДСТВА ОРТОФОСФАТОВ НАТРИЯ НА ОСНОВЕ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ ИЗ ФОСФОРИТОВ ЦЕНТРАЛЬНЫХ КЫЗЫЛКУМОВ
05.17.01 – технология неорганических веществ
А В Т О Р Е Ф Е Р А Т
диссертации на соискание ученой степени
кандидата технических наук
Ташкент – 2011
Работа выполнена на кафедре «Химическая технология неорганических веществ» Ташкентского химико-технологического института.
Научный руководитель: Доктор технических наук, доцент
Мирзакулов Холтура Чориевич
Официальные оппоненты: Доктор технических наук, профессор
Исмаилов Насрулла Патхуллаевич
Кандидат технических наук, доцент
Линкевич Владимир Антонович
Ведущая организация ОАО «Аmmofos-Maxam»
Защита состоится «___» ____________ 2011 года в «____» часов на заседании специализированного совета Д 015.13.01 при Институте общей и неорганической химии Академии наук Республики Узбекистан по адресу: 100170, г. Ташкент, ул. М. Улугбека, 77А. Факс (+99871) 262-79-90,
e-mail: [email protected]
С диссертацией можно ознакомиться
в Фундаментальной библиотеке Академии наук Республики Узбекистан
по адресу: 100170, г. Ташкент, ул. Муминова, 13
Автореферат разослан «___» __________ 2011 г.
Ученый секретарь
Специализированного Совета,
кандидат химических наук Ибрагимова М.А.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Президентом Республики Узбекистан И.А. Каримовым для преодоления последствий мирового экономического кризиса и минимизации воздействий возможных новых кризисов указываются действия по освоению новой конкурентоспособной продукции, наращиванию ее экспорта, расширению географии поставок, выходу на новые рынки. Одними из таких продуктов являются фосфаты натрия. Постановлением Президента Республики Узбекистан № ПП-1071 от 11.03.2009 г. «О программе мер по ускорению строительства и освоению производства новых видов химической продукции» предусматривается организация в Республике Узбекистан производства фосфата натрия и кормовых фосфатов. Другим постановлением Президента Республики Узбекистан № ПП-1306 от 23.03.2010 г. «О программе локализации производства готовой продукции, комплектующих изделий и материалов на основе промышленной кооперации на 2010 год» предусматривается производство фосфата натрия в 2010 г. в количестве 600 т. Однако вышеуказанные постановления не учитывают потребности страны в технических, кормовых и пищевых фосфатах натрия, которые пользуются спросом во многих отраслях промышленности и народного хозяйства.
Производство ортофосфатов натрия базируется на фосфорной кислоте. Производство термической фосфорной кислоты (ТФК) является дорогостоящим и непрерывно сокращается, а вместо неё в технологии квалифицированных марок пищевых и реактивных кислот используют более дешёвую, очищенную экстракционную фосфорную кислоту (ЭФК). Себестоимость ТФК примерно в три раза выше себестоимости очищенной ЭФК.
ЭФК, получаемая кислотным разложением фосфатного сырья, используется в основном, для производства удобрений и технических солей (порядка 87 % от общего выпуска). Тем не менее, ее можно и нужно использовать для получения не только технических фосфатов натрия, но и фосфатов натрия кормовой и пищевой квалификации. Часть технических и пищевых фосфатов натрия в Западной Европе и США уже производится на основе очищенной ЭФК. Эта же тенденция неизбежна и для Республики Узбекистан. Организация производства ортофосфатов натрия позволит обеспечить предприятия Республики импортозамещающим компонентом, использовать местное сырье, обеспечит создание новых рабочих мест.
Таким образом, исследования, направленные на освоение технологии получения ортофосфатов натрия из ЭФК на основе местного сырья, будут весьма востребованы.
Степень изученности проблемы. Производство кормовых и пищевых ортофосфатов натрия на территории стран СНГ базировалось и базируется на основе ТФК. Однако ее производство является весьма энергоемким, что в свете непрерывного роста цен на энергоресурсы приводит ко все большему и большему снижению рентабельности производства.
Существуют способы, основанные на получении кормовых ортофосфатов натрия из очищенной, с помощью органических растворителей, ЭФК (например, в диссертации Волковой В.В. очистка ЭФК осуществлялась трибутилфосфатом). Но данный способ является многостадийным и связан с использованием пожаровзрывоопасных органических растворителей.
В диссертационной работе Белкиной Е.И. (Санкт Петербург, 2004) предлагалась осадительная очистка ЭФК от фтора, мышьяка и прочих примесей. Последние предлагалось осаждать нейтрализацией ЭФК аммиаком, а фосфаты натрия предлагалось получать взаимодействием аммофосной пульпы с щелочью. Основными недостатками являются многостадийность и потребность в дополнительном оборудовании для улавливания и возврата аммиака, а также невозможность получения дигидро- и гидрофосфатов натрия.
Что касается изучения процесса кристаллизации дигидро-, гидро- и фосфата натрия, то детальное изучение этого процесса приведено в диссертации Никандрова М.И. (Нижний Новгород, 2005) лишь для фосфатов натрия, полученных из ТФК. Для ЭФК, да еще из фосфоритов Центральных Кызылкумов (ЦК), такие исследования практически не проводились.
Исследования по получению ортофосфатов натрия различной квалификации из ЭФК носят разрозненный характер и не позволяют создать готовую технологию. Кроме того, результаты известных исследований нельзя перенести на местное сырье в связи с сильным отличием их состава от изученных. Процесс получения ортофосфатов натрия из ЭФК фосфоритов ЦК совершенно не изучен.
Связь диссертационной работы с тематическими планами НИР. Работа выполнена в рамках прикладного проекта № 6-099 «Разработка технологии получения чистых солей фосфатов и полифосфатов натрия и аммония на основе экстракционной фосфорной кислоты Центральных Кызылкумов» на 2009-2011 г.
Цель исследования: физико-химическое обоснование и разработка технологии производства ортофосфатов натрия из ЭФК, полученной на основе фосфоритов ЦК, с установлением оптимальных параметров производства.
Задачи исследования. Из указанной цели исследований вытекает необходимость решения следующих задач:
- проведение литературного обзора по состоянию изученности процесса очистки ЭФК и получения на ее основе фосфатов натрия;
- анализ диаграммы растворимости системы Na2O-Р2О5-H2O с целью теоретического обоснования процесса;
- исследование процесса обессульфачивания ЭФК соединениями кальция;
- исследование процесса нейтрализации ЭФК соединениями натрия с целью ее очистки ее от ионов металлов, фтора и прочих примесей;
- изучение реологических свойств нейтрализованных пульп и растворов;
- изучение процесса отделения осадка от частично нейтрализованного раствора и разработка способа утилизация фосфатного шлама;
- изучение процесса донейтрализации очищенного раствора, полученного путем нейтрализации ЭФК соединениями натрия;
- установление влияния основных технологических параметров на показатели процесса кристаллизации и отделения ортофосфатов натрия;
- разработка материальных балансов производства фосфатов натрия;
- разработка технологической схемы производства фосфатов натрия;
- отработка параметров процесса производства фосфатов натрия;
- оценка экономической эффективности предлагаемых способов производства фосфатов натрия.
Объект и предмет исследования. Объектами исследования являются ЭФК из фосфоритов ЦК, фосфоритный концентрат Ташкура мытый обожженный (ФКТМО), фосфоритная мука Ташкура (ФМТ), карбонат, гидрокарбонат и гидроксид натрия, частично нейтрализованная ЭФК, фосфатный шлам, растворы фосфатов натрия, фосфаты натрия. Предметом исследований является технология производства ортофосфатов натрия на основе ЭФК из фосфоритов ЦК, позволяющая увеличить экспортный потенциал химической промышленности Узбекистана.
При выполнении применялись химический, рентгенографический, ИК-спектроскопический, термический, микроскопический методы исследования.
Основные положения, выносимые на защиту.
- выявленные оптимальные условия процесса обессульфачивания ЭФК из фосфоритов ЦК соединениями кальция;
- выявленные оптимальные условия процесса очистки обессульфаченной ЭФК из фосфоритов ЦК нейтрализацией соединениями натрия;
- выявленные оптимальные условия процесса кристаллизации ортофосфатов натрия, их составы и свойства;
- предложенная технологическая схема производства ортофосфатов натрия на основе ЭФК из фосфоритов ЦК.
Научная новизна. Установлены закономерности влияния технологических параметров на процесс обессульфачивания и очистки ЭФК из фосфоритов ЦК от сопутствующих примесей соединениями кальция и натрия соответственно. С привлечением физико-химических и инструментальных методов получены новые данные о составе образующегося фосфатного шлама и предложены пути его утилизации. Выявлены оптимальные технологические параметры процесса получения фосфатных солей натрия различной чистоты (в том числе и кормовой). Разработана высокоэффективная технология производства ортофосфатов натрия на основе местного сырья с учетом его свойств.
Научная и практическая значимость результатов исследований. Разработана технология получения ортофосфатов натрия на основе ЭФК из фосфоритов ЦК путем ее обесфторивания, обессульфачивания, частичной нейтрализации соединениями натрия, с отделением образующегося шлама, донейтрализации соединениями натрия, с последующей кристаллизацией готового продукта. Предложенная технология апробирована на модельной установке ОАО «Ammofos-Maxam», наработаны опытные партии продукта. Экономический эффект от производства 1 т готовой продукции в зависимости от продукта по сравнению с импортируемыми составляет 1,2-6,7 млн. сум.
Реализация результатов. На опытной установке ОАО «Ammofos-Maxam», имитирующей производственные условия, была отработана технология получения фосфатов натрия различной квалификации (технических и кормовых). Полученные данные легли в основу технологической схемы, материальных балансов, технологического регламента. Технический фосфат натрия на основе ЭФК из фосфоритов ЦК внедрен в производство в промышленном масштабе и выпущено 682 т продукта на сумму 1,289 млрд. сум.
Апробация работы. Основные положения диссертации представлены на: Научно-технической конференции профессорско-преподавательского состава, докторантов, аспирантов, научных сотрудников, магистрантов и студентов ТХТИ «Умидли кимёгарлар-2008» (Ташкент, 2008), Республиканской научно-технической конференции «Технологии переработки местного сырья и продуктов» (Ташкент, 2008), Республиканской научно-практической конференции «Актуальные проблемы химической технологии нефтегазовой промышленности» (Карши, 2009), Республиканской научно-технической конференции «Технологии переработки местного сырья и продуктов» (Ташкент, 2009), Республиканской научно-практической конференции «Кимёнинг долзарб муаммолари» (Самарканд, 2009), III Республиканской научно-практической конференции, посвященной 80-летию академика Ганиева А.Г. «Актуальные проблемы аналитической химии» (Термез, 2010), Международной научно-технической конференции «Современные техника и технологии горно-металлургической отрасли и пути их развития» (Навои, 2010), Республиканской научно-технической конференции «Актуальные проблемы инновационных технологий химической, нефтегазовой и пищевой промышленности» (Кунград, 2010), Республиканской научно-технической конференции «Разработка эффективной технологии получения минеральных удобрений и агрохимикатов нового поколения и применение их на практике» (Ташкент, 2010), Научно-практической конференции молодых ученых «Умидли кимёгарлар – 2011» (Ташкент, 2011), Научно-практической конференции «Актуальные проблемы химии и химической технологии» (Ургенч, 2011), на семинаре Специализированного совета Д 015.13.01 при Институте общей и неорганической химии АН РУз 09.06.2011 г.
Опубликованность результатов. По результатам работ опубликованы: 3 журнальные статьи, 15 тезисов и статей в сборниках научных трудов.
Объём и структура работы. Диссертация состоит из введения, пяти глав, заключения, списка использованной литературы и приложения. Работа изложена на 169 страницах компьютерного текста, включает 27 рисунков и 39 таблиц. Список использованной литературы состоит из 200 наименований.
Автор выражает благодарность к.т.н. Д.Д. Асамову за ценные консультации и помощь при выполнении диссертационной работы.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обосновывается актуальность работы, сформулирована цель и основные задачи исследования, отмечена научная и практическая значимость.
Первая глава представляет собой анализ литературы по состоянию вопроса применения ортофосфатов натрия, спроса на них, объемов их производства, очистки ЭФК от суспендированных и растворенных примесей, растворимости в системе Na2O–Р2О5–H2O, получения на основе ЭФК фосфатов натрия различной чистоты, приведены сведения по химическим и физико-химическим свойствам, на основе чего сформулированы задачи исследования.
Во второй главе описываются методики проведения экспериментов, выполнения химических анализов, определения физических свойств и проведения физико-химических исследований. Химический состав использованного в работе сырья приведен в табл. 1
Таблица 1
Химический состав использованного в работе сырья
| Реагент | Химический состав, мас. % | ||||||
| P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |
| ЭФК (исходная) | 18,31 | 2,32 | 0,31 | 1,12 | 1,36 | 0,93 | 1,25 |
| ЭФК № 1 (обесфторенная) | 20,45 | 2,65 | 0,35 | 1,20 | 1,32 | 0,90 | 0,21 |
| ЭФК № 2 (обесфторенная) | 14,45 | 1,50 | 0,35 | 0,85 | 0,65 | 0,18 | 0,15 |
| ЭФК № 3 (обесфторенная) | 24,62 | 3,17 | 0,42 | 1,43 | 1,58 | 1,08 | 0,25 |
| Оксид кальция | 0,00 | 0,52 | 91,73 | 4,52 | 0,11 | 0,21 | 0,01 |
| ФМТ | 19,24 | 2,34 | 44,07 | 0,97 | 1,05 | 0,67 | 2,20 |
| ФКТМО | 27,50 | 3,31 | 54,46 | 0,99 | 1,87 | 0,70 | 2,70 |
Третья глава посвящена исследованию процесса очистки ЭФК, которая заключается в обесфторивании (подробно изучено Хужамкуловым С.З.), обессульфачивании и ступенчатой нейтрализации с промежуточным отделением фосфатного шлама. При этом для обесфторивания используются маточные растворы фосфатов натрия, полученные при их кристаллизации или перекристаллизации, с содержанием избыточного количества примесей, которые негативно влияют на состав готового продукта. Такое ведение процесс позволяет увеличить выход готового продукта из сырья.
В качестве обессульфачивающих реагентов использовались оксид кальция, ФКТМО и ФМТ. Установлено, что независимо от реагента с увеличением его нормы степень обессульфачивания ЭФК возрастает (рис. 1).
Самое интенсивное возрастание степени обессульфачивания наблюдается в пределах нормы от 75 до 125 %. Самым эффективным реагантом является CaO, а ФМТ и ФКТМО по эффективности можно считать примерно одиноковыми. Тем не менее, использование ФКТМО является более предпочтительным ввиду его доступности. Кроме того, он также способствует некоторому увеличению содержания Р2О5 в ЭФК. Оптимальной нормой ФКТМО можно считать 150-200 %. При этом содержание SO3 в ЭФК снижается до 0,84-0,74 % мас.
  |  |
| Рис. 1. Влияние нормы реагента на степень удаления сульфат-ионов (1, 2, 3) и дикальцинации (4, 5, 6) из ЭФК с помощью: оксида кальция (1, 4), ФМТ (2, 5) и ФКТМО (3, 6) | Рис. 2. Влияние продолжительности обессульфачивания с ФКТМО на степень удаления сульфат-ионов (1, 2, 3) и дикальцинации (4, 5, 6) при температуре 20 °С (1, 4), 50 °С (2, 5) и 70 °С (3, 6) |
С увеличением температуры степень обессульфачивания с помощью ФКТМО (норма 150 % отн.) снижается (рис. 2), что объясняется увеличением растворимости сульфата кальция в ЭФК с повышением температуры. Период массовой кристаллизации при обессульфачивания составляет до 15 минут, затем прирост степени обессульфачивания замедляется, а после 45 минут практически останавливается. Следовательно, оптимальной является температура 20-50 °С, а продолжительность – 45 минут.
Что касается концентрации ЭФК, то с ее увеличением степень обессульфачивания увеличивается, что обясняется снижением растворимости гипса в растворе фосфорной кислоты с увеличением ее концентрации.
Исследование процесса отделения гипса от обессульфаченной ЭФК показало, что суспензия фосфогипса в ЭФК относится к хорошо отстаивающимся (справедливо лишь для СаО и ФКТМО). При использовании ФМТ скорость отстаивания резко снижается: в течение 6 часов она не превышает 65 % отн., а при использовании ФКТМО уже через 1 час достигает 75-93 % отн. Это же справедливо и для фильтрования. При использовании ФМТ скорость фильтрации по раствору не превышала 915 кг/м2·ч, а при использовании ФКТМО достигала 3660 кг/м2·ч.
При получении фосфатов натрия на получаемый продукт накладываются ограничения по содержанию основного вещества и примесей. Производство фосфатов натрия из ЭФК связано с переходом примесей в продукт, что приводит к ухудшению его качества.
В связи с этим, для получения фосфатов натрия высокого качества, были проведены исследования по частичной нейтрализации ЭФК карбонатом, гидроксидом и гидрокарбонатом натрия. С увеличением нормы натриевых соединений содержание всех компонентов в ЭФК снижается. При увеличении нормы соединений натрия более 100-110 % содержание примесных компонентов практически не изменяется.
 |  |
| 1 | 2 |
| Рис 3. Влияние нормы реагента на степень удаления примесей из ЭФК в осадок. | |
В очищенной ЭФК практически отсутствуют оксиды кальция, алюминия железа, а также фтор при норме натриевых соединений 100 % и более, а количества SO3 и MgO уменьшаются лишь в два раза (рис. 3). Полученный при нейтрализиции раствор дигидрофосфата натрия при норме 100 % имеет следующий состав, мас. %: Na2O – 9,14, P2O5 – 20,42, SO3 – 0,52, CaO – 0,091, MgO – 0,72, Al2O3 – 0,065, Fe2O3 – 0,016, F – 0,004. Использование карбоната натрия предпочтительнее из-за его низкой себестоимости.
Максимальное удаление примесных компонентов из ЭФК достигается при норме натриевых соединений 100-110 %, из которых как самый дешевый, предпочтительно, использовать карбонат натрия.
Что касается кинетики процесса нейтрализации, то реакция практически завершается при температуре 60 °С за 30 минут (при этом степень удаления примесей SO3 и MgO относительно меньше других компонентов и составляет 40 % и менее, а СаО, Al2O3, Fe2O3 и F – более 90 %), а при температуре 20 °С – за 60 минут.
Определены реологические характеристики и выведены уравнения регрессии значений для пульп, образующихся при нейтрализации ЭФК из фосфоритов ЦК гидроксидом и карбонатом натрия, а также жидкой фазы, полученной при отделении из вышеуказанных пульп выпавшего осадка. Установлено, что все они характеризуются хорошей транспортабельностью.
Исследование процесса отделения фосфатного шлама от очищенной ЭФК отстаиванием показало, что степень осветления пульпы существенно зависит от нормы карбоната натрия и времени отстаивания. С увеличением нормы карбоната натрия до 100-120 % от стехиометрии степень осветления достигает своего максимального значения, а затем начинает уменьшаться, что обясняется образованием большого количества очень мелких аморфных частиц осадка. Максимальная степень осветления пульпы – 71 % достигается при 100 %-ной норме технического карбоната натрия и времени отстаивания пульпы в течение 300 минут, что не может считаться приемлемым для технологических нужд.
Отделение фосфатного шлама фильтрованием является бесперспективным. Скорость фильтрации по осадку не превышает 32,13 кг/м2·час. При норме карбоната натрия 150 % при оптимальной температуре 60 °С скорость фильтрации даже меньше единицы – 0,58-0,63 кг/м2·час.
Отделение фосфатного шлама центрифугированием следует признать единственно приемлемым. Уже через 15 минут центрифугирования при температуре 80 °С величина соотношения Ж:Т в сгущенной пульпе уменьшается с 14,1-14,5 до значений, которые находится в пределах 1,6-2,0 (что можно считать максимально возможным), а при температуре 60 °С – только до 4,0- 5,0.
Данное явление можно объяснить на основе микроскопических исселедований: на снимке (рис. 4) видны различия в размере частиц, агломератов осадка, что еще раз подтверждает, что 100 %-ная норма технического карбоната натрия при нейтрализации предварительно обесфторенной и обессульфаченной ЭФК является оптимальной.
 |  |
| 1 | 2 |
| Рис. 4. Микроскопические снимки осадка, полученного при нейтрализации ЭФК Na2CO3 при норме, % отн.: 1 – 100, 2 – 200. | |
Глава четвертая диссертационной работы посвящена получению ортофосфатов натрия.
Результаты опытов по кристаллизации упаренных растворов дигидрата дигидрофосфата натрия приведены в табл. 2.
Основным фактором, влияющим на съем осадка с единицы фильтрующей поверхности, является скорость охлаждения растворов. С уменьшением скорости охлаждения раствора резко увеличивается съем осадка. С уменьшением скорости охлаждения растворов с 2,4 до 0,8 °С/час при всех параметрах съем осадка возрастает в среднем в 3,36-3,43 раза. Изменение концентрации и температуры раствора в пределах 52-58 % и 20,0-30,4 °С соответственно не оказывает заметного влияния на съем осадка. С уменьшением скорости охлаждения количество примесей SO3, CaO, MgO, Al2O3, Fe2O3 и F в продукте уменьшается примерно в два раза. Увеличение концентрации раствора свыше 52 % приводит к увеличению содержания примесей в готовом продукте. Аналогично проводили испытания при получении моногидрата дигидрофосфата натрия (скорость охлаждения регулировали начиная с 65 °С) и безводного дигидрофосфата натрия (скорость охлаждения регулировали начиная с 95 °С) приведены в (табл. 3).
Таблица 2
Кристаллизация дигидрата дигидрофосфата натрия
| Конц. р-ра, мас. % | Темпе- ратура, °С | Ско- рость охлаж., °С/час | Ж:Т | Съем осадка, кг/м2·ч | Химический состав продукта, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |||||
| Исходный | – | – | 13,77 | 30,77 | 0,80 | 0,14 | 1,085 | 0,0979 | 0,0241 | 0,0060 | ||
| 52 | 28,2 | 2,4 | 4,61 | 98 | 19,55 | 44,47 | 0,28 | 0,06 | 0,013 | 0,0012 | 0,0013 | 0,0007 |
| 1,6 | 4,59 | 170 | 19,55 | 44,58 | 0,20 | 0,04 | 0,010 | 0,0009 | 0,0011 | 0,0004 | ||
| 0,8 | 4,57 | 336 | 19,57 | 44,62 | 0,17 | 0,03 | 0,007 | 0,0006 | 0,0007 | 0,0002 | ||
| 20,0 | 2,4 | 2,63 | 140 | 19,49 | 44,47 | 0,25 | 0,08 | 0,020 | 0,0011 | 0,0012 | 0,0008 | |
| 1,6 | 2,65 | 239 | 19,51 | 44,55 | 0,20 | 0,06 | 0,015 | 0,0009 | 0,0010 | 0,0006 | ||
| 0,8 | 2,65 | 471 | 19,53 | 44,60 | 0,17 | 0,05 | 0,011 | 0,0007 | 0,0007 | 0,0005 | ||
| Исходный | – | – | 15,36 | 34,32 | 0,89 | 0,15 | 1,210 | 0,1092 | 0,0269 | 0,0067 | ||
| 58 | 30,4 | 2,4 | 1,72 | 163 | 19,50 | 44,33 | 0,38 | 0,10 | 0,023 | 0,0012 | 0,0014 | 0,0006 |
| 1,6 | 1,74 | 279 | 19,52 | 44,47 | 0,27 | 0,07 | 0,017 | 0,0011 | 0,0012 | 0,0005 | ||
| 0,8 | 1,75 | 550 | 19,54 | 44,52 | 0,24 | 0,06 | 0,013 | 0,0008 | 0,0009 | 0,0004 | ||
| 20,0 | 2,4 | 1,12 | 193 | 19,50 | 44,12 | 0,55 | 0,13 | 0,030 | 0,0013 | 0,0015 | 0,0008 | |
| 1,6 | 1,13 | 330 | 19,53 | 44,24 | 0,46 | 0,10 | 0,024 | 0,0012 | 0,0014 | 0,0007 | ||
| 0,8 | 1,14 | 650 | 19,54 | 44,30 | 0,42 | 0,09 | 0,021 | 0,0008 | 0,0010 | 0,0005 | ||
Таблица 3
Кристаллизация моногидрата и безводного дигидрофосфатов натрия
| Конц. р-ра, мас. % | Темпе- ратура, °С | Скорость охлажд-я, °С/час | Соотн. Ж:Т | Съем осадка, кг/м2·ч | Химический состав продукта, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |||||
| Кристаллизация моногидрата дигидрофосфата натрия | ||||||||||||
| Исходный | – | – | 15,89 | 35,50 | 0,92 | 0,16 | 1,252 | 0,1130 | 0,0278 | 0,0070 | ||
| 60 | 47,6 | 0,8 | 23,67 | 257 | 22,07 | 50,31 | 0,27 | 0,07 | 0,017 | 0,0008 | 0,0010 | 0,0004 |
| 40,8 | 0,8 | 12,19 | 442 | 22,09 | 49,97 | 0,57 | 0,11 | 0,026 | 0,0009 | 0,0012 | 0,0005 | |
| Исходный | – | – | 16,16 | 36,09 | 0,94 | 0,16 | 1,273 | 0,1149 | 0,0283 | 0,0071 | ||
| 61 | 49,1 | 0,8 | 12,57 | 413 | 22,06 | 50,27 | 0,30 | 0,08 | 0,020 | 0,0009 | 0,0011 | 0,0005 |
| 40,8 | 0,8 | 7,74 | 590 | 22,10 | 49,85 | 0,67 | 0,13 | 0,030 | 0,0009 | 0,0013 | 0,0005 | |
| Кристаллизация безводного дигидрофосфата натрия | ||||||||||||
| Исходный | – | – | 16,95 | 37,87 | 0,98 | 0,17 | 1,335 | 0,1205 | 0,0297 | 0,0074 | ||
| 64 | 73,9 | 0,8 | 19,53 | 529 | 25,45 | 57,60 | 0,75 | 0,19 | 0,045 | 0,0009 | 0,0010 | 0,0005 |
| 57,4 | 0,8 | 11,02 | 653 | 25,49 | 57,45 | 0,88 | 0,19 | 0,045 | 0,0009 | 0,0010 | 0,0005 | |
| Исходный | – | – | 17,48 | 39,05 | 1,01 | 0,17 | 1,377 | 0,1243 | 0,0306 | 0,0076 | ||
| 66 | 79,5 | 0,8 | 9,72 | 885 | 25,44 | 57,27 | 1,01 | 0,24 | 0,053 | 0,0011 | 0,0013 | 0,0006 |
| 57,4 | 0,8 | 6,12 | 962 | 25,45 | 57,16 | 1,11 | 0,25 | 0,053 | 0,0012 | 0,0013 | 0,0006 | |
Пульпа дигидрофосфата натрия фильтруется значительно лучше, чем при получении дигидрата и моногидрата дигидрофосфата натрия. Основным фактором, от которого зависит время фильтрации, является скорость охлаждения пульпы. При всех исследуемых параметрах процесса с уменьшением скорости охлаждения пульпы с 2,4 до 0,8 °С/час съем осадка с фильтра увеличивается почти в два раза. Уменьшение скорости охлаждения и температуры пульпы от 73,9 до 57,4 °С вызывает незначительное уменьшение количества выпавших в осадок примесей SO3, CaO, MgO, Al2O3, Fe2O3 и F.
Таким образом, оптимальными параметрами получения дигидрата дигидрофосфата натрия являются охлаждение исходного, нейтрализованного карбонатом натрия, раствора со скоростью не более 0,8 °С/час и концентрация раствора не более 52 %. При этом продукт полностью соответствует требованиям ГОСТ и ТУ (TSh), предъявляемым к кормовым и пищевым фосфатам.
С целью увеличения выхода Р2О5 в продукт и получения продукта, соответствующего требованиям нормативной документации, изучалось влияние повторного использования маточного раствора на состав получаемого продукта (дигидрата дигидрофосфата натрия). При этом маточный раствор после кристаллизации продукта с предыдущей стадии подвергали упариванию до заданной концентрации (табл. 4 и 5).
Таблица 4
Влияние повторного использования маточного раствора на состав получаемого продукта
| Стадия | Образец | Химический состав, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | ||
| 1 | Исходный | 15,36 | 34,32 | 0,891 | 0,153 | 1,210 | 0,1092 | 0,0269 | 0,0067 |
| Кристаллы | 19,54 | 44,52 | 0,236 | 0,056 | 0,013 | 0,0008 | 0,0009 | 0,0004 | |
| Раствор | 12,95 | 28,42 | 1,269 | 0,209 | 1,902 | 0,1720 | 0,0419 | 0,0104 | |
| 2 | Исходный | 15,54 | 34,33 | 1,441 | 0,238 | 2,140 | 0,1935 | 0,0472 | 0,0117 |
| Кристаллы | 19,47 | 44,27 | 0,411 | 0,111 | 0,035 | 0,0017 | 0,0021 | 0,0012 | |
| Раствор | 13,29 | 28,62 | 2,032 | 0,311 | 3,350 | 0,3037 | 0,0731 | 0,0177 | |
| 3 | Исходный | 15,78 | 34,31 | 2,307 | 0,355 | 3,773 | 0,3419 | 0,0824 | 0,0200 |
| Кристаллы | 19,34 | 43,17 | 1,250 | 0,285 | 0,105 | 0,0068 | 0,0092 | 0,0039 | |
| Раствор | 13,72 | 29,16 | 2,922 | 0,396 | 5,905 | 0,5368 | 0,1249 | 0,0294 | |
| 4 | Исходный | 15,81 | 34,32 | 3,267 | 0,450 | 6,469 | 0,5879 | 0,1373 | 0,0324 |
| Кристаллы | 18,01 | 39,69 | 3,520 | 0,632 | 0,872 | 0,0452 | 0,0354 | 0,0280 | |
| Раствор | 14,54 | 31,21 | 3,121 | 0,344 | 9,705 | 0,9017 | 0,1961 | 0,0349 | |
При трехкратном повторном использовании маточного раствора степень перехода примесей в кристаллы продукта относительно невысокая; с увеличением кратности повторного использования маточного раствора до четырех эти показатели резко увеличиваются. Это связано с тем, что в ходе повторного использования маточного раствора содержание примесей в продукте постепенно увеличивается. Выход Р2О5 в квалифицированный продукт (кормовой фосфат) составляет 81,63 %, а в пищевой фосфат – не более 43,68 %.
Оптимальным можно считать трехкратное повторное использование маточного раствора, при котором обеспечивается получение дигидрата дигидрофосфата натрия, отвечающего требованиям ГОСТ и ТУ (TSh).
С целью получения более концентрированного продукта кристаллогидраты дигидрофосфата натрия подвергались высушиванию до безводного состояния.
Таблица 5
Влияние повторностей использования маточного раствора на технологические показатели процесса
| Стадия | Соотно- шение Ж:Т | Время фильтр-и, мин | Съем осадка, кг/м2·ч | Степень перехода в кристаллы, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | ||||
| 1 | 1,73 | 0,78 | 589 | 46,59 | 47,52 | 9,69 | 13,41 | 0,40 | 0,25 | 1,25 | 2,18 |
| 2 | 1,74 | 0,71 | 531 | 45,71 | 47,06 | 10,41 | 17,02 | 0,60 | 0,32 | 1,62 | 3,74 |
| 3 | 1,72 | 0,68 | 561 | 45,04 | 46,26 | 19,92 | 29,48 | 1,02 | 0,73 | 4,11 | 7,17 |
| 4 | 1,73 | 1,25 | 420 | 41,71 | 42,37 | 39,46 | 51,47 | 4,94 | 2,82 | 9,45 | 31,68 |
Также выпариванию, с последующим высушиванием, подвергались и исходные растворы дигидрофосфата натрия, использованные для кристаллизации. В табл. 6 представленны данные по составу продукта, полученного высушиванием кристаллогидратов и выпариванием, с последующим высушиванием раствора дигидрофосфата натрия.
Таблица 6
Состав безводного дигидрофосфата натрия, полученного из кристаллогидратов и маточного раствора
| Образец | Химический состав, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |
| NaH2PO4·2H2O | 25,51 | 58,04 | 0,385 | 0,087 | 0,021 | 0,0010 | 0,0011 | 0,0007 |
| NaH2PO4·H2O | 25,52 | 57,64 | 0,714 | 0,137 | 0,032 | 0,0010 | 0,0014 | 0,0006 |
| NaH2PO4 | 25,47 | 57,31 | 0,995 | 0,223 | 0,049 | 0,0011 | 0,0012 | 0,0006 |
| Раствор NaH2PO4 | 24,79 | 55,39 | 1,438 | 0,247 | 1,953 | 0,1762 | 0,0434 | 0,0108 |
Как видно из табл. 6, все составы безводного дигидрофосфата натрия отвечают требованиям к кормовому фосфату, однако безводный дигидрофосфат натрия, полученный без кристаллизации, содержит неприемлемое с точки зрения пищевого фосфата количество примесей, и, кроме того, низкое содержание основного вещества.
Аналогично изучали и кристаллизацию из растворов гидрофосфата натрия (табл. 7). Влияние технологических параметров на показатели процесса аналогично как и в случае с дигидрофосфатом натрия.
Оптимальными технологическими параметрами получения дуодекагидрата гидрофосфата натрия являются температура – 20-27,7 °С, концентрация раствора – 22,0-30,0 %, скорость охлаждения – 1,6-4,8 °С/час, а для гептагидрата гидрофосфата натрия: температура – не более 35,4 °С, концентрация раствора – не менее 43,4 %, скорость охлаждения раствора – 1,6 °С/час, дигидрата гидрофосфата натрия: концентрация раствора – не менее 51,5 %, температура – не более 43,4 °С, скорость охлаждения раствора – не более 1,6 °С/час.
Таблица 7
Кристаллизация дуодекагидрата гидрофосфата натрия
| Конц. р-ра, мас. % | Темпе- ратура, °С | Ско- рость охлажд., °С/час | Ж:Т | Съем осадка, кг/м2·ч | Химический состав продукта, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |||||
| Кристаллизация дуодекагидрата гидрофосфата натрия | ||||||||||||
| Исходный | – | – | 10,14 | 11,00 | 0,24 | 0,04 | 0,35 | 0,0150 | 0,0060 | 0,0012 | ||
| 22,0 | 25,5 | 4,8 | 2,22 | 198 | 15,52 | 18,77 | 0,11 | 0,07 | 0,57 | 0,0018 | 0,0023 | 0,0003 |
| 3,2 | 2,24 | 453 | 15,62 | 18,83 | 0,11 | 0,06 | 0,54 | 0,0017 | 0,0021 | 0,0002 | ||
| 1,6 | 2,26 | 678 | 15,80 | 18,90 | 0,10 | 0,05 | 0,47 | 0,0015 | 0,0018 | 0,0002 | ||
| 20,0 | 4,8 | 1,32 | 198 | 15,41 | 18,67 | 0,17 | 0,08 | 0,61 | 0,0023 | 0,0031 | 0,0003 | |
| 3,2 | 1,32 | 455 | 15,42 | 18,68 | 0,16 | 0,07 | 0,61 | 0,0022 | 0,0028 | 0,0003 | ||
| 1,6 | 1,33 | 685 | 15,43 | 18,69 | 0,16 | 0,07 | 0,61 | 0,0019 | 0,0023 | 0,0002 | ||
| Исходный | – | – | 13,83 | 15,00 | 0,33 | 0,06 | 0,48 | 0,0204 | 0,0082 | 0,0016 | ||
| 30,0 | 27,7 | 4,8 | 0,59 | 265 | 15,41 | 18,64 | 0,21 | 0,07 | 0,61 | 0,0028 | 0,0038 | 0,0004 |
| 3,2 | 0,59 | 609 | 15,42 | 18,65 | 0,20 | 0,07 | 0,61 | 0,0025 | 0,0034 | 0,0004 | ||
| 1,6 | 0,59 | 917 | 15,42 | 18,65 | 0,20 | 0,07 | 0,61 | 0,0023 | 0,0029 | 0,0003 | ||
| 20,0 | 4,8 | 0,37 | 222 | 15,53 | 18,59 | 0,31 | 0,07 | 0,56 | 0,0038 | 0,0051 | 0,0005 | |
| 3,2 | 0,37 | 511 | 15,54 | 18,60 | 0,30 | 0,07 | 0,56 | 0,0036 | 0,0046 | 0,0005 | ||
| 1,6 | 0,37 | 768 | 15,54 | 18,61 | 0,29 | 0,07 | 0,56 | 0,0033 | 0,0038 | 0,0004 | ||
| Кристаллизация гептагидрата гидрофосфата натрия | ||||||||||||
| Исходный | – | – | 17,52 | 19,00 | 0,41 | 0,07 | 0,61 | 0,026 | 0,010 | 0,0021 | ||
| 38 | 40,1 | 1,6 | 2,70 | 714 | 20,04 | 25,21 | 0,29 | 0,15 | 1,31 | 0,004 | 0,005 | 0,0004 |
| 35,4 | 1,6 | 1,50 | 892 | 19,60 | 24,99 | 0,39 | 0,17 | 1,50 | 0,004 | 0,006 | 0,0004 | |
| Исходный | – | – | 20,01 | 21,70 | 0,47 | 0,09 | 0,70 | 0,030 | 0,012 | 0,0024 | ||
| 43,4 | 41,9 | 1,6 | 2,35 | 620 | 17,74 | 24,11 | 0,75 | 0,27 | 2,31 | 0,009 | 0,013 | 0,0010 |
| 35,4 | 1,6 | 0,85 | 950 | 20,24 | 25,05 | 0,66 | 0,15 | 1,28 | 0,008 | 0,011 | 0,0008 | |
| Кристаллизация дигидрата гидрофосфата натрия | ||||||||||||
| Исходный | – | – | 22,13 | 24,00 | 0,52 | 0,09 | 0,77 | 0,033 | 0,013 | 0,0026 | ||
| 48,0 | 63,3 | 1,6 | 8,88 | 568 | 30,36 | 37,31 | 0,32 | 0,16 | 1,48 | 0,004 | 0,006 | 0,0004 |
| 43,4 | 1,6 | 5,64 | 589 | 29,80 | 36,97 | 0,43 | 0,19 | 1,68 | 0,005 | 0,007 | 0,0005 | |
| Исходный | – | – | 28,10 | 30,47 | 0,66 | 0,12 | 0,98 | 0,041 | 0,017 | 0,0033 | ||
| 51,5 | 69,3 | 1,6 | 2,24 | 1455 | 32,20 | 38,16 | 0,25 | 0,09 | 0,78 | 0,003 | 0,004 | 0,0003 |
| 43,4 | 1,6 | 1,62 | 1250 | 32,57 | 38,24 | 0,33 | 0,08 | 0,64 | 0,004 | 0,005 | 0,0004 | |
С целью получения концентрированного продукта кристаллогидраты гидрофосфата натрия подвергались высушиванию до безводного состояния. Также выпариванию, с последующим высушиванием подвергались и исходные растворы гидрофосфата натрия, использованные для кристаллизации. В табл. 8 представленные данные по составу продукта, полученного высушиванием кристаллогидратов и выпариванием, с последующим высушиванием раствора гидрофосфата натрия. Как видно из табл. 8, все составы безводного гидрофосфата натрия отвечают требованиям к кормовому фосфату, однако безводный гидрофосфат натрия, полученный без кристаллизации, содержит неприемлемое с точки зрения пищевого фосфата количество примесей, и, кроме того, низкое содержание основного вещества. Наиболее чистым является гидрофосфат натрия, полученный из 2-х водного кристаллогидрата, что связано с большим соотношением Ж : Т при кристаллизации.
Таблица 8
Состав безводного гидрофосфата натрия, полученного из кристаллогидратов и маточного раствора
| Образец | Химический состав, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |
| Na2HPO4·12H2O | 43,34 | 52,20 | 0,621 | 0,189 | 1,630 | 0,0073 | 0,0085 | 0,0008 |
| Na2HPO4·7H2O | 41,51 | 52,13 | 1,091 | 0,338 | 2,900 | 0,0125 | 0,0177 | 0,0013 |
| Na2HPO4·2H2O | 43,36 | 52,29 | 0,529 | 0,186 | 1,614 | 0,0061 | 0,0083 | 0,0006 |
| Раствор Na2HPO4 | 45,60 | 49,45 | 1,076 | 0,194 | 1,586 | 0,0672 | 0,0270 | 0,0054 |
Наряду с дигидро- и гидрофосфатами натрия фосфат натрия также пользуется повышенным спросом. Для этого были проведены исследования по его получению на основе ЭФК из ФКТМО. Для получения фосфата натрия предлагается донейтрализация раствора гидрофосфата натрия гидроксидом натрия, отделение осадка, кристаллизация и отделение готового продукта.
В табл. 9 приведены результаты исследований по нейтрализации раствора гидрофосфата натрия гидроксидом натрия.
Таблица 9
Влияние технологических параметров на химический состав жидкой фазы при донейтрализации раствора гидрофосфата натрия гидроксидом натрия
| Время, мин | Темпера- тура, °С | Норма, % отн. | Химический состав, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |||
| 15 | 60 | 90 | 20,68 | 17,23 | 0,31 | 0,06 | 0,38 | 0,016 | 0,006 | 0,0012 |
| 100 | 22,55 | 16,81 | 0,29 | 0,06 | 0,35 | 0,014 | 0,005 | 0,0010 | ||
| 110 | 24,31 | 16,41 | 0,23 | 0,05 | 0,24 | 0,012 | 0,004 | 0,0008 | ||
| 80 | 90 | 20,71 | 17,33 | 0,28 | 0,06 | 0,31 | 0,018 | 0,007 | 0,0014 | |
| 100 | 22,57 | 16,88 | 0,24 | 0,05 | 0,25 | 0,015 | 0,005 | 0,0012 | ||
| 110 | 24,33 | 16,47 | 0,19 | 0,04 | 0,16 | 0,013 | 0,005 | 0,0010 | ||
| 30 | 60 | 80 | 18,71 | 17,76 | 0,34 | 0,06 | 0,38 | 0,022 | 0,008 | 0,0016 |
| 90 | 20,68 | 17,19 | 0,30 | 0,06 | 0,34 | 0,015 | 0,005 | 0,0011 | ||
| 100 | 22,54 | 16,72 | 0,26 | 0,05 | 0,28 | 0,012 | 0,004 | 0,0008 | ||
| 110 | 24,31 | 16,33 | 0,20 | 0,05 | 0,19 | 0,010 | 0,003 | 0,0007 | ||
| 120 | 26,00 | 15,99 | 0,15 | 0,03 | 0,05 | 0,009 | 0,003 | 0,0006 | ||
| 80 | 80 | 18,73 | 17,81 | 0,32 | 0,06 | 0,35 | 0,023 | 0,009 | 0,0018 | |
| 90 | 20,71 | 17,30 | 0,27 | 0,06 | 0,29 | 0,018 | 0,006 | 0,0014 | ||
| 100 | 22,56 | 16,84 | 0,23 | 0,05 | 0,22 | 0,015 | 0,005 | 0,0011 | ||
| 110 | 24,33 | 16,44 | 0,17 | 0,04 | 0,13 | 0,012 | 0,004 | 0,0010 | ||
| 120 | 26,02 | 16,09 | 0,07 | 0,02 | 0,01 | 0,011 | 0,004 | 0,0009 | ||
Процесс донейтрализации раствора заканчивается за 15 минут, дальнейшее увеличение продолжительности до 60 минут не приводит к какому-либо существенному изменению химического состава жидкой фазы. Увеличение температуры от 60 до 80 °С практически не влияет на химический состав жидкой фазы. С увеличением нормы гидроксида натрия уменьшается содержания примесей SO3, CaO, MgO, Al2O3, Fe2O3 и F. Наибольшие количества оксида натрия и наименьшие количества примесей содержатся соответственно при норме гидроксида натрия 110 и 120 % в температурном интервале 60-80 °С. При донейтрализации выпадает осадок, который необходимо отделить от жидкой фазы. При норме NaOH 90-110 %, температуре 60-80 °С, соотношении Ж:Т от 58,86 до 76,63, фильтруемость полученной пульпы имеет неудовлетворительные показатели по пульпе (172,52-398,40 кг/м2·ч), осадку (15,09-25,33 кг/м2·ч) и Р2О5 (70,79-264,08 кг/м2·ч). При центрифугировании соотношение Ж:Т в сгущенной части пульпы резко уменьшается в первые пять минут с 62-73 до 8,5-9,5. В дальнейшем, уменьшение соотношения Ж:Т, сильно замедляется и через 15 минут сгущение практически заканчивается при этом Ж:Т становится равным 0,4.
Таким образом, в результате приведенных исследований установлена возможность получения фосфата натрия донейтрализацией раствора гидрофосфата натрия гидроксидом натрия при следующих оптимальных условиях: продолжительность процесса – 30 минут, температура – 60 °С, норма гидроксида натрия – 100-110 %.
При изучении кристаллизации фосфата натрия использовался раствор с концентрацией 18,0 и 25,0 %, температура варьировалась от 20 до 37 °С, а скорость охлаждения – от 3,2 до 9,6 °С/час (табл. 10). Увеличение концентрации раствора от 18,0 до 25,0 % приводит к возрастанию съема осадка с единицы фильтрующей поверхности.
Также наблюдается некоторое увеличение содержания в продукте примесей SO3, CaO, MgO, Al2O3, Fe2O3 и F, но они находятся в допустимых пределах. С понижением температуры наблюдается уменьшение съема осадка. При всех значениях исследуемых параметров с уменьшением скорости охлаждения раствора от 9,6 до 3,2 °С/час увеличивается съем осадка с единицы фильтрующей поверхности. С уменьшением скорости охлаждения раствора от 9,6 до 6,4 °С/час происходит более резкое уменьшение времени фильтрации.
Таким образом, оптимальными условиями кристаллизации дуодекагидрата фосфата натрия являются: концентрация раствора – не менее 25,0 %, температура – 20 °С, скорость охлаждения раствора – не более 3,2 °С/час. Полученный продукт по составу полностью удовлетворяет требованиям ГОСТа к дуодекагидрату фосфата натрия.
При кристаллизации декагидрата фосфата натрия и дуодекагидрата фосфата натрия наблюдаются в основном одинаковые закономерности. Но в отличие от процесса кристаллизации дуодекагидрата фосфата натрия с увеличением концентрации исходного раствора наблюдается незначительное уменьшение содержания в продукте примесей SO3, CaO, MgO, Al2O3, Fe2O3 и F, но они также находится в допустимых пределах. Оптимальными условиями кристаллизации декагидрата фосфата натрия следует считать: концентрация исходного раствора – не более 34,0 %, температура – 54,0 °С, скорость охлаждения раствора – не более 3,2 °С/час.
Таблица 10
Кристаллизация фосфата натрия
| Конц. р-ра, % | Темпе- ратура, °С | Ско- рость охлажд., °С/час | Ж:Т | Съем осадка, кг/м2·ч | Химический состав продукта, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |||||
| Кристаллизация дуодекагидрата фосфата натрия | ||||||||||||
| Исходный | – | – | 10,44 | 7,79 | 0,11 | 0,02 | 0,10 | 0,0067 | 0,0023 | 0,0005 | ||
| 18,0 | 33,4 | 9,6 | 2,89 | 431 | 23,53 | 18,17 | 0,04 | 0,03 | 0,16 | 0,0007 | 0,0007 | 0,0001 |
| 6,4 | 2,89 | 1024 | 23,60 | 18,19 | 0,03 | 0,03 | 0,14 | 0,0006 | 0,0007 | 0,0001 | ||
| 3,2 | 2,90 | 1362 | 23,66 | 18,21 | 0,03 | 0,03 | 0,13 | 0,0006 | 0,0006 | 0,0000 | ||
| 20,0 | 9,6 | 1,89 | 313 | 23,45 | 18,12 | 0,06 | 0,04 | 0,18 | 0,0009 | 0,0010 | 0,0001 | |
| 6,4 | 1,90 | 744 | 23,49 | 18,13 | 0,05 | 0,04 | 0,17 | 0,0008 | 0,0009 | 0,0001 | ||
| 3,2 | 1,90 | 990 | 23,53 | 18,15 | 0,05 | 0,03 | 0,16 | 0,0007 | 0,0008 | 0,0001 | ||
| Исходный | – | – | 14,50 | 10,82 | 0,15 | 0,03 | 0,14 | 0,0094 | 0,0032 | 0,0007 | ||
| 25,0 | 37,0 | 9,6 | 1,22 | 489 | 23,13 | 17,96 | 0,11 | 0,06 | 0,27 | 0,0015 | 0,0019 | 0,0002 |
| 6,4 | 1,23 | 1161 | 23,17 | 17,98 | 0,10 | 0,06 | 0,26 | 0,0014 | 0,0017 | 0,0001 | ||
| 3,2 | 1,23 | 1546 | 23,23 | 18,01 | 0,10 | 0,05 | 0,24 | 0,0012 | 0,0015 | 0,0001 | ||
| 20,0 | 9,6 | 0,84 | 320 | 23,12 | 17,92 | 0,16 | 0,06 | 0,26 | 0,0021 | 0,0026 | 0,0002 | |
| 6,4 | 0,84 | 760 | 23,13 | 17,93 | 0,15 | 0,06 | 0,26 | 0,0019 | 0,0024 | 0,0002 | ||
| 3,2 | 0,84 | 1012 | 23,14 | 17,93 | 0,15 | 0,06 | 0,26 | 0,0017 | 0,0019 | 0,0002 | ||
| Кристаллизация декагидрата фосфата натрия | ||||||||||||
| Исходный | – | – | 19,72 | 14,72 | 0,20 | 0,04 | 0,19 | 0,0127 | 0,0043 | 0,0010 | ||
| 34,0 | 66,4 | 3,2 | 2,06 | 921 | 24,64 | 19,37 | 0,29 | 0,12 | 0,54 | 0,0034 | 0,0042 | 0,0004 |
| 54,0 | 3,2 | 1,24 | 1155 | 25,26 | 19,57 | 0,33 | 0,08 | 0,35 | 0,0041 | 0,0045 | 0,0004 | |
| Исходный | – | – | 22,97 | 17,14 | 0,24 | 0,05 | 0,23 | 0,0148 | 0,0050 | 0,0011 | ||
| 39,6 | 69,5 | 3,2 | 0,62 | 1340 | 25,47 | 19,80 | 0,14 | 0,07 | 0,32 | 0,0017 | 0,0021 | 0,0002 |
| 54,0 | 3,2 | 0,41 | 1422 | 25,44 | 19,73 | 0,21 | 0,07 | 0,32 | 0,0025 | 0,0028 | 0,0002 | |
Как и в случае с кислыми солями для получения концентрированного продукта кристаллогидраты фосфата натрия подвергались высушиванию до безводного состояния. Также выпариванию, с последующим высушиванием, подвергались и исходные растворы фосфата натрия, использованные для кристаллизации. В табл. 11 представленные данные по составу продукта, полученного высушиванием кристаллогидратов и выпариванием, с последующим высушиванием раствора фосфата натрия. Все составы безводного фосфата натрия отвечают требованиям к кормовому фосфату, однако безводный гидрофосфат натрия, полученный без кристаллизации, содержит неприемлемое с точки зрения пищевого фосфата количество примесей, и, кроме того, низкое содержание основного вещества. Наиболее чистым является фосфат натрия, полученный из 12-водного кристаллогидрата, что связано с условиями кристаллизации, обеспечивающими получение качественного продукта.
Таблица 11
Состав безводного фосфата натрия, полученного из кристаллогидратов и маточного раствора
| Образец | Химический состав, мас. % | |||||||
| Na2O | P2O5 | SO3 | CaO | MgO | Al2O3 | Fe2O3 | F | |
| Na3PO4·12H2O | 54,80 | 42,36 | 0,230 | 0,106 | 0,495 | 0,0028 | 0,0032 | 0,0004 |
| Na3PO4·10H2O | 54,39 | 42,16 | 0,576 | 0,156 | 0,711 | 0,0071 | 0,0078 | 0,0006 |
| Раствор Na3PO4 | 55,39 | 41,33 | 0,567 | 0,123 | 0,545 | 0,0357 | 0,0121 | 0,0027 |
Глава пятая посвящена разработке технологической схемы, материального баланса, оценке технико-экономической целесообразности организации производства.
Технологическая схема производства ортофосфатов натрия представлена на рис. 6 (стадия очистки ЭФК и кристаллизации дигидрофосфатов натрия) и рис. 7 (стадия кристаллизации гидрофосфатов и фосфатов натрия).
Обесфторенная ЭФК (с концентрацией 18-21 % Р2О5) из хранилища ЭФК (поз. 1) при температуре 60-80 °С насосом (поз. 2) подается в реактор обессульфачивания (поз. 3), куда из бункера (поз. 4) ленточным дозатором (поз. 5) подается ФКТМО. При этом проводится обессульфачивание ЭФК при соотношении СаО : SO3 = 1,2-1,5 : 1,0 в течение 30-60 мин. Из реактора обессульфачивания пульпа подается в отстойник-сгуститель (поз. 6), где она сгущается в течение 30-60 мин. Затем сгущенная часть (соотношение Ж:Т = 5-7 : 1) разделяется фильтрованием на ленточном вакуум-фильтре (поз. 7). Осветленная и отфильтрованная обессульфаченная ЭФК направляется в хранилище очищенной ЭФК (поз. 8). Обесфторенная и обессульфаченная ЭФК насосом (поз. 9) перекачивается в реактор-нейтрализатор (поз. 10), где она нейтрализуется при 60-80 °С карбонатом натрия, подаваемым из бункера (поз. 11) ленточным дозатором (поз. 12), до соотношения Na2О : Р2O5 = 1,00-1,05 : 1,0. Продолжительность процесса - 30-60 мин. Фосфатный шлам отделяется центрифугированием в центрифуге (поз. 13). Соотношение Ж:Т в сгущенной части пульпы составляет 2,5-3,0 : 1. Во избежание потерь Р2О5 фосфатный шлам прокаливается при температуре 300-350 °С с получением технического полифосфата натрия, необходимого для горнорудной промышленности.
Раствор дигидрофосфата натрия из хранилища (поз. 14) направляется в выпарной аппарат (поз. 16) с принудительной циркуляцией (поз. 18) и выносной греющей камерой (поз. 17), где упаривается при температуре 110-120 °С до концентраций, обеспечивающих получение, после охлаждения, кристаллогидратов с заданным количеством молекул воды: NaH2PO4 – 64-66 %, NaH2PO4·Н2О – 59-61 %, NaH2PO4·2Н2О – 52-58 %. При производстве технических фосфатов натрия пульпа после упарки направляется в БГС для сушки (на схеме не указано).
Раствор дигидрофосфата натрия охлаждается в кристаллизаторе (поз. 19) со скоростью 0,8-1,2 °С / час до температур, обеспечивающих кристаллизацию кристаллогидратов с заданным количеством молекул воды: безводного NaH2PO4 – 58-60 °С, моногидрата NaH2PO4·Н2О – 41-43 °С, дигидрата NaH2PO4·2Н2О – 20-25 °С. При этом обеспечивается кристаллизация крупных, хорошо фильтрующихся кристаллов. Соотношение Ж:Т в конечной суспензии составляет 6-8 : 1. Полученные кристаллы отделяются на вакуум-фильтре (поз. 20) и высушиваются при температуре 30-40 °С до влажности 0,5-1,0 % (не указано). Маточный раствор собирается в сборнике (поз. 21), откуда насосом (поз. 22) перекачивается в хранилище раствора дигидрофосфата натрия (поз. 14).
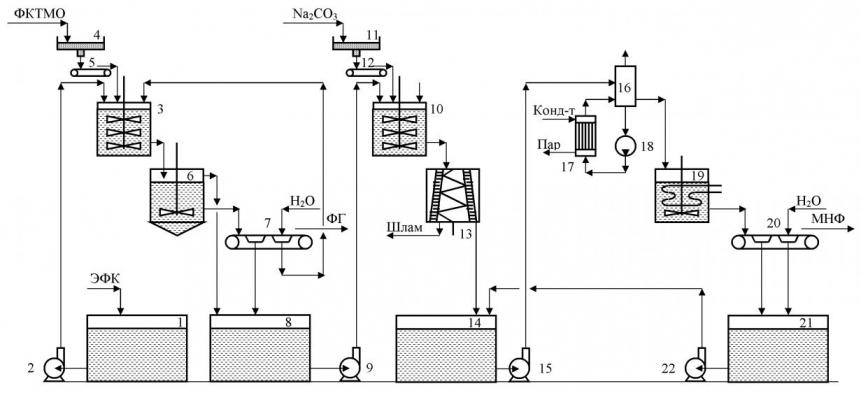
Рис. 6. Принципиальная технологическая схема очистки ЭФК и кристаллизации дигидрофосфатов натрия

Рис. 7. Принципиальная технологическая схема получения гидрофосфатов и фосфатов натрия
При получении гидрофосфата и фосфата натрия раствор дигидрофосфата натрия из сборника (поз. 14) насосом (поз. 15) перекачивается в сборник (поз. 23) откуда насосом (поз. 24) направляется на донейтрализацию в реактор-донейтрализатор (поз. 27), куда из бункера (поз. 25) через ленточный весовой дозатор подается: при получении гидрофосфата натрия карбонат натрия, при получении фосфата натрия гидроксид натрия. При получении гидрофосфата натрия раствор дигидрофосфата натрия донейтрализуется до соотношения Na2О : Р2O5 = 2,00-2,10 : 1,0, фосфата натрия – 3,06-3,15 : 1,0. Температура процесса нейтрализации – 60-80 °С, продолжительность – 15-30 мин. Образовавшийся шлам отделяется в центрифуге (поз. 27).
Раствор собирается в сборнике (поз. 28), откуда он направляется на упарку (поз. 30-32), где упаривается при температуре 110-120 °С до концентраций, обеспечивающих получение после охлаждения кристаллогидратов с заданным количеством молекул воды: Na2HPO4·2Н2О – 49-52 %, Na2HPO4·7Н2О – 40-43 %, Na2HPO4·12Н2О – 27-30 %.
Упаренный раствор гидрофосфата натрия охлаждается со скоростью 1,5-2,5 °С/час в кристаллизаторе (поз. 33) до температур, обеспечивающих кристаллизацию кристаллогидратов с заданным количеством молекул воды: Na2HPO4·2Н2О – 48-51 °С, Na2HPO4·7Н2О – 35-38 °С, Na2HPO4·12Н2О – 20-23 °С. При этом обеспечивается кристаллизация крупных, хорошо фильтрующихся кристаллов, отделение которых осуществляется на ленточном вакуум-фильтре (поз. 34). Соотношение Ж:Т в конечной суспензии составляет (2,0-2,5) : 1. Полученные кристаллы высушиваются при температуре 30-40 °С до влажности 0,5-1,0 %.Концентрация раствора фосфата натрия корректируется до концентраций, обеспечивающих получение после охлаждения кристаллогидратов с заданным количеством молекул воды: декагидрата Na3PO4·10Н2О – 36-39 %, додекагидрата Na3PO4·12Н2О – 20-25 %.
Раствор фосфата натрия охлаждается со скоростью 3-4 °С/час до температур, обеспечивающих кристаллизацию: декагидрата Na3PO4·10Н2О – 55-60 °С, додекагидрата Na3PO4·12Н2О – 20-25 °С. При этом обеспечивается кристаллизация крупных, хорошо фильтрующихся кристаллов. Соотношение Ж:Т в конечной суспензии составляет (1,0-1,5) : 1. Полученные кристаллы высушиваются при температуре 30-40 °С до влажности 0,5-1,0 %.
Маточный раствор собирается в сборнике (поз. 35), откуда насосом (поз. 36) перекачивается в хранилище раствора фосфата натрия (поз. 28). Кратность использования маточного раствора следует ограничить до 2-3 раз. Затем маточный раствор следует направить на стадию обесфторивания ЭФК.
Предварительные технико-экономические расчеты показывают, что полученный экономический эффект от производства 1 т готовой продукции в зависимости от марки по сравнению с импортируемыми составляет 1233,92-6677,52 тыс. сум в зависимости от продукта.
ЗАКЛЮЧЕНИЕ
- Проведенный патентно-литературный поиск, экспериментальные исследования и анализ полученных данных позволили разработать технологию производства солей ортофосфатов натрия технической, кормовой и пищевой чистоты на основе местного сырья, с привязкой к действующим производствам.
- Исследован процесс обессульфачивания ЭФК из фосфоритов ЦК оксидом кальция, ФМТ и ФКТМО. Оптимальными условиями следует считать норму ФКТМО – 150-200 %, температуру обессульфачивания 50-70 °С, время обссульфачивания 45-60 мин. При этом достигается высокая степень обессульфачивания.
- Образующийся фосфогипс хорошо отделяется отстаиванием (для снижения необходимой площади фильтрации) и фильтрацией (для снижения потерь Р2О5) с фосфогипсом. Полученный фосфогипс, содержащий неразложенный фосфорит, рекомендуется направлять в цех получения ЭФК для доразложения, использовать в качестве затравок для лучшей кристаллизации фосфогипса. Имеющиеся примеси солей натрия обеспечивают относительно больший переход фтора в твердую фазу.
- Исследован процесс нейтрализации обесфторенной и обессульфаченной ЭФК карбонатом, гидрокарбонатом и гидроксидом натрия. Установлено, что в зависимости от нормы реагента степень перехода в осадок CaO, Al2O3, Fe2O3 и F достигает 95-99 %, а SO3 и MgO не превышает 45 %. Наиболее оптимальным реагентом по осаждающей способности и цене является карбонат натрия.
- Изучение процесса отделения фосфатного шлама показало, что единственным технологически приемлемым способом является центрифугирование, которое позволяет достичь соотношения Ж:Т в сгущенной части (2-3) :1 уже за 15 минут.
- Изучены реологические свойства неосветленных и осветленных пульп, образующихся при нейтрализации ЭФК соединениями натрия. Показано, что эти растворы могут транспортироваться перекачивающими насосами без затруднений.
- Исследован процесс кристаллизации растворов фосфатов натрия. Установлены оптимальные параметры, обеспечивающие кристаллизацию крупных, хорошо фильтрующихся кристаллов. Установлено, что скорость охлаждения растворов дигидрофосфата натрия не должна превышать 0,8-1,0 °С/час, гидрофосфата натрия не должна превышать 1,5-2,0 °С/час, фосфата натрия не должна превышать 3,2-4,5 °С/час.
- Разработаны технологические схемы и составлены материальные балансы производства фосфатов натрия на основе местного сырья. В условиях ОАО «Ammofos-Maxam» проведены испытания с выпуском опытной партии продукции. Качество получаемых фосфатов натрия по содержанию основного вещества и примесей соответствует требованиям к кормовым фосфатам.
- Производство технического фосфата натрия на основе ЭФК из фосфоритов ЦК внедрено в производство на ОАО «Ammofos-Maxam» и в 2008-2010 гг. выпушено 682 т тринатрийфосфата на сумму 1,289 млрд сум.
- Экономический эффект от производства 1 т готовой продукции в зависимости от марки по сравнению с импортируемыми составляет 1233,92-6677,52 тыс. сум.
СПИСОК ОПУБЛИКОВАННЫХ РАБОТ:
- Мирмусаева К.С., Гиниятуллина Р.И., Бардин С.В., Асамов Д.Д., Мирзакулов Х.Ч. Контроль процесса нейтрализации экстракционной фосфорной кислоты гидрокарбонатом натрия / Умидли кимёгарлар-2008: Труды научно-технической конференции. – 8-11 апреля 2008. – Ташкент (Узбекистан), 2008. – С. 97-98.
- Мирмусаева К.С. Мирзакулов Х.Ч., Асамов Д.Д., Бардин С.В. Разработка технологии получения фосфатных солей натрия на основе экстракционной фосфорной кислоты из термоконцентрата Центральных Кызылкумов / Технологии переработки местного сырья и продуктов. Сборник трудов Республиканской научно-технической конференции ТХТИ. ТПМСП-2008. – 13-14 ноябрь, 2008. – Ташкент (Узбекистан), 2008. – С. 147-149.
- Хужамкулов С.З., Мирмусаева К.С., Эргашев Ж.Ж., Асамов Д.Д., Мирзакулов Х.Ч. Обессульфачивание экстракционной фосфорной кислоты из термоконцентрата Центральных Кызылкумов / Актуальные вопросы в области технических и социально-экономических наук: Республиканский межвузовский сборник научных трудов. – Ташкент (Узбекистан), 2009. – С. 43-45
- Мирмусаева К.С., Асамов Д.Д., Эргашев Ж.Ж., Шамаев Б.Э., Мирзакулов Х.Ч. Исследование процесса нейтрализации экстракционной фосфорной кислоты из обожженного концентрата фосфоритов Ташкура карбонатом натрия / Актуальные вопросы в области технических и социально-экономических наук: Республиканский межвузовский сборник научных трудов. – Ташкент (Узбекистан), 2009. – С. 110-111
- Мирмусаева К.С., Улугбердиева З.Х., Ахмедов З.А., Асамов Д.Д., Мирзакулов Х.Ч. Исследование процесса нейтрализации экстракционной фосфорной кислоты из термоконцентрата фосфоритов Центральных Кызылкумов карбонатом натрия / Актуальные проблемы химической технологии нефтегазовой промышленности: Материалы республиканской научно-практической конференции. – 24-25 апреля, 2009. – Карши (Узбекистан), 2009. – С. 91-93
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Реологические свойства растворов фосфатов натрия из экстракционной фосфорной кислоты / Технологии переработки местного сырья и продуктов: Сборник трудов республиканской научно-технической конференции. – 22-23 октября, 2009. – Ташкент (Узбекистан), 2009. – С. 150-151
- Мирмусаева К.С., Мирзакулов Х.Ч. Состав жидкой и твердой фаз при нейтрализации экстракционной фосфорной кислоты Ташкура гидрокарбонатом натрия / Кимёнинг долзарб муаммолари: Сборник трудов республиканской научно-практической конференции. – 6-7 ноября, 2009. – Ташкент (Узбекистан), 2009. – С. 61
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч., Садыков Б.Б., Волынскова Н.В. Реологические свойства пульп и растворов при нейтрализации экстракционной фосфорной кислоты гидроксидом, гидрокарбонатом и карбонатом натрия // Кимевий технология назорат ва бошкарув. – Ташкент, 2010. – № 1. – С. 24-28
- Мирмусаева К.С., Махкамов Б.А., Асамов Д.Д., Мирзакулов Х.Ч. Состав жидкой фазы, образующейся при нейтрализации экстракционной фосфорной кислоты соединениями натрия / Актуальные проблемы аналитической химии: Сборник трудов III Республиканской научно-практической конференции, посвященной 80-летию академика Ганиева А.Г. – 21-23 апреля, 2010. – Термез (Узбекистан), 2010. – С. 225-226
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Изучение процесса отделения фосфатного шлама, образующегося при нейтрализации экстракционной фосфорной кислоты Ташкура солями натрия / Современные техника и технологии горно-металлургической отрасли и пути их развития: Сборник трудов Международной научно-технической конференции. – 12-14 мая, 2010. – Навои (Узбекистан), 2010. – С. 138-139
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Оригинальная технология производства фосфатов натрия из экстракционной фосфорной кислоты Центральных Кызылкумов / Актуальные проблемы инновационных технологий химической, нефтегазовой и пищевой промышленности. – 28-29 октября 2010. – Кунград, 2010. – С. 156-157
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Нейтрализация экстракционной фосфорной кислоты карбонатом натрия / Разработка эффективной технологии получения минеральных удобрений и агрохимикатов нового поколения и применение их на практике: сборник материалов Республиканской научно-технической конференции. – 25-26 ноября 2010. – Ташкент, 2010. – С. 103-106
- Мирмусаева К.С., Улугбердиева З.Х., Асамов Д.Д., Мирзакулов Х.Ч. Обессульфачивание экстракционной фосфорной кислоты для получения кормовых и пищевых фосфатов / Разработка эффективной технологии получения минеральных удобрений и агрохимикатов нового поколения и применение их на практике: сборник материалов Республиканской научно-технической конференции. – 25-26 ноября 2010. – Ташкент, 2010. – С. 106-109
- Мирмусаева К.С., Асамов Д.Д., Бардин С.В., Мирзакулов Х.Ч., Садыков Б.Б., Волынскова Н.В. Нейтрализация очищенной экстракционной фосфорной кислоты из фосфоритов Ташкура гидрокарбонатом и гидроксидом натрия Кимё ва кимёвий технология. – Ташкент, 2011. – № 1. – С. 7-10
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Исследование процесса получения тринатрийфосфата / Ал-Хоразмий номидаги Урганч Давлат университети. Кимё ва кимё-технология- нинг долзарб муаммолари. Респ. илмий-амалий конф. материаллари тўплами. I том. – Урганч, 2011. – 53-54 б.
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч., Садыков Б.Б., Волынскова Н.В. Исследование процесса нейтрализации очищенной экстракционной фосфорной кислоты из фосфоритов Ташкура карбонатом натрия // Кимевий технология назорат ва бошкарув. – Ташкент, 2011. – № 2. – С. 14-20
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Изучение процесса получения дигидрата дигидрофосфата натрия из экстракционной фосфорной кислоты Ташкура / Актуальные вопросы в области технических и социально-экономических наук. Республиканский межвузовский сборник. – Ташкент, 2011. – С. 116-118
- Мирмусаева К.С., Асамов Д.Д., Мирзакулов Х.Ч. Исследование возможности повторного использования маточных растворов для получения квалифицированного дигидрофосфата натрия / Актуальные вопросы в области технических и социально-экономических наук. Республиканский межвузовский сборник. – Ташкент, 2011. – С. 119-120
Техника фанлари номзоди илмий даражасига талабгор Мирмусаева Камола Сайфуллаевнанинг 05.17.01 – ноорганик моддалар технологияси ихтисослиги бўйича «Марказий изилум фосфоритидан олинган экстракцион фосфор кислотаси асосида натрий ортофосфат тузларини ишлаб чиариш технологияси» мавзусидаги диссертациясининг
РЕЗЮМЕСИ
Таянч сўзлар: Экстракцион фосфор кислотаси, фосфорит уни ва концентрати, натрий карбонат, гидрокорбонат ва гидроксиди, фосфат шлами, натрий фосфат эритмаси, натрий фосфат тузлари, нейтраллаш, ажратиш, булатиш, кристалланиш, физик-кимёвий хоссалар.
Тадиот объектлари: экстракцион фосфор кислотаси, фосфорит уни, аммиак, натрий карбонат, гидрокарбонат ва гидроксиди.
Ишнинг масади: Мааллий фосфорит хом-ашёси асосида олинган экстракцион фосфор кислотасидан натрий ортофосфат тузларини ишлаб чиаришнинг мабул омилларини ўрнатиш билан технологиясини яратиш ва физик-кимёвий асослаш.
Тадиот усуллари: Кимёвий, рентгенофазали, ИК-спектроскопик ва термик талил.
Олинган натижалар ва уларнинг янгилиги: Марказий изилум фосфоритидан олинган экстракцион фосфор кислотасини ўшимчалардан тозалаш жараёнига технологик параметрлар таъсири онунияти ўрганилди, техник, озуабоп ва ози-оват саноати учун натрий ортофосфат технологияси жараёнининг мабул параметрлари аниланди ва натрий фосфат тузларини олишнинг юори самарали технологияси ишлаб чиилди. Физик-кимёвий ва инструментал усулларни ўллаб осил бўлган фосфат шламлари таркиби аида янги маълумотлар олинди ва уларни утилизация илиш йўллари танланди.
Амалий аамияти: Бажарилган илмий тадиот натижалари Марказий изилум фосфоритидан олинган экстракцион фосфор кислотаси асосида юори техник-итисодий кўрсаткичларга эга бўлган техник, озуабоп ва ози-оват саноати учун натрий ортофосфат тузлари олиш технологиясини яратиш учун илмий асос бўлди.
Татби этиш даражаси ва итисодий самарадорлик: Таклиф этилаётган технология “Аммофос-Максам” ОАЖ модель ускунасида синовдан ўтган, техник, озаабоп ва ози-оват саноати учун натрий ортофосфат тузларининг тажриба намунаси ишлаб чиарилди. Олинган маълумотлар асосида принципиал технологик схема ва технологик регламентлар яратилди. Техник итисодий хисоблар импорт орали олинаётган натрий ортофосфатлар билан солиштирганда ар бир тонна натрий ортофосфат тузлари масулот турларига мос равишда 1,2 - 6,7 млн. сўмгача итисодий фойда беришини кўрсатди. Техник учнатрийфосфат «Ammofos-Maxam» ОАЖда ишлаб чиаришга жорий илинган ва 2008-2010 йилларда 1.289 млрд. сўмлик 682 т. учнатрийфосфат ишлаб чиарилди.
ўлланиш соаси: кимё саноати, хал хўжалиги.
РЕЗЮМЕ
диссертации Мирмусаевой Камолы Сайфуллаевны на тему: «Технология производства ортофосфатов натрия на основе экстракционной фосфорной кислоты из фосфоритов Центральных Кызылкумов» на соискание ученой степени кандидата технических наук по специальности 05.17.01 – технология неорганических веществ.
Ключевые слова: экстракционная фосфорная кислота, фосфоритная мука и концентрат, карбонат, гидрокарбонат и гидроксид натрия, фосфатный шлам, растворы фосфатов натрия, фосфаты натрия, нейтрализация, отделение, упаривание, кристаллизация, физико-химические свойства.
Объекты исследования: экстракционная фосфорная кислота, фосфоритная мука, карбонат, гидрокарбонат и гидроксид натрия,
Цель работы: физико-химическое обоснование и разработка технологии ортофосфатов натрия из экстракционной фосфорной кислоты, полученной на основе местного фосфатного сырья, с установлением оптимальных параметров производства.
Методы исследования: химический, рентгенофазовый, ИК-спектроскопический, термический, микроскопический.
Полученные результаты и их новизна: установлены закономерности влияния технологических параметров на процесс очистки экстракционной фосфорной кислоты из фосфоритов Центральных Кызылкумов от сопутствующих примесей; выявлены оптимальные технологические параметры процесса получения фосфатных солей натрия различной квалификации и разработана высокоэффективная технология производства ортофосфатов натрия. С привлечением физико-химических методов получены новые данные о составе образующегося фосфатного шлама и указаны пути его утилизации.
Практическая значимость: результаты выполненных исследований стали научной основой для создания технологии производства фосфатов натрия различной квалификации с высокими технико-экономическими показателями на основе экстракционной фосфорной кислоты из фосфоритов Центральных Кызылкумов.
Степень внедрения и экономическая эффективность: предложенная технология апробирована на модельной установке ОАО «Ammofos-Maxam», наработаны опытные партии технических и кормовых фосфатов натрия. Полученные данные легли в основу создания принципиальной технологической схемы и технологического регламента. Экономический эффект от производства 1 т готовой продукции в зависимости от марки по сравнению с импортируемыми составляет 1,2-6,7 млн. сум в зависимости от продукта. Производство технического тринатрийфосфат внедрено в производство на ОАО «Ammofos-Maxam» и в 2008-2010 гг. выпушено 682 т тринатрийфосфата на сумму 1,289 млрд. сум.
Область применения: Химическая промышленность, народное хозяйство.
RESUME
Thesis of Kamola Sayfulaevna Mirmusayiva on the scientific degree competition of the doctor of philosophy in technical sciences, on speciality 05.17.01 – technology of inorganic compounds, subject: “Technology of sodium phosphates production on the basis of wet process phosphoric acid from Central Kizilkum phosphorites”
Key words: wet process phosphoric acid, phosphorite ore and concentrate, carbonate, hydrocarbonate and sodium hydroxide, phosphates waste, sodium phosphate solution, sodium phosphates, neutralization, separation, evoparation, crystallization, physicochemical properties
Subjects of the inquiry: wet process phosphoric acid, phosphorite ore, carbonate, hydrocarbonate and sodium hydroxide.
Aim of the inquiry: physicochemical determination and development of sodium ortophosphates technology from wet process phosphoric acid, receive on the base of local phosphoric ores, with determination optimal parameters of production.
Method of inquiry: chemical, X-ray, IR-spectral, thermal, microscopic.
The results achieved and their novelty: regularities of the influence of technological parameters on the cleaning process phosphoric acid from Central KyzylKum phosphate from accompanying impurities, identified the optimal technological parameters of the process of obtaining sodium phosphate salts of different grades and developed a highly efficient production technology of sodium orthophosphate. With the attraction of physical and chemical methods to obtain new data on the composition of the resulting phosphate sludge and Ways of disposal.
Practical value: results of the investigations have a scientific basis for the establishment of production technology of sodium phosphate of different grades with high technical and economic indicators based on phosphoric acid from phosphate Central Kyzyl Kum.
Degree of embed and economic effectivity: proposed technology has been tested on «Ammofos-Maxam» a model set, are turned out experimental batches of technical and feed phosphates of sodium. The data obtained to the establishment in principle of the technological scheme and production schedules. The economic effect of production of 1 ton of finished product, depending on the brand, compared with imported is 1,2-6,7 million sum, depending on the product. Production of technical trisodium phosphate implemented in production at «Ammofos-Maxam» OJSS and in 2008-2010 682 t of trisodium phosphate to the amount of 1.289 bln sum.
Sphere of usage: chemical industry and agriculture.

