Фармакогностическое исследование лихниса халцедонского, культивируемого в западной сибири
На правах рукописи
СМОЛЯКОВА
Ирина Михайловна
ФАРМАКОГНОСТИЧЕСКОЕ ИССЛЕДОВАНИЕ
ЛИХНИСА ХАЛЦЕДОНСКОГО,
КУЛЬТИВИРУЕМОГО В ЗАПАДНОЙ СИБИРИ
15.00.02 – фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Томск – 2006 г.
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Сибирский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель:
доктор фармацевтических наук, профессор Калинкина Галина Ильинична
Официальные оппоненты :
доктор химических наук Буркова Валентина Николаевна
кандидат фармацевтических наук Дудко Владимир Владимирович
Ведущая организация :
Государственное образовательное учреждение высшего профессионального образования «Самарский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Защита состоится « ___ » мая 2006 г. в ____ часов на заседании диссертационного совета Д 208.096.04 при ГОУ ВПО СибГМУ Росздрава
634050, г. Томск, Московский тракт, 2
С диссертацией можно ознакомиться в научно-медицинской библиотеке
ГОУ ВПО СибГМУ
634050, г. Томск, пр. Ленина, 107
Автореферат разослан « ___ » апреля 2006 г.
Ученый секретарь диссертационного совета Е.В. Ермилова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Интерес к поиску оригинальных лекарственных средств, обладающих гемореологической активностью, обусловлен широким распространением сердечно-сосудистых заболеваний. Течение таких патологий осложняет синдром повышенной вязкости крови (СПВК) – комплекс изменений гемореологических параметров. Развитие СПВК осложняет протекание ишемической болезни сердца и инфаркта миокарда, артериальной гипертензии, нарушения мозгового кровообращения и инсульта. Для коррекции гемореологических расстройств используются, как правило, препараты синтетического происхождения, являющиеся блокаторами кальциевых каналов, антиагрегантами, средствами, улучшающими мозговое кровоснабжение. При этом данные литературы свидетельствуют об ограниченности ассортимента средств, влияющих на реологические свойства крови. В связи с этим поиск новых, в том числе и растительных средств, оказывающих влияние на реологические свойства крови, является актуальной проблемой.
В лаборатории фармакологии кровообращения НИИ фармакологии ТНЦ РАМН (г. Томск) проведены исследования гемореологических свойств экстрактов растений флоры Сибири (Плотников М.Б. и др., 1998). Установлено, что из растений семейства гвоздичные (Caryophyllaceae) особого внимания заслуживает лихнис халцедонский (Lychnis chalcedonica L.), зарекомендовавший себя как перспективный источник ценных биологически активных веществ – фитоэкдистероидов [Зибарева Л.Н., 1989].
Плотниковым М.Б. с сотрудниками на модели синдрома повышенной вязкости крови in vitro выявлена гемореологическая активность у 40% и 70% этанольных экстрактов лихниса, сопоставимая с препаратом «Танакан», которая проявлялась в ограничении повышения вязкости крови, агрегации эритроцитов и снижении их деформируемости. По исследуемым показателям 40% этанольный экстракт превосходил 70% экстракт. Исследование фракций, полученных из этанольного экстракта лихниса, показало, что бутанольная фракция, в состав которой входят, преимущественно, экдистероиды в сочетании с флавоноидами, проявляла максимальную активность по способности ограничивать рост вязкости крови на модели СПВК in vitro, повышала деформируемость эритроцитов, тогда как этилацетатная фракция, содержащая, в основном, флавоноиды, не оказывала достоверного влияния на формирование синдрома повышенной вязкости in vitro, однако по эффективности обе эти фракции уступали экстракту. Необходимо отметить, что экдистерон, очищенная сумма флавоноидов и кверцетин обладали в эксперименте несколько меньшей активностью по сравнению с исследуемыми фракциями [Плотников М.Б. и др., 2000]. Таким образом, экстракт лихниса, его фракции, а также выделенные из них экдистерон и сумма флавоноидов проявляют в той или иной степени гемореологическую активность, причем, отдельные компоненты оказывают менее выраженное влияние на нормализацию показателей реологии крови, чем цельный экстракт.
Таким образом, анализ данных экспериментальных исследований показывает перспективность дальнейшего изучения лихниса халцедонского для разработки на основе его биологически активных комплексов сердечно-сосудистых препаратов с гемореологическими свойствами.
Однако природные ресурсы лихниса халцедонского очень ограничены, так как он не образует заросли и известно как декоративное растение. В связи с этим сотрудниками Сибирского ботанического сада Томского государственного университета разработаны приемы культивирования лихниса халцедонского в условиях Западной Сибири. При этом растение создает хорошую биомассу и не уступает дикорастущему по содержанию экдистероидов [Зибарева Л.Н., 1989]. Полученных данных недостаточно для внедрения культивируемого вида в медицинскую практику. Прежде всего, кроме фармакологических исследований, необходимо провести его детальное химическое исследование, разработать методики стандартизации сырья, которые могут быть использованы для разработки нормативной документации на данное сырье и препараты.
Цель исследования. На основании химического, анатомо-морфологического и товароведческого исследования лихниса халцедонского, культивируемого в Западной Сибири, предложить методики стандартизации сырья, разработать технологию получения гемореологического средства и его рациональной лекарственной формы.
Задачи исследования:
- Провести исследование надземной части лихниса халцедонского культивируемого, на содержание биологически активных веществ и выявить наиболее значимые;
- Провести детальное химическое исследование фенольных соединений и установить их структуру;
- Разработать числовые показатели и методики качественного обнаружения и количественного определения действующих веществ лихниса;
- Провести анатомо-морфологическое исследование надземной части лихниса и выявить диагностические признаки для определения его подлинности;
- Разработать проект Фармакопейной статьи «Лихниса халцедонского, культивируемого трава»
- Разработать рациональную лекарственную форму на основе биологически активного комплекса лихниса и методики ее стандартизации.
Научная новизна. Впервые проведено детальное исследование фенольных соединений лихниса халцедонского, культивируемого в Западной Сибири. Методом хроматографии на бумаге идентифицирован лютеолин-7-глюкозид и не менее пяти фенолкарбоновых кислот; методом ВЭЖ-хроматографии в надземной части растения обнаружено не менее трех флавоноидов (С-гликозиды). Методом ВЭЖХ-МС установлена структура и идентифицированы кофейная кислота, кумаровая кислота, виценин, неовитексин и полиподин В.
Впервые проведено анатомическое исследование надземной части лихниса халцедонского и выявлены диагностические микроскоскопические признаки сырья.
Обоснована необходимость стандартизации травы лихниса по содержанию фитоэкдистероидов и флавоноидов, которые обусловливают его гемореологические свойства.
Разработаны методики качественного обнаружения и количественного определения в траве лихниса фитоэкдистероидов и флавоноидов методом тонкослойной хроматографии и спектрального анализа.
Разработаны технологические параметры получения спиртового экстракта лихниса и твердой лекарственной формы на его основе, предлагаемых в качестве гемореологических средств.
Практическая значимость. На основании проведенных фармакогностических исследований для медицинской практики предложен новый вид лекарственного растительного сырья и лекарственные средства на основе его биологически активного комплекса в качестве гемореологического средства для лечения сердечно-сосудистых заболеваний.
Результаты микроскопических и химических исследований использованы для разработки методик диагностики и определения качества сырья лихниса и заложены в проект Фармакопейной статьи «Лихниса халцедонского, культивируемого трава».
Для углубленных фармакологических исследований в качестве гемореологических средств предложены спиртовый экстракт лихниса, гранулы и таблетки на его основе.
Для Центров Фармацевтической информации Сибирского региона и студентов медицинских и фармацевтических вузов разработано методическое пособие «Лекарственные растения Сибири в современной терапии сердечно-сосудистых заболеваний», в котором использованы материалы диссертации.
На защиту выносятся результаты фитохимического и анатомо-морфологического исследования лихниса халцедонского, культивируемого в Западной Сибири, и рекомендуемого в качестве источника гемореологических средств.
Апробация работы. Материалы диссертации доложены на IV и V Международном конгрессе молодых ученых и специалистов «Науки о человеке» (Томск 2003, 2004 г.); на Региональной конференции «Разработка, исследование и маркетинг новой фармацевтической продукции» (Пятигорск, 2005 г.); на заседании проблемной комиссии «Изыскание и изучение новых лекарственных средств. Вопросы фармации» (Томск, 2006 г).
Связь задач исследования с проблемным планом фармацевтических наук. Работа выполнена в соответствии с планом научных исследований кафедры фармакогнозии с курсами ботаники и экологии Сибирского государственного медицинского университета и комплексной целевой программой СО АМН РФ «Здоровье человека в Сибири» (№ государственной регистрации 01.85.0069848).
Публикации. По материалам диссертации опубликовано 7 печатных работ.
Экспериментальные исследования по теме диссертации выполнены на кафедрах фармакогнозии с курсами ботаники и экологии, фармацевтической технологии СибГМУ, а также в сотрудничестве с коллективами других научных организаций: Сибирского ботанического сада при Томском государственном университете (лаборатория фитохимии), НИИ Фармакологии СО РАМН г. Томск (лаборатория фармакологии кровообращения), НИИ Органической химии СО РАН г. Новосибирск, Института Фитохимии МОН РК г. Караганда (лаборатория фенольных и стероидных соединений). Сотрудникам данных подразделений и научных учреждений приносим искреннюю благодарность. Особую признательность выражаем д.х.н. Зибаревой Л.Н., д.б.н. Плотникову М.Б., д.х.н. Адекенову С.М., д.х.н. Юсубову М.С.
Объем и структура диссертации. Диссертация изложена на 155 страницах машинописного текста и состоит из введения, обзора литературы, четырех глав экспериментальных исследований, выводов, списка литературы и приложения. Библиографический указатель включает 129 источников литературы, из них 28 зарубежных. Работа иллюстрирована 35 рисунками и 33 таблицами.
Во введении обоснована актуальность проблемы, сформулированы цель и задачи исследования, охарактеризованы научная новизна и практическая значимость работы.
В обзоре литературы (глава 1) приведен краткий анализ проблемы сердечно-сосудистых заболеваний и сопровождающих их гемореологических расстройств, характеристика лекарственных средств синтетического происхождения, применяемых в настоящее время для терапии данной патологии. Показаны перспективы получения гемореологических средств на основе лекарственного растительного сырья. Дана характеристика и степень изученности лихниса халцедонского.
Вторая глава посвящена характеристике объекта и методов исследования.
В третьей главе приведены результаты качественного обнаружения и количественного определения биологически активных веществ лихниса, выделения и установления структуры фенольных соединений и экдистероидов данного растения.
Четвертая глава посвящена разработке методик определения подлинности и стандартизации травы лихниса халцедонского, включенных в проект Фармакопейной статьи «Лихниса халцедонского, культивируемого трава».
В пятой главе изложены результаты по разработке технологии получения жидкого экстракта лихниса и твердой лекарственной формы на его основе, методик их стандартизации, а также оценка безвредности и гемореологических свойств предлагаемого препарата.
В приложении представлен проект Фармакопейной статьи «Лихниса халцедонского, культивируемого трава».
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Объекты и методики исследования
Для исследования была взята надземная часть лихниса халцедонского (Lychnis chalcedonica L.), культивируемого на экспериментальном участке Сибирского ботанического сада Томского государственного университета. Наиболее облиственную надземную часть растения трехлетнего возраста срезали в период отрастания (начало вегетации), бутонизации и массового цветения в 2001-2003 гг. Для заготовки сырья использовали не менее 5 экспериментальных площадок лихниса.
Качественное и количественное определение различных групп биологически активных веществ (БАВ) проводили с помощью общепринятых в фитохимическом анализе методов. Для очистки экстрактов, разделения суммы и идентификации веществ применяли методы избирательной жидкостной экстракции, хроматографии на бумаге и в тонком слое сорбента, ВЭЖХ, УФ- и масс-спектрометрии.
Морфологические признаки сырья изучали и описывали под стереоскопическим микроскопом МБС-10 (увеличения 8х1; 8х2; 8х4). Микроскопические признаки сырья устанавливали на основании анатомического исследования стеблей, листьев и цветков растения, для чего были приготовлены плоскостные препараты. Для получения объективных результатов анализировали не менее десяти препаратов. Готовые препараты изучали под микроскопом МИКМЕД – 1 (увеличения 7х1, 5х8; 7х1, 5х40). Фотографировали с помощью цифрового фотоаппарата «LG» с оптическим адаптером и обрабатывали на компьютере в программе «Photoshop 8.0». Присутствие различных включений доказывали проведением общепринятых гистохимических реакций.
Для оценки качества сырья общепринятыми фармакопейными методиками определяли основные числовые показатели: измельченность сырья, содержание экстрактивных веществ, влажность, золу общую и нерастворимую в 10% растворе кислоты хлористоводородной, содержание органической и минеральной примесей.
Технологические свойства сырья изучены с помощью методик, разработанных Ю.Г. Пшуковым.
Исследования гемореологической активности экстракта лихниса были проведены по методике М.Б. Плотникова на 42 крысах-самцах линии Вистар и 16 крысах-самцах линии SHR (spontaneously hypertensive rats) массой 230-280 г.
Статистическую обработку полученных результатов проводили общепринятым методом с определением средней арифметической (Х) и ошибки средней арифметической (м). Достоверность результатов оценивали параметрически по tкритерию Стьюдента. Обработку результатов фармакологических исследований проводили с использованием непараметрического критерия Манна-Уитни. Различия считали достоверными при Р<0,05. Статистическую обработку проводили с использованием программы “Statistica for Windows 7,0”.
Исследование химического состава лихниса халцедонского
С использованием общепринятых методов анализа было проведено исследование надземной части лихниса на присутствие БАВ. Данные таблицы 1 показывают, что биологически активный комплекс представлен экдистероидами, фенольными соединениями, полисахаридами, сапонинами и витаминами. Наряду с экдистероидами, наиболее значимыми в лихнисе халцедонском являются флавоноиды, которые по данным фармакологического исследования могут обусловливать гемореологические свойства данного растения.
Таблица 1
Результаты количественного определения БАВ
в надземной части лихниса халцедонского
| №п/п | БАВ | Содержание, % от массы абс.-сух. сырья |
| 1 | Фенольные соединения, в том числе: - флавоноиды - гидроксикоричные кислоты - кумарины | 0,72±0,04 0,54±0,03 0,10±0,00 0,08±0,01 |
| 2 | Экдистероиды | 0,65±0,03 |
| 3 | Сапонины | 8,92±0,45 |
| 4 | Полисахариды, в том числе: - водорастворимые - пектиновые вещества - гемицеллюлоза А и В | 11,80 ± 0,52 2,80 ± 0,15 1,90 ± 0,06 7,10 ± 0,35 |
| 5 | Каротиноиды, мг% | 5,19±0,25 |
| 6 | Витамин К, мг% | 1,50±0,08 |
| 7 | Витамин С, мг% | 105,20±5,26 |
В связи с этим, детальное химическое исследование фенольных соединений и экдистероидов представляет первоочередной интерес.
Хроматографическое и спектральное исследование
фенольных соединений и экдистероидов лихниса халцедонского
Для получения данных о фенольных соединениях лихниса, из надземной части получали этанольный экстракт и исследовали его методом хроматографии на бумаге в различных системах растворителей. Детектируя обнаруженные вещества в УФ- и видимом свете после проявления различными реактивами установили, что в растении достоверно присутствуют экдистероиды, флавоноиды в гликозидированной форме и гидроксикоричные кислоты. При исследовании природы флавоноидных гликозидов, столкнулись с фактом, что обычный кислотный гидролиз приводит к образованию только одного агликона, который по хроматографическому поведению соответствует известному веществу лютеолину. Хроматографическое исследование исходного гликозида с известным веществом показало, что он соответствует лютеолин-7-глюкозиду. После применения жесткого гидролиза остальные гликозиды лихниса образовали основные агликоны апигенин и лютеолин. Это позволило сделать вывод, что флавоноиды растения представлены в основном С-гликозидами.
При хроматографическом исследовании спиртового экстракта лихниса с использованием достоверных образцов гидроксикоричных кислот идентифицировали кофейную, п-кумаровую, синаповую, феруловую и хлорогеновую кислоты (табл. 2).
Таблица 2
Хроматографическая характеристика
гидроксикоричных кислот лихниса халцедонского
| Вещество | Значение Rf | Окраска пятен | |
| УФ-свет | Видимый свет, реактив Паули | ||
| кофейная кислота | 0,26 | светло-голубая | коричневая |
| феруловая кислота | 0,32 | голубовато-фиолетовая | фиолетовая |
| синаповая кислота | 0,51 | голубовато-зеленая | голубовато-фиолетовая |
| хлорогеновая кислота | 0,70 | голубая | желто-коричневая |
| п-кумаровая кислота | 0,74 | голубовато-фиолетовая | красно-коричневая |
В результате проведенных исследований с определенной степенью достоверности можно утверждать, что лихнис халцедонский содержит вещества флавоноидного характера – С-гликозидированные производные апигенина и лютеолина, лютеолин-7-глюкозид, а также не менее пяти гидроксикоричных кислот.
Для более детального исследования фенольных соединений из водно-спиртового извлечения методом избирательной экстракции получали хлороформную, этилацетатную и бутанольную фракции. Этилацетатную и бутанольную фракции исследовали с помощью высокоэффективной жидкостной хроматографии и хромато-масс-спектрометрии.
Хроматографический анализ проводили на жидкостном хроматографе с диодно-матричным и масс-селективным детекторами («Agilent 1100 Series LC/MSD»). Детектирование и запись спектров поглощения проводили в интересующем нас диапазоне длин волн (230-500 нм.). Для масс-селективного детектора (модель G1946С) использовали метод химической ионизации при атмосферном давлении (APCI). Проводили сканирование положительных (positive scan) и отрицательных ионов (negative scan) с соотношением m/z от 100 до 1200 (точность измерения при этом составляла 0.1). Детектирование выходящего из колонки элюента проводили одновременно на двух полосах поглощения: 270-310 нм (в этом диапазоне видны все ароматические соединения) и 320-360 нм (область более специфична для природных соединений типа ксантонов, флавонов и кумаринов). Во всех случаях поглощение фиксировалось относительно контрольной полосы 800-900 нм. Разделение проводили на колонке с обращенной фазой «Zorbax Rx-C18», 4.6 150 мм (наполнитель с диаметром частиц 5 мкм, размер пор 80 А). Элюент – смесь 2.3% НСООН-МеОН (линейный градиент от 20 до 90% МеОН с 5-ой до 10-ой минуты), 1 мл/мин.
В качестве основных критериев при выборе предполагаемой структуры использовали время удерживания в сравнении с известными образцами, УФ-спектры и масс-спектры соответствующих пиков на ВЭЖХ, а также базы данных и обзорные статьи по основным спектральным и физико-химическим характеристикам природных соединений.
По данным ВЭЖХ этилацетатной фракции было сделано заключение о присутствии в растении флавоноидов, экдистероидов и фенолкарбоновых кислот (рис. 1, 2).
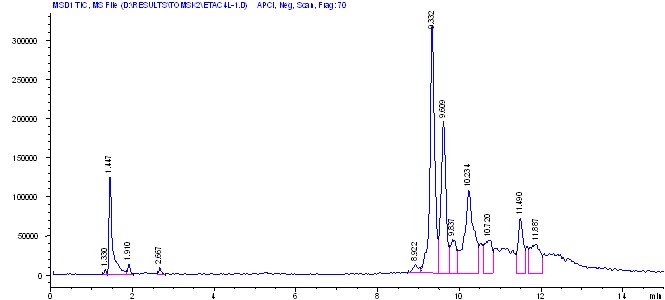
Рис. 1 – Хроматограмма этилацетатной фракции
экстракта лихниса халцедонского с масс-селективным детектором
в режиме APCI Neg. Scan.

Рис. 2 – Хроматограмма этилацетатной фракции
экстракта лихниса халцедонского с масс-селективным детектором
в режиме APCI Pos. Scan.
На хроматограмме этилацетатной фракции экстракта лихниса халцедонского пик со временем удерживания 9.3 мин (УФ-спектр имеет два основных максимума поглощения: 270 и 330 нм), имеющий в масс-спектре интенсивный пик с m/z=565.2 [М+Н]+ в режиме ХИ APCI, Pos. Scan. (рис. 3) и с m/z=563.2 [М–Н]+ в режиме ХИ APCI, Neg. Scan. (рис. 4), идентифицировали как С-дигликозид апигенина – виценин. В качестве сахарных компонентов в данном случае выступают глюкоза и арабиноза.
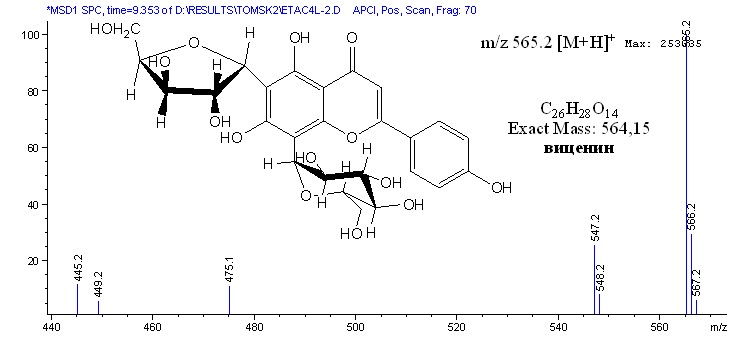
Рис. 3 – Масс-спектр пика на хроматограмме
со временем удерживания 9.3 мин в режиме ХИ APCI, Pos. Scan.
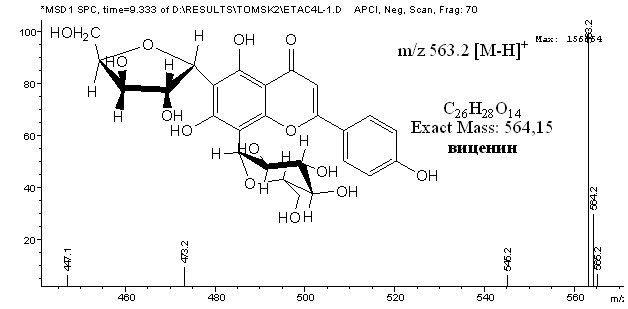
Рис. 4 – Масс-спектр пика на хроматограмме
со временем удерживания 9.3 мин в режиме ХИ APCI, Neg. Scan.
Одинаковая интенсивность пиков в различных режимах сканирования указывала на наличие С-гликозидов и отсутствие О-гликозидов. Обычно, при анализе О-гликозидов в режиме Neg. Scan. максимальную интенсивность имеет пик молекулярного иона [M–H]+, а минимальную интенсивность пик [Mагл.–H]+. В режиме Pos. Scan. максимальную интенсивность имеет пик молекулярного иона агликона [Mагл.+H]+, а минимальную интенсивность пик [M+H]+.
Пик со временем удерживания 9.6 мин (УФ-спектр имеет два максимума поглощения: 271 и 335 нм), имеющий интенсивный пик с m/z=433.2 [М+Н]+ в режиме ХИ APCI, Pos. Scan. (рис. 5) и с m/z=431.2 [М–Н]+ в режиме ХИ APCI, Neg. Scan. (рис. 6), идентифицировали как С-моногликозид апигенина – неовитексин. Кроме того, в этом спектре присутствовали другие пики с различной интенсивностью, один из которых мы отнесли к виценину (С-дигликозид апигенина): m/z=565.2 [М+Н]+ и m/z=563.2 [М–Н]+.

Рис. 5 – Масс-спектр пика на хроматограмме
со временем удерживания 9.6 мин в режиме ХИ APCI, Pos. Scan.
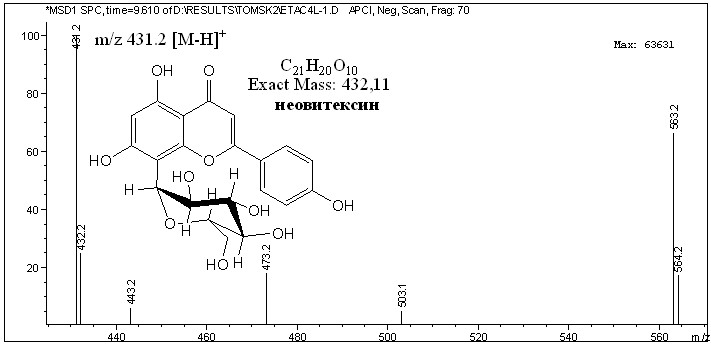
Рис. 6 – Масс-спектр пика на хроматограмме
со временем удерживания 9.6 мин в режиме ХИ APCI, Neg. Scan.
Пик на ВЭЖХ этилацетатной фракции экстракта лихниса со временем удерживания 10.2 мин (УФ-спектр с максимумом 251 нм) идентифицировали с фитоэкдистероидом полиподином В.
В режиме ХИ APCI, Pos. Scan. в масс-спектре присутствует пик m/z=497.3, а в режиме ХИ APCI, Neg. Scan. m/z=495.3, соответствующие пику молекулярного иона+протон [М+Н]+ и пику молекулярного иона минус протон [М–Н]+ соответственно (рис. 7). Этот спектр дает нам, в первую очередь, точную информацию о величине молекулярной массы данного вещества.
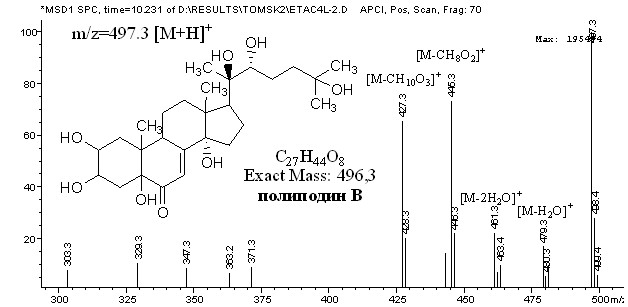
Рис. 7 – Масс-спектр пика на хроматограмме
со временем удерживания 10.2 мин в режиме ХИ APCI, Pos. Scan.
Пики с m/z=479.3 и m/z=461.3 в режиме ХИ APCI, Pos. Scan. соответствовали фрагментам молекулярного иона после отрыва молекул воды [М–Н2О]+ и [М–2Н2О]+ соответственно. А пики с m/z=445.3 и m/z=427.3 в этом же режиме – фрагментам молекулярного иона [М–СН8О2]+ и [М–СН10О3]+. Такой тип фрагментации легко можно предположить по большому количеству гидроксильных групп в структуре полиподина В, связанных с вторичными и третичными атомами углерода.
Пик на ВЭЖХ этилацетатной фракции экстракта лихниса халцедонского со временем удерживания 11.4 имел два масс-спектра в разных режимах (рис. 8, 9). В режиме ХИ APCI, Pos. Scan. в масс-спектре присутствовал пик m/z=815.3, а в режиме ХИ APCI, Neg. Scan. m/z=813.4, соответствующие пику молекулярного иона плюс протон [М+Н]+ и пику молекулярного иона минус протон [М–Н]+ соответственно. Эти два спектра дали нам точную информацию о величине молекулярной массы данного вещества, равную 814. Основываясь на характере фрагментации пика молекулярного иона, отнесли это соединение к производным экдистероидов. Пики с m/z=797.3, m/z=783.3 и m/z=771.3 в режиме ХИ APCI, Pos. Scan. соответствовали фрагментам молекулярного иона после отрыва молекулы воды [М–Н2О]+ и углеродсодержащих фрагментов [М–СН4О]+ и [М–С2Н4О]+. Эти же пики фрагментов молекулярного иона присутствовали и в режиме ХИ APCI, Neg. Scan. (рис. 9).

Рис. 8 – Масс-спектр пика на хроматограмме
со временем удерживания 11.4 мин в режиме ХИ APCI, Pos. Scan.
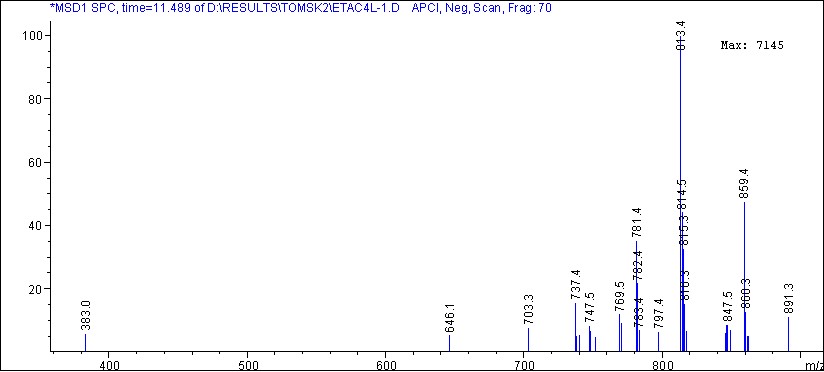
Рис. 9 – Масс-спектр пика на хроматограмме
со временем удерживания 11.4 мин в режиме ХИ APCI, Neg. Scan.
Характер представленных на рисунках 8, 9 масс-спектров позволил предположить, что эти молекулярные пики принадлежат гликозидированным или этерифицированным формам экдистероидов, расшифровка которых для нас не представлялась возможной.
Хроматограммы бутанольной фракции имели сходство с аналогичными хроматограммами этилацетатной фракции, однако на них появились пики со временами удерживания 2.6 и 3.6 мин (рис.10, 11).

Рис. 10 – Хроматограмма бутанольной фракции
экстракта лихниса халцедонского с масс-селективным детектором
в режиме ХИ APCI, Neg. Scan.
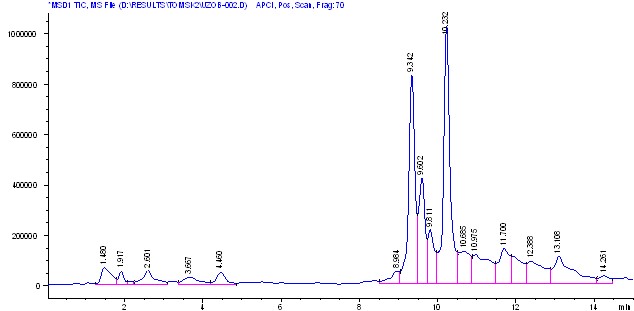
Рис. 11 – Хроматограмма бутанольной фракции
экстракта лихниса халцедонского с масс-селективным детектором
в режиме ХИ APCI, Pos. Scan.
В масс-спектрах в режиме ХИ APCI, Pos. Scan. (рис. 12, 13) присутствовали пики с m/z=235.2 для вещества со временем удерживания 3.6 мин и с m/z=251.2 для вещества со временем удерживания 2.5 мин соответственно.
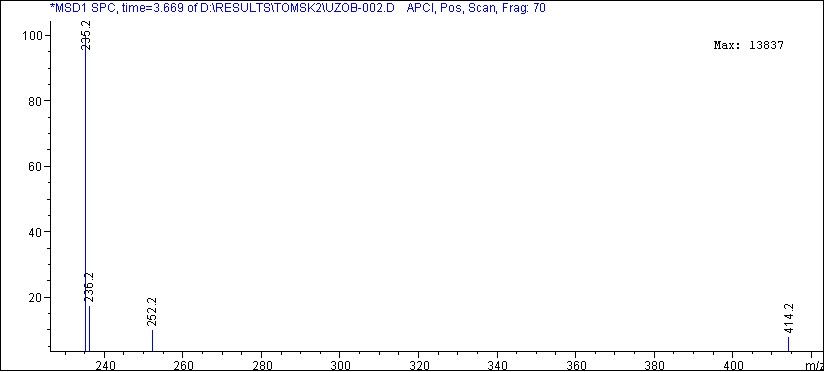
Рис. 12 – Масс-спектр пика на хроматограмме
со временем удерживания 3.6 мин в режиме ХИ APCI, Pos. Scan.
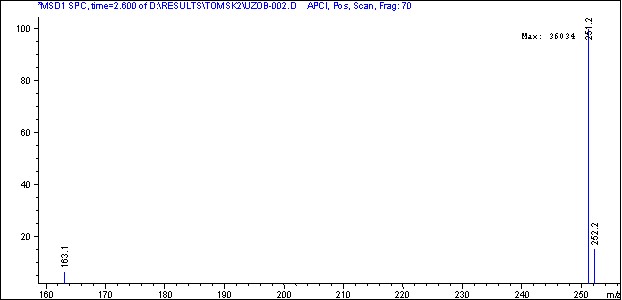
Рис. 13 – Масс-спектр пика на хроматограмме
со временем удерживания 2.6 мин в режиме ХИ APCI, Pos. Scan.
Полученная информация позволила нам отнести данные вещества к производным коричной кислоты – кофейной (время удерживания 2.5 мин) и кумаровой (время удерживания 3.6) кислотам.
Результаты идентификации фенольных соединений и экдистероидов лихниса халцедонского представлены в таблице 3.
Таблица 3
Результаты идентификации биологически активных веществ
лихниса халцедонского ВЭЖХ-МС
| Время удерживания, мин | Величина m/z (молекулярная масса) | Вещество |
| 2.6 | 252 | кофейная кислота (3,4-дигидроксикоричная кислота) |
| 3.6 | 234 | кумаровая кислота (п-гидроксикоричная кислота) |
| 9.3 | 564 | виценин (8-С-син--D- глюкопиранозил, С-С--D- глюкопиранозид апигенина) |
| 9.6 | 432 | неовитексин (8-С-син--D-глюкопиранозид апигенина) |
| 10.2 | 496 | полиподин В |
| 11.4 | 814 | неидентифицированное производное экдистероидов (гликозидированная или этерифицированная форма) |
Таким образом, опираясь на УФ- и масс-спектры, снятые в двух режимах химической ионизации, получена информация, позволяющая с высокой степенью достоверности предполагать структуру БАВ лихниса. Для окончательного подтверждения структуры необходим весь набор спектральных и физико-химических характеристик, которые можно получить только при выделении индивидуальных соединений.
Сравнительный анализ полученных данных и сведений литературы позволил установить, что состав флавоноидов лихниса халцедонского, культивируемого в Западной Сибири и произрастающего в Европейской части России, идентичен.
Разработка методик стандартизации травы лихниса халцедонского
Стандартизацию сырья предложено проводить по двум веществам – экдистероидам и флавоноидам, так как предполагается, что они имеют наибольшую значимость в проявлении гемореологического эффекта экстракта лихниса.
Для определения подлинности сырья использовали метод тонкослойной хроматографии со стандартными образцами лютеолин-7-глюкозида и экдистерона, присутствие которых доказано нами хроматографически.
Определение содержания экдистероидов проводили известным в литературе хроматоспектрофотометрическим методом, при этом нами модифицированы условия максимального извлечения экдистероидов, которыми являются 40% этанол, время извлечения 24 часа, размер частиц сырья 3-5 мм, соотношение сырья и экстрагента 1:30.
Количественное содержание флавоноидов в сырье определяли спектрофотометрическим методом. При этом флавоноиды давали окрашенный комплекс со спиртовым раствором алюминия хлорида, который дает основной максимум поглощения при длине волны 400 нм. Расчет флавоноидов проводили на ГСО лютеолин-7-глюкозида (цинарозид), так как его комплекс с алюминия хлоридом дает аналогичный максимум поглощения при длине волны 400 нм. Присутствие данного гликозида в траве лихниса подтверждено нами хроматографически. Экспериментально подобранные условия экстракции позволяют проводить одновременно максимальное извлечение флавоноидов и экдистероидов.
На основании изучения динамики накопления флавоноидов и экдистероидов лихниса халцедонского установлено, что в качестве лекарственного сырья можно использовать надземную часть растения, собранную в стадии бутонизации и цветения.
Кроме содержания действующих веществ показателями качества сырья лихниса являются влажность, содержание золы и примесей, пределы которых установлены экспериментально.
Для диагностики цельного и измельченного сырья лихниса, кроме хроматографического анализа, проведено анатомо-морфологическое исследование надземной части растения. Диагностически значимыми признаками сырья являются: структура стебля, листа, характерная окраска цветков, строение эпидермы листа с тонкостенными, плотно прилегающими друг к другу клетками с простыми многоклеточными волосками с обеих сторон листа. Устьица многочисленные, диацитного типа, расположены только на нижней эпидерме листа (гипостоматный тип). Строение эпидермы чашелистиков с сильно извилистыми клетками, с устьицами аномоцитного типа и длинными многоклеточными волосками.
На основании проведенных исследований разработан проект ФС «Лихниса халцедонского, культивируемого трава».
Разработка рациональной лекарственной формы
на основе биологически активного комплекса лихниса халцедонского
При разработке рациональной лекарственной формы были определены технологические параметры сырья и изучен ряд факторов, влияющих на процесс экстрагирования экдистероидов и флавоноидов. На основании полученных данных разработан способ получения жидкого экстракта из травы лихниса халцедонского на 40% этаноле.
В качестве твердой лекарственной формы на основе жидкого экстракта предложены гранулы и таблетки. Для выбора рецептуры экспериментально проанализировали 21 вариант прописей. Результаты исследования качества полученных гранул по технологическим параметрам и содержанию действующих веществ (флавоноидов и экдистероидов) позволили выбрать один из вариантов прописей. При получении таблеток использовали уже изученные свойства гранул. В качестве основы для таблеток была выбрана пропись, содержащая густой экстракт лихниса, сахарозу, лактозу, 5% раствор МЦ, а также кальция стеарат.
Изучение безвредности жидкого экстракта лихниса проводили на белых мышах обоего пола при однократном введении препарата в желудок в дозе 5000 мг/кг. Гибели животных не наблюдали в течение 2 недель. Согласно существующей классификации (ГОСТ 12.1.007-76), препарат соответствует IV классу «Вещества малоопасные».
Экспериментальное фармакологическое изучение полученного жидкого экстракта показало, что экстракт обладает умеренной гемореологической активностью.
ВЫВОДЫ
1. В результате химического исследования надземной части лихниса халцедонского, культивируемого в Западной Сибири, установлено, что наиболее значимыми биологически активными веществами в его составе являются: фенольные соединения (0,72±0,04%), экдистероиды (0,65±0,03%), сапонины (8,92±0,45%), полисахариды (11,80 ± 0,52%).
2. Методами хроматографии на бумаге, в тонком слое, ВЭЖХ и хроматомасс-спектрометрии установлено, что флавоноиды растения представлены С-гликозидированными производными апигенина – виценином (8-С-син--D-глюкопиранозил, С-С--D-глюкопиранозид апигенина) и неовитексином (8-С-син--D-глюкопиранозид апигенина), а также лютеолин-7-глюкозидом; гидроксикоричные кислоты представлены кофейной, п-кумаровой, синаповой, феруловой и хлорогеновой кислотами; из фитоэкдистероидов идентифицирован полиподин В.
3. Разработаны методики стандартизации сырья лихниса халцедонского по содержанию экдистероидов и флавоноидов спектрофотометрическим методом, как основных веществ, обусловливающих гемореологические свойства экстрактивного комплекса данного растения.
4. Изучение динамики накопления экдистероидов и флавоноидов в надземной части лихниса показало, что оптимальными сроками заготовки лекарственного сырья – травы являются фазы бутонизации и цветения растения.
5. С помощью анатомо-морфологического исследования установлены диагностические признаки сырья для определения его подлинности, получены достоверные фотоиллюстрации микроскопических признаков.
6. Разработаны числовые показатели сырья для цельной и измельченной травы лихниса халцедонского: содержание экдистероидов не менее 0,6%; флавоноидов не менее 0,5%; экстрактивных веществ, извлекаемых 40% этанолом, не менее 30%; влажности не более 13%; золы общей не более 8%; золы, нерастворимой в 10% растворе кислоты хлористоводородной, не более 3%, органической примеси не более 2%, минеральной примеси не более 1%.
7. На основании полученных результатов разработан проект Фармакопейной статьи «Лихниса халцедонского, культивируемого трава».
8. Обоснован способ получения жидкого экстракта лихниса, предложена рациональная лекарственная форма на его основе – таблетки; проведена оценка их качества, безвредности и гемореологической активности.
ПО ТЕМЕ ДИССЕРТАЦИИ ОПУБЛИКОВАНЫ СЛЕДУЮЩИЕ РАБОТЫ:
1. Перспективы использования лихниса халцедонского (Lychnis chalcedonica L.), в медицинской практике // Сб. статей по материалам IV конгресса молодых ученых и специалистов «Науки о человеке». – Томск, 15-16 мая 2003. – С. 222.
2. Фитохимическое исследование надземной части лихниса халцедонского (Lychnis chalcedonica L.), культивируемого в Западной Сибири // Актуальные проблемы медицины и биологии. Сборник научных работ. – Томск, 2003. – Вып. 2. – С. 40-41 (Соавт.: Г.И. Калинкина, С.Е. Дмитрук, Л.Н. Зибарева).
3. Исследование травы лихниса халцедонского, культивируемого в Западной Сибири // Фармация. – 2004. – № 5. – С. 20-22. (Соавт.: Г.И. Калинкина, Т.П. Березовская, Л.Н. Зибарева, Т.П. Свиридова, С.Е. Дмитрук).
4. Исследование фенольных соединений лихниса халцедонского (Lychnis chalcedonica L.), культивируемого в Западной Сибири // Сб. статей по материалам V конгресса молодых ученых и специалистов «Науки о человеке». – Томск, 20-21 мая 2004. – С. 363.
5. Проблема рационального использования экологического чистого лекарственного растительного сырья // Труды постоянно действующей научно-технической школы-семинара студентов, аспирантов и молодых ученых «Информационные системы мониторинга окружающей среды». – Томск, 2004. – Вып. 3. – С. 51-53. (Соавт.: Г.И. Калинкина, И.А. Туева, А.С. Ангаскиева, Е.А.Лукша, Л.П. Охрименко, Е.Н. Сальникова, А.А. Марьин).
6. Разработка технологии экстрактов лихниса халцедонского и серпухи венценосной – новых гемореологических средств // Сб. научных трудов «Разработка, исследование и маркетинг новой фармацевтической продукции». – Пятигорск, 2005. – Вып. 60. – С. 149-150. (Соавт.: А.С. Ангаскиева, Г.И. Калинкина, Л.Н. Зибарева, Т.Г. Харина, М.Б. Плотников, А.С. Васильев).
7. Фитопрепараты в профилактике и лечении сердечно-сосудистых заболеваний // Учебно-методическое пособие. – Томск, 2005. – 35 с. (Соавт.: А.А. Марьин, А.С. Ангаскиева).
СПИСОК СОКРАЩЕНИЙ:
СПВК – синдром повышенной вязкости крови
ВЭЖХ – высокоэффективная жидкостная хроматография
ВЭЖХ-МС – высокоэффективная жидкостная хромато-масс-спектрометрия
УФ-спетр – ультрафиолетовый спектр
БАВ – биологически активные вещества
ГСО – государственный стандартный образец
ФС – фармакопейная статья
МЦ – метилцеллюлоза

