Влияние оптической изом е рии на фармакокинетику препар а тов атенолола
На правах рукописи
ЧУГАЕВ
Дмитрий Владиславович
ВЛИЯНИЕ ОПТИЧЕСКОЙ ИЗоМЕРИИ на
ФАРМАКОКИНЕТИку препаратов АТЕНОЛОЛА
15.00.02 – Фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Москва – 2008
Работа выполнена в ГОУ ВПО Московская Медицинская Академия им. И.М. Сеченова Росздрава
Научный руководитель: доктор фармацевтических наук, профессор
Раменская Галина Владиславовна
Официальные оппоненты:
доктор фармацевтических наук Чистяков Виктор Владимирович
доктор фармацевтических наук,
профессор Сокольская Татьяна Александровна
Ведущая организация:
Институт стандартизации и контроля лекарственных средств ФГУ «НЦ ЭСМП» Росздравнадзора.
Защита диссертации состоится «___»________________2009 г. в 1400 часов на заседании Диссертационного Совета Д.208.040.09 при ГОУ ВПО Московская Медицинская Академия им. И.М. Сеченова Росздрава по адресу: 119019, Москва, Никитский бульвар, 13.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО ММА имени И.М. Сеченова Росздрава, по адресу: 117998, г. Москва, Нахимовский проспект, д. 49
Автореферат разослан «_____» ______________ 2009 г.
Ученый секретарь
Диссертационного Совета Д.208.040.09,
доктор фармацевтических наук,
профессор Наталья Петровна Садчикова
ОБЩАЯ ХАРАКТЕРИСТИКА ДИССЕРТАЦИИ
Актуальность темы
Стереохимическая специфичность является одним из важнейших свойств всей живой природы. Известно широкое распространение в живой природе оптически активных органических соединений [В.В.Алексеев,1998, Л.В.Андреева, 2006]. Оптически активны белки, полисахариды, нуклеиновые кислоты, флавоноиды, аминокислоты, ряд витаминов (например, витамины К, Е, С - макромолекулы построены из асимметричных фрагментов) [К.С.Сычев, 1998, R.P.Blankfield, 2005, P.J.Ross, 1991].
Большая часть ферментов также проявляет стереохимическое действие, при этом они инициируют превращение только одного из нескольких стереоизомерных веществ (субстратов) [И.А.Ананьева, 2001, Л.Г.Воронков, 2007]. Сорбенты: крахмал, целлюлоза также стереоспецифичны и сорбируют одни из оптически активных веществ в большей степени, чем другие. Во многих случаях из двух оптически активных форм лекарственных препаратов специфическое фармакологическое действие проявляет лишь одна форма или проявляют обе формы, но с различной активностью. Асимметричные синтезы в живых организмах осуществляется с помощью ферментов, молекулы которых также асимметричны, то есть "асимметрия рождает асимметрию" [В.И. Гольданский, В.В. Кузьмин, 1989]. Еще в 1860 году Пастер высказал предположение, что асимметрия молекулярного строения образует "четкую границу между живой и неживой природой" [Пахомов В.П., 2006]. Учитывая различное действие отдельных стереоспецифических лекарственных препаратов, возникает необходимость в разделении их на соответствующие изомеры и затем индивидуальное исследование их фармакологических и токсикологических свойств, установления их чистоты с применением современных способов анализа. Для проведения таких исследований необходимо использовать современные специфические методы анализа (поляриметрию, хроматографию, спектроскопию ЯМР, электрофорез и др.). Таким образом, необходимо изучать лекарственные препараты и биологически активные соединения с учетом их оптической активности, что позволит значительно повысить их фармакологическое действие и снизить токсичность. Важно это и для лекарственных веществ, влияющих на сердечно-сосудистую систему – бета-блокаторов (ацебутолол, пропранолол, атенолол, бупранолол, надолол), блокаторов кальциевых каналов (никардипин, верапамил), и для других лекарственных веществ. Всё вышесказанное определило цель и задачи настоящего исследования.
Цель и задачи исследования
Целью диссертационной работы являлось изучение влияния оптической изомерии на фармакокинетику лекарственных средств, на примере атенолола.
Задачи исследования:
1. Разработать методику количественного определения R- и S- энантиомеров атенолола в растворах и плазме крови.
2. Определить содержание R- и S- атенолола в субстанциях атенолола различных серий.
3. Определить содержание R- и S- атенолола в таблетках различных производителей.
4. Изучить высвобождение R- и S- атенолола из таблеток различных производителей в условиях in vitro.
5. Изучить фармакокинетику R- и S- атенолола у здоровых добровольцев после однократного перорального приема.
Научная новизна
Разработана методика идентификации, разделения и количественного определения изомеров атенолола методом ВЭЖХ в растворах и плазме крови.
Впервые изучены особенности фармакокинетики изомеров атенолола после однократного перорального приема препаратов атенолола различных производителей.
Впервые изучено соотношение изомеров атенолола в субстанциях и препаратах разных производителей.
Определена динамика высвобождения R- и S- атенолола из таблеток в условиях in vitro.
Практическая значимость и внедрение полученных результатов
Полученные результаты показывают необходимость определения R- и S- изомеров в препаратах атенолола, при стандартизации и проведении фармакокинетических исследований.
Результаты диссертационной работы используются при проведении фармакокинетических исследований препаратов атенолола в Институте клинической фармакологии ФГУ НЦ ЭСМП и в Филиале «Клиническая фармакология» НЦ Биомедицинских технологий РАМН.
Апробация диссертации
Результаты работы доложены на межкафедральной конференции фармацевтического факультета ГОУ ВПО ММА им. И.М.Сеченова Росздрава (сентябрь, 2008 г.), на ХV-м Российском национальном конгрессе «Человек и лекарство» (Москва, 2008 г.), восьмом конгрессе молодых ученых и специалистов «Науки о человеке» (Томск, 2007 г.), конференции «Фармация и общественное здоровье» (Екатеринбург, 2008 г.).
Связь исследования с проблемным планом фармацевтических наук
Диссертационная работа выполнена в рамках комплексной темы кафедры фармацевтической химии с курсом токсикологической химии фармацевтического факультета ММА им. И. М. Сеченова «Совершенствование контроля качества лекарственных средств» (№ государственной регистрации 01.200.110545).
Публикации
По результатам проведенных исследований опубликовано 5 печатных работ, в том числе одна в издании, рекомендованном ВАК РФ.
Основные положения, выносимые на защиту
- Условия ВЭЖХ-анализа изомеров атенолола в растворах и плазме крови с помощью хиральной колонки.
- Результаты содержания изомеров атенолола в субстанциях различных серий и препаратов (таблетки 50 мг) разных производителей.
- Динамика высвобождения изомеров атенолола из таблеток в условиях in vitro.
- Динамика концентрации и фармакокинетические параметры изомеров атенолола после однократного перорального приема.
Объем и структура диссертации
Диссертация состоит из введения, 5 глав, выводов и приложений; включает библиографический указатель из 147 источника, из которых 103 на иностранном языке.
Работа представлена на 120 страницах машинописного текста, содержит 33 таблицы и 28 рисунков.
Во введении обоснована актуальность проведенного исследования, сформулированы цель и задачи исследования, показаны научная новизна и практическая значимость работы.
Первая глава диссертационной работы посвящена обзору литературных данных по теме диссертации. Описаны теоретические основы изомерии, оптической активности. Показана взаимосвязь стереохимии с эффективностью и безопасностью лекарственных средств, описаны фармакокинетические различия в действии оптических изомеров различных лекарственных средств, в том числе атенолола. Проведен анализ методик определения изомеров.
Вторая и третья главы посвящены подбору условия для разделения и количественного определения изомеров атенолола. Описаны объекты исследования и тактика проведения фармакокинетического исследования. Приведены хроматографические и метрологические характеристики.
Четвертая глава посвящена изучению соотношения изомеров атенолола в субстанциях и таблетках, и их высвобождения в условиях in vitro.
Пятая глава содержит результаты фармакокинетического исследования изомеров атенолола после однократного перорального приема в виде таблеток разных производителей.
Результаты исследования
Объекты исследования.
- Образцы субстанций атенолола (таблица 1).
Таблица 1
Образцы субстанций атенолола
| № | Наименование образца | Производитель | Примечания |
| 1 | Атенолол – ЗАО «Скопифарм» | Производитель: «Ипка Лабораториз Лтд», Индия Серия 6052 А2 R11 | Срок годности: 02.2006 – 01.2011 |
| 2 | Атенолол – ЗАО «Фармацевтическое предприятие Оболенское» | Производитель: «Ипка Лабораториз Лтд», Индия Серия 5015 А2 М11 | Срок годности: 01.2005 – 12.2009 |
- Образцы таблеток атенолола по 50 мг разных производителей: Атенолол, Pliva Hrvatska d.o.o., Хорватия; Атенолол-ратиофарм, Ratiofarm GmbH, Германия; Атенолол Никомед, Nycomed Danmark AS, Дания; Атенолол, Скопинфарм, Россия; Атенолол-АКОС, Синтез АКО, Россия; Атенолол – ФПО, Оболенское фармацевтическое предприятие, Россия.
- Стандартные образцы изомеров атенолола. При разработке методики и фармакокинетическом исследовании в качестве стандартных образцов использовались R-атенолол и S-атенолол (каталог «Sigma-Aldrich» (таблица 2).
Фармакокинетическая часть выполнялась в рамках исследований по биоэквивалентности согласно Методическим указаниям «Проведение качественных исследований биоэквивалентности лекарственных средств» утвержденным Минздравсоцразвития России в 2004 году. Исследование осуществляли открытым методом по перекрестной и рандомизированной схеме. В качестве добровольцев были привлечены мужчины и женщины, добровольно изъявившие желание участвовать в исследовании. Критериями включения в исследование являлись: - возраст 18-45 лет, масса тела в пределах ± 20% от «идеальной» массы тела для данного пола, возраста и роста, отсутствие патологии желудочно-кишечного тракта, печени, почек, сердечно-сосудистой системы (по предварительным клинико-лабораторным и инструментальным исследованиям), наличие информированного согласия добровольца на включение в исследование.
Прием препаратов и отбора образцов крови осуществлялся согласно схеме, представленной в таблице 3.
Таблица 2
Структура изомеров атенолола (+/- Атенолол (4-(2-Гидрокси-3-[(1-метилэтил) амино] пропокси) бензолацетамид)
| S(-) Атенолол | R(+) Атенолол |
| С14H22N2O3 | |
 |  |
Таблица 3
Схема отбора образцов крови для фармакокинетического исследования
таблеток Атенолола 50 мг
| Время приема препарата, ч. - 8.00 | |||||||||||
| № образца | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| Время после приема, ч | 0 | 0,5 | 1 | 2 | 3 | 4 | 6 | 8 | 10 | 12 | 24 |
Добровольцы принимали внутрь, натощак одну таблетку 50 мг (R, S)-атенолола, запивая 200 мл воды. Спустя 4 часа после приема препарата испытуемые получали стандартный завтрак. Отбор крови производился непосредственно перед и в течение 24 часов после приема препарата.
Образцы крови отбирались из локтевой вены в количестве 10 мл в стеклянные пробирки с добавлением гепарина в интервалы времени в соответствии с утвержденным протоколом. Через 30 минут после отбора, пробы крови центрифугировали в течение 10 минут при 3000 об/мин, полученную плазму хранили в пробирках типа «эппендорф» при температуре -35оС до начала исследования.
Стабильность концентраций атенолола в плазме крови при -35°С в течение двух месяцев подтверждена экспериментально – в контрольных образцах с известным содержанием снижение определяемого вещества в течение всего срока хранения (9 недель) не регистрировалась.
При выборе оптимальных условий разделения изомеров атенолола был проанализирован ряд условий хроматографирования атенолола, такие как подвижная фаза, неподвижная фаза, выбор детектора и аналитической длины волны. Анализ проводился на хроматографе «Shimadzu C-R3A» с УФ - детектором. В качестве неподвижной фазы использовалась хиральная колонка LiChroCART 250-4 ChiraDex с размером частиц 5 m производства Merck KGaA (Darmstadt - Германия). Полученные нами спектры поглощения атенолола в УФ-области, подтвердили наличие максимумов поглощения при 255 нм и 285 нм. Учитывая максимальный коэффициент молярной экстинкции, нами была выбрана длина волны 282 нм.
При выборе скорости потока, руководствовались наиболее оптимальными скоростями, согласно уравнению Ван-Деемптера, для аналитической колонки с внутренним диаметром 4 мм, и размером частиц 5 мкм. То есть, скорость потока составляла 0,7 мл/мин (при оптимальном давлении 120 атм.). Объем введения при подходящей чувствительности - 50 мкл. С целью воспроизводимости времен удерживания, аналитическую колонку термостатировали при температуре 20 0С. Органическим компонентом подвижной фазы был выбран ацетонитрил, который по сравнению с другим часто применяемым растворителем - метанолом, имеет ряд преимуществ: более высокая температура кипения и меньшая вязкость. Ацетонитрил также характеризуется меньшим значением предела прозрачности в УФ - свете по сравнению с метанолом - 195 нм против 205 нм. Было исследовано влияние подвижной фазы различного состава на хроматографические характеристики разделения изомеров атенолола. При этом отношение ацетонитрила и водного компонента в элюентах, позволивших добиться приемлемых параметров разделения, составляло от 5:95 до 15:85, соответственно. Нами было исследовано несколько вариантов подвижных фаз. Состав выбранной подвижной фазы представлен в таблице 4.
Таблица 4
Состав подвижной фазы, использованной для разделения изомеров
атенолола
| Ацетонитрил | 0,03М KH2PO4 | Соотношение | Гексансульфонат натрия | Объем ПФ |
| 7 мл | 193 мл | 1:27 | 35 мг | 200 мл |
Для количественного определения изомеров атенолола готовили растворы сравнения R- и S- атенолола (R(+)- СО и S(-)-СО). Для приготовления растворов сравнения с концентрацией 0,1 мг/мл 10 мг каждого стандарта помещали в мерные колбы вместимостью 100 мл, доводили объем водой дистиллированной до метки (хранили в морозильной камере (-35С) в течение 3 месяцев) и рабочие растворы сравнения (R(+)- РСО и S(-)-РСО). Для приготовления рабочих растворов сравнения R- и S- атенолола с концентрацией 10 мкг/мл по 10 мл каждого раствора сравнения (R(+)- СО и S(-)-СО) помещали в мерную колбу вместимостью 100 мл, доводили объем водой дистиллированной до метки. R(+)- РСО и S(-)-РСО хранили в холодильной камере (+4С) в течение 2 недель.
На рисунке 1 представлена хроматограмма изомеров R,S – атенолола, полученная при УФ - детектировании – длина волны 282 нм.
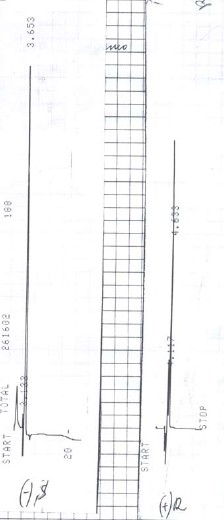
Рисунок 1. Хроматограмма стандартов изомеров R,S – атенолола
Сверху вниз: S - атенолол, R - атенолол.
Ниже представлены параметры разделения изомеров атенолола на выбранной подвижной фазе (ацетонитрил: фосфатный буфер 1:27, 35мг гексансульфоната натрия) (таблица 5).
Таблица 5
Параметры разделения, изомеров атенолола
| Определяемое вещество | tR, мин | K | N | As | R | |
| R-атенолол S-атенолол | 4,6 | 3,1 | 6500 | 0,95 | 0,75 | 1,4 |
| 5,8 | 4,1 | 6900 | 1,0 |
Согласно представленным данным коэффициенты ёмкости и разделения свидетельствуют о достаточном разделении пиков на хроматограмме.
Так как была установлена линейная зависимость между концентрацией изомеров атенолола в интервале 10 мкг/мл - 250 мкг/мл и площадью хроматографического пика, концентрацию соединения в пробах определяли методом абсолютной калибровки по калибровочной кривой. С целью количественной оценки содержания изомеров атенолола в образцах проб строили калибровочный график зависимости площади пика от концентрации препарата в диапазоне концентраций 10 – 250 мкг/мл (таблица 6).
Таблица 6
Результаты измерения площади пика стандартных растворов
+/-атенолола при длине волны 282 нм
| № п/п | концентрация стандартного раствора атенолола, мкг/мл | площадь пика S-атенолола, ед.инт | площадь пика R-атенолола, ед.инт | |
| 1 | 10 | 16094 | 14856 | |
| 2 | 25 | 23132 | 23051 | |
| 3 | 50 | 46326 | 41126 | |
| 4 | 75 | 74315 | 70128 | |
| 5 | 100 | 94025 | 93000 | |
| 6 | 125 | 124332 | 115139 | |
| 7 | 150 | 147275 | 148389 | |
| 8 | 175 | 171942 | 173365 | |
| 9 | 200 | 193503 | 198000 | |
| 10 | 250 | 243514 | 235148 | |
Калибровочная зависимость носила линейный характер (рисунки 2 и 3). Калибровочный график описывался линейным уравнением вида:
y = a + bx, где у – концентрация атенолола (мкг/мл);
х – площадь хроматографического пика атенолола.
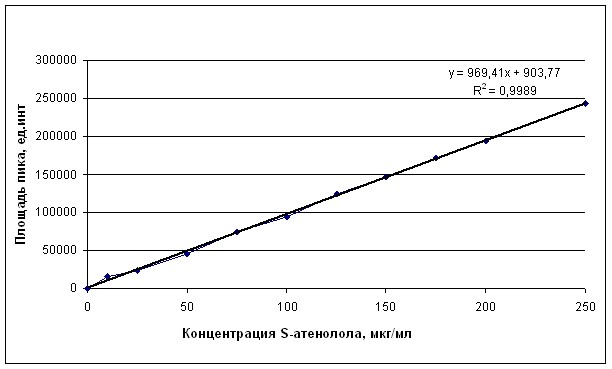
Рисунок 2. Калибровочный график зависимости площади пика от концентрации S-атенолола в диапазоне концентраций 10 – 250 мкг/мл.

Рисунок 3. Калибровочный график зависимости площади пика от концентрации R-атенолола в диапазоне концентраций 10 – 250 мкг/мл.
Величина коэффициента регрессии, оказалось близка к 1 как в случае анализа S- атенолола (r = 0,9989), так и в случае анализа R- атенолола (r = 0,9968).
Для оценки точности и воспроизводимости разработанной методики определения атенолола в растворе по результатам 10 параллельных измерений 5 концентраций препарата были рассчитаны метрологические характеристики метода (таблицы 7 и 8). Полученные результаты позволили говорить о достаточной точности разработанной методики количественного определения изомеров атенолола (относительная величина систематической ошибки не превышала 4,5 % для определения S-атенолола и 4,1 % для R-атенолола).
Разработанная методика была использована для определения содержания R,S- атенолола в образцах субстанций различных серий (таблица 9). Параметры пригодности хроматогафической системы, для исследованных образцов, представлены в таблице 10.
Таблица 7
Метрологические характеристики методики количественного определения S -атенолола (t(95%; 9) = 2,26)
| Концентрация стандартного раствора | 10 | 25 | 50 | 75 | 100 | |
| Содержание изомеров атенолола в стандартных растворах, мкг/мл | х1 | 9,1 | 25,2 | 52,2 | 76,6 | 103,5 |
| х2 | 11,0 | 23,2 | 48,8 | 78,8 | 105,5 | |
| х3 | 10,2 | 24,5 | 51,4 | 68,1 | 91,5 | |
| х4 | 8,9 | 27,1 | 48,8 | 73,2 | 107,4 | |
| х5 | 10,0 | 23,8 | 46,2 | 77.4 | 96,3 | |
| х6 | 10,2 | 26,3 | 44,3 | 78,5 | 103,2 | |
| х7 | 10,1 | 24,8 | 52,8 | 76,3 | 102,4 | |
| х8 | 9,9 | 27,1 | 54,0 | 77,2 | 101,7 | |
| х9 | 10,7 | 24,7 | 53,3 | 75,3 | 98,8 | |
| х10 | 10,3 | 23,9 | 51,1 | 72,1 | 99,1 | |
| Результаты статистической обработки полученных данных | хi | 10,0 | 25,1 | 50,3 | 75,4 | 100,9 |
| s | 0,64 | 1,4 | 3,2 | 3,3 | 4,7 | |
| s | 0,41 | 1,9 | 10,2 | 11,1 | 21,7 | |
| x | 0,4 | 0,8 | 1,9 | 2,1 | 2,9 | |
| хi ± xср | 10,0±0,2 | 25,1±0,4 | 50,3±1,0 | 75,4±1,1 | 100,9±1,5 | |
| ср, % | 4,5% | 3,9% | 4,5% | 3,2% | 3,3% | |
Таблица 8
Метрологические характеристики методики количественного определения R -атенолола (t(95%; 9) = 2,26)
| Концентрация стандартного раствора | 10 | 25 | 50 | 75 | 100 | |
| Содержание изомеров атенолола в стандартных растворах, мкг/мл | х1 | 9,5 | 26,1 | 51,2 | 74,2 | 99,8 |
| х2 | 10,2 | 24,2 | 49,1 | 76,6 | 101,2 | |
| х3 | 10,4 | 24,7 | 51,4 | 73,4 | 103,1 | |
| х4 | 9,3 | 24,3 | 49,2 | 76,1 | 94,6 | |
| х5 | 10,6 | 25,2 | 47,1 | 75,3 | 97,2 | |
| х6 | 10,1 | 26,3 | 53,2 | 74,6 | 101,9 | |
| х7 | 10,5 | 24,7 | 52,8 | 75,3 | 103,4 | |
| х8 | 9,7 | 23,8 | 54,1 | 74,8 | 100,9 | |
| х9 | 10 | 25,4 | 54,6 | 73,8 | 97,2 | |
| х10 | 9,5 | 25,9 | 57,1 | 77,1 | 99,6 | |
| Результаты статистической обработки полученных данных | хi | 9,98 | 25,06 | 52,07 | 75,12 | 99,89 |
| s | 0,46 | 0,85 | 2,97 | 1,2 | 2,82 | |
| s | 0,21 | 0,736 | 8,871 | 1,45 | 7,994 | |
| x | 0,284 | 0,531 | 1,846 | 0,746 | 1,752 | |
| хi ± xср | 9,98±0,145 | 25,06±0,271 | 52,07±0,941 | 74,2±0,380 | 99,89±0,894 | |
| ср, % | 3,28% | 2,44% | 4,08% | 1,14% | 2,02% | |
Таблица 9
Хроматографические параметры разделения изомеров атенолола
| Параметр | Атенолол субстанция – ЗАО «Скопинфарм» | Атенолол субстанция – ЗАО «Фармацевтическое предприятие Оболенское» |
| Коэффициент емкости (k) | kR=0.58 kS=1.01 | kR=0.52 kS=1.08 |
| Число теоретических тарелок (N) | R 6900 S 6500 | R 6900 S 6500 |
| Селективность () | 1,74 | 2,07 |
| Степень разделения, разрешение (R) | 2,3 | 3,5 |
Таблица 10
Хроматографические характеристики и параметры пригодности системы.
| Лекарственное вещество | tR,мин S -атенолола | ts, мин R-атенолола | S/N | RSD% | As | N |
| Атенолол субстанция – ЗАО «Скопинфарм» | 3,558 | 4,778 | 3 | 2,5% | 0,95 | 6500 |
| Атенолол субстанция – ЗАО «Фармацевтическое предприятие Оболенское» | 3,458 | 4,917 | 3 | 2,5% | 1,05 | 6500 |
На рисунках 4 и 5 представлены образцы полученных хроматограмм.


Рисунок 4. Хроматограмма субстанции атенолола – ЗАО «Скопинфарм».


Рисунок 5. Хроматограмма субстанции атенолола – ЗАО «Фармацевтическое
предприятие Оболенское».
Как видно из представленных рисунков, в указанных условиях наблюдается хорошее отделение пика одного изомера от другого.
Результаты количественного определения изомеров атенолола в субстанциях представлены в таблице 11.
Таблица 11
Результаты исследования субстанций атенолола
| ЛС | R-атенолол | S-атенолол |
| Атенолол субстанция – ЗАО «Скопинфарм» | 41,2 % | 58,8 % |
| Атенолол субстанция – ЗАО «Фармацевтическое предприятие Оболенское» | 40,5 % | 59,5 % |
Согласно проведенному исследованию различия в содержании S-атенолола и R-атенолола были статистически не достоверными (р > 0,05).
Таким образом, получено, что различные серии субстанции одного производителя при соблюдении технологии не содержат различий в соотношении изомеров. Однако это соотношение может изменяться в процессе изготовленя лекарственной формы. Поэтому, последующей целью было определение, содержат ли таблетки атенолола необходимое количество левого – «активного» изомера и как он высвобождается в условиях in vitro и in vivo.
Для изучения высвобождения изомеров атенолола in vitro из таблеток различных производителей использовали прибор ERWEKA DT600 - «лопастная мешалка». Тест «растворение» проводили в соответствии с требованиями ОФС 42 0003 – 00 «Растворение». Объем среды растворения составлял 900 мл, температура 37 ± 0,5оС, скорость вращения 75 об/мин, время растворения 30 минут. Среда растворения: вода.
Результаты определения высвобождения R-,S- атенолола из таблеток приведены в таблице 12.
Таблица 12
Кинетика высвобождения атенолола из таблеток (n=6)
| Производитель | Высвобождение, % | ||||||
| 5 | 10 | 15 | 20 | 25 | 30 | ||
| Pliva Hrvatska d.o.o. | R | 44 | 63 | 75 | 80 | 83 | 87 |
| S | 45 | 63 | 78 | 81 | 84 | 85 | |
| Ratiofarm GmbH | R | 43 | 63 | 76 | 80 | 84 | 86 |
| S | 42 | 64 | 75 | 80 | 83 | 86 | |
| Nycomed Danmark AS | R | 46 | 68 | 77 | 81 | 85 | 87 |
| S | 45 | 65 | 75 | 79 | 84 | 86 | |
| Синтез | R | 32 | 50 | 60 | 67 | 70 | 72 |
| S | 36 | 55 | 64 | 69 | 72 | 74 | |
| Скопинфарм | R | 31 | 45 | 57 | 63 | 66 | 68 |
| S | 15 | 33 | 40 | 45 | 53 | 70 | |
| Оболенское ФП | R | 27 | 44 | 55 | 58 | 61 | 64 |
| S | 26 | 41 | 51 | 56 | 59 | 62 | |
На рисунке 6 представлена кинетика высвобождения R- атенолола.
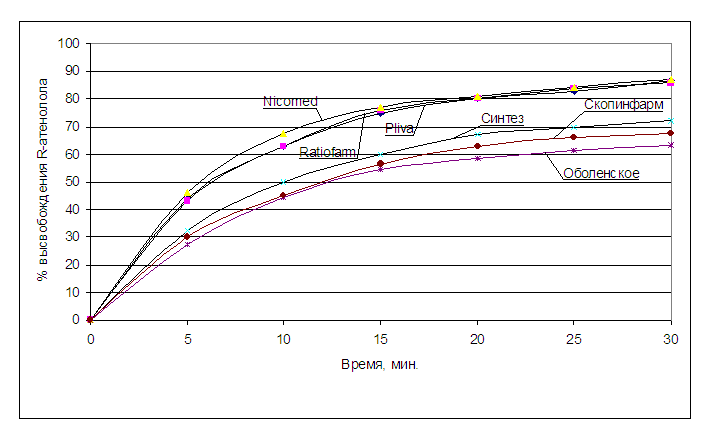
Рисунок 6. Усреднённая кинетика высвобождения R- атенолола in vitro из
таблеток разных производителей.
На рисунке 7 представлена кинетика высвобождения S- атенолола.
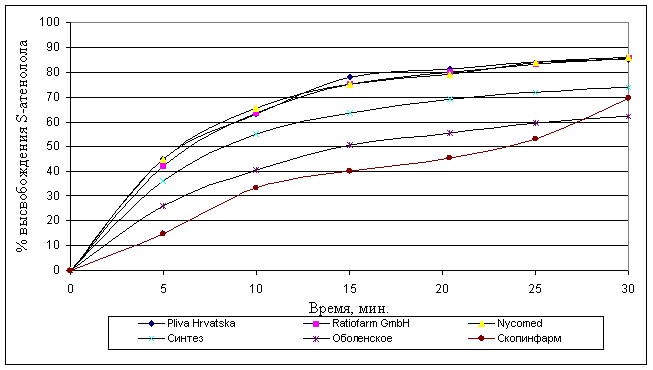
Рисунок 7. Усреднённая кинетика высвобождения S- атенолола in vitro из
таблеток различных производителей.
Как видно из графиков, кинетика высвобождения R- и S- изомеров атенолола из таблеток разных производителей имеет сходный профиль, однако отличается по скорости и степени высвобождения R- и S- атенолола.
Для изучения соотношения содержания изомеров в зарегистрированных таблетках атенолола разных производителей, атенолол извлекали из таблеток следующим образом. Взвешивали 10 таблеток Атенолола 50 мг, измельчали и помещали их в мерную колбу вместимостью 100 мл, добавляли 100 мл подвижной фазы. Встряхивали раствор в течение 25 минут и подвижной фазой доводили объём до метки. После этого раствор фильтровали через стекловолокнистый фильтр, отбрасывая первые 5 мл фильтрата. 1 мл фильтрата, переносили в мерную колбу вместимостью 20 мл и доводили объем раствора до метки подвижной фазой (раствор А). Хранили раствор в защищённом от света месте. Раствор использовали в течение одного дня. Количественный анализ проводили методом ВЭЖХ с хиральной колонкой LiChroCART 250-4 ChiraDex с УФ – детектором при длине волны 282 нм. Для количественного определения изомеров атенолола проводили хроматографирование испытуемого раствора и растворов сравнения. Содержание атенолола в расчете на среднюю массу таблетки проводили по следующей формуле: m = At x n x 200мл, где:
Ar
At – площадь пика R/S-атенолола на хроматограмме испытуемого раствора;
Ar – площадь пика R/S-атенолола на хроматограмме раствора сравнения;
n – содержание атенолола в растворе сравнения, мг/мл.
В результате исследования таблеток атенолола было установлено, что количественный состав изомеров различен (таблица 13).
Таблица 13
Содержание изомеров атенолола в таблетках
| Производитель | R-изомер, % | S-изомер, % |
| Pliva Hrvatska d.o.o., Хорватия | 76 | 24 |
| Ratiofarm GmbH, Германия | 58 | 42 |
| Nycomed Danmark AS AS, Дания | 56 | 44 |
| Атенолол – ФПО, Россия | 75 | 25 |
| Синтез, Россия | 63 | 37 |
| Скопинфарм, Россия | 53 | 47 |
Из представленных данных следует, что таблетки атенолола содержат как S-, так и R-энантиомеры в различных количествах.
Подготовку проб для фармакокинетического исследования проводили следующим способом: к 1 мл плазмы прибавляли 1 мл хлороформа, смесь встряхивали на механическом шейкере в течение 1 минуты, затем центрифугировали в течение 5 минут при 3000 об/мин, отбирали надосадочную жидкость, упаривали, сухой остаток растворяли в 150 мкл подвижной фазы. Через 10 минут аликвоту (100 мкл) вводили в хроматограф. Пробы готовили непосредственно перед анализом. Разделение проводили на колонке «ChiraDex» LiChroCART 250-4 при комнатной температуре. В качестве подвижной фазы использовали смесь ацетонитрила и буферного раствора в соотношении 27:1 (об/об) с добавлением гексансульфоната натрия (буферный раствор содержал 190 мл дигидрофосфата калия рН 4,9). Минимальная определяемая концентрация – 10 нг/мл. Относительная погрешность определения изомеров атенолола при его концентрации от 10 до 50 нг/мл составляла 13,8 %; при концентрации от 50 до 100 нг/мл – 8,5 %. Индивидуальные профили изменения концентрации (С) изомеров атенолола в плазме крови во времени (t), зарегистрированные после приема таблеток атенолола, характеризовали максимальной концентрацией лекарственного вещества (Cmax, наибольшее из измеренных значений) и временем её достижения (tmax), а также площадью под кривой «концентрация – время» в пределах от нуля до момента отбора последней пробы крови (t = 24 ч), рассчитанной методом трапеций (AUC24h).
Время достижения максимальной концентрации для всех препаратов колебалось в интервале времени 3-6 часов. Во всех исследуемых препаратах наибольшие значения концентрации наблюдались для R-изомера, что может быть связано с тем, что атенолол оказывает антиадренергическое действие в неизменённом виде, накапливаясь и выделяясь симпатическими терминалями преимущественно за счет S-изомера, при этом выделяется из организма в неизменённом виде только S-изомер атенолола, в то время как R-изомер накапливается в организме.
На рисунках 8 и 9 представлены фармакокинетические кривые R- и S- атенолола. 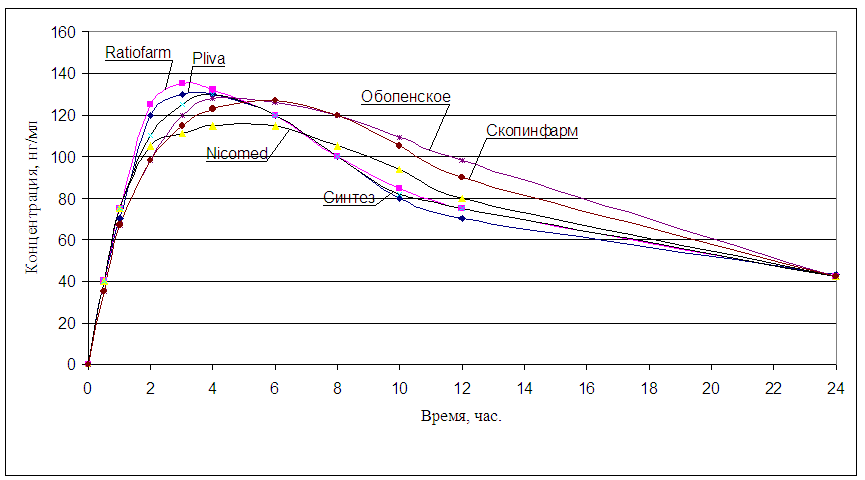
Рисунок 8. Динамика содержания R-атенолола в плазме крови.
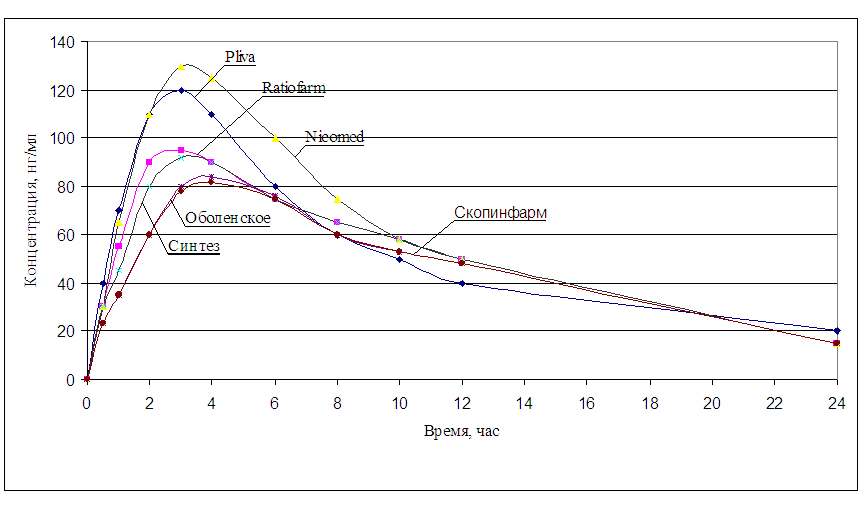
Рисунок 9. Динамика содержания S-атенолола в плазме крови.
Основные фармакокинетические параметры изомеров атенолола представлены в таблице 14.
Таблица 14
Значения фармакокинетических параметров (R,S)-атенолола
разных производителей
| Препарат | Cmax, нг/мл | tmax, час | AUC, нг*ч/мл | t1/2, час | ||||
| R | S | R | S | R | S | R | S | |
| Pliva, Хорватия | 130 | 120 | 3 | 3 | 2543 | 1867 | 6,5 | 5,5 |
| Ratiofarm, Германия | 135 | 95 | 3 | 3 | 2134 | 1956 | 8,2 | 6,5 |
| Nycomed, Дания | 115 | 130 | 4 | 3 | 2806 | 1695 | 9,0 | 6,0 |
| Синтез, Россия | 130 | 92 | 4 | 3 | 1856 | 1759 | 6,5 | 4,5 |
| Скопинфарм, Россия | 127 | 82 | 6 | 4 | 2594 | 1534 | 7,0 | 8,0 |
| Оболенское ФП, Россия | 128 | 84 | 4 | 4 | 2645 | 1598 | 7,0 | 8,0 |
Общие выводы
- Разработана методика определения R- и S- изомеров атенолола в растворах и плазме крови методом ВЭЖХ с применением УФ – детектора и хиральной неподвижной фазы (колонки), что позволило добиться разделения изомеров атенолола.
- Определено соотношение R- и S- изомеров атенолола в субстанциях различных серий (содержание R-изомера составляет в среднем 40-42%, а содержание S-изомера около 58-59 %). Показано, что в различных сериях одного производителя, соотношение R- и S- изомеров статистически достоверно не различалось.
- Определено процентное содержание R- и S- изомеров в таблетках разных производителей. Установлено, что соотношение R- и S- изомеров атенолола в препаратах, выпущенных на разных производствах, достоверно различается, что может быть связано с различиями в технологии изготовления.
- Изучено высвобождение R- и S- атенолола из таблеток в условиях in vitro. Определено, что степень и скорость высвобождения R- и S- атенолола у препаратов, выпущенных на разных производствах, может достоверно различаться.
- Изучена фармакокинетика R- и S- атенолола в плазме крови добровольцев после перорального приема таблеток атенолола разных производителей. Показано, что уровни R- и S- изомеров атенолола в крови могут статистически достоверно отличаться при приеме препаратов разных производителей.
Список работ, опубликованных по теме диссертации
- Чугаев Д.В., Красных Л.М., Смирнова И.Г. Аналитические подходы к изучению фармакокинетических особенностей оптических изомеров лекарственных средств// Биомедицина. – 2006. - №5. - С. 51.
- Чугаев Д.В., Раменская Г.В. Влияние оптических изомеров различных лекарственных средств на их фармакокинетику // Материалы VIII конгресса молодых ученых и специалистов «Науки о человеке» - Томск: СибГМУ. - 2007. - С. 141-142.
- Чугаев Д.В, Раменская Г.В. Влияние оптических изомеров на фармакокинетику лекарственных средств // Фармация. - 2008. - №1. - С. 50 - 52.
- Чугаев Д.В, Раменская Г.В. Разработка методики разделения изомеров атенолола с помощью метода ВЭЖХ // Материалы XV Рос. нац. конф. "Человек и лекарство". – Москва. - 2008. - С. 729.
- Чугаев Д.В, Раменская Г.В. Разделение и определение изомеров с использованием метода ВЭЖХ // Мат. конф. «Фармация и общественное здоровье». - Екатеринбург. - 2008. - С. 316 – 318.

