Фармакогностическое изучение вереска обыкновенного ( calluna vulgaris ( l.) hull.)
На правах рукописи
Онегин Сергей Владимирович
Фармакогностическое изучение
вереска обыкновенного (Calluna vulgaris (L.) Hull.)
15.00.02 – фармацевтическая химия, фармакогнозия
Автореферат
диссертации на соискание ученой степени
кандидата фармацевтических наук
Пермь – 2008
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Ярославская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию РФ».
Научный руководитель – доктор фармацевтических наук,
профессор Фурса Николай Сергеевич
Официальные оппоненты – доктор фармацевтический наук,
профессор Петриченко Василий Михайлович
– доктор фармацевтических наук
профессор Сорокина Алла Анатольевна
Ведущая организация – ГУП ВПО «Рязанский государственный
медицинский университет Федерального агентства
по здравоохранению и социальному развитию РФ»
Защита состоится «18» марта 2008 г. в _____ часов на заседании Диссертационного совета Д 208.068.01 при Государственном образовательном учреждении высшего профессионального образования «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию РФ» по адресу: 614600, г. Пермь, ул. Ленина, д. 48.
С диссертацией можно ознакомится в библиотеке Пермской государственной фармацевтической академии по адресу: г. Пермь, ул. Крупской, д. 46.
Отзыв на автореферат просьба отправлять по адресу Диссертационного совета.
Автореферат разослан «____» февраля 2008 г.
Ученый секретарь
Диссертационного совета Д 208.068.01,
кандидат фармацевтических наук,
доцент Е.В. Метелева
общая характеристика работы
Актуальность темы.
Заболевания сердечно-сосудистой, нервной, пищеварительной и других систем прогрессируют в современном обществе, что нередко связано с ухудшением экологической обстановки. В связи с этим важным направлением фармацевтической науки является поиск безопасных, экологически чистых, не вызывающих побочных эффектов и привыкания препаратов. В этом аспекте заслуживают внимания лекарственные растения, т.к. они не обладают теми недостатками, которые свойственны многим средствам синтетического происхождения. Перспективным для использования в научной медицине растением является вереск обыкновенный (Calluna vulgaris (L.) Hull.), довольно распространенный в РФ и за рубежом. Он занимает большие площади и запасы его значительные (Ареалы деревьев и кустарников СССР, 1986). В отечественной народной медицине вереск применяют довольно широко. Он оказывает мочегонное, противовоспалительное, противомикробное, успокаивающее и другие виды действия. В некоторых странах, например, в Германии и Франции вереск является фармакопейным растением. Несмотря на это, его побеги все еще недостаточно изучены с точки зрения химического состава и фармакологического действия.
Цель и задачи исследования.
Целью работы явилось фармакогностическое изучение побегов вереска обыкновенного из различных мест произрастания на территории Российской Федерации и ближнего зарубежья и разработка методов их стандартизации.
Для выполнения поставленной цели следовало решить следующие задачи:
- провести критический анализ данных литературы по современному состоянию морфолого-анатомических и химико-фармакологических исследований вереска обыкновенного,
- предпринять изучение его химического состава, в частности веществ первичного (аминокислоты, моно- и полисахариды) и вторичного обмена (арбутин, гидроксикоричне кислоты, флавоноиды, полифенольные окисляемые соединения),
- разработать методики количественного определения отдельных классов фенольных соединений в сырье изучаемого растения,
- определить количественное содержание веществ первичного и вторичного обмена в побегах вереска из различных мест произрастания на территории РФ и ближнего зарубежья,
- проанализировать сезонную динамику накопления фенольных соединений для определения оптимальных сроков заготовки сырья,
- исследовать морфолого-анатомические признаки надземных и подземных органов вереска обыкновенного,
- определить основные числовые показатели побегов вереска и составить нормативную документацию (ФСП, ТУ) на них,
- выявить «острую токсичность» побегов вереска и возможности его использования в медицине.
Научная новизна работы.
Впервые проведен углубленный фитохимический анализ побегов вереска обыкновенного, а также выявлены морфолого-анатомические признаки отдельных надземных и подземных органов изучаемого растения. С использованием современных методов (хромато-масс-спектрометрия, ВЭЖХ) проанализирован химический состав органических фракций извлечения надземных органов.
Разработаны методики количественного определения арбутина и гидроксикоричных кислот (хромато-спектрофотометрически и прямой спектрофотометрией), флавоноидов (спектрофотометрически по реакции комплексообразования с алюминия хлоридом) и проведены исследования по стандартизации побегов вереска.
Впервые определено содержание фенольных соединений в сырье вереска, заготовленного в 40 различных регионах РФ, Республике Беларусь и в Украине.
На основании аналитических исследований разработаны Фармакопейная статья предприятия (ФСП) и Технические условия (ТУ) «Побеги вереска».
Впервые изучена сезонная динамика накопления некоторых фенольных соединений в надземной части вереска.
Практическая значимость работы.
Предложены методики стандартизации побегов вереска, позволяющие объективно оценивать их доброкачественность. Результаты качественного обнаружения и количественного определения основных групп ФАВ внедрены и используются в учебном процессе кафедр фармакогнозии Рязанского государственного медицинского университета (акт о внедрении №12 от 16.02.07 г.) и Московской медицинской академии им. И.М. Сеченова (акт о внедрении №47 от 23.04.07 г.).
Разработаны методики количественного определения суммы флавоноидов, суммы гидроксикоричных кислот и арбутина в сырье вереска.
Результаты исследований положены в основу фармакопейной статьи предприятия и технических условий «Побеги вереска» (Ивановская фармацевтическая фабрика, акт о внедрении от 08.02.2006 г.).
Положения, выносимые на защиту:
- итоги изучения химического состава веществ первичного и вторичного обмена побегов вереска обыкновенного,
- результаты морфолого-анатомического исследования надземных и подземных органов упомянутого растения,
- экспериментальные данные по обоснованности использования методики хромато-спектрофотометрического определения арбутина.
Апробация работы.
Основные положения работы доложены и обобщены: на научно-практической конференции, посвященной 85-летию высшего образования на Урале (Пермь, 2001), конгрессе молодых ученых «Науки о человеке» (Томск, 2003), X Российском национальном конгрессе «Человек и лекарство» (Москва, 2003), на ежегодных научных конференциях студентов и молодых ученых Ярославской государственной медицинской академии (Ярославль, 2001-2007); на совместном заседании кафедры фармакогнозии, фармацевтической химии, управления и экономики фармации, фармацевтической технологии фармацевтического факультета ЯГМА (Ярославль, 2007), на научно-практической конференции, посвященной 25-летию фармацевтического факультета ЯГМА (Ярославль, 2007).
Публикации материалов исследования.
По теме диссертации опубликовано 26 работ, из них 6 в журналах. Составлено и издано учебное пособие для преподавателей и студентов на тему «Экологическая оценка техногенного загрязнения Ярославской области», предназначенное для подготовки к занятиям по экологии.
связь задач исследования с проблемным планом фармацевтических наук.
Диссертационная работа выполнена в соответствии с планом научных исследований Ярославской государственной медицинской академии (номер государственной регистрации 01.20.0211931).
Объем и структура диссертации.
Работа изложена на 116 страницах машинописного текста и состоит из введения, обзора литературы (1 глава), материалов и методов (2 глава), экспериментальной части (4 главы), общих выводов, списка литературы и приложения; иллюстрирована 34 рисунками и 34 таблицами. Список литературы включает 186 источников, из них 44 на иностранных языках.
Во введении обоснована актуальность выбранной темы, определены цели и задачи исследования, показана научная и практическая значимость работы.
В обзоре литературы (первая глава) отражено современное состояние данных по химико-фармакологическому изучению и применению в медицине вереска обыкновенного.
Во второй главе приведены материалы и описаны основные методики качественного и количественного анализа.
В третьей главе изложены результаты изучения состава и количественного определения веществ первичного обмена (аминокислот и полисахаридов) вереска.
В четвертой главе обобщены материалы по качественному обнаружению и количественному определению фенольных соединений (фенологликозидов, гидроксикоричных кислот, флавоноидов и полифенольных окисляемых соединений), по изучению сезонной динамики накопления действующих веществ, а также по хромато-масс-спектрометрическому анализу природных соединений побегов вереска.
Пятая глава посвящена морфолого-анатомическому изучению надземных и подземных органов исследуемого растения и товароведческому анализу побегов вереска, а также разработке на них нормативной документации.
В шестой главе отражены результаты определения «острой токсичности» побегов вереска, а также некоторые аспекты создания отдельных лекарственных форм на основе изучаемого растения и их стандартизация.
Приложение включает проект ФСП и ТУ «Побеги вереска», отчет об определении острой токсичности побегов вереска и другие материалы, подтверждающие практическую значимость проведенных исследований.
с о д е р ж а н и е р а б о т ы
объекты и методики исследования
Для изучения качественного состава и количественного содержания веществ первичного и вторичного обмена, а также морфолого-анатомических признаков нами заготовлено более 50 образцов побегов вереска обыкновенного в различных регионах РФ, в Республике Беларусь и в Украине. Сушка сырья воздушно-теневая, для морфолого-анатомического исследования проводилась консервация живого материала на месте сбора. При этом использовали как классические, так и современные методы исследований, в частности спектрофотометрию (СФ-56), фотоэлектроколориметрию (КФК-2), БХ, хромато-масс-спектрометрию (газовый хроматограф 6850 с масс-селективным детектором 5973 фирмы Agilent Technologies), ВЭЖХ (Милихром).
вещества первичного обмена
Вначале мы предприняли изучение качественного состава и провели количественное определение веществ первичного обмена (аминокислот, моно- и полисахаридов).
аминокислоты. Для первоначального обнаружения качественного состава аминокислот побегов вереска обыкновенного использовали БХ в системе н. бутанол-уксусная кислота-вода (4:1:2) с достоверными образцами, в результате которого отметили, что количество аминокислот варьировало в зависимости от органов растения от 6 до 12. При этом их наибольшее количество выявили в цветках. Анализ свободных и связанных аминокислот провели на аминокислотном анализаторе ААА-339 (ЧССР) в стандартных условиях (табл. 1).
полисахариды. Для изучения качественного и количественного состава полисахаридов побегов вереска обыкновенного получали их фракции. После экстракции спиртом из шрота побегов выделили фракции водорастворимых полисахаридов (ВРПС) и пектинов. Их выход
Таблица 1 – Содержание свободных и связанных аминокислот в надземных органах вереска обыкновенного
| Кислота | Содержание аминокислот, мг% | |||||
| свободных | связанных | |||||
| стебли | цветки | листья | стебли | цветки | листья | |
| Аспарагин | 0,362 | 0,594 | 0,070 | 2,894 | 6,464 | 1,916 |
| Треонин | 0,770 | 2,245 | 0,067 | 3,020 | 2,661 | 1,838 |
| Серин | 0,745 | — | 0,095 | |||
| Глутамин | 0,589 | 0,746 | 0,205 | 5,125 | 4,719 | 2,899 |
| Глицин | 0,137 | 0,309 | 0,147 | 1,854 | 1,712 | 1,536 |
| Аланин | 1,585 | 1,226 | 0,148 | 2,655 | 2,365 | 1,672 |
| Валин | 0,156 | 0,405 | 0,494 | 0,960 | 1,254 | 0,307 |
| Метионин | 0,236 | — | — | 0,628 | — | 0,119 |
| Изолейцин | — | 3,323 | — | 3,076 | 4,256 | 0,192 |
| Лейцин | 1,610 | — | 0,860 | |||
| Тиронин | 0,098 | 1,539 | 0,353 | 0,575 | 0,596 | 0,385 |
| Фенилаланин | 0,690 | 0,140 | — | 5,560 | 5,050 | 0,270 |
| Лизин | 3,777 | 0,480 | 0,335 | 1,323 | — | 4,994 |
| Гистидин | 3,876 | 5,119 | 0,157 | 1,334 | 3,491 | 5,191 |
| Аргинин | 1,469 | 1,731 | 0,495 | 6,570 | 7,385 | 6,320 |
| Сумма кислот | 16,100 | 17,857 | 3,426 | 35,574 | 39,953 | 27,639 |
соответственно равнялся 5,29 и 11,38%. При количественном определении установили, что содержание восстанавливающих сахаров в гидролизате водорастворимой фракции составило 2,3%, а в гидролизате фракции пектинов – 1,14%, содержание кислых сахаров – 1,79 и 3,44% соответственно (табл. 2).
Таблица 2 – Результаты качественного обнаружения и количественного определения полисахаридов побегов вереска
| Фракция полиса- харидов | Описание комплекса | Раство- римость в воде | Зола общая | Зола, нераство-римая в 10% HCl | Состав моносахаридов | Содержание полисахаридов | ||
| Выход, % от воздушно-сухого сырья | Моносахаридов, % от навески | |||||||
| кислых | восстанавливающих | |||||||
| Водо- раство- римые полисахариды | Аморфный порошок коричне- вого цвета | Умерен- но растворимый | 4,797 | 0,521 | Галактоза, глюкоза, ксилоза, рамноза, галактуроновая и глюкуроновая кислоты. | 5,29 | 1,79 | 2,3 |
| Пектины | Аморфный порошок светло- серого цвета | Умерен- но растворимый | 3,865 | 0,302 | Глюкоза, фруктоза, арабиноза, рамноза, галактуроновая и глюкуроновая кислоты. | 11,38 | 3,44 | 1,14 |
При анализе одномерной БХ в системах растворителей этилацетат-пиридин-вода (12:1:21) и н. бутанол-уксусная кислота-вода (4:1:2) выявили различия в качественном составе полученных полисахаридов. Общими для обеих фракций являлись глюкоза, рамноза, галактуроновая и глюкуроновая кислоты, дополнительно фракция ВРПС содержала галактозу и ксилозу, а фракция пектинов – фруктозу и арабинозу.
вещества вторичного обмена
При исследовании веществ вторичного обмена первоначально двумерной БХ мы проанализировали качественный состав фенольных соединений надземных органов вереска обыкновенного. При этом нами обнаружено 18 веществ флавоноидной природы, среди гидроксикоричных кислот – не менее 8 веществ, из которых по окраске до и после проявления, по значению Rf при сравнении с достоверными образцами предварительно идентифицировали кверцетин, гиперозид и хлорогеновую кислоту. Причем на основании площади пятен и интенсивности их окрасок после проявления диагностическими реактивами отмечено, что они являются доминирующими фенольными соединениями побегов вереска.
Уточнение данных двумерной хроматографии гидроксикоричных кислот провели на отечественном жидкостном микроколоночном хроматографе «Милихром-4» НПО «Научприбор» (г. Орел), в ходе которого полностью подтвердили, что преобладающей гидроксикоричной кислотой побегов вереска являлась хлорогеновая (табл. 3, рис. 1). Кроме нее, в весьма значительных концентрациях определены хинная и кофейная кислоты, в минимальной концентрации обнаружена феруловая кислота.
 | Рис. 1. Хроматограмма ВЭЖХ-анализа побегов вереска Условные обозначения гидроксикоричных кислот: 1 – хлорогеновая, 2 – кофейная, 3 – феруловая, 4 – хинная. |
Таблица 3 – Содержание гидроксикоричных кислот в побегах вереска обыкновенного
| Кислота | Содержание в образце, мг/мл извлечения | Кислота | Содержание в образце, мг/мл извлечения |
| Хинная | 0,22 | Феруловая | 0,02 |
| Кофейная | 0,12 | Хлорогеновая | 0,45 |
Для подтверждения данных двумерной хроматографии провели выделение флавоноидов в индивидуальном состоянии колоночной хроматографией на полиамиде с дальнейшим их физико-химическим изучением. Так, при исследовании выделенных веществ в УФ-области спектра в присутствии ионизирующих и комплексообразующих реагентов и анализе их ПМР-спектров вещество I охарактеризовали как 3,5,7,4’-тетраоксифлавон (кемпферол), вещество II – как 3,5,7,3’,4’-пентаоксифлавон (кверцетин), вещество III – как 3-О--D-глюкозид кемпферола (астрагалин), вещество IV – как 3-О--D-галактозид кверцетина (гиперозид), вещество V – как 3,5,7,8,4’-пентаоксифлавон (гербацетин), вещество VI – как 8-О--D-глюкозид гербацетина и вещество VII – как 3-О--D-глюкозид кверцетина (изокверцитрин). Их структурные формулы отражены в таблице 4.
Таблица 3 – Структурные формулы отдельных флавоноидов побегов вереска
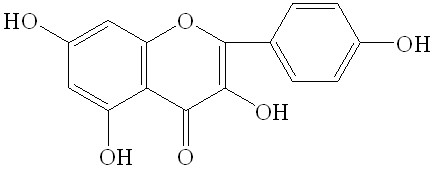 Вещество I – 3,5,7,4’-тетраоксифлавон (кемпферол) Вещество I – 3,5,7,4’-тетраоксифлавон (кемпферол) | 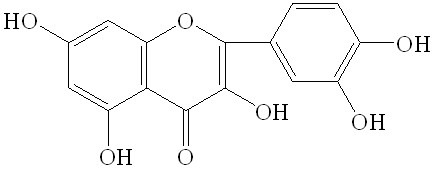 Вещество II – 3,5,7,3’,4’-пентаоксифлавон (кверцетин) Вещество II – 3,5,7,3’,4’-пентаоксифлавон (кверцетин) | |
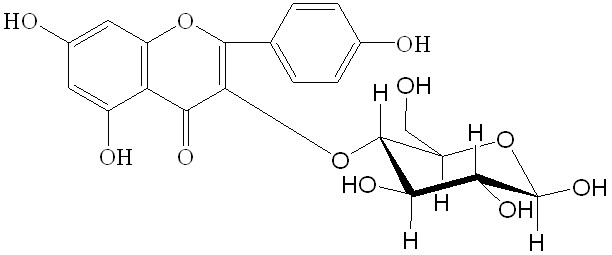 Вещество III – 3-О--D-глюкозид кемпферола (астрагалин) Вещество III – 3-О--D-глюкозид кемпферола (астрагалин) |  Вещество IV – 3-О--D-галактозид кверцетина (гиперозид) Вещество IV – 3-О--D-галактозид кверцетина (гиперозид) | |
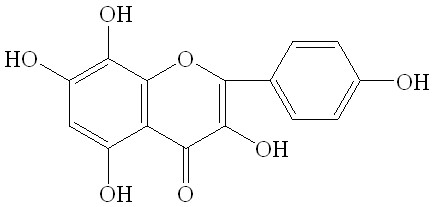 Вещество V – 3,5,7,8,4’-пентаоксифлавон (гербацетин) Вещество V – 3,5,7,8,4’-пентаоксифлавон (гербацетин) | ||
 Вещество VI – 8-О--D-глюкозид гербацетина Вещество VI – 8-О--D-глюкозид гербацетина |  Вещество VII – 3-О--D-глюкозид кверцетина (изокверцитрин) Вещество VII – 3-О--D-глюкозид кверцетина (изокверцитрин) | |
Для выявления и подтверждения преобладающих компонентов суммы гидроксикоричных кислот и суммы флавоноидов провели сравнение спектров поглощения для гидроксикоричных кислот извлечения побегов вереска и стандартов кислот (кофейной, феруловой, хлорогеновой), для флавоноидов – комплексов извлечения вереска, кверцетина-стандарта и гиперозида-стандарта с алюминия хлоридом. Совпадение максимумов спектров поглощения извлечения вереска и стандартов хлорогеновой кислоты и кверцетина (рис. 2 и 3) позволили использовать их в качестве стандартных веществ.
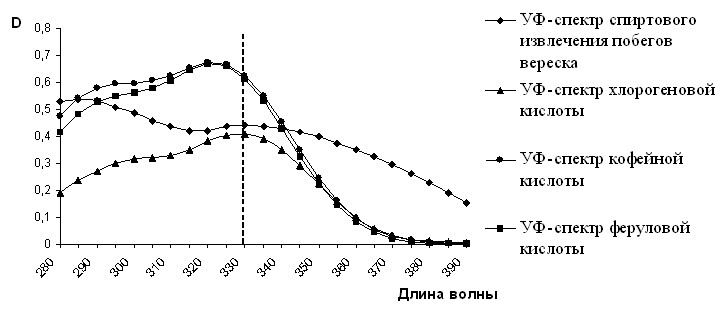
Рис. 2. УФ-спектры поглощения спиртового извлечения побегов вереска
и стандартов гидроксикоричных кислот
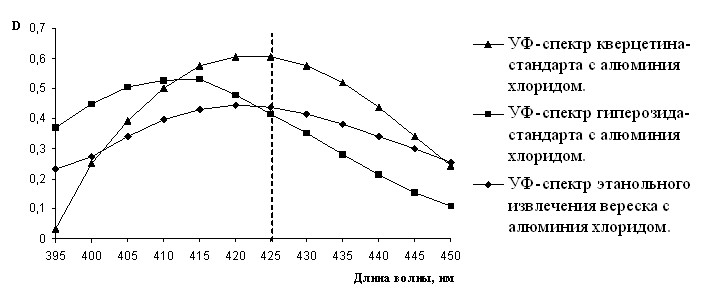
Рис. 3. УФ-спектры поглощения комплексов кверцетина-стандарта, гиперозида-стандарта
и этанольного извлечения побегов вереска обыкновенного с алюминия хлоридом
количественное определение фенольных соединениЙ
Фенологликозиды, гидроксикоричные кислоты, флавоноиды и полифенольные окисляемые соединения – одни из важнейших групп действующих веществ побегов вереска, для стандартизации которых мы предлагаем проводить их количественное определение. При этом нами разработаны методики количественного определения сумм флавоноидов, гидроксикоричных кислот, полифенольных окисляемых соединений, включающие такие параметры как экстрагент и условия экстракции, а также арбутина с использованием хроматографической очистки извлечения и удельного показателя поглощения арбутина-стандарта.
Гидроксикоричные кислоты. Сумму гидроксикоричных кислот определяли методом прямой спектрофотометрии. Оптимальные условия экстракции следующие: экстрагент – 90% спирт этиловый, время и кратность экстракции – 4 раза в течение 30 минут. В качестве стандарта использовали хлорогеновую кислоту производства фирмы «Fluka» (Германия), удельный показатель поглощения которой равнялся 504,425.
Метрологическая характеристика количественного определения суммы гидроксикоричных кислот методом прямой спектрофотометрии приведена в таблице 5. Ошибка определения находилась в пределах ±1,58%.
Таблица 5 – Метрологическая характеристика количественного определения гидроксикоричных кислот
| n | f | X | S2 | S | Sx | P,% | t (p,f) | X | ,% |
| 10 | 9 | 2,148 | 0,0022 | 0,046 | 0,015 | 95 | 2,26 | 0,034 | 1,58 |
Результаты количественного определения гидроксикоричных кислот в побегах вереска обыкновенного из различных мест произрастания отражены в таблице 11. В ходе исследования отметили, что содержание гидроксикоричных кислот варьировало в пределах от 2,343±0,0384% до 9,139±0,1414%. Их минимальные концентрации нами выявлены в образцах, заготовленных в окр. г. Брянска, г. Витебска, отдельных местах произрастания в Ярославской области; а наиболее высокие – в образцах из окр. пос. Смирдомский Чагодощенского района Вологодской области, г. Мурманска, Республики Коми, г. Петрозаводска и других.
Флавоноиды. Для количественного определения суммы флавоноидов в побегах вереска использовали спектрофотометрическую методику. В ее основу положили реакцию комплексообразования с алюминия хлоридом в сочетании со спектрофотометрическим определением оптической плотности комплексов в видимой области, что позволило проводить непосредственное спектрофотометрирование в извлечениях из сырья без дополнительных трудоемких стадий очистки. Оптимальные условия экстракции следующие: экстрагент – 70% спирт этиловый, время и кратность экстракции – 3 раза по 15 минут. Удельный показатель поглощения комплекса кверцетин - алюминия хлорид равнялся 596,1.
Метрологическая характеристика количественного определения суммы флавоноидов по упомянутой методике приведена в таблице 6. Ошибка определения суммы флавоноидов в среднем составила 1,61%.
Таблица 6 – Метрологическая характеристика количественного определения флавоноидов
| n | f | X | S2 | S | Sx | P,% | t (p,f) | X | ,% |
| 10 | 9 | 0,807 | 0,00033 | 0,0182 | 0,0058 | 95 | 2,26 | 0,013 | 1,61 |
Результаты количественного определения флавоноидов в побегах вереска, собранных в различных местах произрастания, обобщены в таблице 11. При этом выявили, что содержание суммы флавоноидов варьировало от 0,413% до 1,386%. Ее минимум приходился на образцы, заготовленные в окр. г. Рыбинска, в окр. местечка Симак, в окр. пос. Нижний, д. Кобостово, д. Малый Солонец Ярославской области, окр. г. Брянска и др., а максимальное содержание – на образцы, собранные в окр. г. Петрозаводска Республики Карелия, окр. г. Вохи Кирилловского района Вологодской области, окр. г. Мурманска, окр. санатория «Малые соли» Некрасовского района Ярославской области, окр. с. Унжа Койгородского района Республики Коми и др.
полифенольные окисляемые соединения (ПОС). Их количественное определение проводили по методике ГФ XI перманганатометрическим титрованием в присутствии индигосульфокислоты (метод Левенталя в модификации А.Л. Курсанова).
Метрологическая характеристика количественного определения ПОС приведена в таблице 7. Ошибка их определения составила в среднем 3,23%. Результаты определений отражены таблице 11.
Таблица 7 – Метрологическая характеристика количественного определения полифенольных окисляемых соединений
| n | f | X | S2 | S | Sx | P,% | t (p,f) | X | ,% |
| 10 | 9 | 6,590 | 0,089 | 0,298 | 0,094 | 95 | 2,26 | 0,213 | 3,23 |
В ходе исследования обнаружили, что содержание ПОС находилось в пределах от 2,410% до 9,406%, причем их максимум отметили в образце из окр. г. Брянск Брянской области, а минимум – в образце из окр. с. Ужга Койгородского района Республики Коми.
арбутин. В отличие от методики ГФ XI издания содержание арбутина определяли прямой хромато-спектрофотометрией с использованием стандарта арбутина фирмы «Sigma» (США). Его максимум поглощения нами отмечен при длине волны 285±2 нм. Он совпадал с максимумом спиртового извлечения побегов вереска (рис. 4).
Вначале мы определили удельный показатель арбутина-стандарта (табл. 8), который составил 72,23 и в дальнейшем использовался при количественном определении.

Рис. 4. Спектры поглощения спиртового извлечения побегов вереска обыкновенного и
арбутина-стандарта
Таблица 8 – Определение удельного показателя поглощения арбутина-стандарта
| Концентрация арбутина, % | D | Метрологическая характеристика | |
| 0,001 | 0,082 | 82,00 | x = 72,23 = ±4,26 x = ±3,32 I0,95 = ±2,23 M = 72,23±2,23 = 1,285 |
| 0,002 | 0,149 | 74,50 | |
| 0,003 | 0,229 | 76,33 | |
| 0,004 | 0,296 | 73,25 | |
| 0,005 | 0,358 | 73,30 | |
| 0,006 | 0,426 | 70,59 | |
| 0,007 | 0,484 | 69,14 | |
| 0,008 | 0,558 | 69,00 | |
| 0,009 | 0,633 | 70,33 | |
| 0,010 | 0,684 | 68,40 | |
| 0,011 | 0,744 | 67,64 |
Оптимальные условия экстракции для арбутина следующие: экстрагент – 70% спирт этиловый, время и кратность экстракции – 3 раза по 30 минут.
Очистку от сопутствующих веществ (другие фенольные соединения) мы проводили с использованием колонки с сорбентом – алюминия оксидом. Учитывая, что при проведении хроматографической очистки часть арбутина задерживалось алюминия оксидом, мы определили коэффициент неполного элюирования (табл. 9), который составил 1,14095.
Таблица 9 – Определение коэффициента неполного элюирования
| Опыт | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| Исходная концентрация раствора арбутина, % | 0,05 | 0,05 | 0,05 | 0,05 | 0,05 | 0,05 | 0,05 | 0,05 |
| Полученная концентрация, % | 0,0424 | 0,0443 | 0,044 | 0,0431 | 0,0429 | 0,046 | 0,433 | 0,0448 |
| Метрологическая характеристика | x = 1,14095 = ±0,03 | М = 1,14095±0,03 = 0,011 | ||||||
Метрологическая характеристика количественного определения арбутина методом прямой спектрофотометрии приведена в таблице 10. Ошибка определения равнялась 1,010%. Результаты анализа отражены в таблице 11.
Таблица 10 – Метрологическая характеристика количественного определения арбутина
| n | f | X | S2 | S | Sx | P,% | t (p,f) | X | ,% |
| 10 | 9 | 4,158 | 0,0034 | 0,0583 | 0,018 | 95 | 2,26 | 0,042 | 1,010 |
Содержание арбутина в побегах вереска находилось в пределах от 1,383% до 5,320%. Его максимум содержался в образце из окр. пос. Смирдомский Чагодощенского района Вологодской области, а минимум – в окр. пос. Прусово Ярославского района Ярославской области.
Сезонная динамика. Для изучения динамики накопления фенольных соединений заготовили побеги вереска по отдельным фазам вегетации (фаза бутонизации и цветения) в 2003 и 2004 годах в одни и те же дни в окрестностях поселка Лопью Койгородского района Республики Коми. Результаты исследования отражены в таблице 12.
Таблица 11 – Результаты количественного определения фенольных соединений в побегах вереска
| № образца | Содержание, % | |||
| флавоноидов | гидроксикоричных кислот | полифенольных окисляемых соединений | арбутина | |
| 1 | 0,828±0,0031 | 4,658±0,0570 | 3,874±0,1176 | 2,181±0,0197 |
| 2 | 0,475±0,0051 | 2,343±0,0384 | 9,406±0,3199 | — |
| 3 | 1,338±0,0121 | 4,558±0,0738 | 3,775±0,1204 | 2,113±0,0182 |
| 4 | 0,952±0,0043 | 5,880±0,0927 | 4,301±0,1301 | 3,265±0,0316 |
| 5 | 0,823±0,0032 | 9,139±0,1414 | 7,082±0,2295 | 5,320±0,0383 |
| 6 | 0,449±0,0020 | 5,710±0,0639 | 5,099±0,1532 | — |
| 7 | 0,712±0,0031 | 4,781±0,0595 | 4,287±0,1415 | 2,358±0,0199 |
| 8 | 0,824±0,0017 | 4,569±0,0412 | 4,753±0,1430 | 2,336±0,0224 |
| 9 | 1,033±0,0065 | 4,303±0,0389 | 4,903±0,1691 | 2,421±0,0196 |
| 10 | 1,019±0,0023 | 4,623±0,0653 | 4,779±0,1463 | 2,205±0,0080 |
| 11 | 1,108±0,0034 | 4,713±0,0437 | 5,276±0,1798 | 1,733±0,0134 |
| 12 | 1,256±0,0111 | 5,977±0,0905 | 3,712±0,1179 | 3,047±0,0226 |
| 13 | 0,749±0,0090 | 4,593±0,0613 | 4,446±0,1553 | 2,968±0,0083 |
| 14 | 0,818±0,0069 | 4,908±0,0843 | 5,028±0,1739 | 3,021±0,0280 |
| 15 | 0,789±0,0036 | 5,006±0,0521 | 3,923±0,1184 | 2,368±0,0148 |
| 16 | 0,680±0,0025 | 5,026±0,0409 | 3,416±0,1091 | 4,063±0,0212 |
| 17 | 0,638±0,0049 | 5,520±0,0798 | 3,716±0,1178 | 2,594±0,0210 |
| 18 | 0,950±0,0020 | 5,248±0,0583 | 4,234±0,1308 | 1,998±0,0069 |
| 19 | 1,215±0,0037 | 5,270±0,0551 | 4,886±0,1683 | 2,297±0,0192 |
| 20 | 0,596±0,0063 | 5,467±0,0635 | 2,833±0,0862 | 2,332±0,0133 |
| 21 | 0,468±0,0041 | 5,319±0,0533 | 3,749±0,1204 | — |
| 22 | 0,413±0,0031 | 4,560±0,0435 | 3,583±0,1080 | 3,368±0,0159 |
| 23 | 0,390±0,0026 | 7,652±0,1173 | 2,958±0,0928 | 2,280±0,0118 |
| 24 | 0,436±0,0048 | 4,352±0,0543 | 2,598±0,0895 | 2,510±0,0169 |
| 25 | 0,775±0,0051 | 4,272±0,0535 | 4,503±0,1540 | 2,448±0,0224 |
| 26 | 0,761±0,0044 | 4,368±0,0527 | 4,862±0,1469 | 1,713±0,0099 |
| 27 | 0,455±0,0041 | 3,648±0,0402 | 3,186±0,1001 | 1,948±0,0047 |
| 28 | 0,499±0,0028 | 3,678±0,0433 | 3,867±0,1302 | 1,637±0,0092 |
| 29 | 0,448±0,0030 | 4,837±0,0710 | 3,499±0,1073 | 3,412±0,0236 |
| 30 | 0,413±0,0010 | 6,018±0,0697 | 3,583±0,1179 | 3,382±0,0118 |
| 31 | 0,690±0,0054 | 4,520±0,0517 | 4,452±0,1487 | 1,383±0,0088 |
| 32 | 0,631±0,0022 | 3,885±0,0643 | 4,410±0,1458 | 2,400±0,0053 |
| 33 | 0,837±0,0047 | 4,341±0,0382 | 4,035±0,1256 | 3,094±0,0157 |
| 34 | 0,881±0,0079 | 2,883±0,0327 | — | — |
| 35 | 1,386±0,0051 | 5,508±0,0969 | 5,519±0,1820 | 2,973±0,0288 |
| 36 | 1,105±0,0084 | 5,769±0,0464 | 2,410±0,0766 | 3,470±0,0285 |
| 37 | 1,036±0,0105 | 4,220±0,0594 | 3,794±0,1194 | 3,086±0,0213 |
| 38 | 0,853±0,0085 | 4,098±0,0424 | 2,569±0,0094 | 3,874±0,1265 |
| 39 | 0,698±0,0060 | 4,125±0,0522 | 3,002±0,0072 | 4,235±0,1282 |
| 40 | 1,027±0,0098 | 3,956±0,0446 | 3,541±0,0150 | 3,875±0,1259 |
Условные обозначения: 1 – Архангельская область, Вишегорский район, окр. д. Слободка, август 2002 г.; 2 – Брянская область, окр. г. Брянска, сентябрь 1999 г.; 3 – Вологодская область, Кирилловский район, озеро Вохи, август 2002 г.; 4 – Вологодская область, Сокольский район, окр. с. Оларево, август 2002 г.; 5 – Вологодская область, Чагодощенский район, окр. пос. Смирдомский, август 2003 г.; 6 – Вологодская область, Череповецкий район, окр. дер. Шулма, июль 2003 г.; 7 – Ивановская область, Ильинский район, окр. дер. Новоиваново, сентябрь 2001 г.; 8 – Костромская область, Нейский район, окр. с. Унжа, август 1999 г.; 9 – Костромская область, окр. г. Костромы, сентябрь 1999 г.; 10 – Костромская область, Макарьевский район, окр. дер. Якимово, август 1995 г.; 11 – Костромская область, Нейский район, окр. г. Нея, август 1994г.; 12 – Мурманская область, окр. г. Мурманск, июль 2004 г.; 13 – Псковская область, окр. г. Остров, август 2004 г.; 14 – Тверская область, окр. г. Удомель, август 1996 г.; 15 – Ярославская обл., Брейтовский район, окр. дер. Остряковка, август 2003 г.; 16 – Ярославская обл., окр. пос. Брейтово, август 1998 г.; 17 – Ярославская обл., Заволжский район, окр. д. Ляпино, сентябрь 2003 г.; 18 – Ярославская обл., Заволжский район, окр. дер. Гаврилово, август 1997 г.; 19 – Ярославская обл., Некрасовский район, окр. санатория “Малые соли”, август 1997 г.; 20 – Ярославская обл., Некрасовский район, станция Тощиха, август 1994 г.; 21 – Ярославская обл., Некрасовский район, станция Тощиха, август 1997 г.; 22 – Ярославская обл., Переславский район, м. Симак, август 2004 г.; 23 – Ярославская обл., окр. г. Рыбинск, август 1998 г.; 24 – Ярославская обл., Рыбинский район, окр. д. Кобостово, июнь 2003 г.; 25 – Ярославская обл., Рыбинский район, окр. пос. Волжский, сентябрь 2000 г.; 26 – Ярославская обл., Рыбинский район, окр. пос. Тихменево, июль 1999 г.; 27 – Ярославская обл., Рыбинский район, окр. с. Коприно, август 2003 г.; 28 – Ярославская обл., Рыбинское водохранилище, остров Майский, август 1998 г.; 29 – Ярославская обл., Ярославский район, окр. д. Малый Солонец, сентябрь 1998 г.; 30 – Ярославская обл., Ярославский район, окр. пос. Нижний, сентябрь 2003 г.; 31 – Ярославская обл., Ярославский район, окр. пос. Прусово, август 2003 г.; 32 – Ярославская обл., Ярославский район, окр. пос. Туношна, август 1999 г.; 33 – Ярославская обл., Ярославский район, Смоленский сосновый бор, июль 1998 г.; 34 – Республика Беларусь, окр. г. Витебск, август 2003 г.; 35 – Республика Карелия, окр. г. Петрозаводск, сентябрь 1999 г.; 36 – Республика Коми, Койгородский район, окр. с. Ужга, август 2004 г.; 37 – Республика Коми, Усть-Вымский район, окр. пос. Студенец, август 2001 г.; 38 – Украина, Львовская обл., Сколевские бескиды, историко-архитектурный заповедник «Тустан», август 2004 г.; 39 – Украина, Львовская обл., окр. пос. Сходница, август 2004 г.; 40 – Украина, Ивано-Франковская обл., окр. г. Яремчи, август 2004 г.
Таблица 12 – Сезонная динамика накопления биологически активных фенольных соединений в побегах вереска обыкновенного
| Время сбора | Фаза вегетации | Содержание, % | ||||
| арбутина | гидрокси- кор. кислот | флаво- ноидов | полифенольных окисляемых соединений | |||
| 2003 | 14 июня | Бутонизация | 5,299±0,0447 | 7,299±0,1253 | 1,164±0,0040 | 5,009±0,1687 |
| 28 июня | —//— | 2,230±0,0139 | 6,203±0,0876 | 1,174±0,0074 | 3,749±0,1275 | |
| 13 июля | —//— | 2,375±0,0230 | 6,016±0,0753 | 1,076±0,0032 | 4,042±0,1216 | |
| 27 июля | Цветение | 2,335±0,0201 | 5,565±0,0618 | 1,028±0,0038 | 4,537±0,1371 | |
| 10 августа | —//— | 2,165±0,0196 | 5,729±0,0504 | 0,942±0,0029 | 4,940±0,1709 | |
| 24 августа | —//— | 3,632±0,0294 | 5,795±0,0648 | 1,063±0,0061 | 3,423±0,1048 | |
| 2004 | 13 июля | Бутонизация | 4,168±0,0265 | 4,908±0,0611 | 1,139±0,0122 | 3,499±0,1196 |
| 27 июля | Цветение | 3,110±0,0076 | 5,800±0,0604 | 0,958±0,0019 | 3,671±0,1134 | |
| 10 августа | —//— | 3,660±0,0247 | 5,531±0,0872 | 1,139±0,0066 | 4,832±0,1505 | |
| 24 августа | —//— | 2,886±0,0208 | 6,294±0,1019 | 1,378±0,0117 | 4,624±0,1390 | |
Из данных, приведенных в таблице 12, следует, что содержание флавоноидов в фазы бутонизации и цветения в 2003 и 2004 годах практически не изменялось и оставалось в пределах 0,9-1,4%. Несколько выше оно было в фазу бутонизации. Содержание гидроксикоричных кислот в начале бутонизации и в конце цветения немного превышало таковое в начале цветения и находилось в пределах 5,5-7,3%. Максимум суммы полифенольных окисляемых соединений приходился на начало бутонизации и середину периода цветения и составлял 5,0% и 4,9% соответственно. Больше всего арбутина накапливалось в фазу бутонизации и затем медленно его содержание снижалось в 2004 году, а в 2003 году в конце цветения оно немного повышалось. На основании изложенного можно заключить, что оптимальными сроками для сбора побегов вереска обыкновенного является период с начала до середины цветения.
Хромато-масс-спектрометрический анализ. При анализе хромато-масс-спектро-метрией этилацетатной, бутанольной и хлороформной фракций спиртового извлечения надземных органов вереска нами выявлено 80 веществ различной химической структуры. При этом в каждой из анализируемых фракций набор соединений специфичен. Так, в этилацетатных фракциях обнаружен цианиданол или (-)-эпикатехин (катехин, цианидол). Почти во всех фракциях содержались метилрезорцин, гидрохинон, а также арбутин, основной фенологликозид растений семейства вересковые.
Среди обнаруженных фенольных соединений довольно большое разнообразие фенолкарбоновых и гидроксикоричных кислот, в ряду которых нами идентифицированы бензойная, 3-фенилмолочная, салициловая, п-гидроксибензойная, п-гидроксифенилуксусная, гентизиновая, протокатеховая, сиринговая, галловая, коричная, п-гидроксикоричная, феруловая, ванилиновая и другие кислоты. Кроме фенолокислот, в ходе анализа нами отмечено наличие фенолальдегидов (фенилэтаналь, п-гидроксибензальдегид), фенолоспиртов (п-гидроксифенилэтанол, 4-гидроксифенилпропанол, фенилэтанол) и других фенольных соединений (галловая кислота, 3,4-дигидрокси-дигидрофуран-2(3Н)-он, скополин).
Помимо целенаправленного анализа разнообразных фенольных соединений нами обнаружены также вещества других классов. Так, сапонины представлены такими известными тритерпеновыми соединениями как - и -амирином, фриедоолеанан-3-олом; стерины – -ситостеролом и стигмастеролом, липиды – олеиновой, декановой, гексановой, октадекановой, гептадекановой, пальмитиновой, пеларгоновой, стеариновой, капроновой, миристиновой, лауриновой, эйкозановой, докозановой и тетракозановой кислотами. Кроме того, определена азелаиновая кислота, производное которой применяется при угревой сыпи. В ряду органических кислот идентифицировали молочную, янтарную, яблочную, лимонную и особенно производные уксусной кислоты; среди сахаров – D-рибозу, арабинофуранозу, ксилофуранозу, D-ксилозу, -D-галактофуранозу, глюкофуранозу, D-галактозу, арабинозу, D-ксилопиранозу, -D-глюкопиранозу, сахарозу, содержавшихся в основном в бутанольных фракциях.
Больше всего природных соединений экстрагировалось этилацетатом из цветков и хлороформом из листьев (табл. 13).
Общими для всех анализируемых органов являлись молочная, янтарная, пеларгоновая, яблочная, капроновая, салициловая, п-гидроксибензойная, лауриновая, гентизиновая,
Таблица 13 – Результаты хромато-масс-спектрометрического исследования этилацетатной фракции цветков вереска
| № п/п | Вещество | Этилацетатная фракция цветков | № п/п | Вещество | Хлороформная фракция листьев | ||
| Время удерживания, мин. | Содержание, % | Время удерживания, мин. | Содержание, % | ||||
| 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 |
| 1 | Молочная кислота | 5,074 | 3,337 | 1 | Бензойная кислота | 6,719 | 3,629 |
| 2 | Мочевина | 6,565 | 0,358 | 2 | Фосфат | 6,766 | 2,011 |
| 3 | Бензойная кислота | 6,740 | 0,480 | 3 | Пеларгоновая кислота | 7,406 | 0,370 |
| 4 | Фосфат | 6,772 | 0,251 | 4 | Яблочная кислота | 8,078 | 0,440 |
| 5 | Янтарная кислота | 7,078 | 0,199 | 5 | п-Гидроксибензальдегид | 7,639 | 0,185 |
| 6 | 3,4-Дигидрокси-дигидро-фуран-2(3Н)-он | 7,512 | 0,267 | 6 | Метилрезорцин | 7,909 | 0,699 |
| 7 | Гидрохинон | 7,681 | 8,449 | 7 | Капроновая кислота | 7,988 | 0,215 |
| 8 | Метилрезорцин | 7,914 | 12,077 | 8 | Салициловая кислота | 8,316 | 1,286 |
| 9 | Арабинофураноза | 8,163 | 0,291 | 9 | Коричная кислота | 8,580 | 0,282 |
| 10 | Салициловая кислота | 8,316 | 0,287 | 10 | п-Гидроксифенилэтанол | 8,628 | 0,177 |
| 11 | п-Гидроксифенилэтанол | 8,633 | 0,491 | 11 | Лауриновая кислота | 9,014 | 0,373 |
| 12 | 3-Фенилмолочная кислота | 8,697 | 1,101 | 12 | 4-Гидроксифенил-пропа-нол-1 | 9,183 | 0,339 |
| 13 | п-Гидроксибензойная кислота | 8,919 | 2,369 | 13 | Ванилиновая кислота | 9,559 | 0,289 |
| 14 | п-Гидроксифенилуксусная кислота | 8,972 | 0,142 | 14 | Азелаиновая кислота | 9,665 | 0,863 |
| 15 | D-Рибоза | 9,051 | 0,502 | 15 | Лимонная кислота | 9,707 | 0,818 |
| 16 | 4-Гидроксифенил-пропа-нол-1 | 9,183 | 0,236 | 16 | 3-Метокси-4-гидрокси-фенилпропанол | 9,797 | 0,952 |
| 17 | Гентизиновая кислота | 9,559 | 0,909 | 17 | Миристиновая кислота | 9,918 | 1,641 |
| 18 | Азелаиновая кислота | 9,665 | 0,402 | 18 | 4-Гидрокси-3-метокси-фенилуксусная кислота | 10,141 | 0,811 |
| 19 | Протокатеховая кислота | 9,781 | 1,576 | 19 | 2,3,5-Триметоксимандело-вая кислота | 10,659 | 0,783 |
| 20 | Миристиновая кислота | 9,924 | 0,149 | 20 | Пальмитиновая кислота | 10,743 | 10,750 |
| 21 | Сиринговая кислота | 10,125 | 0,306 | 21 | 3-Гидрокси-4-метокси-коричная кислота | 10,950 | 0,474 |
| 22 | Галловая кислота | 10,320 | 0,274 | 22 | Гептадекановая кислота | 11,119 | 0,263 |
| 23 | п-Гидроксикоричная кислота | 10,357 | 0,594 | 23 | Олеиновая кислота | 11,481 | 7,431 |
| 24 | Пальмитиновая кислота | 10,738 | 0,954 | 24 | Октадекановая кислота | 11,518 | 2,071 |
| 25 | Феруловая кислота | 10,955 | 0,051 | 25 | Эйкозановая кислота | 12,394 | 0,955 |
| 26 | 3,4-Дигидроксикоричная кислота | 11,093 | 5,497 | 26 | -Амирин | 13,515 | 1,016 |
| 27 | Олеиновая кислота | 11,426 | 0,589 | 27 | -Ситостерол | 23,519 | 2,996 |
| 28 | Стеариновая кислота | 11,516 | 0,373 | 28 | Докозановая кислота | 24,399 | 2,256 |
| 29 | Цианиданол | 15,091 | 0,712 | ||||
| 30 | 3,5-Диметокси-4-гидрокси-коричная кислота | 15,276 | 6,492 | ||||
ванилиновая, азелаиновая, протокатеховая, миристиновая, п-гидроксикоричная, пальмитиновая, 3,4-дигидроксикоричная, олеиновая, стеариновая, эйкозановая, 3,5-диметокси-4-гидроксикоричная кислоты, цианиданол, метилрезорцин, фосфат, -ситостерол, п-гидроксифенилэтанол, D-рибоза.
Некоторые природные соединения содержались лишь в отдельных фракциях главным образом из цветков и листьев. Так, как упоминалось выше, сиринговая кислота обнаружена в этилацетатной фракции, резорцин, ксилофураноза, глюкофураноза, D-ксилоза – в бутанольной, гексановая кислота, фенилэтанол, фенилэтаналь, изоевгенол, гидроксиазулен и алоэ-эмодин – в хлороформной фракциях из цветков; углеводы, пирокатехин, 2-гидроксиуксусная и 3,4,5-тригидроксикоричная кислоты – в бутанольной, а 4-гидрокси-3-метоксифенилуксусная, 2,3,5-триметоксиманделовая, октадекановая, коричная кислоты и п-гидроксибензальдегид – в хлороформной фракциях из листьев.
Микроскопическое изучение. Нами предпринято микроскопическое исследование надземных и подземных органов растения с целью обнаружения микродиагностических признаков и внесения их в проекты ФСП и ТУ. Объектами служили образцы, собранные в августе-сентябре 2001-2002 гг. в окрестностях п. Туношна Некрасовского района Ярославской области в фазу цветения. Анатомическое исследование стеблей, корневища, корней, цветков и листьев выполняли по методике Г.Г. Фурста на живом и фиксированном (96%-ный спирт этиловый + глицерин + вода 1:1:1) материале.
При рассмотрении поперечного среза листа вереска (рис. 5) видно, что его края завернуты вниз и почти соприкасаются друг с другом, образуя небольшую полость, в которую открываются устьица (7). На поперечном срезе хорошо различима кутикула (1), в виде прозрачной полоски по краю листа, однорядная палисадная ткань с верхней и нижней поверхности (2), рыхлая губчатая ткань (3), с хорошо выделяющимися хлоропластами (4). Лист в поперечном срезе характерной треугольной формы. При рассмотрении препарата листа с поверхности нами отмечено, что клетки эпидермиса верхней стороны слегка извилистые, в очертании округлые, без устьиц. Поверхность листа покрыта простыми волосками, причем по центральной жилке и по краю листа длинными одноклеточными волосками (5), а боковые стенки – короткими, одноклеточными, бородавчатыми волосками (6). На внутренней поверхности листа расположены устьица (7), устьичный аппарат парацитный. В мезофиле листа содержатся многочисленные друзы оксалата кальция (8), разнообразные по размерам.
Кроме того, нами изучены микродиагностические признаки подземных (корни и корневища) и других надземных (стебли и цветки) органов вереска.
Товароведческий анализ. Исследования проводили по методикам ГФ XI издания, в ходе которых определены некоторые числовые показатели побегов вереска обыкновенного, в ча-
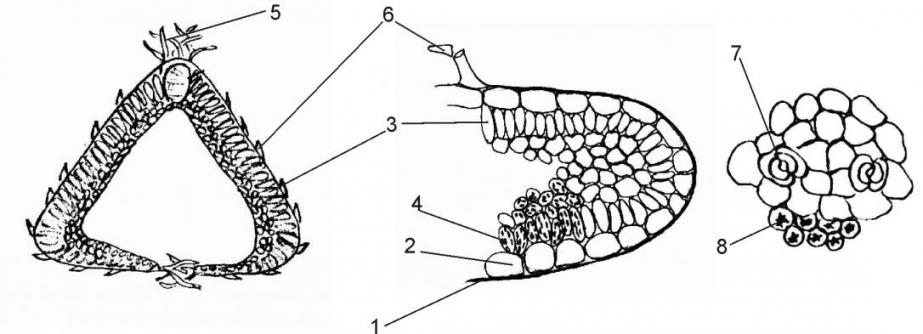
Рис. 5. Препарат с поверхности листа вереска обыкновенного.
Условные обозначения приведены в тексте
стности «Зола общая» (не более 5%), «Зола, нерастворимая в кислоте хлористоводородной» (не более 3%), «Влажность» (не более 12%), «Экстрактивные вещества, извлекаемые водой» (не менее 15%), «Экстрактивные вещества, извлекаемые 70%-ным спиртом этиловым» (не менее 16%).
Разработка нормативной документации. Результаты проведенных исследований положены в основу проектов фармакопейной статьи предприятия (ФСП) и технических условий (ТУ) на побеги вереска обыкновенного для ОАО «Ивановская фармацевтическая фабрика», которые разработали в соответствии с ОСТ 91500.05.001.00 «Отраслевой стандарт. Стандарты качества лекарственных средств. Основные положения» для ФСП, и ГОСТ Р 51740-2001 «Технические условия на пищевые продукты. Общие требования к разработке и оформлению», СанПиН 2.3.2.1290-03 «Продовольственное сырье и пищевые продукты. Гигиенические требования к организации производства и оборота биологически активных добавок к пище» для ТУ.
Разработка лекарственных средств. Нами определена острая токсичность настоя побегов вереска, в результате чего изучаемое растение охарактеризовано как низкотоксичное. Кроме того, на основании наблюдений за животными во время проведения эксперимента выявлен седативный эффект. С использованием побегов вереска составлен сбор «Гербанерв», рекомендуемый для лечения нервных заболеваний, и предложена технология приготовления настойки побегов вереска.
Для сбора «Гербанерв», в состав которого наряду с побегами вереска обыкновенного (1 часть), входят корневища с корнями валерианы лекарственной (4 части), трава зверобоя (2 части), корни цикория обыкновенного (1 часть), трава пустырника пятилопастного (2 части), листья земляники лесной (2 части) и соплодия хмеля (1 часть), определены числовые показатели по методикам ГФ XI: «Влажность» (не более 11%), «Зола общая» (не более 9,5%), «Зола, нерастворимая в хлористоводородной кислоте» (не более 1,6%), «Экстрактивные вещества, извлекаемые водой» (не менее 8,5%), «Экстрактивные вещества, извлекаемые 50% спиртом этиловым» (не менее 10,5%). Как и для побегов вереска, для упомянутой фитокомпозиции определены оптимальные условия экстрагирования фармакологически активных веществ, которые отмечены при троекратной экстракции в течение 15 минут 50% спиртом этиловым. С учетом изложенных данных в сборе «Гербанерв» нами определено содержание суммы гидроксикоричных кислот (1,81%) и флавоноидов (0,29%). Содержание суммы полифенольных окисляемых соединений составило 5,07%.
При получении настойки побегов вереска экстракцию проводили 70%-ным спиртом этиловым (коэффициент поглощения составил 1,6) и настаивали методом мацерации при соотношении сырье-экстрагент 1:5 на протяжении 7 суток, затем отстаивали в течение 3 суток и фильтровали. В полученной таким образом настойке по известным методикам нами определены следующие числовые показатели: сухой остаток (по методике ГФ XI), содержание суммы гидроксикоричных кислот, флавоноидов, полифенольных окисляемых соединений и арбутина (табл. 14).
Таблица 14 – Содержание сухого остатка и некоторых классов фенольных соединений в настойке вереска
| Серия | Содержание, % | ||||
| сухого остатка | суммы гидроксикоричных кислот | суммы флавоноидов | суммы полифенольных окисляемых соединений | арбутина | |
| 114112001 | 26,53 | 3,378±0,0423 | 0,923±0,078 | 3,562±0,1136 | 1,256±0,0071 |
| 01091003 | 20,62 | 4,056±0,0508 | 1,085±0,092 | 4,323±0,1308 | 2,863±0,0161 |
Как видно из данных, приведенных в таблице 14, в настойке, приготовленной в 2001 году (серия 114112001) фармакологически активных веществ несколько меньше, чем в настойке, полученной в 2003 году (серия 010910003), что, вероятно, связано с окислением и разрушением определяемых фенольных соединений.
В народной медицине вереск обыкновенный, в основном, используют в виде настоя. В связи с чем на кафедре фармакологии Ярославской государственной медицинской академии под руководством заведующего кафедрой профессора В.Н. Федорова нами проведено изучение его острой токсичности. Из результатов токсикологических исследований следует, что настой побегов изучаемого растения по величине ДЛ50 являлся практически нетоксичным, т.к. при его внутрижелудочном и внутрибрюшинном введении летальную дозу выявить не удалось. Кроме того, по ходу исследований нами обнаружен в известной мере седативный эффект, т.к. после введения настоя в течение первого часа развивалось двигательное и рефлекторное угнетение, которое проявлялось снижением оборонительного рефлекса и пугливости животных, снижением интенсивности одергивания головы при раздражении роговицы и др.
Выводы
- В листьях, цветках и неодревесневших побегах вереска обыкновенного хроматографией на бумаге обнаружены в свободном состоянии глюкоза и фруктоза, а в гидролизатах – галактоза, глюкоза, ксилоза, рамноза, глюкуроновая и галактуроновая кислоты (во фракции водорастворимых полисахаридов), глюкоза, фруктоза, арабиноза, рамноза, глюкуроновая и галактуроновая кислоты (в комплексе пектиновых веществ).
- Впервые проведен качественный и количественный анализ свободных и связанных аминокислот вегетативных и генеративных органов вереска обыкновенного, в результате которого установлено наличие 15 свободных и связанных аминокислот, в том числе 7 незаменимых. Отмечено, что их количество варьировало от 12 до 15 в зависимости от органа растения. Максимальное содержание аминокислот отмечено в цветках, минимальное – в листьях.
- Методами двумерной БХ, ВЭЖХ и спектрофотометрии проанализирован качественный состав фенольных соединений, представленных флавоноидами, гидроксикоричными кислотами и кумаринами. При этом выявлено не менее 8 гидроксикоричных кислот и 18 веществ флавоноидной природы, среди которых доминировали хлорогеновая кислота и кверцетин.
- Впервые предпринят хромато-масс-спектрометрический анализ природных соединений надземных органов вереска и идентифицировано 80 веществ первичного и вторичного обмена, представленных углеводами, жирными, органическими, оксибензойными и оксикоричными кислотами и другими соединениями. Каждое третье идентифицированное вещество обнаружено во всех надземных органах, в их числе такие фармакологически активные как арбутин, гидрохинон, цианиданол, метилрезорцин, -ситостерол, салициловая и азелаиновая кислоты и другие.
- Разработаны спектрофотометрические методики количественного определения суммы флавоноидов, суммы гидроксикоричных кислот и арбутина в побегах вереска, собранных в 40 местах произрастания в различных регионах РФ и ближнего зарубежья, и установлено, что среднее содержание суммы флавоноидов в них составило 0,778%, суммы гидроксикоричных кислот – 4,979%, суммы полифенольных окисляемых веществ – 4,298%, арбутина – 2,897%.
- Изучена сезонная динамика накопления фармакологически активных фенольных веществ побегов вереска обыкновенного и определены оптимальные сроки их сбора (в период с начала до середины цветения, т.е. с середины июля до середины августа).
- Проведено изучение микродиагностических признаков надземных и подземных органов вереска, по которым их можно идентифицировать.
- При товароведческом анализе побегов вереска определены значения отдельных числовых показателей («Влажность», «Зола общая», «Зола, нерастворимая в 10% растворе хлористоводородной кислоты», «Экстрактивные вещества»), положенных в основу проекта ФСП и ТУ «Побеги вереска», внедренных на Ивановской фармацевтической фабрике.
- При определении острой токсичности настоя побегов вереска отмечено, что по уровню токсичности он отнесен к низкотоксичным веществам. С использованием побегов растения разработана рецептура сбора «Гербанерв» и технология получения настойки, которые стандартизированы по некоторым числовым показателям.
Список работ, опубликованных по теме диссертации
- Фармакохимическое изучение видов семейства вересковые / Н.Г. Марсов, А.Ю. Стельмах, С.Н. Соленникова … С.В. Онегин // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: ДИА-пресс, 2001. – С. 85-86.
- Онегин, С.В. Количественное определение некоторых групп фенольных соединений в траве вереска обыкновенного / С.В. Онегин, А.А. Трубников // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: ДИА-пресс, 2001. – С. 87-88.
- Создание компьютерной программы «Минеральные вещества» ряда лекарственных растений /Т.А. Бакланова, Н.С. Фурса, А.И. Богомолова, С.В. Онегин и др. // Актуальные проблемы фармацевтической науки и образования: итоги и перспективы: Матер. межвуз. науч.-практич. конференции, посв. 85-летию высш. образования на Урале. – Пермь, 2001. – С. 96-97.
- Особенности анатомического строения подземных органов вереска / С.В. Онегин, В.И. Ошмарина, Н.С. Фурса и др. // Актуальные проблемы фармацевтической науки и образования: итоги и перспективы: Матер. межвуз. науч.-практич. конференции, посв. 85-летию высш. образования на Урале. – Пермь, 2001. – С. 111-112.
- Экологическая оценка техногенного загрязнения г. Ярославля и Ярославской области / Н.С. Фурса, Т.А. Бакланова, И.Н. Каграманян … С.В. Онегин // Актуальные проблемы фармацевтической науки и образования: итоги и перспективы: Матер. межвуз. науч.-практич. конференции, посв. 85-летию высш. образования на Урале. – Пермь, 2001. – С. 175.
- Фармакологически активные вещества, фармакологические эффекты и применение отечественных видов вересковых / Т.А. Бакланова, Н.Г. Марсов, М.С. Коротаева … С.В. Онегин и др. // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: Изд-во «Аверс Пресс», 2002. – С. 96-97.
- Некоторые итоги доклинического изучения БАД седативного действия бальзам «Фитосед» / А.А. Трубников, Н.С. Фурса … С.В. Онегин и др. // X Российский национальный конгресс «Человек и лекарство». – М., 2003. – С. 551.
- Фитохимическое исследование веществ первичного обмена отдельных видов семейства вересковые / Н.С. Фурса, М.С. Коротаева, С.В. Онегин, Н.Г. Марсов // X Российский национальный конгресс «Человек и лекарство». – М., 2003. – С. 677-678.
- Куприянова, Н.Е. Разработка спектрофотометрического метода количественного определения арбутина / Н.Е. Куприянова, С.В. Онегин, М.С. Коротаева // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: Изд-во «Аверс Пресс», 2003. – С. 94-95.
- Количественное определение арбутина в отдельных видах семейства вересковые / С.В. Онегин, Н.Е. Куприянова, М.С. Коротаева, А.А. Трубников // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: Изд-во «Аверс Пресс», 2003. – С. 95-96.
- Онегин, С.В. Разработка методики фотоэлектроколориметрического определения арбутина в лекарственном растительном сырье / С.В. Онегин, Д.В. Меньшов, Н.Е. Куприянова // Сборник статей 4-го конгресса молод. ученых «Науки о человеке». – Томск, 2003. – С. 214-215.
- Онегин, С.В. Применение вереска обыкновенного в народной медицине / С.В. Онегин, Н.Е. Куприянова // Материалы X съезда медицинских и фармацевтических работников Ярославской области: Сборник науч. трудов. – Ч. II. - Ярославль, 2003. – С. 375-379.
- Онегин, С.В. Выявление объективной и разработка наиболее достоверной методики количественного определения арбутина в траве вереска обыкновенного / С.В. Онегин, Н.С. Фурса // Современные вопросы фармакогнозии: Межвуз. сборник науч. трудов с международ. участием, посв. 20-летию кафедры фармакогнозии / Под ред. Н.С. Фурсы. – Ярославль: Типография ЯГТУ, 2004. – С. 235-248.
- Возможности стандартизации фитокомпозиции «Гербанерв» / О.В. Чистова, С.В. Онегин, А.А. Трубников, В.Д. Белоногова // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: Изд-во «Аверс Пресс», 2004. – С. 83-84.
- Петровский, О.С. Фитохимическое исследование веществ первичного обмена вереска обыкновенного / О.С. Петровский, Е.А. Акимова, С.В. Онегин // Сборник науч. работ студентов и молод. ученых ЯГМА. – Ярославль: Изд-во «Аверс Пресс», 2004. – С. 77.
- Онегин, С.В. Количественное определение арбутина в траве вереска обыкновенного из различных мест произрастания / С.В. Онегин, Д.В. Меньшов, Е.В. Кузьмина // Сборник науч. работ студентов и молод. ученых, посв. 60-летию Победы. – Ярославль, 2005. – С. 87-88.
- Кузьмина, Е.В. Количественное определение фенольных соединений в траве вереска обыкновенного из разных мест произрастания / Е.В. Кузьмина, С.В. Онегин // Сборник науч. работ студентов и молод. ученых ЯГМА, посв. 60-летию студенческого научного общества. – Ярославль, 2006. – С. 112-113.
- Сравнительный анализ аминокислотного состава надземных органов вереска обыкновенного / С.В. Онегин, Ю.И. Корниевский, В.Г. Корниевская, Н.С. Фурса // Запорожский медицинский журнал. – 2007. - №1. – С. 114-116.
- Онегин, С.В. Количественное определение суммы гидроксикоричных кислот в траве вереска обыкновенного из различных мест произрастания / С.В. Онегин, Н.С. Фурса // Российский медико-биологический вестник имени академика И.П. Павлова. – 2007. – №3. – С. 97-103.
- Фурса, Н.С. Содержание арбутина в траве вереска обыкновенного / Н.С. Фурса, С.В. Онегин // Фармация. – 2007. – №6. – С. 12-14.
- Онегин, С.В. Микроскопическое исследование подземных и надземных органов вереска / С.В. Онегин, В.И. Ошмарина, Ю.И. Корниевский // Современные вопросы теории и практики лекарствоведения: Сборник матер. науч.-практич. конференции с международ. участием, посв. 25-летию фармац. фак-та ЯГМА / Гл. ред. Н.С. Фурса. – Ярославль: изд-во «Найс», 2007. – С. 258-261.
- Фурса, Н.С. Стандартизация травы вереска по основным фенольным соединениям / Н.С. Фурса, С.В. Онегин, Л.И. Бородин // Современные вопросы теории и практики лекарствоведения: Сборник матер. науч.-практич. конференции с международ. участием, посв. 25-летию фармац. фак-та ЯГМА / Гл. ред. Н.С. Фурса. – Ярославль: изд-во «Найс», 2007. – С. 352-354.
- Шелюто, В.Л. Химическое изучение флавоноидов вереска / В.Л. Шелюто, С.В. Онегин, Н.С. Фурса // Современные вопросы теории и практики лекарствоведения: Сборник матер. науч.-практич. конференции с международ. участием, посв. 25-летию фармац. фак-та ЯГМА / Гл. ред. Н.С. Фурса. – Ярославль: изд-во «Найс», 2007. – С. 369-373.
- Онегин, С.В. Хромато-масс-спектрометрический анализ природных соединений травы вереска обыкновенного и арктоуса альпийского / С.В. Онегин, Е.В. Кузьмина, В.Л. Шелюто, Н.С. Фурса // Вестник Пермкой государственной фармацевтической академии. – 2007. - №2. – С. 266-269.
- Фурса, Н.С. Хромато-масс-спектрометрический анализ природных соединений надземных органов вереска обыкновенного / Н.С. Фурса, С.В. Онегин, Е.В. Кузьмина и др. // Запорожский медицинский журнал. – 2007. - №3. – С. 118-124.
- Шелюто, В.Л. Обнаружение, выделение, физико-химическое изучение и количественное определение флавоноидов в траве вереска обыкновенного / В.Л. Шелюто, С.В. Онегин, Н.С. Фурса // Вестник фармации. – 2007. - №2(36). – С. 15-25.

