Исследование функциональных характеристик изоформ сердечного миозина
На правах рукописи
Копылова Галина Васильевна
ИССЛЕДОВАНИЕ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИК ИЗОФОРМ СЕРДЕЧНОГО МИОЗИНА
03.03.01 – физиология
Автореферат
диссертации на соискание ученой степени
кандидата биологических наук
Екатеринбург - 2011
Работа выполнена в лаборатории биологической подвижности Учреждения Российской академии наук Института иммунологии и физиологии Уральского отделения РАН
Научные руководители: Доктор биологических наук
Бершицкий Сергей Юрьевич,
кандидат биологических наук, в.н.с.
Никитина Лариса Валерьевна
Официальные оппоненты: Член-корреспондент РАН, ЗДНРФ,
доктор биологических наук, профессор Мархасин Владимир Семенович,
лауреат Государственной премии РФ,
доктор биологических наук
Прошева Валентина Ивановна
Ведущая организация: ФГУ «Российский кардиологический научно-производственный комплекс» Министерства здравоохранения и социального развития Российской Федерации
Защита состоится «___» ______________2011 г. в _______ часов на заседании совета по защите кандидатских и докторских диссертаций Д 004.027.01 при учреждении РАН Институте иммунологии и физиологии УрО РАН по адресу: 620049, Российская Федерация, г. Екатеринбург, ул. Первомайская, 106.
С диссертацией можно ознакомиться в Центральной научной библиотеке УрО РАН (620041, г. Екатеринбург, ул. С. Ковалевской, д. 22/20), с авторефератом — на сайте учреждения РАН Института иммунологии и физиологии УрО РАН - http://www.iip.uran.ru
Автореферат разослан «___» ______________2011 г.
Ученый секретарь совета по защите кандидатских
и докторских диссертаций Д 004.027.01 при учреждении РАН
Институте иммунологии и физиологии УрО РАН,
доктор медицинских наук, профессор И. А. Тузанкина
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность
Согласно данным ВОЗ, смертность от сердечно-сосудистых заболеваний занимает первое место в мире. Факторы, которые приводят к нарушению работы сердца, многочисленны, но все они, так или иначе, влияют на сократительную функцию кардиомиоцита. Нарушение сократительной функции кардиомиоцита может происходить из-за изменения состава белков сократительного аппарата или вследствие разобщения процессов сопряжения возбуждения с сокращением.
Как известно, генерация силы в мышце осуществляется за счет энергии гидролиза ATФ поперечными мостиками, образованными головками миозиновых молекул, прикрепленными к нитям актина. В сердце млекопитающих имеется два типа тяжелых цепей миозина (ТЦМ): и [Hoh et al.,1977]. Изоформа миозина V1 является гомодимером -тяжелых цепей, а изоформа миозина V3 – гомодимером -тяжелых цепей. По аминокислотной последовательности V1 и V3 изомиозины идентичны на 93 % [Alpert et al., 2002]. Разница в аминокислотных последовательностях между - и -ТЦМ определяет различие их кинетических и механических свойств [Alpert et al., 2002; Krenz et al., 2007].
В рамках интактного сердца имеется заметное различие в экспрессии изоформ миозина V1 и V3 в кардиомиоцитах из разных слоев стенки желудочка [Eisenberg et al., 1985; Litten et al., 1985; Carnes et al., 2004; Reiser et al., 2001]. Экспрессия этих изоформ миозинов зависит от вида животного, его возраста и гормонального статуса [Lompre et al., 1979]. Изменения в экспрессии изоформ происходят также при патологиях сердца [Lompre et al., 1979; van der Velden et al., 1999; Miyata et al., 2000].
Изоформы сердечного миозина отличаются по своим гидролитическим и механическим характеристикам [Sata et al., 1993; Harris et al., 1994; VanBuren et al., 1995; Noguchi et al., 2003; Malmqvist et al., 2004]. На уровне взаимодействия одиночных молекул миозина и актина обнаружено, что изомиозины V1 и V3 отличаются только длительностью единичных перемещений нитей актина [Sugiura et al.,1998; Palmiter et al., 1999].
Наличие изоформ сердечного миозина является приспособлением для оптимизации сократительной функции сердца. Левый желудочек сердца взрослого человека содержит около 7 % -тяжелых цепей миозина [Miyata et al., 2000]. При ишемической и дилатационной кардиомиопатии -изоформа не обнаруживается [Reiser et al., 2001], что снижает сократимость, но повышает экономичность сокращения [Alpert NR, 1972].
В первой половине 90-х годов были обнаружены мутантные формы -цепи миозина (сейчас их известно более ста), приводящие к выраженным клиническим симптомам гипертрофической либо дилатационной кардиомиопатии, которые могут приводить к внезапной смерти [Schmitt et al., 2006].
Различие в соотношениях изоформ V1 и V3 в кардиомиоците, прежде всего, прямо проявляется в различных скоростных характеристиках развития напряжения. Кроме того, очень важен вклад, который разные соотношения изомиозинов вносят в механическую функцию в миокарде через кооперативное влияние прикрепленных поперечных мостиков на сродство тропонина С к кальцию (через механизм мостико–тропониновой кооперативности). Это кооперативное взаимодействие регуляторных и сократительных белков является ключевым механизмом, объясняющим целый ряд феноменов биомеханики активного миокарда, связанных с влиянием механических условий сокращений на активацию сердечной мышцы [Izakov et al., 1991].
Влияние изоформ сердечного миозина на кальциевую регуляцию сокращения сердечной мышцы изучалось в экспериментах на скинированных кардиомиоцитах и препаратах сердечной мышцы [Fitzsimons et al 1998; Metzger et al, 1999; Rundel et al. 2004, 2005; Krenz et al., 2007; Stelzer et al. 2007, 2008]. В настоящем имеется только одна работа по изучению вклада изоформ сердечного миозина в кальциевую регуляцию сокращений миокарда методом искусственной подвижной системы [Noguchi et al., 2003]. Имеющаяся на сегодня информация о вкладе изоформ сердечного миозина в кальциевую регуляцию сокращения сердечной мышцы являются неполной и противоречивой.
Использование метода искусственной подвижной системы позволяет изучать непосредственно взаимодействие регуляторных и сократительных белков на уровне тонкого филамента, что дает возможность избежать артефактов, связанных с пассивными механическими свойствами целой мышцы, либо кардиомиоцита. В рамках этого метода можно задавать различные концентрации свободного кальция и регистрировать связи «pCa-скорость», «pCa-сила», «сила-скорость» на уровне взаимодействующих белков.
Цель работы
Провести систематическое исследование функциональных характеристик изоформ сердечного миозина кролика и оценить их вклад в кальциевую регуляцию сокращений сердечной мышцы.
Задачи исследования
- Исследовать функциональные свойства изоформ сердечного миозина кролика V1 и V3, а именно: актин-активируемую Mg2+-АТФ-азную активность, силогенерирующие и кинетические характеристики.
- В искусственной подвижной системе с регулируемым тонким филаментом исследовать зависимости «рСа-скорость», «рСа-сила» для изоформ сердечного миозина V1 и V3.
- Исследовать связь «сила-скорость» для изоформ сердечного миозина V1 и V3 при насыщающей и ненасыщающей концентрациях кальция в растворе методом искусственной подвижной системы с регулируемым тонким филаментом.
- Получить и проанализировать зависимость «сила-мощность» для изоформ сердечного миозина V1 и V3 при насыщающей и ненасыщающей концентрациях кальция в растворе.
- Проанализировать вклад изоформ сердечного миозина V1 и V3 в кальциевую регуляцию сокращений сердечной мышцы.
Научная новизна
Впервые систематически исследованы функциональные характеристики изоформ V1 и V3 сердечного миозина кролика, используя метод искусственной подвижной системы. Получена и проанализирована связь «рСа-скорость» для изоформ сердечного миозина V1 и V3. Показано, что кальциевая чувствительность и коэффициент Хилла зависимости «рСа-скорость» для изоформ V1 и V3 сердечного миозина не отличаются.
Впервые изучена связь «рСа-сила» для изоформ сердечного миозина V1 и V3. Показано, что при низкой концентрации каждой из изоформ как коэффициент кооперативности, так и кальциевая чувствительность выше для V3, чем для V1, что может иметь адаптивное значение при патологиях, связанных со снижением концентрации миозина.
Впервые на уровне взаимодействующих ансамблей молекул сократительных белков показано, что основные характеристики зависимостей «сила-скорость» и «сила-мощность» сокращения кардиомиоцита и сердечной мышцы в целом определяются свойствами изоформ миозина.
Научная и практическая значимость
Получены новые данные о роли изоформ сердечного миозина в кальциевой регуляции сокращения сердечной мышцы. С помощью метода искусственной подвижной системы показано, что механические свойства сокращения кардиомиоцита и сердечной мышцы в целом определяются составом тяжелых цепей изоформ сердечного миозина. Эти новые данные необходимы для понимания работы сердечной мышцы в норме и ее нарушениях при патологиях сердца, приводящих к изменению состава тяжелых цепей миозина.
Внедрение
Результаты диссертационной работы используются в учебном процессе на кафедре экспериментальной физики физико-технического факультета Уральского федерального университета имени первого Президента России Б.Н.Ельцина; на кафедре нормальной физиологии ГОУ ВПО «Уральской государственной медицинской академии Минздравсоцразвития России».
Положения, выносимые на защиту
- Значения коэффициента кооперативности Хилла зависимости «рСа-сила» для изоформ сердечного миозина V1 и V3 в искусственной подвижной системе при высокой концентрации миозина не отличаются, кальциевая чувствительность выше для изоформы V3; при низкой концентрации каждой из изоформ как коэффициент кооперативности, так и кальциевая чувствительность выше для V3, чем для V1.
- Зависимость «сила-скорость» для изоформ V1 и V3 в искусственной подвижной системе при насыщающей и ненасыщающей концентрациях кальция соответствует гиперболическому уравнению Хилла в области малых нагрузок и отклоняется от него в области больших нагрузок; зависимости «сила-скорость» для изоформ V1 и V3 отличаются при насыщающей и ненасыщающей концентрациях кальция; изоформный состав миозина определяет форму связи «сила-скорость» в мышечных препаратах.
- Максимум развиваемой мощности изоформы V1 выше, чем изоформы V3 и сдвинут в сторону меньших нагрузок при насыщающей и ненасыщающей концентрациях кальция, что может иметь адаптивное значение для поддержания мощности на заданном уровне; мощность, развиваемая каждой из изоформ миозина, не зависит от концентрации свободного кальция во всем диапазоне нагрузок.
Апробация работы и публикации. Результаты работы были представлены на международных конференциях «Biological motility: Basic research and practice» (г. Пущино, 2006 г.); «Biological motility: Achievements and Perspectives» (г. Пущино, 2008 г.); «Biological motility: from Fundamental Achievements to Nanotechnologies» (г. Пущино, 2010 г.); на Международном форуме по нанотехнологиям (г. Москва, 2008 г.); на XXXIV и XXXVI «European Muscle Congress» (г. Дебрецен, Венгрия, 2005 г.; Стокгольм, Швеция, 2007 г.); Joint British-Russian Young Scientists Workshop (Екатеринбург, 2007 г.).
По теме диссертации опубликовано 12 печатных работ, в том числе в изданиях, рекомендованных ВАК – 7 публикаций.
Структура и объем работы. Диссертация состоит из введения, пяти глав, выводов и списка цитируемой литературы (188 источников). Диссертация изложена на 151 странице, содержит 20 рисунков.
Работа была выполнена при поддержке грантов РФФИ, Программы фундаментальных исследований Президиума РАН, гранта Президента РФ для государственной поддержки ведущей школы РФ, HHMI и ИНТАС.
Автор приносит благодарности д.ф.-м. н. Кацнельсону Л.Б. за консультации при построении связей «рСа-скорость», «рСа-сила», «сила-скорость» и обсуждению полученных результатов; Щепкину Д.В. за помощь в проведении экспериментов; к.б.н. Машанову Г.И. за любезно предоставленную программу записи и обработки видеоизображения; Бершицкому Б.Ю. за техническую поддержку экспериментов.
СОДЕРЖАНИЕ РАБОТЫ
Обзор литературы
В обзоре литературы рассматриваются особенности строения, свойства и функциональное значение изоформ сердечного миозина. Представлен обзор исследований вклада изоформ сердечного миозина в кальциевую регуляцию сокращения сердца, полученных в экспериментах на скинированных кардиомиоцитах и препаратах сердечной мышцы, а также методом искусственной подвижной системы. Показано, что имеющаяся на сегодня информация о влиянии изоформ сердечного миозина на кальциевую регуляцию, является неполной и противоречивой.
Материал и методы исследования
Растворы. Состав буфера АВ: 25 мМ KCl, 25 мМ имидазола, 4 мМ MgCl2, 1 мМ ЭГТА и 10 мМ дитиотриэтола, pH 7,5.
Получение белков. Актин выделяли из ацетонового порошка по стандартной методике [Pardee and Spudich, 1982]. Сердечные тропомиозин и тропонин выделяли из миокарда левого желудочка сердца быка методами Smille, 1982 и Potter, 1982 с небольшими модификациями.
Изоформа V1 миозина была получена из миокарда левого желудочка гипертиреоидных, изоформа V3 – гипотиреоидных кроликов [Litten et al., 1985, vanBuren et al., 1995]. Миозин выделяли из левого желудочка сердца кролика по стандартной методике [Margossian и Lowey, 1982] с небольшими модификациями. Состав тяжелых цепей сердечного миозина проверялся методом ПААГ-электрофореза [van der Velden et al., 1999]. Миокард левого желудочка гипертиреоидных кроликов содержал преимущественно изоформу миозина V1 (~90%), гипотиреоидных – изоформу миозина V3 (~90%). В день эксперимента неработающие молекулы миозина удаляли ультрацентрифугированием с F-актином и АТФ [Gordon et al., 1997].
Получение регулируемого тонкого филамента. Регулируемый тонкий филамент, состоящий из актина, тропонина и тропомиозина реконструировали путем смешивания этих белков в следующих концентрациях: 400 нМ ТМРФ-F-актина, 80 нМ тропонина и 100 нМ тропомиозина при 4 С в буфере АВ. Соотношение белков в регулируемых тонких филаментах проверяли с помощью ПААГ-электрофореза [Laemmli, 1970].
Измерение АТФ-азной активности. Актин-активируемая Mg2+-АТФазная активность миозина измерялась колориметрическим методом по свободному неорганическому фосфату [Kodama et al., 1986] при 28 C в буфере АВ, содержащем 0,05 мкМ миозина, от 10 до 30 мкМ F-актина и 1 мМ АТФ. Основные параметры кинетики Михаэлиса-Ментен определялись с помощью графика Лайнуивера-Бэрка.
Эксперименты на искусственной подвижной системе. Для установки был использован инвертированный флуоресцентный микроскоп (Axiovert 200 М, Carl Zeiss MicroImaging GmbH), укомплектованный ртутной лампой HBO 100, набором фильтров для тетраметилродамина (ТРМФ) и масляно-имерсионным объективом Alpha Plan-Fluar 1001,45 (Carl Zeiss MicroImaging GmbH). Изображение меченого актина регистрировалось с помощью EMCCD видеокамеры (Andor Technology) и записывалось на жесткий диск компьютера с помощью программы GMimPro [Mashanov et al., 2007].
Проточная камера состояла из предметного стекла с приклеенным к нему покровным стеклом, внутренняя поверхность которого была покрыта нитроцеллюлозой. В проточную камеру загружали 50 мкл сердечного миозина в высокоионном буфере АВ, содержащем 500 мМ KCl, на 2 мин, затем промывали последовательно высоко- и низкоионным буфером АВ и добавляли 50 мкл БСА в концентрации 0,5 мг/мл на 1 мин. Далее загружали 500 мкг/мл F-актина в буфере АВ с 2 мМ АТФ на 5 мин для блокировки неработающих миозиновых головок; после чего камеру трижды промывали буфером АВ. Далее добавляли 50 мкл раствора флуоресцентно меченых F-актина или тонких регулируемых филаментов в концентрации 10 нМ в буфере АВ, содержащем 100 нМ тропонин и 100 нМ тропомиозини, и инкубировали 10 мин. Затем промывали камеру буфером АВ с 0,5 мг/мл БСА, 3,5 мг/мл люкозы, 0,02 мг/мл каталазы, 0,15 мг/мл глюкозо-оксидазы, 20 мМ ДТТ, 2 мМ АТФ и 0,5 % метиллцеллюлозы. В случае экспериментов с регулируемым тонким филаментом раствор c АТФ содержал дополнительно 100 нМ тропонина и 100 нМ тропомиозина для предотвращения диссоциации регуляторных белков от актина. Необходимая концентрация свободного кальция в растворе достигалась добавлением Ca2+-ЭГТА. Все эксперименты были выполнены при температуре 28 С.
Построение зависимости «рСа-скорость». Для построения зависимости «рСа-скорость» были определены скорости скольжения регулируемого тонкого филамента по изоформам сердечного миозина при концентрациях кальция в растворе проточной камеры от рСа=4 до рСа=8. Скорость скольжения филаментов определяли с помощью компьютерной программы GMimPro. Кривая зависимости «рСа-скорость» была построена согласно уравнению Хилла методом наименьших квадратов:
V = Vmax(1+10h(pCapCa50))1, где рСа – отрицательный десятичный логарифм концентрации кальция в растворе; V и Vmax – скорость при данном значении рСа и максимальная скорость при насыщающей концентрации кальция, соответственно; рCa50 – величина, при которой достигается половина максимальной скорости скольжения филаментов (кальциевая чувствительность), h – коэффициент кооперативности Хилла.
Построение зависимости «pCa-сила». Относительную силу, которая движет филамент при данной концентрации кальция, оценивали по минимальной останавливающей концентрации -актинина, по отношению к минимальной останавливающей концентрации -актинина при насыщающей концентрации кальция. Кривая зависимости «рСа-сила» была построена согласно уравнению Хилла методом наименьших квадратов:
F = 1/[1+10(h(pCa50-pCa))], где: F – безразмерная сила, выраженная в долях к Fmax, h – коэффициент кооперативности Хилла, pCa50 – величина, при которой достигается сила, равная половине максимальной силы. Эксперименты были сделаны при двух концентрациях миозина, загружаемого в проточную камеру: 200 и 300 мкг/мл.
Построение связи «сила-скорость». Для построения зависимости «сила-скорость» определяли скорость скольжения регулируемых филаментов при различных концентрациях -актинина в проточной камере. Эксперименты были проведены при насыщающей (рСа=6,5) и ненасыщающей (рСа=7,0) концентрациях кальция в финальном буфере, содержащем АТФ.
Механическая нагрузка была выражена как отношение концентрации -актинина, загружаемого в камеру, к максимальному значению концентрации -актинина (соответствующему изометрическому состоянию). Теоретическая кривая зависимости «сила–скорость» аппроксимировалось с помощью гиперболического уравнения Хилла: (F/F0+a)·V=b·(1-F/F0), где V – скорость скольжения регулируемого филамента при данной нагрузке, F и F0 –значение нагрузки и максимальное значение нагрузки соответственно, a – константа силы, b – константа скорости. Значения констант a и b были определены методом линеаризации гиперболического уравнения Хилла [Altringham and Johnston, 1982, Lnnergren, 1978].
Определение связи «сила-мощность». Зависимость «сила-мощность» была построена на основании данных, полученных в экспериментах по определению связи «сила–скорость». Мощность определялась по формуле: P = V · F / F0, где V – скорость скольжения регулируемых тонких филаментов при данном уровне нагрузки, F/F0 – относительная сила, выраженная как отношение концентрации -актинина, загружаемого в камеру, к максимальному значению концентрации -актинина.
Статистическая обработка. Эксперименты по определению АТФ-азной активности миозина проводились трижды. Значения Km и Vmax представлены как среднее значение ± стандартное отклонение.
Для построения зависимости «рСа-скорость» была усреднена скорость не менее 100 филаментов для каждого значения рСа в растворе. При определении зависимости «сила–скорость» были усреднены скорости скольжения не менее 100 филаментов при каждом значении концентрации -актинина, загружаемого в камеру. Значения скоростей, силы и мощности представлены как среднее значение ± стандартное отклонение.
Эксперименты по определению зависимостей «рСа-скорость», «рСа-сила» были проведены трижды. Значения коэффициента Хилла и рСа50 для этих зависимостей получены для каждого эксперимента и усреднены. Значения скоростей, сил, коэффициентов Хилла и рСа50 представлены как среднее значение ± стандартное отклонение.
Статистическую обработку полученных данных проводили с помощью компьютерной программы «Microsoft Excel» и «Статистика 6.0», для оценки значимости различий использовался непараметрический критерий Манна-Уитни.
Результаты и их обсуждение
1. Функциональные характеристики изоформ сердечного миозина
Значения Vmax и Кm актин-активируемой Mg2+-АТФ-азной активности для каждой изоформы сердечного миозина. Значения Vmax и Кm, соответственно, были равны: 5,2 ± 0,98 с-1 и 8,09 ± 5,65 мкМ для V1; 3,06 ± 0,93 с-1 и 8,13 ± 2,31 мкМ для V3. Значения Vmax для изоформы V1 в 1,7 раза выше, чем для V3.
Скорость скольжения F-актина по изомиозину V1 составила 1,0 ± 0,1 мкм/с, по V3 – 0,59 ± 0,11 мкм/с. При насыщающей концентрации кальция (рСа=5,0) скорость движения регулируемой тонкой нити для изомиозина V1 была равна 3,69 ± 0,39 мкм/с, для V3 – 2,12 ± 0,21 мкм/с. Скорость скольжения и F-актина, и регулируемой тонкой нити по изоформе V1 в 1,7 раза больше, чем по V3. Сила, развиваемая сердечным изомиозином V3 кролика в 2 раза больше, чем V1.
2. Сравнительная оценка кальциевой активации процессов прикрепления и открепления поперечных мостиков для изоформ сердечного миозина V1 и V3
Для того чтобы оценить вклад каждой изоформы сердечного миозина в кальциевую активацию процессов прикрепления/открепления поперечных мостиков, были получены соотношения «рСа-скорость», «рСа-сила», «сила-скорость», «сила-мощность» для обеих изоформ сердечного миозина.
2.1. Связь «рСа-скорость» для изоформ сердечного миозина V1 и V3
Кривые зависимости «рСа-скорость» имели вид сигмоиды (рисунок 1). Значения коэффициента кооперативности Хилла кривой «рСа-скорость» достоверно не отличались для обеих изоформ сердечного миозина: h = 1,83 ± 0,12 для изомиозина V1 и 1,39 ± 0,39 для изомиозина V3. Кальциевая чувствительность, определяемая величиной рСа50, не различалась для обеих изоформ: для V1 значение рСа50 равнялось 7,56 ± 0,01; для V3 – 7,57 ± 0,01. Аналогичные результаты в отношении кальциевой чувствительности методом искусственной подвижной системы для V1 и V3 кролика получены Noguchi с соавт., 2003. Значение коэффициента кооперативности авторы не определяли.
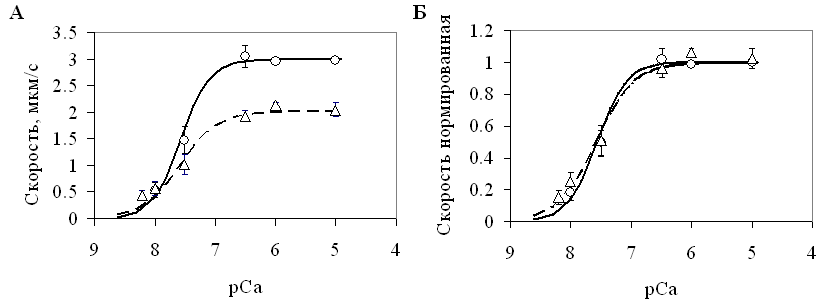
Рисунок 1 – Кривые зависимости скорости движения регулируемого филамента от концентрации кальция для изомиозинов V1 (сплошная линия) и V3 (пунктирная линия).
Примечание: рСа - отрицательный десятичный логарифм концентрации кальция. Кружками и треугольниками обозначены значения скоростей, полученных в экспериментах на искусственной подвижной системе для V1 и V3, соответственно. Линия регрессии соответствует уравнению Хилла. Значения скоростей представлены как среднее значение ± стандартное отклонение по трем экспериментам. Панель А: ненормированные кривые, панель Б: кривые нормированые по скорости.
Обнаружено, что скорость скольжения регулируемого филамента при насыщающей концентрации кальция для обеих изоформ выше, чем скорость F-актина в 3,8 раза. Lu с соавт., 2006 показали, что благодаря аллостерическому влиянию тропомиозина на актин большее количество гидрофобных аминокислотных остатков на актине становится доступным для лучшего стереоспецифического соответствия между актиновой нитью и молекулами миозина, что может служить причиной увеличения скорости скольжения тонкого регулируемого филамента при насыщающей концентрации ионов кальция по отношению к скорости нерегулируемого тонкого филамента.
Согласно теории мышечного сокращения, скорость ненагруженного укорочения не зависит от количества поперечных мостиков [Huxley, 1957]. В связи с этим возникает вопрос, в чем состоит причина зависимости скорости движения филаментов от концентрации кальция в искусственной подвижной системе? Ответ состоит в том, что движение филаментов в такой системе не является ненагруженным. Имеется, по крайней мере, два фактора, которые могут выступать в качестве неучитываемой нагрузки: нитроцеллюлозная поверхность проточной камеры и нефункционирующие белки, связанные с поверхностью камеры и актиновой нитью [Haeberle and Hemric, 1995]. По этой причине, в искусственной подвижной системе с регулируемой тонкой нитью связь «рСа-скорость», которая, фактически, представляет собой связь «рСа-сила» с неучтённой силой, должна быть.
2.2. Связь «рСа-сила» для изоформ сердечного миозина V1 и V3
Было установлено, что при концентрации 300 мкг/мл сердечного миозина, загружаемого в проточную камеру, коэффициенты кооперативности Хилла кривых «pCa-сила» для изоформ сердечного миозина достоверно не различаются (1,54 ± 0,01 для V3 и 1,56 ± 0,01 для V1); при концентрации 200 мкг/мл величина h достоверно больше для изоформы V3, чем для V1 (2,00 ± 0,01 для V3 и 1,76 ± 0,01 для V1). Кроме того, для каждого изофермента с понижением концентрации белка коэффициент кооперативности возрастает (рисунок 2).
Кальциевая чувствительность незначительно, но достоверно различалась у обеих изоформ миозина при концентрации 300 мкг/мл и равнялась 7,32 ± 0,01 и 7,42 ± 0,01 для V1 и V3, соответственно. Однако при концентрации 200 мкг/мл наблюдалось более значительное различие в кальциевой чувствительности: рСа50 = 7,34 ± 0,01 для V1 и рСа50 = 7,93 ± 0,01 для V3. Таким образом, кальциевая чувствительность отношения «рСа-скорость» для изоформы V3 выше, чем для V1, То есть, изоформы сердечного миозина по-разному влияют на зависимость «рСа-сила».
Сдвиг влево кривой зависимости «рСа-сила» для V3 изоформы относительно кривой для V1 можно объяснить различием кинетики мостиков этих двух изоформ. Время присоединённого состояния для изоформы V3 больше, чем для V1 примерно в два раза [Warshaw et al., 1995]. Как полагают Brandt с соавт., 1982 увеличение времени сильно-связанного состояния ведёт к тому, что Ca2+ остается дольше связанным с тропонином С (TnC), что в свою очередь увеличивает кальциевую чувствительность отношения «рСа-сила», то есть, ведёт к сдвигу кривой «рСа-сила» влево.

Рисунок 2 – Нормированные зависимости относительной силы, развиваемой поперечными мостиками изомиозинов V1 и V3, от концентрации свободного кальция, полученные в экспериментах на искусственной подвижной системе.
Примечание: рСа - отрицательный десятичный логарифм концентрации кальция в растворе. (А) – кривые для V1 при концентрациях миозина на поверхности проточной камеры 200 (сплошная линия) и 300 мкг/мл (пунктирная линия). (Б) – те же кривые для изомиозина V3. Кружками обозначена относительная сила при концентрации изомиозинов 200 мкг/мл, ромбами – при концентрации изомиозинов 300 мкг/мл. Относительная сила представлена как среднее значение ± стандартное отклонение по трем экспериментам. Линия регрессии соответствует уравнению Хилла.
Даже незначительное изменение кальциевой чувствительности (на 0,1 рСа при концентрации 300 мкг/мл загружаемого в проточную камеру миозина) имеет существенное физиологическое значение [Bottinelli et al., 1998].
2.3. Связь «сила-скорость» для изоформ сердечного миозина V1 и V3
Известно, что связь «сила-скорость» зависит от концентрации кальция [De Clerck et al., 1977]. Уровень кальция и механические условия через механизмы кооперативности регуляторных и сократительных белков могут существенно модулировать зависимость «сила-скорость». Можно ожидать, что связь «сила-скорость», зарегистрированная при разных уровнях кальция, для изоформ миозина будет отличаться в случае, если кооперативное влияние этих изоформ на кинетику кальций-тропониновых комплексов различно.
Были получены кривые зависимости «сила-скорость» для изоформ сердечного миозина при насыщающей (рСа=6,5) и ненасыщающей (рСа=7,0) концентрациях кальция (рисунок 3). Кривые зависимости «сила-скорость» имели форму гиперболы в области малых нагрузок и отличались от гиперболической в области больших нагрузок. Кроме того, форма кривых для изоформы V1 миозина отличалась от формы кривых для изоформы V3.

Рисунок 3 – Зависимость «сила-скорость» для изоформ сердечного миозина V1 и V3 при рСа = 6,5 и рСа = 7,0.
Примечание: рСа- отрицательный десятичный логарифм концентрации кальция в растворе. Значения силы пронормированы на максимальное значение для каждой изоформы при данном значении рСа. Кружками и треугольниками обозначены экспериментальные данные, полученные при рСа = 6,5 и 7,0, соответственно, аппроксимирующая линия построена с помощью полинома третьей степени методом наименьших квадратов. Значения скоростей представлены как среднее значение ± стандартное отклонение. Сплошная линия представляет собой кривую, соответствующую теоретической кривой, полученной с помощью гиперболического уравнения Хилла методом наименьших квадратов.
Форма кривой зависимости «сила-скорость», получаемая как связь между постнагрузкой и максимальной скоростью укорочения мышцы под этой нагрузкой в экспериментах на папиллярных мышцах и трабекулах отличается от гиперболы.
В области больших нагрузок она имеет характерный изгиб в виде направленной вверх выпуклости [Hennekes et al., 1978, Pagani and Julian, 1984].
Наличие этого изгиба связывали с особенностями метода получения данной зависимости, а не с поведением поперечных мостиков, то есть считалось, что связь «сила-скорость» для популяции поперечных мостиков в кардиомиоците должна иметь гиперболический вид в соответствии с уравнением Хилла.
Форма кривых, полученных Oiwa с соавт., 1990 на центрифужном микроскопе для скелетного миозина и изоформ сердечного миозина [Sugiura et al., 1995], очень похожа на форму полученных нами кривых: в области малых нагрузок кривая «сила-скорость» имеет вид гиперболы. Негиперболический участок на наших кривых и кривых, полученных Suguira с соавт. и Oiwa с соавт., является более выраженным, чем в работах на мышечных волокнах, что можно объяснить особенностями применяемой методики. Можно предположить наличие в искусственной подвижной системе постоянного дополнительного сопротивления движению, независящее от скорости (то есть, типа «сухого» трения). Мы оценили его вклад и показали, что с учетом «сухого» трения форма кривой зависимости «сила-скорость» приближается к форме кривой, полученной в работах на волокне.
Кривые зависимости «сила-скорость», полученные с помощью центрифужного микроскопа для изоформ сердечного [Sugiura et al., 1995] и скелетного миозина [Oiwa et al., 1990] несколько отличаются по форме. Негиперболическая часть кривых для изоформ сердечного миозина выражена сильнее, чем для скелетного миозина. Bottinelli с соавт.., 1991 показали, что для волокон, содержащих одни изоформы скелетного миозина, форма кривой зависимости «сила-скорость» отклоняется от гиперболической в области больших нагрузок (около 0,8 F/F0), а содержащих другие – нет. Этот результат может свидетельствовать о том, что отклонение от гиперболичности является свойством волокна, зависящим от состава сократительных белков.
Таким образом, наличие негиперболического участка на кривой зависимости «сила-скорость», скорее всего, является функциональным свойством самих поперечных мостиков. Кроме того, степень выраженности негиперболической части, возможно, зависит от изоформ миозина.
По нашим данным, максимальная скорость скольжения тонкого филамента по изоформе V1 больше максимальной скорости скольжения по изоформе V3 как при насыщающей, так и при ненасыщающей концентрациях кальция в растворе, также как и скорость укорочения папиллярных мышц [Pagani et al., 1984] и кардиомиоцитов с преимущественным преобладанием быстрой изоформы миозина.
Работы, выполненные на скинированных кардиомиоцитах крысы [Herron et al., 2001, Herron and McDonald, 2002; Korte et al., 2005;], на скинированных папиллярных мышцах трансгенных кроликов [Suzuki et al., 2009] и мышей [Krenz et al., 2003] с преобладанием той или иной изоформы сердечного миозина, показывают, что при всех нагрузках скорость укорочения выше для волокон, содержащих большее количество изоформы V1. По нашим данным, в области малых и средних нагрузок при насыщающей (рСа = 6,5) и ненасыщающей (рСа = 7,0) концентрациях свободного кальция изоформа V1 перемещает регулируемый тонкий филамент быстрее, чем изоформа V3 (рисунок 4).

Рисунок 4 – Зависимость «сила-скорость» для изоформ сердечного миозина V1 и V3 при рСа = 6,5 и рСа = 7,0.
Примечание: рСа - отрицательный десятичный логарифм концентрации кальция. Значения силы пронормированы на максимальное значение для каждой изоформы при данном значении рСа. Кружками и треугольниками обозначены экспериментальные данные, полученные для V1 и V3, соответственно, аппроксимирующая кривая построена с помощью полинома третьей степени методом наименьших квадратов. Значения скоростей представлены как среднее значение ± стандартное отклонение.
Согласно нашим данным, разница в скорости скольжения тонкого филамента по разным изоформам уменьшается с ростом нагрузки: при отсутствии нагрузки скорость для V1 и V3 изоформы отличалась на 45%, а при 0,5 F0 разница составила ~ 25 %, при 0,7 F0 – ~ 5%. В диапазоне от 0,8 F0 скорости скольжения филаментов по V1 или V3 достоверно не отличались при насыщающей и ненасыщающей концентрациях кальция.
При ненасыщающей концентрации кальция Vmax для V1 и V3 изоформы отличалась на 60 %, а при 0,5 F0 составила ~50 %, при 0,75 F0 – ~ 30%. Таким образом, с уменьшением концентрации кальция при одних и тех же нагрузках разница в скоростях быстрой и медленной изоформ миозина увеличилась. Причем это произошло за счет того, что скорость V3 изоформы уменьшилась в большей степени, чем V1 изоформы. Так, значение Vmax для V1 отличалось на 30 % при насыщающей и ненасыщающей концентрациях кальция, а для V3 – на 45 %; при 0,1 F0 на ~22 % и 40 % для V1 и V3, соответственно; при 0,25 F0: ~6 % и 15 % для V1 и V3, соответственно. Таким образом, зависимость «сила-скорость» для V3 изоформы является более чувствительной к концентрации кальция по сравнению с V1.
Для каждой изоформы миозина в области больших нагрузок (начиная с 0,8 от максимальной нагрузки) скорость скольжения тонкого филамента не зависит от концентрации свободного кальция в растворе, то есть, не зависит от количества поперечных мостиков.
В работе Korte с соавт., 2005 на скинированных кардиомиоцитах крысы было показано, что первое – кривизна кривой зависимости «сила-скорость», оцененная по коэффициенту а/F0, возрастала при увеличении доли V3 изоформы в кардиомиоците, второе – при уменьшении концентрации кальция от насыщающей (рСа = 4,5) до ненасыщающей (рСа = 9,0) кривизна кривой зависимости «сила-скорость» достоверно не изменялась. В наших исследованиях форма кривых зависимости «сила-скорость» для изомиозинов V1 и V3 отличалась как при насыщающей, так и при ненасыщающей концентрации кальция в растворе. Степень кривизны кривых для изоформы V3 была выше, чем для V1, что следует из значений отношения а/F0: для изоформы V3 это значение меньше, что также свидетельствует о большей эффективности преобразования энергии гидролиза АТФ в работу изоформой V3.
Таким образом, результаты наших экспериментов на искусственной подвижной системе, позволяют сделать вывод о том, что состав тяжелых цепей миозина определяет форму кривой зависимости «сила-скорость». При изменении концентрации кальция степень кривизны связи «сила-скорость» для изоформы V3 меняется в большей степени, что свидетельствует о её большей чувствительности к изменению концентрации кальция.
2.4. Связь «сила-мощность» для изоформ сердечного миозина V1 и V3
Так как уровень кальция в кардиомиоците в ходе сокращения меняется, а максимальная скорость укорочения зависит от уровня активации, то концентрация кальция должна влиять и на характеристики отношения «сила-мощность».
Была получена зависимость «сила-мощность» для изоформ V1 и V3 при насыщающей (рСа = 6,5) и ненасыщающей (рСа = 7,0) концентрациях кальция в растворе (рисунок 5).
Максимум развиваемой мощности для изоформы V1 оказался больше, чем для изоформы V3 при обеих исследованных концентрациях свободного кальция, что соответствует результатам, полученным ранее на скинированных препаратах папиллярных мышц и кардиомиоцитах кроликов [Robbins et al., 2009], мышей [Krenz et al., 2007] и крыс [Herron et al., 2001; Korte et al., 2005]. Таким образом, результаты наших экспериментов позволяют сделать вывод о том, что мощность, развиваемая кардиомиоцитами и папиллярными мышцами, определяется составом тяжелых цепей миозина.
В наших исследованиях показано, что большая мощность изоформы V1 по сравнению с изоформой V3 достигается, в основном, за счет более высокой её скорости, регистрируемой по скольжению регулируемого филамента.
Согласно нашим данным максимум развиваемой мощности для изоформы V3 незначительно сдвинут в сторону больших нагрузок относительно максимума мощности для изоформы V1 при насыщающей и ненасыщающей концентрациях кальция (рисунок 5). Аналогично результатам [McDonald et al., 1998] на скинированных кардиомиоцитах крысы, наши данные показывают, что с уменьшением уровня кальциевой активации возрастает уровень нагрузки, при которой достигается оптимальное значение мощности (кривая «сила-мощность» сдвигается влево). Такой сдвиг имеет значение для поддержания мощности на оптимальном уровне, несмотря на уменьшение скорости сокращения при низком уровне кальция.
По нашим данным мощность, развиваемая каждой изоформой сердечного миозина, не зависит от концентрации свободного кальция в растворе во всем диапазоне нагрузок. В диапазоне больших нагрузок (от 0,9 F0 до максимума) изоформы V1 и V3 развивают одинаковые мощности как при насыщающей, так и при ненасыщающей концентрациях свободного кальция в растворе. McDonald с соавт., 1998 на скинированных кардиомиоцитах крысы получили такой же результат: в области больших нагрузок выход мощности не зависел от уровня кальция.
Таким образом, в результате наших исследований впервые с использованием метода искусственных подвижных систем мы подтвердили, что мощность, развиваемая кардиомиоцитами и папиллярными мышцами, определяется составом тяжелых цепей миозина. Быстроциклирующая изоформа V1 сердечного миозина 
Рисунок 5 – Зависимость «сила-мощность», полученная в искусственной подвижной системе при насыщающей (рСа = 6,5) и ненасыщающей (рСа = 7,0) концентрации свободного кальция в растворе для V1 (сплошная линия) и V3 (пунктирная линия) изоформ сердечного миозина.
Примечание: рСа - отрицательный десятичный логарифм концентрации кальция. Аппроксимирующая кривая построена с помощью полинома третьей степени методом наименьших квадратов. Значения мощности представлены как среднее значение ± стандартное отклонение.
развивает большую мощность по сравнению с изоформой V3. Наши результаты, как и результаты на скинированных кардиомиоцитах крысы, продемонстрировали, что с уменьшением уровня кальциевой активации возрастает уровень нагрузки, при которой достигается оптимальное значение мощности, что позволяет поддерживать мощность на оптимальном уровне, несмотря на падение скорости сокращения.
Следствием сердечной недостаточности, диабета и гипертиреоидизма является угнетение функции сердца [Eichhorn and Bristow, 1996; Tahiliani and McNeill, 1986], но точный молекулярный механизм этого явления неизвестен. Metzger с соавт., 1999 на грызунах продемонстрировали, что с каждым из этих заболеваний связан сдвиг экспрессии изоформ тяжелых цепей сердечного миозина. Аналогичное явление описано при сердечной недостаточности у человека. Miyata с соавт., 2000 выявили, что левый желудочек здорового человека содержит ~ 7 % -ТЦМ, но на конечных стадиях сердечной недостаточности эта изоформа сердечного миозина в желудочке отсутствует. Отличие в развиваемой мощности V1 и V3 изоформами миозина, а также кардиомиоцитами, содержащими - и -ТМЦ может служить основой для объяснения молекулярного механизма изменения функции сердца при этих заболеваниях.
Выводы
- Актин-активируемая Mg2+-АТФ-азная активность и скорость скольжения как F-актина, так и регулируемого филамента для изоформы V1 в 1,7 раза выше, чем для V3; сила, развиваемая сердечным изомиозином V3 кролика в 2 раза больше, чем изомиозином V1.
- Коэффициент кооперативности Хилла зависимостей «рСа-скорость» и «рСа-сила» для изоформ сердечного миозина, а также кальциевая чувствительность связи «рСа-скорость» достоверно не отличаются; кальциевая чувствительность связи «рСа-сила» для изоформы V3 выше, чем для V1; при низкой концентрации каждой из изоформ и коэффициент кооперативности, и кальциевая чувствительность больше для V3, чем для V1.
- Зависимость «сила-скорость» для изомиозинов V1 и V3, полученная методом искусственной подвижной системы, соответствует гиперболическому уравнению Хилла в области малых нагрузок и отклоняется от него в области больших нагрузок, что и определяет форму данной зависимости для мышечных препаратов.
- Степень кривизны зависимости «сила-скорость», для изоформы V3 выше, чем для изоформы V1; при уменьшении концентрации кальция разница в скоростях скольжения филаментов по изоформам V1 и V3 увеличивается за счет большего снижения скорости по медленной изоформе.
- Мощность, развиваемая каждой изоформой миозина, не зависит от концентрации кальция во всем диапазоне нагрузок; максимум развиваемой мощности изоформы V1 выше, чем изоформы V3, и сдвинут в сторону меньших нагрузок.
- Данные, полученные на молекулярном уровне, свидетельствует о том, что свойства изоформ сердечного миозина определяют активные механические свойства кардиомиоцитов и вносят основной вклад в адаптационную пластичность сердечной мышцы в норме и при патологии.
Практические рекомендации
При разработке исследовательских программ оценки кальциевой регуляции сокращения миокарда в норме и при патологии необходимо использовать полученные результаты по влиянию изоформного состава сердечного миозина на скорость и силу сокращения сердечной мышцы при разных уровнях кальциевой активации.
Список работ, опубликованных по теме диссертации
Публикации в изданиях, рекомендованных ВАК:
- Shchepkin D.V. Effects of cardiac myosin binding protein-C on the regulation of interaction of cardiac myosin with thin filament in an in vitro motility assay / D.V. Shchepkin, G.V. Kopylova, L.V. Nikitina, L.B. Katsnelson, B.Y. Bershitsky // Biochemical and Biophysical Research Communications. – 2010. – Vol. 401. – P. 159-163.
- Shchepkin D.V. Assessment of the effect of cardiac myosin binding protein-C on ‘рСа-velocity’ relationship obtained in an in vitro motility assay / D.V. Shchepkin, G.V. Kopylova, B.Y. Bershitsky, L.V. Nikitina // J Gen Phys. – 2009. – Vol. 134 – 1a-2a.
- Никитина Л.В. Исследование взаимодействия сократительных и регуляторных белков миокарда кролика методом искусственных подвижных систем / Л.В. Никитина, Г.В. Копылова, Д.В. Щепкин, Л.Б Кацнельсон // Биохимия. – 2008. – Т. 73, № 2. – С. 219-227.
- Никитина Л.В. Оценка механической активности сердечных изомиозинов V1 и V3 методом искусственных подвижных систем с регулируемой тонкой нитью / Л.В. Никитина, Г.В. Копылова, Д.В. Щепкин, Л.Б Кацнельсон // Биофизика. – 2008. – Т. 53, № 6. – С. 956-962.
- Kopylova G.V. Mechanical characteristics of different rabbit cardiac isomyosins obtained in an in vitro motility assay with regulated thin filaments / G.V. Kopylova, L.V. Nikitina, D.V. Shchepkin, L.B. Katsnelson // J Muscle Res Cell Motil. – 2007. – Vol. 28. – P. 447.
- Копылова Г.В. Применение метода in vitro подвижных систем для исследования кальций-механической связи в скелетной и сердечной мышцах / Г.В. Копылова, Л.Б. Кацнельсон, Д.А. Овсянников, С.Ю. Бершицкий, Л.В. Никитина // Биофизика. – 2006. – Т. 51, № 5. – С. 781-785.
- Nikitina L. Mechanical and kinetic properties of rabbit cardiac isomyosins V1 and V3 compared in an in vitro motility assay and optical tweezers / L.Nikitina, G.Kopylova and J.E.Molloy // J Muscle Res Cell Motil. – 2005. – Vol. 26(1). – P. 74.
Публикации в сборниках статей, материалах конференций:
- Shchepkin D.V. Effects of cardiac myosin binding protein-C on myocardium contractile activity assessed in an in vitro motility assay / D.V. Shchepkin, G.V. Kopylova, L.V. Nikitina. // Biological Motility: from Fundamental Achievements to Nanotechnologies: international symposium (Pushchino, May 11-15, 2010). – Pushchino, 2010. – P. 237-239.
- Nikitina L.V. pCa-Force relationship assessed in an in vitro motility assay for rabbit cardiac muscle / L.V. Nikitina, G.V. Kopylova, D.V. Shchepkin, L.B. Katsnelson // Biological Motility: Achievements and Perspectives: international symposium (Pushchino, May 11-15, 2008). – Pushchino, 2008. – P. 44-48.
- Никитина Л.В. Связь «рСа-сила» миокарда кролика, полученная техникой in vitro подвижной системы / Л.В. Никитина, Г.В. Копылова, Д.В. Щепкин, Л.Б. Кацнельсон // Сборник тезисов докладов участников Международного конкурса научных работ молодых ученых в области нанотехнологий. – М., 2008. – С. 512-513.
- Копылова Г.В. Определение соотношения - и - тяжелых цепей сердечного миозина в миокарде различных животных методом одномерного SDS гель-электрофореза / Г.В. Копылова, Д.В. Щепкин, Л.В. Никитина // Тезисы докладов XX съезда физиологического общества им. Павлова. – М., 2007. – С. 277.
- Comparison of kinetic characteristics of musculoskeletal and cardiac myosins using the method of regulated contractile systems / G.V. Kopylova, L.V. Nikitina, L.B. Katsnelson, S.Yu.Bershitsky // Biol. motility: basic research and practice: international symposium (Pushchino, 11-15 May, 2006). – Pushchino, 2006. – Р. 25-27.
Список сокращений
АТФ – аденозинтрифосфат
БСА – бычий сывороточный альбумин
ПААГ – полиакриламидный гель
ТМРФ – тетраметилродамин-фаллоидин
ТЦМ – тяжелые цепи миозина
ЭГТА – этиленгликоль тетрауксусная кислота
F-актин – филаментарный актин
TnC – тропонин C
Копылова Галина Васильевна
ИССЛЕДОВАНИЕ ФУНКЦИОНАЛЬНЫХ ХАРАКТЕРИСТИ ИЗОФОРМ СЕРДЕЧНОГО МИОЗИНА
Специальность 03.03.01 - Физиология
Автореферат
диссертации на соискание ученой степени
кандидата биологических наук

