Структура стенки цистерны хили в норме и пр и имплантации стента из никелида титана
На правах рукописи
Герасёнова Екатерина Александровна
СТРУКТУРА СТЕНКИ ЦИСТЕРНЫ ХИЛИ
В НОРМЕ И ПРИ ИМПЛАНТАЦИИ СТЕНТА
ИЗ НИКЕЛИДА ТИТАНА
03.03.04 – клеточная биология, цитология, гистология
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Томск – 2010
Работа выполнена в Учреждении Российской академии медицинских наук Научно-исследовательском институте клинической и экспериментальной лимфологии Сибирского отделения РАМН (г. Новосибирск)
Научный руководитель:
доктор биологических наук, профессор Бгатова Наталия Петровна
Официальные оппоненты:
доктор медицинских наук, профессор Суходоло Ирина Владимировна
кандидат медицинских наук, старший
научный сотрудник Фомина Татьяна Ивановна
Ведущая организация: ГОУ ВПО Новосибирский государственный медицинский университет г. Новосибирск
Защита состоится « » июня 2010 г. в часов на заседании диссертационного совета Д 208.096.03 при Сибирском государственном медицинском университете Федерального агентства по здравоохранению и социальному развитию (634050, г. Томск, Московский тракт, 2)
С диссертацией можно ознакомиться в научно – медицинской библиотеке Сибирского государственного медицинского университета
Автореферат разослан «___»_____________2010г.
Ученый секретарь диссертационного совета А.В. Герасимов
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования. Исследованию структуры лимфатических сосудов и грудного протока (далее – ГП) посвящено много исследований (Борисов А. В., 1987; Mebius R. E. et al., 2006; Boccardo F. et al., 2009). Однако данные литературы крайне противоречивы. Спорными являются вопросы количественного содержания и организации миоцитов и соединительнотканных волокон в разных отделах лимфатических сосудов (Петренко В. М., 2008). Наиболее исследованными являются терминальные отделы грудного протока, тогда как структура стенки цистерны хили изучена недостаточно.
Несмотря на успехи, достигнутые в сосудистой хирургии за последние два десятилетия, проблема лечения больных лимфостазами конечностей продолжает оставаться одной из сложных и актуальных. Предложенные в настоящее время методы консервативного лечения лимфатических отеков после мастэктомии (Karki A. et al., 2009; Pain S. J., 2009; Pilch U. et al., 2009) не всегда дают положительные результаты.
Проблема хирургического лечения лимфедемы верхних конечностей была и остается спорной (Золотаревский В. Я. и др., 1990; Corinne B. et al., 2006). Наибольший интерес представляют операции, устраняющие препятствие на пути лимфооттока и ускоряющие ток лимфы по функционирующим лимфатическим сосудам. Основные операции этой группы предусматривают формирование лимфовенозных соустий (Абалмасов К. Г. и др., 2003; Campisi С. et al., 2007; Damstra R. J. et al., 2008; Boccardo F. M. et al., 2009). Однако данные методы хирургического лечения приносят облегчение не всем пациентам. По данным различных авторов процент положительных результатов после операции наложения микролимфовенозных анастомозов (далее – МЛВА) значительно варьирует и колеблется в пределах от 32 % до 97,25 % (Выренков Ю. Е. и др., 1991).
В литературе имеются единичные упоминания о применении стентов при формировании МЛВА. В 1992 году Shaper N. J. и Rutt D. R. впервые использовали методику стентирования тефлоновыми стентами микролимфовенозных анастомозов в эксперименте, что было более эффективно, чем наложение простых лимфовенозных анастомозов, но со временем привело к окклюзии сосуда (Shaper N. J., Rutt D. R., 1992).
Известно, что высокой степенью биосовместимости обладают пористые материалы на основе никелида титана (далее – TiNi). В связи с тем, что ранее не проводили стентирования лимфатических сосудов и грудного протока стентами из никелида титана, то изучение структуры грудного протока в области цистерны хили и влияние стента из TiNi на стенку сосуда являются актуальными.
Цель исследования. Выявить особенности структурной организации стенки грудного протока крысы в области цистерны хили в условиях нормы и в различные сроки после имплантации в его просвет стента из никелида титана.
Задачи исследования:
- Изучить структурную организацию стенки грудного протока крысы в области цистерны хили в условиях нормы.
- Исследовать структуру стенки грудного протока крысы в области цистерны хили через 7, 14 и 30 суток после имплантации в его просвет стента из никелида титана.
- Изучить ультраструктуру эндотелиальных, мышечных клеток и фибробластов стенки цистерны хили в норме и через 7, 14 и 30 суток после имплантации в ее просвет стента из никелида титана.
- Провести анализ структуры стента из никелида титана методами сканирующей электронной микроскопии и рентгеноспектрального анализа через 7, 14 и 30 суток после его имплантации.
Положения, выносимые на защиту:
- В условиях нормы в стенке грудного протока в области цистерны хили самую большую объемную плотность имеет наружная оболочка. В эндотелиоцитах, выстилающих внутреннюю оболочку цистерны хили, наибольший объем цитоплазмы (16 %) занимают митохондрии. Мышечные клетки средней оболочки имеют многочисленные мио-миоцитарные контакты конец в конец и контакты боковыми поверхностями центральных участков. Фибробласты обнаруживаются во всех оболочках цистерны хили и достоверно не различаются между собой по объемной плотности митохондрий, мембран гранулярной эндоплазматической сети и численной плотности рибосом.
- Имплантация стента из никелида титана в просвет грудного протока в области цистерны хили не приводит к фиброзированию просвета сосуда и нарушению целостности его оболочек, а также не оказывает повреждающего действия на ультраструктурную организацию эндотелиоцитов, фибробластов и миоцитов оболочек сосуда.
- Применение стента из никелида титана для стентирования грудного протока в эксперименте не приводит к деформации стента окружающими тканями, стенозированию и обтурации его просвета тромбоцитами, эластическими и коллагеновыми волокнами, клетками и минеральными отложениями.
Научная новизна исследования. Впервые с использованием световой, электронной микроскопии и морфометрии исследована структура стенки грудного протока крысы в области цистерны хили в условиях нормы. Выявлено, что самую большую объемную плотность имеет наружная оболочка, а наименьшую внутренняя оболочка сосуда. В цитоплазме эндотелиальных клеток (далее – ЭК), выстилающих внутреннюю оболочку грудного протока, наибольшую объемную плотность занимают митохондрии. В мышечных клетках средней оболочки имеют место многочисленные мио-миоцитарные контакты. Фибробласты обнаруживаются во всех оболочках цистерны хили, достоверно не различаются между собой по объемной плотности митохондрий, мембран гранулярной эндоплазматической сети и численной плотности рибосом.
Впервые установлено, что имплантация стента из никелида титана не нарушает структурной целостности стенки грудного протока и не приводит к стенозированию просвета лимфатического сосуда. Не происходит зарастания просвета протока в области цистерны хили мышечной или соединительной тканью. Не отмечается деструктивных изменений в ультраструктурной организации эндотелиоцитов, мышечных клеток и фибробластов оболочек цистерны хили.
Впервые при помощи сканирующей электронной микроскопии изучено состояние стента из никелида титана и проведён рентгеноспектральный анализ фрагментов, взятых с наружной и внутренней поверхностей стента. Показано, что через 7, 14 и 30 суток после постановки стента в грудной проток не происходит обструкции, стенозирования просвета стента и его деформации окружающими тканями. На 14-e и 30-e сутки имплантации в структуре фрагментов стента возможно появление в минимальных количествах новых неорганических отложений, которые не отмечаются через 7 суток после имплантации стента.
Теоретическая и практическая значимость. Полученные количественные и качественные характеристики стенки грудного протока крысы в области цистерны хили в условиях нормы и при имплантации в его просвет стента из никелида титана могут быть использованы для оценки характера и степени поражения крупных лимфатических сосудов в условиях патологии.
Разработанная модель спиралевидного стента из никелида титана и методика постановки стента в грудной проток в области цистерны хили в условиях эксперимента может быть применена для имплантации в соотвествующие по размерам лимфатические сосуды и адаптирована для дальнейшего применения при лечении лимфостазов верхних и нижних конечностей.
Апробация работы. Основные положения работы докладывались и обсуждались на VIII международном симпозиуме и IX Чуйской научно-практической конференции «Проблемы саногенного и патогенного эффектов экологического воздействия на внутреннюю среду организма» (Бишкек, 2007), на международной конференции «Фундаментальные проблемы лимфологии и клеточной биологии» (Новосибирск, 2008), на Всероссийской научно-практической конференции «Инновационные технологии в эстетической медицине и пластической хирургии – »(Новосибирск, 2007), на III Съезде лимфологов России (Москва, 2008).
Результаты работы используются в учебном процессе на кафедре гистологии, эмбриологии и цитологии Новосибирского государственного медицинского университета, а также внедрены в практику научно-исследовательской работы отдела профилактической и экологической лимфологии Учреждения Российской академии медицинских наук Научно-исследовательского института клинической и экспериментальной лимфологии Сибирского отделения РАМН (г. Новосибирск).
Публикации. По теме диссертации опубликовано 6 печатных работ, из них 1 – в ведущем рецензируемом научном журнале, рекомендуемом ВАК Минобрнауки России для публикаций основных результатов диссертации.
Объем и структура работы. Диссертация изложена на 129 страницах машинописного текста и состоит из введения, обзора литературы, главы о материалах и методах исследования, главы о результатах собственных исследований и обсуждения полученных результатов, выводов и списка литературы. Работа иллюстрирована 69 рисунками и содержит 17 таблиц. Библиографический указатель включает 182 источника, из них 75 отечественных и 107 зарубежных авторов.
Личный вклад автора. Весь материал, представленный в диссертации, получен, обработан и проанализирован лично автором.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Исследование было проведено на 60 белых крысах породы Вистар массой тела 300 – 350 г, полученных из вивария Института цитологии и генетики Сибирского отделения РАН (г. Новосибирск). В течение всего эксперимента животные получали стандартный виварный рацион. Все манипуляции с лабораторными животными проводили в соответствии с правилами, принятыми Европейской конвенцией по защите позвоночных животных, используемых для экспериментальных и иных научных целей (Страсбург, 1986).
Крысы были разделены на 4 группы по 15 особей в зависимости от сроков выведения из опыта. В контрольную группу вошли интактные животные, у которых осуществлялся забор и изучение структуры грудного протока вне условий стентирования. Стенты изготавливались на базе НИИ теоретической и прикладной механики СО РАН из TiNi проволоки диаметром 70 мкм при помощи мини-токарного станка. Первая опытная группа была представлена животными, которым был установлен стент из никелида титана в цистерну хили грудного протока на 7 суток. Вторая опытная группа состояла из животных, которым был установлен стент из никелида титана в цистерну хили грудного протока на 14 суток. В третьей опытной группе содержались животные, которым был установлен стент из никелида титана в цистерну хили грудного протока на 30 суток.
Для изучения структурной организации стенки грудного протока в условиях нормы и после стентирования в световом микроскопе и просвечивающем режиме электронного микроскопа, образцы сосуда из области цистерны хили фиксировали в 1-процентном растворе ОsО4 на фосфатном буфере, дегидратировали в этиловом спирте возрастающей концентрации и заключали в эпон. Из полученных блоков готовили полутонкие срезы толщиной 1 мкм, окрашивали толуидиновым синим, изучали под световым микроскопом и выбирали необходимые участки для исследования в электронном микроскопе. Из отобранного материала получали ультратонкие срезы толщиной 35 – 45 нм на ультратоме LKB–Nova, контрастировали насыщенным водным раствором уранилацетата, цитратом свинца и изучали в электронном микроскопе (JEOL, Japan). При увеличении 4000 в электронном микроскопе фотографировали различные участки грудного протока в области цистерны хили. Фотографии с негативов печатали при увеличении 8000 – 15000.
Для изучения поверхности стентов с помощью сканирующей электронной микроскопии их помещали в 2-процентный раствор глютарового альдегида с 2-процентным параформом на фосфатном буфере (0,02М, рН = 7,4). Далее осуществлялась проводка образцов по обезвоживающим растворам для подготовки материала к сканирующей электронной микроскопии (Ларионов П. М. и др. 2000). Сканирующий электронный микроскоп был снабжён энерго-дисперсионным спектрометром “OXFORD” для рентгеноспектрального микроанализа. В режиме рассеянных электронов отбирали участки с наружной и внутренней поверхностей стента со стандартно-ориентированной поверхностью относительно детектора. Затем устанавливался размер исследуемой площади по 1000 мкм2, устанавливалось время счета – 50 секунд для каждого исследования. Определяли энергетические спектры микроэлементного состава стенки стента. Полученные цифровые значения микроэлементного состава статистически обрабатывали.
Морфометрические исследования проводили с помощью программы обработки изображений Image Tool 3.00, а также при помощи многоцелевой открытой и закрытой тестовых систем при конечном увеличении в 32000 раз.
Таблица 1
Стереометрические символы, используемые при морфометрическом исследовании стенки сосуда
| Символы | Параметры | Размерность |
| Vv | Объемная плотность структур | мкм3/ мкм3 |
| Sv | Поверхностная плотность структур в объеме | мкм2/ мкм3 |
| NA | Численная плотность профилей структур в площади среза | мкм0/ мкм2 |
Примечание. Обозначение и размерность параметров приведены согласно рекомендациям Международного стереологического общества.
Статистическую обработку данных и графическое изображение результатов проводили с использованием программ Statistica 6,0 Excel 2003.
Определяли средние величины исследуемых морфометрических показателей и ошибку средней (M ± m). Достоверность различий сравниваемых средних величин определяли на основании критерия Стьюдента (для нормального распределения), (Плохинский Н. А., 1970). Различия между средними величинами считали достоверными при Р 0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Морфометрическое исследование стенки грудного протока в условиях нормы выявило, что самой большой по толщине является наружная оболочка. Ее объемная плотность была больше на 14,6 % средней и на 20,7 % внутренней оболочек сосуда (таблица 2). В цитоплазме эндотелиальных клеток, выстилающих внутреннюю оболочку грудного протока, определяли большое количество микропиноцитозных везикул и электронноплотных митохондрий с хорошо развитыми кристами. Мышечные клетки средней оболочки имели различный диаметр, преимущественно веретеновидную форму и многочисленные мио-миоцитарные контакты. Фибробласты обнаруживали во всех оболочках цистерны хили. Цитоплазма данных клеток характеризовалась разделением на внутреннюю, более плотную часть, окружающую ядро (эндоплазму), и периферическую, сравнительно светлую и образующую отростки эктоплазму. Эндоплазма содержала большую часть органелл, а эктоплазма была заполнена преимущественно элементами цитоскелета.
При сравнительном морфометрическом анализе оболочек грудного протока в области цистерны хили интактных крыс контрольной группы и животных трех опытных групп нами было выявлено, что величины показателей объемной плотности внутренней, средней и наружной оболочек достоверно не различаются. Наибольшую объемную плотность в структуре грудного протока в области цистерны хили у всех исследованных животных имела наружная оболочка, а наименьшую – внутренняя оболочка сосуда (таблица 2).
Таблица 2
Результаты морфометрического исследования стенки грудного протока крыс в области цистерны хили в норме и в различные сроки после имплантации стента из никелида титана (M ± m)
| Исследованные параметры | Контрольная группа (n = 15) | 1-я группа 7 суток (n = 15) | 2-я группа 14 суток (n = 15) | 3-я группа 30 суток (n = 15) |
| Vv внутренней оболочки | 19,85 ± 4,8 | 20,6 ± 2,5 | 19,8 ± 2,5 | 20,25 ± 2,8 |
| Vv средней оболочки | 25,6 ± 5,4 | 26,5 ± 3,8 | 27,7 ± 3,2 | 25,8 ± 3,5 |
| Vv наружной оболочки | 40,2 ± 7,3 | 42,5 ± 4,2 | 43,4 ± 4,8 | 41,05 ± 3,9 |
При изучении ультраструктурной организации эндотелиоцитов, выстилающих внутреннюю оболочку грудного протока, было выявлено, что у животных всех исследуемых групп данные клетки в основном имели вытянутую форму с многочисленными цитоплазматическими выростами на люминальной поверхности. В цитоплазме эндотелиальных клеток определяли большое количество микропиноцитозных везикул и электроноплотных митохондрий с хорошо развитыми кристами. Морфометрический анализ показал, что в цитоплазме эндотелиальных клеток грудного протока наибольшую объемную плотность занимали митохондрии. Не отмечали достоверных различий в величине данного показателя у животных различных экспериментальных групп.
Наблюдали тенденцию к возрастанию численной плотности свободных рибосом и уменьшению всех видов микровезикул в эндотелиоцитах, выстилающих цистерну хили, у крыс первой опытной группы по сравнению с соответствующими показателями у животных интактной группы (рис. 1).

Примечания: 1) К – контрольная группа. 2) 1, 2, 3 – опытные группы.
Рис. 1. Объемная плотность микропиноцитозных везикул в цитоплазме эндотелиоцитов грудного протока в области цистерны хили
Наши данные согласуются с данными литературы о том, что поверхность эндотелиоцитов лимфатических сосудов неровная, имеет многочисленные тонкие цитоплазматические выросты и участки западения. В ядрах располагается грубый, равномерно распределенный хроматин. Величина эндотелиоцитов может значительно различаться. В крупных клетках может быть два и более ядер (Сушко А. А., 1966).
В ультраструктурной организации мышечных клеток средней оболочки грудного протока в области цистерны хили нами также не было отмечено достоверных различий у животных разных групп. Миоциты имели преимущественно веретеновидную форму и были вариабельны по диаметру. В цитоплазме клеток определяли многочисленные гранулы гликогена. По периферии ядер располагался гетерохроматин. По данным ряда авторов, между миоцитами средней оболочки грудного протока имеются или мио-миоцитарные контакты типа нексусов, или мышечные клетки связаны друг с другом при помощи пальцевидных отростков (Борисова Р. П., 1982, Борисов А. В., 1984, Петренко В. М., 2008). У животных всех опытных групп отмечали сохранение описанных выше мио-миоцитарных контактов.
Морфометрическое исследование миоцитов грудного протока позволило выявить, что у крыс первой опытной группы на 35 % была увеличена объемная плотность мембран гранулярной эндоплазматической сети и имела место тенденция к возрастанию численной плотности прикрепленных рибосом, по сравнению с соответствующими показателями у крыс контрольной группы. В двух других опытных группах величины данных показателей не имели значительных отклонений от соответствующих значений у крыс контрольной группы (рис. 2, 3).
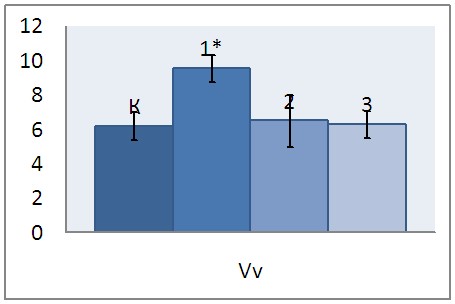
* статистически значимые различия по сравнению с контролем (p 0,05)
Примечания: 1) К – контрольная группа. 2) 1, 2, 3 – опытные группы.3.
Рис. 2. Объемная плотность мембран гранулярной эндоплазматической сети в цитоплазме миоцитов средней оболочки грудного протока в области цистерны хили
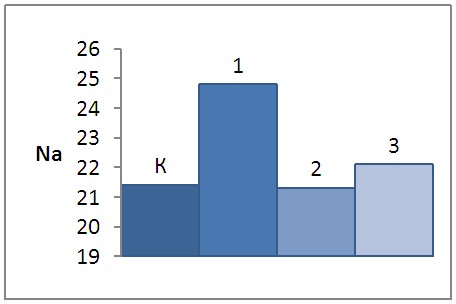
Примечания: 1) К – контрольная группа. 2) 1, 2, 3 – опытные группы.
Рис 3. Численная плотность прикрепленных рибосом в цитоплазме миоцитов средней оболочки грудного протока в области цистерны хили
Ультраструктурная организация фибробластов стенки грудного протока животных всех опытных группах не отличалась от структуры соответствующих клеток сосуда животных контрольной группы. Фибробласты имели вытянутую отросчатую форму и светлое ядро. Цистерны гранулярного эндоплазматического ретикулюма (далее – ГЭР) имели большую протяженность.
Наблюдали единичные лизосомы, небольшое число митохондрий и липидных включений. Ультраструктурная организация фибробластов соответствовала описанию строения данных клеток в условиях нормы другими авторами (Boggon R. P., Palfrey A. J., 1970; Boggon R. P., Palfrey A. J., 1973).
Полученные результаты свидетельствуют, что установка стента в просвет грудного протока крысы в области цистерны хили не оказывает повреждающего действия на целостность стенки сосуда и не приводит к нарушению ультраструктурной организации эндотелиоцитов, миоцитов и фибробластов. Незначительное повышение объемной плотности мембран ГЭР и численной плотности прикрепленных рибосом в миоцитах, а также снижение всех видов везикул в эндотелиоцитах грудного протока, отмечаемые у крыс первой опытной группы, которым стент был установлен на 7 суток, может быть следствием приспособительных изменений в клетках к условиям стентирования.
При изучении поверхности стента из никелида титана с помощью сканирующей электронной микроскопии и проведении рентгеноспектрального анализа фрагментов, взятых с его внутренней и наружной поверхностей через 7 суток эксперимента, не было выявлено обструкции и стенозирования просвета стента, а также деформации его окружающими тканями.
Наши данные о структуре стента при его постановке на 7 суток в просвет грудного протока согласуются с результатами, полученными при стентировании коронарных артерий (Абугов С. А. и др., 2001) и проведении эндоваскулярного стентирования подвздошных вен (Капранов С. А. и др., 2001). Авторы не отмечали случаев дислокации или нерасправления стентов. Ни у одного больного не было выявлено острого или подострого тромбоза стента после имплантации.
При исследовании энергетических спектров с фрагментов стента нами было обнаружено присутствие углерода, кислорода, серы и фосфора на фоне основных составляющих никелид титанового стента.
При анализе структуры стента через 14 суток после его установки в просвет грудного протока в области цистерны хили не наблюдали обструкции просвета стента и деформации окружающими тканями. Отмечали появление в некоторых фрагментах новых неорганических отложений в минимальных количествах, а именно Са, S, Al, Na, P и Si, которые не были отмечены в структуре стентов у животных первой опытной группы при постановке стента на 7 дней. Этот факт, по-видимому, является отражением участия лимфатической системы не только в водном и электролитном обмене, но и минеральном и свидетельствует о нормальном функционировании лимфатического русла (Титов А. Т. и др., 2000; Ларионов П. М. и др., 2003).
При проведении сканирующей электронной микроскопии поверхности стента через 30 суток после его постановки в просвет грудного протока в области цистерны хили не было выявлено деформации стента, обтурации его тромбоцитами, волокнами или клеточными элементами.
 Примечание. 2, 3 – опытные группы.
Примечание. 2, 3 – опытные группы.
Рис. 4. Неорганические отложения в структуре стента при его имплантации в просвет грудного протока на 14 и 30 суток
В третьей опытной группе отмечали появление в нескольких фрагментах неорганических отложений Са, S, Al, Na, P и Si, которые также были обнаружены в структуре стентов животных второй опытной группы. Вышеперечисленные неорганические элементы определялись в небольших количествах. Не отмечали возрастания величины данных показателей в структуре стентов животных третьей опытной группы по сравнению со стентами, установленными животным второй группы.
Полученные результаты могут свидетельствовать о том, что появление этих неорганических отложений не имеет существенного значения для химических свойств стента и не оказывает значимого влияния на структурную организацию стенки грудного протока в области цистерны хили при имплантации стента в просвет сосуда.
ВЫВОДЫ
- В условиях нормы в структуре цистерны хили самую большую объемную плотность имеет наружная оболочка; в эндотелиоцитах наибольший объем цитоплазмы занимают митохондрии; в мышечных клетках средней оболочки имеются многочисленные мио-миоцитарные контакты; в фибробластах преобладающими по численной плотности являются прикрепленные и свободные полисомальные рибосомы.
- Имплантация стента из никелида титана в просвет цистерны хили на 7, 14 и 30 суток эксперимента не приводит к нарушению целостности его оболочек и не оказывает повреждающего действия на ультраструктурную организацию эндотелиоцитов, фибробластов и миоцитов оболочек сосуда.
- Через 7 суток после имплантации стента из никелида титана в эндотелиоцитах внутренней и миоцитах средней оболочек цистерны хили развиваются структурные изменения, отражающие повышение их функциональной активности.
- Применение стента из никелида титана для стентирования грудного протока в области цистерны хили в течение 7, 14 и 30 суток эксперимента не приводит к деформации стента окружающими тканями, стенозированию и обтурации его просвета тромботическими, клеточными элементами и минеральными отложениями.
- В условиях имплантации никелид титанового стента в просвет грудного протока в течение 7 суток на фрагментах его наружной и внутренней поверхностей выявлено присутствие углерода, кислорода, серы и фосфора.
- При имплантации никелид титанового стента в течение 14 и 30 суток эксперимента в структуре его фрагментов в минимальных количествах обнаруживаются кальций, алюминий, натрий и кремний.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Полученные количественные и качественные характеристики стенки грудного протока крысы в области цистерны хили в условиях нормы и при имплантации стента из никелида титана могут быть использованы для оценки характера и степени поражения крупных лимфатических сосудов в условиях патологии.
- Материалы работы могут использоваться в учебном процессе при чтении лекций и ведении практических занятий по изучению строения стенки лимфатического протокам в области цистерны хили.
- Разработка метода стентирования лимфатических сосудов стентами из никелида титана позволит в дальнейшем предложить методику изготовления спиралевидных стентов из этого материала для стентирования микролимфовенозных анастомозов при лечении лимфостазов верхних и нижних конечностей.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Герасёнова Е. А, Бгатова Н. П., Ларионов П. М., Нимаев В. В., Дамбаев Г. Ц. Оценка эффективности стентирования грудного протока NiTi стентом в эксперименте на ранних сроках // Бюллетень Сибирского отделения Российской академии медицинских наук. – 2008. № 5. С. 32 – 37, автора – 0,15 п.л.
- Алтухов И. А., Солуянов Ю. М., Тупикова Е. А. Микрохирургические методики в лечении больных с вторичной лимфедемой верхней конечности после радикальной мастэктомии // Сибирский онкологический журнал. – 2007. С. 8 – 9, автора – 0,08 п.л.
- Колинько А. Н., Нимаев В. В., Тупикова Е. А., Кочеткова М. В., Комбанцев Е. А. Оценка качества жизни у больных с вторичной лимфедемой верхних конечностей // Успехи современного ествествознания. – 2008. № 1. С. 107, автора – 0,03 п.л.
- Нимаев В. В., Тупикова Е. А. Реабилитация больных с постэктомической лимфедемой верхних конечностей // Проблемы саногенного и патогенного эффектов экологического воздействия на внутреннюю среду организма : материалы VIII междунар. симп. и IX Чуйской научно-практ.конф. Бешкек., 2007. С.137 141, автора – 0,3 п.л.
- Комбанцев Е. А., Нимаев В. В., Смагин А. А., Кочеткова М. В., Герасёнова Е. А. Межлестничные лимфотропные инъекции в лечении постмастэктомического синдрома // Фундаментальные проблемы лимфологии и клеточной биологии : материалы междунар. конф. – Новосибирск, 2008. Т. 1. С. 183 184, автора – 0,05 п.л.
- Нимаев В. В., Шумков О. А., Колинько А. Н., Кочеткова М. В., Тупикова Е. А. Результаты наложения микролимфовенозных анастомозов у больных с постмастэктомической лимфедемой верхних конечностей // Инновационные технологии в эстетической медицине и пластической хирургии – 7 : материалы Всероссийской научно-практической конференции. Новосибирск, 2007. С. 27, автора – 0,03 п.л.
Благодарность за предоставление TiNi проволоки и консультации по ее использованию как имплантационного материала с памятью формы Гюнтеру Виктору Эдуардовичу, доктору технических наук, профессору, директору Научно-исследовательского института медицинских материалов и имплантатов с памятью формы при Сибирском физико-техническом институте им. В. Д. Кузнецова и Томском государственном университете
Благодарность за помощь в изготовлении спиралевидного стента из TiNi проволоки Анискину Владимиру Михайловичу, кандидату физико-математических наук, старшему научному сотруднику Учреждения Российской академии наук Института теоретической и прикладной механики им. С.А. Христиановича Сибирского отделения РАН

