Ионный механизм регуляции роста популяций нормальных и опухолевых клеток в организме
МИНИСТЕРСТВО ЗРАВООХРАНЕНИЯ И СОЦИАЛЬНОГО РАЗВИТИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ
ГОУ ВПО «КРАСНОЯРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ ПРОФЕССОРА В.Ф. ВОЙНО-ЯСЕНЕЦКОГО»
На правах рукописи
ЗАМАЙ ТАТЬЯНА НИКОЛАЕВНА
ИОННЫЙ МЕХАНИЗМ РЕГУЛЯЦИИ РОСТА ПОПУЛЯЦИЙ НОРМАЛЬНЫХ И ОПУХОЛЕВЫХ КЛЕТОК в организме
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора биологических наук
03.03.01 – физиология, 14.03.03 – патологическая физиология
Новосибирск-2011
Работа выполнена на кафедре биохимии Красноярского государственного медицинского университета им. проф. В.Ф. Войно-Ясенецкого и кафедре медицинской биологии Института фундаментальной биологии и биотехнологии Сибирского федерального университета.
| Научные консультанты: | доктор медицинских наук, профессор САЛМИНА Алла Борисовна доктор биологических наук, профессор МЕДВЕДЕВ Леонид Нестерович |
| Официальные оппоненты: | доктор биологических наук АЙЗМАН Роман Иделевич |
| доктор биологических наук АРХИПОВ Сергей Алексеевич | |
| доктор биологических наук МАКАРОВА Ольга Петровна | |
| Ведущая организация: | Сибирский государственный медицинский университет |
Защита состоится _12 мая_ 2011 года на заседании диссертационного совета
С диссертацией можно ознакомиться в библиотеке
Автореферат разослан
Ученый секретарь диссертационного совета,
кандидат биологических наук Бузуева И.И.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность и постановка проблемы
Исследование механизмов регуляции роста клеточных популяций – одна из наиболее важных задач физиологии и патофизиологии, направленных на разработку новых подходов к лечению пролиферативных заболеваний, вызванных выходом клеток из-под контроля регуляции пролиферации (Епифанова О.И., 2003; Lee M.H., Yang H.Y., 2002; Lee M.H., Yang H.Y., 2003; Lee M.H., Yang H.Y., 2003; Stewart Z.A. et al., 2003). В настоящее время постулируется несколько уровней регуляции пролиферации – молекулярный, клеточный, тканевой, органный и организменный. Нарушение регуляторных механизмов возможно на любом из них. Подробно исследованы механизмы регуляции пролиферации и их нарушения на молекулярном и клеточном уровнях (Епифанова О.И., 2003; Basi G., Draetta G., 1995; Roussel M.F., 1999; Miller M.E., Cross E.R., 2001; Ho A., Dowdy S.F., 2002; Knowles M.A., 2005). Предложены модели регуляции на уровне клеточной популяции и организма (Эмануэль Н.М., 1977; Донцов В.И., 1990; Варфоломеев С.Д., Гуревич К.Г., 1999; Шаровская Ю.Ю. и др., 2001; Dilman V.M., 1994; Giancotti F.G., Ruoslahti E., 1999). Однако общепринятой феноменологической модели, в которой бы все регуляторные уровни были увязаны в единую функциональную систему, пока не найдено.
В норме рост клеточных популяций всегда отражает потребности организма и определяется генетической программой метаболизма, дифференцировки и специализации. Помимо этого рост популяции зависит от доступности метаболических субстратов и влияния внешних факторов (Эмануэль Н.М., 1977; Варфоломеев С.Д., Гуревич К.Г., 1999). Каждая клетка в составе популяции представляет собой сложную функциональную саморегулирующуюся систему, все компоненты которой взаимосвязаны и взаимозависимы, а сигнальная система в норме позволяет удерживать параметры гомеостаза в контролируемых пределах. При силе воздействия, превышающей пороговые значения, адекватная приспособительная реакция клетки может потребовать перехода на иной уровень функционирования. Запуск соответствующей программы гомеостаза на уровне клеточной популяции может вызывать гипертрофию, гиперпролиферацию или стимулировать апоптоз (Медведев Л.Н., 1988; Меерсон Ф.З., Малышев И.Ю., 1993). Естественно, что переход клеток на новый уровень будет определяться потребностями организма и условиями среды, однако стратегию поведения каждая клетка выбирает в зависимости от наличия в ней энергетических и пластических ресурсов, специализации и, исходя из своего функционального состояния. Однако ведущий фактор, регулирующий переход клетки из одного состояния в другое, учитывающий одновременно и потребности многоклеточного организма как единого целого, и потребности отдельных элементов (клеток) этого целого, пока не определен. Поиску этого ведущего фактора – сквозной сигнальной системы многоуровневой регуляции пролиферации и ее ключевых параметров и посвящено настоящее исследование.
Все многоклеточные организмы в норме обладают уникальной системой иерархически организованных и взаимосвязанных механизмов регуляции размера клеточных популяций, обеспечивающихся балансом между рост-стимулирующими и рост-ингибирующими сигналами, позволяющими контролировать рост клеточной массы согласно потребностям организма. В условиях эмбрионального и постэмбрионального развития, адаптации к стресс-факторам и регенерации баланс между этими сигналами временно сдвигается в сторону рост-стимулирующих, а при онкогенной трансформации – их сдвиг становится практически необратимым. Но, так или иначе, и в нормальных, и в неопластических клетках стимуляция пролиферации происходит вследствие активации экспрессии генов, контролирующих клеточный цикл (Knowles M., Selby P., 2005), тонкие механизмы регуляции которого до конца не поняты.
Благодаря интенсивному развитию молекулярной биологии большие надежды на прогресс в раскрытии механизмов, контролирующих митотическую активность клеток, возлагаются на исследования структурных и функциональных свойств сигнальных молекул, являющихся компонентами сложных и разветвленных внутриклеточных сигнальных систем, регулирующих функциональное состояние клетки. Однако выяснилось, что одни и те же внеклеточные сигнальные молекулы и внутриклеточные мессенджерные системы стимулируют различные, часто противоположные, клеточные эффекты – от пролиферации до апоптоза (Gomperts B. et al., 2003). Доказательств множественности эффектов регуляторных молекул в научной литературе представлено достаточно много (Gomperts B. et al., 2003). Но до сих пор остается загадкой, каким образом клетки из такого большого количества возможных вариантов поведения сразу и практически безошибочно выбирают единственно верную стратегию, позволяющую им самим выживать и обеспечивать потребности целого организма.
Понимание механизмов регуляции функционального состояния клетки в парадигме только молекулярной биологии не может быть достигнуто, поскольку в молекулярно-биологических исследованиях игнорируется специфичность условий, в которых функционируют белки и нуклеиновые кислоты в условиях in vivo. Обычно все среды, используемые для клеточных культур или бесклеточных систем при изучении структуры и функций сигнальных молекул, стандартизованы. Однако в клетках и во внеклеточном матриксе в зависимости от физиологического состояния организма содержание катионов натрия, калия, кальция и протонов водорода может быть неодинаковым, вследствие чего конформация биополимеров в разных физиологических условиях будет отличаться. Установлено, что усиление гидратации белковой молекулы, зависящей от содержания катионов натрия в среде, вызывает удлинение молекулы, а ослабление гидратации ведет к сокращению ее длины (Lee B., Richards F.M., 1971).
Ионы являются важными факторами регуляции клеточного ответа на внешние сигналы, поскольку они: а) способны реагировать на все даже слабые внеклеточные стимулы изменением своих концентраций в цитозоле; б) имеют эффективные механизмы поддержания своего гомеостаза; в) обладают способностью быстро и обратимо изменять конформацию белковых молекул; г) находятся в центре регуляции основных метаболических путей (энергетических, информационных и метаболических). В то же время данные о роли этих катионов в регуляции пролиферации отрывочны (Болдырев А.А., 2008; Веренинов А.А. и др., 2004; Маленков А.Г., 2006; Медведев Л.Н., 1988; Меерсон Ф.З., Малышев И.Ю.,1993; Fillon S. et al, 2001; Lang F. et al, 2007; Vereninov A.A. et al, 2001; Yurinskaya V.E. et al, 2005) и не позволяют сложить полную картину их участия в регуляции ростовых процессов в популяциях нормальных и опухолевых клеток в организме. Нет и единой точки зрения на механизмы системной организации взаимодействия различных уровней регуляции пролиферации – клеточного, тканевого, органного и организменного, без понимания, которых трудно проследить причинно-следственную связь и, таким образом, понять этиологию заболевания. Все это затрудняет поиск новых более эффективных методов терапии, устраняющих причину пролиферативной патологии.
Естественным является предположение, что основные регуляторные системы надо искать среди сигнальных систем, пронизывающих все уровни регуляции пролиферации, в которых ведущая роль принадлежит поддержанию параметров гомеостаза организма в целом. Основной предпосылкой для поиска такой сигнальной системы стали исследования, показывающие зависимость митотической активности клетки от ее размеров. На основании анализа литературы (Анохин П.К., 1980; Меерсон Ф.З., Малышев И.Ю., 1993; Иванова Л.Н., 1996; Поляков В.Ю. и др., 2006; Yamamoto T., 1992; Pendergrass et al, 1994; Lang F et al, 1998; Rouzaire-Dubois B. et al., 2000; Rajasekaran S.A. et al., 2001; Kotova O. et al., 2006; Schoner W., Scheiner-Bobis G., 2007; Lang F. et al., 2007; Schelling I.R., Jawdeh B.G.A., 2008) нами была сформулирована рабочая гипотеза об ионных механизмах регуляции роста клеточных популяций в многоклеточном организме.
Основные экспериментальные факты, лежащие в основе гипотезы:
- Увеличение объема клеток до определенных величин стимулирует их пролиферацию в клеточных культурах (Lang F. et al., 1998; Rouzaire-Dubois B. et al., 2000; Levin M., 2007; Hibino T. et al., 2006; Adams D.S. et al., 2007 и др.).
- Объем клеток зависит от соотношения ионов во внутри- и внеклеточном пространстве (Liu R. et al., 2005; Okada Y., 2006 и др.).
- Гормоны и биологически активные вещества, регулирующие пролиферацию, изменяют объем клеток, модулируя работу ионных транспортеров (Graf J., Haussinger D., 1996; Lang F. et al., 1998; Kotova O. et al., 2006; Lang F., 2007 и др.).
Гипотеза о ведущей роли ионной регуляции роста клеточных популяций в многоклеточном организме
Регуляция роста клеточных популяций в многоклеточном организме осуществляется с помощью механизмов, контролирующих баланс ионов натрия, калия, кальция, хлора и протонов водорода во внутри- и внеклеточном пространстве. В регуляции роста клеточных популяций участвуют все иерархические уровни, способствующие поддержанию баланса ионов на уровне клетки, клеточной популяции, органа и организма в целом (Рис.1).
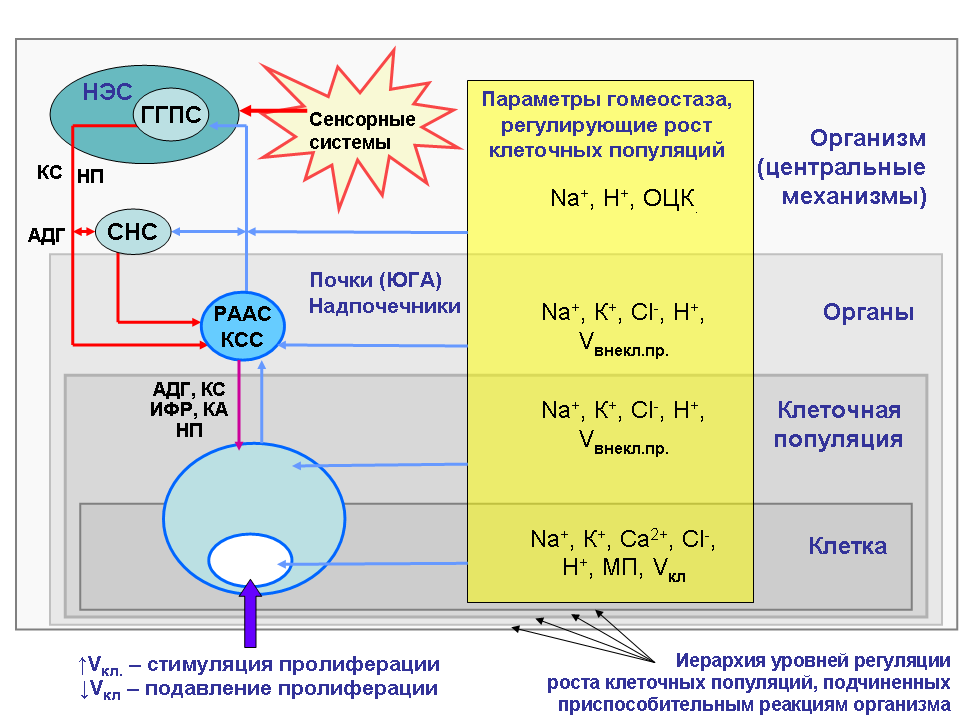
Рис.1. Механизм ионной регуляции роста клеточных популяций в условиях многоклеточного организма
НЭС – нейроэндокринная система, ГГПС – гипоталамо-гипофизарная система, СНС – симпатическая нервная система, РААС – ренин-ангиотензин- альдостероновая система, КСС – кортикостероидная система, ЮГА – юкстагломерулярный аппарат, КС – кардиотонические стероиды, НП – натрийуретические пептиды, АДГ – антидиуретический гормон, ИФР – инсулиноподобный фактор роста, КА – катехоламины, ОЦК – объем циркулирующей крови, МП – мембранный потенциал, V – объем клетки.
Замыкающим механизмом, определяющим удержание функционального состояния, обеспечивающего размер клеточных популяций вблизи генетически запрограммированного уровня, служат клеточные механизмы поддержания ионного гомеостаза – RVD и RVI. Генетически запрограммированные уровни ионного гомеостаза отвечают эволюционно отобранным и закрепленным стратегиям поведения клеточных популяций, обеспечивающим их приспособительную реакцию в составе целого организма.
Не изучено:
- участие отдельных ионов в регуляции объема клеток в условиях многоклеточного организма а, следовательно, и роста клеточных популяций;
- механизмы, с помощью которых организм может индуцировать переход ионного гомеостаза на уровень, обеспечивающий стимуляцию роста клеточных популяций;
- участие почек в создании в организме условий, способствующих росту клеточных популяций.
Цель исследования
Оценка роли ионного гомеостаза в регуляции роста популяций нормальных и опухолевых клеток в организме.
Задачи исследования
- Изучить особенности роста популяций опухолевых и нормальных клеток у животных в различных физиологических состояниях.
- Оценить роль энергетического статуса и физико-химических свойств мембран в регуляции роста популяций нормальных и опухолевых клеток карциномы Эрлиха.
- Сопоставить изменения баланса катионов кальция, натрия, калия и протонов водорода в популяциях опухолевых и нормальных клеток в условиях их роста и деградации и оценить роль этих ионов в регуляции ростовых процессов.
- Оценить способность экзогенных веществ, участвующих в регуляции ионного гомеостаза, модулировать скорость роста популяций нормальных и опухолевых клеток в организме и изучить механизм их действия.
- Изучить способность препаратов, снижающих содержание катионов натрия в клетках, подавлять онкогенез.
- Оценить роль почек в создании в организме условий, способствующих росту клеточных популяций под влиянием стресс-факторов и в условиях опухолевого роста.
- Разработать феноменологическую модель ионного гомеостаза как одного из ведущих механизмов регуляции роста клеточных популяций.
Научная новизна работы
В работе впервые:
- Установлено, что срочная адаптация к физическим (холод) и химическим (алкоголь) экстремальным факторам среды характеризуется подавлением активности Na,К-АТФазы в почках и головном мозге, а долговременная – двукратным повышением активности фермента.
- Выявлено, что стимуляция пролиферативных процессов в асцитных клетках карциномы Эрлиха при опухолевом росте и почках при адаптации к холоду сопровождается накоплением катионов натрия.
- Получены данные, свидетельствующие о том, что содержание катионов кальция в асцитных клетках и их чувствительность к одному из наиболее важных пара- и аутокринных регуляторов (экзогенному АТФ) зависит от фазы опухолевого роста и определяется уровнем активных форм кислорода.
- Получена динамика роста асцитной карциномы Эрлиха in vivo, которая отличается от описанных в литературе, временным подавлением роста опухоли, что является дополнением к существующим представлениям о динамике опухолевого роста.
- Выявлено трехкратное снижение содержания катионов кальция в ядрах опухолевых клеток легкого у больных раком легкого в фазу их повышенной митотической активности, что подтверждает важную роль ядерного кальция в регуляции экспрессии генов.
- Показано, что в условиях in vivo введение инсулина и уабаина увеличивают, а введение фуросемида, АТФ и 2,7% NaCl подавляют скорость роста асцитной карциномы Эрлиха. Установлено, что причиной противоопухолевого эффекта фуросемида в условиях in vivo является стимуляция процессов элиминации опухолевых клеток.
- Установлено, что высокочастотное ЭМП стимулирует эритропоэз, увеличивая в кровеносном русле долю молодых эритроцитов и ретикулоцитов, и повышает эффективность системы активного транспорта катионов кальция в миокарде.
- Выявлено, что у мышей с асцитной карциномой Эрлиха экскретируемая фракция воды и натрия снижена.
- Показано, что спиронолактон (антагонист альдостерона) уменьшает скорость роста асцитной карциномы Эрлиха.
- Предложена феноменологическая модель ионной регуляции роста клеточных популяций, в которой все регуляторные уровни увязаны в единую функциональную систему.
Положения, выносимые на защиту
- Адаптация животных к стресс-факторам стимулирует увеличение в тканях содержания катионов натрия, калия и воды. Опухолевые клетки обладают аномально высокой концентрацией катионов натрия, не характерной для нормальных клеток. Повышение содержания катионов натрия в нормальных и опухолевых клетках способствует увеличению их размеров и является необходимым условием активации в них митотических процессов.
- Пусковым сигналом, стимулирующим митотическую активность в нормальных и опухолевых клетках, является внутриклеточный кальций, содержание которого в момент стимуляции пролиферации возрастает в несколько раз. Концентрация свободного кальция в асцитных клетках и их чувствительность к АТФ определяется фазой роста карциномы Эрлиха и зависит от уровня активных форм кислорода.
- Скорость роста популяций нормальных и опухолевых клеток регулируется веществами, изменяющими размер клеток. Инсулин и уабаин увеличивают, а фуросемид, гипертонический NaCl и АТФ снижают рост популяций нормальных и опухолевых клеток, стимулируя в них процессы клеточной элиминации.
- Важным элементом регуляции роста клеточных популяций в условиях in vivo являются почки, которые путем снижения экскретируемой фракции натрия задерживают в организме катионы натрия, способствуя клеточному набуханию, являющемуся необходимым условием стимуляции процессов клеточного деления. Спиронолактон, подавляющий действие альдостерона, снижает скорость опухолевого роста.
- При пролиферативных патологиях часть клеточной популяции переходит в новое стационарное состояние, параметры ионного гомеостаза которого поддерживаются клетками новообразования и организмом вблизи новой константы. Восстановление параметров ионного гомеостаза до исходного уровня может способствовать подавлению опухолевого процесса.
Теоретическая и практическая значимость
Важность работы для фундаментальной науки и практической медицины обусловлена необходимостью понимания молекулярных механизмов адаптации организма к экстремальным факторам среды и причин трансформации нормальных клеток в онкогенные. Результаты исследования баланса катионов натрия, калия, кальция и функционирования ионных насосов в условиях роста популяций нормальных и опухолевых клеток способствуют определению роли ионного гомеостаза в процессах адаптации живых организмов к экстремальным факторам среды и в индукции онкогенеза.
Полученные результаты расширяют представление о механизмах взаимного влияния катионов натрия, калия, кальция, протонов водорода и АФК в организме при онкогенезе и адаптации к экстремальным условиям. Выявленные закономерности метаболических изменений в асцитных клетках при стимуляции и торможении роста опухоли создают основу для разработки методов оптимизации путей коррекции патологических состояний организма, вызванных развитием опухоли.
Исследование влияния АТФ на опухолевые клетки имеют практическую ценность в связи с его применением в медицинской практике в качестве фармакологического препарата, использующегося для подавления развития патологических процессов. Выявлено, что разнонаправленность эффектов АТФ может зависеть от функционального состояния клеток, определяющего скорость опухолевого роста, поскольку чувствительность асцитных клеток к АТФ зависит от его фазы.
Данные доказывают, что действие фармакологических препаратов, использующихся в клинической практике для повышения содержания катионов кальция в неопластических клетках, в зависимости от стадии роста опухоли могут вместо цитотоксического эффекта стимулировать развитие гиперпролиферации, обостряющей течение онкологического процесса.
Полученные результаты открывают перспективы, позволяющие разрабатывать способы подавления опухолевого роста веществами, снижающими размеры опухолевых клеток. Таким образом, эффективность противоопухолевой терапии может быть улучшена дополнением к традиционным способам лечения препаратов, способствующих снижению содержания внутриклеточного натрия в опухолевых клетках.
Результаты исследования могут найти применение в теоретической и экспериментальной физиологии, биохимии, патологической физиологии, клеточной биологии и фармакологии. Материалы диссертации используются при чтении курсов «Биохимия мембран», «Биохимические механизмы адаптации», «Биохимия мышечного сокращения», «Биоэнергетика» и «Биохимия тканей» студентам, обучающимся по специальности «Общая биохимия» на кафедре медицинской биологии СФУ. Методы, изложенные в диссертации, включены в разделы практикумов по биофизике и биохимии на кафедре физико-химической биологии и медицинской биологии Института фундаментальной биологии и биотехнологии СФУ, используются студентами при выполнении курсовых, дипломных, магистерских и диссертационных работ.
Апробация работы
Основные результаты доложены на международной конференции «Гомеостаз» в Красноярске (1997), 9-м Международном симпозиуме “Реконструкция гомеостаза” в Красноярске (1998), Российской конференции с международным участием «Организм и окружающая среда: жизнеобеспечение и защита человека в экстремальных условиях» в Москве (2000), XVIII физиологическом съезде им. И.П. Павлова в Казани (2001), Международной конференции «Рецепция и внутриклеточная сигнализация» в Пущино (2003, 2005, 2007, 2009), XIX физиологическом съезде им. И.П. Павлова в Екатеринбурге (2005), межрегиональной научно-практической конференции «Объединение субъектов Российской Федерации и проблемы природопользования в Приенисейской Сибири» в Красноярске (2005), 1 съезде физиологов СНГ в Дагомысе (2005), XX физиологическом съезде им. И.П. Павлова в Москве (2007), съезде биохимиков и молекулярных биологов в г. Новосибирске (2008), всероссийской конференции с международным участием «Молекулярная онкология» в Новосибирске (2008), научно-практической конференции в рамках Второй общегородской ассамблеи «Красноярск. Технологии будущего» (2009), на расширенном заседании кафедры медицинской биологии Института фундаментальной биологии и биотехнологии Сибирского федерального университета (2010).
Публикации
Основные положения диссертации опубликованы в 3 8 печатных работах, 14 из них – в журналах, рекомендованных ВАК.
Объем и структура диссертации
Диссертационная работа изложена на 328 страницах машинописного текста и состоит из списка сокращений, введения, аналитического обзора литературы, описания объектов и методов исследований, результатов собственных исследований, заключения, выводов, списка цитируемой литературы. Работа иллюстрирована 129 рисунками, 14 таблицами. В библиографический список включено 435 источника, из них 113 опубликовано в отечественной печати, а 325 – в зарубежной.
основные Объекты и методы исследования
В работе были использованы следующие реактивы: NaCl, KCl, CaCl2, MgCl2, KH2PO4, MgSO4, Na2HPO4, NaHCO3, глюкоза, глутамат, лаурилсульфат натрия, ЭДТА, хлорная кислота ацетат натрия, ТХУ, тиобарбитуровая кислота, феррицианид калия, NaOH (ч.д.а. «Реахим», Россия), ЭГТА, уабаин, дигитонин, HEPES, Fura-2/AM, ATP-Na2, Chelex, пирен, флуоресцеин-изотионат изомер 1, фиколл, коллагеназа, NaN3, Rhodamin-123 («Sigma», USA), флуоресцентные красители Hoechst 33342 и Propidium iodide (Molecular Probes, Eugene OR, USA); комплекс арабиногалактана с платиной (любезно предоставлен Старковым А.К. и Кагаем Б.Е. – Институт химии и химических технологий СО РАН), цисплатин («Ebewe», Австрия), стандартные наборы для определения общих липидов (Lachema), общего кальция (Кальций-Ново) и креатинина (Chemapol).
Объекты исследования
Эксперименты выполнены на крысах-самцах линии Вистар, белых аутбредных крысах-самцах и белых мышах-самцах линии ICR. Объектами исследования служили асцитные клетки карциномы Эрлиха, адипоциты бурой жировой ткани, клетки корковой и мозговой зон почек, кардиомиоциты, миоциты скелетной мускулатуры, фибробласты, нормальные и опухолевые клетки ткани легкого больных раком легкого. В качестве стресс-факторов были использованы ЭМП, холод, алкоголь, физическая нагрузка и гиподинамия.
В работе с больными соблюдались этические принципы, предъявляемые Хельсинской Декларацией Всемирной медицинской ассоциации (World Medical Association Declaration of Helsinki) (1964, 2000 ред.).
Все эксперименты с животными были выполнены в соответствии с этическими принципами и нормативными документами, рекомендованными Европейским научным фондом (ESF) и декларацией о гуманном отношении к животным.
Методы исследования биохимических параметров
Энергетическое состояние кардиомиоцитов и асцитных клеток оценивали методом 31Р-ЯМР-спектроскопии на жидкостном ЯМР–спектрометре Bruker Avance DPX 200. Приготовление экстрактов осуществляли по методике, описанной Бубновской Л.Н. (Бубновская Л.Н. и др., 2002.). Активность Са-АТФазы, экто-АТФазы, Na,К-АТФазы определяли по концентрации ортофосфата, образующегося в ходе гидролиза АТФ. Количественное определение ортофосфата проводили методом Ратбуна и Бетлах (Rathbun W.B. Betlach M.V., 1969). Белок определяли по методу Лоури (Lowry O.H. et al., 1951). Активность Са-насоса саркоплазматического ретикулума миокарда крыс оценивали помощью катионселективных электродов, сигналы от которых усиливались и поступали на аналого-цифровой преобразователь, откуда передавались на компьютер, где обрабатывались с помощью специальной программы. Скорость гидролиза АТФ определяли по нарастанию в среде протонов водорода, транспорт Са2+ через мембрану саркоплазматического ретикулума – по уменьшению активности катионов кальция в инкубационной среде. Содержание РНК и ДНК определяли по модифицированному методу Шмидта и Тангаузера с последующей спектрофотометрией (Трудолюбова М.Р., 1977). Перекисное окисление липидов в миокарде, головном мозге и крови оценивали по содержанию малонового диальдегида (Стальная И.Д., Гаришвили Т.Г., 1977), окислительную модификацию белка – по образованию битирозиновых сшивок (Дубинина Е.Е. и др., 2002). Восстановительный потенциал крови определяли потенциометрически по увеличению содержания протонов водорода, образующихся в среде после добавления образцов крови.
Методы исследования клеточных параметров
Митотический индекс оценивали микроскопически (Рогозин Е.А., 2003) на микроскопе Olympus. Апоптоз и некроз клеток определяли методом флуоресцентной микроскопии на микроскопе Olympus с помощью прижизненных красителей Hoechst 33342 и Propidium iodide. Скорость эндогенного дыхания исследуемых образцов определяли полярографически. Cобственную флуоресценцию NAD(P)H оценивали спектрофлуориметрически (Petty H. R., 2001). Определение микровязкости мембран клеток проводили спектрофлуориметрически с помощью гидрофобного зонда пирена на спектрофлуориметре Aminco Bowman Series 2, Thermo Spectronic (USA). Мембранный потенциал митохондрий определяли спектрофлуориметрически с помощью флуоресцентного зонда Rhodamin-123 (Vergun O. et al., 1999).
Методы исследования параметров ионного гомеостаза
Концентрацию внутриклеточного кальция определяли с помощью флуоресцентного зонда Fura-2AM на спектрофлуориметре Aminco Bowman Series 2, Thermo Spectronic (USA), и рассчитывали по формуле [Са2+]i = Ks (F-Fmin)/(Fmax-F), где F – интенсивность флуоресценции зонда в пробе (отн. ед.). Fmax – флуоресценция зонда насыщенного кальцием, измеренная после добавления в пробу 6 мкМ дигитонина. Fmin – собственная флуоресценция зонда, свободного от кальция, измеренная после добавления 5 мМ ЭГТА. Ks – коэффициент связывания зонда с Са2+ (135 нМ при 250С). Определение рН в клетках проводили с помощью флуоресцеина изотиоцианата изомера I (ФИ) на спектрофлуориметре Aminco Bowman Series 2, Thermo Spectronic USA (Gore M.G., 2000). Содержание катионов натрия и калия определяли методами пламенной фотометрии и атомно-абсорбционной спектроскопии.
Методы исследования физиологических параметров
Температуру ядра тела оценивали по величине ректальной температуры, измеренной с помощью электротермометра ТПЭМ-1. Функциональное состояние почек определяли по величине диуреза, скорости клубочковой фильтрации и реабсорбции натрия после 2% водной нагрузки.
Статистическая обработка результатов исследований
Статистическую обработку результатов проводили в программах Origin 5.0 и Statistica 7.0. Проверку гипотезы о статистической достоверности различий выборок проводили с помощью непараметрического критерия Манна-Уитни.
ОСНОВНЫЕ результаты исследования
Закономерности роста популяций нормальных и опухолевых клеток
Для выявления универсальных закономерностей, сопровождающих рост клеточных популяций в многоклеточном организме, нами были выбраны различные экспериментальные модели, для которых характерна повышенная митотическая активность клеток. Такими моделями стали популяции опухолевых клеток (асцитная карцинома Эрлиха, опухолевые клетки рака легкого человека, индуцированный онкогенез) и популяции нормальных клеток в состоянии эмбрионального и постэмбрионального развития, регенерации и адаптации к стресс-факторам.
Рост клеточных популяций в составе многоклеточного организма в норме всегда подчиняется принципам целесообразности и регулируется соотношением рост-ингибирующих и рост-активирующих факторов. Стимуляция роста популяций нормальных клеток происходит при регенерации, адаптации к стресс-факторам и в процессе индивидуального развития организма. В наших экспериментах адаптация к электромагнитному полю, холоду и физической нагрузке увеличивала массу сердца, печени, селезенки, головного мозга почек и межлопаточной бурой жировой ткани (Рис.2) путем стимуляции в них процессов пролиферации, о чем свидетельствовало повышение величины отношения ДНК/белок во всех исследованных тканях.
Особенности регуляции пролиферации опухолевых клеток изучали на асцитной карциноме Эрлиха. При подробном исследовании динамики увеличения опухолевой массы мы обнаружили, что кривая роста карциномы имела отличия от классической S-образной (Эмануэль Н.М., 1977; Варфоломеев С.Д., Гуревич К.Г., 1999). Отличительной особенностью кривой в наших экспериментах стало временное подавление опухолевого роста на 12-е сутки развития карциномы, сопровождающееся снижением митотической активности асцитных клеток (Рис.3).
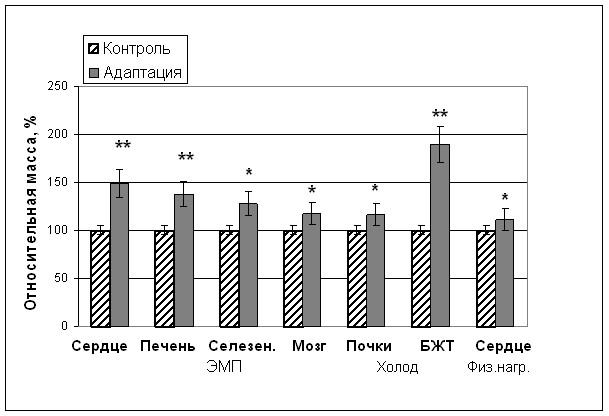
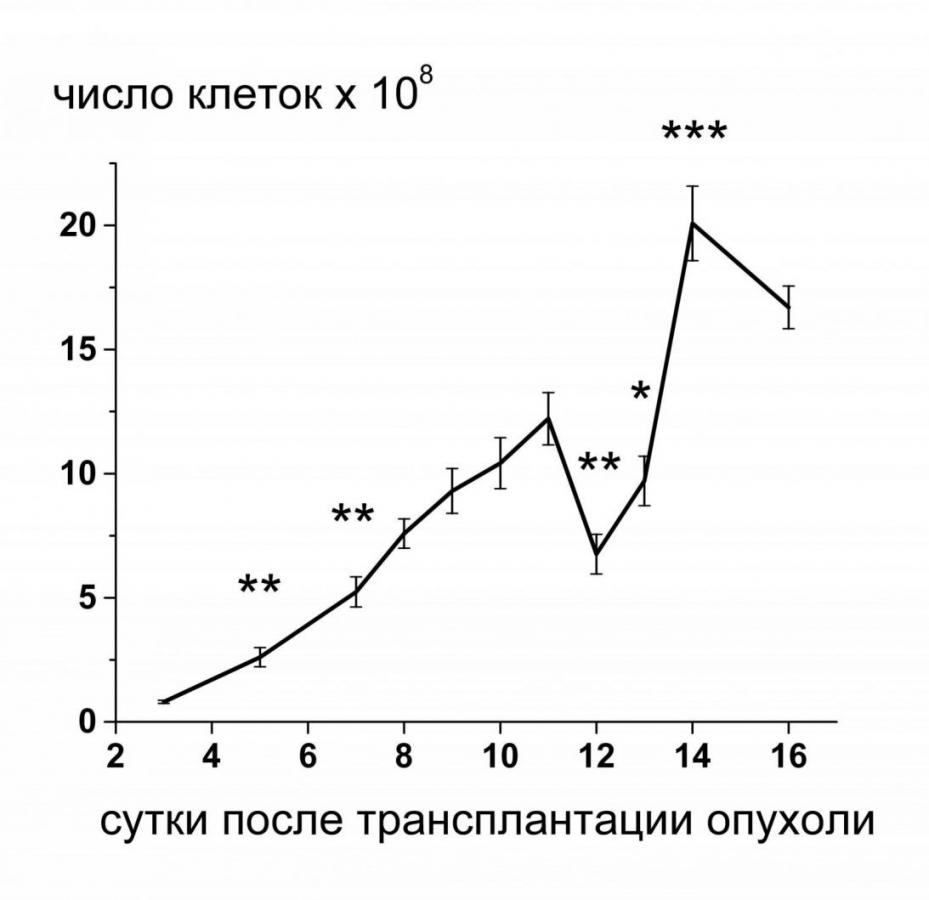
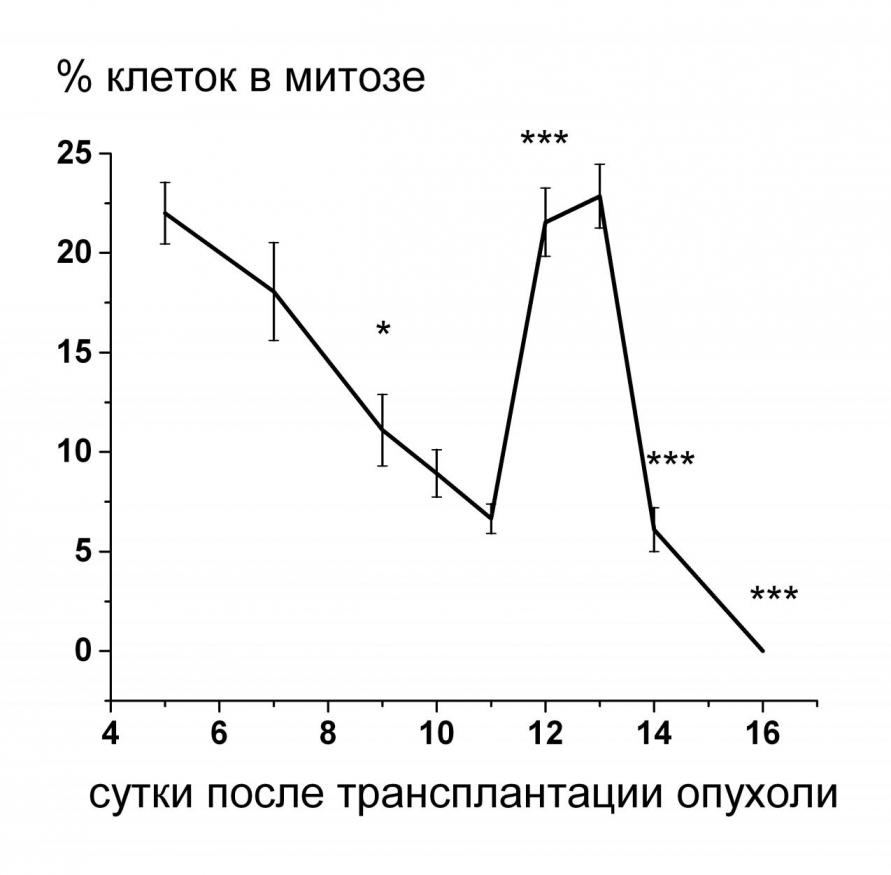
Рис.2. Изменение относительной массы отдельных органов при адаптации животных к ЭМП, холоду и физической нагрузке. Примечание (достоверность отличия от контроля): * – P<0,05; ** – P<0,01.
(а) (б)
Рис.3. Динамика роста асцитной карциномы Эрлиха (n=30 животных на точку) –(а); изменение величины митотического индекса в ходе роста АКЭ – (б). Примечание (достоверность отличия от предыдущей точки): * – P<0,05; ** – P<0,01; *** – P<0,001.
Исследование качественного состава опухолевой массы показало, что доля некротических клеток в опухоли на протяжении ее роста практически не менялась. До 10-ых суток было стабильным и количество клеток в состоянии апоптоза, но на 11-ые сутки количество апоптотических клеток резко увеличивалось (Рис.4).
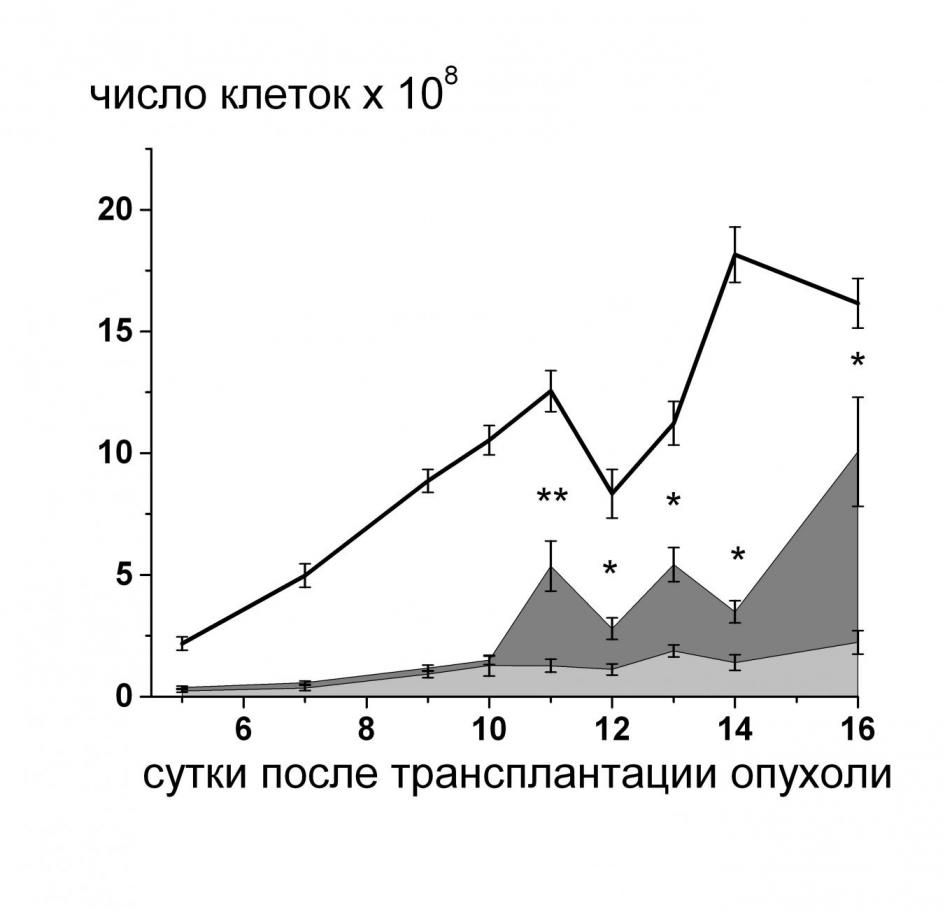
Рис.4. Изменение числа жизнеспособных, апоптотических и некротических клеток в ходе роста карциномы Эрлиха. Примечание (достоверность отличия от предыдущей точки): *– P<0,05;** – P<0,01.
– доля клеток находящихся в состоянии апоптоза;
– доля клеток находящихся в состоянии некроза.
Структурно-метаболические особенности популяций нормальных и опухолевых клеток в условиях их роста
Для выявления основных факторов, которые могли бы влиять на рост популяций нормальных и опухолевых клеток, изучали их энергетический статус и вязкость клеточных мембран.
Оценка энергетического статуса клеточных популяций
Энергетический статус клеток оценивали по скорости эндогенного дыхания, функциональному состоянию митохондрий и изменению отношения Pi/-NTP в клеточных популяциях нормальных и опухолевых клеток. Проведенные эксперименты показали, что скорость потребления кислорода клетками миокарда в условиях адаптации к электромагнитному излучению не изменялась, хотя мембранный потенциал митохондрий и содержание в них катионов кальция значительно возрастало, что свидетельствовало о повышении функциональной активности митохондрий. Такой вывод подтверждался и снижением отношения Pi/-NTP, измеренного с помощью 31ЯМР-спектроскопии.
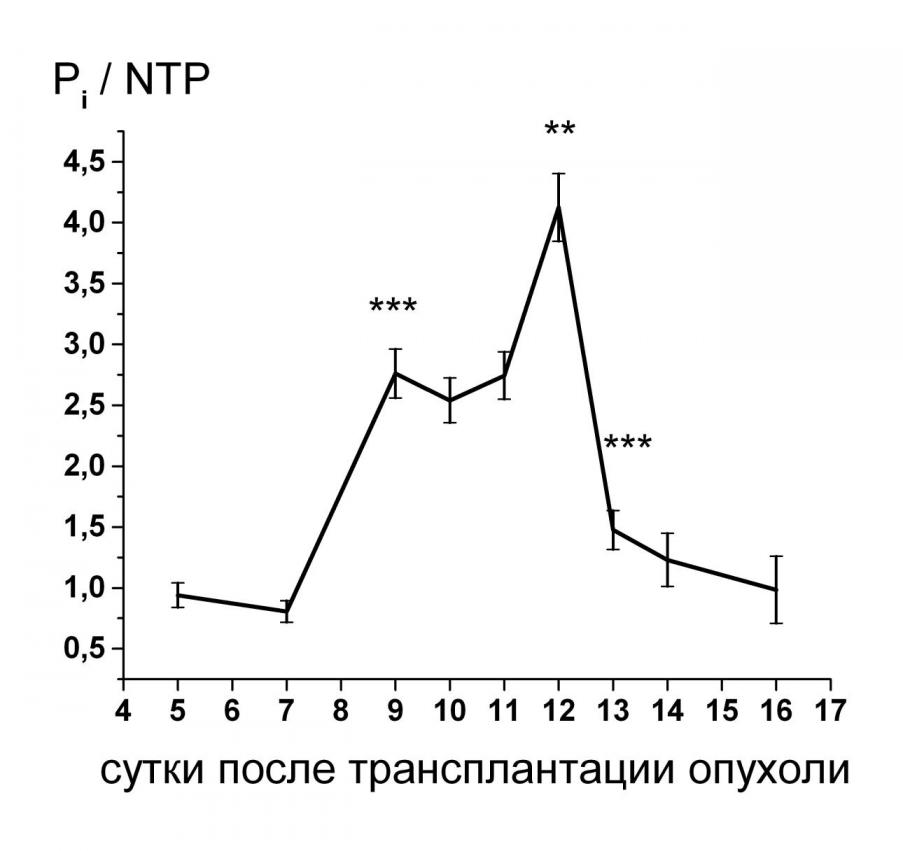
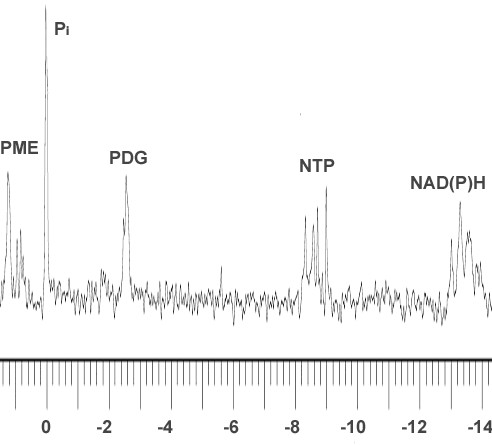
Определение скорости эндогенного дыхания в процессе роста карциномы Эрлиха показало, что потребление кислорода асцитными клетками на протяжении всего роста опухоли оставалось неизменным (в среднем около 2 мкмоль О2/мг белка/мин), хотя величина отношения Pi/-NTP претерпевала в процессе роста значительные колебания (Рис.5). Таким образом, результаты исследований не выявили четкой зависимости между энергетическим статусом клеток и ростом клеточных популяций.
а б
Рис.5. Типичный 31ЯМР-спектр экстракта асцитных клеток (а) и изменение Pi/-NTP (б) в асцитных клетках в процессе роста карциномы Эрлиха. Примечание (достоверность отличия от предыдущей точки): ** – P<0,01; *** – P<0,001.
Оценка вязкости клеточных мембран
В регуляции функциональной активности клеток важную роль играют структурные характеристики клеточных мембран, поскольку они определяют активность мембранно-связанных ферментов, каналов и рецепторного аппарата. При переходе клеток из состояния покоя в митотический цикл происходит дисагрегация внутримембранных частиц, повышается текучесть липидного бислоя, в целом мембрана становится менее стабильной (Епифанова О.И., 2003). Поэтому предполагается, что физико-химические свойства клеточных мембран являются прогностическими для оценки роста клеточных популяций нормальных и опухолевых клеток. Полагают, что основные свойства опухолей (неограниченная пролиферация, анаплазия, метастазирование, способность к инвазивному росту) являются результатом изменений поверхности опухолевых клеток, связанных с нарушением физико-химических свойств плазматической мембраны.
В наших исследованиях стимуляция митотической активности в популяциях нормальных клеток сопровождалась разнонаправленными изменениями микровязкости клеточных мембран (Табл.1). В популяции опухолевых клеток в разные фазы роста карциномы Эрлиха, характеризующиеся как стимуляцией, так и подавлением митотической активности, значимых изменений микровязкости клеточных мембран также не обнаружено.
Таблица 1. Изменение коэффициента эксимеризации пирена в некоторых органах и тканях крыс при адаптации к стресс-факторам, регенерации ожоговой раны и в процессе эмбрионального и постэмбрионального развития
| Группа крыс | Белок/липидная зона, Jэ/Jм | Липидный бислой, Jэ/Jм |
| Адаптация к ЭМП | ||
| Лимфоциты | ||
| Контроль (n=10) | 2,119±0,300 | 2,350±0,341 |
| Опыт (n=10) | 1,128±0,223** | 1,201±0,235** |
| Эритроциты | ||
| Контроль (n=10) | 0,039±0,004 | 0,035±0,005 |
| Опыт (n=10) | 0,057±0,006* | 0,036±0,005 |
| СР миокарда | ||
| Контроль (n=11) | 0,097±0,009 | 0,083±0,007 |
| Опыт (n=12) | 0,080±0,007* | 0,100±0,009* |
| Адаптация к гиподинамии | ||
| Миокард | ||
| Контроль (n=11) | 0,231±0,025 | 0,081±0,009 |
| Опыт (n=12) | 0,260±0,032 | 0,086±0,008 |
| Адаптация к гиподинамии | ||
| Скелетная мускулатура | ||
| Контроль (n=11) | 0,157±0,020 | 0,06±0,008 |
| Опыт (n=12) | 0,240±0,030* | 0,08±0,009* |
| Адаптация к холоду | ||
| Почки | ||
| Контроль (n=11) | 0,65±0,090 | 0,33±0,043 |
| 1 час (n=9) | 0,05±0,009* | 0,25±0,034 |
| 3 часа (n=10) | 0,05±0,006* | 0,05±0,005** |
| 4 недели (n=12) | 0,4±0,050* | 0,25±0,039 |
| Онтогенез | ||
| Почки | ||
| Эмбрионы (n=15) | 0,074±0,009 | 0,040±0,003 |
| Новорожденные (n=11) | 0,049±0,006* | 0,023±0,001* |
| 4 недели (n=10) | 0,065±0,009 | 0,031±0,002* |
Примечание (достоверность отличия от контроля): * – P<0,05;*** – P<0,01.
В целом совокупность полученных результатов показала отсутствие однозначной зависимости между энергетическим статусом, вязкостью плазматической мембраны и ростом популяций нормальных и опухолевых клеток.
Особенности ионного гомеостаза в популяциях нормальных и опухолевых клеток в условиях стимуляции пролиферативных процессов
Роль катионов кальция в регуляции роста популяций нормальных и опухолевых клеток
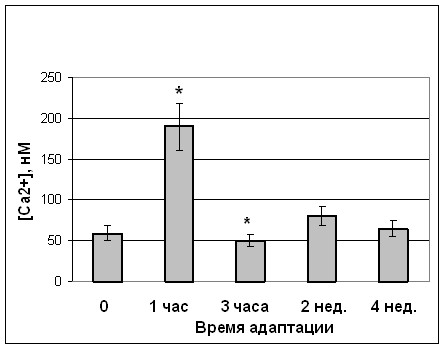
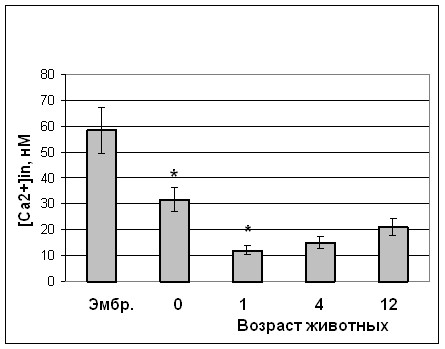
Наиболее важным мессенджером, регулирующим процессы пролиферации, дифференцировки и апоптоза в нормальных и опухолевых клетках, считается внутриклеточный кальций (Whitaker M., 2001; Azhar M., 2001), уровень которого всегда изменяется под влиянием внешних сигналов (Berridge M.J. et al., 2003). При исследовании роли кальция в регуляции роста клеточных популяций при адаптации к холоду нами обнаружено почти четырехкратное его увеличение практически сразу после воздействия низкой температуры. При продолжении действия стресс-фактора содержание свободного кальция в клетках падало до уровня контроля и лишь незначительно колебалось на протяжении всей адаптации (Рис.6). Уровень катионов кальция в клетках почек в условиях эмбрионального и постэмбрионального развития был повышенным у эмбрионов и новорожденных, а в условиях дальнейшего постэмбрионального развития снижался (Рис.6).
а б
Рис.6. Изменение содержания свободного кальция в клетках почек при адаптации к холоду (а) и в процессе онтогенеза (б). Примечание (достоверность отличия от контроля):* – P<0,05.
Регенерация вызывала повышение концентрации Са2+ в фибробластах только в период индукции пролиферации (Рис.7). Адаптация к физической нагрузке и гиподинамии также увеличивала уровень Са2+ (Рис.8), однако при физической нагрузке наблюдалось многократное повышение, тогда как при гиподинамии это повышение составляло только 25%.
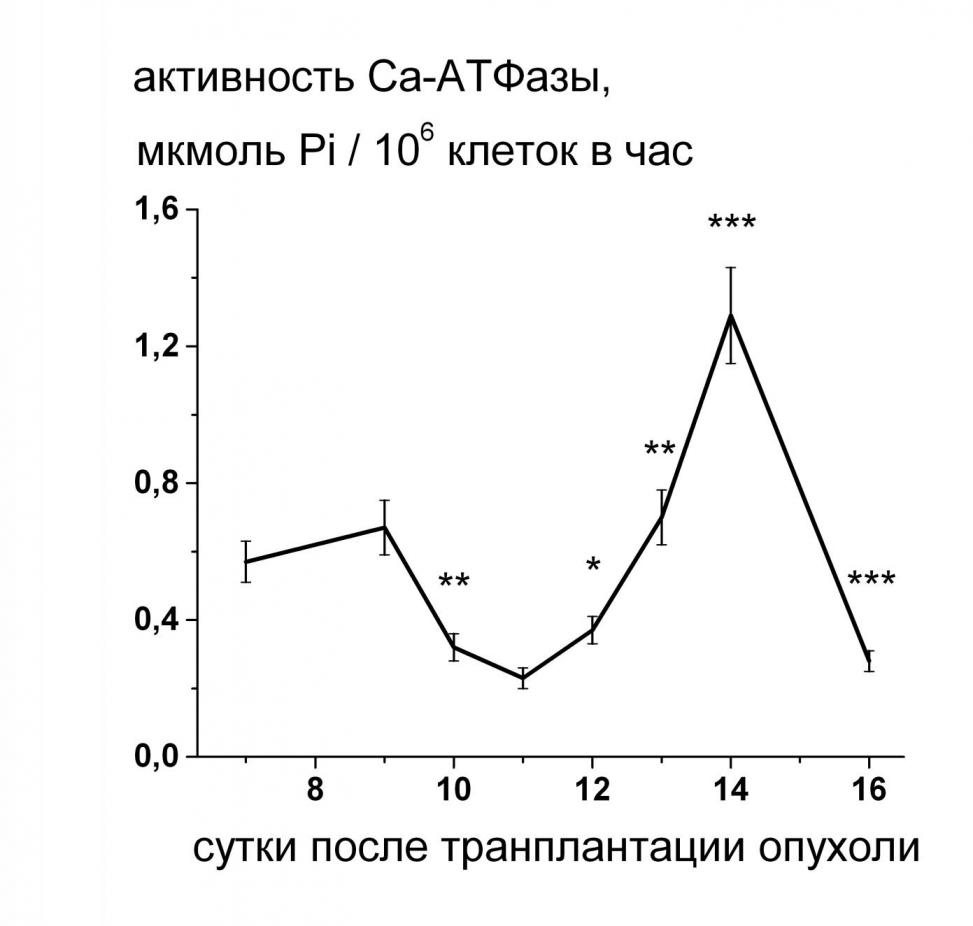
Рост содержания катионов кальция в клетках, выявленный нами при воздействии стресс-факторов, вызывал компенсаторное увеличение активности Са-АТФазы (Рис.9), которая, вероятно и являлась основным фактором восстановления гомеостаза катионов кальция в условиях продолжающегося воздействия стресс-факторов.
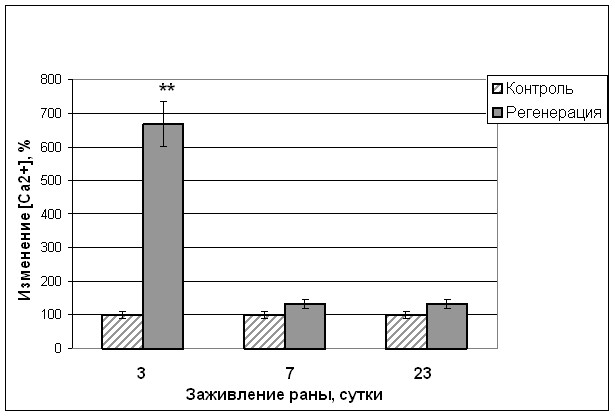
Рис.7. Изменение концентрации свободного кальция в фибробластах при регенерации в процессе заживлении ожоговой раны. Примечание (достоверность отличия от контроля): ** – P<0,01.
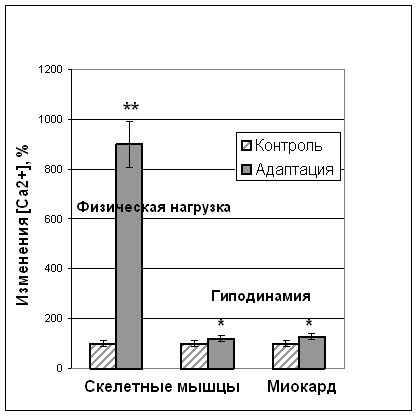
Рис.8. Изменение содержания свободного кальция в миокарде и скелетной мускулатуре при адаптации крыс к физической нагрузке и гиподинамии. Примечание (достоверность отличия от контроля):* – P<0,05; ** – P<0,01.
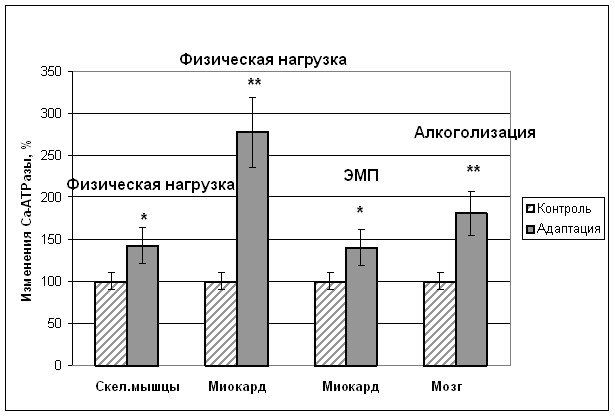
Рис.9. Изменение активности Са-АТФазы в скелетной мускулатуре, миокарде и головном мозге при адаптации животных к физической нагрузке, ЭМП и хронической алкогольной интоксикации.
В асцитных клетках концентрация катионов кальция в процессе роста карциномы Эрлиха претерпевала значительные колебания и имела два пика повышения (Рис.10). Первый пик приходился на фазу, характеризующуюся индукцией апоптотических процессов в опухоли, а второй наблюдался в фазу стимуляции пролиферации после временного подавления роста опухоли. Причем изменение концентрации катионов кальция, сопровождающееся ростом опухоли, соответствовала такой степени изменений, которая стимулировала пролиферацию нормальных клеток при адаптации. Таким образом, результаты исследований позволили предположить, что как подавление роста клеточных популяций, так и его стимуляция могут регулироваться катионами кальция, однако амплитуда изменений уровня катионов кальция в индукции различных функциональных состояний неодинакова. При исследовании изменений активности Са-АТФазы в процессе роста карциномы Эрлиха мы установили, что стимуляция фермента происходила через двое суток после повышения концентрации внутриклеточного кальция (Рис.10).
При изучении внутриклеточного баланса катионов кальция у больных мелкоклеточным раком легкого было обнаружено двукратное увеличение содержания свободного кальция в цитозоле опухолевых клеток, сопровождающееся трехкратным снижением его в ядрах (Табл.2), что подтверждает предположение о важной роли ядерного кальция в регуляции экспрессии генов (Андрющенко П.И., Зоценко Д.М., 2003; Поляков В.Ю. и др., 2006).