Выявление психоэмоциональных расстройств у больных острым инфарктом миокарда, их влияние на течение острого инфаркта миокарда и коррекция
На правах рукописи
Беневская Мария Александровна
ВЫЯВЛЕНИЕ ПСИХОЭМОЦИОНАЛЬНЫХ РАССТРОЙСТВ У БОЛЬНЫХ ОСТРЫМ ИНФАРКТОМ МИОКАРДА, ИХ ВЛИЯНИЕ НА ТЕЧЕНИЕ ОСТРОГО ИНФАРКТА МИОКАРДА И КОРРЕКЦИЯ
14.01.05 – КАРДИОЛОГИЯ
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
МОСКВА – 2011
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Российский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель:
Заслуженный деятель науки
Российской Федерации,
доктор медицинских наук, профессор Люсов Виктор Алексеевич
Официальные оппоненты:
доктор медицинских наук, профессор Глезер Мария Генриховна
доктор медицинских наук, профессор Орлов Владимир Аркадьевич
Ведущая организация: Московский государственный медико-стоматологический университет
Защита диссертации состоится «14» февраля 2011 г. в 14.00 часов на заседании диссертационного совета Д 208.072.08 при ГОУ ВПО РГМУ по адресу: 117997, Москва, ул. Островитянова, д.1.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ Росздрава по адресу: 117997, Москва, ул. Островитянова, д.1
Автореферат разослан « 12 » января 2011 г
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор А.К.Рылова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
В России за последние 5 лет сердечнососудистая заболеваемость возросла почти на 20% и достигает 15 млн. человек, что существенно превышает аналогичный показатель в большинстве развитых странах мира.
Общая заболеваемость ишемической болезнью сердца (ИБС) составляет 4890,1 на 100.000 человек, острым инфарктом миокарда (ОИМ) 144,3 на 100.000 человек.
Высокие показатели заболеваемости и летальности обуславливают актуальность дальнейшего изучения факторов, влияющих на развитие, течение и возникновение осложнений инфаркта миокарда.
Сопутствующие ОИМ психоэмоциональные расстройства оказывают негативное влияние на клиническое течение постинфарктного периода, функциональное состояние сердечнососудистой системы и качество жизни пациентов.
В связи с этим в последние годы большой интерес специалистов вызывает проблема коморбидности этих заболеваний.
Данные эпидемиологического исследования на основе программы ВОЗ «MONICA» показали, что риск развития инфаркта миокарда связан с депрессией. Установлено, что депрессия является прогностическим фактором увеличивающим риск кардиальной смертности в период от 6 до 18 месяцев после ОИМ.
Установлено, что при заболеваниях сердечнососудистой системы чаще всего отмечаются психогенные невротические реакции на сам факт соматического страдания, а также неврозоподобные расстройства преимущественно в виде астенических, тревожных и депрессивных состояний. Показано их отчетливое негативное влияние на клиническое течение и прогноз кардиальной патологии, совокупное качество жизни больных, приверженность к лечению и выполнению врачебных рекомендаций. Все это диктует необходимость своевременного выявления и адекватного лечения психоэмоциональных расстройств у больных сердечнососудистыми заболеваниями (ССЗ).
В настоящее время психоэмоциональные расстройства рассматриваются в качестве общемедицинской, а не сугубо психиатрической проблемы. Проявления этих расстройств, такие как снижение тонуса, общей активности, нарушения сна, сердцебиения и др., очень тесно переплетаются с клиническими симптомами ССЗ. Поэтому больные с типичными проявлениями психопатологических расстройств обращаются, прежде всего, к участковым врачам, кардиологам, врачам общей практики.
Опираясь на вышеизложенное, представляется целесообразным углубленное изучение вопросов выявления и коррекции психоэмоциональных нарушений у больных острым инфарктом миокарда, разработка алгоритма диагностики и лечения этой категории больных.
Цель исследования
Изучение влияния психоэмоциональных нарушений и их терапевтической коррекции на клиническое течение острого инфаркта миокарда.
Задачи исследования
- Определить влияние психоэмоциональных расстройств на клиническое течение инфаркта миокарда.
- Исследовать взаимосвязь психоэмоциональных нарушений и локализации инфаркта миокарда.
- Изучить взаимосвязь между психоэмоциональным и вегетативным статусом больных острым инфарктом миокарда.
- Выявить психоэмоциональные расстройства у больных острым инфарктом миокарда с помощью метода фрактального анализа голоса пациента.
- Проанализировать влияние терапии афобазолом на психоэмоциональный, вегетативный и соматический статус больных инфарктом миокарда с сопутствующими психоэмоциональными расстройствами.
Научная новизна
В работе установлено, что у больных острым инфарктом миокарда клинические проявления инфаркта миокарда, состояние вегетативной регуляции сердечного ритма зависят от их психоэмоционального статуса. Показано, что психоэмоциональные расстройства утяжеляют проявления инфаркта миокарда, снижают толерантность к физической нагрузке, снижают вариабельность ритма сердца, способствуя тем самым возникновению сердечнососудистых осложнений. Показана возможность использования фрактального анализа голоса для диагностики психоэмоциональных расстройств у больных острым инфарктом миокарда и контроля лечения психотропными препаратами.
Определено, что у больных острым инфарктом миокарда и сопутствующим психоэмоциональными нарушениями добавление анксиолитика - афобазола к стандартной терапии улучшает не только психоэмоциональное состояние, но и их соматический статус. Выявлено положительное действие афобазола на вегетативную регуляцию сердечнососудистой системы, проявляющееся уменьшением вегетативного дисбаланса.
Практическая значимость работы
Установлено, что психоэмоциональные расстройства у больных острым инфарктом миокарда отрицательно влияют на клинические проявления инфаркта миокарда, ухудшают самочувствие пациентов. В соответствии с этим, обоснованна необходимость проведения оценки психосоматического статуса пациентов острым инфарктом миокарда в целях своевременного распознавания и лечения психоэмоциональных расстройств.
Полученные в работе данные позволяют рекомендовать новый метод фрактального анализа голоса у больных острым инфарктом миокарда для выявления психоэмоциональных расстройств.
Внедрение результатов работы в практику
Основные положения диссертационной работы внедрены и используются в работе 2 и 6 отделений неотложной кардиологии с блоком кардиореанимации ГКБ №15 им. О.М.Филатова г. Москвы, а также в учебном процессе на кафедре Госпитальной терапии №1 лечебного факультета ГОУ ВПО Российского государственного медицинского университета МЗ РФ.
Апробация работы
Апробация работы состоялась 31 августа 2010 года на совместном заседании кафедры Госпитальной терапии №1 лечебного факультета ГОУ ВПО РГМУ МЗ РФ и сотрудников отделений 2, 6, 20, 21, 22, 23 ГКБ №15 им. О.М.Филатова г. Москвы.
Структура и объем диссертации
Диссертационная работа изложена на 115 страницах и состоит из 5 глав: введения, обзор литературы, материал и методы исследования, обсуждения полученных результатов, выводов, практических рекомендаций и списка литературы. Работа содержит 44 таблицы, 20 рисунков, 4 клинических примера. Библиографический список включает в себя 55 отечественных и 87 иностранных источников.
Характеристика больных и методы исследования
В настоящее исследование был включен 71 больной острым инфарктом миокарда, поступивший в блок интенсивной терапии (51 мужчина и 20 женщин). Возраст больных варьировал от 37 до 75 лет, средний возраст составил 58,3+ 2,7 года.
Все больные находились на лечении во 2-м кардиологическом отделении с блоком интенсивной терапии 15 ГКБ им. О.М. Филатова, где располагается клиническая база кафедры Госпитальной терапии № 1л/ф ГОУ ВПО РГМУ.
В исследование включали больных, госпитализированных в период с сентября 2007 по январь 2010 года в связи с острым инфарктом миокарда, у которых отсутствовали противопоказания по соматическому состоянию для назначения анксиолитиков и согласившиеся на участие в исследовании. Диагноз острого инфаркта миокарда был установлен на основании анамнеза заболевания, клинической картины, ферментодиагностики, электрокардиографии, в соответствии с рекомендациями ВНОК (2004 г).
В исследование были включены пациенты, у которых ИБС манифестировала ОИМ, допускалось наличие стенокардии в течение месяца до развития инфаркта миокарда.
Распределение больных по полу и возрасту представлено в табл. 1.
Таблица 1
Распределение исследованных больных по полу и возрасту
| возраст пол | 31-40 | 41-50 | 51-60 | 61-70 | 71-80 | всего |
| Мужчины | 3 | 15 | 17 | 14 | 2 | 51 |
| Женщины | - | 2 | 5 | 7 | 6 | 20 |
| Итого | 3 | 17 | 22 | 21 | 8 | 71 |
В исследование не включались пациенты, у которых по результатам тестирования с помощью шкал депрессии и тревоги выявлялись психоэмоциональные нарушения тяжелой степени, требовавшие наблюдения психиатром, а также имевшие в анамнезе психоэмоциональные расстройства, по поводу которых было необходимо лечение психиатром.
Инфаркт миокарда передней локализации наблюдался у 43 больных, нижний – у 23 больных, циркулярный – у 5 больных.
Таблица 2
Локализация инфаркта миокарда у исследованных больных по данным электрокардиографии
| Локализация ИМ | Группа 1А (n=29) | Группа 1Б (n=20) | Группа 2 (n=22) | |||
| асб. | % | абс. | % | абс. | % | |
| Передний | 17 | 58.6 | 14 | 70 | 12 | 54.5 |
| Нижний | 10 | 34.5 | 5 | 25 | 8 | 36.4 |
| Циркулярный | 2 | 6.9 | 1 | 5 | 2 | 9.1 |
| Всего: | 29 | 100,0 | 20 | 100,0 | 22 | 100,0 |
По анамнестическим данным стенокардия в течение месяца, предшествовавшая развитию ОИМ – 22 человека, артериальная гипертензия отмечалась у 67 больных, гиперхолестеринемия – у 30 больных, сахарный диабет II типа – у 4 больных. Из других сопутствующих заболеваний наиболее часто встречались язвенная болезнь двенадцатиперстной кишки – у 7 больных, ожирение II-III степени (ИМТ>30) – у 15 больных, хронический бронхит – у 5 больных, остеохондроз позвоночника – у 9 больных. Курение – 41 человек. По частоте встречаемости сопутствующих заболеваний, таких как артериальная гипертензия (93,8% в 1-й группе, 95,5% во 2-й группе), гиперхолестеринемия (44,9% и 36,4% соответственно), сахарный диабет II типа (6,1 % и 4,5% соответственно), ожирение II-III ст. (20,4% и 22,7% соответственно), группы достоверно не различались, р>0,05.
Всем больным проводилась стандартная терапия аспирином, антикоагулянтами, -блокаторами, ингибиторами АПФ, гиполипидемическими препаратами. Нитраты перорально были назначены 17 больным, антагонисты кальциевых каналов – 6 больным.
29 больным был проведен системный тромболизис тканевым активатором плазминогена (актилизе, Boehringer Ingelheim, Германия). 22 больным проведена экстренная коронароангиография с эндоваскулярным вмешательством. 43 пациентам была выполнена отсроченная коронароангиография с последующим эндоваскулярным вмешательством. После подписания информированного согласия, проведения тестирования с помощью специализированных шкал депрессии и тревоги, фрактального анализа голоса, пациенты были распределены на 2 группы.
1 группа – больные ОИМ с сопутствующими психоэмоциональными расстройствами состояла из 1А группы, которым проводилась корректирующая терапия афобазолом (n = 29), средний возраст составил 55,3 + 2,6 лет; и 1Б группа - которым не проводилась корректирующая терапия афобазолом (n = 20). Средний возраст составил 58,7 ±3,9 лет.
2 группа - без сопутствующих психоэмоциональных расстройств (группа сравнения) (n = 22). Средний возраст составил 52,6 + 2,4 года.
При разделении пациентов на группы учитывалось наличие или отсутствие у больных психоэмоциональных расстройств, а также согласие на проведение корректирующей терапии.
Методы исследования.
При включении в исследование, на 2-е сутки пребывания в стационаре, учитывались жалобы пациента, далее следовал сбор анамнеза, физикальный осмотр. Последующая оценка клинического состояния больных проводилась через 10-14 дней и 3 месяца.
Электрокардиографическое исследование выполняли по стандартной методике с записью показателей в 12-ти стандартных отведениях (электрокардиограф фирмы «Shiller», Швейцария). Электрокардиограмму снимали на 2-е сутки пребывания больного в стационаре, через 10-14 дней и 3 месяца. Анализ ЭКГ проводили по стандартной методике рекомендованной экспертами ВОЗ.
Суточное мониторирование ЭКГ проводили с использованием холтеровских мониторов и компьютерной программы, разработанной фирмой Shiller (Швейцария). Исследование проведено всем больным на 2-14 сутки госпитализации и через 3 месяца. Длительность непрерывной записи составляла 24 часа. Регистрация проводилась по отведениям V5m и IIIm. Для оценки вариабельности ритма сердца использовались временные показатели:
- SDNN (мс) — стандартное отклонение R–R-интервалов. Характеризует состояние механизмов регуляции; указывает на суммарный эффект влияния на синусовый узел симпатического и парасимпатического отделов автономной нервной системы.
- RMSSD (мс) — квадратный корень из среднего значения квадратов разностей величин последовательных интервалов R–R. Показатель активности парасимпатического звена вегетативной регуляции.
- pNN50 (%) — процент последовательных интервалов R–R, различие между которыми превышает 50 мс. Также демонстрирует активность парасимпатической нервной системы.
Критериями ишемии миокарда считали преходящее снижение сегмента ST горизонтального или косонисходящего характера на 100 мкВ и более от исходного уровня. Характер снижения сегмента ST определяли по двум точкам, расположенным относительно друг друга по оси ординат: 1-я находилась на расстоянии 60 мсек от точки J, 2-я – на расстоянии 80 мсек от точки J. В случае исходного подъема сегмента ST отсчет производили от количественных значений функциональной пробы. Также анализировали число желудочковых и наджелудочковых экстрасистол, наличие прочих нарушений ритма.
Эхокардиографическое исследование проводили по общепринятой методике (Мухарлямов Н.М., Беленков Ю.Н., 1981) на аппарате «Logic-400» (General electric, США). Трансторакальное ЭХО-КГ исследование выполнялось всем больным на 2-14 сутки госпитализации и через 3 месяца. Определялись конечно-диастолический (КДР) и конечно-систолический (КСР) размеры левого желудочка (ЛЖ), толщина межжелудочковой перегородки (ТМЖП) и задней стенки (ТЗС) в конце диастолы. Методом дисков (модифицированный алгоритм Simpson) определялась фракция выброса ЛЖ. Нарушение локальной кинетики левого желудочка оценивались по Gibson R.S. et al.
Тредмил-тест проводился всем пациентам (при отсутствии абсолютных противопоказаний) на 10-14 сутки госпитализации и через 3 месяца. Тест с дозированной физической нагрузкой, лимитированный по появлению симптомов и/или признаков ишемии, выполнялся на оборудовании Cardio Control Workstation (Голландия) по протоколу модифицированный R.Bruce. Проба считалась положительной при возникновении типичного приступа стенокардии, при котором больной обычно останавливался или принимал нитроглицерин, и сопровождающегося горизонтальным или косонисходящим снижением сегмента ST на 1 мм в точке J + 80мсек, по крайней мере, в одном отведении, что и являлось критерием остановки пробы. При отсутствии клинических и ЭКГ признаков ишемии миокарда тест прекращался по достижение больным субмаксимальной частоты сердечных сокращений (ЧСС).
Изучение психического статуса выполнялось на 2-е сутки пребывания в стационаре и через 3 месяца. Больные заполняли Госпитальный опросник депрессии и тревоги HADS. При интерпретации данных учитывается суммарный показатель по каждой подшкале, при этом выделяются 3 области значений: 0-7 баллов – норма; 8-10 баллов - субклинически выраженная тревога/депрессия; 11 баллов и выше - клинически выраженная тревога/депрессия. Также больные заполняли опросник депрессии Бека (Beck Depression Inventory). При интерпретации данных учитывался суммарный балл по всем категориям: 0-9 – отсутствие депрессивных симптомов; 10-15 – легкая депрессия (субдепрессия), 16-19 – умеренная депрессия; 20-29 – выраженная депрессия (средней тяжести); 30-63 – тяжелая депрессия.
На основании данных полученных в ходе заполнения HADS и BDI больные дифференцировались на группы: страдающих психоэмоциональными расстройствами (легкой и средней степени выраженности) и без указанных психоэмоциональных расстройств (группа сравнения).
Оценка голоса с помощью метода фрактального анализа выполнялась на 2-е сутки госпитализации и через 3 месяца. Программное обеспечение для анализа речевых сигналов разной эмоциональной окрашенности позволяет рассчитывать спектральные характеристики речи: пиковые частоты (форманты, обертоны), спектральную плотность энергии, а также строить шумовую аппроксиманту спектра для получения фрактальной размерности речевого сигнала. Нейтральное, спокойное состояния принято за 100% (контрольная группа). При наличии эмоции «горе» фрактальная размерность речевого сигнала снижается. При состоянии радости и эмоции гнева имеет место повышение фрактальной размерности.
Лабораторное обследование выполнялось по стандартным методикам в условиях клинико-диагностической лаборатории стационара.
Методика лечения: Пациентам 1А группы проводилась комбинированная терапия: стандартная терапия, включавшая -блокаторы, ингибиторы АПФ, аспирин, статины, антикоагулянты в дозировках, согласно национальным клиническим рекомендациям Всероссийского научного общества кардиологов, а также терапия афобазолом. Афобазол назначался перорально в течение 4-х недель по 5 мг 3 раза в день, после еды.
Пациентам 1Б группы и пациентам 2-ой группы проводилась только стандартная терапия, описанная выше.
Методы статистического анализа. Статистическую обработку полученных данных проводили на IВМ РС Pentium, используя статистическую графическую систему Quattro. Применялись стандартные методы вариационной статистики с определением достоверности различий по критерию Стьюдента, где значение p<0,05 считалось достоверным. Все данные, полученные в ходе обследования 71 больного острым инфарктом миокарда с сопутствующими психоэмоциональными расстройствами и без них, были внесены в базу данных Statistica версии 6.0. Статистический анализ данных осуществлялся с использованием пакета программ Statistica 6.0 производства StatSoft, (США).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Для решения поставленной задачи все больные на основании результатов тестирования с помощью шкал депрессии и тревоги HADS и опросника депрессии Бека были распределены на группы с наличием и отсутствием психоэмоциональных нарушений.
1 группа, представленная больными ОИМ с сопутствующими психоэмоциональными расстройствами, состояла из 49 человек (34 мужчин и 15 женщин). 1А группа - больные, которым проводилась терапия афобазолом – 29 человек (21 мужчина и 8 женщин) и 1Б группа - 20 больных (15 мужчин и 5 женщин), которым не проводилась терапия препаратом.
2 группа больных острым инфарктом миокарда без сопутствующих психоэмоциональных расстройств, состояла из 22 пациентов (15 мужчин и 7 женщин), являлась контрольной.
При интерпретации данных учитывался суммарный показатель по каждой подшкале HADS и опроснику Бека. Выделялись следующие области значений: по шкале HADS 0-7 баллов (норма) и по опроснику Бека от 0 до 9 баллов (отсутствие депрессивных симптомов) – такие пациенты включались во 2-ю группу (контрольную). 1 группа - больные, набравшие по шкале HADS 8-10 баллов (субклинически выраженная тревога/депрессия), 11 баллов и выше (клинически выраженная тревога/депрессия), а также по опроснику Бека 10-15 баллов (легкая депрессия (субдепрессия)), 16-19 – (умеренная депрессия); 20-29 – выраженная депрессия (средней тяжести).
Пациенты, получившие от 30 до 63 баллов (тяжелая депрессия) в исследование не включались, поскольку им было необходимо более тщательное обследование психиатром и проведение соответствующей терапии. Таким пациентам была рекомендована консультация психиатра.
Начальный уровень тревожно-депрессивных расстройств по шкале Бека составил в 1А группе 15,2 + 0,8 баллов, в 1Б группе 13,0 + 0,6; в контрольной группе (2 группа) 5,6 + 0,4. При оценке по шкале HADS: 1А группа 9,8 + 2,7 балла, 1Б группа 10,3 + 2,1 балла, контрольная группа 4,2+1,3 балла. По результатам тестирования в 1А группе у 17 (58,6%) пациентов были выявлены тревожно-депрессивные расстройства легкой степени тяжести, у 12 (41,4%) пациентов – средней степени тяжести, в 1 Б группе – 11 (55%) и 9 (45%) пациентов соответственно.
Динамика общей суммы баллов по психометрическим шкалам исходно и через 3 месяца представлена на рисунке 1. При оценке выраженности психоэмоциональных расстройств по шкале HADS в 1А группе на фоне терапии афобазолом отмечена выраженная редукция с 9,8+ 2,7 до 6,5+ 1,4 балла, (р< 0,05), в то время как в 1Б группе без психокорректирующей терапии средний балл оставался высоким: исходно 10,3+2,1 и 9,1+1,9 в конце наблюдения (р< 0,05). В контрольной группе существенных изменений не выявлено (4,2+1,3 балла и 3,9+1,0 соответственно (р<0,05)).
Рисунок 1. Динамика общей суммы баллов по шкале HADS.
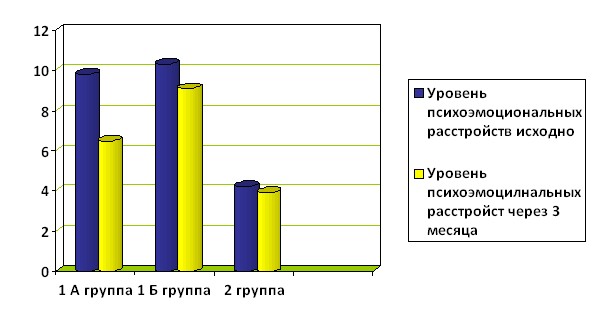 * - достоверность различий между группами при р < 0,05;
* - достоверность различий между группами при р < 0,05;
Подобная тенденция отмечена и по данным тестирования по шкале Бека. При оценке выраженности психоэмоциональных расстройств по шкале Бека в 1 А группе на фоне терапии афобазолом отмечено уменьшение количества баллов с 17,2 + 0,8 до 7,1+1,3 балла (р<0,05), в 1Б группе (без психокорректирующей терапии) средний балл исходно был 16,0 + 0,6, в конце наблюдения составил 15,8+ 1,6 (р<0,05). В контрольной группе также без существенной динамики: 5,6 + 0,4 балла и 4,7+0,9 соответственно (р<0,05).
Рисунок 2. Динамика общей суммы баллов по шкале Бека (исходно и через 3 месяца).
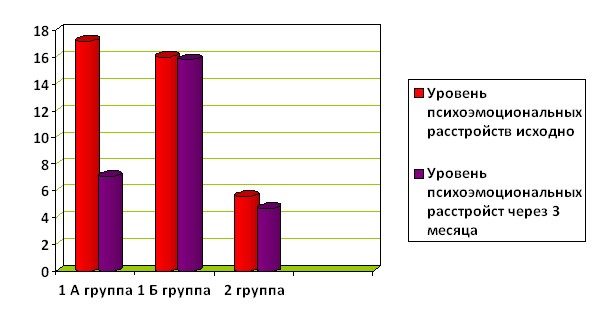 - достоверность различий между группами при р < 0,05
- достоверность различий между группами при р < 0,05
Всем больным проводилась также оценка психоэмоционального состояния с помощью методов фрактального анализа голоса.
Эталоном для оценки показателей фрактальной размерности речевого сигнала в контрольной группе (n=22) – пациенты без сопутствующих психоэмоциональных нарушений по результатам шкал, были показатели фрактальной размерности речевого сигнала, полученные сотрудниками Института высшей нервной деятельности и нейрофизиологии РАН при воспроизведении профессиональными актерами нейтрального, спокойного состояния, принятому за 100%. Показатели фрактальной размерности речевого сигнала у контрольной группы (2-я группа) также соответствовали 100%. Далее следовало сравнение показателей фрактальной размерности речевого сигнала 1А группы с контрольной и 1Б группы с контрольной.
Исходно в 1А группе показатель фрактальной размерности речевого сигнала составил 71,3+2,6%, в 1Б группе - 70,1+1,9% (р = 0,03). Для оценки чувствительности метода фрактального анализа речевого сигнала была произведена оценка значений показателя фрактальной размерности речевого сигнала в зависимости от степени выраженности психоэмоциональных нарушений. Обнаружено, что при выраженных расстройствах показатель снижается в большей степени.
При оценке выраженности психоэмоциональных расстройств методом фрактального анализа голоса через 3 месяца отмечена следующая динамика. В 1А группе на фоне терапии афобазолом отмечено увеличение показателя фрактальной размерности речевого сигнала с 71,3+2,6% до 98,0+ 1,7% (р<0,05), в то время как в 1Б группе без психокорректирующей терапии данный показатель остался без существенной динамики: исходно 70,1+1,9% и 73,5+2,1% в конце наблюдения (р<0,05).
Рисунок 3. Динамика показателя фрактальной размерности речевого сигнала в исследуемых группах (исходно и через 3 месяца).
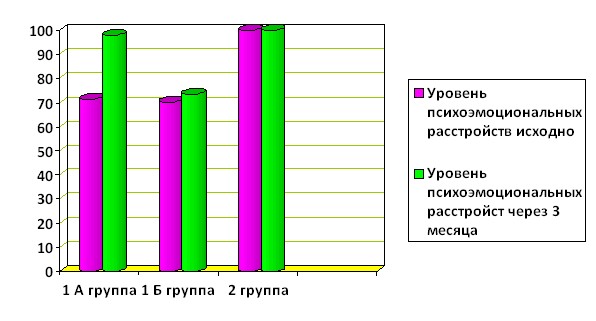 - достоверность различий между группами при р < 0,05;
- достоверность различий между группами при р < 0,05;
В нашей работе установлено, что фрактальный анализ речевого сигнала может применяться как скрининговый метод для выявления психоэмоциональных расстройств у больных ОИМ, поскольку является достаточно чувствительным даже при начальных проявлениях тревожно-депрессивных расстройств. При сопоставлении с данными тестирования с помощью шкал депрессии и тревоги было установлено, что у пациентов, которые набрали 8-10 баллов по шкале HADS и от 10 до 15 баллов по шкале BDI, что соответствует депрессии легкой степени выраженности, показатель фрактальной размерности речевого сигнала достоверно снижался до 68 % (р<0.05). В нашем исследовании метод показал 100% чувствительность, выявив психоэмоциональные нарушений у 49 пациентов, что подтверждено данными опросников. Ни у одного из 22 пациентов контрольной группы метод фрактального анализа речевого спектра не определил сопутствующих психоэмоциональных расстройств, что соответствует результатам специализированных шкал.
В ходе нашего наблюдения выявилось существенное различие по локализации инфаркта миокарда в сравниваемых группах. Так, у больных ОИМ с сопутствующими психоэмоциональными нарушениями (1-я группа) преобладала передняя локализация инфаркта миокарда – 63,3% (31 чел.), тогда как у больных острым инфарктом миокарда, протекающим без сопутствующих психоэмоциональных расстройств (2-я группа) частота встречаемости переднего инфаркта миокарда – 54,5% (12 чел.).
Встречаемость инфаркта миокарда различной локализации представлена на рис. 4.
Первая группа (n = 49)
Вторая группа (n = 22)
По данным эхокардиографии сократительная функция ЛЖ (ФВ), измеренная в период госпитализации и в конце наблюдения у исследуемых групп больных достоверно не различалась, как между группами с сопутствующими психоэмоциональными расстройствами и контрольной, так и после проведенного лечения.
Таблица 3
Сократительная функция ЛЖ по данным эхокардиографии, измеренная на периоде госпитализации и в конце наблюдения у исследованных больных
| Группы наблюдения | Группа 1А (n=29) | Группа 1Б (n=20) | Группа2 (n=22) |
| ФВ ЛЖ (%) на момент госпитализации | 51,88+1,7 | 56,97+2,3 | 55,68+2,1 |
| ФВ ЛЖ (%) через 3 месяца | 52,36+2,3 | 57,73+2,9 | 57,76+2,4 |
Как следует из приведенной таблицы 4, достоверных различий изменения ФВ ЛЖ не выявлено (для критерия Уилкоксона p>0,05 при сравнении до и после во всех группах).
Рисунок 5. Динамика изменения ФВ ЛЖ в исследуемых группах больных.

Целью настоящей работы было изучение влияния психоэмоциональных расстройств на течение острого инфаркта миокарда. Одним из прогностических факторов является вариабельность ритма сердца (ВРС).
Общая характеристика динамики показателей вариабельности сердечного ритма в исследуемых группах представлена на рисунке 6.
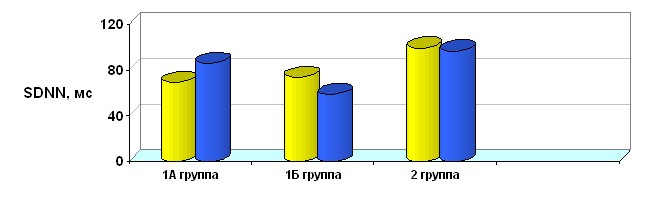
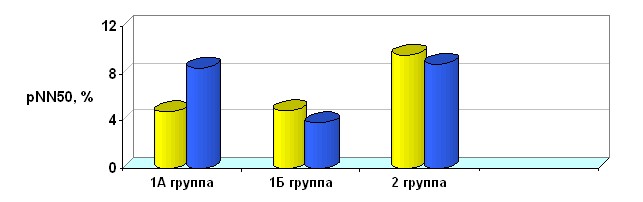
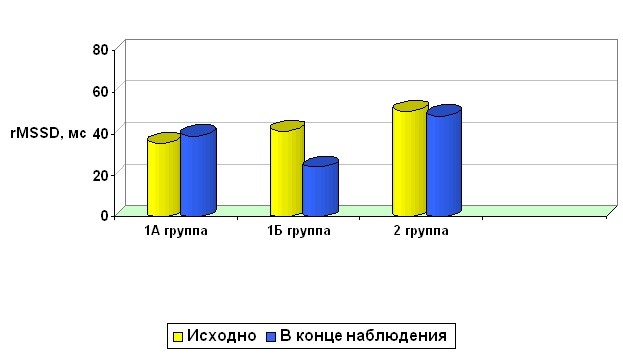
Примечание. * - достоверность различий между группами при р < 0,05; ** - при р < 0,01.
Рисунок 6. Общая характеристика показателей вариабельности сердечного ритма в исследуемых группах.
У больных инфарктом миокарда получено снижение влияния на синусовый узел симпатического и парасимпатического отделов автономной нервной системы – SDDN, более выраженное в группе больных острым инфарктом миокарда с сопутствующими психоэмоциональными расстройствами, по сравнению с контрольной группой. Показатели активности парасимпатической нервной системы (pNN50) достоверно не различались. Таким образом, вариабельность ритма сердца достоверно отражает стойкое повышение активности симпатической вегетативной нервной системы преимущественно в группе больных ОИМ с сопутствующими психоэмоциональными нарушениями.
При изучении вариабельности ритма сердца у больных инфарктом миокарда с сопутствующими психоэмоциональными расстройствами через 3 месяца получено достоверное снижение влияния на синусовый узел симпатического и парасимпатического отделов автономной нервной системы (SDDN) и значительное подавление активности парасимпатической нервной системы (pNN50) в 1Б группе, не получавших терапию афобазолом. Так, в группе больных инфарктом миокарда с сопутствующими психоэмоциональными расстройствами, без терапии афобазолом значения SDNN составили 58,62 ± 2,72 мсек, в 1А группе, получавшей афобазол - 86,0 ± 12,04 мсек, в контрольной группе (2 группа) - 96,48 ± 4,75 (р<0,02). Показатель активности парасимпатической вегетативной нервной системы - pNN50 – был существенно ниже в группе пациентов с сопутствующими психоэмоциональными расстройствами, не получавшими терапию афобазолом: 3,83 ± 0,58%, тогда как в группе, которой проводилась психокорректирующая терапия составил - 8,48 ± 2,25 %, а в контрольной группе - 8,83 ± 1,29, р<0,05. Показатели вариабельности ритма сердца свидетельствуют о выраженном вегетативном дисбалансе у больных 1 Б группы, не получавших терапию афобазолом, по сравнению с контрольной группой и группой больных, которым была проведена корректирующая терапия. Таким образом, можно сделать вывод, что своевременная коррекция психоэмоциональных нарушений способствует нормализации показателей вариабельности сердечного ритма, тем самым улучшая прогноз течения инфаркта миокарда. Исследуемые группы были сопоставимы по тяжести соматического состояния, инфаркта миокарда, а также методам проведенного лечения, что минимизирует влияние других факторов на показатели вариабельности ритма сердца, кроме сопутствующих психоэмоциональных расстройств. Полученные данные позволяют сделать вывод об отрицательном воздействии психоэмоциональных расстройств на клинические проявления ИМ, проявляющимся нарушением вегетативной регуляции сердечно-сосудистой системы с преобладанием симпатической активности, снижением ВСР и увеличением риска жизнеопасных желудочковых аритмий.
По частоте встречаемости изменений конечной части желудочкового комплекса (37,9% в 1А группе, 35,0% в 1Б группе, 31,8% во 2-ой группе), группы достоверно не различались, р>0,05.
Таблица 4
Результаты суточного мониторирования ЭКГ по Холтеру
во время госпитализации у исследуемых групп больных
| Изменение ST-T | Группа 1А (n=29) | Группа 1Б (n=20) | Группа 2 (n=22) | |||
| абс. | % | абс. | % | абс. | % | |
| Подъем | 4 | 13,8 | 2 | 10,0 | 2 | 9,1 |
| Депрессия | 7 | 24,1 | 5 | 25,0 | 5 | 22,7 |
| Не выявлено | 18 | 62,1 | 13 | 65,0 | 15 | 68,2 |
*Для всех значений р>0.05 по критерию Уилкоксона
Еще одним показателем течения и прогноза инфаркта миокарда является толерантность к физической нагрузке, определяемая с помощью пробы с дозированной физической нагрузкой. В результате коморбидности кардиологической и аффективной патологии обнаруживают реципрокные соотношения, выражающиеся усугублением как психических, так и соматических расстройств. У больных ИБС с психоэмоциональными расстройствами достоверно ниже толерантность к физической нагрузке по данным нагрузочных тестов по сравнению с больными с аналогичным соматическим статусом без тревоги и депрессии. Больные ИБС при наличии депрессии чаще жалуются на приступы стенокардии, ограничение физической активности, имеют худшее качество жизни и меньше удовлетворены результатами лечения, по сравнению с больными без психоэмоциональных расстройств. У больных острым инфарктом миокарда с психоэмоциональными нарушениями исходно толерантность к физической нагрузке была ниже, чем у больных острым инфарктом миокарда без сопутствующих психоэмоциональных расстройств. Так, в 1А группе низкая и средняя толерантность к физической нагрузке была у 19 больных - 65,5%, в 1Б группе – у 12 пациентов - 60%, в контрольной группе этот показатель составил 10 больных - 45,5%. У большинства пациентов 1А и 1Б группы причиной прекращения пробы послужило возникновение типичного для них приступа стенокардии без появления ишемических изменений на ЭКГ или же отказ пациента в связи с общей усталостью. Жалобы на боли чаще встречались в этих же группах - 1А группа – 11 (37,9%) больных, 1Б группа - 9 (45%) больных, в то время как в контрольной группе (2 группа) болевой синдром возник только 6 (27,3%) пациентов, причем у 4 пациентов болевой синдром сопровождался изменениями на ЭКГ, у 2 (9,1%) проба была прекращена только из-за появления на ЭКГ признаков ишемии миокарда без болевого синдрома.
Таблица 5
Результаты пробы с дозированной физической нагрузкой
в период госпитализации у исследованных больных
| Группы наблюдения/ Проба ВЭМ | Группа 1А (n=29) | Группа 1Б (n=20) | Группа 2 (n=22) | |||
| абс. | % | абс. | % | абс. | % | |
| Положительная проба | 3 | 10,3 | 0 | 0,0 | 6 | 27,3 |
| Низкий и средний порог | 19 | 65,5 | 12 | 60,0 | 10 | 45,5 |
| Высокий порог и отрицательная проба | 10 | 34,5 | 8 | 40,0 | 12 | 54,5 |
| Болевой синдром | 11 | 37,9 | 9 | 45,0 | 6 | 27,3 |
| Болевой синдром + ишемия миокарда (ЭКГ) | 2 | 6,9 | 0 | 0,0 | 4 | 18,2 |
| Ишемия на ЭКГ (болевой синдром отсутствует) | 0 | 0,0 | 0 | 0,0 | 2 | 9,1 |
По результатам пробы с дозированной физической нагрузкой, проведенной, в конце наблюдения выявлено, что в группе получавшей терапию афобазолом увеличилась толерантность пациентов к физической нагрузке - 17 больных(58,6%), а также снизилось количество пациентов, у которых развивался болевой синдром во время теста - 3 пациента (10,3%). В то же время в группе больных инфарктом миокарда с сопутствующими психоэмоциональными нарушениями, которым не проводилась психокорректирующая терапия (1Б группа) толерантность к физической нагрузке возросла не столь значительно.
Таблица7
Результаты пробы с дозированной физической нагрузкой
в конце периода наблюдения у исследуемых групп пациентов
| Тредмил тест | Группа 1А (n=29) | Группа 1Б (n=20) | Группа 2 (n=22) | |||
| абс. | % | абс. | % | абс. | % | |
| Положительная проба | 1 | 3,4 | 0 | 0,0 | 2 | 9,1 |
| Низкий и средний порог | 12 | 41,4 | 10 | 50,0 | 8 | 36,4 |
| Высокий порог и отрицательная проба | 17 | 58,6 | 10 | 50,0 | 12 | 54,5 |
| Болевой синдром | 3 | 10,3 | 7 | 35,0 | 3 | 13,6 |
| Болевой синдром + ишемия миокарда (ЭКГ) | 1 | 3,4 | 0 | 0,0 | 2 | 9,1 |
| Ишемия на ЭКГ (болевой синдром отсутствует) | 0 | 0,0 | 0 | 0,0 | 0 | 0,0 |
Таким образом, исходно сниженная толерантность к физической нагрузке у больных инфарктом миокарда с сопутствующими психоэмоциональными нарушениями, повышается на фоне проводимой терапии афобазолом.
Раннее выявление и коррекция психоэмоциональных расстройств у больных острым инфарктом миокарда позволит улучшить прогноз течения основного заболевания и качества жизни таких пациентов.
Выводы
- У больных острым инфарктом миокарда психоэмоциональные нарушения развиваются 1,2 раза чаще при поражении передней стенки ЛЖ.
- Сопутствующие острому инфаркту миокарда психоэмоциональные расстройства не влияют на сократительную функцию ЛЖ.
- Больные инфарктом миокарда и психоэмоциональными расстройствами имеют более выраженный синдром вегетативной дистонии. Для них также характерно нарушение механизмов регуляции вегетативного тонуса, заключающееся в преобладании активности симпатической нервной системы с активацией центральных эрготропных механизмов и уменьшении парасимпатической активности.
- У больных инфарктом миокарда с сопутствующими психоэмоциональными нарушениями толерантность к физической нагрузке ниже, чем у пациентов без психоэмоциональных расстройств.
- Метод фрактального анализа голоса может быть использован для первичной (скрининговой) диагностики психоэмоциональных расстройств у больных острым инфарктом миокарда.
- Присоединение афобазола к стандартной терапии инфаркта миокарда у больных с сопутствующими психоэмоциональными нарушениями позволяет добиться улучшения соматического статуса, уменьшения проявлений вегетативной дисфункции, повышения толерантности к физической нагрузке.
Практические рекомендации
- У больных острым инфарктом миокарда, необходимо проведение оценки психосоматического статуса для выявления психоэмоциональных нарушений.
- Для выявления психоэмоциональных расстройств у больных острым инфарктом миокарда, целесообразно для первичной (скрининговой) диагностики применение метода фрактального анализа речевого спектра, поскольку он не требует никаких действий от пациента.
- Для уменьшения уровня психоэмоциональных расстройств и улучшения клинического состояния больных инфарктом миокарда рекомендуется использование корректирующей терапии в комплексе со стандартным лечением.
- Для больных острым инфарктом миокарда в качестве корректирующей терапии рекомендуется применение афобазола (1 таблетка 3 раза в день; 15 мг в сутки).
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ:
- Беневская М.А., Люсов В. А., Волов Н.А., Лебедева А.Ю., Кудинова М.А. Методы диагностики тревожно-депрессивных расстройств у больных острым инфарктом миокарда // Российский кардиологический журнал. – 2010;1:77-82.
- Беневская М.А., Люсов В.А., Волов Н.А. Коррекция тревожно-депрессивных расстройств у больных острым инфарктом миокарда //Материалы научно-практической конференции ГКБ № 60 «Клиническая гериатрия в многопрофильном стационаре». – 2010; с. 213-216.
- Беневская М.А., Кудинова М.А. Взаимосвязь психоэмоциональных нарушений и локализации инфаркта миокарда. //Материалы V Национального конгресса терапевтов. Основной сборник. 2010; с. 120.

