Клинико-прогностическое значение метаболической терапии у больных инфарктом миокарда
На правах рукописи
БЕЛЬКОВ
Алексей Викторович
КЛИНИКО-ПРОГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ МЕТАБОЛИЧЕСКОЙ ТЕРАПИИ У БОЛЬНЫХ ИНФАРКТОМ МИОКАРДА
14.01.05 – кардиология
14.03.06 – фармакология, клиническая фармакология
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2011
Работа выполнена на кафедре госпитальной терапии с курсами семейной медицины, клинической фармакологии и клинической лабораторной диагностики ГОУВПО «Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова» Министерства здравоохранения и социального развития Российской Федерации.
Научные руководители:
заслуженный деятель науки РФ,
академик РАМН,
доктор медицинских наук,
профессор Шабров Александр Владимирович
доктор медицинских наук,
профессор Бурбелло Александра Тимофеевна
Официальные оппоненты:
доктор медицинских наук,
профессор Перепеч Никита Борисович
доктор медицинских наук,
профессор Звартау Эдвин Эдуардович
Ведущее учреждение:
ФГОУВПО «Военно – медицинская академия им. С.М. Кирова» МОРФ
Защита диссертации состоится «15» июня 2011 года в «____» часов на заседании диссертационного совета Д 208.086.01 в ГОУВПО «Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова» Министерства здравоохранения и социального развития Российской Федерации (195067, Санкт-Петербург, Пискаревский пр., д. 47).
С диссертацией можно ознакомиться в библиотеке ГОУВПО «Санкт-Петербургская государственная медицинская академия им. И.И.Мечникова» Министерства здравоохранения и социального развития Российской Федерации.
Автореферат разослан «____» мая 2011 года.
Ученый секретарь диссертационного совета
доктор медицинских наук,
профессор Соколова Людмила Андреевна
Список сокращений
HF – высокочастотный
LF – низкочастотный
АД – артериальное давление
ВСР – вариабельность сердечного ритма
ИБС - ишемическая болезнь сердца
ИМ – инфаркт миокарда
КГ – контрольная группа
ЛЖ – левый желудочек
ЛПВП – липопротеины высокой плотности
ЛПНП – липопротеины низкой плотности
ОХ – общий холестерин
ПНЖК – полиненасыщенные жирные кислоты
ППЖ – поздние потенциалы желудочков
СН – сердечная недостаточность
ТГ – триглицериды
ТМЗ – триметазидин
ТШХ – тест с шестиминутной ходьбой
ФВ – фракция выброса
ЭКГ – ВР – ЭКГ высокого разрешения
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Сердечно-сосудистые заболевания сохраняют ведущее место в структуре общей смертности в России и во многих иных странах мира. Так в России в 2008 году болезни системы кровообращения составили 56 % среди всех причин смерти. При этом показано, что в структуре сердечно-сосудистой патологии большая часть приходится на долю ишемической болезни сердца (ИБС). Социальную значимость проблемы усиливает наблюдающаяся в последние годы тенденция увеличения новых случаев кардиальных заболеваний, в том числе с фатальным исходом, у молодых людей трудоспособного возраста (Чазов Е.И., 2007, Беленков Ю.Н., 2008). Причинно–следственные связи, лежащие в основе комплекса постинфарктных изменений миокарда, стали предметом пристального изучения относительно недавно. Непосредственное воздействие ишемического фактора ведет к гибели части кардиомиоцитов. Это в свою очередь ведет к увеличению нагрузки на «интактный» миокард, что приводит к активации регуляторных нейрогуморальных систем, ведущих к возникновению и прогрессированию постинфарктного ремоделирования, которое в значительной степени определяет прогноз больного с постинфарктным кардиосклерозом (Беленков Ю.Н., 2002). Важнейшими составляющими постинфарктного ремоделирования левого желудочка (ЛЖ) являются изменения формы, размера и толщины миокарда, как в зоне инфаркта, так и в неповрежденных участках, что приводит к возникновению явлений сердечной недостаточности. Другим фактором прогноза больного после инфаркта миокарда (ИМ) являются нарушения ритма, являющиеся самостоятельным фактором риска внезапной смерти. Известно, что только в первый год после ИМ более половины смертей связано с фатальными нарушениями ритма сердца (Myerburg R., 2000). Учитывая высокую распространенность внезапной смерти после ИМ, в настоящее время во всем мире у этих больных активно проводятся исследования показателей вариабельности сердечного ритма (ВСР) и параметров электрической нестабильности миокарда по выявляемости поздних потенциалов желудочков (ППЖ) для поиска дополнительных возможностей прогнозирования и профилактики фатальных желудочковых аритмий.
Для лечения неосложненного ИМ и вторичной профилактики ИБС используются -адрено-блокаторы, ингибиторы АПФ, антиагреганты, антикоагулянты, статины. Однако сохраняющаяся высокая частота внезапной смерти у пациентов после ИМ показывает, что возможности предупреждения жизнеопасных желудочковых аритмий остаются недостаточными.
Одними из разрабатываемых в последнее время медикаментозных методов лечения ИМ является применение препаратов -3 полиненасыщенных жирных кислот (ПНЖК) и метаболических цитопротекторов. Экспериментальными и клиническими исследованиями показано, что -3 ПНЖК оказывают противовоспалительное, гиполипидемическое, антиагрегантное и противоаритмическое действие и увеличивают продолжительность жизни больных с ИБС (Бурячковская Л.И. и др., 2007). Также в многочисленных, рандомизированных, контролируемых исследованиях продемонстрирована антиишемическая эффективность триметазидина (ТМЗ) (Васюк Ю.А., 2008). Положительный эффект препарата обусловлен оптимизацией использования кислорода кардиомиоцитами, способствуя синтезу большего количества молекул АТФ и тем самым улучшая баланс между потребностью миокарда в кислороде и его поступлением. Однако, несмотря на многочисленные исследования, в настоящее время многие аспекты действия ТМЗ, -3 ПНЖК не изучены. В частности недостаточно изучено влияние этих препаратов у больных ИМ при их раннем назначении (с 1 суток заболевания) на клиническое течение заболевания, характер постинфарктного ремоделирования, динамику ВСР и выявляемость ППЖ. В то время как в рекомендациях ВНОК по лечению ИБС эти препараты рассматриваются в качестве препаратов метаболического действия.
Это и определило проведение настоящего исследования влияния терапии триметазидином и -3 полиненасыщенными жирными кислотами на клиническое течение заболевания, показатели систолической и диастолической функции левого желудочка, показатели электрической нестабильности миокарда, баланс звеньев вегетативной нервной системы в динамике наблюдения в течение 6 месяцев у пациентов, перенесших инфаркт миокарда.
Цель исследования: оценить влияние триметазидина, -3 ПНЖК в составе сочетанной терапии на клиническое течение заболевания, функциональное состояние левого желудочка и некоторые предикторы внезапной коронарной смерти у пациентов, перенесших инфаркт миокарда, при использовании препаратов с 1-х суток заболевания.
Задачи исследования:
1. Изучить влияние сочетанной терапии, (стандартная + -3 ПНЖК или триметазидин) на клиническое течение инфаркта миокарда.
2. Изучить влияние сочетанной терапии на показатели систолической и диастолической функции миокарда левого желудочка у больных инфарктом миокарда.
3. Оценить значимость сочетанной терапии на вариабельность сердечного ритма у больных инфарктом миокарда.
4. Оценить значимость сочетанной терапии на выявляемость поздних потенциалов желудочков у больных инфарктом миокарда.
5. Разработать рекомендации по применению триметазидина, -3 полиненасыщенных жирных кислот в комплексной терапии больных острым инфарктом миокарда.
Научная новизна исследования.
Установлено, что включение в комплексное лечение больных инфарктом миокарда триметазидина или -3 полиненасыщенных жирных кислот улучшает клиническое течение заболевания, выявлено улучшение систолической функции миокарда левого желудочка при добавлении к стандартной терапии триметазидина, а при добавлении -3 полиненасыщенных жирных кислот выявлено улучшение диастолической функции миокарда.
Впервые выявлено, что в группах пациентов, получавших дополнительно к основной терапии ТМЗ или -3 полиненасыщенные жирные кислоты, с 3-го месяца лечения происходило достоверно более быстрое восстановление показателей ВСР (изменение вегетативного баланса в пользу парасимпатического отдела), с дальнейшей их положительной динамикой к 6 месяцам исследования по сравнению с контрольной группой.
Впервые определено, что применение -3 ПНЖК с первых суток острого ИМ уменьшает выявляемость поздних потенциалов желудочков у больных инфарктом миокарда в сравнении со стандартной терапией, и терапией, включающей триметазидин. Длительность применения препарата должна быть не менее 2 месяцев.
Выявлено, что на фоне применения препарата, содержащего -3 полиненасыщенные жирные кислоты происходит достоверно большее снижение общего холестерина, липопротеидов низкой плотности и триглицеридов, в сравнении со стандартной терапией включающей статины и терапией, дополненной триметазидином.
Теоретическая и практическая значимость работы
Включение триметазидина в составе комплексной терапии сопровождается достоверным улучшением систолической функции миокарда, а применение -3 полиненасыщенных жирных кислот сопровождается улучшением диастолической функции. Включение в комплексную терапию пациентов с инфарктом миокарда триметазидина или -3 полиненасыщенных жирных кислот способствует более быстрому восстановлению показателей вариабельности сердечного ритма. Применение -3 полиненасыщенных жирных кислот способствует снижению регистрации поздних потенциалов желудочков, более быстрой нормализации липидного состава крови. Триметазидин в дополнение к стандартной терапии можно рекомендовать пациентам, имеющим сниженную ВСР в остром периоде инфаркта миокарда и/или нарушение систолической функции миокарда левого желудочка с 1-х суток течения заболевания. Назначение -3 полиненасыщенных жирных кислот показано больным ИМ, с дислипидемией, имеющим сниженную ВСР, наличие ППЖ, и с диастолической дисфункцией миокарда левого желудочка, курсом не менее 2 месяцев.
Основные положения, выносимые на защиту
1. Назначение с первых суток в составе комплексной терапии триметазидина или -3 полиненасыщенных жирных кислот, пациентам с инфарктом миокарда, приводит к улучшению клинического течения заболевания, по данным теста с шестиминутной ходьбой в более ранние сроки, чем у пациентов со стандартной терапией.
2. Применение триметазидина в составе комплексной терапии, в ранние сроки пациентам с инфарктом миокарда, способствует восстановлению систолической функции миокарда быстрее, чем у пациентов со стандартной терапией и терапией, включавшей -3 полиненасыщенные жирные кислоты, тогда как при назначении в составе комплексной терапии -3 полиненасыщенных жирных кислот происходит более ранняя нормализация диастолической функции миокарда ЛЖ.
3. При добавлении в комплексную терапию больным инфарктом миокарда триметазидина или -3 полиненасыщенных жирных кислот, происходит более раннее и полное восстановление показателей ВСР, чем у пациентов, получавших только стандартную терапию.
4. Назначение в ранние сроки в составе комплексной терапии -3 полиненасыщенных жирных кислот приводит к уменьшению выявляемости ППЖ, по сравнению с группами пациентов, принимавших стандартную терапию, или получавших в дополнение к стандартной терапии триметазидин.
5. Дополнение стандартной терапии, включающей статины, триметазидином не оказывает влияния на показатели липидного обмена, тогда как в группе, дополненной назначением к стандартной терапии -3 полиненасыщенных жирных кислот, наблюдается более выраженное снижение уровня общего холестерина, липопротеинов низкой плотности и триглицеридов, повышение уровня липопротеинов высокой плотности.
Личный вклад автора. Личное участие автора осуществлялось на всех этапах работы и включало планирование и проведение исследований по всем разделам диссертации, формулирование целей и задач, определение объема и методов исследования, подбор, перевод и анализ литературы по теме диссертационной работы. Самостоятельно проведено первичное клиническое обследование 84 пациентов с инфарктом миокарда; проведены сбор анамнеза, физикальное и клиническое обследование с оценкой результатов теста с шестиминутной ходьбой (ТШХ), осуществлено динамическое наблюдение за больными с повторным комплексным обследованием на 15 сутки, через 3 месяца и 6 месяцев. Лично автором выполнялись следующие методики: электрокардиография, анализ данных эхокардиографии, анализ показателей ВСР, оценка данных ЭКГ – высокого разрешения (ЭКГ-ВР), данных липидного спектра крови. Статистическая обработка полученных данных проводилась с участием сотрудников кафедры системного анализа и управления ГОУВПО «Санкт-Петербургский государственный политехнический университет».
Реализация и апробация работы.
Основные положения и практические рекомендации диссертации внедрены и используются в работе кардиологического отделения Санкт-Петербургской городской многопрофильной больницы №2, отделения по лечению больных инфарктом миокарда, отделения интенсивной кардиологии и реанимации клинической больницы Петра Великого, а так же в лекциях и на занятиях со студентами, интернами и клиническими ординаторами на кафедре факультетской терапии с курсом интервенционной кардиологии и кафедре госпитальной терапии с курсами семейной медицины, клинической фармакологии и клинической лабораторной диагностики ГОУВПО СПбГМА им. И.И. Мечникова.
Основные материалы исследований доложены на первой международной научной конференции «Донозология – 2005. Экологические и медицинские проблемы возникновения донозологических и патологических состояний в условиях мегаполисов », Санкт-Петербург, научно-практической конференции сотрудников и студентов СПбГМА им.И.И. Мечникова «Человек и его здоровье» (2005 г., Санкт-Петербург). Апробация работы прошла на расширенном заседании проблемной комиссии «Проблемы диагностики, лечения и профилактики заболеваний сердечно-сосудистой системы и других внутренних органов» и кафедры госпитальной терапии с курсами семейной медицины, клинической фармакологии и клинической лабораторной диагностики СПбГМА им. И.И. Мечникова 9.03.2011 г.
По теме диссертации опубликовано 10 научных работ, в том числе 1 статья в ведущем издании, рекомендованном ВАК.
Объем и структура диссертации:
Диссертация изложена на 122 страницах машинописного текста и включает введение, обзор литературы, описание материала и методов исследования, изложение собственных результатов, обсуждение полученных результатов, выводов и практических рекомендаций. Работа содержит 21 таблицу и 16 рисунков. В работе использовано 202 источника литературы, из них 86 отечественных.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Работа проводилась на кафедре госпитальной терапии с курсами клинической фармакологии, семейной медицины и клинической лабораторной диагностики ГОУВПО СПбГМА им. И.И. Мечникова. В исследование было включено 87 пациентов, поступивших в отделение реанимации и интенсивной терапии клиники кардиологии, из них в статистическую обработку вошло 84 пациента. Три пациента были исключены из исследования: один – отказался от приема препарата из-за плохой переносимости (отрыжка рыбьим жиром), и двое – из-за нерегулярного приема препаратов.
Все пациенты перенесли впервые возникший острый ИМ передней стенки левого желудочка с элевацией сегмента ST и с успешно проведенным системным тромболизисом активатором плазминогена алтеплазой. Критериями эффективности тромболитической терапии считались: купирование болевого синдрома, нормализация сегмента ST и возникновение реперфузионных нарушений ритма. Все пациенты были сопоставимы по возрасту и полу. Возрастной состав пациентов колебался от 48 до 67 лет, средний возраст составил 55,5 лет. Исследование рандомизировано по порядку поступления больных в клинику. В стандартную терапию были включены антикоагулянты, дезагреганты (аспирин), ингибиторы АПФ, -блокаторы, статины, нитраты по необходимости.
В зависимости от препаратов, дополняющих стандартную терапию, все пациенты были разделены на 3 группы, которые были сопоставимы по таким модифицируемым факторам риска как курение, артериальная гипертензия, дислипидемия, масса тела:
I группа (29 пациентов) – контрольная группа (КГ), больные получали только стандартную терапию;
II группа (27 пациентов) – в дополнение к стандартной терапии больные принимали триметазидин в дозе 70 мг/сутки;
III группа (28 пациентов) – в дополнение к стандартной терапии больные получали препарат, содержащий -3 ПНЖК (полиен) по 3 грамма/сутки (750-900 мг в пересчете на -3 ПНЖК).
Все препараты назначались в первые 24 часа от начала инфаркта миокарда, длительность применения не менее 6 месяцев. Полиен назначался курсами по 2 месяца с двухмесячным перерывом. Наблюдение за пациентами продолжалось в течение 6 месяцев от начала терапии. Исследования выполнялись в сроки: 1-е сутки, 15-е сутки, 3 мес., 6 мес. У всех больных оценивались клиническая картина, данные электрокардиографии, биохимические данные, наличие ППЖ, вариабельность сердечного ритма, некоторые морфологические и функциональные параметры миокарда ЛЖ.
Оценку клинического течения заболевания у больных и оценку функционального класса сердечной недостаточности, проводили с помощью ТШХ по общепринятой методике на 21 сутки и через 6 месяцев лечения. Пациентам выполнялись контрольные ЭКГ-исследования, с анализом сердечного ритма, частоты сердечных сокращений, ишемических изменений. Суточное мониторирование артериального давления проводилось на 1 сутки и через 6 месяцев лечения. Биохимические исследования: анализ крови: (КФК-МВ, тропонин Т – в первые сутки, липидограмма в сроки: 1-е сутки, 15-е сутки, 3 месяца, 6 месяцев). Липидный спектр крови оценивали по уровню общего холестерина, холестерина ЛПНП, холестерина ЛПВП, триглицеридов в плазме крови. Исследования производились в центральной лаборатории СПбГМА стандартным набором реактивов.
Вариабельность сердечного ритма оценивали по показателям во временной и частотной областях согласно международным стандартам. Ритмокардиограммы регистрировались в течение 5-ти минут в горизонтальном положении больного при произвольном дыхании после 10-15 минутного отдыха в одно и то же время суток (11-13 часов), не менее чем через два часа после еды. Поздние потенциалы желудочков регистрировались с помощью ЭКГ высокого разрешения по стандартной методике, утвержденной в 1991 году комитетом экспертов при Европейской и Американской ассоциациях кардиологов.
Статистическая обработка результатов проводилась после оценки характера распределения полученных данных с помощью стандартных пакетов программ Statistica 6.0 и Excel MS XP. Критический уровень достоверности (р) нулевой статистической гипотезы принимали при р<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Анализ динамики показателей ЭКГ у больных за весь период наблюдения различий между исследуемыми группами не выявил. У всех больных наблюдалась нормализация как частоты сердечных сокращений, так и процессов реполяризации. При анализе результатов суточного мониторирования артериального давления (АД) выявлена нормализация показателей во всех исследуемых группах к 6 месяцу терапии, достоверных различий уровня АД при сравнении исследуемых групп пациентов не выявлено. Это свидетельствует о том, что антигипертензивный эффект достигался за счет средств, входящих в стандартную схему терапии, а исследуемые нами препараты не оказывали существенного влияния на показатели АД в указанные сроки.
После определения толерантности к физической нагрузке и оценки тяжести сердечной недостаточности (СН) к окончанию исследования клиническое улучшение выявлено во всех исследуемых группах, что продемонстрировано снижением ФК СН, достоверным улучшением показателей ТШХ. При сравнении показателей ТШХ между группами выявлено, что в группе ТМЗ по сравнению с группой со стандартной терапией уже на 21 сутки выявлено достоверное улучшение показателей ТШХ. При этом как в группе ТМЗ, так и в группе -3 ПНЖК к окончанию срока лечения по сравнению с КГ выявлено достоверное увеличение проходимой пациентами дистанции в процессе выполнения ТШХ, что свидетельствует о положительном влиянии исследуемых препаратов на клиническое течение и прогноз заболевания в раннем постинфарктном периоде.
Динамика показателей систолической и диастолической функции миокарда на фоне терапии. Оценка состояния систолической функции миокарда ЛЖ производилась по величине фракции выброса (ФВ), а диастолической – по анализу данных соотношения скоростей трансмитрального кровотока и изменения скорости реверсивной волны в легочные вены. Одновременно на основании динамики параметров толщины миокарда и конечных систолического и диастолического размеров (объемов) проводилась оценка степени постинфарктного ремоделирования миокарда.
Сравнение средних величин ФВ (рис.1) в 1-е сутки заболевания демонстрирует, что сократительная способность миокарда в среднем была одинакова во всех группах, что говорит о сопоставимости групп, а её средняя величина – о сохранности её у значительной части больных.
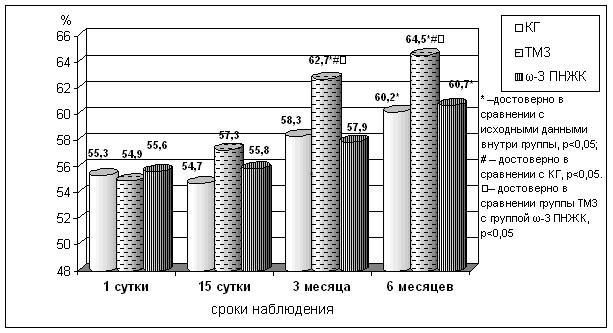
Рис. 1. Характер изменения систолической функции (по величине ФВ в %) в зависимости от характера терапии
Характер показателей ФВ на фоне терапии имеет определенные зависимости от характера лекарственной программы. На фоне применения триметазидина тенденция к улучшению систолической функции выявляется уже к концу острейшего периода постинфарктного ремоделирования. А через 3 и 6 месяцев показатели ФВ оказываются в пределах величин, которые регистрируются у практически здоровых людей. Так, в группе триметазидина к 3 месяцу лечения ФВ выросла на 14,2%, а к 6 месяцу на 17, 5% относительно исходных данных. При сравнении данной группы с КГ и группой -3 ПНЖК в срок 3 месяца выявлено достоверное (р<0,05) увеличение ФВ, с сохраняющейся положительной динамикой к окончанию исследования. В противоположность с группой получавшей ТМЗ, включение -3 ПНЖК в программу лечения не оказывает влияния на параметры систолической функции. Средние величины ФВ в этой группе сходны с величинами, которые определялись в группе со стандартной терапией.
Для оценки типа диастолической дисфункции в нашей работе мы использовали анализ соотношения ранней и поздней скоростей трансмитрального кровотока с учетом скорости реверсивной волны в легочные вены. Все пациенты внутри групп были разделены на подгруппы по типу диастолической дисфункции с выделением ригидного, псевдонормального и рестриктивного (прогностически самого неблагоприятного) типов. Исходно при анализе в общей группе больных (без выделения групп в зависимости от получаемой терапии) диастолическая дисфункция была найдена у всех пациентов, включенных в исследование. С целью статистической обработки, и сравнения полученных данных, для оценки тяжести диастолической дисфункции, у больных, включенных в исследование, использовали интегральный параметр оценки тяжести диастолической дисфункции, основанный на присвоении каждому типу определенного кода. При анализе полученных данных (табл. 1) найдено достоверное уменьшение степени диастолической дисфункции во всех трех группах к 6-ти месяцам наблюдения. При сравнении между группами в срок 6 месяцев выявлено достоверное уменьшение степени диастолической дисфункции в группе -3 ПНЖК по сравнению, как с показателями в КГ, так и в группе с применением ТМЗ. Это позволяет сделать вывод о влиянии терапии, включающей -3 ПНЖК на состоянии диастолической функции и объясняет найденные положительные изменения величины дистанции шестиминутной ходьбы.
Таблица 1
Динамика интегрального показателя тяжести диастолической дисфункции
| Группа | Тип дисфункции, код | Кол-во случаев до лечения | Средняя величина кода | Кол-во случаев через 6 месяцев | Средняя величина кода |
| КГ | N=1 | 0 | 2,55±0,053 | 1 | 2,34±0,052* |
| Rig=2 | 17 | 20 | |||
| PN=3 | 8 | 5 | |||
| RS=4 | 4 | 3 | |||
| ТМЗ | N=1 | 0 | 2,52±0,51 | 1 | 2,30±0,051* |
| Rig=2 | 16 | 19 | |||
| PN=3 | 8 | 5 | |||
| RS=4 | 3 | 2 | |||
| ПНЖК | N=1 | 0 | 2,61±0,054 | 2 | 2,14±0,048*#° |
| Rig=2 | 15 | 21 | |||
| PN=3 | 9 | 4 | |||
| RS=4 | 4 | 1 |
________________
N – нормальный тип дисфункции, Rig – ригидный, PN – псевдонормальный, RS – рестриктивный;
* –достоверно в сравнении с исходными данными, р<0,05;
# – достоверно в сравнении с КГ, р<0,05;
° – достоверно при сравнении группы -3 ПНЖК с группой ТМЗ р<0,05.
Таким образом, полученные в работе данные свидетельствуют, что у больных после инфаркта возникает как систолическая, так и диастолическая дисфункция миокарда, сопровождающаяся его ремоделированием, а включение в программу терапии таких больных триметазидина может улучшать состояние систолической функции, а -3 ПНЖК – диастолической функции (что клинически сопровождается улучшением показателя дистанции шестиминутной ходьбы).
Влияние триметазидина, -3 ПНЖК на вариабельность сердечного ритма. Параметры, характеризующие ВСР, имеют важное прогностическое значение для оценки степени риска внезапной смерти у пациентов перенесших ИМ. По нашим данным в 1-е сутки ИМ у всех обследованных пациентов имелось значительное снижение как временных, так и спектральных показателей ВСР, что свидетельствовало о возникающем дисбалансе между симпатическим и парасимпатическим отделами вегетативной нервной системы. При изучении динамики временных показателей установлено, что у пациентов всех групп происходит постепенное увеличение ВСР, приближаясь к нормальным показателям. Однако при сравнении оказывается, что наиболее полное и быстрое восстановление показателей произошло в группах с добавлением триметазидина или -3 ПНЖК по сравнению с контрольной группой. Данные динамики временных показателей представлены в таблице 2.
Таблица 2
Динамика временных показателей ВСР на фоне терапии
| Группа | Показатель | 1 сутки | 15 сутки | 3 мес. | 6 мес. |
| КГ | SDNN, мс | 23,6±5,51 | 28,1±5,83 | 30,6±4,26 | 32,7±4,58* |
| RMSSD, мс | 17,3±3,68 | 19,1±4,64 | 20,8±3,67 | 23,2±3,24* | |
| pNN50 | 2,9±0,44 | 3,4±0,52 | 4,0±0,61 | 5,1±0,67* | |
| ТМЗ | SDNN, мс | 24,2±4,42 | 34,2±5,12* | 41,1±4,35*# | 44,6±5,43*# |
| RMSSD, мс | 17,9±4,33 | 23,5±4,24 | 28,7±4,12*# | 31,6±4,15*# | |
| pNN50 | 3,1±0,35 | 3,9±0,45 | 6,2±0,8*# | 9,8±0,92*# | |
| ПНЖК | SDNN, мс | 24,9±5,87 | 31,4 ±4,75 | 39,6±5,17*# | 42,5±5,23*# |
| RMSSD, мс | 17,1±4,47 | 22,6±5,54 | 27,9±4,29*# | 29,8±4,61*# | |
| pNN50 | 3,2±0,4 | 4,1±0,48 | 5,9±0,62*# | 9,1±0,75*# |
________________
* –достоверно в сравнении с исходными данными, р<0,05;
# – достоверно в сравнении с КГ, р<0,05.
При анализе динамики показателя SDNN выявлено достоверное увеличение показателя во всех группах пациентов к 6 месяцу лечения. Впервые достоверное возрастание показателя SDNN по сравнению с первыми сутками лечения выявлено на 15 сутки лечения в группе триметазидина. Далее на 3 месяце лечения в группах триметазидина и -3 ПНЖК выявлено достоверное возрастание показателя SDNN по сравнению, как с первыми сутками лечения, так и с контрольной группой, что свидетельствовало о более быстром восстановлении ВСР в этих группах. К 6 месяцу происходило дальнейшее достоверное увеличение показателя в группах триметазидина и -3 ПНЖК по сравнению, как с первыми сутками лечения, так и с контрольной группой.
Анализируя динамику показателя RMSSD, отражающего кратковременную смену частоты ритма, зависящую от вагусного влияния, выявлено достоверное увеличение показателя к 6 месяцам во всех исследуемых группах. Однако в группах триметазидина и -3 ПНЖК по сравнению с контрольной группой, как на 3, так и на 6 месяц исследования отмечено (аналогично с показателем SDNN) достоверно более быстрое восстановление показателя RMSSD.
При изучении динамики показателя pNN50, отражающего влияние парасимпатического звена регуляции, имелось достоверное увеличение показателя, начиная с 3 месяца исследования, с дальнейшей положительной динамикой к 6 месяцу исследования в группах триметазидина и -3 ПНЖК по сравнению с 1-ми сутками и с контрольной группой. В контрольной группе достоверное увеличение показателя pNN50 по сравнению с 1 сутками выявлено только на 6 месяце исследования. Такие изменения показателя pNN50 свидетельствуют о увеличении влияния парасимпатического звена регуляции под влиянием -3 ПНЖК и триметазидина.
Таким образом, анализируя динамику временных показателей ВСР, нами установлено постепенное восстановление показателей во всех исследуемых группах. В контрольной группе достоверные изменения произошли только к 6 месяцу исследования. В группах триметазидина и -3 ПНЖК начиная с 3-го месяца и с дальнейшей положительной динамикой к 6 месяцам исследования, выявлено достоверно более быстрое и полное восстановление изучаемых нами временных показателей ВСР, по сравнению с контрольной группой и с исходными результатами (увеличение SDNN, RMSSD, pNN50), что свидетельствовало о возрастании роли парасимпатического звена регуляции, играющего защитную роль в возникновении опасных желудочковых аритмий.
При оценке спектральной мощности колебаний, отражающей вклад тех или иных периодических составляющих в динамике изменения ритма, было выявлено снижение всех спектральных показателей, что обусловлено дисбалансом вегетативной нервной системы, характерном для больных ИМ. По нашим данным, у пациентов с ИМ имело место преобладание симпатических влияний над парасимпатическими. Данные динамики спектральных показателей представлены в таблице 3.
Таблица 3
Динамика спектральных показателей ВСР на фоне терапии
| Группа | Показатель | 1 сутки | 15 сутки | 3 мес. | 6 мес. |
| КГ | TP, мс2 | 855,2±99,05 | 1080,9±128,53 | 1244,6±147,26* | 1302,7±157,58* |
| LF, мс2 | 304,3±75,68 | 340,8±81,64 | 392,0±86,07 | 436,2±93,24 | |
| HF, мс2 | 62,9±22,34 | 76,4±28,52 | 97,3±30,61 | 129,5±38,67* | |
| LFn | 82,8±12,1 | 81,6±10,3 | 80,1±11,7 | 77,1±11,3 | |
| HFn | 17,1±7,3 | 18,3±8,5 | 19,8±7,9 | 22,8±8,2 | |
| LF/HF | 4,9±1,8 | 4,5±1,9 | 4,0±1,4 | 2,5±1,1* | |
| ТМЗ | TP, мс2 | 838,7±96,34 | 1295,0±133,16* | 1661,3±172,68*# | 2056,3±201,43*# |
| LF, мс2 | 317,3±63,12 | 378,8±73,36 | 424,7±76,07 | 460,1±87,65* | |
| HF, мс2 | 67,1±20,61 | 111,4±37,47 | 224,3±54,63*# | 287,8±81,46*# | |
| LFn | 82,5±9,9 | 77,2±10,2 | 64,3±9,6 | 61,5±10,1* | |
| HFn | 17,4±7,8 | 22,7±8,3 | 35,6±8,6*# | 38,4±8,9*# | |
| LF/HF | 4,7±1,7 | 3,4±1,5 | 1,8±1,0*# | 1,6±0,9*# | |
| ПНЖК | TP, мс2 | 856,1±98,74 | 1135,9±137,72* | 1442,7±164,27* | 1962,3±214,67*# |
| LF, мс2 | 313,6±63,12 | 363,3±67,64 | 402,4±81,07 | 456,0±92,32* | |
| HF, мс2 | 76,1±19,39 | 103,1±28,86 | 210,5±48,63*# | 251,8±78,46*# | |
| LFn | 82,2±11,4 | 79,6±10,3 | 67,7±10,7 | 65,4±10,1* | |
| HFn | 17,7±9,3 | 20,3±9,8 | 32,2±10,7*# | 34,5±10,8*# | |
| LF/HF | 4,6±1,9 | 3,9±2,2 | 2,1±1,2*# | 1,9±1,0*# |
________________
* –достоверно в сравнении с исходными данными, р<0,05;
# – достоверно в сравнении с контрольной группой, р<0,05;
Среднее значение показателя TP (общей мощности спектра) среди всех групп в первые сутки ИМ было равно 849,7 мс2. Начиная с 15 суток наблюдения, выявлено увеличение мощности спектра во всех группах. В контрольной группе достоверное увеличение мощности происходило, начиная с 3 месяцев наблюдения. В группе триметазидина общая мощность спектра достоверно возросла уже на 15 сутки лечения, по сравнению с 1 сутками, и отмечалось ее дальнейшее увеличение вплоть до окончания исследования (в сроки 3 месяца и 6 месяцев). По сравнению с группой -3 ПНЖК достоверных различий не получено. В группе пациентов получавших -3 ПНЖК отмечено более медленное увеличение спектральной мощности, по сравнению с группой триметазидина, но быстрее, чем в контрольной группе. По сравнению с 1 сутками наблюдения нами выявлено достоверное увеличение показателя уже к 15 суткам, с сохраняющейся положительной динамикой к окончанию исследования, а к 6 месяцам выявлено достоверное увеличение показателя по сравнению с КГ.
При изучении низкочастотного (LF) и высокочастотного (HF) компонентов спектра в первые сутки исследования выявлено значительное снижение этих показателей. В дальнейшем выявлена положительная динамика показателей во всех группах к 6 месяцам наблюдения. С целью минимизации влияния изменений общей мощности спектра на уровень LF и HF компонентов, а также большей наглядности их соотношения выполнена нормализация показателей. При анализе динамики нормализованных показателей во всех группах выявлено постепенное увеличение доли высокочастотного компонента спектра относительно низкочастотного компонента, соответственно и снижение индекса вагосимпатического взаимодействия (соотношения LF/HF) во всех группах. Это говорит о восстановлении баланса двух звеньев вегетативной нервной системы – уменьшении влияния симпатического отдела и усилении влияния вагусной активности. В контрольной группе достоверное изменение показателя LF/HF произошло только к 6 месяцам лечения. В группах с добавлением к основной терапии триметазидина или -3 ПНЖК достоверное изменение показателя, по сравнению с 1 сутками и с контрольной группой, произошло уже к 3 месяцам лечения, с дальнейшей положительной динамикой к 6 месяцам. При сравнении динамики показателя между группами -3 ПНЖК и ТМЗ достоверных различий не выявлено.
Таким образом, при анализе изменений ВСР во всех группах к 6 месяцам отмечалось постепенное увеличение показателей парасимпатической и снижение маркеров симпатической активности по сравнению с исходными данными. Однако, у пациентов получавших в дополнение к основной терапии с 1 суток лечения триметазидин или -3 ПНЖК происходило достоверно более быстрое повышение ВСР, свидетельствующее о увеличении парасимпатического тонуса, играющего защитную роль в возникновении фатальных желудочковых аритмий, над симпатическим по сравнению с исходными данными и результатами контрольной группы.
Влияние терапии триметазидином и -3 ПНЖК на выявляемость поздних потенциалов желудочков у больных ИМ. По результатам многочисленных исследований последних лет наличие поздних потенциалов желудочков у больных ИМ является значимым предиктором внезапной кардиальной смерти. В нашем исследовании количество пациентов, у которых на 1 сутки определялась задержанная электрическая активность, было следующим: всего ППЖ выявлены у 29 из 84 пациентов (35%). К окончанию исследования ППЖ выявлялись у 18 пациентов, что составило 21% от общего количества больных.
Анализируя динамику выявляемости ППЖ к 6 месяцу исследования, нами выявлено умеренное снижение выявляемости в контрольной группе (с 34% до 28%) и группе триметазидина (с 33% до 22%), в группе -3 ПНЖК обнаружено более значительное уменьшение выявляемости (с 36% до 11%). Динамика поздних потенциалов желудочков по показателям в исследуемых группах в течение 6 месяцев после ИМ представлена в таблице 3.
Таблица 3
Динамика показателей поздних потенциалов желудочков в исследуемых группах в течение 6 месяцев после ИМ
| Группы | Показатель | 1 сутки | 15 сутки | 3 мес. | 6 мес. |
| КГ | TQRS | 118,4±11,2 | 121,4±9,3 | 125,2±7,6 | 119,8±8,4 |
| LAS40 | 41,5±6,8 | 43,1±8,6 | 42,8±6,6 | 41,7±5,3 | |
| RMS40 | 16,8±3,2 | 18,3±4,9 | 19,1±4,1 | 20,8±4,2 | |
| ТМЗ | TQRS | 121,1±9,8 | 122,0±8,8 | 122,7±8,3 | 117,3±6,8 |
| LAS40 | 42,1±8,1 | 43,8±10,2 | 40,3±6,9 | 37,6±5,6 | |
| RMS40 | 15,8±4,1 | 17,9±5,8 | 22,4±3,6 | 24,2±3,8* | |
| ПНЖК | TQRS | 120,4±8,2 | 118,2±7,8 | 108,4±5,9*#° | 104,6±6,5*#° |
| LAS40 | 42,3±5,8 | 40,4±5,9 | 36,2±6,4 | 32,9±5,1*# | |
| RMS40 | 16,2±3,4 | 22,2±4,8 | 26,8±4,2*# | 28,5±4,5*# |
*- достоверно в сравнении с исходными данными, р < 0,05.
# - достоверно при сравнении с КГ, р <0,05
° - достоверно при сравнении группы -3 ПНЖК с группой ТМЗ, р <0,05
На 15 сутки лечения достоверных изменений показателей ЭКГ-ВР при сравнении с данными, полученными на 1 сутки ИМ, и с данными между исследуемыми группами не выявлено. В срок 3 месяца в контрольной группе и группе триметазидина достоверных изменений показателей ППЖ не произошло. Однако, в группе -3 ПНЖК в этот же срок выявлено достоверное улучшение показателей TQRS и RMS40 по сравнению с 1 сутками лечения, а также недостоверная тенденция к уменьшению LAS40. Сравнивая показатели ППЖ между группами, установлено достоверное улучшение показателей TQRS и RMS40 в группе -3 ПНЖК по сравнению с контрольной группой, также выявлено достоверное снижение показателя TQRS по сравнению с группой триметазидина. Анализируя динамику показателей ППЖ в срок 6 месяцев, установлено отсутствие достоверных изменений в контрольной группе. В группе триметазидина отмечалось достоверное увеличение показателя RMS40 по сравнению с первыми сутками лечения, по сравнению с контрольной группой достоверных изменений не выявлено. В группе -3 ПНЖК в срок 6 месяцев выявлена достоверная нормализация всех трех показателей по сравнению, как с первыми сутками лечения, так и с контрольной группой, а по показателю TQRS по сравнению с группой ТМЗ.
Таким образом, нами установлено, что в контрольной группе и группе триметазидина не произошло достоверных изменений выявляемости ППЖ. При добавлении к стандартной терапии -3 ПНЖК уже начиная с 3 мес. и с сохранением положительной тенденции к окончанию исследования произошло достоверное снижение выявляемости ППЖ, что может свидетельствовать о воздействии исследуемого препарата на электрофизиологический феномен ППЖ и способствовать снижению риска возникновения фатальных желудочковых аритмий. Динамика показателей ЭКГ-ВР и уменьшение выявляемости ППЖ на фоне приема -3 ПНЖК, свидетельствует о наличии у препарата свойств предупреждения развития аритмий.
Изменение показателей липидного спектра до и после терапии триметазидином и -3 ПНЖК. Влияние применяемых нами лекарственных средств, на липидный состав крови мы оценивали, анализируя уровни общего холестерина (ОХ), липопротеинов низкой плотности (ЛПНП), липопротеинов высокой плотности (ЛПВП) и триглицеридов. Исходно дислипидемия выявлена у большинства пациентов с повышенным уровнем ОХ. На фоне проводимой как стандартной терапии, включающей статины, так и терапии с добавлением ТМЗ или -3 ПНЖК отмечалось достоверное снижение уровня холестерина во всех исследуемых группах, начиная с 3 месяцев с дальнейшей динамикой к 6 месяцам наблюдения.
При анализе динамики ОХ наиболее выраженное достоверное снижение показателя произошло в группе с добавлением -3 ПНЖК. Уже на 15 сутки снижение составило 15,7%, к окончанию исследования 27,9%. Начиная с 3 месяцев и к моменту окончания исследования в группе -3 ПНЖК выявлено достоверно более быстрое снижение показателя по сравнению с КГ и группой ТМЗ. Практически аналогичная картина наблюдалась при анализе уровней ЛПНП, ТГ – достоверное снижение показателей во всех группах с 3 месяцев, с достоверно более быстрой динамикой в группе -3 ПНЖК. Также в группе пациентов, принимавших -3-ПНЖК выявлено достоверное повышение ЛПВП с 3 месяцев наблюдения по сравнению с КГ и группой ТМЗ, на фоне постепенной нормализации показателя во всех исследуемых группах с 3 месяцев лечения, с дальнейшей положительной динамикой к 6 месяцам. Таким образом, нами установлено положительное влияние стандартной терапии, включавшей статины и исследуемые препараты на показатели липидограммы, с наиболее быстрой нормализацией в группе -3-ПНЖК.
ВЫВОДЫ
1. Включение триметазидина и препарата -3 полиненасыщенных жирных кислот в программу терапии пациентов в острый период инфаркта миокарда приводит к улучшению функционального состояния миокарда: на 21 (или к моменту выписки) сутки заболевания параметры теста шестиминутной ходьбы в группах больных оказались (достоверно) лучше, особенно в группе применения триметазидина, с сохраняющейся положительной динамикой к 6 месяцам наблюдения.
2. Включение триметазидина в программу терапии больных после инфаркта миокарда в течение первых 6 месяцев заболевания способствует достоверному улучшению систолической функции миокарда, уменьшению конечного диастолического и конечного систолического объемов левого желудочка, что клинически проявляется меньшим функциональным классом сердечной недостаточности по сравнению с контрольной группой. В то же время применение препарата -3 полиненасыщенных жирных кислот не оказывает такого влияния на параметры систолической функции миокарда.
3. Включение препарата -3 полиненасыщенных жирных кислот в программу терапии больных после инфаркта миокарда в течение первых 6 месяцев заболевания сопровождается достоверным улучшением состояния диастолической функции, что клинически проявляется меньшим функциональным классом сердечной недостаточности по сравнению с контрольной группой. Такого влияния триметазидина на состояние диастолической функции не найдено.
4. Включение триметазидина и -3 полиненасыщенных жирных в программу терапии больных после инфаркта миокарда в течение первых 6 месяцев заболевания, приводит к достоверно более раннему восстановлению вегетативного баланса за счет увеличения парасимпатической активности (достоверно более быстрому восстановлению как временных, так и частотных показателей ВСР), начиная с 3 го и до 6 месяцев лечения, по сравнению с контрольной группой.
5. Включение -3 полиненасыщенных жирных в программу терапии больных после инфаркта миокарда в течение первых 6 месяцев, приводит к достоверному снижению выявляемости ППЖ, начиная с 3 месяцев лечения, по сравнению, как с контрольной группой, так и с группой триметазидина, что свидетельствует о воздействии препарата на аритмогенный субстрат. Применение триметазидина в дополнение к стандартной терапии не оказывает достоверного влияния на выявляемость ППЖ.
6. Включение -3 полиненасыщенных жирных в программу терапии больных после инфаркта миокарда в течение первых 6 месяцев способствует достоверно более быстрому снижению уровней общего холестерина, ЛПНП, ТГ, и повышению уровня ЛПВП. Применение триметазидина в дополнение к стандартной терапии не оказывает достоверного влияния на показатели липидограммы.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. С целью улучшения течения постинфарктного периода, профилактики ВКС у пациентов с инфарктом миокарда, показано применение препаратов, влияющих на метаболические процессы с 1 суток заболевания.
2. Пациентам, в остром периоде инфаркта миокарда, имеющим сниженную ВСР, нарушение систолической функции миокарда левого желудочка, можно рекомендовать триметазидин в дозе 70 мг/сутки в дополнение к стандартной терапии.
3. Пациентам, имеющим сниженную ВСР, наличие ППЖ, с дислипопротеинемией и с диастолической дисфункцией миокарда левого желудочка можно рекомендовать -3 ПНЖК в дозе 750-900 мг продолжительностью лечения не менее 2-х месяцев, в дополнение к стандартной терапии.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Бельков А.В. Применение метаболического цитопротектора триметазидина у больных с постинфарктным кардиосклерозом и явлениями сердечной недостаточности А.В. Бельков // Вестник СПбГМА им. И.И. Мечникова. – СПб., 2003. – № 1 (4) (Приложение). – С. 34.
- Бельков А.В. Клинико-прогностическое значение применения триметазидина у больных инфарктом миокарда / А.В. Бельков, И.В. Архаров, А.С. Руссин // Актуальные вопросы внутренних болезней : сб. научных трудов. – СПб.: СПбГМА им. И.И.Мечникова, 2005. – С. 32-34.
- Бельков А.В. Применение клопидогреля в дополнение к стандартной терапии острого инфаркта миокарда с подъемом сегмента ST. А.С. Руссин, И.В. Архаров, А.В. Бельков // Актуальные вопросы внутренних болезней : сб. научных трудов. – СПб.: СПбГМА им. И.И.Мечникова, 2005. – С. 48-49.
- Бельков А.В. Оптимизация оказания медицинской помощи пациентам с острым инфарктом миокарда в условиях мегаполиса. / А.В. Бельков, А.С. Руссин, А.В Яцкевич, Е.Б. Вострикова, Ф.Б. Исаков // Донозология-2005. Экологические и медицинские проблемы возникновения донозологических и патологических состояний в условиях мегаполисов : материалы Первой международной научной конференции. (СПб, 9-10 июня 2005). – СПб., 2005. – С. 236-238.
- Бельков А.В. Предикторы возникновения рецидивирующих расстройств коронарного кровотока у больных инфарктом миокарда после тромболизиса / А.В. Бельков, А.С. Руссин // Человек и его здоровье – 2005 : материалы науч.-практ. конф. сотрудников и студентов СПбГМА им. И.И. Мечникова. – СПб., 2005. – С. 27-28.
- Бельков А.В. Проблема метаболической цитопротекции в остром периоде ОИМ / А.С. Руссин, И.В. Архаров, А.В. Бельков, В.В. Елтищева, Н.Г. Марова // Человек и его здоровье – 2005 : материалы науч.-практ. конф. сотрудников и студентов СПбГМА им. И.И. Мечникова. – СПб., 2005. – С. 232-233.
- Бельков А.В. Влияние триметазидина на предикторы внезапной смерти / А.В. Бельков, А.С. Руссин, Н.Г. Марова, Е.Б. Вострикова // Вестник аритмологии. – 2006. – Приложение А : тезисы докл. VII междунар. славянского конгресса по электростимуляции и клинической электрофизиологии сердца «Кардиостим – 2006». – СПб., 2006. – С. 132.
- Бельков А.В. Влияние метаболической терапии на реперфузионные нарушения ритма / А.С. Руссин, А.В. Бельков, Н.Г. Марова, Е.Б. Вострикова // Вестник аритмологии. – 2006. – Приложение А : тезисы докл. VII междунар. славянского конгресса по электростимуляции и клинической электрофизиологии сердца «Кардиостим – 2006». – СПб., 2006. – С. 158.
- Бельков А.В. Клинико-прогностическое значение метаболической терапии у больных инфарктом миокарда // А.В. Бельков, А.С. Руссин, М.И. Садикью, М.Г. Колесниченко, А.Т. Бурбелло // Профилактическая и клиническая медицина. – СПб., 2010. – № 2 – С. 82-84.
- Бельков А.В. Влияние терапии метаболическими препаратами на некоторые предикторы внезапной смерти у больных инфарктом миокарда / А.В. Бельков, А.С. Руссин, М.Г. Колесниченко // Профилактическая и клиническая медицина. – СПб., 2011 – № 1 (38). – С. 287.

