Состояние овариального резерва при некоторых формах бесплодия
На правах рукописи
ЖОРДАНИДЗЕ
ДИАНА ОМАРОВНА
СОСТОЯНИЕ ОВАРИАЛЬНОГО РЕЗЕРВА ПРИ НЕКОТОРЫХ ФОРМАХ БЕСПЛОДИЯ
14.01.01 – Акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2011
Работа выполнена на кафедре акушерства, гинекологии, перинатологии и репродуктологии факультета послевузовского профессионального образования врачей ГОУ ВПО «Первый Московский Государственный Медицинский Университет им. И.М. Сеченова».
Научные руководители:
доктор медицинских наук, профессор НАЗАРЕНКО Татьяна Алексеевна
доктор биологических наук, профессор ФАНЧЕНКО Николай Дмитриевич
Официальные оппоненты:
доктор медицинских наук, профессор САМОЙЛОВА Татьяна Евгеньевна
доктор медицинских наук, профессор КАЛИНИНА Елена Андреевна
Ведущая организация: ГОУ ВПО «Московский государственный медико-стоматологический университет Росздрава»
Защита состоится «_____» ________2011 г., в ________ ч. на заседании диссертационного совета Д 208.048.01 при ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» (101000, Москва, ул. Покровка, д. 22а).
С диссертацией можно ознакомиться в библиотеке ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии».
Автореферат разослан «____» __________2011г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор ЗАЙДИЕВА Я.З.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
В последние десять лет широко обсуждается понятие «овариального резерва» и его значение для выбора методов лечения бесплодия у женщин. Несмотря на значительное количество работ, до сих пор не установлена диагностическая ценность отдельных параметров в определении функционального состояния яичников при различных формах бесплодия. Ранее использовался термин «фолликулярный пул», определяя его количеством примордиальных фолликулов в яичниках (Боярский К.Ю. 2000). Однако вряд ли такое определение можно считать информативным, так как неинвазивными методами исследования невозможно определить число примордиальных и функциональную полноценность растущих фолликулов. Скорее всего, овариальный резерв определяет функциональное состояние репродуктивной системы, полноценность которой обеспечивает рост, развитие фолликула, созревание ооцита в доминантном фолликуле, овуляцию и оплодотворение полноценной яйцеклетки (Назаренко Т.А., Мишиева Н.Г. 2005). Применительно к методам стимуляции яичника полноценный овариальный резерв обеспечивает адекватный ответ яичника на введение индукторов (Onagawa T. 2004; Steiner A.Z. 2006).
Диагностическая значимость тех или иных тестов, определяющих состояние овариального резерва, достаточно подробно освещена в литературе. Вместе с тем, представлено множество диагностических тестов для определения относительно простой клинической ситуации – ответит ли яичник на введение индукторов и какой характер ответа можно прогнозировать (Smotrich D., 1996; Galtier-Dereure F. et al., 1996; Van Rooij I.A. et al., 2004; Partridge A.H., 2010).
Считается актуальным вопрос о выборе наиболее значимых маркеров для оценки овариального резерва. Определение одного из параметров может дать ложный результат, но совокупность всех показателей, как правило, точно характеризует состояние овариального резерва.
Несомненно, что состояние овариального резерва, отражающее прогностический потенциал женщины, во многом определяет успех лечения бесплодия. Бесспорна зависимость резерва от возраста пациентки и произведенной резекции яичников (Корсак В.С., 1996; Мишиева Н.Г., 2008; Боярский К.Ю., 2009). Вместе с тем, влияние других многочисленных факторов: генетических, аутоиммунных, факторов внешней среды, ожирения, образа жизни, вредных привычек, продолжает интенсивно изучаться. В этой связи внимание исследователей привлекает оценка состояния овариального резерва при СПКЯ, что дает возможность не только прогнозировать успех восстановления репродуктивной функции, но и уточнить патогенетические механизмы формирования и течения этого заболевания. Не менее интересным является изучение состояния овариального резерва при необъяснимом бесплодии и малых формах наружного генитального эндометриоза, когда явная причина инфертильности не установлена. Подобные исследования не достаточно полно представлены в литературе, что обуславливает актуальность исследований в этой области. Предполагается, что оценка состояния овариального резерва позволит не только прогнозировать адекватность и эффективность используемого метода индукции овуляции и, в конечном итоге, оптимизировать тактику лечения бесплодия, но и приблизиться к пониманию патогенетических механизмов формирования синдрома поликистозных яичников (СПКЯ), бесплодия при наружном генитальном эндометриозе (НГЭ), и, возможно, уточнить причины бесплодия неясного генеза.
Вышеизложенное определило цель настоящего исследования: изучить состояние овариального резерва при различных формах функционального бесплодия и оценить его влияние на параметры фолликуло- и оогенеза в программах ЭКО.
Задачи исследования
1. Провести сравнительный анализ параметров овариального резерва у женщин с бесплодием, обусловленным СПКЯ, эндометриозом (малые формы) и идиопатическим бесплодием.
2. Оценить эффективность оперативного лечения СПКЯ и гормонального лечения аГнРГ малых форм наружного генитального эндометриоза у пациенток с бесплодием.
3. Определить особенности ответа яичников на введение индукторов овуляции, количество и качество ооцитов и эмбрионов при указанных формах бесплодия.
4. Исследовать динамику гормональных параметров периферической крови в индуцированном цикле в зависимости от исходного состояния овариального резерва и характера фолликулогенеза.
5. Исследовать гормональный состав фолликулярной жидкости и провести сравнение полученных данных со значениями уровней гормонов в периферической крови, характером фолликуло-, оо- и эмбриогенеза.
6. На основании обобщения полученных данных усовершенствовать тактику ведения пациенток с функциональным бесплодием, базирующуюся на оценке состояния их овариального резерва.
Научная новизна
В работе впервые проведена сравнительная оценка состояния овариального резерва у женщин с различными формами бесплодия: СПКЯ, малыми формами наружного генитального эндометриоза и идиопатическим бесплодием. Показано различное состояния овариального резерва у указанных групп пациенток, обуславливающее тактику достижения беременности и прогнозирующее ответ яичников на гонадотропную стимуляцию в программе ЭКО. Установлено, что уровень АМГ может прогнозировать успех хирургического лечения бесплодия при СПКЯ. Доказана нецелесообразность использования аГнРГ у пациенток с бесплодием, ассоциированным с малыми формами наружного генитального эндометриоза.
Выявлено, что уровни половых стероидов в фолликулярной жидкости не коррелируют с числом и качеством полученных ооцитов в программе ЭКО, что ставит под сомнение целесообразность исследования внутрифолликулярного окружения ооцита.
Преовуляторное снижение уровня АМГ в индуцированном цикле говорит о возможном рекрутировании дополнительного пула малых антральных фолликулов.
Практическая значимость
Для клинической практики предложен диагностико-лечебный алгоритм, определяющий тактику ведения больных с бесплодием, обусловленным СПКЯ, малыми формами наружного генитального эндометриоза и неустановленного генеза. Определены группы пациенток, у которых возможно восстановить естественную фертильность оперативными и консервативными методами лечения, выделены и охарактеризованы больные, у которых целесообразно проводить программу ЭКО уже на первых этапах лечения бесплодия. Установлены клинико–лабораторные характеристики пациенток с СПКЯ, которым целесообразно проводить хирургическое лечение с целью достижения беременности, при этом снижение уровня АМГ в 2 и более раза по сравнению с исходными значениями может прогнозировать эффективность проведенного вмешательства. Доказана нецелесообразность назначения аГнРГ в послеоперационном периоде пациенткам с бесплодием и малыми формами наружного генитального эндометриоза. Уточнены принципы стимуляции яичников при исследуемых формах бесплодия, которые обеспечивают оптимальные условия оо- и эмбриогенеза.
Положения, выносимые на защиту:
1. Состояние овариального резерва у пациенток с функциональным бесплодием определяет особенности планирования лечебных мероприятий, направленных на достижение беременности. Тактика, предполагающая восстановление естественной фертильности, может быть эффективной лишь у пациенток молодого возраста с хорошими показателями овариального резерва.
2. Хирургическое лечение бесплодия при СПКЯ показано пациенткам, имеющим определенные клинико-лабораторные показатели (молодой возраст, большой объем яичников с наличием симптома «ожерелья», неадекватный ответ при назначении индукторов овуляции), критерием эффективности проведенной операции может служить снижение уровня АМГ в 2 и более раза по сравнению с исходным. При бесплодии, ассоциированном с малыми формами наружного генитального эндометриоза, без клинических проявлений заболевания, назначение аГнРГ в послеоперационном периоде не повышает частоты наступления беременности.
3. Выбор протокола стимуляции функции яичников при проведении программы ЭКО должен базироваться на оценке состояния овариального резерва и обеспечивать рост от 8 до 15 фолликулов, при этом потери оо- и эмбриогенеза минимальны.
4. Уровни половых гормонов в фолликулярной жидкости не отражают параметры фолликуло- и оогенеза и не могут служить маркерами числа и качества полученных ооцитов, уровень АМГ в периферической крови и фолликулярной жидкости прямо пропорционально коррелирует с числом преовуляторных фолликулов, полученных ооцитов и объективно отражает состояние овариального резерва. Двукратное снижение уровня АМГ в периферической крови в преовуляторном периоде стимулированного цикла по сравнению с исходным значением может свидетельствовать о рекрутировании дополнительного пула малых антральных фолликулов.
Апробация работы
Апробация диссертации была проведена на заседании кафедры акушерства, гинекологии, перинатологии и репродуктологии ФППО врачей ГОУ ВПО «Первый Московский Государственный Медицинский Университет им. И.М. Сеченова» от 28 декабря 2010 г.
Внедрение результатов работы в практику
Результаты исследования внедрены в клиническую практику отделения сохранения и восстановления репродуктивной функции ФГУ «НЦ АГ и П им. академика В.И. Кулакова» Минздравсоцразвития России. Материалы работы используются для практических занятий и лекций со слушателями семинаров ФГУ «НЦ АГ и П им. академика В.И. Кулакова» Минздравсоцразвития России, аспирантами и клиническими ординаторами. По теме диссертации опубликовано 8 научных работ, из них 2 — по перечню ВАК РФ.
Структура и объем диссертации
Диссертация состоит из введения, 5 глав, выводов, практических рекомендаций и списка литературы. Работа изложена на 144 страницах машинописного текста, содержит 18 таблиц. Библиографический указатель содержит 129 источников, из них 55 отечественных и 74 иностранных авторов.
СОДЕРЖАНИЕ РАБОТЫ
Материал и методы исследования
Для выполнения цели исследования и поставленных задач проведено комплексное клинико–лабораторное обследование 132 женщин с различными формами функционального бесплодия, поступивших в отделение сохранения и восстановления репродуктивной функции ФГУ «НЦ АГиП им. В.И. Кулакова» Минздравсоцразвития России в период с 2006 по 2010 гг.
1-ю группу исследования составили 54 пациентки с СПКЯ в возрасте от 22 до 37 лет (средний возраст 28,8±3,4 лет); диагноз установлен на основании общепринятых критериев Роттердамского консенсуса (2003 г.).
2-ю группу исследования составили 52 женщины в возрасте от 24 до 37 лет (средний возраст 32,5±3,6 лет), с малыми формами наружного генитального эндометриоза, установленного эндоскопическим методом при отсутствии другой патологии репродуктивной системы.
3-ю группу исследования составили 26 женщин в возрасте от 25 до 37 лет (средний возраст 29,8±2,6 лет), с идиопатическим бесплодием, при котором на фоне сохранения всех функций репродуктивной системы беременность не наступала в течение 1 года и более регулярной половой жизни без предохранения.
Группу сравнения составили 38 пациенток в возрасте от 20 до 34 лет (средний возраст 31,8±3,7 лет), имеющие трубно–перитонеальную форму бесплодия, регулярный овуляторный менструальный цикл и фертильную сперму мужа. Эти женщины перенесли 1 лапароскопическую операцию на маточных трубах без резекции яичников.
Всем женщинам, вошедшим в исследование, проведены следующие методы обследования:
I. Общеклинические: сбор анамнеза, общий и гинекологический осмотры.
II. Оценивали состояние овариального резерва общепринятыми методами исследования: гормональное обследование включало определение в сыворотке крови уровней лютеинизирующего гормона (ЛГ), фолликулостимулирующего гормона (ФСГ), антимюллерового гормона (АМГ), эстрадиола (Е2); ультразвуковое исследование объема яичников и количества антральных фолликулов в них.
III. Лапароскопия и гистероскопия в необходимом лечебном объеме: электрокоагуляция очагов НГЭ, электрокаутеризация яичников при СПКЯ.
IV. Стимуляция функции яичников в программах ВРТ: контролируемая индукция овуляции, программа ЭКО.
V. Оценка качества ооцитов и эмбрионов по существующим международным критериям.
В работе были применены следующие статистические методы обработки данных: критерий Шапиро–Уилка для проверки на нормальность распределений; критерий 2 для таблиц сопряженности признаков 2*2 и 2*4 в том числе с использованием поправки; однофакторный дисперсионный анализ; сравнительный анализ переменных с помощью непараметрического критерия Вилкоксона–Манна–Уитни для несвязанных совокупностей; сравнительный анализ средних тенденций с помощью Т–критерия Стьюдента для несвязанных совокупностей; ранговый корреляционный анализ Спирмена. Для автоматизации статистической обработки использовали статистический пакет «Statistica for Windows 6.0».
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
При исследовании состояния яичников у женщин с СПКЯ установлено значительное повышение всех показателей овариального резерва. У всех пациенток данной группы объем яичников и количество антральных фолликулов в них был значительно большим, чем в других группах исследования и группе сравнения. Уровень АМГ периферической крови также оказался достоверно выше в этой группе и составил 4,5±2,3 нг/мл. Средний уровень ЛГ у пациенток с СПКЯ составил 10,2±4,7 МЕ/л, что было выше, чем в других группах исследования и группе сравнения.
На первом этапе лечения бесплодия 30 женщинам с СПКЯ, требующим коррекции метаболического синдрома или проявления клинических и/или биохимических симптомов гиперандрогении, проведена соответствующая терапия метформином и антиандрогенными препаратами. Через 3–4 месяца лечения оценивали характер менструального цикла и овуляторную функцию. У 6 пациенток после проведенного лечения произошла нормализация менструального цикла, у 3–х (10%) из них спонтанно наступила беременность. Очевидно, что нормализация метаболических нарушений и проявлений гиперандрогении является необходимым этапом при лечении бесплодия у пациенток с СПКЯ. И хотя после проведения первого этапа лечения частота наступления беременности оказалась невысокой (10%), предварительная подготовка положительно сказалась на последующем лечении бесплодия у этих пациенток.
После проведения подготовительного лечения у 88,9% (n=48) женщин были проведены циклы контролируемой индукции овуляции с внутриматочной инсеминацией спермой мужа или без нее. Стимуляцию проводили с использованием КЦ с малыми дозами рФСГ или без него в течение 2–4 циклов, у части пациенток использовали только рФСГ. СГЯ развился у 15 пациенток, что составило 31,2%. Данный метод лечения бесплодия у пациенток с СПКЯ привел к наступлению беременности всего у 14,5% (n=7) больных, что значительно ниже представленных в литературе данных – эффективность данного метода лечения по мнению некоторых авторов достигает 50 % (Чеботникова Т.В., Холодова Ж.Л., 2008).
В нашем исследовании из числа пациенток, у которых беременность не наступила в течение 2–4 циклов стимуляции яичников, была выделена группа из 20 женщин для проведения хирургического лечения СПКЯ. Лапароскопическим доступом проводили щадящую электрокаутеризацию яичников. Хирургическое лечение проводили женщинам моложе 30 лет с ИМТ менее 25 кг/м, показателем ЛГ выше 10 МЕ/л, с объемом яичников более 15 см и расположением фолликулов в виде ожерелья. Кроме того, у части пациенток (15 женщин) при проведении стимуляции развился СГЯ средней и тяжелой степени. Всем этим женщинам после хирургического лечения проведена оценка восстановления овуляции и уровень АМГ. Из них у 30% (n=6) пациенток уровень АМГ снизился вдвое по сравнению с исходными цифрами (6,6 и 3,4 нг/мл соответственно), на фоне чего произошло восстановление овуляторного менструального цикла, а у 37% наступила беременность. Результаты проведенных наблюдений показали, что восстановление ритма менструаций, овуляция и последующая беременность имели место лишь у тех пациенток, у которых произошло снижение уровня АМГ после операции в 2 и более раза. Таким образом, уровень АМГ является маркером, прогнозирующим эффективность проведенной операции. Пациентки с СПКЯ у которых консервативное и хирургическое лечение бесплодия оказалось эффективным 24% (n=13), по ряду параметров отличались от женщин с неэффективным лечением бесплодия – 76% (n=41). Длительность бесплодия у женщин с положительным исходом лечения составила 3,9±0,8 лет, а у пациенток с отрицательным исходом – 6±2,1 лет. Инсулинрезистентность зарегистрирована у 20% пациенток с положительным исходом лечения и у 46% женщин с отрицательным результатом. Уровень ЛГ был также достоверно ниже в группе забеременевших пациенток. В таблице 1 представлена характеристика пациенток с положительным и отрицательным результатом лечения бесплодия.
Таблица 1.
Сравнительная характеристика пациенток с СПКЯ с положительным и отрицательным исходом лечения бесплодия
| Положительный исход лечения бесплодия (n= 13) | Отрицательный исход лечения бесплодия (n=41) | |
| Возраст, лет | 26,7±1,8* | 29,3±3,4 |
| Длительность бесплодия | 3,9±0,8* | 6±2,1 |
| ИМТ, кг/м | 22,1±3,8* | 25,7±3,8 |
| Уровень, АМГ нг/мл | 5,8±4,1 | 4,2±1,6 |
| Уровень, ЛГ МЕ/л | 9,5±4,8* | 11,2±5,2 |
| Объем яичников, см | 16±5,8* | 18,1±5,6 |
| Число антральных фолликулов | 13,7±2,7 | 13,3±2,7 |
| Уровень Т, нмоль/л | 2,5±1,2 | 2,3±0,9 |
| Уровень ДГА-С, мкмоль/л | 5,7±2,2 | 4,3±3,4 |
| Инсулинорезистентность | 20% | 46% |
*р<0,05 – достоверные различия между группами.
Таким образом, указанные признаки могут служить критериями отбора женщин с СПКЯ для различных методов лечения бесплодия и выделения группы, которой целесообразно использовать методы вспомогательной репродукции уже на первом этапе лечения – это женщины старшего возраста, с длительным бесплодием, ожирением, инсулинрезистентностью, высоким уровнем ЛГ.
В нашем исследовании показатели овариального резерва у пациенток с НГЭ I–II степени распространения находились в пределах нормы, но имелась тенденция к их снижению по сравнению с овариальным резервом пациенток группы сравнения. Уровень ФСГ при НГЭ в среднем был 9,5±2,3 МЕ/л, а при трубно–перитонеальном бесплодии – 8,1±2,5 МЕ/л. Уровень АМГ оказался ниже в группе с НГЭ по сравнению с трубно–перитонеальным фактором бесплодия – 1,6±0,7 и 1,9±0,7 нг/мл, соответственно. По данным УЗИ объем яичников при НГЭ составил 6,43±2,3см, число антральных фолликулов – 6,1±1,7, а при трубно–перитонеальном бесплодии объем яичников составил в среднем 7,9±3,8 см, число антральных фолликулов – 6,9±2,8. Следовательно, результаты данного сравнения показали тенденцию к снижению овариального резерва при малых формах эндометриоза.
Первым этапом терапии бесплодия у пациенток с НГЭ было хирургическое, при котором проводили электрокоагуляцию очагов эндометриоза. После проведения лапароскопии лечение эндометриоза препаратами аГнРГ получали 34,6% женщин (n=18). Лечение проводили депо-формами препаратов аГнРг в течении 2–3 месяцев. Лечение эндометриоза препаратами аГнРГ не проводилось у 65,4% женщин (n=34).
Через 6–8 месяцев после проведенного хирургического лечения или последней инъекции препарата аГнРГ, все женщины были обследованы и оценено состояние их репродуктивной функции. Беременность наступила у 4 женщин, из них у 3х – после лапароскопической коагуляции очагов эндометриоза, у 1 пациентки после лечения препаратами аГнРГ, всего 7,7% забеременевших от общей группы больных. Следует отметить, что в нашем исследовании не было различий по частоте наступления беременности между получавшими и не получавшими лечение препаратами аГнРГ после операции (5,5% и 7,9%, соответственно). Судя по полученным результатам, целесообразность лечения эндометриоза I–II степени распространения препаратами аГнРГ ставится под сомнение, так как различий по частоте наступления беременности найдено не было.
В группе пациенток с НГЭ с целью достижения беременности 31 женщине была проведена стимуляция функции яичников в цикле контролируемой индукции овуляции с внутриматочной инсеминацией спермой мужа или без нее. Стимуляцию яичников проводили с использованием КЦ с малыми дозами рФСГ или только рФСГ в течение 2–3 циклов. Доза препарата на цикл лечения составила 500–1300 МЕ. Беременность наступила у 16,1 % женщин (n=5). СГЯ не развился ни у одной женщины с НГЭ. Всего забеременели до момента ЭКО в группе с НГЭ 9 женщин, что составило 17,3%. Беременность наступила у пациенток более молодого возраста (30±3 и 33±3,4 лет, соответственно), с недлительным анамнезом бесплодия. Более того, показатели овариального резерва у них оказались выше и были сопоставимы с таковыми у женщин с трубно–перитонеальным бесплодием.
При оценке состояния овариального резерва у пациенток с идиопатическим бесплодием были найдены некоторые различия с группой сравнения. Так, уровень ФСГ в группе с бесплодием неясного генеза составил в среднем 6,8±2,1МЕ/л, а в группе сравнения – 8,1±2,5МЕ/л, уровень АМГ оказался 2,7±1,4 нг/мл и 1,9±0,7 нг/мл в группе сравнения. Вероятно, различия в уровнях гормонов ФСГ и АМГ связана с разницей в возрасте пациенток этих групп (29,8±2,6 и 31,8±3,7 лет, соответственно). Уровни ЛГ и Е2 в группе с бесплодием неясного генеза и группе сравнения не различались. У всех пациенток данной группы показатели гормонов крови были в норме.
С целью достижения беременности 23 женщинам этой группы была проведена стимуляция функции яичников с внутриматочной инсеминацией спермы мужа или без нее. Стимуляцию яичников проводили с использованием КЦ с добавлением рФСГ или только с рФСГ в течение 2–4 циклов, у всех пациенток был адекватный фолликулогенез. Доза препарата на цикл лечения составила 500-1000 МЕ. СГЯ развился у двух пациенток. В результате беременность наступила у 21,7% (n=5) из них. При сравнении параметров овариального резерва пациенток с бесплодием неясного генеза с положительным и отрицательным результатом лечения различий не было найдено.
При проведении сравнительного анализа показателей овариального резерва пациенток исследуемых групп были выявлены различия по длительности менструального цикла, уровнями ФСГ, АМГ, объемом яичников и количеством антральных фолликулов в них, что представлено на рисунке 1.
 Рис. 1. Сравнительный анализ параметров овариального резерва пациенток исследуемых групп.
Рис. 1. Сравнительный анализ параметров овариального резерва пациенток исследуемых групп.
* достоверно значимые различия с группой сравнения (р<0,05);
** достоверно значимые различия с группой СПКЯ (р<0,05);
*** достоверно значимые различия с группой НГЭ (р<0,05).
Всем пациенткам исследуемых групп с отрицательным результатом предварительного лечения бесплодия с целью достижения беременности было предложено проведение программы ЭКО. Всего в программу ЭКО вступили 98 женщин, из них 41 с СПКЯ, 39 женщин с НГЭ и 18 – с бесплодием неясного генеза. В группе СПКЯ начальная доза вводимого гонадотропина составляла в среднем 190±50,5МЕ, длительность стимуляции составила 10,6±1,6 дней, и доза гонадотропина на курс лечения в программе ЭКО составила 1995±655,5МЕ, что было значительно ниже, чем в группе сравнения. Меньшие дозы вводимого индуктора коррелируют с высокими показателями овариального резерва у этих пациенток и повышенной чувствительностью яичников к экзогенной стимуляции. Более того, в группе СПКЯ даже при минимальной стимуляции яичников по данным УЗ контроля зарегистрировано 27,4±7,2 растущих фолликулов, но размер их чаще был разнокалиберным от 13 до 20 мм. Очевидно, этот факт может указывать на качественную разницу этих фолликулов. При трансвагинальной пункции аспирировано в среднем 25,1±5,9 фолликулов, из которых получено 18,2±7,1 ооцитов, что было достоверно больше, чем в группе сравнения (10,6±7,9 фолликулов, и 9,6±7,4 ооцитов, соответственно). Тем не менее, обращает на себя внимание тот факт, что у пациенток с СПКЯ разница между числом пунктированных фолликулов и полученных ооцитов составила – 28%, а в группе сравнения эта разница составила 10%. Известно, что хорошими показателями принято считать случаи, когда число пунктированных фолликулов и полученных из них ооцитов различаются между собой незначительно, например, при пункции 10 фолликулов получают 8–9 ооцитов. У пациенток с СПКЯ пункция значительного количества фолликулов завершилась получением гораздо меньшего числа ооцитов. Это может быть связано как с техническими сложностями, имеющими место при пункции значительно гиперстимулированного яичника с наличием фолликулов различной величины, так и с возможным феноменом «пустого фолликула». Вероятно, при СПКЯ в рост вступают и малые антральные фолликулы, которые не способны дать полноценный по своему качеству ооцит. После оплодотворения стадии 4–8 бластомеров достигло всего 8,3±4,2 (45,6%) эмбрионов, из них стадии бластоцисты достигли 5,3±2,5 (29,1%) эмбрионов, тогда как в группе сравнения эти показатели составили 64,5% и 42,7% (р<0,05). Следует отметить, что большое количество полученных ооцитов при СПКЯ, не всегда дает соответствующего количества «хороших» эмбрионов. Очевидно, это связанно с низким качеством полученных ооцитов. В группе СПКЯ криоконсервировать в среднем удалось 17% бластоцист из полученного количества эмбрионов после их переноса в полость матки, что было достоверно ниже, чем в группе сравнения – 23%, и свидетельствует о том, что при СПКЯ мы получаем эмбрионы значительно худшего качества, чем при трубно–перитонеальном генезе бесплодия.
В группе с НГЭ в программу ЭКО для достижения беременности вступили 39 пациенток, (75% от общего числа обследуемых женщин этой группы). Начальная доза вводимого рФСГ составила 246±69,2 МЕ в среднем, длительность стимуляции 12±2,1 дней, а суммарная доза индуктора оказалась 2832±943,7 МЕ. Среднее количество индуктора, потраченного для стимуляции яичников, при НГЭ оказалось больше, чем в группе сравнения (2318±888,5 МЕ), и это, скорее всего, связано с тенденцией к снижению овариального резерва при эндометриозе. Произведена трансвагинальная пункция в среднем 9,1±3,1 фолликулов, при которой получено 7,1±4,3 ооцитов, что достоверно не отличается от группы сравнения 10,6±7,9 и 9,6±7,4 соответственно. После оплодотворения стадии 4–8 бластомеров достигли 4,8±2,7 (67,6%) эмбрионов, из них стадии бластоцисты достигли 3,2±2,5 (45%) эмбрионов. Как видно, у пациенток с НГЭ получено гораздо меньше ооцитов, чем при СПКЯ, но эмбрионов высокого качества в процентном соотношении оказалось больше, что еще раз подтверждает факт низкого качества ооцитов и, соответственно, эмбрионов при большом количестве пунктированных фолликулов. Вместе с тем, несмотря на более высокие дозы гонадотропинов, используемых для стимуляции яичников у больных с НГЭ, число растущих, пунктированных фолликулов оказалось гораздо меньше, чем при ТПБ – 10,1±4,1, 9,1±3,1 фолликулов и 12,9±8, 10,6±7,9 соответственно. Среднее количество перенесенных эмбрионов в цикле составило 2,1±0,4. В группе пациенток с НГЭ криоконсервировать в среднем удалось 16% бластоцист из полученного количества эмбрионов, что достоверно меньше, чем в группе сравнения (23%). Это связанно с небольшим количеством полученных эмбрионов.
Из группы пациенток с бесплодием неясного генеза 18 женщинам для достижения беременности была проведена программа ЭКО. Доза рФСГ составила в среднем 187,1±62,2 МЕ в день. Стимуляция яичников проводилась 11,4±2,1 дней, и суммарная доза рФСГ была 2134±648,3 МЕ. Следует отметить, что параметры стимуляции яичников в группе больных с бесплодием неясного генеза не отличались от таковых группы сравнения по показателям расхода препарата в день (187,1±72,2 и 191,5±59,4 МЕ, соответственно) и на цикл стимуляции (2134±648,3 и 2318±888,5 МЕ соответственно).
У пациенток с идиопатическим бесплодием при стимуляции яичников по данным УЗ контроля зарегистрирован рост 12,7±5,4 фолликулов, трансвагинальная пункция произведена 10,8±4,5 фолликулов в среднем, при которой получено 8,1±3,9 ооцитов, что не отличается от группы сравнения: количество растущих фолликулов 12,9±8, аспирировано 10,6±7,9 фолликулов и получено 9,6±7,4 ооцитов. После оплодотворения стадии 4–8 бластомеров достигли 6,6±2,7 (75,3%) эмбрионов, до стадии бластоцисты доросли 4,2±2,1 (51,8%) эмбриона. В среднем произведен перенос 2,2±0,4 эмбрионов. Произведена криоконсервация 27% эмбрионов из полученных. Эти данные также сопоставимы с группой сравнения – до стадии 4–8 бластомеров доросли 6,2±2,2 (64,6%) эмбрионов, 4,1±1,9 (42,7%) бластоцист, и криоконсервировать удалось 23% эмбрионов. Сравнительная характеристика показателей фолликуло-, оо- и эмбриогенеза пациенток исследуемых групп представлена на рисунке 2.
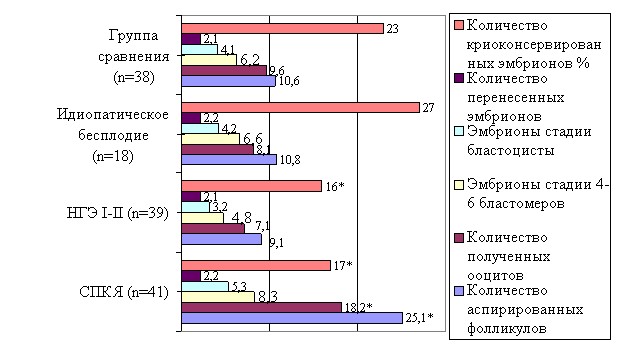
Рис. 2 Сравнительная характеристика фолликуло-, оо- и эмбриогенеза в различных группах исследования и группе сравнения.
* р<0,05 статистически значимые отличия от группы сравнения.
Во всех группах исследования и группе сравнения в программе ЭКО производили оценку гормонального статуса периферической крови и фолликулярной жидкости, полученной при трансвагинальной пункции яичников. В периферической крови пациенток оценивали уровни Е2, П и АМГ в первый день стимуляции, в день введения овуляторной дозы чХГ и в день переноса эмбрионов. Уровень Е2 в периферической крови в цикле стимуляции отражал количество аспирированных фолликулов. Так, при аспирации до 5 фолликулов оказался 3382,4±1314,5 пмоль/л, 5–15 фолликулов – 9342,4±5166,8 пмоль/л и больше 15 фолликулов – 15925,2±3223,4 пмоль/л. Базальный уровень АМГ также оказался выше у пациенток с большим количеством аспирированных фолликулов. В день введения индуктора овуляции уровень АМГ снижался по сравнению с исходным уровнем у больных всех групп исследования и в группе сравнения. Следует отметить, что снижение концентрации АМГ в преовуляторный период у пациенток с большим количеством аспирированных фолликулов оказалось большим, в количественном выражении, чем у женщин, которым была произведена пункция менее 5 фолликулов. При пункции менее 5 фолликулов базальный уровень АМГ был 1,0±0,3 нг/мл, и в день введения индуктора овуляции – 0,5±0,3 нг/мл, 5–15 фолликулов – до начала стимуляции 2,7±1,6 и 1,5±0,8 нг/мл в день введения триггера овуляции, и в случае пункции более 15 фолликулов 3,7±1,3 и 2±0,7 нг/мл соответственно. Вместе с тем, относительно исходных уровней АМГ это снижение оказалось одинаковым (в 2 раза). Вероятно, снижение концентрации АМГ в преовуляторный период связанно с включением в рост малых антральных фолликулов, которые продуцируют АМГ. Следовательно, можно предположить, что снижение концентрации АМГ в преовуляторный период стимулированного цикла может быть связанно с уменьшением фолликулярного пула.
В нашей работе производили исследование гормонов в фолликулярной жидкости, полученной при трансвагинальной пункции яичников в программе ЭКО. В смешанной фолликулярной жидкости, полученной из всех аспирированных фолликулов, мы определяли уровни эстрадиола, прогестерона, АМГ и ингибина В. Уровни эстрадиола и прогестерона были определены также в фолликулярной жидкости отдельных фолликулов. Вместе с исследованием этих гормонов в фолликулярной жидкости учитывали уровни гормонов в периферической крови в цикле стимуляции, количество аспирированных фолликулов, объем полученной фолликулярной жидкости и получение ооцита при аспирации фолликула.
Как оказалось, уровни эстрадиола и прогестерона в фолликулярной жидкости не отражают количества пунктированных фолликулов, т.е. концентрация этих гормонов была одинакова у женщин с пункцией как 5, так и 20 фолликулов. Соответственно уровни этих гормонов не коррелировали с уровнями Е2 и П в периферической крови в цикле стимуляции. Более того, концентрации Е2 и П в фолликулярной жидкости отдельного фолликула соответствовали таковой в жидкости, полученной в результате пункции всех имеющихся фолликулов, уровни Е2 1195251±949889 пмоль/л и П 39794±13098 нмоль/л в отдельной фолликулярной жидкости и Е2 – 904196±104059 пмоль/л, П – 41075±14497 нмоль/л в общей фолликулярной жидкости соответственно.
Объем полученной фолликулярной жидкости также не отражал концентрацию эстрадиола и прогестерона в ней, при объеме жидкости до 1,5 мл уровни Е2 и П составили 1079168±867137 пмоль/л и 37032±16923 нмоль/л, при объеме 1,0-3,0 мл Е2 был 1257771±953194 пмоль/л и П – 39358±12971 нмоль/л, и при объеме фолликулярной жидкости более 3,0 мл Е2 – 1331861±1109342 пмоль/л и П – 37874±10120 нмоль/л. Более того, не было различий в концентрации этих гормонов между фолликулами из которых были получены ооциты и так называемыми «пустыми» фолликулами. При наличии ооцита в фолликуле уровень Е2 1125946±971486 пмоль/л и уровень П – 38376±13473 нмоль/л, в «пустых» фолликулах Е2 – 1472015±954096 пмоль/л и П – 39036±10301 нмоль/л.
Таким образом, можно предположить, что секреция этих гормонов в фолликуле происходит автономно, регулируется внутрифолликулярными факторами, которые, по всей видимости, вырабатываются клетками гранулезы, и именно секреторная активность этих клеток обеспечивает уровень внутрифолликулярного окружения. Следует отметить, что уровни гормонов (Е2 и П) в фолликулярной жидкости были на порядок выше, чем в периферической крови, но совершенно не отражали ни число полученных фолликулов, ни исходное состояние овариального резерва.
Кроме Е2 и П, в ФЖ были определены концентрации АМГ и ингибина В. Концентрация АМГ в ФЖ оказалась достоверно выше у пациенток с большим количеством пунктированных фолликулов. Так, при пункции менее 5 фолликулов уровень АМГ оказался 2,8±1,9 нг/мл, 5–15 фолликулов – 4,6±3,9 нг/мл и при пункции более 15 фолликулов – 4,1±2,9 нг/мл. Обращает на себя внимание то, что при «бедном» ответе яичников (менее 5 фолликулов) уровень АМГ оказался низким, но практически не было различий между умеренным ответом (5–15 фолликулов) и гиперответом (более 15 фолликулов).
Ингибин В был определен только в фолликулярной жидкости, так как его роль в периферической крови достаточно ясна. Оказалось, что концентрация ингибина В также положительно коррелирует с количеством аспирированных фолликулов. Так при СПКЯ, когда было пунктировано больше фолликулов АМГ и ингибин В оказался выше чем при эндометриозе, когда при пункции получали не более 5 фолликулов. При СПКЯ уровни АМГ и ингибина В в фолликулярной жидкости оказались 4,7±3,3 и 18±8,4 нг/мл, а при НГЭ АМГ – 1,8±1,1 нг/мл и ингибин В – 15,5±8,7 нг/мл. Также уровень АМГ в фолликулярной жидкости положительно коррелировал с базальным уровнем этого гормона в периферической крови.
Следовательно, в отличие от эстрадиола и прогестерона, уровни АМГ и ингибина В коррелировали с исходным состоянием овариального резерва, уровнем эстрадиола в периферической крови в преовуляторном периоде, числом фолликулов и ооцитов. Вместе с тем, уровни АМГ и ингибина В в фолликулярной жидкости были достоверно ниже при малом числе (менее 5) пунктированных фолликулов. При пункции 5–15 и более 15 фолликулов достоверных различий в концентрациях этих гормонов не выявлено. Уровни гормонов периферической крови и ФЖ в цикле стимуляции представлены в таблице 2.
Таблица 2. Уровни гормонов в периферической крови и фолликулярной жидкости в цикле стимуляции
| Количество аспирированных фолликулов | <5 фолликулов | 5–15 фолликулов | >15 фолликулов |
| Периферическая кровь | 3382,4±1314,5* ** | 9342,4±5166,8 | 15925,2±3223,4 |
| Уровень Е2, пмоль/л в день введения индуктора овуляции | |||
| Уровень П, нмоль/л в день переноса эмбрионов в полость матки | 189,5±123,7 | 300±167,4 | 262,6±143,6 |
| Базальный уровень АМГ, нг/мл | 1,0±0,3* ** | 2,7±1,6 | 3,7±1,3 |
| Фолликулярная жидкость | 810761±82575 | 1091274±133460 | 810554±96144 |
| Эстрадиол, пмоль/л | |||
| Прогестерон, нмоль/л | 40069±13766 | 42686±15411 | 40471±14315 |
| АМГ, нг/мл | 2,8±1,9 * ** | 4,6±3,9 | 4,1±2,9 |
| Ингибин В, нг/мл | 11,4±8 * ** | 19,4±9,1 | 17,4±8,9 |
*р<0,05 достоверные различия с группой 5–15 фолликулов; **р<0,05 достоверные различия с группой >15 фолликулов.
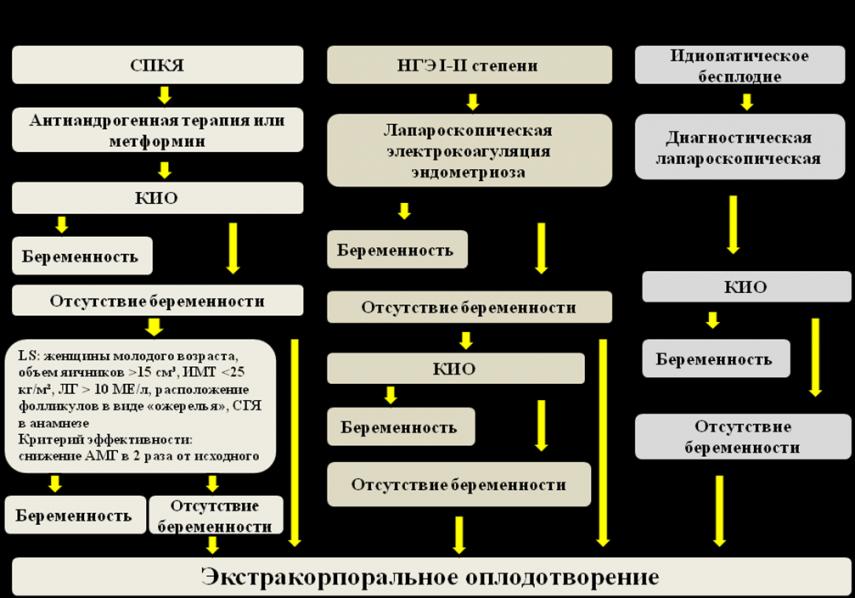
Несмотря на детальное исследование уровней гормонов в фолликулярной жидкости, сравнения с множеством факторов (концентрация в периферической крови, количество пунктированных фолликулов, объем фолликулярной жидкости, наличие ооцита в аспирированном фолликуле), нам не удалось выяснить значимость этих исследований. Это не привело к уточнению прогноза проводимой программы ЭКО. Выявленные изменения концентраций АМГ в процессе индуцированного цикла как в периферической крови, так и в фолликулярной жидкости, представляются интересными и могут явится поводом для дальнейших исследований роли АМГ в прогнозе исхода программ ВРТ. Таким образом, состояние овариального резерва определяет ответ яичников на экзогенную стимуляцию и прогнозирует степень гиперстимуляции яичников. Вместе с тем, высокие параметры овариального резерва не всегда гарантируют их адекватный ответ на экзогенную стимуляцию, а наоборот, сопровождаются выраженной гиперстимуляцией и большими потерями в процессе фолликуло-, оо- эмбриогенеза. Эта ситуация в полном объеме имеет место у пациенток с СПКЯ, что диктует необходимость выбора другой тактики подготовительного и основного лечения, направленного как на снижение сверхвысоких параметров яичников, так на использование модифицированных схем стимуляции. Пациентки с НГЭ имеют тенденцию к сниженным показателям овариального резерва, что отчетливо проявляется при проведении стимуляции яичников – большие дозы экзогенных гонадотропинов приводят к весьма бедному ответу яичников и сниженным показателям эмбриогенеза. Это делает обоснованными рекомендации как можно более раннего использования программ ВРТ у этого контингента больных. Полученные данные позволили разработать алгоритм ведения пациенток с функциональным бесплодием.
ВЫВОДЫ
1. При функциональном бесплодии состояние овариального резерва у женщин, сопоставимых по возрасту, различно; нормальные показатели имеют пациентки с бесплодием неясного генеза, повышенные – женщины с СПКЯ, а при наличии малых форм наружного генитального эндометриоза имеется тенденция к снижению параметров овариального резерва.
2. Состояние овариального резерва определяет реакцию яичников на стимуляцию экзогенными гонадотропинами; гиперстимуляция яичников, сопряженная с высокими показателями овариального резерва и характеризующаяся ростом более 20 фолликулов, сопровождается выраженными потерями на этапах оо–эмбриогенеза (до 30%), вследствие плохого качества ооцитов и эмбрионов; при сниженных показателях овариального резерва и росте не более 4 фолликулов, потери ооцитов и эмбрионов достигают 27%.
3. Эффективность лечения, направленного на восстановление естественной фертильности с применением консервативных и хирургических методов, при СПКЯ составляет 24%, при малых формах НГЭ – 17,3 %, при бесплодии неясного генеза – 21,7%. Беременность чаще наступает у женщин молодого возраста с длительностью бесплодия не более 4 лет и нормальными показателями овариального резерва.
4. Хирургическое лечение бесплодия при СПКЯ эффективно (37% беременности) у пациенток молодого возраста, с ИМТ менее 25 кг/м, ЛГ выше 10 МЕ/л, объемом яичников более 15см, расположением фолликулов в виде ожерелья и с синдромом гиперстимуляции яичников в анамнезе. Критерием эффективности проведенной операции является снижение уровня АМГ в 2 и более раза от исходного.
5. Послеоперационное назначение аГнРГ при малых формах наружного генитального эндометриоза не повышает частоту наступления беременности – 5,5 и 7,9% соответственно.
6. Оптимальными являются параметры фолликуло-, оо- и эмбриогенеза при росте не менее 8 и не более 15 фолликулов, при этом число полученных ооцитов составляет 86% от числа пунктированных фолликулов, эмбрионов 3-го дня на стадии 8 бластомеров – 71%, на стадии бластоцисты 50%, при переносе 2-х эмбрионов 25% от оставшихся, пригодны для криоконсервации. Указанные параметры характерны для пациенток, имеющих нормальные показатели овариального резерва.
7. Уровень эстрадиола в периферической крови коррелирует с числом преовуляторных фолликулов и полученных ооцитов, но значения Е2 и П в фолликулярной жидкости не имеют корреляции с периферической кровью, не зависят от числа полученных ооцитов, не отличаются при исследовании в общей фолликулярной жидкости и в жидкости каждого фолликула, и не могут объективно отражать число и качество полученных ооцитов.
8. Уровень АМГ снижается в преовуляторный период индуцированного цикла по сравнению с исходным в 1,5 и более раз. Базальный уровень АМГ прямо пропорционально коррелирует с числом полученных ооцитов, концентрация АМГ в фолликулярной жидкости значительно ниже при получении малого числа ооцитов (менее 5), но нет достоверных различий в уровнях АМГ при получении 5–15 и более 15 ооцитов.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. При определении тактики лечения бесплодия у пациенток с функциональным бесплодием необходимо учитывать возраст, длительность бесплодия и состояние овариального резерва. Лечение методами, направленными на восстановление естественной фертильности, может быть эффективно лишь у женщин молодого возраста с хорошими показателями овариального резерва. Длительность такого лечения до момента проведения ЭКО не должно превышать 6–8 месяцев.
2. Хирургическое лечение бесплодия у женщин с СПКЯ целесообразно проводить в случае молодого возраста, отсутствия ожирения, наличия увеличенного объема яичников с симптомом «ожерелья», неадекватной реакцией на стимуляцию. При снижении АМГ после операции в 2 и более раза, по сравнению с исходным значением целесообразно проводить мониторирование собственного цикла, т.к. вероятность восстановления овуляции и наступления беременности высока. Если уровень АМГ не уменьшился, рекомендуется после операции проводить стимуляцию яичников.
3. При бесплодии, ассоциированном с малыми формами НГЭ, без клинических проявлений эндометриоза, назначение в послеоперационном периоде аГнРГ нецелесообразно. Необходимо использовать период в 6 месяцев для наступления спонтанной или стимулированной беременности. При отсутствии беременности в течение этого периода целесообразно приступить к программе ЭКО.
4. При проведении программы ЭКО у пациенток с функциональным бесплодием схему стимуляции яичников целесообразно подбирать в соответствии с показателями овариального резерва, при этом стремясь получить не более 15 но и не менее 8 преовуляторных фолликулов.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1. Кикнадзе Д.О., Абубакиров А.Н., Назаренко Т.А., Кирмасова А.В. Состояние овариального резерва при различных формах эндометриоза // Материалы 9-го Всероссийского научного форума «Мать и дитя».— М., 2007. — С.35.
2. Назаренко Т.А., Мишиева Н.Г., Абубакиров А.Н., Жорданидзе Д.О. Овариальный резерв в прогнозе лечения бесплодия // Материалы 2-го международного конгресса по репродуктивной медицине «Репродуктивное здоровье семьи». – М., 2008. – С.342–343.
3. Жорданидзе Д.О., Назаренко Т.А., Кондриков Н.И., Мишиева Н.Г. Состояние овариального резерва при некоторых формах бесплодия // Материалы 2-го регионального научного форума «Мать и дитя». – М., 2008. – С.143–144.
4. Гатаулина Р.Г., Назаренко Т.А., Гус А.И., Саркисов С.Э., Ежова Л.С., Жорданидзе Д.О., Менжинская И.В. Новые подходы к коррекции внутриматочной патологии у женщин при подготовке к проведению программы ЭКО // Материалы 2-го регионального научного форума «Мать и дитя». – М., 2008. – С.156–157.
5. Сухих Г.Т., Файзулин Л.З., Квасов А.В., Карнаухов В.Н., Непша О.С., Абубакиров А.Н., Жорданидзе Д.О., Герасимова А.А., Трофимов Д.Ю. Исследование генетического полиморфизма HLA II класса у пациенток с наружным генитальным эндометриозом // Проблемы репродукции. – 2009. - Т.15. – №1. – С. 89–92 (перечень ВАК).
6. Жорданидзе Д.О., Назаренко Т.А., Муллабаева С.М. Изменение концентраций антимюллерового гормона при стимуляции яичников гонадотропинами // Материалы 4-го международного конгресса по репродуктивной медицине. – М., 2010. – С.257–258.
7. Кирмасова А.В., Назаренко Т.А., Чечурова Т.Н., Дуринян Э.Р., Жорданидзе Д.О. Важность реверсии и конверсии у женщин с СПКЯ на протяжении их жизни // Материалы 23-го международного конгресса с курсом эндоскопии «Новые технологии в диагностике и лечении гинекологических заболеваний». – М., 2010. – С.197–198.
8. Жорданидзе Д.О., Назаренко Т.А., Дуринян Э.Р., Иванец Т.Ю. Состояние овариального резерва при некоторых формах функционального бесплодия // Акушерство и гинекология. – 2010.- №5. – С. 25–31 (перечень ВАК).

