Кардиоваскулярные заболевания при патологии суставов и остеопорозе в прибайкалье
На правах рукописи
Храмцова Наталья Анатольевна
КАРДИОВАСКУЛЯРНЫЕ ЗАБОЛЕВАНИЯ
ПРИ ПАТОЛОГИИ СУСТАВОВ И ОСТЕОПОРОЗЕ
В ПРИБАЙКАЛЬЕ
14.01.04- внутренние болезни
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Иркутск, 2010
Работа выполнена в государственном образовательном учреждении дополнительного профессионального образования «Иркутский государственный институт усовершенствования врачей Федерального агентства по здравоохранению и социальному развитию»
Научный консультант - заслуженный деятель науки РФ,
член-корреспондент РАМН,
доктор медицинских наук, профессор
Александр Александрович Дзизинский
Официальные оппоненты: доктор медицинских наук, профессор
Юрий Аркадьевич Горяев,
доктор медицинских наук, профессор
Татьяна Ефимовна Курильская
доктор медицинских наук, профессор
Геннадий Васильевич Матюшин
Ведущая организация – Государственное образовательное учреждение высшего профессионального образования «Казанский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Защита состоится «___» октября 2010 года в _____часов на заседании диссертационного совета ДМ208.031.01 в ГОУ ДПО «Иркутский государственный институт усовершенствования врачей Федерального агентства по здравоохранению и социальному развитию» по адресу: 664079, г. Иркутск, м-н Юбилейный, 100.
С диссертацией можно ознакомиться в библиотеке ГОУ ДПО «Иркутский государственный институт усовершенствования врачей Федерального агентства по здравоохранению и социальному развитию» (664079, г.Иркутск, м-н Юбилейный, 100).
Автореферат разослан «__» ______________________2010 г.
Ученый секретарь диссертационного совета
кандидат медицинских наук, доцент Стародубцев А.В.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Ревматоидный артрит (РА) – это хроническое воспалительное заболевание суставов с негативным влиянием не только на качество, но и продолжительность жизни пациентов. Как известно, главной причиной преждевременной смертности у этих больных являются кардиоваскулярные осложнения (Myllykangas- Luosojarvi R.A. et al., 1995; Kitas G. et al., 2001). Риск сердечно-сосудистых событий при РА выше в среднем в 3 раза по сравнению с общей популяцией, и это, как утверждают эпидемиологические исследования, приводит к сокращению продолжительности жизни на 5-10 лет (Watson D.J. et al., 2003; Hurlimann, D, et al., 2004). Проспективные наблюдения за больными ревматоидным артритом подтвердили высокую частоту сердечно-сосудистых заболеваний, причем этот показатель существенно не менялся после учета традиционных факторов кардиоваскулярного риска (Chae CU, et al., 2001; del Rincon, I.D. et al., 2001; Grover, S, et. al., 2006).
В современной концепции атерогенеза хроническое воспаление рассматривается как ключевой патогенетический механизм этого процесса (Ross R., 1999). По мнению большинства исследователей, при обсуждении причин повышенного кардиоваскулярного риска у больных, страдающих ревматоидным артритом, приоритетное место должно отводиться единым иммунопатологическим механизмам прогрессирования атеросклероза и ревматоидного артрита (Насонов Е.Л., 2003). Эпидемиологические данные подтверждают ассоциацию маркеров воспаления с сердечно-сосудистой заболеваемостью (Libby P., 2002). Наряду с традиционными представлениями, маркеры воспаления отражают хронический аутоиммунный воспалительный процесс при ревматических заболеваниях, и в то же время многие из них рассматриваются как предикторы кардиоваскулярных осложнений (Мазуров В.И. и соавт., 2009).
Неоднозначны мнения в отношении доминирующего вклада традиционных факторов кардиоваскулярного риска у больных ревматоидным артритом. Почти у половины пациентов, страдающих РА, кардиоваскулярные осложнения развивались при отсутствии «классических» предикторов атеросклероза (Maradit-Kremers H., 2005). Согласно концепции N.Sattar et al. (2003), традиционные факторы имели ключевое значение лишь до формирования развернутого ревматоидного артрита. В последующем более значимыми становились показатели активности заболевания, которые отражали выраженность системного аутоиммунного воспаления. Наряду с традиционными факторами кардиоваскулярного риска у больных РА наиболее специфический вклад, как подтвердил ряд исследователей, оказывали маркеры активности воспаления и в большей степени высокий уровень СРБ (Мутовина З.Ю., 2007; Мальчевская Е.А., 2008; Бочкова Ю.В., 2008).
Широко обсуждается в литературе также проблема высокой распространенности артериальной гипертонии у пациентов, страдающих ревматоидным артритом, в сравнении с группами здоровых людей, сопоставимых по полу и возрасту (Mikuls T.R., 2001; Sattar N., 2003). Наиболее вероятной причиной повышения артериального давления у больных ревматоидным артритом традиционно считается прием нестероидных противовоспалительных препаратов (НПВП), в том числе селективных ЦОГ- 2 ингибиторов (Pope J.E., 1993). Так, по результатам мета-анализов на фоне приема НПВП среднее АД увеличивалось в среднем на 5,5 мм рт.ст. (Johnson A.G. et al., 1994). Продолжительный прием НПВП ассоциировался с негативным изменением суточного профиля артериального давления и увеличением числа нон-дипперов, больных с неадекватно высоким давлением в ночные часы (Аничков Д., Шостак Н., 2003).
Недостаточно сведений о прямом влиянии воспаления на риск развития артериальной гипертонии, но при этом есть данные о корреляции АД с уровнем ИЛ- 6 у здоровых мужчин (Chae C.U., 2001). Ряд исследователей подтвердили существование неспецифического воспаления при артериальной гипертонии (Ощепкова Е.В. и соавт., 2007). В некоторых крупных проспективных эпидемиологических работах показана прогностическая значимость С-реактивного белка – маркера воспаления – в отношении развития артериальной гипертонии у лиц с нормальным давлением (Chae C.U., et al., 2001; Kearney P.M. et al., 2005). Клинических работ по изучению роли СРБ в течении АГ и поражении органов-мишеней значительно меньше, и их результаты противоречивы.
Согласно мнению F.Wolfe et al., основанному на данных эпидемиологического исследования, ревматоидный артрит — независимый предиктор ИБС в общей популяции (Wolfe F., 2003). Почти у половины пациентов, страдающих РА, по результатам суточного мониторирования ЭКГ была обнаружена безболевая ишемия (Wislowska M., 1998). Наличие ревматоидного артрита, особенно в сочетании с гиперлипидемией, статистически значимо повышало риск развития инфаркта миокарда (Fischer L.M. et al., 2004). При этом бессимптомное атипичное течение острого коронарного синдрома было установлено у каждого пятого больного РА с достоверно более частым развитием фатальных исходов по сравнению с группой лиц без артрита, сопоставимой по полу и возрасту (Banks M. et al., 2000; Douglas K. M., 2006).
Наряду с кардиоваскулярной патологией, при ревматоидном артрите серьезные социально-экономические последствия ассоциируются с остеопорозом и переломами, что приводит к значительным показателям инвалидности и смертности, особенно среди больных пожилого возраста (Беневоленская Л.И., 2003). Снижение минеральной плотности костной ткани (МПКТ) у больных РА вероятно является независимым фактором кардиоваскулярного риска (Гавва Т.Н., 2009).
Для анкилозирующего спондилита данные о распространенности кардиоваскулярной патологии весьма ограничены. В крупнейшей на сегодняшний день работе, касающейся причин смерти больных анкилозирующим спондилитом, показан риск фатальных цереброваскулярных событий в 2 раза превышающий аналогичный популяционный показатель. Для других кардиоваскулярных событий этот риск был выше почти в полтора раза (Radford E.P.et al., 1977).
У больных остеоартрозом нередко наблюдается повышение СРБ как предиктора неблагоприятного течения кардиоваскулярной патологии (Джураев И.Э. и соавт., 2009). Полученные рядом исследователей данные свидетельствуют о высокой (72,7%) частоте сочетания остеоартроза с артериальной гипертонией (Леганова Н.М., и соавт., 2009). У большинства больных ОА выявлены значительные нарушения липидного и углеводного обменов (Пащенко Л.С. и соавт., 2009).
Таким образом, сведения о кардиоваскулярной патологии при заболеваниях суставов неоднозначны. Ряд исследователей утверждают о частоте сердечно-сосудистых событий, сравнимой с общепопуляционными показателями. Мнения оппонентов по этому вопросу сходятся в отношении высокой кардиоваскулярной заболеваемости при ревматоидном артрите, спондилоартритах и доминирующем вкладе, наряду с традиционными факторами риска, активности воспаления. Продолжается дискуссия о частоте и факторах риска кардиоваскулярной патологии у больных остеоартрозом. Особенности климато-географических, экологических и экономических условий Восточной Сибири предполагают проведение региональных исследований для изучения частоты, факторов риска и клинико-патогенетических взаимосвязей кардиоваскулярных осложнений при патологии суставов, что и определило цели настоящего исследования.
Цель исследования: изучить частоту, структуру и факторы риска сердечно-сосудистой патологии при заболеваниях суставов (ревматоидный артрит, серонегативные спондилоартриты и остеоартроз) в Иркутской области и Республике Бурятия с определением клинико-патогенетических взаимосвязей кардиоваскулярной патологии и активностью воспаления.
Основные задачи исследования:
- Изучить частоту, структуру и факторы риска артериальной гипертонии у больных ревматоидным артритом.
- Изучить поражение органов-мишеней у больных РА в сочетании с артериальной гипертонией.
- Изучить особенности течения и факторы риска ишемической болезни сердца у больных ревматоидным артритом.
- Оценить общий сердечно-сосудистый риск при РА и разработать на основании выделенных факторов риска математическую модель прогнозирования.
- Изучить клинико-патогенетические взаимосвязи сердечно-сосудистой патологии и минеральной плотности костной ткани у больных ревматоидным артритом.
- Изучить частоту, структуру и факторы риска кардиоваскулярной патологии при остеоартрозе и спондилоартритах.
- Изучить качество оказания кардиологической помощи при патологии суставов в Прибайкалье.
Научная новизна. Впервые на территории Прибайкалья исследованы частота, структура и факторы риска кардиоваскулярной патологии у больных, страдающих ревматоидным артритом, серонегативными спондилоартритами и остеоартрозом.
Впервые в условиях одномоментного поперечного исследования проведена комплексная оценка морфо-функционального состояния основных органов-мишеней (сердца, сосудов и почек) у больных с патологией суставов в сочетании с артериальной гипертонией. Впервые изучена частота, структура, факторы риска и особенности течения ишемической болезни сердца у данной категории больных.
На основании выделенных факторов впервые разработана математическая модель прогнозирования и оценки общего сердечно-сосудистого риска у больных, страдающих ревматоидным артритом. Впервые установлен ряд закономерностей клинико-патогенетических взаимосвязей активности воспаления, сердечно-сосудистой патологии и состояния минеральной плотности костной ткани. Впервые были проанализированы факторы риска и исходы переломов у больных ревматоидным артритом в сочетании с кардиоваскулярными осложнениями.
Впервые проведена оценка качества оказания кардиологической помощи больным с патологией суставов в Прибайкалье.
Практическая значимость. Полученные в результате исследования объективные данные о частоте, структуре и факторах риска таких социально значимых заболеваний, как артериальная гипертония, ИБС, хроническая болезнь почек у пациентов, страдающих ревматоидным артритом, спондилоартритами и остеоартрозом, являются основой для разработки дифференцированных подходов к ранней диагностике и профилактике кардиоваскулярной патологии у данной категории больных. Разработанный на основании выделенных факторов способ прогнозирования сердечно-сосудистого риска у больных ревматоидным артритом позволит оптимизировать диагностические и лечебно-профилактические мероприятия.
Выделение групп повышенного кардиоваскулярного риска среди больных ревматоидным артритом и спондилоартритами создает возможность модифицировать факторы риска для улучшения прогноза. Выявленные в работе данные о качестве оказания кардиологической помощи больным с патологией суставов необходимы, для разработки и планирования тактики ведения этих пациентов на амбулаторном этапе.
Внедрение результатов работы. Материалы работы используются в педагогической, научной и клинической деятельности на кафедрах терапии и кардиологии, семейной медицины и геронтологии Иркутского института усовершенствования врачей. Результаты исследования и практические рекомендации внедрены в работу областного Центра профилактики и лечения ревматических заболеваний и остеопороза, Иркутского городского ревматологического Центра, лечебных учреждений г. Иркутска, Иркутской области и республики Бурятия.
Разработаны: «Способ прогнозирования переломов проксимального отдела бедренной кости» патент РФ № 2238037 от 20 октября 2004 г.; «Способ прогнозирования сердечно-сосудистого риска при ревматоидном артрите» (заявка на изобретение №2009127983/14 приоритет от 20.07.2009).
Положения, выносимые на защиту:
1. Общий сердечно-сосудистый риск при ревматоидном артрите ассоциируется с артериальной гипертонией, сниженной скоростью клубочковой фильтрации, остеопенией и/или остеопорозом, дислипидемией, толщиной комплекса интима-медиа и уровнем СРБ. Наиболее значимыми факторами риска развития кардиоваскулярных заболеваний и их осложнений у больных ревматоидным артритом являются прием высоких суммарных доз глюкокортикоидов и продолжительность РА свыше 10 лет.
2. При ревматоидном артрите встречается изолированная систолическая артериальная гипертония с высоким уровнем пульсового давления, что ассоциируется с активностью воспаления и выраженным поражением органов-мишеней.
3. Имеется значимая взаимосвязь между тяжестью кардиоваскулярной патологии и выраженностью воспаления у больных ревматоидным артритом и спондилоартритами.
4. В клинической практике на территории Прибайкалья отмечается объективная недооценка частоты и тяжести сердечно-сосудистой патологии у больных ревматоидным артритом и спондилоартритами.
Апробация работы. Материалы диссертации представлены на III Российском Симпозиуме по остеопорозу (Санкт-Петербург, 2000), III съезде ревматологов России (Рязань, 2001), республиканской научно-практической конференции по остеопорозу (Иркутск, 2001), конференции молодых ревматологов России (Москва- Звенигород, 2002), Конгрессе «Человек и лекарство» (Владивосток, 2005), Областной научно-практической конференции Иркутского отделения Ассоциации ревматологов России (Иркутск, 2007), научно- практической конференции терапевтов (Улан – Удэ, Бурятия, 2008), республиканской конференции по проблемам остеопороза (Улан–Удэ, Бурятия, 2008), научно-практической конференции молодых ученых (Иркутск, 2006, 2008, 2009), Юбилейной научно-практической конференции (Иркутск, 2008), V съезде ревматологов России (Москва, 2009), городской конференции терапевтов (Братск, 2009), Национальном конгрессе кардиологов России (Москва, 2009).
Публикации. По теме диссертации опубликовано 48 работ, из них 10 статей в рецензируемых журналах, рекомендованных ВАК РФ для публикации основных результатов диссертации на соискание ученой степени доктора наук, методические рекомендации для врачей и монография.
Объем и структура диссертации. Диссертация изложена на 253 страницах. Текстовая часть (224 страницы) состоит из введения, обзора литературы, материалов и методов исследования, 4 глав собственных исследований, обсуждения полученных результатов, выводов, практических рекомендаций и приложения. Работа проиллюстрирована 56 рисунками и 77 таблицами. Указатель литературы содержит 269 источника, из них 84 работы отечественных и 185 зарубежных авторов.
СОДЕРЖАНИЕ РАБОТЫ
1. Материалы и методы исследования
Исследование было проведено в 3 этапа
1этап. Скрининговое анкетирование и ретроспективный анализ медицинской документации 1050 пациентов РА и серонегативными спондилоартритами (СА) в г. Иркутске, Иркутской области и Республике Бурятии за период с 2003 по 2008 гг. включительно. Формирование групп проводилось случайным методом из репрезентативной выборки больных ревматоидным артритом и СА. Критериями включения был возраст старше 18 лет, достоверный диагноз РА (АРА, 1987 г.) и спондилоартрита (1991). Средний возраст больных РА составил 55,4±11,6 лет, СА-51,7±13,6 лет, продолжительность заболевания 14,7 (2; 21) лет и 14,9 (3; 21) лет соответственно.
2 этап. Аналитическое одномоментное поперечное исследование с изучением кардиоваскулярной патологии у 257 пациентов РА. Критерии включения: женщины и мужчины с ревматоидным артритом, верифицированным по критериям AРA (1987г.). Средний возраст пациентов составил 53 (22; 69) лет, продолжительность РА – 14,4 (2; 21) лет. В исследовании преобладали женщины с умеренной степенью активности по DAS 28, серопозитивностью по РФ, со 2-й и 3-й рентгенологической стадиями заболевания. Функциональная недостаточность суставов соответствовала в преобладающем большинстве 2 ФК.
3 этап. Изучение сердечно-сосудистой патологии у больных серонегативными спондилоартритами и остеоартрозом, а также в контрольной группе у лиц без патологии суставов. Первую группу (n=75) составили пациенты, страдающие серонегативными спондилоартритами, из них анкилозирующим спондилитом 48 чел. (64%), псориатическим артритом – 27 чел. (36%), стратифицированные по возрасту и полу (по пятилетним стратам). Вторая группа (n=30), сформирована из пациентов с остеоартрозом не менее 2-ой рентгенологической стадии поражения крупных суставов, была сопоставима по полу и возрасту (по пятилетним стратам). Диагноз ОА верифицирован по критериям R. Altman. Контрольная группа (n=30) без патологии суставов стратифицирована по возрасту (по пятилетним стратам) и полу.
Дизайн всего исследования представлен в табл. 1.
Таблица 1
Дизайн исследования
| Всего обследовано 1110 человек | ||||||||||
| 1 этап (1050 пациентов)-РА (n=750), СА (n=300) г. Иркутск, Иркутская область и Республика Бурятия (ретроспективный анализ медицинской документации) | ||||||||||
| 2 этап - больные РА (n=257) средний возраст 53 (22; 69) год – одномоментное поперечное исследование больных РА | ||||||||||
| Оценка факторов риска (n=257), стратификация риска (n=257), оценка качества жизни (n=257), | Поражение сердца: ЭКГ(n=257), ЭХОКГ(n=257), ХМ ЭКГ(n=257), СМАД (n=257). | Поражение сосудов (330 исследований): УЗДГ сонных артерий (n=110), пробы с ЭЗВД (n=110), пробы с ЭНВД (n=110), офтальмоскопия и микрофотографирование (n=100 чел., 200 фотографий) | Поражение почек: креатинин сыворотки крови (n=257), СКФ (n=257), МАУ (n=257) | ОДМ (n=150) СРБ (n=257) липидограмма (n=257) | ||||||
| 3 этап - группа 1 (n=75) больные спондилоартритами, средний возраст 51 (22; 68) год. | ||||||||||
| Оценка факторов риска (n=75), стратификация риска (n=75), оценка качества жизни (n=75), | Поражение сердца: ЭКГ(n=75), ЭХОКГ(n=75), ХМЭКГ(n=75), СМАД (n=75) Липидограмма (n=75), СРБ (n=75) | Поражение сосудов (150 исследований): УЗДГсонных артерий (n=50), пробы сЭЗВД (n=50), пробы сЭНВД (n=50) | Поражение почек: креатинин сыворотки крови (n=75), СКФ (n=75), МАУ (n=75) | |||||||
| группа 2 (n=30) – больные остеоартрозом средний возраст 56 (39; 70) год. | ||||||||||
| Оценка факторов риска (n=30), стратификация риска (n=30), | Поражение сердца: ЭКГ(n=30), ЭХОКГ(n=30), ХМ ЭКГ(n=30) СРБ (n=30) липидограмма (n=30) СМАД (n=30) | Поражение сосудов: (90 исследований) УЗДГ сонных артерий (n=30), пробы с ЭЗВД (n=30), пробы с ЭНВД (n=30), | Поражение почек: креатинин сыворотки крови (n=30), СКФ (n=30) | |||||||
| Контрольная группа (n=30) – без патологии суставов средний возраст 53±7,3 год. | ||||||||||
| Оценка факторов риска (n=30), стратификация риска (n=30), СРБ (n=30) липидограмма (n=30) | Поражение сердца:ЭКГ(n=30), ЭХОКГ(n=30), ХМ ЭКГ(n=30) СМАД (n=30) | Поражение сосудов: УЗДГ сонных артерий (n=30), пробы с ЭЗВД (n=30), пробы с ЭНВД (n=30) | Поражение почек: креатинин сыворотки крови (n=30), СКФ (n=30), МАУ (n=30) | |||||||
ЭЗВД – эндотелийзависимая вазодилатация; ЭНЗВД- эндотелийнезависимая вазодилатация; СМАД – суточное мониторирование АД; ОДМ – остеоденситометрия; ХМ – холтеровское мониторирование; МАУ – микроальбуминурия; СКФ – скорость клубочковой фильтрации; МПКТ – минеральная плотность костной ткани.
М е т о д ы и с с л е д о в а н и я представлены в таблице 2.
Таблица 2
| Методика оценки суставного синдрома и качества жизни | Методика оценки сердечно-сосудистой патологии | Статистические методы |
| Ревматоидный артрит: Индекс активности DAS 28, R-стадии по Штейнброкеру; Cеронегативные спондилоартриты: Индекс активность - BASDAI; Индекс функциональных нарушений- BASFI; рентгенологические изменения (BASRI); тяжесть поражения кожи при псориатическом артрите-индекс PASI. Остеоартроз Рентгенологическая стадия- по J.H.Kellgrena и J.Lawrence; тяжесть ОА- индексы Lequesne; WOMAC; ВАШ боли и общего состояния; МПКТ-двухэнергетическая рентгеновская абсорбциометрия («DPX- IQ» Lunar, США); СРБ индекс коморбидности Charlson Шкала Цунга ; опросник HAQ | Суточное мониторирование АД и ЭКГ- бифункциональные мониторы Cardio Tens – 01 и Meditech card(x)plore (Венгрия); ЭКГ - Schiller AT – 10 Plus, «Schiller», Швейцария; ЭХОКГ- Toshiba Aplio (Япония); Гипертрофия миокарда ЛЖ- индекс Соколова – Лайона; ИММЛЖ по Penn – convention; Морфо-функциональное состояние сосудов- линейный датчик 7,5-8,5 МГц в В – режиме с цветным доплеровским картированием потока (LogiqBookXP «General Electrics», США), функция эндотелия неинвазивным способом по D. S. Celermajer; Функциональное состояние почек- креатинин сыворотки крови по Яффе в модификации Поппера на биохимическом анализаторе «Synchron EL – ISE» («Beckman/Соulter», США); альбумин в утренней моче нефелометрическим методом анализатором «Array- 360» («Beckman/Coulter», США); соотношение альбумин/креатинин мочи (мг/ммоль); СКФ по формулам MDRD(Modification of Renal Disease Study) и Cocroft – Gault; Исследование сосудов сетчатки глаза- прямая офтальмоскопия с ретинофотографией на фундус- камере Canon CF- 60UV («Canon», Япония); Липидограмма ферментативным методом на автоматическом анализаторе «В/М HITACHI 902» («Roche – B/M», Франция). Оценка 10-летнего риска кардиоваскулярной смерти в соответствии с Европейскими рекомендациями по шкале SCORE | Нормальность распределения по критериям Колмогорова – Смирнова, Lilliefors; данные в виде среднего арифметического значения и стандартного отклонения (SD), медиан (Ме) и интерквартилных интервалов (ИИ); количественный анализ дисперсионным методом по Friedman, для парных критериев- Student и Wilcoxon matched pairs test, при сравнении 2 групп- двусторонний тест Student или критерий Mann–Whitney; качественный анализ- двумерные таблицы сопряженности критерия по Пирсону; пошаговый логистический регрессионный анализ с определением величины OR; связь количественных признаков - корреляционный анализ, в том числе с поправкой Спирмена; дискриминантный анализ c oценкой канонической дискриминации, статистики – Уилксона, расстояния Махалонобиса и % правильности распознавания.; кластерный анализ методом итеративной группировки k - средних (k – means clastering) (к.т.н.Михалевич И.М.); «Epi info ver.6», «Biostatistica 4.0 McGraw – Hill», Statistica 6.0 («Statsoft», США). |
2. Результаты работы и их обсуждение
2.1. Артериальная гипертония у больных ревматоидным артритом
На первом этапе нашего исследования частота артериальной гипертонии оценивалась у 750 больных ревматоидным артритом по результатам анкетирования и анализа медицинской документации в г.Иркутске, Иркутской области и Республике Бурятия (рис.1).
Рис.1 Частота артериальной гипертензии по результатам анкетирования и анализа мед.документации (n=750).
Показатели распространенности АГ в среднем составили 35,9%, у мужчин гипертония была установлена у 62 чел. (38,5%), у женщин – 207 чел. (35,1%, р>0,05). Методом СМАД из 257 обследованных больных РА артериальная гипертония в соответствии с критериями ВНОК диагностирована у 138 (53,7%) пациентов. Среди мужчин, болеющих РА, частота АГ составила 54,1% (26 чел.), среди женщин - 53,6% (112 чел.), p=0,16. Показатели уровней АД представлены в табл. 3.
Таблица 3
Показатели АД у больных РА
| РА с АГ, n=138 (Ме, ИИ) | РА без АГ, n=119 (Ме, ИИ) | Контроль, n=30 (Ме, ИИ) | |
| 1 | 2 | 3 | |
| Офисное САД (мм.рт.ст.) | 149,6 1-2(0,003) (132; 167) | 122 2-3(0,80) (105; 135) | 125 1-3(0,009) (110; 137) |
| Офисное ДАД (мм.рт.ст) | 84,1 1-2 (0,03) (80; 95) | 76 2-3(0,90) (72; 81) | 78 1-3(0,06) (72; 80) |
| Офисное ПД (мм.рт.ст) | 65,5 1-2(0,008) (50; 79) | 46 2-3(0,60) (42; 55) | 42 1-3(0,006) (40; 58) |
| САД-24 | 133,51-2 (0,007) (123; 141) | 120 2-3 (0,80) (113; 124) | 123 1-3 (0,005) (113; 124) |
| ДАД-24 | 72,2 1-2(0,60) (65; 79) | 70 2-3 (0,70) (66; 78) | 75 1-3 (0,90) (68; 77) |
| ПД-24 | 60,3 1-2(0,005) (53; 65) | 50 1-3(0,004) (42; 56) | 45 2-3 (0,05) (42; 53) |
САД-24, ДАД – 24 и ПД – 24 – среднесуточные значения САД, ДАД и ПД.
В группе больных РА в сочетании с артериальной гипертонией медиана САД при офисном измерении и СМАД была достоверно выше по сравнению с больными РА без АГ и контрольной группой (149,6 мм.рт.ст. против 122 и 125 мм.рт.ст. соответственно, p<0,01). При этом установлены высокие показатели пульсового АД у больных РА в сочетании с АГ, так медиана ПД при офисном измерении и при СМАД в этой группе составила 65,5 мм.рт.ст. и 60,3 мм.рт.ст. соответственно против 46 мм.рт.ст и 50 мм.рт.ст в группе РА без гипертонии (р<0,01) и 42 мм.рт.ст. и 45 мм.рт.ст. (р<0,01) в контрольной группе. Частота систолодиастолической (СДАГ) гипертонии составила 78,3%, изолированной систолической артериальной гипертензии (ИСАГ) – 21,7%. (рис. 2).
Рис.2. Частота СДАГ и ИСАГ среди больных РА (**р<0,01).
Суточный профиль колебаний уровней АД как показатель вариабельности в дневные и ночные часы по результатам СМАД распределился у больных РА следующим образом (рис. 3). Из 257 пациентов число дипперов (пациентов с физиологическим типом суточного индекса и нормальным снижением АД в ночные часы) составило 59,9%.
Рис.3. Характеристика суточного индекса артериального давления у больных РА
У 78 (30,4%) пациентов, страдающих РА, выявлен патологический тип суточного профиля нон-диппер (non-dipper), характеризующийся недостаточным снижением АД в ночные часы. У 13 (5,1%) пациентов суточный индекс колебаний АД соответствовал типу night–peaker (найт- пикер), у 12 (4,6%) больных выявлен тип овер-диппер (over-dipper), характеризующийся неадекватно низким уровнем АД ночью. Факторами риска, ассоциируемыми с патологическими типам вариабельности АД, явились впервые выявленная (нелеченная) гипертония (OR-4,5; p<0,01), пульсовое АД выше 55 мм.рт.ст. (OR-3,9; p<0,01), высокая активность РА по DAS 28 (OR-3,8; p< 0,01) и снижение СКФ < 60 мл/мин (OR-3,2; p< 0,05).
Таким образом, у больных РА установлена высокая частота артериальной гипертонии, превышающая соответствующие показатели общепопуляционной распространенности АГ, и данные, полученные по материалам медицинской документации (53,7% против 39,5% и 35,9% соответственно, р<0,05). Не отмечено достоверных различий в частоте гипертонии между мужчинами и женщинами. У трети обследуемых больных АГ была установлена впервые. Среди больных РА встречалась изолированная систолическая артериальная гипертония, патогенетические предпосылки для формирования которой в настоящее время являются предметом дискуссии и будут обсуждены в следующих разделах.
2.1.1. Факторы риска артериальной гипертонии
У обследуемых на первом этапе 750 пациентов РА были проанализированы традиционные факторы риска АГ (рис.4).
Рис. 4. Традиционные факторы риска артериальной гипертензии у больных РА (**р<0,01).
Из классических факторов кардиоваскулярного риска у мужчин по сравнению с женщинами доминировало влияние возраста - 80 чел. (49,7%) против 150 чел. (24,5%, р<0,001), и значимым предиктором АГ явилось курение – 62 чел. (38,5%) и 8 чел. (1,4%, р<0,001) соответственно. У женщин достоверно чаще встречалось абдоминальное ожирение - 265 чел. (45%) против 28 чел. (17,4%, р<0,001) и метаболический синдром – 118 чел (20%) и 16 чел. (9,9%, р<0,05) соответственно. С одинаковой частотой у лиц обоего пола были установлены случаи семейного анамнеза ранних сердечно-сосудистых событий, дислипидемии и гипергликемии. Более чем у половины больных РА с установленной по результатам СМАД гипертонией, классические предикторы сердечно-сосудистого риска отсутствовали, что предполагает вклад других факторов, вероятно ассоциирующихся с последствиями ревматоидного артрита.
Методом пошаговой логистической регрессии установлены наиболее значимые факторы риска АГ у больных, страдающих РА (рис. 5).
Рис.5. Факторы риска АГ при ревматоидном артрите (n=257; *р<0,05; **p<0,01).
Таким образом, при РА, наряду с традиционными кардиоваскулярными факторами, такими как наследственность, дислипидемия, снижение СКФ, гипергликемия и гиподинамия, показано существенное влияние на риск АГ приема глюкокортикоидов и НПВП, в том числе и селективных ЦОГ–2 ингибиторов, высокой активности и продолжительность свыше 10 лет РА.
2.1.2. Поражение органов-мишеней у больных ревматоидным артритом
М о р ф о ф у н к ц и о н а л ь н о е с о с т о я н и е с о с у д о в у больных РА представлено в табл. 4.
Таблица 4
Сравнительная характеристика состояние сосудов при ревматоидном артрите
| Показатели | РА с АГ, n=63 | РА без АГ, n=47 | Контроль, n=30 | DAS28>5,1 n=30 |
| 1 | 2 | 3 | 4 | 5 |
| ТИМ ОСА, мм (Ме, Ии) | 1,03 (2-3)** (0,91; 1,08) | 0,78 (0,69; 1,05) | 0,85 (2-4)** (0,69; 1,04) | 0,98(4-5)* (0,85; 1,01) |
| Частота бляшки ОСА (n, %) | 29 (46,0) (2-3)** | 9 (19,1) | 5 (16,7) (2-4)** | 12 (40)(3-5)**; (4-5)** |
| ЭЗВД на 90 сек.% (Ме, Ии) | 1,9 (2-3)** (-3,2; 7,1) | 3,2 (-3,0; 7,5) | 3,5 (2-4)** (-2,5; 8,1) | 2,7(4-5)* (-2,8; 8,0) |
| Частота ЭЗВД (n, %) | 54 (85,7) (2-3)** | 28 (59,6) | 15 (50) (2-4)** | 18 (60) (2-5)** |
| ЭНЗВД, % (Ме, Ии) | 6,9 (2-3)** (2,9; 13,2) | 11,3 (5,4; 15,2) | 11,5 (2-4)** (4,9; 16,0) | 8,0(4-5)*; (3-5)* (4,0; 12,2) |
| Частота ЭНЗВД (n, %) | 29 (46,0) (2-3)* | 15 (31,9) | 10 (33,3) (2-4)* | 12 (40) |
| ЛПИ | 1,01 (0,90; 1,13) | 1,17 (0,95; 1,17) | 1,07 (0,90; 1,23) | 1,05 (0,90; 1,15) |
*p<0,05; **p<0,01
Как видно из таблицы 4, сосудистая дисфункция значительно преобладала у пациентов РА в сочетании с артериальной гипертонией и высокой активностью воспаления по DAS 28. При этом морфофункциональные характеристики сосудов у больных РА без гипертонии и высокой активности воспаления были сопоставимы с контролем. Значимыми предикторами сосудистой дисфункции у больных, страдающих ревматоидным артритом, явились активность воспаления по DAS 28 (OR-9,45, р<0,01), продолжительность РА более 10 лет (OR-6,69, р<0,01), гипергликемия (OR-4,19, р<0,05), прием глюкокортикоидов в суммарной дозе свыше 3,0 г. в пересчете на преднизолон (OR-3,98 и 3,01, соответственно), артериальная гипертония (OR-4,75, р<0,01), уровень холестерина ЛПНП > 3,0 ммоль/л (OR-3,76, р<0,01) и снижение скорости клубочковой фильтрации (OR-3,83, p<0,01).
Сравнительная характеристика состояния сосудов глазного дна представлена в табл.5.
Таблица 5
Сравнительная характеристика параметров ангиопатии при РА
| Признак | РА с АГ, n=60 (Ме, ИИ) | РА без АГ, n=40(Ме, ИИ) | РА(DAS28>5,1), n=30 (Me,ИИ) |
| 1 | 2 | 3 | 4 |
| СREA(эквивалент центр.артерии), мкм | 165, 12-3(p=0,45) (153; 184) | 162,0 3-4(p=0,46) (149; 181) | 167,4 2-4(p=0,50) (155; 186) |
| CRVE (эквивалент вен сетчатки), мкм | 212,2 2-3 (p=0,08) (190; 232) | 206,1 3-4 (p=0,15) (188; 230) | 209,7 2-4 p=(0,11) (191; 231) |
| Отношение СREA/ CRVE, (a/v) | 0,76 2-3 (p=0,23) (0,7; 0,9) | 0,83 3-4 (p=0,13) (0,7; 1,0) | 0,79 2-4 (p=0,56) (0,7; 0,9) |
| Частота фокального сужения артериол (n, %) | 7 2-3(p=0,52) (11,7) | 3 3-4(p=0,71) (7,5) | 3 2-4(p=0,86) (10) |
| Артериоло-венулярные перекресты (%) | 12 2-3 (p=0,21) (20) | 6 3-4 (p=0,87) (15) | 5 2-4 (p=0,34) (16,7) |
| Угол бифуркации артериол (°) | 74,8 2-3 (p=0,38) (72; 81) | 71,5 3-4 (p=0,29) (69; 78) | 73,7 2-4 (p=0,89) (72, 80) |
| Угол бифуркации венул (°) | 74,5 2-3 (p=0,24) (73; 80) | 72,0 3-4 (p=0,31) (67; 79) | 74,7 2-4 (p=0,90) (71; 80) |
| Средняя длина сегмента артериол, мкм | 2905 2-3 (p=0,10) (2630; 3342) | 3050 3-4 (p=0,44) (2900; 3402) | 3011 2-4 (p=0,09) (2890; 3300) |
| Средняя длина сегмента венул, мкм | 3290 2-3 (p=0,88) (2876; 3510) | 32502-4 (p=0,75) (2980; 3408) | 3215 3-4 (p=0,90) (2963; 3408) |
| Относительный диаметр артериол, (у.е) | 36,9 2-3 (p=0,89) (30; 45) | 37,8 3-4 (p=0,51) (30; 46) | 37,0 2-4 (p=0,72) (30; 45) |
| Относительный диаметр венул, (у.е) | 34,5 2-3 (p=0,81) (27; 38) | 33,7 3-4 (p=0,76) (26; 38) | 35,2 2-4 (p=0,92) (27; 38) |
| Извитость артериол, (у.е) | 0,03 2-3 (p=0,04) (0,01; 0,04) | 0,016 3-4 (p=0,04) (0,01; 0,04) | 0,03 2-4 (p=0,89) (0,01; 0,04) |
| Извитость венул, (у.е) | 0,03 2-3 (p=0,04) (0,01; 0,04) | 0,02 3-4 (p=0,98) (0,01; 0,04) | 0,02 2-4 (p=0,04) (0,01; 0,04) |
Параметры сосудистого ремоделирования у больных РА в сочетании с АГ соответствовали картине гипертонической ангиопатии с выраженным изменением посткапиллярного звена микроциркуляции сетчатки. При этом достоверно более интенсивная извитость артериол у больных с артериальной гипертонией в сочетании с высокой активностью воспаления при РА не исключало вероятного васкулита микроциркуляторного русла.
Корреляционный анализ показателей сосудистой дисфункции представлен в табл. 6.
Таблица 6
Корреляция параметров показателей сосудистой дисфункции
| Признак 1 | Признак 2 | РА, n=110 | |
| r | Р | ||
| ТИМ ОСА (мм) | СС риск по SCORE (%) | 0,25 | 0,001 |
| ТИМ ОСА (мм) | СКФ (мл/мин) | -0,28 | 0,0001 |
| ЭЗВД, % ЭНЗВД, % | ИММЛЖ (г/м 2 ) | -0,23 -0,24 | 0,0001 0,0001 |
| ТИМ ОСА (мм) Извитость артериол, (у.е) | СРБ (мг/дл) | 0,28 0,18 | 0,001 0,048 |
| ТИМ ОСА (мм) | DAS28 | 0,20 | 0,005 |
| ТИМ ОСА (мм) ЭЗВД, % ЭНЗВД, % | Суммарная доза ГК (г) | 0,26 -0,22 -0,23 | 0,0001 0,001 0,001 |
| ТИМ ОСА (мм) ЭЗВД, % ЭНЗВД, % СREA, мкм СREA/ CRVE,(a/v) Извитость артериол, (у.е) | ПД – 24 мм.рт.ст. | 0,20 -0,28 -0,29 -0,21 -0,27 0,29 | 0,003 0,001 0,001 0,016 0,009 0,005 |
| ТИМ ОСА (мм) | РФ МЕд\мл. | 0,22 | 0,002 |
| СREA, мкм ТИМ ОСА (мм) | САД - 24 | -0,21 0,28 | 0,047 0,001 |
Корреляционная зависимость с высокой степенью достоверности установлена между показателями сосудистой дисфункции и уровнем пульсового артериального давления, что вполне объяснимо, поскольку сосудистая ригидность и создает условия для формирования последнего. Выявлена также взаимосвязь морфофункциональных маркеров сосудистой дисфункции со скоростью клубочковой фильтрации, индексом массы миокарда, маркерами воспалительной активности РА и суммарной дозой ГК.
Таким образом, у больных РА в сочетании с АГ в 46% случаев обнаружены атеросклеротические бляшки, частота эндотелиальной дисфункции составила 85,7%. Ремоделирование сосудов ассоциировалось с артериальной гипертонией и высокой активностью РА, что предполагает вклад последнего в развитие хронического воспаления сосудистой стенки.
Ф у н к ц и о н а л ь н о е с о с т о я н и е п о ч е к у больных РА
На первом этапе исследования по результатам анализа медицинской документации 750 пациентов, страдающих РА, минимальное повышение уровня креатинина было установлено у 119 чел. (15,9%). Недифференцированная протеинурия выявлена у 285 больных РА, что составило 38%. Показатели расчетной СКФ по формуле MDRD составили в среднем 65,2±4,9 мл/мин на 1.73 кв. м., по формуле Cocroft – Gault – 67,5±5,1 мл/мин. Снижение СКФ ниже 60 мл/мин выявлено у 293 (39,1%) пациентов, при сочетании РА с артериальной гипертонией этот показатель составил 59,9%. Значения СКФ в разные возрастные периоды, а также в зависимости от продолжительности РА представлены на рис. 6.
Рис.6. Скорость клубочковой фильтрации в зависимости от возраста и продолжительности РА (n=750).
На графике видно, что скорость клубочковой фильтрации закономерно снижалась с возрастом, и наименьшие показатели зарегистрированы в возрастной период после 70 лет. При этом до 59 летнего возраста намечался некоторый подъем СКФ, что объясняется нарастающей гиперфильтрацией с последующим угнетением фильтрационной способности почек. Так, в возрасте 20-39 значения СКФ составили в среднем 80,2±7,5мл/мин, в 40-49 лет – 85,3±7,0 мл/мин, в 50-59 лет – 90,0±4,5 мл/мин и после 60 лет -62,7±4,9 мл/мин и 59,0±3,9 соответственно. Подобная тенденция прослеживалась и при анализе зависимости СКФ от продолжительности ревматоидного артрита. При давности РА до 4 лет значения СКФ в среднем составили 79,0±6,9 мл/мин, от 5 до 10 лет – 77,2±7,5 мл/мин, от 10 до 14 лет 68,1±6,4 мл/мин и более 15 лет 65,3±6,4 мл/мин и 57,0±5,6 мл/мин соответственно. Снижение скорости клубочковой фильтрации за возрастной период от 20 до 70 лет произошло почти в 1,5 раза.
При детальном изучении патологии почек у больных ревматоидным артритом на втором этапе показатели креатинина составили у женщин 89,2 (85; 127) мкмоль/л, у мужчин- 92,0 (87; 134) мкмоль/л, расчетные показатели СКФ по MDRD 62,2 (55; 85) мл/мин и 63,5 (52; 84) мл/мин, по Cocroft – Gault 65,3 (56; 86) мл/мин и 64 (52; 85) мл/мин. соответственно. Частота снижения скорости клубочковой фильтрации ниже 60 мл/мин по MDRD составила у женщин–124 чел. (59,3%), у мужчин-22 (45,8%), по Cocroft – Gault 119 чел. 56,9% и 22 чел. 45,8% соответственно. Надо отметить, что частота снижения скорости клубочковой фильтрации была значимо выше показателей гиперкреатининемии: 59,3% (MDRD) и 56,9% (Cocroft – Gault) против 19,1% (р<0,01) у женщин и 45,8% (MDRD, Cocroft – Gault) против 14,6% ( р<0,01) у мужчин соответственно. Частота микроальбуминурии не превышала 15% как у мужчин, так и у женщин. Сравнительная характеристика больных РА в зависимости от функционального состояния почек показана в таблице 7.
Таблица 7
Сравнительная характеристика пациентов с РА в зависимости от СКФ
| Признак | СКФ ниже 60 мл/мин, n=146 | Нормальная СКФ, n=111 |
| Возраст (годы) | 66 (29;69) | 54 (30; 64) ** |
| Длительность менопаузы у женщин (лет) | 15 (1;40) | 7 (1; 36)** |
| Длительность РА (годы) | 14 (5; 20) | 8 (8; 15)* |
| Частота высокой активности РА | 42 (33,6%) | 23 (20,7%)* |
| Частота приема глюкокортикоидов | 55 (37,7%) | 48 (43,2%) |
| Кумулятивная доза ГК (гр.) | 5,6 (2,9; 7,1) | 1,9 (0,9; 3,2)** |
| Частота артериальной гипертензии | 96 (65,8%) | 42 (37,8%)** |
| Частота приема гипотензивной терапии# | 70 (72,9%) | 26 (61,9%) |
| Частота приема ИАПФ/БРА# | 51 (53,1%) | 20 (47,6%) |
| Частота достижения целевого уровня АД # | 23 (23,9%) | 12 (28,6%) |
| Частота изолированной систолической АГ | 29 (19,9%) | 1 (0,9%)** |
| Величина пульсового АД (ПАД) за 24 час. | 58,2 (49,8; 66,3) | 42,8 (40,1; 52,3)* |
| СРБ (мг/дл) | 1,07 (0,47; 5,01) | 0,68 (0,25; 1,5)* |
| ВАШ боли (оценивается пациентом, cм) | 6,5±2,3 | 4,6±1,9** |
| ИМТ (кг/м2 ) | 24,6±4,4 | 25,4±4,4 |
| Суммарный риск (по SCORE) | 7,5±0,9 | 3,2±0,4** |
| Толщина комплекса интима – медиа (мм) | 0,98±0,06 | 0,84±0,07** |
| Частота эндотелиальной дисфункции | 63 (51,6%) | 20 (25,6%)** |
| Общий холестерин (ммоль/л) | 5,36±0,9 | 4,9± 0,6** |
| ХС ЛПНП (ммоль/л) | 3,2± 0,4 | 2,5±0,3** |
# по отношению к числу больных АГ
Снижение скорости клубочковой фильтрации ассоциировалось с возрастом больных, длительностью менопаузы у женщин, высокой активностью РА и кардиоваскулярными осложнениями: эндотелиальной дисфункцией, гипертрофией миокарда ЛЖ, артериальной гипертонией с высоким пульсовым АД и атерогенной дислипидемией. В группе больных со сниженной СКФ при недостоверном преобладании в лечении ИАПФ/БРА, частота достижения целевых уровней АД была практически одинаковой.
Логистический регрессионный анализ позволил выделить факторы риска почечной дисфункции у больных с ревматоидным артритом, и значимые из них в рейтинговом порядке представлены в табл. 8.
Таблица 8
Факторы риска развития почечной дисфункции при РА
| Фактор | РА со СКФ<60 мл/мин, n=146 | РА СКФ>60, n=111 | OR(доверительный интервал) | Р по |
| (n, %) | (n, %) | |||
| Нон-диппер по СМАД | 52 (35,6) | 26 (23,4) | 1,85(1,0<OR<3,27) | 0,048 |
| ХС ЛПНП > 3,0 ммоль/л | 60 (41,1) | 28 (25,2) | 2,07(1,16<OR<3,68) | 0,011 |
| Возраст > 50 лет | 76 (52,1) | 37 (33,3) | 2,17 (1,26<OR<3,74) | 0,004 |
| Гипергликемия или СД | 30 (20,5) | 11 (9,9) | 2,35(1,06<OR<5,28) | 0,03 |
| РА более 10 лет | 112 (76,7) | 60 (54,1) | 2,80(1,58<OR<4,96) | 0,000 |
| ОХС > 5,0 ммоль/л | 56 (38,4) | 20 (18,0) | 2,83 (1,52<OR<5,33) | 0,000 |
| Суммарн. риск Score>5% | 58 (39,7) | 20 (18,0) | 3,00(1,61<OR<5,03) | 0,000 |
| АГ | 96 (65,8) | 42 (37,8) | 3,15 (1,83<OR<5,46) | 0,000 |
| ИСАГ(ПД > 55 мм.рт.ст) | 29(19,9) | 1 (0,9) | 4,38 (1,52<OR<13,6) | 0,003 |
| Активность DAS 28>5,1 | 55 (37,7) | 10 (9,0) | 6,10 (2,81<OR<13,6) | 0,000 |
| Микроальбуминурия | 36 (24,7) | 2 (1,8) | 17,8(4,05<OR<109,0 | 0,000 |
Проследить негативное влияние НПВП на скорость клубочковой фильтрации удалось путем сравнительного анализа больных РА со сниженной СКФ и контрольной группой (при соответствующей рандомизации по уровню СКФ). Так, длительный прием НПВП в первой группе подтвердили 129 пациентов, что составило 88,4%, во второй – 2 чел. (33,3% по отношению к числу больных со сниженной СКФ), OR-14,8; р<0,000. В отношении селективных ЦОГ-2 ингибиторов отмечена та же тенденция: 45 чел. (30,8%) против 1 чел. (16,6%) соответственно, OR-2,19; p=0,02. При этом продолжительное течение РА, как фактор риска снижения СКФ, косвенно может подтверждать длительное лекарственное поражение почек, в силу высокого удельного веса принимаемых НПВП среди больных ревматоидным артритом.
Результаты корреляционной зависимости скорости клубочковой фильтрации представлены в табл. 9.
Таблица 9
Корреляция параметров показателей почечной дисфункции
| Признак 1 | Признак 2 | РА, n=257 | |
| r | P | ||
| СС риск по SCORE (%) | СКФ (мл/мин) | -0,17 | 0,042 |
| ИММЛЖ (г/м 2 ) | СКФ (мл/мин) | -0,20 | 0,037 |
| СРБ (мг/дл) | СКФ (мл/мин) | -0,31 | 0,001 |
| DAS28 | СКФ (мл/мин) | -0,29 | 0,002 |
| Возраст (годы) | СКФ (мл/мин) | -0,33 | 0,000 |
| РА (годы) | СКФ (мл/мин) | -0,29 | 0,001 |
| ТИМ (мм) | СКФ (мл/мин) | -0,28 | 0,0001 |
| ПД – 24 (мм.рт.ст) | СКФ (мл/мин) А/кр, мг/моль | -0,31 0,20 | 0,000 0,032 |
| САД – 24 (мм.рт.ст.) | СКФ (мл/мин) | -0,19 | 0,026 |
А/кр- соотношения альбумин/креатинин мочи;.
Наиболее убедительная зависимость прослеживается между СКФ и возрастом больных, уровнем СРБ, пульсовым давлением и продолжительностью РА.
Обратнопропорциональная корреляция скорости клубочковой фильтрации и риском сердечно-сосудистых событий по SCORE в разные возрастные периоды у больных РА показана на рис.7.
Рис. 7. Динамика СКФ и риска по SCORE в разные возрастные периоды.
Из графика видно, что рост кардиоваскулярного риска по Score сопряжен с отрицательной динамикой СКФ, и это важно учитывать в клинической практике, особенно у больных РА.
По результатам наших наблюдений, снижение СКФ при ревматоидном артрите ассоциировалось с высокой активностью воспаления, и в этом случае поражение почек традиционно рассматривалось как наиболее частое осложнение хронического воспаления. Длительная противовоспалительная терапия НПВП, в том числе и селективными ЦОГ – 2 ингибиторами оказывала стойкое негативное влияние на формирование почечной дисфункции, в противоположность мнениям о нейтральных эффектах последних. Убедительно показаны клинико-патогенетические взаимосвязи сниженной СКФ с артериальной гипертонией, в том числе с высоким пульсовым АД, атерогенной дислипидемией и другими сердечно-сосудистыми осложнениями. Высокая частота артериальной гипертонии (65,8%) у больных РА со СКФ ниже 60 мл/мин подтверждает влияние гемодинамичеких факторов риска на функциональное состояние почек. При этом отсутствие гипертонии у 35% пациентов со сниженной СКФ предполагает не меньший вклад последствий РА.
Г и п е р т р о ф и я м и о к а р д а ЛЖ
Гипертрофия миокарда левого желудочка у больных РА оценивалась по результатам ЭКГ и данным ЭХОКГ с расчетом индекса массы миокарда (табл. 10). Из таблицы видно, что более чем у 40% больных РА была установлена гипертрофия ЛЖ, при отсутствии значимых различий по частоте и структуре в зависимости от пола.
Таблица 10
Характеристика поражения миокарда при РА
| Показатель | Женшины, n=209(Mе, ИИ) | Мужчины, n=48 (Mе,ИИ) | p |
| Индекс Соколова Лайона,мм | 26,9 (18; 38) | 25,8 (19; 37) | 0,52 |
| Частота гипертрофии по ЭКГ (n, %) | 70 (33,5) | 20 (41,7) | 0,36 |
| ИММЛЖ, г\м | 105 (94; 114) | 115 (102; 123) | 0,12 |
| Гипертрофия по ИММЛЖ (n, %) | 85 (40,7) | 20 (41,7) | 0,71 |
| Частота концентрической ГЛЖ(n, %) | 31 (14,8) | 6 (12,5) | 0,67 |
| Частота эксцентрической ГЛЖ (n, %) | 38 (18,2) | 9 (18,8) | 0,92 |
| Концентрическое ремоделирование (n, % ) | 48 (23) | 10 (20,8) | 0,75 |
| Нормальная геометрия ЛЖ (n, % ) | 92 (44) | 23 (47,9) | 0,62 |
Пошаговый многофакторный логистический регрессионный анализ позволил выделить факторы, влияющие на патологическое ремоделирование миокарда у больных РА (рис. 8).
Рис.8. Факторы риска гипертрофии миокарда ЛЖ при РА (*p<0,05; **p<0,01)
У больных РА с гипертрофией миокарда ЛЖ достоверно чаще встречалось сочетание с артериальной гипертонией, в том числе высоким ПД, что вполне определяет гемодинамические предпосылки формирования патологического ремоделирования. Выявлена также ассоциация гипертрофии ЛЖ с возрастом старше 50 лет, избыточной массой тела, гиперхолестеринемией, продолжительностью и высокой активностью РА. Длительный прием глюкокортикоидов в высоких дозах, снижение СКФ и ЧСС-24 свыше 70 уд/мин увеличивали риск ГЛЖ у больных РА в более чем 2 раза.
В таблице 11 представлены результаты корреляционных взаимосвязей ИММЛЖ.
Таблица 11
Корреляционный анализ ИММЛЖ у больных РА
| Признак 1 | Признак 2 | Коэффициент корреляции, r | P |
| ИММЛЖ (г/м 2 ) | Суммарная доза ГК, г. | 0,21 | 0,001 |
| ИММЛЖ(г/м 2 ) | СС риск по SCORE (%) | 0,28 | 0,000 |
| ИММЛЖ (г/м 2 ) | СКФ (мл/мин) | -0,20 | 0,037 |
| ИММЛЖ (г/м 2 ) | СРБ (мг/дл) | 0,20 | 0,009 |
| ИММЛЖ (г/м 2 ) | ИМТ (кг/м) | 0,36 | 0,000 |
| ИММЛЖ (г/м 2 ) | ОТ (см) | 0,33 | 0,000 |
| ИММЛЖ (г/м 2 ) | ПД – 24 | 0,19 | 0,044 |
| ИММЛЖ (г/м 2 ) | ЭЗВД, % ЭНЗВД, % | -0,23 -0,24 | 0,0001 0,0001 |
Таким образом, частота гипертрофии миокарда ЛЖ по данным ЭКГ составила 35%, по ИММЛЖ - 40,9%. Ключевую роль в формировании гипертрофии миокарда ЛЖ у больных РА, как показали наши расчеты, играют артериальная гипертония с высоким ПД, ЧСС - 24 свыше 70 уд/мин, возраст, избыточная масса тела и гиперхолестеринемия. Убедительная корреляция между ИММЛЖ, суммарной дозой ГК, СРБ и СКФ подтверждают влияние воспаления и РА в формирование негативного профиля ремоделирования миокарда.
2.2. Ишемическая болезнь сердца у больных РА
На первом этапе нашего исследования был проведен анализ частоты и структуры ишемической болезни сердца у 750 больных РА в г.Иркутске, Иркутской области, республики Бурятия по результатам анкетирования и анализа медицинской документации. ИБС была выявлена у 142 больных, что составило 18,9%. В структуре клинических форм ИБС доминировала стенокардия напряжения второго функционального класса, которая была диагностирована у 122 больных РА, что составило 85,9% от числа всех случаев с ИБС и 16% к числу опрошенных. Кроме этого, постинфарктный кардиосклероз установлен у 20 (14,1%) пациентов, страдающих РА. Диагностика ИБС на амбулаторном этапе основывалась большей частью на жалобах пациентов без детальной инструментальной верификации. Основным методом при постановке диагноза ИБС была стандартная ЭКГ. Проба с физической нагрузкой не проводилась ни в одном из анализируемых случаев, что вполне объяснимо, учитывая функциональную недостаточность суставов у больных РА. Частота проведения суточного мониторирования ЭКГ по результатам медицинской документации составила не более 10%.
Детальная верификация ИБС проводилась на втором этапе нашего наблюдения у 257 пациентов РА. Жалобы на боли в области сердца предъявляли 205 (79,8%) обследуемых пациентов РА. Типичные ангинозные боли установлены у трети больных – 62 (24,1%). Наибольший удельный вес составили вертеброгенные кардиалгии – 100 (38,9%) пациентов.
По результатам ЭКГ покоя ишемические изменения были зафиксированы у 13,6% больных РА, БЛНПГ – 7%, ПИКС – 8,9%. У 21% больных отмечена фибрилляция предсердий.
Структура и частота выявленной патологии после ХМ ЭКГ представлена в таблице 12.
Таблица 12
Структура патологии по результатам ХМ ЭКГ
| Показатели | Жен. n=209 (n,%) | Муж.n=48 (n,%) | n=257 (n,%) |
| Нарушения ритма | 164 (78,5) | 40 (83,3) | 204 (79,4) |
| Экстрасистолия | 87 (41,6) | 10 (20,8)* | 97 (37,7) |
| Фибрилляция предсердий | 60 (28,7) | 14 (29,1) | 74 (28,8) |
| Синусовая тахикардия | 109 (52,1) | 30 (62,5) | 139 (54,1) |
| Ишемия | 43 (20,6) | 18 (37,5)* | 61 (23,7) |
| Нарушения проводимости | 64 (30,6) | 19 (39,6) | 83 (32,3) |
| БЛНПГ | 12 (5,7) | 6 (12,5) | 18 (7,0) |
| БПВЛНПГ | 27 (12,9) | 6 (12,5) | 33 (12,8) |
| АV блокады | 25 (11,9) | 7 (14,6) | 32 (12,5) |
| ПИКС | 16 (7,7) | 7 (14,6) | 23 (8,9) |
| Без патологии | 74 (35,4) | 7 (14,6) | 81 (31,5) |
*р<0,05 (по )
Сравнительная характеристика патологии, выявленной методом ХМ ЭКГ и ЭКГ покоя, представлена в таблице 13.
Таблица 13
Сравнительная характеристика частоты выявленной ЭКГ патологии
| Патология | ЭКГ n,% | ХМ ЭКГ n,% | р (по ) |
| Без патологии | 126 (49) | 81 (31,5) | 0,0007 |
| Ишемия | 35 (13,6) | 61 (23,7) | 0,004 |
| ПИКС | 23 (8,9) | 23 (8,9) | 1,0 |
| ФП | 54 (21) | 74 (28,8) | 0,04 |
| БЛНПГ | 18 (7) | 18 (7) | 1,0 |
| БПВЛНПГ | 33 (12,8) | 33 (12,8) | 1,0 |
| AV блокады | 13 (5) | 32 (12,5) | 0,004 |
| Экстрасистолия | 88 (34) | 97 (37,7) | 0,4 |
Метод суточного мониторирования ЭКГ у больных РА позволил достоверно чаще по сравнению с ЭКГ покоя верифицировать ишемические изменения, фибрилляцию предсердий и нарушения AV проводимости. Число нормальных электрокардиограмм без патологии после проведения ХМ значительно уменьшилось и составило 81 (31,5%) против 126 (49%), р<0,01.
Наиболее значимые факторы риска ИБС у больных РА представлены на рис. 9. Наряду с традиционными, такими как возраст, гипергликемия, дислипидемия, высокая ЧСС, избыточная масса тела, семейный анамнез ССЗ, курение и артериальная гипертензия, установлены предикторы, ассоциирующиеся с хроническим воспалением. Так, высокая активность и продолжительность РА более 10 лет, ВАШ боли > 50 мм, прием глюкокортикоидов свыше 12 мес. в суммарной дозе более 3,0 г.в пересчете на преднизолон, а также сопутствующая анемия, которая является частым осложнением РА, увеличивают риск ишемической болезни сердца у данной категории больных.
Рис.9. Факторы риска ИБС у больных РА (*р<,05; **p<0,01)
Таким образом, частота ИБС у больных, страдающих ревматоидным артритом, составила 118 чел (45,9%), в том числе больных со стенокардией напряжения- 62 (52,5%) чел., безболевой ишемией – 30 (25,4%) чел. и 26 чел.(22,1%) с нарушением ритма. Особенностью течения ИБС при РА явилась высокая частота безболевых форм, ассоциация с активностью воспаления и приемом глюкокортикоидов.
2.3. Оценка общего сердечно-сосудистого риска у больных РА
Общий сердечно-сосудистый риск у больных ревматоидным артритом мы оценили с учетом степени повышения АД, поражения органов – мишеней и наличия ассоциированных клинических состояний после детального проведения клинической и инструментальной верификации (рис. 10 и 11).
Рис. 10. Сравнительная характеристика стадий АГ у больных РА (*р<0,01)
Из графика видно, что после детальной оценки у больных РА достоверно значимо снизился удельный вес пациентов со второй стадией АГ, и выросла частота больных с ассоциированными клиническими состояниями и высоким риском осложнений.
Рис. 11. Сравнительная характеристика показателей общего риска у больных РА (*р<0,05; **p<0,01).
Подход к прогнозированию сердечно-сосудистого риска у больных РА по совокупности признаков привел к группированию объектов для выявления наиболее сильных неблагоприятных предикторов. Для решения этого вопроса была проведена кластеризация всей выборки (n=207, количество больных после коррекции по значимости оцениваемых признаков) и сформировано 3 кластера. В первый вошло 101 (48,8%) больных, во второй – 74 (35,7%), в третий – 32(15,5%) (рис.12).

Рис. 12. Распределение кластеров по результатам дискриминантного анализа.
Точность и статистическая достоверность распределения групп оценивалась с помощью дискриминантного анализа. Высокие значения канонической корреляции (Canonic.R=0,941) и критерия хи–квадрат (=630,4) при нулевой вероятности не отвергнуть нулевую гипотезу (p=0,000) и совпадении результатов дискриминации и кластерного анализа в 95% случаев позволили предполагать надежность модели, построенной на основе предложенных переменных. Ключевыми факторами распределения на кластеры явились ПАД; прием ГК; активность РА по DAS 28>3,2; эндотелиальная дисфункция; ТИМ > 0,9; ИМТ; состояние МПКТ; ИММЛЖ и стадия РА. Кластерные усреднения и евклидовы метрики позволили оценить расстояние между кластерами и проследить близость и/или удаленность членов кластера друг от друга (табл. 14).
Таблица 14
Евклидовы расстояния и их квадраты между кластерами
| Номер кластера | Эвклидовы расстояния и их квадраты между кластерами (Euclidean Distances between Clusters Distances below diagonal Squared distances above diagonal) | ||
| 1 | 2 | 3 | |
| 1 | 0,000000 | 0,929871 | 1,198645 |
| 2 | 0,964298 | 0,000000 | 0,332783 |
| 3 | 1,094827 | 0,576874 | 0,000000 |
Наиболее приближенными друг к другу оказались кластеры 2 и 3 (рис.13). Пациенты первого кластера по сравнению со вторым и третьим, имели наименьший риск сердечно-сосудистых заболеваний и их осложнений. Второй и третий кластер составили пациенты с сердечно-сосудистыми заболеваниями и высоким риском осложнений по SCORE, при этом третий кластер отличался выраженностью и тяжестью оцениваемых признаков.
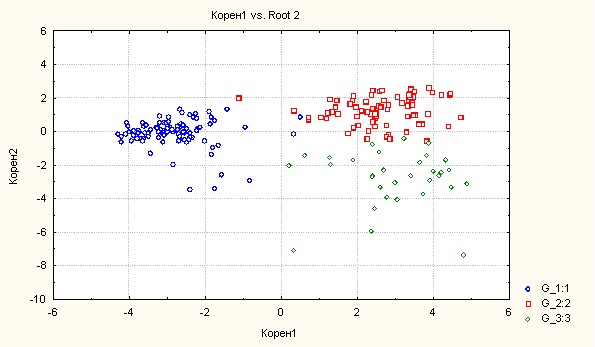
Рис. 13. Расстояние между кластерами
Общими показателями для последних двух классов явились артериальная гипертония, скорость клубочковой фильтрации менее 60 мл/мин, снижение МПКТ до степени остеопении и/или остеопороза, гиперхолестеринемия, уровень ХС ЛПНП более 3,0 ммоль/л и продолжительность РА свыше 5 лет. Интересно было проанализировать и обнаружить факторы, которые явились ключевыми для выделения третьего кластера. Наибольший сердечно-сосудистый риск у больных РА ассоциировался с длительным приемом глюкокортикоидов в суммарной дозе, превышающей 5,0 г. в пересчете на преднизолон и продолжительностью ревматоидного артрита более 10 лет. Второй кластер может быть рассмотрен как группа риска тяжелых кардиоваскулярных осложнений при ревматоидном артрите. Факторами, которые наряду с выше перечисленными переменными, позволили объединить пациентов во второй кластер, явились пульсовое давление более 55мм.рт.ст., высокая активность воспаления по DAS 28, гиперхолестеринемия, ТИМ>0,9 мм и гипертрофия ЛЖ. Эти показатели можно расценивать как серьезные предикторы негативного прогноза в отношении сердечно-сосудистых заболеваний. Анализ и сравнительная характеристика больных после кластеризации представлена в табл. 15.
Таблица15
Сравнительная характеристика больных после распределения на кластеры
| Признак | Кластер 1, n=101 (абс.чис., %) | Кластер 2 n=74 (абс.чис., %) | Кластер 3 (n=32) (абс.чис., %) |
| 1 | 2 | 3 | |
| Возраст >50 лет | 36 (35,6) | 35 (47,3) | 20 (62,5) (1-3) **; (2-3) * |
| РА более 10 лет | 55 (54,5) | 55 (74,3) | 29 (90,6) (1-2)**;(1-3)**; (2-3)** |
| Наследств.по ССЗ | 22 (21,8) | 25 (33,8) | 15 (46,9) (1-2)*; (1-3)** |
| ОХС > 5,0 ммоль/л | 20 (19,8) | 26 (35,1) | 16 (50) (1-2)*; (1-3)**; (2-3)* |
| ХСЛПНП > 3,0ммоль/л | 26 (25,7) | 28 (37,8) | 18 (56,3) (1-3)**; (2-3)** |
| ВАШ боли > 50мм | 25 (24,8) | 35 (47,3) | 22 (68,8) (1-2)**; (1-3)**; (2-3)** |
| DAS 28> 5,1 | 19 (18,1) | 15 (20,3) | 19 (59,4) (1-3)**; (2-3)** |
| Суммарн. доза ГК>3г. | 16 (15,8) | 20 (27,0) | 19 (59,4) (1-3)**; (2-3)** |
| Суммарн. доза ГК > 5г | 5 (4,9) | 9 (12,2) | 12 (37,5) (1-3)**; (2-3)** |
| Гипергликемия или СД | 10 (9,9) | 7 (9,5) | 16 (50) (1-3)**; (2-3)** |
| СКФ < 60 мл/мин | 56 (55,4) | 35 (47,3) | 27 (84,4) (1-3)**; (2-3)** |
| Частота АГ | 35 (34,7) | 30 (40,5) | 26 (81,3) (1-3)**; (2-3)** |
| ПД – 24> 55 мм.рт.ст. | 8 (7,9) | 11 (14,9) | 9 (28,1) (1-3)**; (2-3)* |
| ТИМ ОСА >0,9 | 10 (9,9) | 15 (20,3) | 13(40,6) (1-2)*; (1-3)**; (2-3)** |
| ЭД (n,%) | 32 (31,7) | 23 (31,2) | 25 (78,1) (1-3)**; (2-3)** |
| Гипертрофия по ИММЛЖ | 25 (24,8) | 35 (47,3) | 22 (68,8) (1-2)**; (1-3)**; (2-3)** |
| ОП (L2-L4) | 26 (25,7) | 25 (33,8) | 22 (68,8) (1-3)**; (2-3)** |
| ОП ( total hip) | 12 (11,9) | 8 (10,8) | 19 (59,4) (1-3)**; (2-3)** |
| Частота переломов | 20 (19,8) | 23 (31,2) | 20 (62,5) (1-3)**; (2-3)** |
(* p<0,05; **p<0,01 по)
Дискриминантный анализ позволил на основании выделенных по результатам наших наблюдений факторов построить математическую модель прогнозирования сердечно-сосудистого риска у больных РА. Коэффициент канонической корреляции R составил 0,877. Значения статистики лямбда Уилксона 0,231 свидетельствуют о хорошей дискриминации (при показателях - 291,5, р<0,01). Установленным признакам были присвоены градации (Х1 - 12) и числовые значения, где:
Х1 – уровень общего холестерина больше 5,0 ммоль/л: нет – 0, есть – 1;
Х2 – скорость клубочковой фильтрации менее 60 мл/мин: нет – 0, есть – 1;
Х3 – пульсовое артериальное давление более 55 мм.рт.ст.: нет – 0, есть – 1;
Х4– уровень холестерина ЛПНП больше 3,0 ммоль/л: нет – 0, есть – 1;
Х5 – активность РА по DAS 28 больше 3,2: нет – 0, есть – 1;
Х6 – длительность заболевания РА более 10 лет: нет – 0, есть – 1;
Х7 – среднесуточная ЧСС более 70 уд/мин: нет – 0, есть – 1;
Х8 – суммарная доза ГК более 3,0 в пересчете на преднизолон: нет – 0, есть – 1;
Х9 – интенсивность болевого синдрома по ВАШ, оцениваемая пациентом, более 50 мм: нет – 0, есть – 1;
Х10 –толщина комплекса интима медиа (ТИМ) более 0,9 или наличие атеросклеротической бляшки (по результатам УЗДГ сонных артерий): нет – 0, есть – 1;
Х11 – продолжительность менопаузы более 5 лет: нет – 0, есть – 1;
Х12 – уровень СРБ более 1,5 мг/дл: нет – 0, есть – 1.
Значения Х1-Х12 – это стандартизованные исходные данные, рассчитанные по формуле: Z = (Х I – Х)/s, где Z – значения исходного распределения, Х I – результаты измерений распределения с исходной размерностью, Х и s – среднее значение и стандартное отклонение. Определены значения констант F1 и F2: F1 = -1,68; F2 = -3,25.
Установлены коэффициенты дискриминантной функции К1j и K2j, результаты полученной дискриминации представлены в табл. 16.
Таблица 16
| Факторы риска | Градации | К1j | K2j |
| 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть 0 - нет, 1 – есть | -0,56 -1,08 -0,34 -0,89 -0,33 -0,41 -0,41 -0,37 -0,29 -0,34 -0,29 0,25 | 0,79 1,55 0,49 1,28 0,48 -0,58 0,58 0,53 0,43 0,48 0,42 -0,36 |
Установив градации и числовые значения факторов риска, определяют прогностические коэффициенты F1 и F2 по следующим формулам:
F1= - 1,68 – 0,56*Х1 – 1,08*Х2 – 0,34*Х3 – 0,89*Х4 – 0,33*Х5 – 0,41*Х6 – 0,41*Х7 – 0,37*Х8 – 0,29*Х9 – 0,34*Х10 – 0,29* Х11 + 0,25*Х12
F2= - 3,25 + 0,79*Х1 + 1,55*Х2 + 0,49*Х3 + 1,28*Х4 + 0,48*Х5 – 0,58*Х6 + 0,58*Х7 + 0,53*Х8 + 0,43*Х9 + 0,48* Х10 + 0,42* Х11 – 0,36*Х12
При абсолютной величине F2 большей абсолютной величины F1 прогнозируют высокий риск, а при значении F2 меньше F1 - низкий риск развития сердечно-сосудистых заболеваний и их осложнений у пациентов, страдающих ревматоидным артритом.
Клинические наблюдения свидетельствуют о том, что данная математическая модель позволяет осуществить прогноз развития сердечно-сосудистых осложнений у конкретного больного, страдающего РА с правильностью распознавания более 90%.
2.4. Клинико-патогенетические взаимосвязи сердечно-сосудистой патологии и МПКТ у больных РА
Проблема остеопороза и переломов, традиционно ассоциировалась с возрастом, продолжительной менопаузой, гиподинамией и низким ИМТ. Хорошо известна проблема вторичного остеопороза у больных, страдающих РА. На риск развития переломов при РА по результатам наших наблюдений влияли продолжительное течение РА, активность по DAS 28, болевой синдром, высокие по сравнению с больными без переломов показатели СРБ. Характеристика больных с переломами представлена в табл. 17.
Таблица 17
Характеристика больных РА с переломами
| Показатель | РА с переломами, n=78 (М, SD) | РА без переломов, n=179 (М, SD) | P |
| Возраст, лет | 60,8±10,6 | 52,2±11,8 | 0,000 |
| Менопауза, годы | 14,1±5,5 | 4,5±5,8 | 0,000 |
| ОТ, см | 100,5±8,2 | 104,1±7,0 | 0,000 |
| РА, годы | 14,9±8,5 | 9,8±8,0 | 0,000 |
| ОХС, ммоль/л | 5,3±1,5 | 4,5±1,3 | 0,000 |
| ХС ЛПНП, ммоль/л | 3,2±1,2 | 2,5±0,9 | 0,000 |
| ХС ЛПВП, ммоль/л | 0,85±0,3 | 1,1±0,4 | 0,000 |
| ТГ, ммоль/л | 2,3±0,7 | 1,4±0,6 | 0,000 |
| СРБ, мг/дл | 2,7±1,2 | 1,2±0,9 | 0,000 |
| Ходьба < 1 ч/сутки (n,%) | 70 (89,7) | 115 (64,2) | 0,000* |
| ВАШ боли, мм | 61,4±8,5 | 41,6±10,9 | 0,000 |
| Активность по DAS 28 | 6,9±2,1 | 3,5±2,5 | 0,000 |
| Прием ГК (n,%) | 48 (61,5) | 55 (30,7) | 0,000* |
| Прием ГК, мес. | 22,5±5,3 | 11,2±4,9 | 0,000 |
| Суточная доза, мг/сут | 7,9±2,5 | 5,0±0,9 | 0,000 |
| Суммарная доза ГК, г | 5,1±2,2 | 1,8±0,9 | 0,000 |
| Число в/суст. инъекций | 15,5±4,1 | 7,8±2,6 | 0,000 |
| Неэффективность БТ | 24 (30,8) | 29 (16,2) | 0,012* |
| СКФ < 60 мл/мин | 56 (71,8) | 90 (50,3) | 0,002* |
| Частота ИБС (n,%) | 49 (62,8) | 69 (38,5) | 0,000* |
* р по
Как видно из результатов сравнительного анализа, прием глюкокортикоидов, в том числе и в виде внутрисуставных инъекций, убедительно ассоциировался с переломами у больных РА. Неэффективность и/или непереносимость базисной терапии достоверно чаще была установлена у больных с переломами, что является вполне предсказуемым, так как это создает предпосылки для прогрессирования ревматоидного артрита и остеопороза. Наибольший интерес представляет состояние липидного спектра у больных с переломами в виде статистически значимых атерогенных дислипидемий. Более чем у 60% больных РА с переломами наблюдалось сочетание с ИБС. Снижение скорости клубочковой фильтрации у больных РА, как показано по нашим наблюдениям, также формирует условия для прогрессирования остеопатии с развитием переломов.
Остеопороз в группе больных с переломами по результатам ОДМ выявлен у 29 чел. (64,5%), без переломов – 44 чел. (41,9%), р<0,01. Частота остеопороза вне зависимости от наличия переломов у больных РА составила в среднем 48,7%. Остеопенический синдром установлен у 11 (24,4%) пациентов с переломами против 28 (26,7%) - без переломов, р>0,05. Лишь у 5 (11,1%) пациентов с переломами (в группе больных РА без переломов этот показатель составил 33 (31,4%, р<0,01) состояние минеральной плотности костной ткани соответствовали нормальным показателям. Почти у половины больных, страдающих РА, установлен остеопороз, у трети пациентов – остеопения. Следовательно, более чем 70% больных РА имели дефицит костной массы различной степени выраженности.
Статистически значимые факторы риска ОП и переломов у больных РА представлены в табл. 18.
Таблица 18
Факторы риска остеопороза и переломов при РА
| Показатель | РА с ОП и переломами, n=29 (n,%) | РА без ОП и переломов, n=61 (n,%) | OR |
| РА> 10 лет | 27 (93,1) | 33 (54,1) | 11,3**(4,5<OR<29,7) |
| СРБ>1,5 мг/дл | 15 (51,7) | 10 (16,4) | 5,46**(2,8<OR<11,6) |
| Акт. по DAS 28 >5,1 | 13 (44,8) | 9 (14,8) | 4,64**(2,2<OR<9,6) |
| Суммарная доза ГК>3.0 | 13 (44,8) | 10 (16,4) | 4,30**(2,1<OR<8,83) |
| Переломы в анамнезе | 13 (44,8) | 10 (16,4) | 4,30**(2,1<OR<8,83) |
| ОХС>5,0 ммоль/л | 14 (48,3) | 12 (19,7) | 3,69**(1,71<OR<7,2) |
| ХС ЛПНП>3,0 ммоль/л | 15 (51,7) | 15 (24,6) | 3,2** (1,71<OR<6,20) |
| Частота ИМ | 4 (13,8) | 3 (4,9) | 3,0* (0,99<OR<10,3) |
| СКФ < 60 мл/мин | 22 (75,9) | 32 (52,5) | 2,81** (1,47<OR<5,3) |
| ВАШ боли, мм | 16 (55,2) | 20 (32,8) | 2,48**(1,3<OR<4,59) |
| Частота АГ | 19 (65,5) | 29 (47,5) | 2,09*(1,14<OR<3,85) |
| Высокий риск по Score | 8 (27,6) | 10 (16,4) | 2,04* (0,97<OR<4,32) |
| Частота ИБС | 16 (55,2) | 25 (40,9) | 1,76* (0,97<OR<3,24) |
*р<0,05; **<0,01 (по )
Наиболее значимыми факторами, влияющими на развитие остеопороза с переломами при РА, явились продолжительность ревматоидного артрита свыше 10 лет, уровень СРБ более 1,5 мг\дл и высокая активность по DAS 28. Не менее важную роль в нашем наблюдении подтвердил факт приема глюкокортикоидов в суммарной дозе свыше 3,0 г. Указания на переломы в анамнезе увеличивали риск последующих переломов при РА в более чем 4 раза. Установлено статистически значимое влияние сопутствующей кардиоваскулярной патологии на риск развития ОП и переломов при РА. Причем в последнем случае убедительно можно предполагать лишь о влиянии коморбидных состояний на повышенный риск падений и переломов у данной категории больных. Получила свое подтверждение ассоциация ОП и его осложнений с атерогенными дислипидемиями и снижением скорости клубочковой фильтрации.
Единые факторы риска ОП и кардиоваскулярной патологии у больных РА представлены на рис. 14.
Рис. 14. Единые факторы риска при РА.
Учитывая вышеуказанное, необходимо формировать группы повышенного риска сердечно-сосудистых заболеваний и остеопороза при ревматоидном артрите и наибольшую прогностическую значимость в этом отношении имеет высокая активность РА, его продолжительность свыше 10 лет, прием глюкокортикоидов, снижение скорости клубочковой фильтрации и ассоциация с атерогенными дилипидемиями.
Ключевым маркером воспаления традиционно признан С-реактивный белок. В таблице 19 представлены результаты корреляции СРБ с МПКТ и некоторыми количественными показателями, отражающими сердечно-сосудистую патологию.
Таблица 19
Корреляционный анализ СРБ при РА
| Признак 1 | Признак 2 | Коэффициент корреляции, r | P |
| CРБ, мг\дл | ТИМ ОСА (мм) | 0,28 | 0,001 |
| CРБ, мг\дл | Извитость артериол, (у.е) | 0,18 | 0,048 |
| CРБ, мг\дл | СКФ (мл/мин) | -0,31 | 0,001 |
| CРБ, мг\дл | ПД-24 по СМАД | 0,21 | 0,0031 |
| CРБ, мг\дл | ОХС, ммоль/л ХС ЛПНП, ммоль/л ХС ЛПВП, ммоль/л | 0,20 0,19 -0,18 | 0,009 0,003 0,003 |
| CРБ, мг\дл | ИММЛЖ (г/м 2 ) | 0,20 | 0,009 |
| CРБ, мг\дл | Т-критерий (L2-L4) | -0,18 | 0,002 |
Из таблицы видно, что взаимосвязи СРБ с некоторыми клиническими эквивалентами при ревматоидном артрите очевидны. Как обсуждалось в предыдущих главах, установлена статистически значимая корреляция СРБ с ТИМ общей сонной артерии и ангиопатией сетчатки, что подтверждает влияние воспаления на сосудистую дисфункцию у больных, страдающих РА. Установлены связи СРБ со СКФ, показателями липидного спектра и ИММЛЖ. Вполне предсказуемой выглядит обратно пропорциональная корреляция СРБ с Т-критерием поясничного отдела позвоночника по остеоденситометрии у пациентов РА. Интересно, что не получено статистически значимой зависимости СРБ и показателя Т-критерия области шейки бедра. Эти данные подтверждают клинические наблюдения в отношении доминирующей патологии позвоночника при РА и остеопорозе.
Таким образом, частота переломов у больных РА составила 25,3%. Остеопороз и переломы у больных РА были связаны с возрастом, длительностью менопаузы, гиподинамией и ИБС. Наиболее значимыми предикторами дефицита МПКТ и переломов явились высокая активность по DAS 28 и продолжительность РА свыше 10 лет, атерогенные дислипидемии, уровень СРБ, переломы в анамнезе, прием ГК и снижение скорости клубочковой фильтрации. Единые факторы риска ОП и кардиоваскулярной патологии при РА позволят формировать группы повышенного риска.
2.5. Кардиоваскулярная патология у больных спондилоартритами и остеоартрозом
2.5.1. Кардиоваскулярная патология у больных спондилоартритами
Ч а с т о т а а р т е р и а л ь н о й г и п е р т о н и и оценивалась у 300 больных серонегативными спондилоартритами в г.Иркутске, Иркутской области, республики Бурятия по результатам анкетирования и анализа медицинской документации. В Иркутске и Братске этот показатель составил 25%, Ангарске – 20%, Усть – Илимске –20,8%, других регионах Иркутской области и республики Бурятия -23,2%. В среднем частота АГ по результатам первого этапа составила 24 %, у мужчин - 23,1%, у женщин -26,2% (р>0,05). После проведения СМАД артериальная гипертония была выявлена у 28 пациентов, что составило 37,3%, при этом у 26,7% больных, страдающих СА, гипертония была выявлена впервые.
Для установления факторов риска артериальной гипертензии у больных СА, проведен пошаговый многофакторный логистический регрессионный анализ, и статистически значимые результаты представлены в табл. 20.
Таблица 20
Факторы риска АГ у больных спондилоартритами
| Фактор | с АГ (n=28) | Без АГ(n=47) | OR(доверительный интервал) | Р |
| абс.число(%) | абс.число(%) | |||
| СРБ>1,5 мг\дл | 19 (67,9) | 9 (19,1) | 8,91 (2,70<OR<30,6) | 0,000 |
| Системные проявления | 18 (64,3) | 9 (19,1) | 7,60 (2,34<OR<25,6) | 0,000 |
| Гиперурикемия | 11 (39,3) | 5 (10,6) | 5,44 (1,44<OR<21,5) | 0,008 |
| ТГ > 2,0 ммоль/л | 14 (25) | 8 (17) | 4,88 (1,50<OR<16,3) | 0,003 |
| СА более 10 лет | 20 (71,4) | 17 (36,2) | 4,41 (1,44<OR<13,9) | 0,003 |
| Утр. сков. > 120 мин | 18 (64,3) | 14 (29,8) | 4,24 (1,41<OR<13,1) | 0,004 |
| СКФ < 60 мл/мин | 12 (42,9) | 9 (19,1) | 3,17 (0,99<OR<10,3) | 0,028 |
| Прием ГК | 12 (42,9) | 10 (21,3) | 2,78 (0,89<OR<8,79) | 0,048 |
Таким образом, частота АГ при спондилоартритах по результатам медицинской документации составила 24%, по СМАД – 37,3%, р<0,05. Факторами риска гипертонии явились высокая активность воспаления, гиперурикемия, гипертриглицеридемия, продолжительность спондилоартри-та свыше 10 лет, снижение СКФ и прием ГК.
П о р а ж е н и е с о с у д о в п р и с п о н д и л о а р т р и т а х
У пациентов, страдающих анкилозирующим (АС) и псориатическим спондилоартритами (ПсА), толщина комплекса интима–медиа составила в среднем 0,84 (0,79;1,05) мм. У трети обследованных больных (9 чел 30%) СА степень утолщения комплекса интима – медиа соответствовала состоянию сосудистой бляшки. Частота ЭЗВД составила 50%, ЭНЗВД – 60%, т.е. более чем у половины больных СА параметры сосудистых реакций соответствовали критериям эндотелиальной дисфункции, т.е. вариабельность диаметра плечевой артерии была менее <10% от исходных показателей. Факторами риска сосудистой дисфункции у больных, страдающих серонегативными спондилоартритами, явились артериальная гипертензия (OR-4,87; р<0,01), СРБ>2,0 мг\дл (OR-4,05, р<0,01), прием ГК (OR-3,88, р<0,01), снижение СКФ (OR-2,77; p<0,01) и возраст старше 50 лет (OR-2,45, р<0,05).
Показатели корреляционной зависимости маркеров сосудистого ремоделирования у больных СА представлены в табл. 21.
Таблица 21
Корреляция параметров показателей сосудистой дисфункции у больных СА
| Признак 1 | N | Признак 2 | СА, n=30 | |
| r | Р | |||
| СС риск по SCORE (%) | 50 | ТИМ ОСА (мм) | 0,24 | 0,045 |
| СКФ (мл/мин) | 50 | ТИМ ОСА (мм) | -0,20 | 0,047 |
| СРБ (мг/дл) | 50 | ТИМ ОСА (мм) | 0,29 | 0,011 |
| Активность по BASDAI | 30 | ТИМ ОСА (мм) | 0,28 | 0,025 |
| Суммарная доза ГК (г) | 50 | ТИМ ОСА (мм) | 0,24 | 0,015 |
Наиболее убедительная корреляционная зависимость установлена между толщиной КИМ, скоростью клубочковой фильтрации, уровнем СРБ, активностью АС по BASDAI, риском сердечно-сосудистых осложнений по SCORE и суммарной дозой ГК.
Ф у н к ц и о н а л ь н о е с о с т о я н и е п о ч е к исследовалось на первом этапе наших наблюдений у 300 пациентов, страдающих СА. Минимальное повышение уровня креатинина установлено у 30 чел. (10%). Частота недифференцированной протеинурии составила 28% и была зафиксирована у 84 больных СА. Показатели расчетной скорости клубочковой фильтрации по формуле MDRD составили в среднем 67,4±5,1мл/мин на 1.73 кв. м., по формуле Cocroft – Gault – 66,5±4,1 мл/мин. Снижение СКФ ниже 60 мл/мин установлено у 78 больных СА, что составило 26 %.
При детальном изучении функционального состояния почек показатели креатинина составили у больных анкилозирующим спондилитом 80,1 (78; 107) мкмоль/л, псориатическим артритом - 91,0 (88; 124) мкмоль/л, р<0,05. Повышение креатинина >133 мкмоль у мужчин и 124 мкмоль у женщин установлено при АС в 16,7% случаев, при ПсА- 25,9%. Снижение СКФ < 60 мл/мин по MDRD было зафиксировано у 12 мужчин (25%) и 9 женщин (33,3%), по Cocroft – Gault – 11 чел. (22,9%) и 9 чел. (33,3%) соответственно. Частота снижения скорости клубочковой фильтрации составила в среднем 28% по формуле MDRD и 26,7% по Cocroft – Gault. Микроальбуминурия у больных АС установлена в 12,5% случаев, ПсА – 14,8%.
Наиболее значимыми факторами риска дисфункции почек у пациентов, страдающих серонегативными спондилоартритами, явились высокая активность болезни с системными проявлениями (OR-11,0; 3,0-42,7, p<0,01), продолжительное течение свыше 10 лет СА (OR-3,64; 1,09-12,6, p<0,01), прием НПВП (OR-10,2; 2,39-50,1, p<0,01), гиперурикемия (OR-7,27; 1,89-29,2, p<0,01). Установлено также, что гиперхолестеринемия (OR-7,88; 2,25-29,0, p<0,01), повышение ХС ЛПНП (OR-4,21; 1,28-14,1, p<0,01) и гипертриглицеридемия (OR-11,5; 3,10-45,3, p<0,01) особая значимость которой в большей степени была замечена у больных псориатическим спондилоартритом, внесли серьезный вклад в формирование риска ХБП. Корреляционный анализ показал обратнопропорциональную зависимость скорости клубочковой фильтрации с СРБ (r=-0,21; p<0,05), суммарной дозой глюкокортикоидов (r=-0,22; p<0,05), возрастом (r=-0,23; p<0,05), продолжительностью СА (r=-0,29; p=0,01), ТИМ общей сонной артерии (r=-0,20; p<0,05), а также концентрацией в сыворотке триглицеридов (r=-0,23; p<0,05) и мочевой кислоты (r=-0,24; p<0,05).
Г и п е р т р о ф и я миокарда ЛЖ по ЭКГ была выявлена у 21,3% больных, по ЭХОКГ – после расчета индекса массы миокарда ЛЖ- 30,7% (р>0,05). Показатели ИММЛЖ у больных АС составили 111,3±8,3 г/м, псориатическим артритом - 110,4±7,5 г/м, (р=0,607). Прямой сравнительный анализ данных ЭХОКГ с контрольной группой не показал значимых различий, отмечено лишь преобладание у больных СА числа случаев аортальной регургитации, что может быть проявлением аортита как частого системного проявления СА (при СА-15 чел.(20%), в контроле- 3 чел.(10%), р=0,048).
Таким образом, поражение органов- мишеней при спондилоартритах в большей степени ассоциируется с активностью основного заболевания. Корреляционная зависимость показателей почечной и сосудистой дисфункции с активностью воспаления подтверждают это предположение.
Частота и ш е м и ч е с к о й б о л е з н и с е р д ц а у больных СА, установленная на первом этапе исследования при анализе медицинской документации, составила 10%. В структуре нозологических форм ИБС доминировала стенокардия напряжения. Детальная верификация ИБС проводилась у 75 пациентов путем анализа жалоб больных, оценки факторов риска, проведения стандартной ЭКГ, ЭХОКГ и суточного мониторирования ЭКГ. При анализе болевого синдрома был установлен высокой процент вертеброгенных кардиалгий (46 пациентов – 61,3%), что объясняется вовлечением позвоночника практически во всех клинических вариантах СА. Частота стенокардии напряжения составила 14 чел. (18,7%), при этом частота безболевой ишемии – 3 (30% ко всем случаям ишемии по ЭКГ). Структура выявленной патологии после проведения ХМ ЭКГ представлена в табл.22.
Таблица 22
Структура патологии по результатам ХМ ЭКГ
| Показатели | АСА, n=48 (n,%) | ПсА, n=27 (n,%) | Всего, n=75 (n,%) |
| Нарушения ритма | 23 (47,9) | 15 (55,6) | 38 (50,7) |
| Экстрасистолия | 18 (37,5) | 10 (37,0) | 28 (37,3) |
| ФП | 5 (10,4) | 4 (14,8) | 9 (12) |
| Синусовая тахикардия | 20 (41,7) | 13 (48,1) | 33 (44) |
| Ишемия | 6 (12,5) | 4 (14,8) | 10 (13,3) |
| Нарушения проводимости | 8 (16,7) | 3 (11,1) | 11 (14,7) |
| Без патологии | 11 (22,9) | 5 (18,5) | 16 (21,3) |
Таким образом, частота ИБС по данным мед. документации составила 10%, после детальной верификации – 24 чел. (32%), р<0,01. Структура ИБС представлена стенокардией напряжения 14 чел (58,3%), безболевой ишемией – 3 (12,5%) и нарушением ритма, ассоциированным с ИБС 7 (29,2%). Наиболее значимыми факторами, влияющими на развитие ИБС у больных СА, явились артериальная гипертензия (OR-3,5; р<0,01) и атерогенные ДЛП (OR-2,1; р<0,05).
2.5.2. Кардиоваскулярная патология у больных остеоартрозом
Ч а с т о т а а р т е р и а л ь н о й г и п е р т о н и и у больных ОА методом СМАД составила 40 %, впервые выявленной - лишь 6,7%.
У обследуемых больных с ОА структура традиционных факторов риска АГ представлена на рис. 15.
Рис.15. Факторы риска артериальной гипертензии у больных остеоартрозом
Наибольшую значимость у данной категории больных приобретают факторы, ассоциирующиеся с избыточной массой тела, абдоминальным ожирением и метаболическим синдромом, что объясняется ключевой ролью этих признаков в формировании самого остеоартроза. Не установлено статистически значимого влияния показателей тяжести остеоартроза, уровня СРБ на риск артериальной гипертонии у данной категории больных.
Показатели м о р ф о ф у н к ц о н а л ь н о г о с о с т о я н и я с о с у д о в у пациентов, страдающих остеоартрозом, представлены в таблице 23. Сравнительный анализ с контрольной группой показал достоверные различия лишь по частоте установления бляшек (11 чел (36,7%) против 5 чел (16,7%), р<0,01, соответственно), при недостоверных различиях по частоте эндотелиальной дисфункции (16 чел (53,3%) против 15 чел (50%), р=0,77).
Таблица 23
Характеристика поражения сосудов при ОА
| Показатель | ОА, n=30 (Ме, Ии) |
| Толщина интима – медиа, мм | 0,89 мм (0,79; 1,07) |
| Частота установления бляшки (n, %) | 11 (36,7) |
| ЛПИ (лодыжечно-плечевой индекс) | 1,12 (0,97; 1,24) |
| ЭЗВД на 90 сек., % | 7,6 (4,0; 11,1) |
| Частота эндотелиальной дисфункции по ЭЗВД (n, %) | 16 (53,3) |
| ЭНЗВД, % | 8,6 (5,7; 13,1) |
| Частота эндотелиальной дисфункции по ЭНЗВД (n, %) | 15 (50) |
При оценке ф у н к ц и о н а л ь н о г о с о с т о я н и я п о ч е к минимальная гиперкреатининемия установлена у 8 чел. (26,7%). Показатели СКФ по MDRD составили 62,0 (53; 83) мл/мин, снижение СКФ<60 мл\мин было установлено у 3 пациентов, что составило 10%. Частота микроальбуминурии составила 6,7%. Сравнительный анализ больных ОА с контрольной группой показал преобладание гиперкреатининемии (8 чел. (26,7%) против 4 чел. (13,3%), р<0,05), по другим параметрам достоверных различий установлено не было.
Таким образом, частота АГ у больных ОА составила 40 %. Наиболее значимыми для развития АГ явились факторы, ассоциирующиеся с избыточной массой тела, абдоминальным ожирением и метаболическим синдромом. Поражение органов-мишеней при остеоартрозе не имеет принципиальных особенностей и соответствует, вероятнее всего, популяционному состоянию.
2.6. Качество оказания кардиологической помощи при патологии суставов в Иркутской области
Детальное изучение сердечно-сосудистой патологии у больных, страдающих ревматоидным артритом и серонегативными спондилоартритами, позволило убедиться в том, что существует реальная проблема в вопросах диагностики и, следовательно, своевременного лечения кардиоваскулярных заболеваний у пациентов с патологией суставов. Наглядно продемонстрировать это могут показатели впервые выявленной патологии по результатам наших наблюдений (рис. 16). Из графика видно, что частота впервые выявленной кардиоваскулярной патологии в среднем составила 20% и наибольший удельный вес в структуре занимали артериальная гипертония и дислипидемии.
Рис. 16 Частота впервые выявленной патологии у больных РА и спондилоартритами
Опрос больных РА и спондилоартритами показал, что пациенты с хронической патологией суставов, наблюдающиеся у терапевтов, отмечали достоверно более высокий процент назначений дополнительных методов обследования для диагностики кардиоваскулярной патологии (рис.17). При этом даже рутинное измерение АД врачами – терапевтами проводилось практически во всех анализируемых случаях, в сравнении с этим врачи- ревматологи измерение АД проводили лишь у 22% опрошенных респондентов.
Рис. 17. Частота назначения дополнительных методов обследования пациентам с патологией суставов (**p<0,01)
Гипотензивную терапию регулярно, как показал первый этап исследования, принимали 50,7%, больных РА и 41,7% - пациентов СА. Длительный прием статинов подтвердили в среднем лишь 4% больных, страдающих ревматоидным артритом и СА.
Структура назначаемой терапии больным с патологией суставов представлена на рис.18. Из графика видно, что наибольший удельный вес среди гипотензивных препаратов занимали мочегонные. Второе место в структуре препаратов разделили ИАПФ, антагонисты кальция и бета-блокаторы. Незначительный процент назначаемых дезагрегантов можно объяснить высокой частотой приема неселективных НПВП. Отмечены низкие показатели назначения блокаторов ренин-ангиотензин-альдостероновой системы.
Рис.18. Структура назначаемой кардиологической терапии (n=305)
Таким образом, результаты наших наблюдений показали очевидную недооценку тяжести кардиоваскулярной патологии больных РА и серонегативными спондилоартритами, что требует оптимизации подходов к качеству оказания кардиологической помощи больным с патологией суставов на территории Прибайкалья.
Выводы
- Частота артериальной гипертонии у больных ревматоидным артритом была существенно выше, чем в популяции и составила 53,7%. Значимыми прогностическими факторами риска АГ у данной категории больных, наряду с традиционными, такими как наследственность, дислипидемия, гипергликемия, снижение СКФ и гиподинамия, явились прием НПВП и глюкокортикоидов, высокая активность РА и его продолжительность свыше 10 лет.
- У больных ревматоидным артритом в сочетании с артериальной гипертонией в 46% случаев обнаружены атеросклеротические бляшки общей сонной артерии, в 85,7% - эндотелиальная дисфункция. Наличие эндотелиальной дисфункции у больных РА без гипертонии в сочетании с высокой активностью воспаления предполагает вклад последнего в формирование этой дисфункции.
- Значимыми факторами риска прогрессирования почечной недостаточности при РА явились микроальбуминурия, артериальная гипертония, дислипидемия, гипергликемия и возраст больных. Ассоциация сниженной СКФ с активностью воспаления, высокой частотой приема НПВП, продолжительностью РА свыше 10 лет предполагает негативный вклад хронического воспаления и лекарственного поражения в формирование почечной дисфункции у данной категории больных.
- Частота гипертрофии миокарда ЛЖ при РА составила 40,9%. В ее формировании ключевую роль играли артериальная гипертония, в том числе с высоким пульсовым давлением, ЧСС - 24 свыше 70 уд/мин, возраст, избыточная масса тела и гиперхолестеринемия. В то же время значимая корреляция между ИММЛЖ и суммарной дозой глюкокортикоидов, СРБ, СКФ подтверждает влияние воспаления и последствий РА на формирование негативного профиля ремоделирования миокарда.
- Частота ИБС у больных РА составила 45,9%, особенностью ее течения явилась безболевая ишемия у каждого четвертого пациента (25,4%). Наряду с традиционными факторами риска ИБС, такими как возраст, гипергликемия, дислипидемии, высокая ЧСС, избыточная масса тела, семейный анамнез ССЗ, курение и артериальная гипертония, установлены предикторы, ассоциирующиеся с хроническим воспалением - высокая активность и продолжительность ревматоидного артрита более 10 лет, ВАШ боли>50 мм, прием глюкокортикоидов свыше 12 мес. в суммарной дозе более 3,0 г в пересчете на преднизолон, а также сопутствующая анемия, как частое осложнение РА.
- Комплексная оценка факторов риска позволяет на основе разработанной математической модели с учетом дислипидемии, снижения СКФ, высокого пульсового давления, активности РА и его продолжительности свыше 10 лет, приема ГК, ТИМ и уровня СРБ прогнозировать сердечно-сосудистый риск у больных ревматоидным артритом.
- Едиными факторами риска кардиоваскулярной патологии и остеопороза с переломами при РА явились высокая активность по DAS 28, дислипидемия, снижение СКФ<60 мл/мин, прием ГК и продолжительность РА более 10 лет
- Частота АГ при спондилоартритах составила 37,3%. Факторами риска ее развития установлены высокая активность воспаления, гиперурикемия, гипертриглицеридемия, длительность спондилоартрита свыше 10 лет, снижение СКФ и прием ГК. Поражение органов-мишеней при спондилоартритах ассоциировалось с АГ и активностью основного заболевания.
- Частота ИБС при серонегативных спондилоартритах составила 32%. Наиболее значимыми факторами риска ИБС у больных СА явились артериальная гипертония (OR-3,5; р<0,01) и атерогенные ДЛП (OR-2,1; р<0,05).
- Частота АГ у больных ОА составила 40 %. Значимыми факторами риска ее развития явились избыточная масса тела, абдоминальное ожирение и метаболический синдром. Поражение органов-мишеней при остеоартрозе не имело принципиальных особенностей.
- Частота впервые выявленной сердечно-сосудистой патологии у больных РА и спондилоартритами составила в среднем 20%, что свидетельствует о недостаточной настороженности врачей в отношении кардиоваскулярной патологии у данной категории пациентов. При этом прием гипотензивной терапии подтвердили 50,7% больных РА и 41,7%-спондилоартритами, статины получали лишь 4 % больных.
Практические рекомендации
1. Больные РА являются группой повышенного риска кардиоваскулярных осложнений, вероятность развития которых возрастает при продолжительном течении РА, приеме глюкокортикоидов, низкой минеральной плотности костной ткани, что необходимо учитывать в клинической практике.
2. С помощью разработанной нами модели прогноза сердечно-сосудистых осложнений предлагается на основании выделенных факторов сформировать среди больных РА группы повышенного риска для проведения ранних лечебно-профилактических мероприятий.
3. На амбулаторном этапе при диспансерном наблюдении больных РА и спондилоартритами необходима оценка традиционных кардиоваскулярных факторов риска, регулярное измерение АД, в том числе пульсового давления, контроль липидов и микроальбуминурии, расчет скорости клубочковой фильтрации, проведение ЭКГ, ХМ ЭКГ и УЗДГ сонных артерий.
4 Всем больным, страдающим ревматоидным артритом, для исключения остеопороза и/или остеопенического синдрома необходимо соответствующее обследование, включающее оценку факторов риска, проведение рентгенографии позвоночника и остеоденситометрии.
5.Необходимо оптимизировать качество диагностики и лечения кардиоваскулярной патологии у больных с заболеваниями суставов, для чего следует включить в программы обучения врачей–ревматологов Прибайкалья вопросы диагностики и лечения ИБС, артериальной гипертонии и ХБП (в соответствии с Национальными рекомендациями ВНОК).
Публикации по теме диссертации
- Изучение роли климато-географических и экологических факторов в патогенезе остеопороза/ Л.В.Меньшикова, М.Л.Меньшиков, И.В.Ушаков, Н.А.Храмцова//2 Всероссийский съезд ревматологов: тезисы докладов.- Тула.- 1997.- с.124.
- Меньшикова, Л.В. Коррекция психологического статуса у больных тяжелым системным остеопорозом / Л.В.Меньшикова, А.А. Дзизинский, Н.А.Храмцова//VIII Российский национальный конгресс «Человек и лекарство»: материалы – М., 2001.- С. 283-284.
- Храмцова, Н.А. Структурные особенности проксимального отдела бедренной кости как фактор риска переломов бедра в популяции г. Иркутска / Н.А.Храмцова, Л.В,Меньшикова // Научно-практическая ревматология, - М.- 2002. - №3- С.17-21.
- Исходы переломов проксимального отдела бедра у лиц пожилого возраста и их медико-социальные последствия / Л.В.Меньшикова, Н.А,Храмцова, О.Б.Ершова, О.М.Лесняк и соавт. //Научно-практическая ревматология.- 2002.- №4, - С. 11-14.
- Храмцова,Н.А. Медико-социальные проблемы переломов проксимального отдела бедра / Н.А.Храмцова, Л.В. Меньшикова //Актуальные проблемы современной ревматологии: сборник научных трудов.- Волгоград.- 2002.- С.135-136.
- Меньшикова, Л.В. Эпидемиология остеопороза и переломов конечностей среди лиц старше 50 лет в Иркутской области / Л.В.Меньшикова, Н.А.Храмцова, О.В.Грудинина// Актуальные проблемы современной ревматологии: сборник научных работ. - Волгоград, 2002. - С.85.
- Menschikova, L. V. Mortality after hip fracture: 2-year follow- up study / L. V. Menschikova, N.A. Khramtsova // Fourth European Symposium on Clinical and Economic Aspects of Osteoporosis and Osteoarthritis. – Nice, 14-17 november, 2003.- P.127.
- Храмцова,Н.А. Плотность костной ткани у лиц с переломами бедра в популяции г.Иркутска/ Н.А. Храмцова, Л.В.Меньшикова // Научно-практическая ревматология.- 2003,- №2 - С.104.
- Храмцова,Н.А. Отдаленные исходы переломов проксимального отдела бедра в популяции г.Иркутска / Н.А. Храмцова, Л.В.Меньшикова // II конференция с международным участием «Проблема остеопороза и переломов в ортопедии и травматологии».- Москва, 2003.- С. 133-134.
- Меньшикова, Л.В. Анализ частоты остеопороза у мужчин / Л.В.Меньшикова, Н.А. Храмцова, О.В.Грудинина // Российский конгресс по остеопорозу: материалы.- М., 2003.- С.66.
- Menschikova, L. V. Incidence of hip and forearm fractures in the population of East Siberia, Russia / L. V. Menschikova, N.A. Khramtsova //30-th European Symposium on Calcified Tissues.-Rome, Italy.- 8-12 May 2003. P. 322.
- Вторичный остеопороз и факторы риска его развития у женщин с ревматоидным артритом /Е.В.Белых, Л.В.Меньшикова, Н.А.Храмцова, И.М.Михалевич//Актуальные проблемы клинической медицины: материалы юбилейной научн.- практич. конф., посвященной 25- летнию Иркутского ГИУВа.- 2004.- с.13-15.
- Храмцова,Н.А. Факторы риска переломов проксимального отдела бедренной кости в России (по данным многоцентрового исследования) / Н.А. Храмцова, Л.В.Меньшикова // Актуальные проблемы клинической медицины: материалы юбилейной научн.- практич. конф., посвященной 25- летнию Иркутского ГИУВа.- 2004.- с.30.
- Храмцова,Н.А. Клинико-эпидемиологическая характеристика поражений проксимального отдела бедра при остеопорозе в популяции г.Иркутска// Актуальные проблемы клинической и экспериментальной медицины: материалы межрегиональной научно-практической конференции молодых ученых Сибири.- Иркутск, 2003. - С.28.
- Регистр диспансеризации больных с артериальной гипертонией / Н.В.Шкодина, И.Л.Кабанова, Ю.Ю.Смирнова, Н.А. Храмцова // Актуальные проблемы клинической медицины: материалы юбилейной научно-практической конференции, посвященной 25-летию Иркутского ГИУВа.–Иркутск, 2004. - С.55.
- Храмцова Н.А.. Влияние избыточной массы тела на состояние миокарда у больных артериальной гипертонией /Н. А. Храмцова, Н.В.Шкодина, А.М.Бедин // Актуальные проблемы клинической медицины: материалы юбилейной научно-практической конференции, посвященной 25-летию Иркутского ГИУВа.–Иркутск, 2004. - С.53.
- Храмцова, Н.А. Артериальная гипертония и метаболический синдром / Н.А.Храмцова, Н.В.Шкодина, А.М.Бедин // Актуальные проблемы клинической медицины: материалы юбилейной научно-практической конференции, посвященной 25-летию Иркутского ГИУВа.–Иркутск, 2004. - С.54.
- Частота болей в суставах у городских и сельских жителей России (предварительные результаты)/ Ш.Эрдес, и соавт. Н.А. Храмцова // Тер.архив.- 2005.- Т 77.- №5.- С. 65-69.
- Храмцова, Н.А. Состояние липидного спектра у женщин с ревматоидным артритом / Н.А.Храмцова, Е.В.Белых, С.Н. Рожкова // «Актуальные проблемы клинической и экспериментальной медицины»: материалы межрегиональной научно-практической конференции молодых ученых.- Иркутск.- 2006.-С.52-53.
- Храмцова, Н.А. Оценка сердечно-сосудистого риска у лиц с ревматоидным артритом / Н.А. Храмцова, Н.В. Шкодина, Е.В. Белых // Вестник Санкт – Петербургской гос.мед академии им. И.И.Мечникова.- 2007.- Т.2, №2.- С.187.
- Храмцова, Н.А. Дислипидемии у женщин с ревматоидным артритом / Н.А. Храмцова, Л.В. Меньшикова, Е.В. Белых // Вестник Санкт – Петербургской гос.мед академии им. И.И.Мечникова.- 2007.- Т.2, №2.- С.186.
- Опыт применения карведилола при хронической сердечной недостаточности / Н.В.Шкодина, И.Л.Кабанова, Ю.Ю.Смирнова, Н.А. Храмцова //Современные направления диагностики, лечения и профилактики заболеваний: материалы сборника Дорожной клинической больницы.- Чита.- 2007.- С.167-168.
- Храмцова, Н.А. Оценка общего состояния по ВАШ при ревматоидном артрите в сочетании с ИБС / Н.А.Храмцова, Л.В.Меньшикова, Е.В.Трухина // III Всероссийская конференция «Социальные аспекты ревматических заболеваний: боль – междисциплинарная проблема»: материалы. Научно-практическая ревматология- 2007.- №2.- С.142.
- Храмцова, Н.А. Факторы риска артериальной гипертонии у женщин с ревматоидным артритом /Н.А.Храмцова, А.А.Дзизинский // Кардиоваскулярная терапия и профилактика.- 2007.- 6 (5).- С.331.
- Структура психогенных расстройств у пациентов с острым коронарным синдромом / Н.А.Храмцова, Н.В. Шкодина, Ю.Ю.Смирнова, А.М. Бедин // Кардиоваскулярная терапия и профилактика.- 2007.- Т.6 №5 (прил.1).- С.331-332.
- Храмцова, Н.А. Факторы риска кардиоваскулярной патологии при ревматоидном артрите / Н.А.Храмцова, Н.В.Земляничкина, Е.В.Трухина //Сиб. мед.журн. – 2007.- №7, С.42-44.
- Храмцова, Н.А. Суставной синдром в практике врача терапевта. Учебное пособие для врачей // Иркутск: РИО ГИУВа.- 2007.- 40 с.
- Храмцова, Н.А. Противовоспалительные препараты в практике врача терапевта: пособие для врачей // Иркутск: РИО ГИУВа.- 2007.- 22 с.
- Храмцова, Н.А. Морфофункциональное состояние сосудов при ревматоидном артрите в сочетании с артериальной гипертензией / Н.А.Храмцова, Н.В.Земляничкина // Всероссийская Конференция «Инновационные технологии в ревматологии»: материалы тезисов.- Научно-практическая ревматология.- 2008.- №2 (прил.).- С.50.
- Храмцова, Н.А. Дислипидемии у женщин с ревматоидным артритом / Н.А.Храмцова, Е.В.Белых//Всероссийская Конференция «Инновационные технологии в ревматологии»: материалы тезисов.- Научно-практическая ревматология.- 2008.-№2 (прил.).- С.52.
- Храмцова, Н.А. Функциональное состояние почек при ревматоидном артрите / Н.А. Храмцова, А.А. Дзизинский, Н.В. Земляничкина, Е.В.Трухина // Кардиоваскулярная терапия и профилактика.- 2008.- 7 (6).- С.394.
- Храмцова, Н.А. Морфофункциональное состояние сосудов при ревматоидном артрите в сочетании с артериальной гипертонией / Н.А.Храмцова, А.А.Дзизинский, Н.В.Земляничкина//«Гипертоническая болезнь и вторичные артериальные гипертонии»: материалы IV Всероссийской научно-практической конф.- М.,- 2008.- С.20.
- Храмцова, Н.А. Кардиоваскулярный риск у женщин с ревматоидным артритом / Н.А. Храмцова, Н.В.Земляничкина, Е.В.Трухина // Актуальные проблемы клинической медицины: материалы XIII итоговой научно-практической конференции Иркутского ГИУВа.- Иркутск.- 2008.- С. 64-65.
- Стрекаловская, Ф.П. Анализ случаев ревматоидного артрита в г.Усть- Илимске / Ф.П. Стрекаловская, Н.А.Храмцова, В.С.Каримова // Актуальные проблемы клинической медицины: материалы XIII итоговой научно-практической конференции Иркутского ГИУВа.- Иркутск.- 2008.- С. 50-52.
- Храмцова, Н.А. Эндотелиальная дисфункция при ревматоидном артрите в сочетании с артериальной гипертонией / Н.А. Храмцова, А.А. Дзизинский, Н.В.Земляничкина, Н.В.Шкодина// Актуальные проблемы клинической медицины: материалы XIII итоговой научно-практической конференции Иркутского ГИУВа.- Иркутск.- 2008.- С. 63-64.
- Храмцова, Н.А. Пульсовое давление и сердечно-сосудистый риск при ревматоидном артрите / Н.А.Храмцова, А.А. Дзизинский // Кардиоваскулярная терапия и профилактика.- 2009.- 8 (2)- С.339.
- Храмцова, Н.А. Остеопороз и кардиоваскулярный риск при ревматоидном артрите // Н.А. Храмцова, Е.В.Белых, Т.Н. Петрачкова // V съезд ревматологов России: материалы съезда.- М.- 2009.- С. 121.
- Храмцова, Н.А. Дисфункция почек - влияние артериальной гипертонии при ревматоидном артрите // Н.А.Храмцова, А.А.Дзизинский // V съезд ревматологов России: материалы съезда.- М.- 2009.- С. 121.
- Почечная дисфункция и гипертрофия миокарда при ревматоидном артрите / Е.В.Белых, Н.А.Храмцова, С.Н.Рожкова // V съезд ревматологов России: материалы съезда.- М.- 2009.- С. 19.
- Качество оказания кардиологической помощи при ревматоидном артрите/Н.Э.Самбурова, Н.А.Храмцова, Л.В.Меньшикова, Н.Б. Лагерева // V съезд ревматологов России: материалы съезда.- М.- 2009.- С. 100.
- Храмцова, Н.А. Минеральная плотность костной ткани и кардиоваскулярная патология при ревматоидном артрите / Н.А.Храмцова, Н.В.Земляничкина, Л.В.Меньшикова // Сиб.мед.журн.- 2009.- №2.- С.54-56.
- Храмцова, Н.А. Функциональное состояние сосудов при ревматоидном артрите /Н.А.Храмцова, Н.В.Земляничкина, Е.В.Трухина // Сиб.мед.журн.- 2009.- №3.- Т.86,- С. 59-61.
- Храмцова, Н.А.Частота артериальной гипертензии при ревматоидном артрите / Н.А. Храмцова, А.А.Дзизинский, Н.В.Шкодина, Н.Б.Лагерева, Н.В. Земляничкина// Сиб.мед.журн.- 2009.- №7.Т. 90- С.43-46.
- Храмцова, Н.А. Частота переломов и сердечно-сосудистый риск при ревматоидном артрите / Н.А.Храмцова, А.А.Дзизинский, Л.В.Меньшикова, Н.В. Земляничкина // Сиб.мед.журн. - 2009.- №7.Т-90- С.110-111.
- Храмцова, Н.А. Кардиоваскулярная патология при ревматоидном артрите. Монография / Н.А.Храмцова, А.А.Дзизинский //Иркутск: РИО ГИУВа - 2010.-с. 148.
- Храмцова, Н.А. Пульсовое давление и кардиоваскулярный риск при ревматоидном артрите / Н.А. Храмцова, А.А.Дзизинский, Н.В. Земляничкина // Сиб. мед. журн. 2010.- №2. С. 81-84.
- Храмцова, Н.А. Оценка сердечно-сосудистого риска у больных ревматоидным артритом. Методические рекомендации для врачей // Иркутск: РИО ГИУВа - 2010.-с. 15.
- Храмцова, Н.А. Артериальная гипертония при серонегативных спондилоартритах/ Н.А. Храмцова, А.А.Дзизинский, Т.И.Батудаева // Сиб. мед. журн. 2010.- №3. С. 86-88.
Список сокращений
АГ – артериальная гипертония
АД – артериальное давление
АО – абдоминальное ожирение
АС - анкилозирующий спондилит
БЛНПГ – блокада ЛНПГ
БПВЛНПГ – блокада передней ветви ЛНПГ
БТ – базисная терапия
ВАШ – визуальная аналоговая шкала
ГК – глюкокортикоиды
ГУ – гиперурикемия
ДАД – диастолическое АД
ДЛП - дислипидемии
ИЛ – 6 – интерлейкин 6
ИММЛЖ – индекс массы миокарда левого желудочка
ИСАГ – изолированная систолическая АГ
ЛПИ- лодыжечно-плечевой индекс
ЛПНП – липопротеиды низкой плотности
МАУ – микроальбуминурия
МС – метаболический синдром
МПКТ- минеральная плотность костной ткани
ОДМ – остеоденситометрия
ОП - остеопороз
ОТ- объем талии
ОХС – общий холестерин
ПД – пульсовое давление
РА – ревматоидный артрит
СА – спондилоартриты
САД- систолическое АД
СДАГ – систолодиастолическая АГ
СМАД – суточное мониторирование АД
СКФ – скорость клубочковой фильтрации
ССЗ – сердечно-сосудистые заболевания
ТГ - триглицериды
ТИМ ОСА– толщина интима медиа общей сонной артерии
ХМ ЭКГ – холтеровское мониторирование ЭКГ
ХС ЛПНП – холестерин липопротеиды низкой плотности
ХС ЛПВП - холестерин липопротеиды высокой плотности
ЭД – эндотелиальная дисфункция
ЭЗВД/ЭНЗВД – эндотелийзависимая и независимая вазодилатация

