Повышение эффективности диагностики и лечения больных с одонтогенными воспалительными заболеваниями челюстно-лицевой области на основе лазерно-флюоресцентных технологий в условиях стоматологической по
На правах рукописи
Попов Сергей Николаевич
ПОВЫШЕНИЕ ЭФФЕКТИВНОСТИ ДИАГНОСТИКИ И ЛЕЧЕНИЯ БОЛЬНЫХ С ОДОНТОГЕННЫМИ ВОСПАЛИТЕЛЬНЫМИ ЗАБОЛЕВАНИЯМИ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ НА ОСНОВЕ ЛАЗЕРНО-ФЛЮОРЕСЦЕНТНЫХ ТЕХНОЛОГИЙ В УСЛОВИЯХ СТОМАТОЛОГИЧЕСКОЙ ПОЛИКЛИНИКИ
14.01.14 – Стоматология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва - 2013
Работа выполнена в Федеральном государственном бюджетном образовательном учреждении высшего профессионального образования «Российский университет дружбы народов»
Научный руководитель:
Доктор медицинских наук, профессор Гунько Валерий Иосифович
Официальные оппоненты:
Мамедов Адиль Аскерович - доктор медицинских наук, профессор, заведующий кафедрой стоматологии детского возраста и ортодонтии ГБОУ ВПО Первый Московский государственный медицинский
университет имени И.М.Сеченова Минздрава России
Алимский Анатолий Васильевич - доктор медицинских наук, профессор, Заслуженный деятель науки РФ, заведующий научно-организационным отделом ФГБУ «Центральный научно-исследовательский институт стоматологии и челюстно-лицевой хирургии Минздрава России»
Ведущая организация:
ГБОУ ВПО «Московский государственный медико-стоматологический университет им. А.И. Евдокимова» Министерства Здравоохранения России
Защита состоится «_______» ________________ 2013 года в _______ часов
На заседании диссертационного Совета Д 208.040.14 при ГБОУ ВПО «Первый Московский государственный медицинский университет им. И. М. Сеченова» Минздрава России (119991, г. Москва, ул. Трубецкая, д. 8., стр.2)
С диссертацией можно ознакомиться в ЦНМБ Первого Московского государственного медицинского университета им. И.М. Сеченова Минздрава России по адресу: 117998, г. Москва, Нахимовский проспект, д. 49.
Автореферат разослан “_____ ” _________________ 2013 г.
Ученый секретарь диссертационного совета Платонова
доктор медицинских наук, профессор Валентина Вениаминовна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы исследования
Анализ данных статистики за последние 40 лет показывает, что число больных с одонтогенными воспалительными заболеваниями челюстно-лицевой области (ОВЗ ЧЛО) неуклонно нарастает (Козлов В.А., 2003). Соответственно этому, в период с 1980 по 2007 гг. в научных исследованиях в области хирургической стоматологии и челюстно-лицевой хирургии (ЧЛХ) в преобладающем большинстве случаев (27,8%) выявлены ОВЗ ЧЛО (Полякова Ю.В., 2008). Однако среди них встречаются лишь единичные сообщения о путях повышения качества оказания помощи больным с ОВЗ ЧЛО в условиях стоматологической поликлиники (СП) (Полякова Ю.В., 2008). В настоящее время в СП увеличивается количество взрослых пациентов с острыми гнойными периоститами (ОГП) и апикальными периодонтитами (АП) (Шаргородский А.Г., 2002). Это ведет к значительным экономическим потерям (Христофорандо Д.Ю., 2005): ОГП чаще встречаются у мужчин в возрасте 40-49 лет (Тимофеев А.А., 2002), то есть у наиболее трудоспособного населения.
На этом фоне встречаются случаи осложненного течения ОГП, обусловившего госпитализацию до 23,85 % пациентов (Вербицкая и соавт., 2002; Игнатьева О.В. и соавт., 2008). Причинами этого могут служить как неадекватное хирургическое пособие в условиях СП, так и назначение (в большинстве случаев), при наличии показаний, антимикробных препаратов (АМП) без учета чувствительности этиологической микрофлоры к ним у больных с ОГП.
В целом, консервативно-хирургическое лечение больных с ОВЗ ЧЛО (в частности, АП и ОГП) в условиях СП недостаточно эффективно по ряду причин: сокращение, а зачастую отсутствие, общегосударственных мероприятий по диспансеризации населения по профилактике кариеса и его осложнений как основного фактора, определяющего этиологию ОВЗ ЧЛО; отсутствие возможности проведения микробиологических исследований по месту лечения больных (Шаргородский А.Г., 2002); несоответствие возможностей клинической микробиологии потребностям и условиям СП (Бажанов Н.Н.,,1996; Пашков Е.П., 2002).
В связи с этим, наше внимание привлекли современные достижения в лазерной технике, позволяющие проводить индикацию, дифференциацию микробов и сравнительную оценку эффективности различных АМП с помощью экспресс-метода лазерно-флюоресцентной диагностики (ЛФД) (ажанов Н.Н.,, Воробьев А.А., Пашков Е.П., Александров М.Т., 1990-2008 гг.). Разработка была рекомендована к внедрению и одобрена Президиумом РАМН (постановление №165, от 3 ноября 1999 года, протокол №20), отмечена государственной премией РФ в области науки и техники (указ президента РФ от 5 августа 2002 года № 831). Метод ЛФД был отработан в стоматологии при стационарном лечении больных с ОВЗ ЧЛО (Платонова В.В., 1999; Шайхалиев А.И., 2001; Черкесов И.В., 2007; Геворков Г.Л., 2009), для оценки гигиенического состояния полости рта (Филатов М.В., 2003), диагностики гингивита у подростков (Синяева М.Л., 2006), дифференциальной диагностики кариозных поражений зубов (Зайцева Е.В., 2000). Указанные предпосылки явились основанием для применения ЛФД в специфических условиях СП для экспресс-индикации заболеваний и процессов микробной природы и объективного экспресс-выбора АМП на этапах комплексного лечения больных с ОВЗ ЧЛО.
Цель работы: повышение эффективности и качества лечения больных с одонтогенными воспалительными заболеваниями челюстно-лицевой области в условиях стоматологической поликлиники на основе разработки физико-химических методов диагностики одонтогенной инфекции.
Задачи:
- на основе систематизации и анализа статистических данных оказания стоматологической помощи в поликлинике выявить причинно-следственные связи поступательного развития одонтогенных воспалительных заболеваний челюстно-лицевой области;
- провести разработку методики и экспериментально-теоретическое обоснование физико-химической технологии на основе лазерно-флюоресцентной диагностики для повышения эффективности диагностики и комплексного лечения больных с наиболее часто встречающимися нозологиями одонтогенных воспалительных заболеваний челюстно-лицевой области (острый гнойный периостит) в условиях стоматологической поликлиники;
- разработать алгоритм подбора предпочтительных антимикробных препаратов в комплексном лечении больных с острым гнойным периоститом на основе физико-химической технологии сочетания лазерно-флюоресцентной диагностики и препарата детергентного действия (мирамистин);
- клинически обосновать эффективность разработанной диагностической физико-химической технологии повышения качества лечения пациентов с острым гнойным периоститом;
- оценить экономическую эффективность широкого внедрения разработанной диагностической физико-химической технологии индикации одонтогенной инфекции в практику стоматологических поликлиник.
Научная новизна
1) Экспериментально и клинически обосновано применение новой физико-химической технологии на основе лазерно-флюоресцентной диагностики в условиях стоматологической поликлиники в комплексном лечении больных с одонтогенными воспалительными заболеваниями челюстно-лицевой (острый гнойный периостит).
2) Разработана физико-химическая методика дополнительного применения детергента (мирамистин 0,1%) для повышения чувствительности и экспрессности метода лазерно-флюоресцентной диагностики и индивидуального экспресс-контроля эффективности воздействия антимикробного препарата на микрофлору из одонтогенных очагов инфекции.
3) Разработаны новые алгоритмы этиотропного лечения больных с одонтогенными воспалительными заболеваниями челюстно-лицевой (острый гнойный периостит) в условиях стоматологической поликлиники на основе применения разработанного физико-химического метода.
Научные положения, выносимые на защиту:
- анализ состояния проблемы, разработка концепции и экспериментально-теоретическое обоснование новой физико-химической технологии на основе лазерно-флюоресцентной диагностики для повышения эффективности диагностики и лечения больных с наиболее часто встречаемыми одонтогенными воспалительными заболеваниями челюстно-лицевой (острый гнойный периостит) применительно к условиям стоматологической поликлиники;
- клиническое обоснование эффективности разработанной диагностической технологии для повышения качества лечения пациентов с острыми гнойными периоститами как наиболее часто встречаемой в амбулаторной стоматологической практике нозологии одонтогенной инфекции;
- экономическое обоснование применения разработанной диагностической физико-химической медицинской технологии применительно к условиям работы в стоматологической поликлинике.
Практическая значимость
Использование разработанной физико-химической технологии на основе лазерно-флюоресцентной диагностики в условиях стоматологической поликлиники дает возможность проводить индивидуальное экспресс-определение (1,5-2 ч.) чувствительности микрофлоры к антимикробным препаратам, назначаемым в комплексном лечении больных с острыми гнойными периоститами, что позволит сократить сроки лечения на 1,1 сут, уменьшить количество перевязок до одной, снизить расходы по бюджету здравоохранения на 46,26 руб. на одного больного, в пересчете на одну стоматологическую поликлинику - на 44039,52 - 58657,68 руб. в год, а для 720 поликлиник РФ - на 31 708 454,4 руб. в год.
Практическое использование полученных результатов
Материалы исследования используются при оказании хирургической помощи больным с острым гнойным периоститом в условиях стоматологической поликлиники МУ ЦГБ г. Железнодорожный Московской области.
Апробация результатов исследования
Основные положения работы доложены на: 2-й отчетной конференции СНО стоматологического факультета ММА имени И.М. Сеченова (2006 г.); 2-й Международной научно-практической конференции «Научно-техническое творчество молодежи – путь к обществу, основанному на знаниях» (Москва, 27 июня-02 июля 2010 г. Работа награждена дипломом 1 степени и удостоена золотой медали); на симпозиуме «Амбулаторная хирургическая стоматология: достижения, перспективы развития» в рамках 25 Всероссийской научно-практической конференции «Актуальные проблемы стоматологии» (Москва, 25-28 апреля 2011 г.); на XVI международной конференции челюстно-лицевых хирургов и стоматологов «Новые технологии в стоматологии» (Санкт-Петербург, 16-18 мая 2011 г.); на всероссийском конкурсе по поддержке высокотехнологичных инновационных молодежных проектов 21 февраля 2012 г., где получен грант № ИК-15; совместном заседании кафедр общей стоматологии, хирургической стоматологии и челюстно-лицевой хирургии медицинского факультета РУДН от 24 октября 2012 г.
Личный вклад автора
Автору принадлежит ведущая роль в формировании концепции, организации исследования, разработке физико-химической технологии индикации одонтогенной инфекции (ОИ) на основе ЛФД в условиях СП, алгоритмов ее проведения при лечении больных с ОГП, анализе и обобщении полученных результатов. Вклад автора является определяющим и заключается в непосредственном участии на всех этапах исследования.
Публикации
По теме диссертации опубликовано 9 научных работ, из них 3 в изданиях, рекомендованных ВАК РФ. Приоритет разработки подтвержден Патентом РФ № 2381766 от 08.06.2007.
Объем и структура диссертации
Диссертация состоит из введения, обзора литературы, 3 глав материалов и методов исследования, результатов собственных исследований, обсуждения результатов, выводов, практических рекомендаций и списка литературы. Диссертация изложена на 126 страницах машинописного текста, иллюстрирована 59 рисунками, содержит 18 таблиц. Библиографический указатель литературы содержит 180 источников, из них 143 отечественных и 37 иностранных.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы
Первый этап работы включал систематизацию и анализ статистических данных оказания медицинской помощи больным в условиях СП. Объектом анализа выбраны данные оказания стоматологической помощи населению в медицинском частном учреждении - Поликлинике “ОАО Газпром” (МЧУ ПГ), а также в стоматологической поликлинике МУ ЦГБ г. Железнодорожный Московской области (СП МО). Сравнительный анализ в данных двух СП проводился за четырехлетний период – с 2005 по 2008 гг.
На втором этапе работы при разработке новой концепции индикации и дифференциации заболеваний и процессов микробной природы в стоматологии мы исходили из того, что, во-первых, при использовании лазерного излучателя с длиной волны 0,63 мкм (красная часть спектра) мы наблюдаем флюоресценцию порфиринов микробов (80-90%) и распавшихся клеток (детрит). Это показано в спектральных исследованиях физиками (Васильев Е.Н., 2009) и клиническими микробиологами с использованием альфааминолевуленовой кислоты - предшественника синтеза порфиринов (Морозова О.А., 2001; Пашков Е.П., 2002). Во-вторых, анализ интенсивности флюоресценции и ее спектральных характеристик (по данным представленной выше литературы) как маркеров наличия аэробной (пик на 670 нм) и анаэробной (пик на 700 нм) микрофлоры и ее концентрации (чем выше нормированная мощность флюоресценции М, тем выше концентрация микробов) не дает ответа на ВАЖНЫЙ ДЛЯ ПАЦИЕНТА И ЛЕЧАЩЕГО ВРАЧА ВОПРОС: КАК ОПРЕДЕЛИТЬ, ЖИВАЯ (АКТИВНАЯ) ИЛИ «УБИТАЯ» (не активная, не участвующая в развитии воспалительного процесса) МИКРОФЛОРА В ПАТОЛОГИЧЕСКОМ ОЧАГЕ? Это связано с тем, что микрофлора, как живая, так и убитая, флюоресцируют одинаково (т.е. по своим амплитудно-спектральным показателям практически не различимы). При стационарном лечении больных врач имеет возможность мониторировать методом ЛФД процесс и эффективность лечения больного и по градиенту уменьшения М делать выводы о положительных результатах лечения (именно такой методический подход отмечен в работах по применению ЛФД при стационарном лечении больных с ОВЗ ЧЛО). В условиях работы в СП такая технология не приемлема. Поэтому мы по предложению проф. Александрова М.Т. и акад. РАМН проф. Бажанова использовали детергентные препараты и ЛФД индикацию их действия на микробы. У «убитых» микробов М после добавления к ним детергента практически никогда не увеличивалась (варьирование параметров было в пределах ошибки измерений), а у живых микробов всегда отмечали ее достоверное увеличение (обоснование представлено в результатах исследования). Представленное концептуальное решение было проверено как в эксперименте, так и в клинических условиях СП.
В частности, нами проведено подтверждение указанной концепции во второй экспериментальной части работы на очагах ОИ твердых тканей зуба, в том числе при оценке чувствительности и специфичности методики ЛФД, на базе кафедры госпитальной хирургической стоматологии ММА им. И.М. Сеченова, а также кафедры микробиологии, вирусологии и иммунологии Первого МГМУ им. И.М. Сеченова на флотирующей микрофлоре 245 корневых каналов (КК) удаленных зубов (n=153). Проводилась механическая обработка по методике «Step back» с помощью К- и Н-файлов, лубриканта «Эндогель»; медикаментозная обработка после каждой смены инструмента перекисью водорода 3% (n=21); хлоргексидина биглюконатом 2% (n=35); гипохлоритом натрия 3% (n=40); перекисью водорода, барбатированной оксидом азота (n=15); перекисью водорода 3% в сочетании с гипохлоритом натрия 3% (n=42). Световод установки ЛФД с помощью специального углового наконечника подводился к устью КК контактно, стабильно для снятия показателей до начала обработки Мn, в процессе нее и по завершению Мn+1. Показатель Мn+1 сравнивался с показателем М1 интактной эмали или дентина. Были обработаны и проанализированы 459 спектров флюоресценции.
На третьем этапе работы проведены клинико-лабораторные исследования по подбору предпочтительных АМП при лечении больных с ОГП на базе СП МО.
Клинические характеристики и распределение больных по группам
В соответствии с целью и задачами исследования проведено комплексное обследование и лечение 73 больных с ОГП разного пола различных возрастных групп (табл. 1,2). В основной группе больных локализация ОГП была в области верхней челюсти (ВЧ) у 15 человек, в области нижней (НЧ) – у 12 человек. В группе сравнения у больных с ОГП локализация была в области ВЧ у 18 человек, в области НЧ – у 12 человек.
Основной лечебной манипуляцией, проводившейся у всех больных, была периостотомия и дренирование раны.
Таблица 1
Характеристика пациентов 2-х групп исследования по полу
| № группы | Количество пациентов | Пол | |||
| Женщины | Мужчины | ||||
| абс. | % | абс. | % | ||
| Группа сравнения I | 44 | 16 | 21,9 | 28 | 38,3 |
| Основная II | 29 | 11 | 15,1 | 18 | 24,7 |
| Всего | (100%) | 27 | 37,0 | 36 | 63,0 |
Таблица 2
Характеристика пациентов 2-х групп исследования по возрасту
| Возраст, лет | Группа сравнения I, человек | Основная группа II, человек |
| <25 | 2 | 5 |
| 26-35 | 10 | 5 |
| 36-50 | 7 | 5 |
| >50 | 25 | 14 |
Характеристика групп больных по объему оказанной ургентно помощи представлена в табл. 3. Если проводилась только периостотомия, то при наличии показаний причинный зуб рекомендовалось удалить после полного стихания воспалительных явлений (5-7 дней), либо стоматолог-терапевт планово назначал больного для проведения полноценного ЭЛ также после стихания воспаления.
Таблица 3
Характеристика пациентов 2-х групп исследования по виду лечебных манипуляций
| Группа | Только периостотомия | Удаление причинного зуба и периостотомия | Раскрытие полости причинного зуба и периостотомия |
| Группа сравнения I | 16 | 26 | 2 |
| Основная II | 14 | 13 | 2 |
У больных группы сравнения при наличии показаний (наличие сопутствующей соматической патологии, сложное удаление зуба одномоментно с периостотомией, сохранение причинного зуба, отсутствие санации полости рта) назначалась эмпирическая антимикробная терапия, исходя из общепринятых данных о видовом составе возбудителей ОИ.
У больных основной группы с помощью разработанного физико-химического метода, включающего сочетанное применение ЛФД и детергента (мирамистин), в течение 1,5-2 часов устанавливалась чувствительность микрофлоры из патологического очага к одному из предположительных АМП.
Динамику послеоперационного периода в обеих группах оценивали на вторые сутки после проведенного вмешательства (на первой перевязке) у больных обеих групп. Выздоровление констатировали по следующим критериям: нормализация температуры тела; уменьшение болевого синдрома до незначительной болезненности/дискомфорта в области постоперационной раны (ПР); уменьшение отечности мягких тканей соответствующей области лица; отсутствие гиперемии кожных покровов; отсутствие инфильтрата в области ПР; незначительная выраженность налета фибрина в области ПР. При сохранении хотя бы одного из данных критериев, дренаж заменяли на новый с медобработкой ПР смесью перекиси водорода 3% и хлоргексидина 0,02% в соотношении 1:1 и продолжали наблюдение за пациентом до полного его выздоровления.
Алгоритм разработанной физико-химической методики сочетания ЛФД с детергентом (мирамистин) для подбора АМП
Всем больным основной группы II с помощью стерильной иглы диаметром 0,9 мм после проведенной местной анестезии и до выполнения периостотомии проводили аспирацию экссудата из патологического очага в количестве 0,5-1,0 мл. Далее 1,0-1,5 мл полученного после разведения (для увеличения количества) физиологическим раствором в два раза исходного экссудата разделяли на части по 0,25 мл в пробирках «Эппендорф». Число исходных проб составляло 4-6. К каждой из проб добавлялся АМП, проводилась экспозиция в течение 60 мин.
Далее после экспозиции к смеси экссудата с АМП добавлялся детергент (мирамистин 0,01%-0,5%) для оценки наличия живых микробов. Эта технология разработана нами и является физико-химической, поскольку сочетает физические явления (ЛФД) с химическим агентом (мирамистин). Необходимость применения детергента вызвана тем, что для эндогенных порфиринов, содержащихся внутри всех видов микробов, характерно наличие «тушения флюоресценции», что не позволяет им эффективно преобразовывать поглощаемое лазерное излучение во флюоресценцию (Иванова М.А., 2010). Применение детергента позволяет высвободить эндогенные порфирины из внутриклеточного состояния во внешнюю среду и таким образом интегрально повысить интенсивность флюоресценции без изменения спектральной характеристики объекта исследования (и в тоже время различить живые и «убитые» микробы и тем самым оценить эффективность антимикробного лечения в целом). Кроме этого, это позволяет существенно повысить информативность и чувствительность ЛФД (особенно при исходно низких показателях флюоресценции, что иногда встречается у некоторых пациентов) (общеизвестно, что М линейно зависима от концентрации порфиринов микробов). Важно подчеркнуть, что поскольку детергентное воздействие реализуется практически сразу, нет необходимости в длительной экспозиции смеси экссудата с АМП (24 ч.) для выявления его эффекта, что и требуется соответственно условиям СП. Таким образом, использование детергента определило новизну применения технологии ЛФД как метода экспресс-определения чувствительности микроба к АМП и эффективности антимикробного воздействия (определение живых и «убитых» микробов). Нами проведен анализ оптимальной и минимально возможной детергентной концентрации мирамистина от 0,01% до 0,5% (изготовлено в ЗАО «Инфамед»).
Результаты ЛФД учитывали следующим образом: если М образца исследуемого экссудата с АМП после 60-минутной экспозиции увеличивалась, а после добавления мирамистина имелось значительное повышение М, это являлось свидетельством присутствия живых микробов. Данный препарат считался неэффективным.
Все исследования проводились с использованием сертифицированных установок Флюол» (рег. удостоверение № ФС 02012006/5578-06), «Спектролюкс МБ» (№ФС 022а2005/2087-05) и «ЛЭСА» (ФСР 2008/03784).
Расчет экономической эффективности новой сочетанной физико-химической методики применения технологии ЛФД и мирамистина
В системе ОМС по коду услуги 009351 «Перевязка гнойных ран» трудозатраты в денежном эквиваленте составляют 46,26 руб. (программа «Сирена») (S). Зная количество перевязок больных в основной группе (Х) и группе сравнения (Y), вычислялась эта разница R= Y-Х и умножалась на S. Обращаемость больных с ОГП в определенную СП в год обозначим как К. Формула расчета экономической эффективности (Е) при использовании ЛФД у больных с ОГП будет следующей: Е=RSК= … руб/год. Эта цифра (Е) соотносилась со стоимостью закупки для СП сертифицированной установки «Флюол».
Результаты собственных исследований и их обсуждение
В 37% всех случаев эндодонтического лечения (ЭЛ) в МЧУ ПГ проводилась девитализация зубов «по ортопедическим показаниям». При этом полностью запломбированными (по данным интраоральной рентгенографии и панорамной зонографии) из 1022 зубов оказались только 346 (34%) зубов, в 6 % случаев у апексов этих зубов определялись деструктивные процессы (р0,001).
Анализ работы пародонтологического кабинета МЧУ ПГ в период с 2005 по 2009 гг. представлен на рис. 1. Видно значительное несоответствие объема оказываемой помощи количеству прикрепленных пациентов.
Те же проблемы недополучения пародонтологической помощи выявлены и в СП МО (рис. 2). Сложившаяся ситуация не может не сказываться и на успехе ЭЛ, поскольку связь между пульпой и пародонтом является доказанной (Гутман Дж.Л. и соавт, 2008; Иванов В.С. и соавт, 2003). На этом фоне успех ЭЛ в РФ в отдаленные сроки составляет лишь 29 % (Хохрина Т.Г., 2007). Хронический очаг ОИ, возникший в результате некачественного ЭЛ, является причиной развития ОВЗ ЧЛО в 85-98% наблюдений (Хохрина Т.Г., 2007), в частности, ОГП в 65% случаев (Абрамович А.М. и соавт., 2003), поэтому и заболеваемость ОГП в условиях СП не снижается.
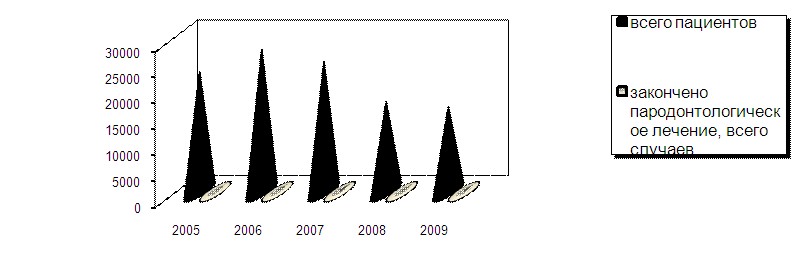
Рис. 1. Анализ пародонтологического лечения в МЧУ ПГ.
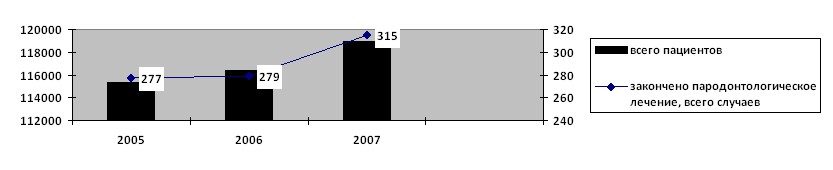 Рис. 2. Анализ показателей пародонтологического лечения в СП МО.
Рис. 2. Анализ показателей пародонтологического лечения в СП МО.
Аналогичны и показатели распространенности кариеса зубов и его осложнений в условиях данных стоматологических поликлиник (табл. 4).
Таблица 4
Сравнительный анализ оказания помощи взрослому контингенту
| распространен- ность кариеса | кариес на 1000 человек | осложнения кариеса на 1000 человек | удаления на 1000 человек | санаций на 1000 человек | |
| МЧУ ПГ | 85,3% | 1131,5 | 174,2 | 146,8 | 210,3 |
| СП МО | 59,2% | 216,1 | 106,8 | 154,8 | 1,2 |
Несмотря на лучшее техническое оснащение (наличие лазерного аппарата SIROLaser ™, микроскопа ZEISS PRO EGRO, стоматологических установок производства фирмы SironaC2+, ортопантомографа Orthophos Sirona), более квалифицированный кадровый состав (один кандидат медицинских наук и один доктор медицинских наук в МЧУ ПГ и отсутствие ученых степеней у врачей в СП МО), меньшее количество прикрепленных пациентов (20460 чел. против 118994 чел.), лучшее территориальное расположение МЧУ ПГ, проблемы оказания помощи в условиях данных СП в целом сходны. Это подтверждает несовершенство некоторых имеющихся методик лечения больных в условиях СП.
Результаты экспериментального этапа работы.
Установлено, что показатель М1 интактной эмали в среднем составляет 8.9±0,4 относительных единиц флюоресценции, а у интактного дентина - 7.2±0,3 (различия М недостоверны (p>0,05)), т.е. они оказались близки между собой. К данному показателю должен стремиться параметр Мn+1 очага ОИ после этиотропного воздействия на него. Полученные числовые данные об изменении М в ходе такого воздействия на флотирующих микробов в основном просвете КК удаленных зубов, как модели очага ОИ, представлены в табл. 5.
Таким образом, в данном эксперименте еще раз подтверждены имеющиеся данные о наиболее эффективных АМП для местного воздействия на микрофлору из очагов ОИ в условиях СП, а также проведена оценка чувствительности (Ч) и специфичности (S) ЛФД при воздействии на очаги ОИ.
Мn флотирующей микрофлоры в основном просвете КК зуба, удаленного по клиническим показаниям, до какого-либо антимикробного воздействия на нее, всегда выше в 2-10 раз, чем М1 эмали иммунных зон зуба или интактного дентина (очищенного ультразвуком). Ч составляет 99,5%. При исследовании интактных тканей удаленных зубов не было выявлено М1, по интенсивности равной Мn флотирующей микрофлоры инфицированного КК удаленного зуба. М интактной ткани зуба (эмаль или дентин) в 2-10 раз ниже. S составляет 99,5%. Таким образом, выявлены высокая чувствительность и специфичность метода ЛФД для оценки качества санации очага ОИ (на модели инфицированного КК зуба), что позволяет применять ее на клиническом этапе.
Таблица 5
Сравнительная характеристика антисептиков при воздействии на микрофлору очагов ОИ (на примере КК удаленных зубов)
| Антисептик | Среднее снижение М в КК, % | Отношение к показателям М1, % |
| Перекись водорода 3% | 3,7 | 182 |
| Хлоргексидин 2% | 33,4 | 153 |
| Гипохлорит Na 3% | 45,9 | 53 |
| Перекись водорода 3% + NO | 63,9 | 5 (Р<0,01) 6 |
| Перекись водорода 3%+ гипохлорит Na 3% | 72,8 |
Повышение чувствительности метода ЛФД с помощью детергента.
В ходе эксперимента нами совместно с профессором Александровым М.Т. (при непосредственной консультативной помощи акад. РАМН, проф. Бажанова Н.Н.) установлено, что при добавлении мирамистина к микробосодержащему субстрату из очага ОИ в случае наличия большого количества живых микробов высвобождаются эндогенные порфирины, что приводит к резкому усилению спектральной интенсивности флюоресценции без изменения ее амплитудно-спектральных характеристик. При наличии мертвых микробов такого усиления не наблюдается (рис. 3). В ходе экспериментов нами было установлено, что данный эффект реализуется только для начальной концентрации мирамистина 0,1% и выше.
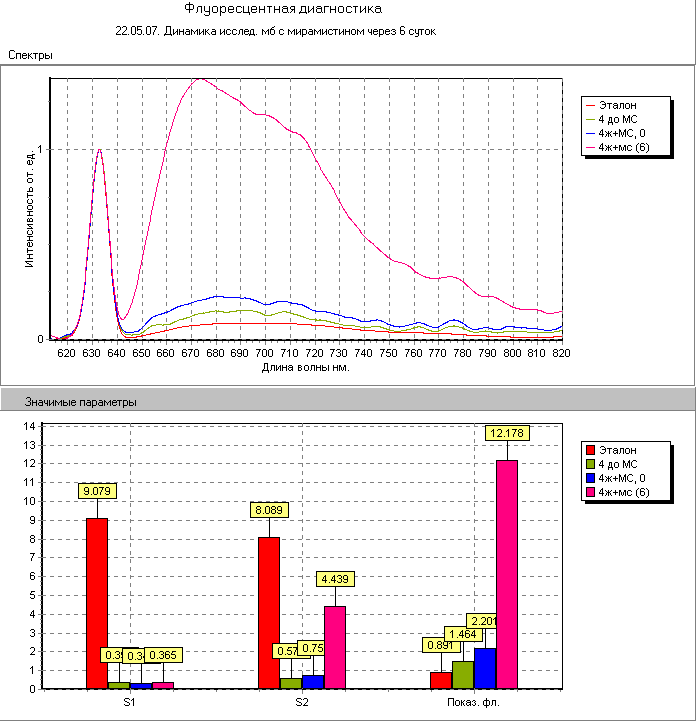
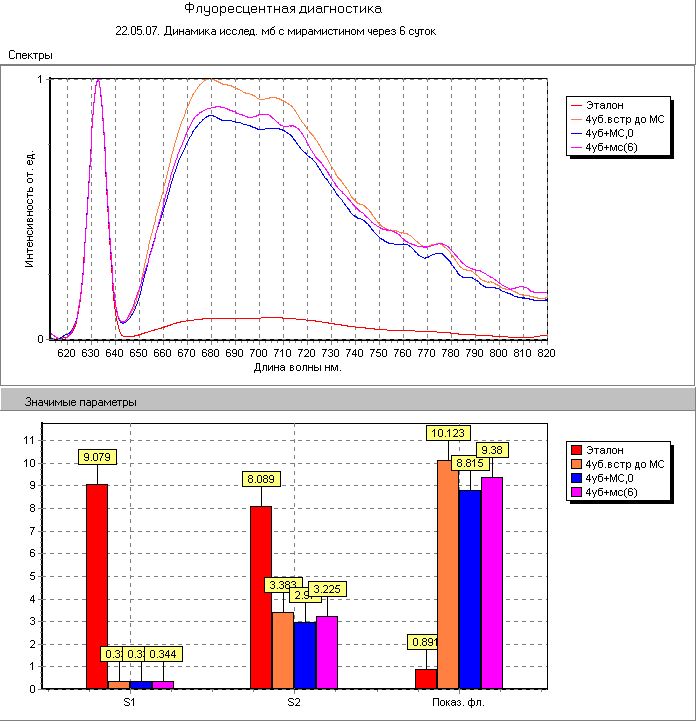
Рис. 3. Спектры флюоресценции микробов из очага ОИ после воздействия мирамистином 0,1% при наличии живых микробов (слева-повышение флюоресценции) и мертвых (справа-отсутствие такового).
Результаты применения физико-химической технологии сочетания ЛФД и мирамистина 0,1% при подборе предпочтительных АМП.
Сравнительная характеристика течения постоперационного периода у больных основной группы и группы сравнения с ОГП приведена ниже. На всех диаграммах анализируемые параметры приведены в %.
У 26 больных основной группы II на 2-е сутки после проведения хирургического пособия видимая отечность мягких тканей соответствующей анатомической области лица практически отсутствовала (89,3%) или была незначительно выражена у 3 больных(10,7%). У больных группы сравнения, как правило, видимая отечность мягких тканей соответствующей зоны лица сохранялась или была более выражена, чем при первичном приеме, в 100% случаев (р<0,05). Динамика остальных показателей представлена на рис. 4-6.
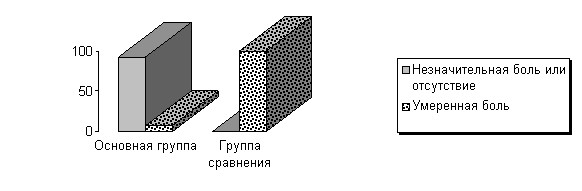
Рис. 4. Выраженность болевого синдрома на 2-е сутки после хирургического пособия у больных с ОГП (на первой перевязке) (р<0,001).
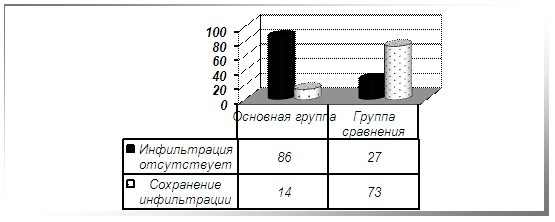
Рис. 5. Наличие инфильтрации краев в области ПР на 2-е сут (р<0,05).
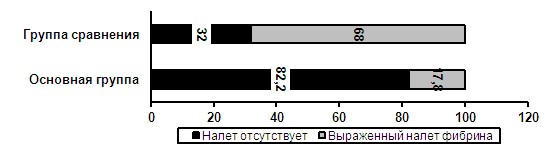
Рис. 6. Выраженность налета фибрина в области ПР на 2-е сут (р<0,05).
Дополнительное применение мирамистина 0,1% для суждения о механизме действия данного АМП представлено на рис. 7-9.
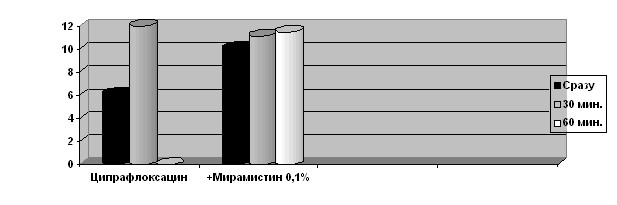
Рис. 7. Этап подбора ципрафлоксацина.
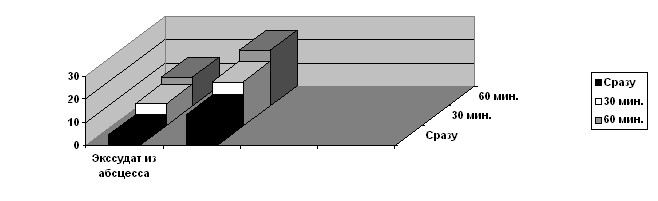 Рис. 8. Экссудат из патологического очага при ОГП.
Рис. 8. Экссудат из патологического очага при ОГП.
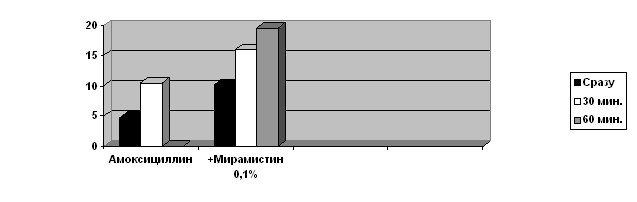
Рис. 9. Пробы с амоксициллином.
В обоих случаях через 30 мин видно повышение М. Это можно трактовать как значительное бактерицидное действие для данных концентраций АМП или размножение микробов при неэффективности АМП. Именно мирамистин 0,1% помогает решить этот вопрос: при контрольном его добавлении к смесям экссудата с АМП в образце с амоксициллином видно значительное повышение М – значит, в образце много живых микробных тел и исходное повышение М было связано с неэффективностью препарата и размножением микробов при экспозиции смеси. В образце с ципрафлоксацином такого повышения не наблюдается, значит, повышение М в смеси экссудата с ципрафлоксацином связано со значительным бактерицидным его воздействием для данной концентрации. Для данной микрофлоры конкретного пациента предпочтительным АМП является ципрофлоксацин. Если бы не был проведен тест с мирамистином 0,1%, у лечащего врача появился бы «выбор» между двумя препаратами, что могло бы привести к неверному назначению антибиотикотерапии.
В целом, в результате назначения адекватной антимикробной терапии в основной группе больных с ОГП установлено сокращение сроков лечения больных и количества перевязок (табл. 6) (р<0,001).
Таблица 6
Сроки лечения и количество перевязок у больных с ОГП
| Группа больных с СА | Клиническое излечение, сут. | Количество перевязок |
| Основная | 3,08±0,24 | 1 |
| Контрольная | 4,18 ± 0,12 | 1,8±0,1 |
Алгоритм сочетанного применения новой разработанной нами медицинской физико-химической технологии на основе ЛФД и препарата детергентного действия (мирамистин 0,1%) иллюстрируют рис. 10-13. С помощью метода ЛФД в течение 1,5 часов установлена наибольшая чувствительность микрофлоры к ципрафлоксацину.
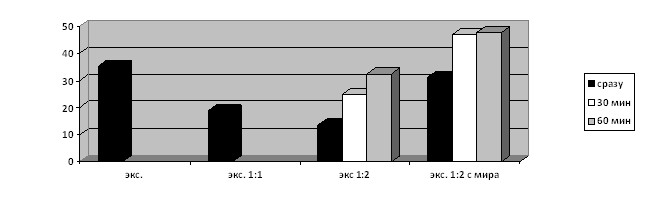 Рис. 10. Экссудат из очага ОИ в разведениях физ. Раствором в один (1:1) и два (1:2) раза и после добавления 0,1% мирамистина.
Рис. 10. Экссудат из очага ОИ в разведениях физ. Раствором в один (1:1) и два (1:2) раза и после добавления 0,1% мирамистина.
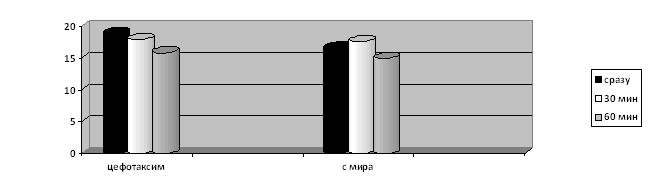
Рис. 11. Цефотаксим эффективен: при экспозиции экссудата с ним М падает, после добавления мирамистина 0,1% повышение незначительно (не превышает таковое в сравнении экссудата 1:2 с мирамистином 0,1%).
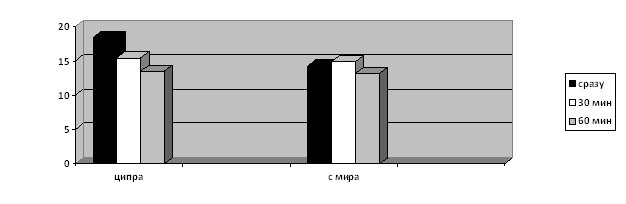
Рис. 12. Ципрафлоксацин более эффективен, чем цефотаксим-при экспозиции М падает более значительно, при добавлении мирамистина 0,1% М практически не повышается (микробы «убиты»). Предположителен бактерицидный механизм действия (живых микробов нет).
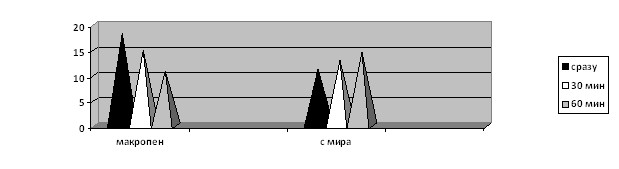
Рис. 13. Макропен эффективен, однако механизм действия бактериостатический (имеется повышение М после добавления мирамистина 0,1% - есть живые микробы после экспозиции).
Вывод: микрофлора из ОГП чувствительна к цефотаксиму, ципрафлоксацину и макропену. Однако из предложенных АМП предпочтителен ципрафлоксацин ввиду его бактерицидного действия (по сравнению с макропеном) и отсутствия (по сравнению с цефотаксимом) повышения М после добавления мирамистина 0,1% (отсутствие живых микробов).
Расчет экономической эффективности от предлагаемой физико-химической медицинской технологии подбора предпочтительных АМП в комплексном лечении больных с ОГП
Учитывая, что в основной группе проводилась одна перевязка, а в группе сравнения, как правило, две перевязки (в среднем 1,8), то разница расходов на лечение по бюджету здравоохранения составляет 46,26 руб. на одного человека. Экстраполируя эти данные на СП МО, с учетом количества пациентов, обратившихся с ОГП в различные годы (рис. 14.), можно было бы уменьшить расходы в системе ОМС на лечение таких пациентов в условиях данной СП на: 46,26 руб.*952=44039,52 руб. в 2005 году; на 58657,68 руб. в 2008 году.

Рис. 14. Обращаемость больных с ОГП по данным СП МО.
Стоимость сертифицированной установки «Флюол» для проведения ЛФД в базовой комплектации составляет 390 000 руб. Окупаемость данной установки только при лечении больных с ОГП может составить: 390000/44040 или 39000/58657,68, то есть, 6,7-9 лет в условиях одной СП.
Данные цифры могут колебаться в сторону уменьшения или увеличения, поскольку зависят от множества факторов (географического положения, объема прикрепленного населения, количества врачебных ставок и др.), но они отражают перспективы применения ЛФД в условиях СП в экономическом плане.
ВЫВОДЫ
- Распространенность одонтогенных воспалительных заболеваний челюстно-лицевой области остается стабильно высокой (59,2%-85,3%). При этом качество оказания помощи продолжает оставаться на низком уровне: успех эндодонтического лечения зубов составляет лишь 34%, то есть в 66% случаев после такого «лечения» зуб остается источником одонтогенной инфекции; при этом сохраняется высоким процент депульпирования зубов по «ортопедическим показаниям» (37%); объемы оказываемого пародонтологического лечения не соответствуют 100% распространенности заболеваний пародонта у взрослого населения.
- Установленная 100% диагностическая чувствительность и специфичность модифицированной нами на основе применения нефлюоресцирующего детергентного препарата (мирамистин 0,1%) методики лазерно-флюоресцентной диагностики позволяет применять ее в условиях стоматологической поликлиники для индикации наличия аэробной и анаэробной микрофлоры и их смесей (ассоциаций) из очагов одонтогенной инфекции. Детергентное воздействие мирамистина в установленной оптимальной концентрации (0,1%) на микрофлору из очагов одонтогенной инфекции позволяет определить, живая (активная) или мертвая микрофлора преобладает в данном очаге и, тем самым, оценить эффективность антимикробного лечения в целом.
- Разработанная физико-химическая технология сочетанного применения лазерно-флюоресцентной диагностики и детергента (мирамистин 0,1%) и ее клинический алгоритм способствует повышению экспрессности лазерно-флюоресцентной диагностики в 12 раз (с 24 до 2 часов). Это дает возможность индивидуального подбора предпочтительных антимикробных препаратов в комплексном лечении больных с острым гнойным периоститом непосредственно в условиях стоматологической поликлиники, что позволит сократить сроки лечения данных больных на 1,1 сут.
- Применение разработанной технологии позволит уменьшить стоимость лечения по бюджету на 46,26 руб. на одного пациента с острым гнойным периоститом, а в условиях одной стоматологической поликлиники - на 44039,52 - 58657,68 руб./год, для 720 стоматологических поликлиник России - на 31 708 454,4 руб./год.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Необходимо внедрение массовой профилактики кариеса зубов и его осложнений, заболеваний пародонта как основного фактора, определяющего этиологию одонтогенных воспалительных заболеваний челюстно-лицевой области в условиях стоматологической поликлиники, а также диспансеризации всех слоев населения.
- Для подбора предпочтительных антимикробных препаратов в комплексном лечении больных с острыми гнойными периоститами рекомендуется применять разработанную нами физико-химическую медицинскую технологию сочетанного применения метода лазерно-флюоресцентной диагностики и препарата детергентного действия (мирамистин 0,1%) по соответствующему алгоритму: с помощью стерильной иглы диаметром 0,9 мм после проведенной местной анестезии и до выполнения периостотомии проводится аспирация экссудата из патологического очага в количестве 0,5-1,0 мл. Далее 1,0-1,5 мл полученного после его разведения физиологическим раствором в два раза разделяется на части по 0,25 мл в пробирках «Эппендорф» (число исходных проб 4-6). К каждой из проб добавляются различные антимикробные препараты, проводится экспозиция в течение 60 мин. Далее после экспозиции к смеси экссудата с антимикробным препаратом добавляется мирамистин 0,1%. Если нормированная мощность флюоресценции М образца исследуемого экссудата с антимикробным препаратом после 60-минутной экспозиции увеличилась, а после добавления мирамистина 0,1% имеется значительное повышение М, это является свидетельством присутствия живых микробов. Данный препарат считается неэффективными и наоборот.
Список работ, опубликованных по теме диссертации
- Александров М.Т., Гапоненко О.Г., Хоменко В.А., Попов С.Н., Воропаева М.И., Новожилова Н.Е., Василенко О.Ю., Васильев Е.Н., Миланич А.И., Мищенко И.М. Патент 2381766 от 08.06.2007. Способ оценки качества обработки корневых каналов зуба при эндодонтическом лечении.
- Александров М.Т., Гунько В.И., Пашков Е.П., Попов С.Н., Терехов А.С., Васильев Е.Н., Иванченко О.Н., Родионов А.Д. Применение лазерно-конверсионной диагностики в стоматологии (обзор) // Сб. тр. научно-практической конференции Студенческого научного общества стоматологического факультета, посвященный памяти академика РАМН, профессора Н.Н. Бажанова. – М.: Первый МГМУ им. И.М. Сеченова, 19 апреля 2011. – С.4-5.
- Александров М.Т., Пашков Е.П., Быков А.С., Гунько В.И., Попов С.Н., Иванченко О.Н., Родионов А.Д., Гизатуллин Р.М. 20-летний опыт применения лазерно-флюоресцентной диагностики в клинической микробиологии // Вестник РАМН. – 2011. – № 1. – С. 35-39.
- Александров М.Т. Лазерная клиническая биофотометрия (теория, эксперимент, практика) – М.: Техносфера, 2008. – 584 с. – Александров М.Т., Попов С.Н., Родионов А.Д., Аразашвили Л.Д., Гизатуллин Р.М. Глава 9 // Лазерная медицинская технология оценки качества обработки корневых каналов зуба при эндодонтическом лечении. - С. 304-308.
- Гунько В.И., Пашков Е.П., Попов С.Н., Быков А.С., Родионов А.Д., Александров М.Т., Иванченко О.Н. Гизатуллин Р.М.. Повышение эффективности диагностики и лечения больных с гнойно-воспалительными заболеваниями на основе применения лазерно-флуоресцентной диагностики // Вестник РУДН. – 2012. – № 1. – С.93-98.
- Иванченко О.Н., Попов С.Н., Александров М.Т., Иванова Е.В., Волков Е.Е., Серебряков Е.И. Ретроспективный анализ клинико-статистических данных оказания стоматологической помощи в ведомственной поликлинике // Российский стоматологический журнал. – 2010. – № 5– С.38-45.
- Попов С.Н. Оценка качества обработки корневого канала зуба методом лазерной флюоресценции // II Международная научно-практическая конференция «Научно-техническое творчество молодежи – путь к обществу, основанному на знаниях»: сб. науч. докл. – М.: МГСУ, 29 июня - 02 июля 2010. – С.329-330.
- Попов С.Н. Возможности и перспективы применения лазерно-конверсионной диагностики в стоматологии // Материалы II научно-практической конференции молодых ученых «Современные технологии в экспериментальной и клинической стоматологии». – М., 19 мая 2011. – С. 122-125.
- Холопова Е.В., Александров М.Т., Пашков Е.П., Попов С.Н. Повышение эффективности диагностики и лечения больных с одонтогенными воспалительными заболеваниями челюстно-лицевой области на основе лазерно-флюоресцентных технологий в условиях стоматологической поликлиники // III Международная научно-практическая конференция «Научно-техническое творчество молодежи – путь к обществу, основанному на знаниях»: сб. научн. докл. – М.: МГСУ, 28 июня - 01 июля 2011. – С. 446-447
СПИСОК СОКРАЩЕНИЙ
ОВЗ ЧЛО - одонтогенные воспалительные заболевания ЧЛО
ЛФД - лазерно-флюоресцентная диагностика
СП - стоматологическая поликлиника
ОГП - острый гнойный периостит
АП - апикальный периодонтит
КК - корневой канал
ЭЛ - эндодонтическое лечение
ОИ - одонтогенная инфекция
ПР - постоперационная рана
Подписано в печать.
Формат А4
Бумага офсетная. Печать цифровая.
Тираж 100 экз. Заказ № z0935
Типография ООО “Ай-клуб” (Печатный салон МДМ)
119146, г. Москва, Комсомольский пр-т, д.28

