Ультразвуковой допплерографический мониторинг мозговой гемодинамики при врожденной патологической извитости внутренних сонных артерий
На правах рукописи
ИСАКОВА
Ольга Ивановна
УЛЬТРАЗВУКОВОЙ ДОППЛЕРОГРАФИЧЕСКИЙ МОНИТОРИНГ МОЗГОВОЙ ГЕМОДИНАМИКИ ПРИ ВРОЖДЕННОЙ ПАТОЛОГИЧЕСКОЙ ИЗВИТОСТИ ВНУТРЕННИХ
СОННЫХ АРТЕРИЙ
14.01.13 – лучевая диагностика, лучевая терапия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург – 2012
Работа выполнена в Государственном бюджетном образовательном учреждении высшего профессионального образования «Алтайский государственный медицинский университет» Министерства здравоохранения и социального развития Российской Федерации.
Научный руководитель:
доктор медицинских наук
профессор Брюханов Александр Валерьевич
Официальные оппоненты:
доктор медицинских наук
профессор Мазур Виктор Григорьевич
доктор медицинских наук
профессор Ремнев Андрей Геннадьевич
Ведущее учреждение: Государственное бюджетное образовательное учреждение высшего профессионального образования «Московский государственный медико-стоматологический университет» Министерства здравоохранения и социального развития Российской Федерации
Защита состоится « 28 » февраля 2012 г. в ___ на заседании Совета по защите докторских и кандидатских диссертаций Д 215.002.11 в федеральном государственном военном образовательном учреждении высшего профессионального образования «Военно-медицинская академия им. С.М.Кирова» Министерства обороны Российской Федерации (194044, Санкт-Петербург, ул. Академика Лебедева, 6)
С диссертацией можно ознакомиться в фундаментальной библиотеке федерального государственного военного образовательного учреждения высшего профессионального образования «Военно-медицинская академия им. C.М.Кирова» Министерства обороны Российской Федерации
Автореферат разослан «____» января 2012 г.
Ученый секретарь совета
доктор медицинских наук профессор
Головко Александр Иванович
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Несмотря на снижение смертности от церебро-васкулярных заболеваний, проблема нарушений мозгового кровообращения – ранняя диагностика, профилактика, предупреждение в настоящее время и в России, и за рубежом продолжает оставаться актуальной (Кадыков А.С. и др., 1996; Казанцева И.В., 2008). Нарушения мозгового кровообращения регистрируются уже с раннего детского возраста (Смирнова Ю.В., 2000). Основная их причина – патологическая извитость внутренней сонной артерии (ПИ ВСА) (Куликов В.П., 2000; Евтушенко С.К., Евтушенко О.С. и др., 2003; Лисовский Е.В., Яворская О.Л. и др., 2005; Лобов М.А., Казанчан П.Г. и др., 2006). Частота врожденной ПИ ВСА варьирует от 9 до 43% (Верещагин Н.В. и др., 1972; Покровский А.В. и др., 1992; Жулев Н.М., 2004). Признак извитой внутренней сонной артерии передается по наследству по аутосомно-доминантному (37,7%) и аутосомно-рецессивному типу (39,3%) (Смирнова Ю.В., 2007), считается проявлением сосудистого синдрома недифференцированной дисплазии соединительной ткани (Нечаева Г.И., 2008). Извитость у детей клинически проявляется хронической цереброваскулярной недостаточностью в 93,6% случаев; в 4,3% является причиной преходящих нарушений мозгового кровообращения, в 2,1% - ишемического инсульта. У 19,3% пациентов детского возраста с эпилептическими припадками диагностируется ПИ ВСА (Смирнова Ю.В. и др., 2007). Основным звеном патогенеза нарушений мозгового кровообращения при врожденной ПИ ВСА у детей считаются локальные нарушения гемодинамики в виде турбуленции в зоне максимальной ангуляции со снижением кровотока за зоной деформации, что обуславливает снижение скорости кровотока в средней мозговой артерии (СМА) и снижение перфузии мозга (Герасименко И.Н., 1998; Куликов В.П., Хорев Н.Г., 2000; Смирнова Ю.В., 2007).
На ведущую роль турбуленции при ПИ ВСА в развитии нарушений мозгового кровообращения указывают Джибладзе Д.Н. (1996); Кухтевич И.И.(1998); Кунцевич Г.И. (2006) и другие. О тромбоэмболическом механизме воздействия приобретенных ПИ ВСА на мозговую гемодинамику вследствие артерио-артериальной эмболии пристеночными тромбами, образующимися в местах длительно существующих перегибов и в петлях, говорили еще в 1972 году Верещагин Н.В., Левина Г.Я..
Развитие в последние два десятилетия ультразвукового транскраниального мониторинга с эмболодетекцией, большое число работ по диагностике кардиальной и артерио-артериальной эмболии сосудов мозга (Шевченко Ю.Л., Одинак М.М. и др., 2006; Гайдар Б.В, Семенютин В.Б., Парфенов В.Е., Свистов Д.В., 2008; Сандриков А.А. и др., 2009) – все вместе взятое позволило нам предположить также тромбоэмболический механизм развития нарушений мозгового кровообращения при врожденной ПИ ВСА у детей. Патогенное воздействие на сосуды мозга микроэмболов, образующихся из форменных элементов крови вследствие спонтанной агрегации в дезорганизованных турбулентных потоках на участках извитостей ВСА, является одной из ведущих причин развития цереброваскулярных нарушений при данной патологии. Современные ультразвуковые методы, проведенные комплексно – дуплексное сканирование экстракраниальных отделов брахиоцефальных сосудов (УЗДС), дуплексное сканирование транскраниальное и транскраниальная допплерография (ТКДГ) с возможностью мониторирования и эмболодетекцией – подтвердили предположения о новом патогенетическом механизме развития цереброваскулярных нарушений при врожденной патологической извитости внутренних сонных артерий у детей.
Цель исследования – совершенствование ранней диагностики и профилактики нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий на основании проведения комплексного ультразвукового исследования.
Основные задачи исследования:
- Выявить и оценить степень изменений показателя линейной скорости кровотока в средних мозговых артериях, вызванных локальными нарушениями гемодинамики на участках патологических извитостей внутренних сонных артерий у детей.
- Выделить варианты патологической извитости внутренних сонных артерий и определить связь микроэмболических сигналов в средних мозговых артериях с локальными нарушениями гемодинамики, возникающими на извитых участках внутренних сонных артерий.
- Дать характеристику физических параметров типов микроэмболических сигналов, регистрируемых в средних мозговых артериях у детей с патологическими извитостями внутренних сонных артерий.
4. C помощью метода транскраниальной допплерографии с возможностью мониторирования и эмболодетекции доказать тромбоэмболический характер нарушений мозгового кровообращения при патологической извитости внутренних сонных артерий у детей.
Научная новизна. Настоящая работа является первым научным иссле-дованием в определении тромбоэмболического характера нарушений мозго-вого кровообращения у детей с патологической извитостью внутренних сон-ных артерий.
С помощью единого современного комплексного ультразвукового исследования – дуплексного сканирования сосудов и транскраниальной допплерографии с возможностью мониторирования и эмболодетекции – показано, что в дезорганизованных турбулентных потоках на участках извитых внутренних сонных артерий из форменных элементов крови образуются микроагреганты двух типов, регистрируемые в средних мозговых артериях как микроэмболические сигналы (МЭС). Определены их физические параметры.
Практическая значимость работы. Обоснована целесообразность комплексного подхода – проведения дуплексного сканирования сосудов, транскраниальной допплерографии с возможностью мониторирования и эмболодетекции, нейрофизиологических, лабораторных методов - при обследовании детей с патологической извитостью внутренних сонных артерий. Показаны клинические, гемодинамические и функциональные критерии значимости этой патологии.
Полученные результаты УЗДС и ТКДГ с возможностью мониторирования и эмболодетекции у детей с ПИ ВСА свидетельствуют о тромбоэмболическом, как наиболее вероятном, механизме нарушений мозгового кровообращения при данной патологии, являются основой для назначения патогенетического лечения.
Основные положения, выносимые на защиту:
- Локальные нарушения гемодинамики в виде турбуленции в зоне извитостей внутренних сонных артерий у детей не приводят к снижению линейной скорости кровотока в средних мозговых артериях. В дезорганизованных турбулентных потоках из форменных элементов крови образуются микроагреганты двух типов, регистрируемые в средних мозговых артериях как микроэмболические сигналы.
- Регистрация в средних мозговых артериях микроэмболических сигналов у детей с патологической извитостью внутренних сонных артерий позволяет предположить тромбоэмболический механизм нарушений мозгового кровообращения при данной патологии.
- Транскраниальная допплерография с возможностью мониторирования и эмболодетекции является высокоинформативным методом раннего выявления риска микроэмболизации средних мозговых артерий у детей с патологической извитостью внутренних сонных артерий.
Личный вклад автора в проведенное исследование. Диссертант самостоятельно отбирала пациентов для исследования, подготавливала базу данных, заполняла регистрационные карты, обрабатывала полученные материалы. Автором выполнено ультразвуковое дуплексное сканирование, ТКДГ-мониторирование с эмболодетекцией 92 пациентам. Достоверность полученных результатов подтверждается достаточным объемом клинического материала, использованием методик, адекватных поставленным задачам, применением методов статистического анализа. Изложение и интерпретация полученных материалов, формулирование выводов и практических рекомендаций выполнены соискателем самостоятельно.
Апробация материалов диссертации. Материалы и основные положения диссертационной работы доложены и обсуждены на XIV международной конференции “Современное состояние методов неинвазивной диагностики в медицине” (2007); V Cъезде Российской ассоциации специалистов ультразвуковой диагностики в медицине (2007); российской научно-практической конференции “Нарушения мозгового кровообращения: диагностика, профилактика, лечение” (2010). Апробация диссертации состоялась на конференции кафедр лучевой диагностики АГМУ, МГМСУ, СибГМУ, ОГМУ, НГМУ, отдела функциональной и ультразвуковой диагностики КГБУЗ “ДЦАК” 21 октября 2011 года.
Публикации по теме диссертации. По теме диссертации опубликовано 12 научных работ в материалах научных конференций, симпозиумов и сборниках научных трудов, из них 3 в журналах, рекомендованных ВАК для публикации научных результатов диссертаций на соискание ученой степени. Соискателем получен патент на изобретение № 2421141 “Способ определения риска микроэмболизации средней мозговой артерии у детей с патологической извитостью внутренней сонной артерии”, приоритет от 02.11.2009г., зарегистрирован в Гос. реестре 20.06.2011.
Объем и структура диссертации. Диссертация изложена на 145 страницах машинописного текста, содержит 44 таблицы, 23 рисунка, пять клинических наблюдений. Состоит из введения, 4 глав, заключения, выводов, практических рекомендаций и списка литературы, включающего 90 отечественных и 80 иностранных источников.
СОДЕРЖАНИЕ РАБОТЫ.
Работа основана на анализе результатов комплексного клинико- диагностического обследования 92 пациентов, состоявших на диспансерном учете у детского невролога в КГБУЗ “Диагностический центр Алтайского края” в период 2007-2009 годов. У всех детей исследовался экстракраниальный и мозговой кровоток c мониторированием и эмболодетекцией последнего.
Материал и методы исследования. В основную группу были включены 70 детей с диагнозом вегето-сосудистой дистонии (ВСД), в анамнезе у которых по данным предварительного дуплексного сканирования сосудов были выявлены извитости или деформации экстракраниальных отделов внутренних сонных артерий, одно- и двухсторонние, при этом по данным предварительной эхокардиографии отсутствовала патология сердца (инфекционный эндокардит, миксома и другие опухоли сердца, кардиомиопатия, митральный и другие пороки, пролапсы, регургитации, открытое овальное окно) как возможный источник кардиальной эмболии. Среди пациентов преобладали мальчики – 42 (60 %). Девочек было 28 (40%). Средний возраст мальчиков составил 11.9±3.1 лет, средний возраст девочек – 10.6±2.7 лет. Для контрольной группы были отобраны 22 ребенка с диагнозом ВСД, у которых при предварительном дуплексном сканировании не была выявлена патология (извитости или деформации) внутренней сонной артерии и по данным эхокардиографии отсутствовала патология сердца как возможный источник кардиальной эмболии. В группе было 10 мальчиков (45.5%) и 12 девочек (54.5%), cредний возраст обоих полов 12±2.7 лет.
Всем детям было проведено клиническое, лабораторное, инструментальное нейрофизиологическое, функционально-диагностическое и ультразвуковое исследования.
Клинические методы исследования включали изучение жалоб, анамнеза болезни, объективное исследование общего и неврологического статуса.
Из лабораторных исследований всем пациентам выполнен развернутый анализ венозной крови на автоматическом гематологическом анализаторе Sysmex, XT-2000i (Япония), в том числе с обязательным анализом морфометрических характеристик тромбоцитов: количество тромбоцитов (10*3/ml), средний объем тромбоцитов (fl), тромбокрит (%), широта распределения (%) (Суворова А.В., Зорькина А.В.,1997). Исследования первичного тромбоцитарного и коагуляционного гемостаза проводились согласно методическим рекомендациям Баркагана З.C., Момота А.П., (1998). Определяли функциональные свойства тромбоцитов (адгезию, агрегацию с индукторами – АДФ, коллагеном, адреналином, ф. Виллебранда), агрескрин-тест (ГАТ), АПТВ-время, фибриноген, протромбиновое время автоматическим способом на агрегометре “Chrono-log 490” (США) и на коагулометре St Art 4, Stago (США).
Для определения функционального состояния мозга и степени выраженности нарушений проведены нейрофизиологические исследования стандартными методами на аппаратах фирмы Medelec, Англия: электроэнцефалография (ЭЭГ) на DG Compact 32, вызванные потенциалы Р300 – на аппарате Sapphire Premiere, исследование магнитной стимуляции пирамидного тракта (МС ПТ) – на аппарате Sapphire 2M.
Ультразвуковые методы включали дуплексное сканирование экстракраниальных сосудов, дуплексное сканирование транскраниальное и транскраниальную допплерографию с возможностью мониторирования и эмболодетекции. Дуплексное сканирование экстракраниальных сосудов выполнено на аппаратах VIVID–3 и VIVID–7 фирмы General Electric. Определяли форму извитости экстракраниального отдела ВСА: С-, S-, петлеобразную, волнообразную (НХ), а также наличие или отсутствие локального нарушения гемодинамики в зоне извитости. Локальным нарушением гемодинамики считали появление на участке изгиба сосуда дезорганизованного потока крови в виде турбуленции. Сканирование проводилось линейными датчиками с диапазоном частоты ультразвукового сигнала 7–12 МГц в режиме реального времени. В процессе исследования использовался В-режим, цветовое кодирование по скорости (ЦДК), импульсно-волновая допплерография и их сочетание (триплексный режим). В В-режиме получали визуальное черно-белое изображение стенок и просвета сосуда в зоне деформации. В режиме ЦДК судили о наличии турбулентности на обследуемом извитом участке сосуда. Ей соответствовали локальные изменения цветовой картограммы – смена цвета красного на синий и наоборот из-за изменения хода сосуда, нарушение монотонности цвета за счет вкраплений участков светлых (высокоскоростные) и темных (низкоскоростные потоки) оттенков. Триплексный режим позволял отмечать скоростной профиль потока на извитом участке. Турбулентному потоку соответствовала деформация огибающей допплеровского спектра, уменьшение или исчезновение спектрального окна, увеличение (по сравнению с проксимальным участком) линейной скорости кровотока в зоне максимальной деформации не менее, чем на 30 %. Корректная количественная оценка показателей кровотока внутри деформированного сегмента представляла известные трудности, поэтому основным критерием локального нарушения гемодинамики была качественная характеристика дезорганизованного потока.
Извитости экстракраниальных отделов внутренних сонных артерий с локальным нарушением гемодинамики в зоне изгибов были отнесены в разряд патологических извитостей внутренних сонных артерий (ПИ ВСА). Извитости внутренних сонных артерий без локального нарушения гемодинамики в зоне изгибов были отнесены в разряд деформаций внутренних сонных артерий - деформации ВСА (Куликов В.П., 1997).
Дуплексное сканирование транскраниальное средней мозговой артерии, cегмента М1, проводилось на аппаратах VIVID-3 и VIVID-7 фирмы General Electric микроконвексными датчиками с диапазоном частот 2–3 МГц в режиме реального времени. В процессе исследования использовался В-режим, цветовое кодирование по скорости (для идентификации средней мозговой артерии), импульсно-волновая допплерография для определения количественных показателей.
Транскраниальную допплерографию с возможностью мониторирования и эмболодетекцией проводили на ультразвуковом диагностическом комплексе Ангиодин-2К (НПФ БИОСС, Россия), оснащенном программным обеспечением ООО БИОСОФТ-М. Исследование средних мозговых артерий выполняли через переднее височное окно с помощью специального головного шлема с закрепленными на нем ультразвуковыми датчиками. После мониторирования в режиме “обсервер” на полученных спектрограммах проводили анализ зарегистрированных высокочастотных интенсивных сигналов (HITS) по продолжительности, мощности, частоте. Уточняли нахождение HITS в частотной области между огибающей и нейтральной линией (показатель SPR >1 при детализации). Для повышения достоверности отнесения HITS к эмболическим сигналам использовали их специфическую особенность обладать четко выраженным «ядром» – показатель SPT>2.3 на амплитудно-частотной характеристике при детализации. Рассчитывая, что МЭС у пациентов с ПИ ВСА должны образовываться из микроагрегантов форменных элементов под воздействием сил сдвига, возникающих в дезорганизованных турбулентных потоках на участках извитостей, мы предположили наличие таких свойств МЭС, как небольшой размер, низкая частота (близкая к частоте фонового кровотока) и материальный состав. Поэтому для исследования эмболии алгоритм автодетекции включал следующие параметры настройки (в соответствии с Рекомендациями Международного Симпозиума по церебральной гемодинамике, 1995): порог детекции – 5 дБ, порог режекции – 6.5 дБ, порог длительности – 4 мс, нижний порог частоты детекции – 125 Гц, верхний порог – 1600 Гц. Дополнительно, в целях эксперимента, для обработки МЭС низкой интенсивности, которые теоретически должны регистрироваться у пациентов с ПИ ВСА, включался режим трассировки всех сигналов высокой интенсивности, что позволяло значительно повысить информативность процесса исследования интракраниальной эмболизации.
При проведении транскраниальной допплерографии с эмболодетекцией оценивали количество МЭС, их частотные, мощностные, временные характеристики. Учитывались технические и методологические аспекты эмболодетекции, определенные Международной Согласительной Группой в 1998 году: височным доступом, датчиками частотой 2 МГц, диаметром 1,5 см, с одновременной локацией первых сегментов обеих СМА на глубине 45 - 56 мм в течение 40 - 60 минут. После обследования пациента проводился тщательный анализ характеристик зарегистрированных МЭС для определения их соответствия базовым критериям, принятым Согласительным комитетом 9-го Международного симпозиума по церебральной гемодинамике в 1995 году.
Полученные результаты были подвергнуты обработке с применением методов медицинской статистики при помощи пакета прикладных программ STATISTICA (Реброва О.Ю., 2006).
Для оценки эффективности диагностики ТКДГ с эмболодетекцией был использован статистический анализ чувствительности, специфичности и точности (Васильев А.Ю., Малый А. Ю., 2007).
Результаты исследования и их обсуждение. Всего у 70 (100%) пациентов основной группы дуплексным сканированием обследовано 140 (100%) экстракраниальных отделов внутренних сонных артерий (таблица 1).
Таблица 1
| Форма извитости ВСА | Правая ВСА | Левая ВСА | Всего | % |
| ПИ ВСА | 30 | 33 | 63 | 45.0 |
| Деформации ВСА | 32 | 27 | 59 | 42.1 |
| Типичный ход ВСА | 8 | 10 | 18 | 12.9 |
| Всего | 70 | 70 | 140 | 100 |
Выявлены 122 извитые ВСА (63 (45%) ПИ ВСА, 59 (42.1%) деформаций ВСА). 18 (12.9%) артерий имели типичный ход. У 52 (74%) пациентов выявлены двухсторонние извитости ВСА, у 18 (26%) – односторонние. Преобладали S- образные формы – 73 (52.1%), в 49(34%) из них регистрировалось локальное нарушение гемодинамики, что согласуется с литературными данными. С-образных было 20 (14.3%). Только в 6 (4.3%) из них регистрировалось локальное нарушение гемодинамики. Во всех 6 (4.3%) петлеобразных извитостях регистрировался дезорганизованный турбулентый поток. Ни в одной из 23(16.4%) ВСА с нарушением хода – НХ – локальное нарушение гемодинамики выявлено не было. Всего в основной группе из 70 (100%) пациентов у 18 (25.7%) выявлены двухсторонние ПИ ВСА (первая подгруппа), у 27 (38.6%) пациентов выявлены односторонние ПИ ВСА (вторая подгруппа), у 25 (35.7%) пациентов выявлены одно-, двухсторонние деформации ВСА (третья подгруппа).
Формы патологической извитости ВСА представлены на сканограмме 1.


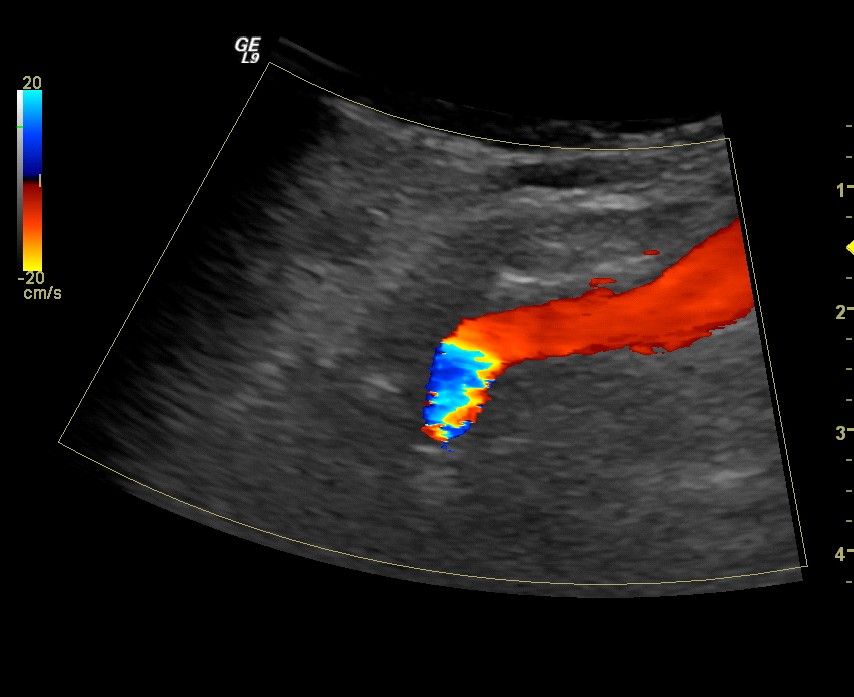
a b c
Сканограмма 1. a. S-образная патологическая извитость экстракраниального отдела правой ВСА; b. Петлеобразная патологическая извитость правой ВСА; с. С-образная патологическая извитость правой ВСА.
У пациентов первой (I) подгруппы регистрировались только S- и С-образные формы: у 15 (83.3%) имели место двухсторонние S-образные ПИ ВСА, у 2 (11.1%) пациентов – двухсторонние С-образные ПИ ВСА, 1 (5.6%) пациент с S-образной ПИ ВСА справа и С-образной ПИ ВСА слева. Во второй (II) подгруппе пациентов также преобладали S- образные извитости (27,50,0%). Локальное нарушение гемодинамики регистрировалось в 18 (33%) S-образных, в 3 (5%) С-образных, в 6 (11%) петлеобразных.
В третьей (III) подгруппе детей преобладали деформации неопределенной формы, НХ – 19 (38%), S-образных – 15 (30%), С-образных деформаций – 4 (8%).
Средние величины линейных скоростей кровотока (ЛСК) в СМА во всех трех подгруппах находились в пределах нормативных возрастных значений.
Таблица 2
Показатели средних величин ЛСК в ВСА и СМА во II подгруппе с односторонними ПИ ВСА
| Линейная скорость кровотока | ПИ ВСА правая | ПИ ВСА левая | p | СМА ипси-латеральной правой ПИ ВСА | СМА ипси-латеральной левой ПИ ВСА | p |
| (M±m) | 69.81 ±16.55 | 70.11 ±16.54 | 0.94 | 128.11 ±22.25 | 130.92 ±24.33 | 0.65 |
Во II подгруппе показатели кровотока в СМА на стороне ПИ ВСА у 13 пациентов II подгруппы были выше на 2-16%, у 14 пациентов – ниже только на 1-14% по сравнению с одноименной контрлатеральной артерией. Сравнительный анализ скоростей кровотока на экстракраниальных участках ВСА, предшествующий участкам извитостей, (с локальным и без локального нарушения гемодинамики) показал их статистическую незначимость (p=0,94). Нами не зарегистрировано статистически значимого (p=0.65) различия в скоростях мозгового кровотока в СМА, которое могло быть спровоцировано локальными нарушениями гемодинамики в виде турбуленции на участках извитостей гомолатеральных ВСА. Это совпадает с мнением ряда исследователей, считающих ПИ ВСА у детей локально гемодинамически значимыми неосложненными, то есть не вызывающими дистальный дефицит кровотока в ипсилатеральной СМА (Лелюк В.Г., Лелюк С.Э.,2007). Тем не менее, эти данные расходятся с мнением других авторов, считающих основным звеном патогенеза нарушений мозгового кровообращения при ПИ ВСА снижение скорости кровотока в СМА, вызванное локальными нарушениями гемодинамики в виде турбуленции в зоне извитости (Никитин Ю.М., 1997; Смирнова Ю.В., Суворова А.В., 2007).
Высокоинтенсивные микроэмболические сигналы методом ТКДГ с детекцией регистрировались в 35 (97.2%) из 36 (100%) CМА у пациентов I подгруппы; в 30 СМА (27 (100%) СМА на стороне ПИ ВСА и в 3 (14.3%) на стороне деформаций ВСА) у пациентов II подгруппы. Ни в одной из СМА у пациентов III подгруппы высокоинтенсивные сигналы не регистрировались.
Всего МЭС регистрировались в 62 (98%) из 63 (100%) ПИ ВСА, в 3 (5%) из 59 (100%) деформациях ВСА.
Количество МЭС в час у пациентов I подгруппы варьировалось от 1-2 до 21-40 и более, в том числе у одного пациента в обеих СМА регистрировались кластеры (сливные или групповые) МЭС (таблица 3). Клиническая симптоматика воздействия МЭС на мозговую гемодинамику проявляется при регистрации множественных МЭС (Bibikian V. Et al., 1994).
Таблица 3
Соотношение числа сосудов и зарегистрированных в них МЭС в I подгруппе двухсторонних ПИ ВСА (n=35)
| Кол-во сосудов | N=13 | n=8 | n=2 | n=5 | n=3 | n=4 | 2 |
| Число МЭС/час | 1-2 | 3-5 | 6-10 | 11-20 | 21-40 | Более 41 | Кластеры |
Количество МЭС в час у пациентов II подгруппы также варьировалось от 1-2 до 21-40 и более, в том числе у одного пациента в в одной СМА регистрировались кластеры МЭС (таблица 4).
Таблица 4
Соотношение числа сосудов и зарегистрированных в них МЭС во II подгруппе односторонних ПИ ВСА (n=30)
| Кол-во сосудов | n=11 | n=7 | n=3 | n=6 | n=2 | n=1 | 1 |
| Число МЭС/час | 1-2 | 3-5 | 6-10 | 11-20 | 21-40 | Более 41 | Кластеры |
Продолжительность всех зарегистрированных сигналов составила 4-31 мс. Согласно базовым критериям, принятым в 1995 году Международной согласительной группой, они были расценены как микроэмболические.
Интенсивность (мощность) микроэмболического сигнала – это комплексный физический показатель, характеризующий в совокупности его морфологический состав и размер. Интенсивность всех зарегистрированных сигналов по отношению к фоновому кровотоку составила от 7 до 40 дБ.
Частота микроэмболического сигнала косвенно характеризует его морфологический состав и позволяет разделять на материальные и газовые. Все зарегистрированные нами микроэмболические сигналы находились в частотном диапазоне от 125 до 776 Гц, то есть были материальными.
При построении графика переменной – частоты МЭС – с помощью критериев Шапиро–Уилка и Лиллиефорса для проверки на нормальное распределение величин выявлено явно выраженное распределение микроэмболических сигналов в обеих подгруппах на три частотных диапазона: 125- 200 Гц, 201-400 Гц, 401-800 Гц. (рисунок 1).
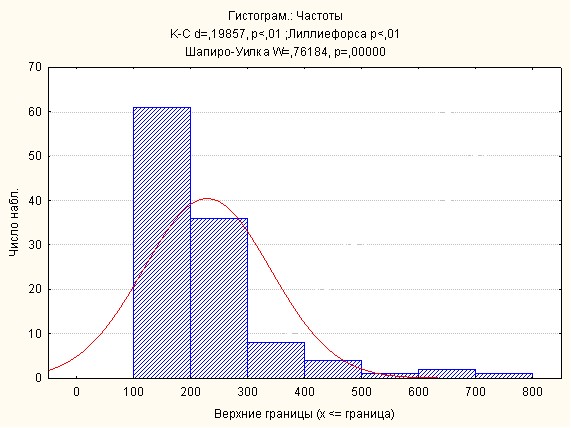
Рис. 1. График переменной “частоты МЭС”, построенный с помощью критериев Шапиро-Уилка для проверки на нормальное распределение величин
По физическому параметру МЭС “продолжительность” нами выявлены статистически значимые различия между I и III группами (p=0.015), между II и III группами (p=0,013). Между I и II группами статистически значимых различий не выявлено (p=0,9).
По физическому параметру “интенсивность” (мощность) выявлены статистически значимые различия между I и III группами (p=0,024), между II и III группами (p=0,04). Между I и II группами статистически значимых различий не выявлено (p=0,68). Следовательно, МЭС в частотном диапазоне 125-200 Гц и в частотном диапазоне 200-400 Гц были морфологически идентичны. По нашим расчетам, на участках патологических извитостей в турбулентных потоках образовывались микроагреганты из форменных элементов крови двух типов, красные и белые. Красные микроагреганты состоят преимущественно из эритроцитов, меньше тромбоцитов и фибрина. Они более крупные по размерам. Белые микроагреганты состоят преимущественно из тромбоцитов, меньше эритроцитов и фибрина. По размерам меньше красных. Красные микроагреганты, как более приближенные к фоновому кровотоку, находятся в более низком частотном диапазоне. Значит, морфологически идентичные МЭС I и II частотных диапазонов – красные микроагреганты. Белые микроагреганты представлены III частотным диапазоном зарегистрированных МЭС.
Таблица 5
Характеристика физических параметров МЭС в зависимости от частотных диапазонов
| Параметры МЭС (средняя величина-медиана) | Частотные диапазоны | ||
| 125-200 Гц (n=28) | 201-400 Гц (n=29) | 401-800 Гц (n=10) | |
| Количество | 7.3 | 6.7 | 13.5 |
| Продолжительность, мс | 16.87 | 17.03 | 10.2 |
| Интенсивность,дБ | 19.07 | 18.56 | 13.6 |
| Частота, Гц | 159.7 | 252.2 | 659.2 |
На рисунке 2 представлен микроэмболический сигнал I частотного диапазона.
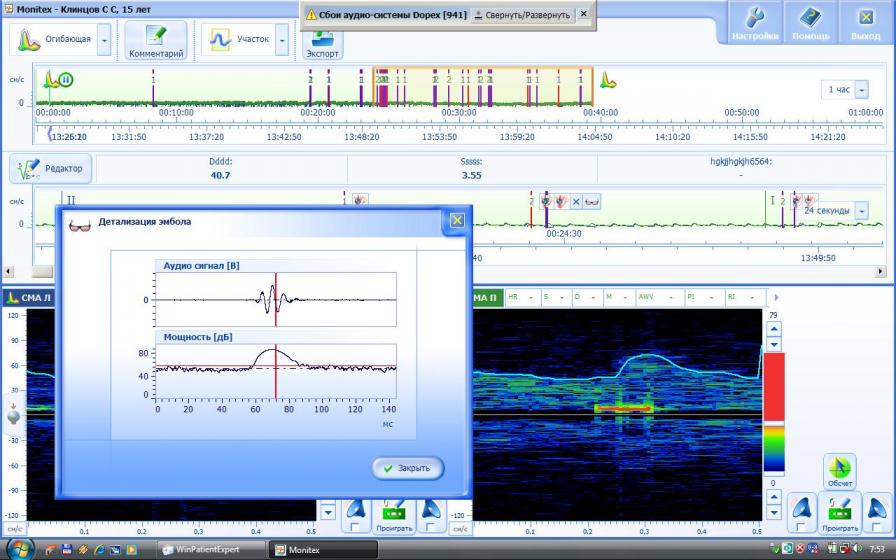
Рис. 2. Физические параметры МЭС: продолжительность 19 мс, интенсивность 33,4 дБ, частота 153 Гц
У пациентов I подгруппы в 80% (32 cосуда), у пациентов II подгруппы в 93.3%(28 cосудов) случаев регистрировались красные микроагреганты, которые имели следующие физические характеристики: частотный диапазон 125– 400 Гц, среднюю длительность 17 мс, cреднюю интенсивность 19 Дб.
В 20 % (8 сосудов) у пациентов I подгруппы, в 6,7% (2 сосуда) у пациентов II подгруппы регистрировались белые микроагреганты, которые имели следующие физические характеристики: частотный диапазон 401 - 800 Гц, среднюю длительность 10,2 мс, среднюю интенсивность 13,6 Дб.
В численном отношении (количество МЭС/час) белых микроагрегантов регистрировалось в два раза больше. Белые микроагреганты считаются более стойкими, труднее разбиваются, но клинически опаснее красные как более крупные (Kesler C.M., 1992).
Во II подгруппе в 3(14,3%) из 21 (100%) СМА на стороне деформаций ВСА регистрировались микроэмболические сигналы - красные микроагреганты. Регистрация в СМА МЭС на стороне деформации ВСА может объясняться следующим. По законам физики смена ламинарного течения жидкости на турбулентное происходит при превышении числа Рейнольдса - количественная мера турбулентности потока (Osborn Reynolds, 1883) - выше критического значения (Маслов А.А., Миронов С.Г., 2010). Во всех трех случаях исходная ЛСК на экстракраниальных участках деформаций ВСА была выше 100см/сек. Вероятно, скорость в ВСА не менее 100см/cек в сочетании с деформацией могла привести к появлению дезорганизованных потоков, не зарегистрированных при дуплексном сканировании.
Факт отсутствия регистрации МЭС в СМА при повторном ТКДГ мониторинге с детекцией после курса терапии тренталом, тормозящим агрегацию тромбоцитов и снижающим вязкость крови, у 8(44.4%) пациентов I подгруппы и 11 (40.7%) пациентов II подгруппы, дополнительно свидетельствовал о происхождении МЭС из агрегантов форменных элементов крови, образующихся вследствие их спонтанной агрегации в турбулентых дезорганизованных потоках на участках ПИ ВСА.
Структура и разнообразие сопутствующей соматической патологии, без существенных различий между группами, объяснялись проявлениями недифференцированной дисплазии соединительной ткани, одним из проявлений которой является ВСД (Гавалов С.М., 1999; Земцовский Э.В., 1998, Кадурина Т.И., 2000, Нечаева Г.И., 2008).
Синдром ВСД проявлялся цефалгиями. Преобладающее число пациентов I (17, 94,45%), II (25, 92.6%), III (22, 88%) подгрупп страдали цефалгиями достоверно чаще (p<0,05), чем пациенты контрольной группы (10, 45.5%). Клинически значимые головные боли встречались только в подгруппах основной группы, приблизительно c одинаковой частотой (p>0,05). Из клинически значимых головные боли с тошнотой и рвотой на пике болей, головные боли пульсирующего характера с подъемом артериального давления встречались только в I и II подгруппах.
Жалобы, характерные для астенического синдрома (нарастающая слабость, усталость, быстрая утомляемость при нагрузках, физических и умственных, чаще во второй половине дня или к концу уроков в школе) достоверно чаще встречались у пациентов всех подгрупп основной группы, чем в контрольной (p<0,05).
Жалобы, характерные для синдрома психовегетативных нарушений (эмоциональная лабильность, плаксивость, нарушение сна, раздражительность, гиперактивность), одинаково присутствовали в I и II подгруппах (p>0,05) и встречались достоверно чаще (p<0,05), чем в III подгруппе и в контрольной группе.
Ухудшение зрения отмечали только пациенты I и II подгрупп основной группы.
В анамнезе только у пациентов I и II подгрупп основной группы были зарегистрированы транзиторные ишемические атаки (ТИА), эпилептические припадки. Только в I и II подгруппах основной группы у пациентов по данным электроэнцефалографии (ЭЭГ) регистрировались очаги активности: эпиактивности, патологической активности, снижение порога судорожной или пароксизмальной готовности (в анамнезе у 8 из них имели место эпиприступы, у 3 – ТИА). Достоверно чаще (p<0,05) очаги активности регистрировались в I подгруппе основной группы.
Патологические изменения по данным вызванных потенциалов P300 (ВП P300) регистрировались с одинаковой частотой в I и II подгруппах и достоверно чаще (p< 0,05), чем в III подгруппе основной группы. Снижение объема оперативной памяти по данным ВП P300 регистрировались с одинаковой частотой в I и II подгруппах и достоверно чаще (p= 0,05), чем в III подгруппе.
Анализ клинических данных (выявленные у пациентов I и II подгрупп частота головных болей, астенический синдром, синдром психовегетативных нарушений), данные ЭЭГ и ВП P300 (статистически значимое различие в регистрации очагов активности и снижения объема оперативной памяти у пациентов с ПИ ВСА) могли быть следствием патогенного воздействия МЭС на мозговую микроциркуляцию за счет механической блокады и спазма артериол, приведших к ишемизации мозговой ткани.
По данным общего анализа крови в подгруппах основной группы и контрольной не выявлено статистически значимых различий всех показателей, за исключением параметра MPV- средний объем тромбоцитов. Он был достоверно выше в подгруппах основной группы (p<0,05). Известно, что средний объем тромбоцитов и их количество находятся в обратной зависимости (Баркаган З.С., Момот А.П., 1999). Таким образом, в подгруппах основной группы имело место скрытое относительное снижение числа тромбоцитов. При исследовании адгезивно-агрегационной функции тромбоцитов агрегация тромбоцитов с коллагеном была снижена у каждого третьего пациента с ПИ ВСА, у каждого 8 пациента с деформациями ВСА (статистически незначимо). Отклонения в агрегации с другими индукторами были еще менее значимы. Адгезия не была изменена ни в одном случае. Выявлены статистически значимые различия только в снижении фактора Виллебранда (p=0.01). Он ниже в I и II подгруппах основной группы. С активным участием фактора Виллебранда происходит активация, дегрануляция, адгезия тромбоцитов в высокоскоростных турбулентных потоках (Долгов В.В., Свирин П.В., 2005). Следовательно, снижение фактора Виллебранда и относительное снижение общего числа тромбоцитов в I и II подгруппах основной группы косвенно могли свидетельствовать об использовании их на образование микроагрегантов в турбулентных потоках на участках извитых внутренних сонных артерий.
Относительно сниженную агрегацию тромбоцитов с индуктором – коллагеном у трети пациентов с ПИ ВСА, статистически незначимую, мы рассматриваем как защитную реакцию организма на возможные клинические проявления воздействия МЭС на мозговые структуры. Вероятно также, что функциональная активность тромбоцитов при обычном исследовании венозной кубитальной крови не отражает реальных изменений их агрегационных свойств в экстракраниальных артериях.
Референтным методом для определения диагностической эффективности результатов ТКДГ- мониторирования с эмболодетекцией, проведенных всем пациентам основной группы (n=70), служило дуплексное сканирование (таблица 6).
Таблица 6
Диагностическая достоверность ТКДГ с детекцией микроэмболии
| Общее число сосудов, исследованное с помощью ТКДГ | Не выявлено МЭС при ТКДГ, число сосудов | Чувствительность метода ТКДГ, % | Специфичность метода ТКДГ,% | Точность метода ТКДГ,% |
| 63 ПИ ВСА, 59 деформаций ВСА | 1 56 | 98,4 | 94,9 | 96,7 |
Чувствительность метода ТКДГ в нашем исследовании составила 98,4%, специфичность – 94,9%, точность – 96,7%. Прогностичность положительного результата составила 98,4%, прогностичность отрицательного результата – 94,9 %.
Ультразвуковая допплерография с эмболодетекцией является высокоинформативным методом раннего выявления риска микроэмболизации средней мозговой артерии и возможного развития нарушений мозгового кровообращения у пациентов с ПИ ВСА.
Процесс микротромбообразования с последующей эмболизацией средних мозговых артерий только за счет самоактивации форменных элементов крови в дезорганизованных турбулентных потоках может идти в любом извитом сосуде, и последствия его могут приводить к морфологическим изменениям мозговой ткани.
Учитывая трудности корректного подбора допплеровского угла для измерения ЛСК на участке извитости сосуда при дуплексном сканировании, можно считать метод транскраниальной допплерографии с мониторированием и эмболдетекцией наиболее оптимальным как на этапе скрининга, так и на этапе заключительной диагностики.
На основании вышеизложенного мы предлагаем cчитать извитую внутреннюю сонную артерию патологической (ПИ ВСА) при выявлении по данным дуплексного сканирования локального нарушения гемодинамики в виде турбуленции и при регистрации по данным транскраниальной допплерографии микроэмболических сигналов в ипсилатеральной средней мозговой артерии.
ВЫВОДЫ
1. Показатели линейных скоростей кровотока в бассейнах средних мозговых артерий у детей c извитостями внутренних сонных артерий находились в пределах нормативных возрастных значений. При односторонней патологической извитости внутренних сонных артерий статистически значимой (p=0.65) асимметрии линейной скорости кровотока в средних мозговых артериях не зарегистрировано.
2. Патологическая извитость, признаком которой считали локальные нарушения гемодинамики в виде турбуленции, регистрировалась в 51% извитых сосудов. Она проявлялась в S-, C- и петлеобразных вариантах. Из выявленных преобладали S- образные формы (40,2%). В петлеобразных извитостях всегда регистрировалось локальное нарушение гемодинамики.
3. По данным транскраниальной допплерографии с мониторированием и эмболодетекцией микроэмболические сигналы в средних мозговых артериях регистрировались на стороне извитых внутренних сонных артерий в 97,2% у детей с патологическими извитостями внутренних сонных артерий, в 14,3% у детей с деформациями внутренних сонных артерий.
4. Выявлены два типа микроэмболических сигналов - красные и белые. Красные микроэмболические сигналы регистрировались в 80 % случаев: частотой 125–400 Гц, средней длительностью 17 мс, cредней интенсивностью 19 Дб. Белые микроэмболические сигналы регистрировались в 20 % случаев: частотой 400–800 Гц, средней длительностью 10.2 мс, средней интенсивностью 13.6 Дб.
5.Транскраниальная допплерография с мониторированием и эмболодетекцией является высокоинформативным методом раннего выявления риска микроэмболизации средних мозговых артерий и возможного развития нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий. Чувствительность метода составила 98.4%, специфичность – 94.9%, точность – 96.7%, прогностичность положительного результата – 98.4%, прогностичность отрицательного результата – 94.9 %.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Всем пациентам детского возраста с диагнозом вегето-сосудистой дистонии необходимо включать скрининговое дуплексное сканирование экстракраниальных артерий для выявления извитостей внутренних сонных артерий c локальным нарушением гемодинамики в виде турбуленции – патологических извитостей.
- Детям с установленным диагнозом патологической извитости внутренних сонных артерий необходимо назначение скрининговой транскраниальной допплерографии с возможностью мониторирования и эмболодетекцией.
- При регистрации микроэмболических сигналов в средних мозговых артериях на стороне патологической извитости внутренних сонных артерий необходимо включать пациента в группу риска по нарушениям мозгового кровообращения для проведения своевременной профилактики этих нарушений и подбора оптимального патогенетического лечения.
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
1.Федюнина, Н.Г. Динамический амбулаторный мониторинг микроэмболии сосудов мозга у больных с хронической цереброваскулярной недостаточностью / Н.Г. Федюнина, О.И. Исакова, В.П. Куликов, О.В. Лямина // Современное состояние методов неинвазивной диагностики в медицине «Ангиодоп –2007»: сборник научных трудов. – СПб, 2007. – C. 34–36.
2. Федюнина, Н.Г. Ультразвуковая детекция микроэмболии мозга у больных с хронической цереброваскулярной недостаточностью / Н.Г. Федюнина, О.И. Исакова, В.П. Куликов // Ультразвуковая и функциональная диагностика, 2007. – № 4. – С. 250.
3.Федюнина, Н.Г. Транскраниальная допплерография с детекцией эмболов как метод профилактики эмболического инсульта/ Н.Г. Федюнина, О.И. Исакова, В.П. Куликов, Н.Г. Хорев // Материалы региональной научно-практической конференции. – Белокуриха, 2007. – C. 345–347.
4. Федюнина, Н.Г. Мониторинг церебральной эмболии в амбулаторных условиях / Н.Г. Федюнина, Н.Г. Хорев, В.П. Куликов, Н.Г. Хорев, О.И. Исакова, О.А. Пелеганчук // Медицинская диагностика. Управление. Качество. – ДиаМА, 2007. – C. 59–61.
5.Федюнина, Н.Г. Ультразвуковая диагностика микроэмболии при хронических нарушениях мозговой гемодинамики / Н.Г. Федюнина, О.В. Лямина, Т.Н. Ядрышникова, О.И. Исакова, Н.Г. Хорев // Актуальные проблемы клинической неврологии. Материалы Всероссийской юбилейной научно-практической конференции. – СПб, 2009. – C. 161–162.
6. Исакова,О.И. К вопросу о патогенезе нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий / О.И. Исакова, Н.Г. Федюнина, Т.Э. Шульц, Е.А. Козлова, М.Е. Свищева // Сборник научно-практических трудов, посвященный 20-летию Ставропольского краевого консультативно-диагностического центра.- Ставрополь, 2009. – C. 82–83.
7. Федюнина,Н.Г. Применение амбулаторного мониторинга для диагностики церебральной микроэмболии / Н.Г. Федюнина, О.И. Исакова, Т.Н. Ядрышникова, // Российский клинико-фармацевтический вестник. – 2009. – № 1. – C. 13.
8. Исакова, О.И. Инструментальные средства транскраниальной допплерографии в исследовании патогенеза нарушений мозгового кровообращения у детей с патологической извитостью внутренней сонной артерии / О.И. Исакова, И.А. Филатов // Материалы IV Всероссийского национального конгресса лучевых диагностов и лучевых терапевтов “Радиология-2010”. – М., 2010. – C. 178–179.
9. Исакова, О.И. Использование метода транскраниальной допплерографии в исследовании патогенеза нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий / О.И. Исакова // Нарушения мозгового кровообращения: диагностика, профилактика, лечение. Материалы российской научно-практической конференции. - Пятигорск, 2010. – C. 89–90.
- Исакова О.И. Инструментальные средства транскраниальной допплерографии в исследовании патогенеза нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий / О.И. Исакова, В.А. Елыкомов, И.А. Филатов, Н.Г. Федюнина, Е.А. Козлова, Т.Э. Шульц, Г.П. Иткин // Вестник трансплантологии и искусственных органов. – 2008. – № 6 (44). – C. 53–60.
11. Адаскин, А.В. Мультимодальные средства функциональной диагностики летного состава гражданской авиации /А.В. Адаскин, О.И. Исакова, В.В. Cергейчик, И.А. Филатов, Д.А.Загребин // Вестник Московского авиационного института. – 2011. – Т.18. – № 3. – C. 152–160.
12. Исакова, О.И. Тромбоэмболический механизм нарушений мозгового кровообращения у детей с патологической извитостью внутренних сонных артерий / О.И. Исакова // Врач – аспирант. –2011. – № 6 (49). – C. 51– 59.
Патент на изобретение
1. Исакова, О.И. Способ определения риска микроэмболизации средней мозговой артерии у детей с патологической извитостью внутренних сонных артерий / О. И. Исакова, И. А. Филатов, И. В. Елыкомов, Г. О. Сапего // № 2421141, приоритет 02.11.2009, зарегистрирован в Госреестре 20.06.2011.

