Хламидийная и микоплазменная инфекция лор-органов (
На правах рукописи
Руденко Виктория Владимировна
Хламидийная и микоплазменная инфекция ЛОР-органов
(14.01.03 – Болезни уха, горла и носа)
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2013 г.
Работа выполнена на кафедре оториноларингологии лечебного факультета ГБОУ ВПО «Российский национальный исследовательский медицинский университет им.Н.И.Пирогова» Минздрава РФ
Научные руководители
Пальчун Владимир Тимофеевич - член-корр. РАМН, заслуженный деятеля науки РФ, доктор медицинских наук, профессор, почетный заведующий кафедрой оториноларингологии лечебного факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава РФ.
Гуров Александр Владимирович - доктор медицинских наук, профессор кафедры микробиологии и вирусологии лечебного факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава РФ, старший научный сотрудник отдела клинической фармакологии ГБУЗ «Московский научно-практический Центр оториноларингологии им. Л.И. Свержевского» Департамента здравоохранения города Москвы.
Официальные оппоненты
Туровский Андрей Борисович - доктор медицинских наук, заместитель директора по медицинской части ГБУЗ «Московский научно-практический Центр оториноларингологии им. Л.И. Свержевского» Департамента здравоохранения города Москвы.
Никифорова Галина Николаевна - доктор медицинских наук, профессор кафедры оториноларингологии ГБУЗ МО МОНИКИ им. М.В. Владимирского.
Ведущая организация:
ГБОУ ВПО «Московский государственный медико-стоматологический университет имени А.И. Евдокимова» Минздрава РФ
Защита диссертации состоится 19 сентября 2013г. в 13 ч на заседании диссертационного совета Д 850.003.01 в ГБУЗ «Московский научно-практический Центр оториноларингологии им. Л.И. Свержевского» Департамента здравоохранения города Москвы, по адресу: 117152, Москва, Загородное шоссе, д. 18а, стр. 2.
С диссертацией можно ознакомиться в библиотеке ГБУЗ «Московский научно-практический Центр оториноларингологии им. Л.И. Свержевского» Департамента здравоохранения города Москвы.
Автореферат разослан « » августа 2013 года.
Ученый секретарь диссертационного совета
кандидат медицинских наук Ю.В. Лучшева
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Воспалительная патология уха, горла и носа является в настоящее время одной из актуальных проблем современного здравоохранения (Пальчун В.Т., Крюков А.И. 2013). При этом воспалительный процесс может быть вызван не только традиционными бактериальными патогенами, но и микроорганизмами с атипичными свойствами, в частности, хламидиями или микоплазмами.
Актуальность проблемы хламидийной и микоплазменной инфекции в оториноларингологии обусловлена не столько значительным распространением этих микроорганизмов в популяции, сколько их дискутабельной ролью в развитии воспалительного процесса в структуре респираторного тракта. Различные виды микоплазм и хламидий могут являться причиной ряда заболеваний урогенитального тракта, этиологическим фактором преждевременных родов, невынашивания беременности, нарушения репродуктивной функции, случаев мертворождения (Лупан И.Н. 1997; Курдина М.И., Колмогорова И.В. 2004). С другой стороны, отмечается возможность бессимптомного носительства микоплазм и хламидий у клинически здоровых лиц (Курдина М.И., Колмогорова И.В. 2004).
К настоящему времени получены достаточно убедительные данные, свидетельствующие о том, что сочетание внутриклеточной инфекции с традиционной бактериальной микрофлорой зачастую создает максимально благоприятные условия для возникновения и хронизации таких заболеваний, как синусит, фарингит, средний отит (Principi N., Esposito S. 2002). В последние годы с появлением новых, современных методов диагностики инфекционных заболеваний появилась возможность дифференциальной диагностики типичных и атипичных состояний, вызывающих гнойно-воспалительную патологию ЛОР - органов, включая атипичных патогенов и, в первую очередь, хламидий и микоплазм.
Целью исследования явилось определение в современных условиях частоты встречаемости и особенностей клинической картины воспалительных заболеваний ЛОР-органов, обусловленной хламидийной и микоплазменной инфекцией с разработкой лечебно-диагностического алгоритма этой патологии.
Задачи исследования:
- Выявить частоту встречаемости хламидийной и микоплазменной инфекции ЛОР-органов в современных условиях.
- Выявить основные клинические особенности течения хламидийной и микоплазменной инфекции ЛОР-органов.
- Изучить спектр типичной бактериальной микрофлоры при воспалительных заболеваниях ЛОР-органов у больных с клиническими проявлениями характерными для хламидийной и микоплазменной инфекции.
- Выявить наиболее чувствительные и специфичные методы диагностики хламидийной и микоплазменной инфекции у пациентов с патологией ЛОР-органов и разработать шкалу вероятности инфицирования ЛОР-органов атипичными микроорганизмами.
- Разработать алгоритм адекватной терапии воспалительных заболеваний ЛОР-органов, обусловленных хламидийной и микоплазменной инфекцией.
Научная новизна
- Впервые, благодаря использованию высокоспецифичных и чувствительных методов исследования, установлена достоверная частота встречаемости поражений верхних дыхательных путей и уха, хламидийной и микоплазменной этиологии.
- Впервые установлены достоверные диагностические критерии хламидийного и микоплазменного поражения ЛОР-органов.
- Впервые установлено, что ПЦР в real-time режиме является более специфичным и чувствительным методом диагностики хламидийной и микоплазменной инфекции ЛОР-органов.
- Впервые предложена шкала вероятности активного инфицирования ЛОР-органов хламидиями и микоплазмами, что позволяет оптимизировать тактику диагностики и своевременно назначить лечение, а, следовательно, снизить риск распространения инфекции.
Практическая значимость работы:
Установлены клинические симптомы, позволяющие заподозрить наличие атипичной инфекции ЛОР-органов, предложен оптимальный алгоритм для диагностики данной инфекции в современных условиях.
Разработан алгоритм эффективной антибактериальной терапии воспалительных заболеваний ЛОР-органов, хламидийной и микоплазменной этиологии в современных условиях. Разработанный лечебно-диагностический алгоритм хламидийной и микоплазменной инфекции ЛОР-органов может быть использован в работе практических оториноларингологов в поликлиниках и стационарах.
Внедрение полученных результатов исследования в практику:
Результаты, полученные в диссертационной работе, внедрены в работу ЛОР - отделений ГКБ №1 им. Н.И. Пирогова и оториноларингологического отделения ГБУЗ «Московский научно-практический центр оториноларингологии» ДЗМ. Результаты исследований включены в учебную программу студентов, врачей-интернов, ординаторов кафедры оториноларингологии лечебного факультета ГБОУ ВПО «Российский национальный исследовательский медицинский университет им. Н.И.Пирогова» Минздрава РФ.
Основные положения, выносимые на защиту:
- Хламидийная инфекция ЛОР-органов является относительно редко встречающейся патологией, в сравнении с поражениями микоплазменной этиологии.
- Воспалительные заболевания ЛОР-органов хламидийной и микоплазменной этиологии имеют признаки малосимптомного воспаления, носят затяжной, рецидивирующий характер.
- Для атипичной инфекции, вызванной хламидиями и микоплазмами, характерно двустороннее поражение ЛОР-органов, в сочетании с поражением нижних дыхательных путей и конъюнктивитом.
- Метод диагностики хламидийной и микоплазменной инфекции – ПЦР в real-time режиме является наиболее специфичным и чувствительным методом и по своей чувствительности и специфичности, превосходит ПЦР с использованием гель-электрофореза.
Апробация работы:
Материалы диссертации доложены на X, XI Всероссийской научно-практической конференции «Наука и практика в оториноларингологии» (Москва, 2011, 2012 г.).
Апробация диссертации проведена на совместной научно-практической конференции сотрудников кафедры оториноларингологии лечебного факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова Минздрава РФ, научно-исследовательской лаборатории «Патологии ЛОР - органов», ГБУЗ МНПЦО ДЗМ, ЛОР - отделений и консультативно-диагностического центра ГКБ №1 им Н.И. Пирогова г. Москвы 25 июня 2013 года, протокол апробации №25/2013
Публикации:
По теме диссертации опубликовано 8 печатных работ, из них 3 – в центральной печати.
Объем и структура диссертации
Диссертация изложена на 119 страницах печатного текста, состоит из введения, литературного обзора, 4 глав собственных исследований, заключения, выводов, практических рекомендаций и списка литературы, включающего 114 отечественных и 52 зарубежных авторов. Работа иллюстрирована 26 таблицами и 16 рисунками.
Содержание работы
Общая характеристика больных и методов исследования
Нами было обследовано 420 пациентов, находившихся на стационарном лечении в ЛОР-отделениях ГКБ №1 им. Н.И. Пирогова в период с 2011 по 2013гг. с воспалительными заболеваниями ЛОР-органов, среди них 174 мужчины и 246 женщин в возрасте от 15 до 80 лет, средний возраст которых составил 39±1,4 лет.
Методы исследования.
Клинико-лабораторное исследование. Всем пациентам производили стандартное клиническое обследование: выясняли жалобы, собирали анамнез заболевания и жизни. Лабораторное исследование включало: клинический анализ крови, общий анализ мочи, биохимический анализ крови, определение группы крови и резус-фактора, исследование крови на НВs - антиген, антитела к HCV, RW, ВИЧ. Также, всем пациентам производили ЭКГ и рентгенографию органов грудной клетки, а при наличии показаний - рентгенографию или КТ ОНП, височных костей.
Осмотр ЛОР – органов включал: пальпацию регионарных лимфоузлов, осмотр и пальпацию области проекции ОНП, пальпацию мест выхода тройничного нерва, переднюю риноскопию, оро- и мезофарингоскопию, заднюю риноскопию, непрямую ларингоскопию, отоскопию и пальпацию заушной области, козелка, акуметрию, аудиологическое исследование (тональную пороговую аудиометрию, тимпанометрию). По показаниям проводили эндоскопическое исследование полости носа, носоглотки, используя жесткие эндоскопы фирмы «KARLSTORZ» (Германия) с углом зрения 0, 70 градусов.
Микробиологическое исследование - ПЦР диагностика в real-time режиме. В качестве материала для исследования использовали патологическое отделяемое из очагов воспалительного поражения ЛОР-органов. Во всех случаях исследуемый материал помещали в пробирку типа Эппендорф с физиологическим раствором. Пробирки с биологическим материалом, доставляли в молекулярно-биологическую лабораторию, на базе кафедры микробиологии и вирусологии РНИМУ им. Н.И. Пирогова.
Тотальную ДНК из клинического материала для проведения ПЦР в режиме реального времени выделяли с помощью набора реагентов «К-сорб» (Синтол, Москва) в соответствии с инструкцией производителя.
ПЦР в режиме реального времени (ПЦР-РВ) для определения количества копий генов 16S рРНК и ПЦР-скрининга в ходе клонирования проводили в приборе CFX96 (Bio-Rad, США). В реакционную смесь добавляли пару праймеров gpo-1, mgso-1 для амплификации ДНК бактерий рода Mycoplasma или chlam-1, chlam-2 для амплификации ДНК бактерий родов Chlamydia, Chlamydophila до финальной концентрации 0,2 мкМ каждого праймера и 2-10 мкл препарата ДНК.
Для определения абсолютного количества копий генов 16S рРНК микоплазм и хламидий в образцах клинического материала использовали метод калибраторных кривых. Для этого параллельно с исследуемыми образцами проводили ПЦР-РВ с серийными десятикратными разведениями калибраторных плазмид в известных концентрациях, содержащих клонированные фрагменты соответствующих генов.
Для определения видовой принадлежности амплифицированных фрагментов генов 16S р-РНК проводили их клонирование и секвенирование. Клонирование ПЦР-продуктов в вектор pAL-TA проводили с использованием стандартных методик.
Поиск нуклеотидных последовательностей генов 16S рРНК, полученных при секвенировании, проводили в базе данных GenBank с помощью алгоритмов NCBI BlastN, Megablast с использованием параметров по умолчанию. Идентификацию вида считали успешной при совпадении изучаемой последовательности с последовательностью известного вида из базы данных GenBank на не менее чем 98%.
Статистический анализ проводили при помощи пакета LibreOffice Calc.
Микробиологическое исследование - ПЦР диагностика методом гель-электрофореза. В качестве материала для исследования использовали патологическое отделяемое из очагов воспалительного поражения ЛОР – органов. Во всех случаях исследуемый материал помещали в пробирку типа Эппендорф с физиологическим раствором.
Пробирки с биологическим материалом доставляли в молекулярно-биологическую лабораторию, на базе кафедры микробиологии и вирусологии РНИМУ им. Н.И. Пирогова. При разработке диагностической ПЦР-тест-системы находили небольшой фрагмент ДНК (мишень), строго специфичный для конкретного возбудителя. С помощью ПЦР амплифицировали именно этот участок и затем идентифицировали продукт амплификации (ампликон) методом электрофореза в агарозном геле. Каждый цикл диагностики проходил в три стадии: 1. Денатурация - расплетение цепей двунитевой ДНК - не ферментативный процесс, который протекает при температуре 950С. 2. Присоединение (отжиг) праймеров. При этом праймеры присоединяются только к выбранным специфичным для данного возбудителя фрагментам ДНК и не взаимодействуют ни с какими другими последовательностями ДНК. В результате присоединения праймеров образуются структуры [ДНК-матрица + праймер], являющиеся «затравочными» комплексами. 3. Элонгация. Под действие температуры 70-750С, происходит достраивание праймеров, путём комплементарного синтеза на матрицах одноцепочечных фрагментов ДНК. Этот процесс осуществляли с помощью специального фермента - Taq-полимеразы (термоустойчивой ДНК-полимеразы) и свободных нуклеотидов (в качестве строительного материала).
ПЦР проводили в амплификаторе – приборе, в котором циклично автоматически поддерживался заданный режим температур, позволяющий многократно последовательно проходить основные этапы ПЦР. Учёт реакции проводили с помощью электрофореза в агарозном геле. Если в исследуемой пробе в результате ПЦР накапливались ампликоны (фрагменты ДНК одинакового размера), то они оказывались на одном расстоянии от старта и видны как полоса на гелевой дорожке. Если положение полосы на гелевой дорожке соответствовало расчётной для использованной пары праймеров, т.е. находились на том же расстоянии от старта, что и полоса положительного контроля, такой результат расценивали как положительный.
Микробиологическое исследование - бактериологический метод. Бактериологическое исследование проводили на базе бактериологических лабораторий кафедры микробиологии и вирусологии РНИМУ им. Н.И. Пирогова. Материалом для исследования служили посевы из пораженных ЛОР-органов.
При заборе материала соблюдались все правила асептики. Сразу после забора патологического материала, ватный тампон погружали в транспортную среду, в качестве которой использовали стерильный сердечно-мозговой бульон (BHI, BBL, USA). В течение 40 минут, собранный материал доставляли в лабораторию, где производили предварительную инкубацию в термостате при температуре 37,0 С в течение 3 часов, затем производили посев на плотные питательные среды: BHI-агар (BBL, USA) с 5% крови, среду Endo (BBL, USA), Staphylococcus agar (BBL, USA), Columbia agar base (OXOID, England) с 5% крови, налидиксовой кислотой (15 мг/л), колистином (10 мг/л), Cetrimid agar (BBL, USA), Enterococcus agar (bioMerieux, France), Sabouraud Dextrose agar (bioMerieux, France) с добавлением хлорамфеникола. На этих средах производилась инкубация в термостате при 37С в течение 1-2 суток. В течение 3 суток инкубировали чашки со средой Sabouraud Dextroseagar. Полученные колонии микроорганизмов подвергали макро- и микроскопическому изучению, производили подсчет количества колоний каждого типа. Далее выделяли собственно чистую культуру микроорганизмов. Посев на скошенный агар использовали для бактерий аэробного спектра, а при наличии облигатно-анаэробных микроорганизмов, использовали плотные питательные среды на чашке с тестом на анаэробиоз. Для идентификации грамотрицательных палочек применяли следующие системы: API-20 E (bioMerieux, France), системы ENTERO-test (LACHEMA, Чехия), сред Гисса (НПО «Питательные среды», Махачкала, Россия). Для идентификации грамположительных кокков использовали системы API-20 STAPH (bioMerieux, France). Для определения стрептококков применяли систему API-20 STREPT (bioMerieux, France).
Для идентификации дрожжевых и филаметозных грибов использовали системы API-Cand (bioMerieux, France). А также оценивали их характер роста на средах Sabouraud Dextrose agar с хлорамфениколом, BHI-агар с кровью, учитывали морфологические свойства в нативном препарате.
При интерпретации полученных результатов, учитывали как качественный, так и количественный состав естественной микрофлоры, содержавшийся в опытном образце. Высеянные микроорганизмы, не имеющие отношения к естественной микрофлоре ЛОР-органов, или обнаруженные в большом количестве бактерии определенного вида, расценивали как этиологически значимые.
Серологическое исследование – иммуноферментный анализ (ИФА). Все серологические исследования проводили в клинической лаборатории «Медсервис диагностика», на базе ГКБ №1. У исследуемых пациентов, утром, натощак из локтевой вены производили забор крови в объеме 5,0-5,5 мл в вакуумную центрифужную пробирку с С клот-активаром. Далее пробирку помещали в холодильную камеру, где она хранилась при температуре от +3C до +5 C не более 3-х часов. В последующем, соблюдая холодовой режим, пробирку доставляли в лабораторию «Медсервис диагностика», где ее выдерживали в термостате при температуре +37C в течение 40-45 мин., после чего центрифугировали 20 мин при 3000 об/мин. Часть образцов сыворотки при помощи набора реагентов «ХламиБест», фирмы ЗАО «Вектор-Бест» использовали для выявления видоспецифических иммуноглобулинов класса А, М, G к антигенам различных хламидий. Оставшиеся образци исследовали при помощи тест-системы «микоплазмоз- Ig A, M, G - антитела», фирмы ООО «ИмДи-спектр» для выявления иммуноглобулинов класса А, М, G к антигенам микоплазм.
Статистический анализ проводили с использованием базы данных Microsoft Access, а также при помощи разработанной на кафедре медицинской кибернетики и информатики РНИМУ им. Н.И. Пирогова программы для персонального компьютера, позволяющей проводить точное сравнение организованных пользователем групп данных и выявлять достоверные критерии с использованием статистических непараметрических критериев, не зависящих от характера распределения - точного критерия Фишера и критерия хи-квадрат.
Результаты собственных исследований и их обсуждение.
После проведенного микробиологического исследования (ПЦР диагностики в real-time режиме), подтвержденного методом ИФА, все пациенты были разделены на 2 группы. Основную группу составили 108 пациентов с выявленной, по результатам проведенных исследований, атипичной инфекцией (хламидийной и микоплазменной). Оставшиеся пациенты, с отрицательными результатами ПЦР и ИФА (312 человек), составили контрольную группу.
Все пациенты основной группы (108 человек), в зависимости от локализации патологического процесса, были разделены на 3 подгруппы: I -30 пациентов с заболеваниями носа и околоносовых пазух (ОНП); II – 57 пациентов с заболеваниями глотки и гортани; III – 21 пациент с заболеваниями среднего уха (см. табл. №1).
По результатам изучения анамнеза заболевания необходимо отметить, что у 30 (27,8%) пациентов основной группы заболевание возникло впервые. 21 пациент (19,4%) отмечали обострения заболевания несколько раз в течение одного года, а 9 (8,3%) - на протяжении двух лет, при этом рецидивирующий характер течения болезни в течение двух лет (5 и более эпизодов) наблюдался у 48 пациентов (44,4%).
Для больных основной группы было характерно двустороннее и одностороннее поражение ЛОР-органов (в 77,8% и в 22,2%, соответственно).
Табл. №1 Распределение больных основной группы в зависимости от локализации воспалительной патологии ЛОР – органов (n=108)
| Заболевание | Количество больных | % | |
| I подгруппа Заболевания носа и ОНП | Острый и хронический катаральный гаймороэтмоидит | 21 | 19,4 |
| Хронический гнойный гаймороэтмоидит | 3 | 2,8 | |
| Хронический продуктивный гаймороэтмоидит (пристеночно-гиперпластический, полипозный и кистозный) | 6 | 5,6 | |
| Всего | 30 | 27,8 | |
| II подгруппа Заболевания глотки и гортани | Хронический тонзиллит ТАФI и ТАФ II | 30 | 27,8 |
| Паратонзиллярный абсцесс | 9 | 8,3 | |
| Хронический трахеоканюленоситель | 12 | 11,1 | |
| Острый и хронический катаральный ларингит | 6 | 5,6 | |
| Всего | 57 | 52,8 | |
| III подгруппа Заболевания уха | Хронический гнойный средний отит, мезотимпанит | 10 | 9,2 |
| Хронический гнойный средний отит, эпитимпанит, холестеатомная форма | 11 | 10,2 | |
| Всего | 21 | 19,4 | |
| ИТОГО | 108 | 100 |
В контрольную группу вошли 312 пациентов с воспалительной патологией ЛОР-органов, у которых по результатам наших исследований (ПЦР в real-time режиме) хламидийная и микоплазменная инфекция не была обнаружена. В зависимости от характера поражения, все больные указанной группы были также разделены на 3 подгруппы: I - 180 пациентов с заболеваниями носа и ОНП; II – 36 пациентов с заболеваниями глотки и гортани; III - 96 пациентов с заболеваниями среднего уха (см. табл. №2).
По результатам изучения данных анамнеза заболевания было установлено, что данные состояния возникли впервые у 138 (44,2%) больных. 75 пациентов (24%) отмечали от 2 до 3 эпизодов обострения в течение года. У 15 пациентов (4,8%) заболевание характеризовалось рецидивирующим течением на протяжении двух лет, а у 84 пациентов (26,9%) - более двух лет.
Двусторонний характер поражения ЛОР-органов встречался также часто, как и односторонний (в 57,9% и 42,1% случаев, соответственно).
Табл. №2 Распределение больных контрольной группы в зависимости от локализации воспалительной патологии ЛОР – органов (n=312)
| Заболевание | Количество больных | % | |
| I подгруппа Заболевания носа и ОНП | Острый и хронический катаральный гаймороэтмоидит | 78 | 25 |
| Острый и хронический гнойный гаймороэтмоидит | 54 | 17,3 | |
| Хронический продуктивный гаймороэтмоидит (пристеночно-гиперпластический, полипозный и кистозный) | 42 | 13,5 | |
| Острый и хронический фронтит | 6 | 1,9 | |
| Всего | 180 | 57,7 | |
| II подгруппа Заболевания глотки и гортани | Хронический тонзиллит ТАФI и ТАФII | 6 | 1,9 |
| Паратонзиллярный абсцесс | 9 | 2,9 | |
| Хронические трахеоканюленосители | 2 | 0,7 | |
| Отечно-инфильтративный ларингит | 7 | 2,2 | |
| Острый и хронический катаральный ларингит | 12 | 3,8 | |
| Всего | 36 | 11,5 | |
| III подгруппа Заболевания уха | Острый катаральный средний отит | 21 | 6,7 |
| Экссудативный средний отит | 12 | 3,9 | |
| Хронический гнойный средний отит, мезотимпанит | 45 | 14,4 | |
| Хронический гнойный средний отит, эпитимпанит, холестеатомная форма | 18 | 5,8 | |
| Всего | 96 | 30,8 | |
| ИТОГО | 312 | 100 |
Результаты клинического обследования.
Сравнительный анализ клинического течения воспалительных заболеваний ЛОР-органов у больных основной и контрольной группы показал следующее. У больных основной группы достоверно реже, чем у пациентов контрольной группы (в 4,6 раза) встречались впервые возникшие заболевания (р=0,004). Двусторонний характер поражения ЛОР-органов достоверно чаще (в 1,9 раза) встречается у пациентов основной группы, чем контрольной (р=0,006). По результатам математического анализа частоты встречаемости сопутствующей патологии отмечено, что в основной группе достоверно чаще встречались пневмония (в 2,9 раза, р=0,003), коньюктивит (в 4,6 раза, р=0,000001), пародонтит (в 4,2 раза, р=0,0003).
По результатам сравнительного математического анализа у пациентов I-ых подгрупп (с заболеванием носа и ОНП) обеих групп слизистый характер отделяемого при выполнении диагностической пункции ОНП, был получен практически в одинаковом проценте случаев (60% и 43% соответственно, р=0,5). Гнойное отделяемое встречалось только у пациентов контрольной группы в 30% случаев (р=0,004). Слизисто-гнойное отделяемое у пациентов основной группы встречалось в 2 раза реже, чем у пациентов контрольной группы (11,1% и 23,3%, соответственно, р=0,04) (см. табл.№3).
Таблица №3 Характер патологического процесса у пациентов с острым и хроническим гаймороэтмоидитом в контрольной и основной группе (n=210)
| Заболевание | Основная группа (n=30) | Контрольная группа (n=180) | Коэффициент Р |
| катаральный характер процесса | 18 (60%) | 78 (43%) | 0,5 |
| гнойный характер процесса | 0 | 54 (30%) | 0,004 |
| слизисто-гнойный характер процесса | 3(11,1%) | 42 (23,3%) | 0,04 |
У 6 (5,6%) пациентов основной группы и 42 (13,5%) контрольной группы по данным КТ имел место выраженный характер течения продуктивного хронического воспаления в верхнечелюстных пазухах (ВЧП), в связи с чем данным пациентам были выполнены хирургические вмешательства (эндоскопические эндоназальные операции, радикальные операции на ВЧП по Колдуэлл-Люку).
По результатам сравнительного математического анализа у пациентов II-ых подгрупп (с заболеванием глотки и гортани) основной и контрольной групп в основной группе достоверно чаще, чем в контрольной (в 14 раз), встречались жалобы на стекание слизи по задней стенки глотки, в отличие от пациентов контрольной группы (р=0,00007).
Всем пациентам с хроническим тонзиллитом (ХТ) токсико-аллергической формой (ТАФ) II, как в основной, так и в контрольной группе, проводили хирургическое лечение: двустороннюю тонзиллэктомию.
Всем пациентам с хроническим рубцовым стенозом подскладочного отдела гортани, являвшихся хроническими трахеоканюленосителями, как в основной, так и в контрольной группе, производили ларинготрахеопластику.
По результатам сравнительного математического анализа у пациентов III-их подгрупп (с заболеванием среднего уха) при проведении КТ височных костей, пациентам с хроническим гнойным средним отитом в контрольной группе в 87% случаев, наблюдали деструкцию в аттико-антральной области, а в основной группе - в 30% случаев (р=0,000032).
Всем пациентам с хроническим гнойным эпитимпанитом, выполняли санирующую слухосохраняющую операцию на височной кости.
Изучив результаты клинических анализов крови у пациентов основной и контрольной группы, мы установили, что у больных контрольной группы достоверно чаще имел место лейкоцитоз (27,9% и 11,1%, соответственно, р=0,004).
Результаты микробиологического исследования – ПЦР диагностика в real-time режиме. Для диагностики атипичных микроорганизмов мы выбрали метод ПЦР в real-time режиме, как наиболее точную методику, позволяющую минимизировать риск ложноположительных результатов. По результатам исследования пациентов основной группы I подгруппы (с заболеванием носа и ОНП) только в 16,7% случаев была диагностирована хламидийная инфекция (C.trachomatis и C. pneumoniae). При этом микоплазменная инфекция выявлялась существенно чаще (в 83,3% случаев). Среди микоплазменных патогенов, наиболее часто (в 30% случаев) в этой группе встречалась M. pneumoniaе, реже (в 20% случаях) - M. salivarium.
По результатам молекулярно-генетического исследования у пациентов II подгруппы (с заболеванием глотки и гортани) у подавляющего большинства пациентов с диагнозом ХТ была выявлена микоплазменная инфекция (в 50,9% случаев), при этом наиболее часто выделялась M. salivarium (в 42,1% случаев). Хламидийная инфекция, также являлась редкостью. Так, у одного пациента с ХТ ТАФ II были выявлены ассоциации микроорганизмов: M. salivarium и C.trachomatis. А хламидии в виде монокультур выявлялись в 15,8% и были представлены видами: C.pneumoniae и C. trachomatis.
Помимо этого, у одного пациента с диагнозом правосторонний паратонзиллярный абсцесс были выявлены ассоциации двух видов микоплазм в полости паратонзиллярного абсцесса: M. orale и M. timone. Данный результат в ходе исследования мы наблюдали только однократно и расцениваем его, как крайне редко встречающуюся ситуацию.
После проведенного молекулярно-генетического исследования у пациентов III подгруппы (с заболеванием среднего уха) были получены следующие результаты: хламидийная инфекция не была обнаружена ни у одного пациента. Наиболее часто встречающимися видами микоплазм являлись: M. salivarium у 10 пациентов (47,6%), M. pneumoniaе у 4 пациентов (19,1%) и M. hominis у 4 пациентов (19,1%). При этом стоит отметить, что микоплазменная инфекция в силу своих биологических свойств не является этиологически значимым фактором развития хронического гнойного среднего отита и не вызывает деструктивные процессы в среднем ухе.
Помимо качественного определения искомых микроорганизмов, мы осуществили их количественный анализ, а именно определили число копий генов 16S рРНК бактерий рода Mycoplasma и Chlamydia, Chlamydophila. Мы осуществили количественный анализ в 108 образцах. Проанализировав полученные данные, мы установили определенную закономерность. Максимальное число копий генов 16S рРНК, выявлялось в случаях с максимально выраженными клиническими симптомами основного заболевания. Высокое число атипичных бактерий в очаге поражения коррелировалось также с выраженностью симптомов сопутствующих заболеваний, в частности, бронхолегочной системы, урогенитального тракта и заболеваний глаз.
Результаты микробиологического исследование (ПЦР диагностики методом гель-электрофореза). С целью подтверждения более высокой чувствительности и специфичности методики ПЦР в real-time режиме, у пациентов контрольной группы, мы провели классическое исследование ПЦР методом гель-электрофореза, который в настоящее время наиболее часто используют в рутинной лабораторной практике. По результатам проведенного исследования у 32% больных были получены положительные результаты при помощи ПЦР диагностики методом гель-электрофореза. При этом микоплазмы были выявлены в 28% случаев, хламидии - в 4% случаев. Необходимо отметить, что среди лабораторных методов, применяющихся в настоящее время с целью диагностики атипичных инфекций, данная методика характеризуется большим количеством положительных результатов. Именно поэтому, следующим этапом, всем пациентам с выявленной атипичной инфекцией (по результатам ПЦР гель-электрофореза) было проведено серологическое исследование с целью серодиагностики. При этом ни в одном случае не было выявлено признаков наличия атипичной инфекции в организме. Анализируя полученные данные, можем заключить, что классическая методика ПЦР (методом электрофореза) обладает существенно меньшей чувствительностью и специфичностью, характеризуется часто встречающимися ложноположительными результатами.
Результаты бактериологического исследования. По результатам исследования наиболее часто выявлявшимися микроорганизмами у пациентов I подгруппы (с заболеванием носа и ОНП) с острым воспалением ОНП в основной группе явились S.viridans (22%) и S.pneumoniae (22%). Несколько реже встречалась H.influenzae (16%) (см. рис. №1).
Несколько иная структура микробного пейзажа была характерна для пациентов с острым воспалением ОНП в контрольной группе. Так, в 41% случаев высевали S.pneumoniae, в 32% - H.influenzae, несколько реже (в 16% случаев) - M.catarrhalis, в 5% - S.pyogenes и S.aureus (см. рис. №1).
Рисунок №1Спектр микрофлоры, высеянной у пациентов с острым синуситом в основной (n=11) и в контрольной группах (n=60)
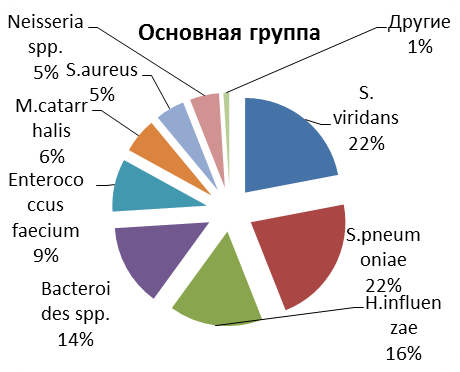
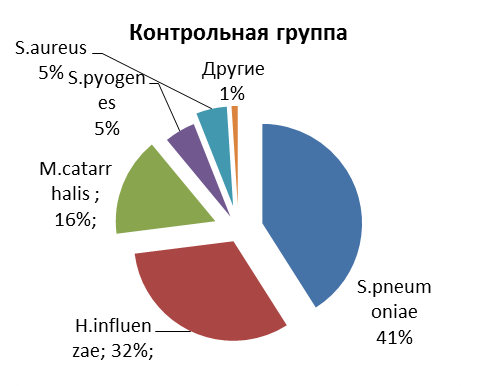
У больных с хроническим воспалением ОНП, существенным образом отличался спектр возбудителей. Так, в основной группе, наиболее часто встречались S.aureus - в 28% случаев, S.epidermidis- в 17% и S. viridans- в 15% случаев (см. рис. №2).
Рисунок №2 Спектр микрофлоры, высеянной у пациентов с хроническим синуситом в основной (n=19) и контрольной группах (n=120)
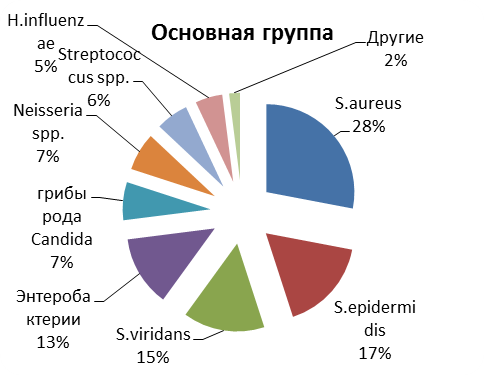
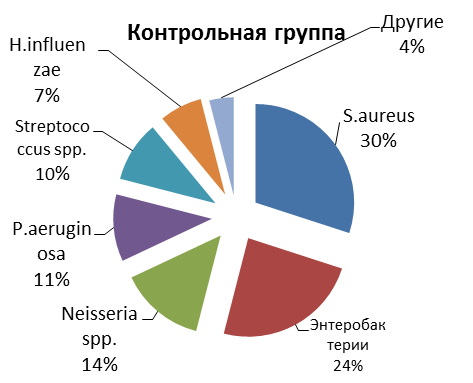
У больных с хроническим гнойным синуситом в контрольной группе наиболее часто были высеяны следующие микроорганизмы: S.aureus (30%), энтеробактерии (24%), P.aeruginosa (11%), Streptococcus spp (10%) (см. рис. №2).
По результатам исследования характера микрофлоры у пациентов II подгруппы (с заболеванием глотки и гортани) в основной группе у больных с ХТ ТАФ I и II в 28% случаев высеян S.pyogenes, в 25% - Streptococcus spp., в 15% - Corynebacterium spp. и Neisseria spp. и в 9% - Staphylococcus spp. (см. рис №3).
Рисунок №3 Спектр микрофлоры, высеянный у пациентов с хроническим тонзиллитом в основной (n=30) и контрольной группах (n=6)
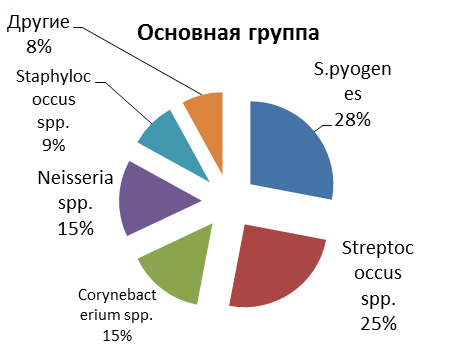
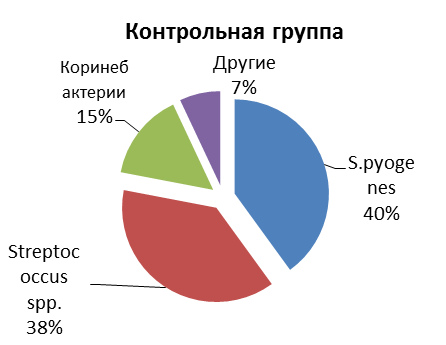
У 6 пациентов контрольной группы, страдавших ХТ высевали Streptococcus pyogenes в 40% случаев, Streptococcus spp. - в 38%, коринебактерии - в 15 % случаев (см. рис №3).
У больных с хроническим стенозом трахеи (основная группа), являющихся хроническими трахеоканюленосителями, в 100% случаев высевали ассоциации микроорганизмов. В составе микробных ассоциаций, наиболее часто высевали P.aeruginosa - в 42% случаев, Acinetobacter baumanii - в 28% и Klebsiella pneumoniae - в 12% случаев.
У 18 больных с острым катаральным ларингитом, как в основной, так и в контрольной группах, состав микрофлоры был однотипным. Наиболее часто высевали S.pneumoniae (40%), несколько реже (30%) - H.influenzae и M.catarrhalis (10%).
По результатам исследования наиболее часто выявлявшимися микроорганизмами у пациентов Ш подгруппы (с заболеванием среднего уха) у больных хроническим средним отитом в основной группе были ассоциации энтеробактерии (Proteus, Escherichia, 35%) и грибов родов Candida и Aspergillus (40%). У больных хроническим средним отитом в контрольной группе чаще всего высевали S.aureus – в 35% случаев, грибы родов Candida и Aspergillus - в 26%, энтеробактерии - 15%, а P.aeruginosa – в 13% случаев. При этом в 100% случаев встречались ассоциации микроорганизмов, состоящие из 2-3 возбудителей.
Результаты проведенных микробиологических исследований свидетельствуют о том, что в основной группе больных преобладали условно-патогенные микроорганизмы, относящиеся к представителям транзиторной нормальной микрофлоры слизистой оболочки ЛОР-органов, в то время как в контрольной группе наиболее часто высевались грамположительные (Streptococcus spp и S. aureus) и грамотрицательные микроорганизмы, преимущественно энтеробактерии, Р.aeruginosa и H.influenzae, являющиеся основными возбудителями типичных гнойно-воспалительных заболеваний ЛОР-органов.
Результаты серологического метода исследования. Во всех случаях с целью подтверждения наличия активной микоплазменной или хламидийной инфекции у больных основной группы с положительными результатами ПЦР в real-time режиме мы применяли метод ИФА диагностики. При этом, определив титр специфических антител (Ig классов М и G), можно было, косвенно, установить стадию заболевания.
Сопоставив результаты ПЦР в реальном времени с полученными результатами метода ИФА у 108 пациентов, мы определили, что в 86% случаев определяются диагностически значимые титры IgG и IgM в крови (Р=0,000000001). В 13 % случаев при положительных результатах ПЦР результаты ИФА были отрицательными. И, наоборот, у 312 пациентов ПЦР исследование имело отрицательный результат, в то время как у 10% больных (р= 0,00007) по результатам ИФА нами были диагностированы высокие титры IgG и IgM, что может быть связано с наличием активной атипичной инфекции в других системах (нижние дыхательные пути, урогенитальный тракт, суставы, лимфатические узлы и т.д.). У большинства больных с диагнозом ХТ титр Ig класса М и G не достигал диагностически значимых показателей, что, скорее всего, свидетельствует о второстепенном значении атипичной инфекции в воспалительном процессе в структуре небных миндалин.
Рациональный алгоритм терапии хламидийной и микоплазменной инфекции. Всем больным с острым воспалением ОНП производили пункции пазух и назначали антибактериальный препарат из группы макролидов (14-членные или 16-членные) или хинолонов III-IV поколения.
Пациентам с хроническим гнойным среднем отитом, включая послеоперационный период, также проводили антибактериальную терапию с применением хинолонов (фторхинолонов) IV поколения (моксифлоксацина), учитывая значительную роль анаэробной микрофлоры при данном заболевании (см. табл. №4).
Всем пациентам с ХТ ТАФ II и пациентам с хроническим рубцовым стенозом подскладочного отдела гортани, являвшихся хроническими трахеоканюленосителями, в послеоперационном периоде проводили антибактериальную терапию с применением хинолонов (фторхинолонов) III поколения (левофлоксацина). Аналогичная антибактериальная терапия (левофлоксацин) была назначена пациентам с острым катаральным ларингитом, учитывая преобладание грамотрицательной микрофлоры, включая неферментирующиею бактерии у пациентов с заболеваниями гортани (см. табл. №4).
В случае наличия осложненного течения сопутствующих заболеваний, со стороны бронхолегочной системы или урогенитального тракта, а также при имеющихся явлениях диспепсии или индивидуальной непереносимости макролидов мы назначали хинолоны III-IV поколения (левофлоксацин, моксифлоксацин). В остальных случаях использовали препараты-макролиды (14-членные или 16-членные – кларитромицин, джозамицин).
Эффективными методами воздействия на грибковую микрофлору, встречающуюся в качестве сопутствующей патологии при воспалительных заболеваниях ЛОР – органов у больных с хламидийной и микоплазменной инфекцией, являются антибактериальные препараты (см. табл. №4) в сочетании с местным применением фунгицидных препаратов (нафтифин, нитрофунгин, клотримазол).
Табл. №4 Рекомендуемые схемы антибактериальной терапии пациентов с верифицированной атипичной инфекцией
| Лекарственный препарат | Суточная дозировка | Длительность терапии |
| Кларитромицин (макролид 14-членный) | по 1 табл. 500мг Х 2 р/д | 14 дней |
| Джозамицин (макролид 16-членный) | по 1 табл. 500 мг Х 2 р/д | 12-14 дней |
| Левофлоксацин (хинолон III поколения)* | по 1 табл. 500 мг Х 1 р/д | 10-14 дней |
| Моксифлоксацин (хинолон IV поколения)* | по 1 табл. 400 мг Х1 р/д | 7-10 дней |
*- классификация R. Quintiliani (1999)
После начала терапии у больных I подгруппы основной группы с 3 суток (± 0,8) отмечалось уменьшение, а к 5 суткам (±1,2) – исчезновение основных симптомов гайморита (р=0,0032). Через 1 месяц при проведении ИФА исследования антител к атипичным возбудителям в крови не было обнаружено.
У пациентов с ХТ, а также у больных с паратонзиллярным абсцессом отмечалось значительное уменьшение жалоб и объективных симптомов заболевания к 5 суткам (±1,1; р=0,0024). Выписка из стационара производилась, в среднем, на 6 сутки (±1,5; р=0,038).
Больные, являющиеся хроническими трахеоканюленосителями, а также пациенты с острым и хроническим катаральным ларингитом отмечали улучшение самочувствия на 6 сутки (±1,2) после начала лечения (р=0,048).
У больных хроническим гнойным среднем отитом после хирургической санации гнойного очага и начала антибактериальной терапии, улучшение самочувствия отмечалось на 7 сутки (±1,2; р=0,034). При этом период реконвалесценции протекал на протяжении 3-4 недель и характеризовался уменьшением гноетечения и эпидермизацией послеоперационной полости.
Эффективность терапии у пациентов всех групп оценивали по результатам контрольного ИФА исследования. Через 4-5 недель (±1,6) антител к атипичным возбудителям не было обнаружено.
На фоне проводимого лечения в 100% было достигнуто клиническое улучшение самочувствия на 8 сутки (±1,6), а в последующем - выздоровление, что было подтверждено результатами клинического, микробиологического и иммунологического исследования.
Прогноз вероятности инфицирования ЛОР-органов хламидиями и микоплазмами. Учитывая тот факт, что ПЦР в real-time режиме – пока еще дорогостоящая и не получившая широкого распространения методика, нами была предложена шкала прогнозирования риска активного инфицирования ЛОР-органов хламидийными и микоплазменными патогенами. Данная шкала разработана с учетом математического анализа данных, в которую были включены только статистически достоверные критерии (табл. №5).
Таблица №5 Прогнозирование риска инфицирования ЛОР-органов хламидиями и микоплазмами
| № | Значение | Количество баллов |
| 1 | Слизистый характер отделяемого | 1 |
| 4 | Заболевание бронхо-легочной системы в анамнезе | 1 |
| 5 | Заболевания урогенитального тракта в анамнезе | 1 |
| 6 | Двусторонний характер поражения ЛОР-органов | 1 |
| 8 | Отсутствие лейкоцитоза в крови при наличии воспаления | 1 |
| 9 | Отсутствие лечебного эффекта от применения -лактамных антибиотиков | 1 |
| 10 | Длительное трахеоканюленосительство | 1 |
| 2 | Стекание слизи по задней стенке глотки | 2 |
| 3 | Коньюктивит в анамнезе | 2 |
| 7 | Рецидивирующий характер течения заболевания | 2 |
Суммируя баллы, получаем результат, величина которого прямо пропорциональна вероятности активной колонизации ЛОР-органов хламидиями и микоплазмами, на основании чего даны рекомендации по дальнейшему ведению данных пациентов ( см. табл №6).
Табл. №6 Шкала вероятности колонизации ЛОР-органов хламидиями и микоплазмами и алгоритм ведения пациентов
| Сумма баллов | Ожидаемый % наличия атипичной инфекции | Тактика ведения пациентов |
| 1-5 | <50 % | Рекомендуется проведение ПЦР исследования в реальном времени и в случае положительного результата, необходимо назначение антибактериальной терапии (14-членными или 16-членнными макролидами или хинолонами III-IV поколения) |
| 6-9 | 50-75% | При достаточно высокой вероятности инфицирования атипичными патогенами рекомендуется проведение ИФА. В случае положительного результата, показана постановка ПЦР в real-time режиме (количественное исследование) и антибактериальная терапия. |
| 10-13 | 76-95% | Рекомендовано проведение антибактериальной терапии с применением макролидов (14-членные или 16-членные) или хинолонов III-IV поколения. |
ВЫВОДЫ:
- Микоплазменная инфекция ЛОР-органов встречается в 22% случаев, в то время как хламидийная инфекция диагностируется значительно реже - в 4% случаев.
- Воспалительные заболевания ЛОР-органов хламидийной и микоплазменной этиологии имеют признаки малосимптомного воспаления (в 40 % случаев), носят затяжной, рецидивирующий характер (в 70% случаев). Хламидийная инфекция характеризуется появлением серозного отделяемого (в 87% случаев), а микоплазменная - преимущественно слизистого (85%), реже слизисто-гнойного (11,1%, р=0,004). Для атипичной инфекции чаще всего было характерно двустороннее поражение (в 77,8 % случаев) ЛОР – органов в сочетании с поражением нижних дыхательных путей (91,7%) и конъюнктивитом (52,8%).
- Наиболее информативным методом диагностики хламидийной и микоплазменной инфекции является ПЦР в real-time режиме, который по своей чувствительности и специфичности более чем в два раза превосходит ПЦР методом гель-электрофореза.
- Оптимальными лекарственными препаратами для лечения воспалительной патологии ЛОР-органов хламидийной и микоплазменной этиологии являются современные 14 – и 16-членные макролиды и респираторные хинолоны III-IV, которые показали свою эффективность в 100% случаев.
- Разработанная нами шкала прогноза риска инфицирования хламидийной и микоплазменной инфекции, на основании которой предложен лечебно-диагностический алгоритм ведения пациентов с атипичной инфекцией ЛОР-органов, позволяет в ранние сроки диагностировать и эффективно провести адекватную терапию данной патологии.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Наличие серозного характера воспалительного процесса, сопутствующей патологии в виде бронхолегочных заболеваний, конъюнктивита, двустороннего поражения ЛОР-органов, схожей симптоматики у родственников, является косвенным свидетельством наличия атипичного процесса, вызванного хламидиями и микоплазмами.
- Для верификации хламидийной или микоплазменной инфекции рекомендуется использовать методику ПЦР в real-time режиме, подтвержденную результатами ИФА.
- При проведении антибактериальной терапии у больных с микоплазменной и хламидийной инфекцией ЛОР-органов, учитывая биологические свойства возбудителя, необходимо строгое соблюдением дозировки, кратности и длительности применения антибактериального препарата. При наличии семейного анамнеза заболевания, необходимо назначить курс антибактериальной терапии родственникам пациента.
- В случае наличия осложненного течения сопутствующих заболеваний, со стороны бронхолегочной системы или урогенитального тракта, а также при имеющихся явлениях диспепсии или индивидуальной непереносимости макролидов, рекомендовано назначать хинолоны III-IV поколения. В остальных случаях мы рекомендуем использовать современные макролиды (14-членные или 16-членные).
Список печатных работ.
- Особенности течения хламидийной и микоплазменной инфекции в оториноларингологии/ Пальчун В.Т., Гуров А.В., Руденко В.В.// Материалы X Всероссийского конгресса оториноларингологов «Наука и практика в оториноларингологии» М., 2011 – с. 37-38.
- Возможности применения Фромилида Уно в терапии гнойно-воспалительных заболеваний ЛОР – органов у больных сахарным диабетом/ Гуров А.В., Бирюкова Е.В., Юшкина М.А., Руденко В.В.// Лечебное дело. - №1.- 2012. – с. 74-78.
- Хламидийная и микоплазменная инфекция в оториноларингологии (систематический обзор)/ Пальчун В.Т., Гуров А.В., Руденко В.В.// Вестник оториноларингологии.-№6-2012- с.91-97.
- Клинические проявления хламидийной и микоплазменной инфекции у больных с заболеваниями носа и околоносовых пазух/ Гуров А.В., Дербенева М.Л., Руденко В.В.//Вековые традиции, новые технологии. 210 лет на страже здоровья России. Материалы юбилейной научно-практической конференции ГКБ№1 им. Н.И. Пирогова М., 2012-с.56-58.
- Современные методы диагностики хламидийной и микоплазменной инфекции в оториноларингологии. / Гуров А.В., Дербенева М.Л., Руденко В.В.//Вековые традиции, новые технологии. 210 лет на страже здоровья России. Материалы юбилейной научно-практической конференции ГКБ№1 им. Н.И. Пирогова М., 2012-с.58-60.
- Особенности диагностики хламидийной и микоплазменной инфекции в оториноларингологии/ Пальчун В.Т., Гуров А.В., Руденко В.В.// Материалы XI Всероссийского конгресса оториноларингологов «Наука и практика в оториноларингологии» М., 2012 – с. 23-25.
- Клинические проявления хламидийной и микоплазменной инфекции у больных с заболеваниями носа и околоносовых пазух/ Пальчун В.Т., Гуров А.В., Руденко В.В.// Материалы XI Всероссийского конгресса оториноларингологов «Наука и практика в оториноларингологии» М., 2012 – с. 198-199.
- Современные возможности терапии хронических очагов бактериальной патологии глотки типичной и атипичной природы/ Гуров А.В., Гусева О.А., Руденко В.В., Ордер Р.Я., Резаков Р.А. // Лечащий Врач.-№3-2013- с. 62-65.

