Клинико-экспериментальное обоснование применения диодного лазерного излучения с длиной волны 0,81 мкм в лечении больных доброкачественными новообразованиями кожи
На правах рукописи
ШТИРШНАЙДЕР ЮЛИЯ ЮРЬЕВНА
КЛИНИКО-ЭКСПЕРИМЕНТАЛЬНОЕ ОБОСНОВАНИЕ
ПРИМЕНЕНИЯ ДИОДНОГО ЛАЗЕРНОГО ИЗЛУЧЕНИЯ
С ДЛИНОЙ ВОЛНЫ 0,81 МКМ В ЛЕЧЕНИИ БОЛЬНЫХ
ДОБРОКАЧЕСТВЕННЫМИ НОВООБРАЗОВАНИЯМИ КОЖИ
14.01.10 – кожные и венерические болезни
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2010
Работа выполнена в отделе дерматологии Федерального государственного учреждения «Государственный научный центр дерматовенерологии Росмедтехнологий».
Научные руководители:
доктор медицинских наук Владимир Анатольевич Волнухин
доктор медицинских наук Вера Анатольевна Смольянникова
Официальные оппоненты:
доктор медицинских наук Вероника Владимировна Мордовцева
доктор медицинских наук,
профессор Владимир Павлович Туманов
Ведущее научное учреждение: Российский Университет Дружбы Народов, Москва
Защита диссертации состоится « 26 » мая 2010 г. в 12 часов на заседании Диссертационного совета Д 208.115.01 при Федеральном государственном учреждении «Государственный научный центр дерматовенерологии Росмедтехнологий» по адресу: 107076, г. Москва, ул. Короленко, д. 3, стр. 6.
С диссертацией можно ознакомиться в библиотеке ФГУ «ГНЦД Росмедтехнологий» (г. Москва).
Автореферат разослан « 23 » апреля 2010 г.
Ученый секретарь
Диссертационного совета
кандидат медицинских наук Наталия Константиновна Иванова
Общая характеристика работы
Актуальность проблемы. В последние годы наблюдается постоянный рост заболеваемости населения различными новообразованиями кожи (Ключарева С.В. и соавт., 2005, 2007; Юцковская Я.А. и соавт., 2006; Кубанова А.А. и соавт., 2007; Дубенский В.В., Дубенский Вл.В., 2008), значительную долю которых составляют доброкачественные новообразования кожи (Курдина М.И., 1993; Кубанова А.А. и соавт., 2004; Малишевская Н.П. и соавт., 2005; Дубенский Вл.В., 2009). В связи с этим актуальным является совершенствование подходов к профилактике и лечению данной патологии.
Среди существующих методов лечения основное место занимают методы оперативного лечения новообразований кожи: хирургическое иссечение, электрокоагуляция, криотерапия, радиохирургия, лазерная деструкция и другие. Однако каждый из этих методов может вызывать те или иные побочные реакции: отеки, кровотечения, пузыри, рубцы, диспигментации и др. (Дубенский В.В., 2008). Кроме того, ни один из них не обеспечивает идеальный косметический результат, удовлетворяющий пациента и врача.
В настоящее время для лечения новообразований кожи все чаще применяют различные типы высокоинтенсивных лазеров: углекислотные, неодимовые, рубиновые, медные и др. (Самцов А.В. и соавт., 2001; Юцковская Я.А. и соавт., 2006; Victor E. et al., 2000). Особое место среди них занимают диодные лазеры, генерирующие излучение в ближнем инфракрасном диапазоне (0,76-1,4 мкм). Они экономичны, компактны, надежны в эксплуатации, относительно дешевы, позволяют подводить излучение к обрабатываемому объекту посредством гибкого светововолокна (Заварзин В.Н. и соавт., 2003; Бойко Э.В. и соавт.,1999; Гришанов В.Н. и соавт., 1999).
Диодное лазерное излучение поглощается основными хромофорами кожи - меланином, гемоглобином и водой (Landthaler M., Hohenleutner U., 2006), сравнительно хорошо проникает в ткани, обеспечивая термокоагуляцию дефектов кожи с минимальным термическим повреждением окружающих и подлежащих тканей. Поглощение излучения гемоглобином позволяет получать надежный гемостаз и оптимизировать тем самым процессы регенерации послеоперационного раневого дефекта.
В литературе имеются публикации о применении диодных лазеров для эпиляции волос, коагуляции сосудов, проведения оперативных вмешательств в абдоминальной хирургии, нейрохирургии, урологической, офтальмологической и стоматологической практике (Соколова Г.Н. и соавт., 2000; Dierickx C.C. et al., 1998; Campos V.B. et al., 2000; Baugh W.P. et al., 2001; Bombeccari G.P. et al., 2009). Отдельные сообщения посвящены лечению некоторых кожных заболеваний: псевдофолликулита (Kauvar A.N., 2000), фибролипом (Capodiferro S. et al., 2008), сенильного кератоза (Desiate A. et al., 2009) и др. В то же время эффективность удаления диодными лазерами доброкачественных новообразований кожи мало изучена. Морфологические изменения в коже, а также особенности динамики заживления раны после воздействия данного вида излучения не выяснены. Перечисленный круг вопросов определил актуальность, а также цель и задачи настоящего исследования.
Цель работы. Разработка метода лечения больных доброкачественными новообразованиями кожи диодным лазерным излучением с длиной волны 0,81 мкм средней мощности на основании клинико-экспериментальных и морфологических исследований особенностей течения раневого процесса.
Задачи исследования
1. Изучить характер морфологических изменений, развивающихся в коже морских свинок под действием диодного лазерного излучения с длиной волны 0,81 мкм средней мощности.
2. Провести сравнительную оценку морфологических изменений кожи экспериментальных животных после однократного воздействия диодным лазерным излучением, электротоком и жидким азотом.
3. Исследовать особенности репаративных процессов в экспериментальных ранах при деструкции кожи диодным лазерным излучением, электротоком и жидким азотом.
4. Разработать метод лечения доброкачественных новообразований кожи диодным лазерным излучением с длиной волны 0,81 мкм средней мощности и изучить эффективность его применения у больных меланоцитарными невусами, паукообразными гемангиомами, обыкновенными бородавками, папилломами.
5. Провести сравнительное изучение эффективности лечения больных обыкновенными бородавками методами лазерной деструкции, электрокоагуляции и криохирургии жидким азотом.
Научная новизна
В экспериментах на морских свинках установлен характер морфологических изменений, развивающихся в коже под действием диодного лазерного излучения с длиной волны 0,81 мкм средней мощности, проявляющихся формированием четких границ зоны коагуляционного некроза со слабовыраженной воспалительной реакцией вокруг него, эффективным гемостазом, незначительным отёком. Полученные данные расширяют представления о механизмах деструктивного действия диодного лазерного излучения ближнего инфракрасного диапазона.
Выявлена зависимость степени деструкции кожи от дозы диодного лазерного излучения, характеризующаяся увеличением, как глубины, так и площади зоны некроза при повышении его мощности от 1 до 3,5 Вт.
Установлены преимущества деструктивного действия на кожу экспериментальных животных диодного лазерного излучения перед электрокоагуляцией, заключающиеся в формировании полноценного гемостаза и менее выраженного перифокального воспаления, что свидетельствует о меньшей травматизации прилегающих тканей.
Показано, что морфологические изменения, возникающие в коже животных после облучения диодным лазером, отличаются от изменений, вызванных воздействием жидкого азота, формированием четких границ зоны некроза и отсутствием диффузного воспаления, что приводит к раннему формированию грануляционной ткани, сокращению сроков эпителизации раневого дефекта и предотвращает развитие побочных эффектов.
Обоснована целесообразность применения в лечении больных доброкачественными новообразованиями кожи: меланоцитарными невусами, паукообразными гемангиомами, обыкновенными бородавками, папилломами диодного лазерного излучения с длиной волны 0,81 мкм средней мощности.
Выявлены преимущества лечения больных обыкновенными бородавками диодным лазерным излучением перед электрокоагуляцией и криохирургией жидким азотом, характеризующиеся более редким развитием побочных эффектов и небольшими сроками регенерации операционных ран.
Практическая значимость
На основании комплексных клинико-экспериментальных исследований разработан эффективный метод лечения диодным лазерным излучением с длиной волны 0,81 мкм больных меланоцитарными невусами, паукообразными гемангиомами, обыкновенными бородавками, папилломами, позволяющий при радикальном удалении опухолей уменьшить побочные эффекты и сроки регенерации операционных ран за счет минимального повреждения прилежащих тканей и обеспечения надежного гемостаза. Разработанный метод может применяться в амбулаторных условиях для терапии доброкачественных новообразований кожи.
Основные положения, выносимые на защиту
1. Морфологические изменения, развивающиеся при деструкции кожи диодным лазерным излучением с длиной волны 0,81 мкм, мощностью 1-3,5 Вт в непрерывном режиме, характеризуются формированием четких границ зоны коагуляционного некроза, эффективным гемостазом, слабовыраженными воспалительными явлениями вокруг зоны некроза, незначительным отеком и фрагментацией коллагеновых волокон в верхней части дермы.
2. Деструкция кожи диодным лазером имеет преимущества перед электрокоагуляцией, заключающиеся в формировании полноценного гемостаза и менее интенсивного перифокального воспаления, что свидетельствует о ее меньшем травмирующем действии на окружающие ткани.
3. Морфологические изменения, возникающие в коже животных после облучения диодным лазером, отличаются от изменений, вызванных криодеструкцией, наличием четких границ зоны некроза и отсутствием диффузных воспалительных явлений, что способствует сокращению сроков эпителизации раневого дефекта.
4. Особенностями репаративных процессов, развивающихся в экспериментальных ранах при деструкции кожи диодным лазером, в отличие от репаративных процессов, наблюдающихся после воздействия электротоком и жидким азотом, являются отсутствие вторичного инфицирования, меньшее повреждение окружающей здоровой кожи, более короткие сроки заживления ран.
5. Деструкция кожи диодным лазерным излучением с длиной волны 0,81 мкм, мощностью 1-3,5 Вт в непрерывном режиме, является эффективным методом удаления обыкновенных бородавок, папиллом, меланоцитарных невусов и паукообразных гемангиом, позволяющим достичь хорошего эффекта у 89% пациентов.
6. Фотодеструкция обыкновенных бородавок диодным лазером предпочтительнее удаления их методами электрокоагуляции и криодеструкции жидким азотом, поскольку сопровождается меньшей болезненностью, реже вызывает побочные эффекты и позволяет сократить сроки заживления операционных ран.
Внедрение результатов исследования в практику здравоохранения
Метод внедрен в практическую работу Консультативно-диагностического Центра ФГУ «ГНЦД Росмедтехнологий», кожно-венерологического отделения ФГУ «ГВКГ имени Н.Н.Бурденко». Результаты исследований используются в учебном процессе ФГУ «ГНЦД Росмедтехнологий», кафедры дерматовенерологии и косметологии ГОУ ДПО РМАПО Росздрава, кожно-венерологического отделения ФГУ «ГВКГ имени Н.Н.Бурденко», ГКБ № 14 им. В.Г. Короленко г. Москвы.
По материалам диссертационной работы утверждена медицинская технология № ФС-2006/253-У от 15.08.2006 «Применение высокоинтенсивного диодного лазерного излучения с длиной волны 0,81 мкм в лечении доброкачественных новообразований кожи»
Публикации. По материалам исследований опубликовано 11 печатных работ, в том числе пять в рецензируемых журналах, рекомендованных ВАК Минобрнауки РФ.
Апробация работы. Основные положения работы и результаты исследований представлены и обсуждены на научно-практической конференции ФГУ «ГНЦД Росмедтехнологий» (Москва, 2002), а также на XIV Междисциплинарном научном симпозиуме «Новое в дерматовенерологии, андрологии, акушерстве и гинекологии: наука и практика» (Москва, 2009), конференции «Современные достижения лазерной и малоинвазивной медицины и их применение в практическом здравоохранении» (Дмитров, 2009), заседании Московского научного общества дерматовенерологов им. А.И. Поспелова (Москва, 2010).
Объем и структура диссертации
Диссертационная работа изложена на 119 страницах компьютерного текста, состоит из введения, обзора литературы и 3 глав, результатов собственных исследований, заключения, выводов, практических рекомендаций, списка литературы, включающего в себя 75 отечественных и 92 зарубежных источника и списка сокращений. Материалы диссертации иллюстрированы 18 таблицами и 30 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
Диссертационная работа основана на клинических и экспериментальных исследованиях и выполнена на 145 больных и 178 морских свинках. У больных и в эксперименте применяли 3 метода деструкции кожи: облучение диодным лазером с длиной волны 0,81 мкм, электрокоагуляцию и криохирургию жидким азотом.
Для лазерной деструкции кожи использовали лазерный хирургический аппарат «КРИСТАЛЛ» (Россия) (регистрационный номер МЗ РФ 29/01101100/213903 от 17.02.2003, сертификат соответствия РОСС RU.ИМО2.В10686), генерирующий излучение с длиной волны 0,81 мкм, в непрерывном режиме мощностью до 4,5 Вт. Процедуры проводили с использованием гибкого светооптического волокна (диаметр 0,6 мм). При работе с лазером дополнительно применяли аппарат для эвакуации/фильтрации дыма и газов «VAPOR-VAC II» («ELLMAN international, inc.», США; регистрационный номер МЗ РФ 2000/581 от 20.10.2000).
Электрокоагуляцию осуществляли аппаратом ЭХВЧ-20 «МТУСИ» (регистрационный номер ФС 022б1997/0358-04 от 27 июля 2004 г., сертификат соответствия РОСС RU.ИМ 24.ВОО256). Воздействие электротоком проводили в режиме электрокоагуляции с мощностью 12 Вт, при легком контакте игольчатого наконечника электрода с поверхностью кожи.
Криодеструкцию жидким азотом проводили методом зонда с использованием криодеструктора «КриоИней» (регистрационный номер МЗ РФ 29/15040698/1893-01 от 29.07.1998, сертификат соответствия РОСС RU. UМО/ВО2761 №4545675). Использовались насадки круглой формы с гладкой контактной поверхностью, площадью 1 мм и 1 см. Охлажденный криозонд помещали перпендикулярно поверхности кожи и плотно прижимали к ней.
Экспериментальные исследования. Экспериментальная часть работы выполнена на 178 морских свинках-самцах светлого окраса, весом 200-300 граммов.
В первой серии экспериментов проведено изучение характера макро- и микроскопических изменений, возникающих после однократного воздействия на кожу диодного лазерного излучения с длиной волны 0,81 мкм у 55 морских свинок. У животных был исследован диапазон доз лазерного излучения, способных вызывать деструктивные изменения в коже. С этой целью на кожу боковой поверхности туловища точечно воздействовали лазером в течение 5 секунд (в непрерывном режиме работы аппарата) при мощности излучения 0,5; 1; 1,5; 2,5; 3,5 и 4,5 Вт. Через 1 час из зон облучения брали биоптаты для патоморфологического исследования. У 40 морских свинок (4 группы по 10 животных в каждой) проведено сравнительное морфометрическое исследование гистологических срезов для оценки глубины и площади некроза, возникшего после лазерного облучения с мощностью 1; 1,5; 2,5; 3,5 Вт (при экспозиции 5 секунд).
Во второй серии экспериментов проведены сравнительные наблюдения и морфологические исследования состояния раневого дефекта через 1 час и 1 сутки после однократного воздействия на кожу (при экспозиции 5 секунд) диодным лазерным излучением, электротоком и жидким азотом у 60 морских свинок (по 10 животных в каждой группе). Деструкцию кожи лазером проводили в непрерывном режиме, контактным способом, при мощности излучения 2,5 Вт, электрокоагуляцию – мощностью 12 Вт игольчатым электродом, криодеструкцию жидким азотом - с помощью насадки с контактной поверхностью, площадью 1 мм. В группах животных, у которых деструкция кожи осуществлялась диодным лазером и электротоком, проведен морфометрический анализ глубины и площади некроза, сформировавшегося соответственно через 1 час и 1 сутки после воздействия указанными физическими факторами. Морфометрия изменений кожи после воздействия жидким азотом не представлялась возможной в связи с отсутствием зональности и четких границ повреждения.
В третьей серии экспериментов были изучены особенности репаративных процессов и морфологических изменений, развивавшихся в операционной ране при воздействии на кожу диодным лазерным излучением (мощность 2,5 Вт), электротоком и жидким азотом у 63 морских свинках, (3 группы по 21 животному в каждой). Для этого на левой и правой боковых поверхностях туловища животных формировали по 1 ране, площадью 1 см2 и глубиной деструкции до подкожно-жирового слоя (воздействие жидким азотом проводили с помощью насадки с контактной поверхностью площадью 1 см2). В ранах на правой боковой поверхности туловища животных в разные сроки эпителизации (через 3, 5 и 10 суток) осуществляли забор биопсийного материала для анализа морфологических изменений в коже. Раны на левой боковой поверхности оставляли под наблюдением с целью анализа динамики репаративных процессов, которые оценивали по следующим характеристикам: наличие признаков воспаления (гиперемия, отек, отделяемое из раны), вторичного инфицирования или кровотечения. Интенсивность признаков оценивали по балльной шкале (от 0 до 3 баллов): 0 баллов соответствовал отсутствию признака, 1, 2 и 3 балла соответствовали слабой, умеренной и выраженной интенсивности признака. Регистрировали сроки эпителизации раны.
Патоморфологические и морфометрические исследования. Всего изучено 178 гистологических препаратов кожи морских свинок. Забор биоптатов проводили под эфирным наркозом. После стандартной аппаратной гистологической проводки ткани заливали в парафин (Leica EG 1160, Германия), серийные срезы толщиной 5 мкм изготавливали на ротационном микротоме (SHANDON, Великобритания), растягивали на предметных стеклах. Окраску гемотоксилин-эозином осуществляли в автоматическом устройстве (ST 5010 AUTOSTAINER XL, YUNG, Германия). Препараты заключали под покровное стекло. Гистологические изменения кожи изучали в световом микроскопе (Leica DM 4000B, Германия), изображения документировали цифровой камерой (Leica DFC 320, Гемания). Оценивали характер повреждения эпидермиса и дермы, интенсивность воспалительной реакции, сосудистых изменений и сроки развития репаративных процессов в ране. Морфометрический анализ проводили с помощью программы «AdobePhotoshop 6.0» по методике Г.Г. Автандилова (2002). Для этого в 5 полях зрения каждого препарата при увеличении х100 и обратной чувствительности 20 методом случайной выборки анализировали участки, в которых измеряли глубину некроза и площадь некроза.
Клинические исследования. Изучение эффективности лечения доброкачественных новообразований кожи лазерным излучением с длиной волны 0,81 мкм проведено у 95 больных: 23 – меланоцитарными невусами, 22 – паукообразными (звездчатыми) гемангиомами, 25 - обыкновенными бородавками, 25 – папилломами. У 75 пациентов обыкновенными бородавками, локализовавшимися на кистях, проведено сравнительное изучение эффективности и побочных реакций лечения лазерным излучением с длиной волны 0,81 мкм, электрокоагуляции и криохирургии жидким азотом.
Больным меланоцитарными невусами, бородавками и папилломами удаление осуществляли под местной (инфильтрационной) анестезией 2% раствором лидокаина. Больным паукообразными гемангиомами обезболивание не проводили в связи с кратковременностью воздействия и с целью предотвращения развития нежелательного отека.
Ближайшие результаты лечения оценивали в течение 1 месяца с частотой осмотра 1 раз в неделю по радикальности удаления новообразований, срокам эпителизации операционной раны, частоте развития и интенсивности побочных реакций (наличию болевых ощущений в послеоперационный период, воспалительных явлениях – отека, гиперемии, отделяемого из раны, кровотечений, вторичного инфицирования). Интенсивность побочных эффектов оценивали по балльной шкале симптомов (от 0 до 3 баллов). Ноль баллов соответствовал отсутствию признака; 1, 2 и 3 балла соответствовали минимальной, умеренной и максимальной выраженности признака.
Отдаленные результаты лечения оценивали через 6 месяцев после удаления новообразований. Анализировали частоту и сроки развития рецидивов, характер сформировавшегося рубца (гипер-, нормо- или атрофический рубец), наличие/отсутствие диспигментаций (гипо – или гиперпигментаций). При радикальном удалении новообразований, отсутствии рецидива и диспигментации кожи, формировании на месте новообразования нормотрофического рубца эффект расценивали как хороший. При радикальном удалении, отсутствии рецидива и образовании гипертрофического/атрофического рубца и/или наличии диспигментации кожи эффект расценивали как удовлетворительный. При нерадикальном удалении и/или наличии рецидива эффект расценивали как неудовлетворительный.
Статистический анализ. Статистическую обработку данных проводили с помощью пакета прикладных программ SPSS 16 (SPSS, Inc., США). Анализ количественных и порядковых данных осуществлялся с применением параметрических (t-критерий Стьюдента) и непараметрических критериев Манна-Уитни и Краскела-Уоллеса, а качественных данных - с помощью таблиц сопряженности и критерия и точного критерия Фишера. Описание распределений количественных и порядковых признаков в выборках представляли в виде средних и среднеквадратических отклонении или медиан и границ интерквартильных отрезков, качественных номинальных признаков – в виде абсолютных частот и процентов. Различия считали статистически значимыми при Р<0,05.
Результаты собственных исследований
Характер морфологических изменений, развивающихся в коже экспериментальных животных, при воздействии диодным лазерным излучением с длиной волны 0,81 мкм средней мощности.
При оценке действия различных мощностей лазерного излучения (через 1 час после воздействия) установлено, что мощность 0,5 Вт не вызывала существенного повреждения кожи морских свинок. Признаки деструкции эпидермиса отсутствовали, в месте воздействия отмечались лишь незначительные уплощение кератиноцитов и пикноз ядер. Изменения со стороны дермы были слабовыраженными и проявлялись в некотором уплотнении коллагеновых волокон в зоне непосредственного воздействия. Придатки кожи были интактны.
После воздействия лазерного излучения с мощностью 1; 1,5; 2,5; 3,5 и 4,5 Вт на коже визуально определялся точечный дефект, размером, равным диаметру светооптического волокна, с карбонизацией коричневатого цвета и легкой гиперемией вокруг. Отека, отделяемого из раны, кровотечения не отмечалось.
При морфологическом исследовании биоптатов кожи в эпидермисе и дерме обнаруживали очаг коагуляционного некроза. Перифокальные изменения практически отсутствовали. В прилегающих участках сосочковой дермы наблюдали отек и незначительную фрагментацию коллагеновых волокон. Экстравазаты эритроцитов не выявляли, просветы сосудов в большей части дермы незначительно расширены. В придатках кожи наблюдалась умеренная дистрофия эпителия волосяных фолликулов и небольшая его десквамация с очаговым пикнозом ядер.
Морфометрическим исследованием установлено статистически значимое (при сравнении групп по критерию Стьюдента во всех случаях Р<0,001) увеличение глубины и площади некроза при повышении мощности излучения от 1 до 3,5 Вт, что свидетельствует о зависимости деструктивного действия лазерного излучения от его дозы (табл. 1).
Увеличение мощности лазерного излучения свыше 3,5 Вт приводило к значительному нарастанию перифокальных изменений в коже, выражавшихся в
Таблица 1. Глубина и площадь зоны некроза кожи морских свинок через 1 час после воздействия различными дозами диодного лазерного излучения.
| 1 Вт | 1,5 Вт | 2,5 Вт | 3,5 Вт | |
| Глубина поражения, мм | ||||
| М±SD | 1,41±0,17 | 1,96±0,09 | 2,66±0,15 | 3,03±0,09 |
| Мин/Макс | 1,05/1,65 | 1,8/2,17 | 2,39/2,86 | 2,83/3,2 |
| 95% ДИ | [1,29; 1,53] | [1,89; 2,03] | [2,55; 2,76] | [2,96; 3,09] |
| Площадь поражения, мм | ||||
| М±SD | 1,26±0,09 | 2,21±0,01 | 2,6±0,04 | 2.92±0,08 |
| Мин/Макс | 1,1/1,42 | 2,2/2,22 | 2,51/2,65 | 2,8/3,01 |
| 95% ДИ | [1,2; 1,32] | [2,21; 2,22] | [2,57; 2,62] | [2,87; 2,97] |
появлении отека и фрагментации коллагеновых волокон, и дистрофии клеток эпителия волосяных фолликулов. Таким образом, оптимальным энергетическим диапазоном лазерного излучения, вызывавшем деструкцию кожи с минимальным повреждением прилежащих тканей, являлся диапазон мощности от 1 до 3,5 Вт.
При сравнительном изучении изменений, развивающихся у морских свинок через 1 час после воздействия электротоком и жидким азотом, установлено, что в группе электрокоагуляции на коже животных отмечался участок карбонизации темно-коричневого цвета с незначительной гиперемией вокруг, размер которого незначительно превышал диаметр электрода. При гистологическом исследовании кожи обнаруживали обширный участок коагуляционного некроза, вокруг которого формировался субэпидермальный пузырь с выраженными дистрофическими изменениями кератиноцитов и разрушением придатков кожи, а также резкое полнокровие сосудов. В группе криодеструкции жидким азотом в зоне контакта криозонда с кожей развивались гиперемия и отек, не имевшие четких границ. В гистологических препаратах четких границ зоны некроза не выявлялось, отмечались резко выраженный отек дермы, полнокровие сосудов, признаки образования субэпидермального пузыря.
При оценке повреждений кожи, развивавшихся через 1 сутки после воздействия физическими факторами, в группе лазерной деструкции визуальных изменений в коже не наблюдали. При гистологическом исследовании вокруг зоны коагуляционного некроза выявляли воспалительный инфильтрат из нейтрофилов и лимфоцитов. В сосочковом и верхних отделах ретикулярного слоев дермы обнаруживали умеренный отек и незначительную фрагментацию коллагеновых волокон. Придатки кожи в перифокальной зоне были дистрофически изменены, но не разрушены. Экстравазаты эритроцитов не наблюдали (табл. 2).
В группе электрокоагуляции при визуальной оценке вокруг раневого дефекта, покрытого струпом, были видны отек и гиперемия. В препаратах наблюдали увеличение отека и площади субэпидермального пузыря, интенсив-
Таблица 2. Морфологические изменения в коже морских свинок через 1 сутки после однократного воздействия диодным лазерным излучением с длиной волны 0,81 мкм, электротоком и жидким азотом.
| Морфологический признак | Лазерная деструкция | Электро-коагуляция | Крио- деструкция |
| Некроз | +++ | +++ | ++ |
| Воспалительные изменения (отек, инфильтрация тканей лейкоцитами) | ++ | +++ | +++ |
| Перифокальные изменения (фрагментация коллагеновых волокон, дистрофические изменения клеток эпителия и придатков кожи, поляризация ядер клеток эпидермиса) | + | +++ | +++ |
| Сосудистые изменения (полнокровие, экстравазаты) | + | +++ | ++ |
Примечание. + – минимальное проявление признака, ++ – умеренное проявление признака, +++ – максимальное проявление признака.
ной инфильтрации нейтрофилами и лимфоцитами; в дерме присутствовали обширные экстравазаты эритроцитов, отмечалось резкое полнокровие сосудов, в некоторых из них выявлялся стаз лейкоцитов. В группе криодеструкции жидким азотом при визуальной оценке отмечали нарастание отека и гиперемии, в месте криовоздействия наблюдали формирование тонкого струпа. В гистологических препаратах выявляли увеличение в размерах субэпидермального пузыря, в дерме обнаруживали резкое полнокровие сосудов, увеличение отека и формирование диффузного воспалительного инфильтрата, который не отграничивал зону поражения от неизмененных тканей. Отмечалось резкое полнокровие сосудов.
Морфометрическое исследование не выявило значимых различий глубины и площади некроза через 1 час после воздействия диодным лазерным излучением (2,66±0,15 мм и 2,6±0,04 мм, соответственно) и электротоком (2,75±0,07 мм и 2,69±0,14 мм, соответственно) (рис. 1), однако через 1 сутки глубина и площадь некроза после воздействия электротоком оказались статистически значимо больше (4,45±0,11 мм и 9,49±0,2 мм, соответственно), чем при воздействии лазерным излучением (3,71±0,08 мм и 8,24±0,01 мм, соответственно) (значимость определялась по t-критерию Стьюдента). При сравнении показателей деструкции кожи через 1 час и спустя 1 сутки после воздействия лазерным излучением и электротоком площадь некроза возрастала в значительно большей степени, чем глубина некроза. Проведение морфометрического исследования после воздействия жидким азотом было невозможно, так как отсутствовала зональность и четкие границы повреждения.
 |  |
Рисунок 1. Глубина и площадь некроза кожи морских свинок через 1 час и 1 сутки после воздействия диодным лазерным излучением и электротоком (средние значения).
Полученные данные свидетельствуют о том, что лазерная деструкция обладает рядом преимуществ, по сравнению с электрокоагуляцией и криовоздействием жидким азотом, в частности, сопровождается более ранним и четким формированием коагуляционного некроза, незначительными воспалительными явлениями и эффективным гемостазом, меньше травмирует окружающие ткани, что способствует более быстрой и полноценной регенерации раневого дефекта.
Особенности репаративных процессов, развивающихся в экспериментальных ранах после деструкции кожи диодным лазерным излучением, электротоком и жидким азотом. Заживление ран, образовавшихся в результате воздействия на кожу указанных физических факторов, происходило под струпом. При визуальной оценке динамики репаративных процессов установлено, что в группе воздействия лазером до начала эпителизации проходило значимо меньшее количество дней, чем в группе воздействия азотом (Р<0,001) и электротоком (Р<0,001). Окончательная эпителизация операционных ран после воздействия лазерным излучением также наблюдалась в более короткие сроки (14 дней). После воздействия электротоком и жидким азотом сроки эпителизации ран составляли соответственно 16 дней (P<0,001) и 26 дней (P<0,001) (рис. 2).
Анализ побочных эффектов, наблюдавшихся в экспериментальных ранах показал, что у всех морских свинок после воздействия физическими факторами развивались воспалительные явления (гиперемия, отек, отделяемое из раны), однако интенсивность и длительность их существования в группах животных различались. При сравнении групп с использованием U-критерия Манна-Уитни продолжительность воспалительных явлений в группе лазерной деструкции оказалась значимо ниже, чем в группах воздействия электротоком (Р=0,005) и жидким азотом (Р<0,001). Интенсивность воспаления в группе лазерной деструкции не отличалась от таковой в группе электрокоагуляции, но была

Рисунок 2. Сроки начала и окончания эпителизации экспериментальных ран (медианы и квартили).
значимо ниже, чем в группе криохирургии жидким азотом (Р<0,001 по U-критерию Манна-Уитни (рис. 3).
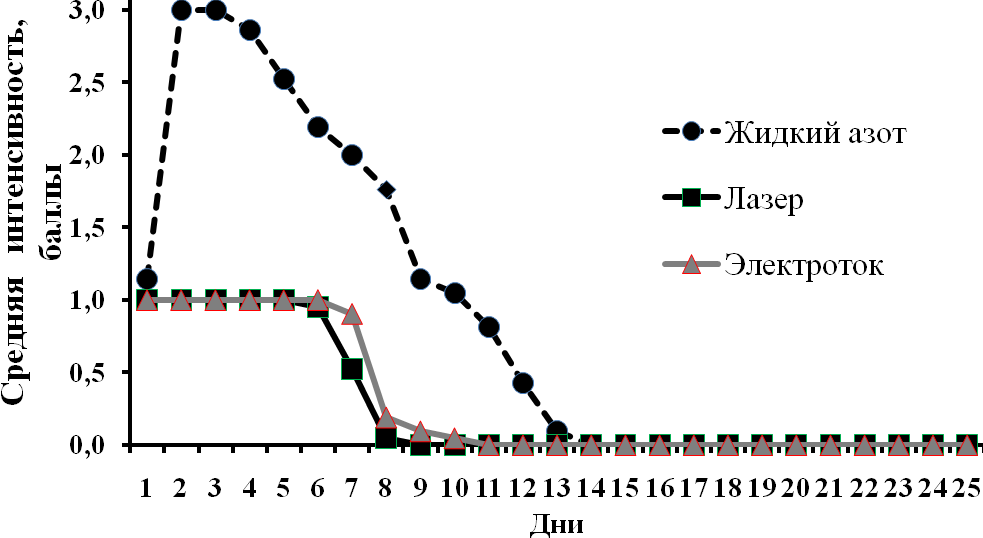
Рисунок 3. Динамика воспалительных явлений у экспериментальных животных.
Кроме воспалительных явлений наблюдали также такие побочные эффекты, как кровотечение и вторичное инфицирование ран (табл. 3). При сравнении групп по точному критерию Фишера установлено, что частота встречаемости кровотечений в группе лазерной деструкции была значимо ниже, чем в группе электрокоагуляции (Р<0,001) и не отличалась от таковой в группе криодеструкции (Р=0,107). Вторичное инфицирование ран в группе лазерной деструкции не встречалось. В группе электрокоагуляции оно развивалось статистически значимо чаще, чем в группе лазерной деструкции (P=0,021), статистических различий по частоте его развития в группах криохирургии и лазерной деструкции не выявлено (P=0,232).
Таблица 3. Частота развития кровотечений и вторичного инфицирования ран при деструкции кожи морских свинок диодным лазером, электротоком и жидким азотом.
| Показатели | Лазерная деструкция | Электро- коагуляция | Крио- деструкция |
| Кровотечение | |||
| Частота, абс (%) | 4 (19%) | 21 (100%) | 0 |
| 95% ДИ | [5,4%;41,9%] | [83,9%;100%] | [0%;16,1%] |
| Вторичное инфицирование | |||
| Частота, абс (%) | 0 | 6 (28,6%) | 3 (14,3%) |
| 95% ДИ | [0%;16,1%] | [11,3%;52,2%] | [3%;36,3%] |
При гистологическом исследовании биоптатов кожи, взятых через 3 суток после нанесения ран, в группе лазерной деструкции вокруг зоны некроза отмечались незначительный отек, фрагментация коллагеновых волокон, слабовыраженная воспалительная реакция, локализующаяся только вокруг зоны повреждения. В группе электрокоагуляции выявляли зону некроза, воспалительный вал и зону перифокальных изменений, представленных выраженным отеком, фрагментацией и истончением коллагеновых волокон. В области перифокальных изменений и воспалительного вала наблюдали экстравазаты эритроцитов. В группе криодеструкции жидким азотом четкая зональность отсутствовала. Воспалительные изменения носили обширный диффузный характер. Наблюдали выраженный отек, дистрофию кератиноцитов и формирование субэпидермального пузыря.
При анализе гистологических препаратов через 5 суток после деструкции кожи в группе лазерного воздействия выявлено уменьшение зоны коагуляционного некроза, пролиферация пластов многослойного плоского эпителия с проникновением их под некротизированные ткани, увеличение количества сосудов вокруг участков некроза, что свидетельствовало о начале репаративных процессов. Воспалительные изменения были представлены скудными лимфо-гистиоцитарными инфильтратами с незначительной примесью нейтрофилов. В группе электрокоагуляции были видны участки лизиса коагуляционного некроза, отек дермы с выраженной инфильтрацией нейтрофилами, небольшие экстравазаты эритроцитов. Придатки кожи вокруг зоны некроза были разрушены. Признаков начала репаративных процессов не отмечалось. В группе криодеструкции поврежденные ткани оставались неотграниченными от неизмененных участков воспалительным валом. Отмечался резко выраженный отек с формированием субэпидермального пузыря, сопровождавшийся полнокровием сосудов и диффузной инфильтрацией лимфоцитами и нейтрофилами.
При изучении морфологических изменений, развившихся спустя 10 суток, в группе лазерной деструкции раны выглядели полностью эпителизированными, в дерме отмечали признаки сформировавшегося рубца в виде четко ориентированных пучков коллагеновых волокон. В группе электрокоагуляции эпидермис выглядел восстановленным, наблюдались признаки формирования рубца: коллагеновые волокна располагались параллельно эпидермису в виде тонких пучков. Вместе с тем в субэпидермальных отделах сохранялись фокусы грануляционной ткани. В группе криодеструкции в коже выявляли участок некроза, вокруг которого наблюдали резко выраженный отек. Сохранялись субэпидермальный пузырь и воспалительная инфильтрация лейкоцитами, появлялись фокусы пролиферации сосудов, однако полноценная грануляционная ткань отсутствовала.
Таким образом, результаты проведенных исследований свидетельствуют о том, что репаративные процессы, развивавшиеся в экспериментальных ранах после деструкции кожи диодным лазерным излучением с длиной волны 0,81 мкм, характеризуются меньшей продолжительностью и интенсивностью гиперемии кожи, отека и отделяемого из ран, отсутствием вторичного инфицирования, редким развитием кровотечений, более короткими сроками эпителизации раневых дефектов. Морфологически они характеризуются менее выраженными воспалительными явлениями, ранним формированием грануляционной ткани с быстрым переходом ее в зрелую соединительную.
Результаты лечения больных меланоцитарными невусами, паукообразными гемангиомами, обыкновенными бородавками, папилломами диодным лазерным излучением с длиной волны 0,81 мкм. На основании полученных данных разработан метод лечения больных доброкачественными новообразованиями кожи диодным лазерным излучением средней мощности с длиной волны 0,81 мкм. Воздействие лазерным излучением проводили в амбулаторных условиях в непрерывном режиме работы, контактным способом, с мощностью от 1,5 до 2,5 Вт сканирующими движениями световода. Экспозиция лазерного излучения зависела от типа новообразования и площади его основания. При лечении меланоцитарных невусов и папиллом она варьировала от 2-3 секунд до 1-2 минут. При паукообразных гемангиомах воздействие лазерным излучением проводили в течение 1-2 секунд только на центральную узелковоподобную часть новообразования; окружающие веерообразно расходящиеся сосуды впоследствии исчезали самостоятельно. Обыкновенные бородавки, требующие более глубокой обработки, удаляли послойно, сканирующими движениями в течение 1-2 минут. После удаления пациентам рекомендовали смазывать послеоперационную рану растворами красителей, избегать травматизации, контакта с водой и инсоляции, а также самостоятельного удаления струпа до окончания процесса заживления. При вторичном инфицировании назначали водорастворимые мази или присыпки, содержащие антибиотики.
Под наблюдением находились 95 больных доброкачественными новообразованиями кожи (табл. 4). Ни у одного из пациентов не было выявлено заболеваний, наличие которых могло повлиять на процессы нормального заживления послеоперационной раны (сахарный диабет, гипертоническая болезнь, нарушения системы свертывания крови, болезни соединительной ткани, психические расстройства).
Таблица 4. Клиническая характеристика больных.
| Меланоцитарные невусы (n=23) | Паукообразные гемангиомы (n=22) | Обыкновенные бородавки (n=25) | Папилломы (n=25) | |
| Возраст, годы | 36,04±8,99 | 31,64±12,19 | 23,72±6,79 | 34,48±18,63 |
| Пол (муж./жен.) | 5/18 | 5/17 | 7/18 | 13/12 |
| Длительность болезни, годы | 26,22±10,48 | 4,71±8,24 | 2,16±2,97 | 2,01±2,66 |
Примечание. Возраст и длительность болезни приведены в виде средних значений, пол указан в абсолютных частотах.
Применение диодного лазерного излучения позволило радикально удалить новообразования у 94 (98,9%) больных. У 1 больной паукообразной гемангиомой не удалось провести полноценную деструкцию центральной части новообразования за 1 процедуру. Сроки эпителизации операционных ран варьировали при лечении меланоцитарных невусов от 7 до 28 дней (в среднем 14,3±5,3), паукообразных гемангиом – от 7 до 21 дня (в среднем 12,1±4,0), обыкновенных бородавок - от 7 до 40 дней (в среднем 15,5±3,8), папиллом – от 7 до 20 дней (в среднем 10,3±3,7). После полного заживления операционных ран у большинства больных на коже формировались нормотрофические рубцы цвета нормальной кожи.
Из побочных эффектов, в основном, наблюдали болезненность и воспалительные явления в виде гиперемии, отека и отделяемого из ран (табл. 5). Кровотечение зарегистрировано лишь у 2 больных папилломами, что объясняется недостаточной коагуляцией питающего сосуда. Зуда кожи, образования пузырей или вторичного инфицирования послеоперационной раны не отмечено ни в одном случае.
В результате проведенного лечения хороший эффект был достигнут у 85 больных (89,5%) (рис. 4). Удовлетворительный эффект констатирован у 7 пациентов (7,4%). Среди них у 4 пациентов (4,2%) после процедур лазерной деструкции вокруг послеоперационного рубца возник ободок гиперпигментации светло-коричневого цвета, у 3 больных (3,2%) образовались гипертрофические рубцы. Развития гипопигментации или атрофических рубцов не отмечено ни в одном случае. Неудовлетворительный эффект наблюдали у 3 больных (3,2%): у 1 больной паукообразной гемангиомой не удалось провести радикальное удаление новообразования за 1 процедуру, у 2 больных бородавками через 4 месяца после полной эпителизации операционной раны развился рецидив заболевания.
Комплаентность больных к лечению была удовлетворительной, большинство из них были удовлетворены результатами проведенной терапии.
Таблица 5. Частота развития побочных эффектов при лечении доброкачественных новообразований кожи диодным лазером с длиной волны 0,81 мкм (абсолютные частоты, в скобках проценты).
| Побочные эффекты | Группы больных | |||
| Невусы (n=23) | Папилломы (n=25) | Гемангиомы (n=22) | Бородавки (n=25) | |
| Болезненность после процедуры | 3 (13%) | 0 | 0 | 3 (12%) |
| Отек | 0 | 0 | 1 (4,5%) | 3 (12%) |
| Отделяемое из раны | 6 (26,1%) | 2 (8%) | 4 (18,2%) | 6 (24%) |
| Гиперемия | 0 | 0 | 0 | 3 (12%) |
| Кровотечение | 0 | 2 (8%) | 0 | 0 |
Проведенные исследования свидетельствуют о высокой эффективности применения диодного лазерного излучения с длиной волны 0,81 мкм средней мощности в лечении доброкачественных новообразований кожи.
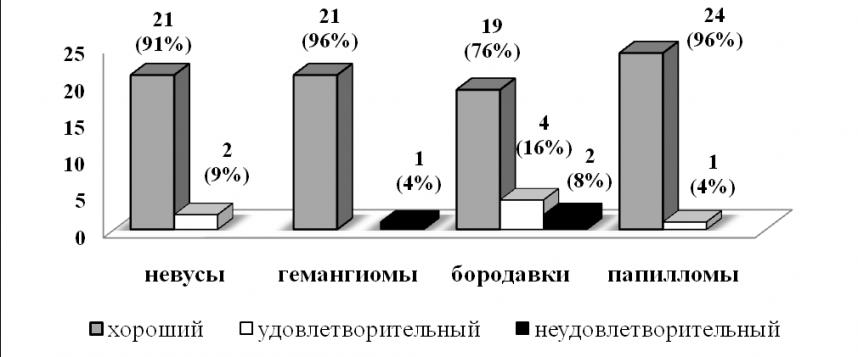
Рисунок 4. Результаты лечения больных доброкачественными новообразованиями кожи диодным лазером с длиной волны 0,81 мкм.
Радикальное удаление новообразований удалось провести у 98,9% наблюдавшихся больных, хороший эффект лечения достигнут у большинства пациентов. Данный метод лечения является малоболезненным и в большинстве случаев бескровным, хорошо переносится больными и легко выполнимым в амбулаторных условиях, что делает его доступным широкой клинической практике.
Сравнительное изучение эффективности лечения больных обыкновенными бородавками методами лазерной деструкции, электрокоагуляции и криохирургии жидким азотом. У 75 больных обыкновенными бородавками на кистях, проведено сравнительное изучение эффективности и побочных эффектов лечения лазерным излучением с длиной волны 0,81 мкм, электротоком и жидким азотом. Значимых различий в распределении по полу (Р=0,072 по критерию ), возрасту и длительности заболевания (соответственно Р=0,177 и Р=0,67 по H-критерию Краскела-Уоллеса) между группами не выявлено. Таким образом, можно считать наблюдавшиеся группы однородными по полу, возрасту и длительности заболевания.
Применение указанных методов лечения позволило у всех больных получить радикальный эффект. Наименьшие сроки (5,64±0,99 дней) начала эпителизации отмечены в группе лечения лазером (при сравнении с двумя другими группами Р<0,001 по U-критерию Манна-Уитни), наибольшие (11,04±2,65 дней) – в группе лечения жидким азотом (рис. 5). Сроки окончания эпителизации в группе лечения лазером (15,48±3,81 дней) были статистически значимо меньше, чем в группе лечения жидким азотом (24±9,9 дней; Р<0,001 по U-критерию Манна-Уитни), но не отличались от таковых в группе электрокоагуляции (18,4±6,26 дней; Р=0,16 по U-критерию Манна-Уитни).
 |
Анализ частоты развития побочных эффектов показал, что лазерная деструкция гораздо реже сопровождалась болезненностью в послеоперационном периоде и не вызывала зуд (табл. 6). При лечении лазером ни в одном случае не наблюдалось кровотечений, в то время как при электрокоагуляции и криохирургии они развились соответственно у 14 и 3 пациентов. Вторичное инфицирование ран при лазерной деструкции и криохирургии не отмечалось, однако встречалось при электрокоагуляции бородавок. В отличие от электрокоагуляции при удалении бородавок лазером реже развивались гиперемия и отделяемое из ран (соответственно P=0,001 и P=0,01), по сравнению с криодеструкцией реже встречались отек (P=0,012), отделяемое из ран (P=0,001) и образование пузырей (P=0,001).
Таблица 6. Частота развития побочных эффектов при лечении больных обыкновенными бородавками методами лазерной деструкции, электрокоагуляции и криохирургии жидким азотом (абсолютные частоты, в скобках проценты).
| Побочные эффекты | Методы лечения | Р1 | Р2 | Р3 | ||
| Лазер | Электро ток | Жидкий азот | ||||
| Болезненность после процедуры | 3 (12%) | 25 (100%) | 25 (100%) | <0,001 | <0,001 | - |
| Зуд | 0 | 0 | 23 (92%) | - | <0,001 | <0,001 |
| Отек | 3 (12%) | 7 (28%) | 12 (48%) | 0,289 | 0,012 | 0,244 |
| Отделяемое из раны | 6 (24%) | 16 (64%) | 19 (76%) | 0,01 | 0,001 | 0,538 |
| Гиперемия | 3 (12%) | 15 (60%) | 5 (20%) | 0,001 | 0,702 | 0,009 |
| Образование пузырей | 0 | 0 | 25 (100%) | - | <0,001 | <0,001 |
| Кровотечение | 0 | 14 (56%) | 3 (12%) | <0,001 | 0,235 | 0,002 |
| Вторичное инфицирование | 0 | 4 (16%) | 0 | 0,11 | - | 0,11 |
Примечание. Р1-значимость различий между группами лечения лазером и электротоком; Р2 – значимость различий между группами лечения лазером и жидким азотом; Р3 – значимость различий между группами лечения электротоком и жидким азотом (точный критерий Фишера).
В группе лечения лазером 78% больных (рис. 6) не имели ни одного побочного эффекта, у остальных 22% больных этой группы наблюдали от 1 до 4 побочных эффектов, тогда как при электрокоагуляции и криохирургии частота встречаемости 4-6 побочных эффектов была у большинства больных (Р<0,001 при сравнении с каждой из двух других групп по U-критерию Манна-Уитни). Таким образом, анализ количества побочных эффектов говорит о том, что наиболее предпочтительным, с этой точки зрения, является лечение лазером, наименее – жидким азотом.
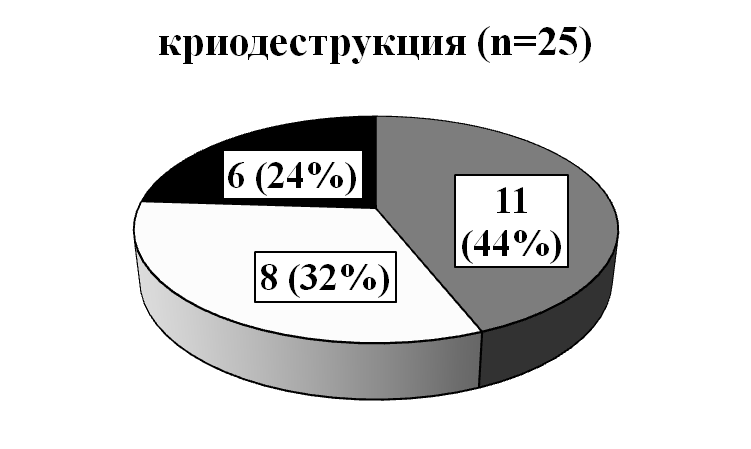
Отдаленные результаты лечения больных прослежены в течение 6 месяцев. Хороший эффект констатирован при лазерной деструкции у 76% больных, при электрокоагуляции – у 56%, при лечении жидким азотом – у 44%, удовлетворительные результаты наблюдали соответственно у 16, 20 и 32% пациентов (рис. 7).
Рецидивы в период от 1 до 4 месяцев после полного заживления послеоперационной раны наблюдали при лечении лазером, электротоком и жидким азотом соответственно у 2 (8%), 6 (24%) и 6 (24%) больных. У большинства пациентов на месте ран формировались гладкие нормотрофические рубцы.
У 3 (12%) пациентов группы лазерной деструкции, 6 (24%) пациентов группы электрокоагуляции и 4 (16%) пациентов группы лечения жидким азотом наблюдали гипертрофический характер рубцевания. Гиперпигментация кожи в области послеоперационного рубца отмечалась после лазерной деструкции у 1 (4%) пациента, после электрокоагуляции – у 3 (12%) больных,
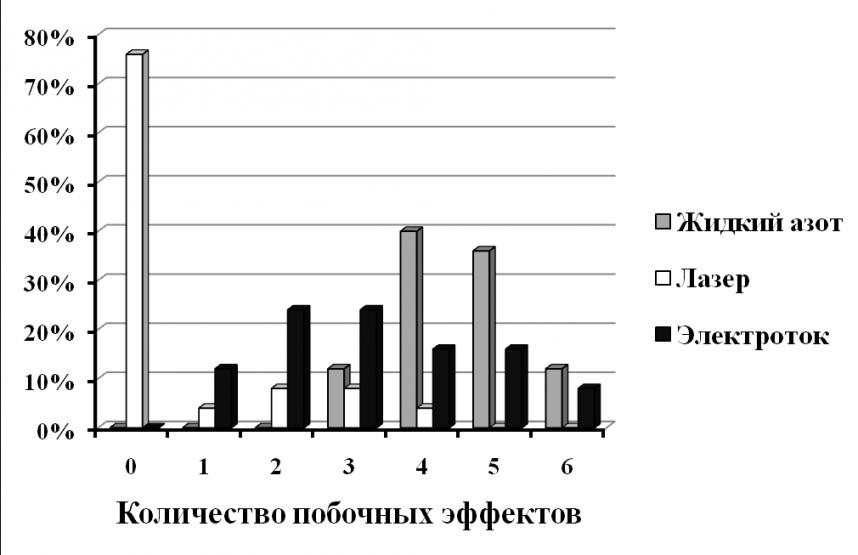
Рисунок 6. Частотное распределение больных по числу побочных эффектов в зависимости от метода лечения.
при криохирургическом лечении – у 4 (16%) больных. Развития атрофических рубцов или гипопигментации не отмечено ни в одном случае.
 |  |
 |
|
Рисунок 7. Результаты лечения больных обыкновенными бородавками кистей диодным лазером, жидким азотом и электротоком.
При сравнении выявили, что значимых различий по эффекту (по точному критерию Фишера) в группах лечения лазером и электротоком (Р=0,289), лазером и жидким азотом (Р=0,079), электротоком и жидким азотом (Р=0,662) не отмечено.
Таким образом, лечение больных обыкновенными бородавками кистей диодным лазерным излучением с длиной волны 0,81 мкм имеет преимущества перед электрокоагуляцией и криодеструкцией жидким азотом, в частности, является менее болезненным, реже вызывает побочные эффекты и позволяет сократить сроки эпителизации операционных ран. Полученные данные обосновывают целесообразность использования в клинической практике диодного лазерного излучения с длиной волны 0,81 мкм средней мощности при лечении больных доброкачественными новообразованиями кожи.
ВЫВОДЫ
1. В экспериментах на морских свинках установлено, что диодное лазерное излучение с длиной волны 0,81 мкм средней мощности (1-4,5 Вт в непрерывном режиме) оказывает на кожу деструктивное действие, морфологические проявления которого характеризуются формированием четких границ зоны коагуляционного некроза, незначительными воспалительными явлениями и отеком прилежащих тканей, эффективным гемостазом. При мощности лазерного излучения от 1 до 3,5 Вт отмечаются минимальные перифокальные изменения.
2. Морфологические изменения, вызванные в коже экспериментальных животных однократным воздействием диодного лазерного излучения, отличаются от изменений, наблюдаемых при электрокоагуляции, менее выраженными воспалительными и перифокальными изменениями, более полноценным гемостазом. При криодеструкции жидким азотом, в отличие от воздействия лазерным излучением, не формируются четкие границы зоны некроза, воспалительные явления имеют ярко-выраженный и диффузный характер.
3. Репаративные процессы, развивающиеся в экспериментальных ранах при деструкции кожи диодным лазером, по сравнению с ранами после воздействия электротоком и жидким азотом, характеризуются отсутствием вторичного инфицирования, редким развитием кровотечений, более короткими сроками эпителизации раневых дефектов. Морфологические изменения проявляются ранним формированием грануляционной ткани с быстрым переходом ее в зрелую соединительную ткань и ранней эпителизацией.
4. Применение диодного лазерного излучения с длиной волны 0,81 мкм средней мощности в лечении 95 больных меланоцитарными невусами, паукообразными гемангиомами, обыкновенными бородавками и папилломами позволило произвести радикальное удаление новообразований в 98,9% наблюдавшихся случаев и достичь хорошего эффекта у 89,5% пациентов.
5. Лечение больных обыкновенными бородавками диодным лазером имеет преимущества перед электрокоагуляцией и криодеструкцией жидким азотом, поскольку обладая одинаковой эффективностью, является менее болезненным, реже вызывает побочные эффекты и позволяет сократить сроки эпителизации операционных ран.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Лечение больных новообразованиями кожи диодным лазерным излучением проводят под местной инфильтрационной анестезией 2% раствором лидокаина. Воздействия осуществляют контактным способом, сканирующими движениями световода в непрерывном режиме работы аппарата. Мощность и экспозиция облучения зависят от величины новообразования, характера и степени васкуляризации удаляемых тканей.
2. Для удаления небольших экзофитных новообразований (невусов, капиллярных гемангиом, папиллом) с размерами не более 1 см в диаметре используют мощность излучения от 1 до 2,5 Вт. При удалении образований с размерами более 1 см в диаметре или появлении кровотечения мощность увеличивают до 3-4,5 Вт, что позволяет быстрее достичь гемостаза. Время облучения варьирует от 1-2 секунд до 2-3 минут, при наличии большого количества элементов проводят несколько сеансов с интервалом в 1-2 недели.
3. Обыкновенные бородавки, требующие более глубокой обработки, следует удалять послойно, до основания, при непрерывном режиме и мощности излучения 2-3,5 Вт. Образовавшийся струп иссекают ножницами, затем дно раны вторично облучают лазером, что позволяет более тщательно обработать рану, достичь гемостаза, предотвратить вторичное инфицирование и получить удовлетворительный косметический результат.
4. После облучения разрушенные ткани удаляют марлевым тампоном, смоченным спиртом или раствором перекиси водорода, что позволяет провести ревизию основания удаляемого элемента и удостовериться в его полном разрушении. Если новообразование разрушено не полностью, проводят повторное воздействие лазерным излучением до полного удаления патологической ткани.
5. После удаления новообразований наложения повязки, как правило, не требуется. Пациенту рекомендуют 2-4 раза в сутки смазывать раневую поверхность растворами красителей (бриллиантового зеленого, фукорцина), избегать травмирования раны и контакта с водой, а также самостоятельного удаления струпа до окончания процесса заживления. При вторичном инфицировании назначают водорастворимые мази или присыпки, содержащие антибиотики. Для профилактики возникновения гиперпигментаций на месте удаленных новообразований в течение 6 месяцев после лечения необходимо избегать инсоляции и использовать солнцезащитный крем.
6. Для коррекции ухода за послеоперационной зоной, а также контроля полноты и качества лечения обязателен повторный осмотр больного лечащим врачом. При отсутствии полного излечения проводят 1-2 повторные процедуры лазерной деструкции.
СПИСОК НАУЧНЫХ РАБОТ, ОПУБЛИКОВАННЫХ
ПО ТЕМЕ ДИССЕРТАЦИИ
1. Волнухин В.А. Лечение доброкачественных новообразований кожи высокоинтенсивным диодным инфракрасным лазером /Волнухин В.А., Коваленко Ю.Ю., Гомберг М.А. // VIII Всерос. съезд дерматовенерологов. Тез. науч. работ. – М., 2001. - Т.I. – С. 107-108.
2. Федоров С.М. Комбинированная деструкция доброкачественных новообразований и очагов папилломавирусной инфекции на коже и слизистых оболочках / Федоров С.М., Гомберг М.А., Коваленко Ю.Ю. и др. // VIII Всерос. съезд дерматовенерологов. Тез. науч. работ. – М., 2001. – Т. I. – С.154.
3. Коваленко Ю.Ю. Использование высокоинтенсивного диодного инфракрасного лазерного излучения в лечении пациентов с саркомой Капоши / Коваленко Ю.Ю., Волнухин В.А. // Вестн. последиплом. мед. образования. – 2001. - №1. – С. 55.
4. Васильев М.М. Случай гигантской кондиломы Buschke-Loewenstein / Васильев М.М., Степанова Ю.Н., Коваленко Ю.Ю. // Клин. дерматол. и венерол. – 2002. - №1. – С.15-17.
5. Смольянникова В.А. Экспериментальное обоснование применения высокоинтенсивного диодного инфракрасного лазерного излучения при лечении доброкачественных новообразований кожи / Смольянникова В.А., Волнухин В.А., Коваленко Ю.Ю. и др. // I Рос. Конгр. дерматовенерологов: Тез. науч. работ. – СПб. 2003. - Т.1. – С. 237.
6. Коваленко Ю.Ю. Лечение массивных аногенитальных бородавок подофиллотоксином в комбинации с высокоинтенсивным диодным инфракрасным лазерным излучением / Коваленко Ю.Ю. // I Рос. Конгр. дерматовенерологов: Тез. науч. работ. – СПб. 2003. – Т. 2. – С. 156.
7. Кубанова А.А. Применение высокоинтенсивного диодного лазерного излучения с длиной волны 0,81 мкм в лечении доброкачественных новообразований кожи. Медицинская технология №ФС-2006/253-У от 15 августа 2006 г. / Кубанова А.А., Самсонов В.А., Коваленко Ю.Ю. и др. // Вестн. дерматол. и венерол. – 2008. - №2. – С.35-38.
8. Штиршнайдер Ю.Ю. Динамика морфологических изменений в ране после воздействия высокоинтенсивным диодным лазерным излучением с длиной волны 0,81 мкм: экспериментальные исследования / Штиршнайдер Ю.Ю., Смольянникова В.А., Волнухин В.А. // Хирург. – 2008. - №10. – С.27-32.
9. Штиршнайдер Ю.Ю. Анализ степени деструкции кожи экспериментальных животных при воздействии различными дозами высокоинтенсивного диодного лазерного излучения с длиной волны 0,81 мкм / Штиршнайдер Ю.Ю., Волнухин В.А., Смольянникова В.А. // Вестн. последиплом. мед. образования. – 2009. - №2. – С.60-61.
10. Штиршнайдер Ю.Ю. Эффективность терапии меланоцитарных невусов диодным лазером с длиной волны 0,81 мкм / Штиршнайдер Ю.Ю., Волнухин В.А., Смольянникова В.А. // Вестн. последиплом. мед. образования. – 2009. - №3-4. – С.20.
11. Штиршнайдер Ю.Ю. Клиническая эффективность применения диодного лазера в лечении доброкачественных новообразований кожи / Штиршнайдер Ю.Ю., Волнухин В.А. // Вестн. дерматол. и венерол. – 2009. - №6. – С.98-103.
СПИСОК ИСПОЛЬЗОВАННЫХ СОКРАЩЕНИЙ
абс. – абсолютное число;
ДИ – доверительный интервал;
мин/макс – минимальное/максимальное значение
мкм – микрометры;
М – среднее;
SD – среднее квадратическое (стандартное) отклонение.

