Орексинэргические нейроны гипоталамуса крыс wistar после введения липополисахарида
На правах рукописи
Перекрест София Владимировна
Орексинэргические нейроны гипоталамуса крыс wistar после введения липополисахарида
14.00.16 – патологическая физиология
АВТОРЕФЕРАТ
Диссертации на соискание ученой степени
кандидата биологических наук
Санкт-Петербург – 2009
Работа выполнена в отделе Общей патологии и патофизиологии, Научно-исследовательском институте Экспериментальной медицины Северо-Западного отделения Российской Академии Медицинских Наук
Научный руководитель:
Академик РАМН
Корнева Елена Андреевна
Официальные оппоненты:
1. Шестакова Светлана Алексеевна, доктор медицинских наук, профессор кафедры Патологической физиологии Санкт-Петербургского государственного медицинского университета им. акад. И.П. Павлова.
2. Кветная Татьяна Викторовна, доктор биологических наук, руководитель лаборатории Биогеронтологии Санкт-Петербургского института биорегуляции и геронтологии СЗО РАМН.
Ведущая организация:
Российская Военно-медицинская академия им. С.М. Кирова.
Защита состоится «23» июня 2009 г. в «11» часов на заседании диссертационного совета Д001.022.02 при Научно-исследовательском институте Экспериментальной медицины СЗО РАМН по адресу: 197376, Санкт-Петербург, ул. Академика Павлова, д. 12.
С диссертацией можно ознакомиться в научной библиотеке Научно-исследовательского института Экспериментальной медицины СЗО РАМН по адресу: 197376, Санкт-Петербург, ул. Академика Павлова, д. 12.
Автореферат разослан «22» мая 2009 г.
| Ученый секретарь диссертационного совета д.м.н. | П.А. Дыбан |
общая характеристика работы
Актуальность проблемы
Одним из перспективных научных направлений, интенсивно развивающихся в мире, является иммунофизиология, рассматривающая процессы взаимодействия нервной и иммунной системы. Особое внимание уделяется роли гипоталамуса в нейроиммунных взаимодействиях, что обуславливается его функциональными особенностями. Как известно, гипоталамус представляет собой центр регуляции многих вегетативных функций, таких как терморегуляция, водно-солевой обмен, пищевое поведение, цикл сон/бодрствование, функций иммунной системы. К настоящему времени открыто и изучено большое количество гипоталамических нейропептидов, принимающих участие в регуляции вегетативных функций организма. Одними из этих нейропептидов являются орексины.
Орексины А и В — нейропептиды, открытые в 1998 году, синтез которых осуществляется небольшой популяцией гипоталамических нейронов от общего пептида-предшественника препроорексина. Орексин-содержащие нейроны участвуют в регуляции различных физиологических процессов (поддержания энергетического баланса, регуляции состояния сна и бодрствования, пищевого поведения, ответных реакций на стресс и восприятие боли) (Beukmann C. et al, 2002; Espana R.A. et al, 2001; Ida T. et al, 1999; Dube M.G. et al, 1999; Ida T. et al., 2000; S. Watanabe et al, 2005; Swanson L.W. et al, 2005).
Основное количество орексин-содержащих нейронов мозга локализовано в перифорникальной зоне латеральной гипоталамической области (Peyron C., 1998). Аксоны этих нейронов достигают различных отделов головного и спинного мозга. Высокая плотность распределения отростков орексин-содержащих нейронов выявлена в гипоталамических структурах (Peyron C., 1998), вовлеченных в регуляцию функций иммунного ответа (переднее гипоталамическое ядро, заднее гипоталамическое поле, латеральная гипоталамическая область и вентро-медиальное гипоталамическое ядро) (Корнева Е.А., Хай Л.М., 1963; Лесников В.А., 1993; Shanin SN et al, 2005; Wenner M. et al, 2000). В этих же структурах локализованы нейроны, имеющие рецепторы к орексину (Hervieu G.J. et al, 2001; Trevedi P., 1998; Taheri S. et al, 1999). Рецепторы к орексину или их мРНК обнаружены и на клетках различных тканей, участвующих в реализации иммунного ответа (клетки селезенки, надпочечников, печени, стволовые клетки фенотипа CD34+) (Randeva H.S. et al, 2001; Zhang S. et al, 2005; Steidl U., 2004).
Установленные к настоящему времени многочисленные факты могут свидетельствовать в пользу возможного участия системы орексин-содержащих нейронов и самого орексина в регуляции функций иммунной системы. Наличие нейро-иммунных взаимодействий не вызывает сомнений, однако механизмы их до сих пор остаются не до конца раскрытыми и нуждаются в дальнейших исследованиях. Известно, что нейроны LHA участвуют в регуляции функций иммунной системы, например, электростимуляция этой области гипоталамуса, где и локализованы орексин-содержащие нейроны, усиливает цитотоксическую активность NK клеток селезенки (Wrona D., 2003; Wenner M. et al, 2000). Нейроны латеральной гипоталамической области также связаны полисинаптически с нейронами, иннервирующими селезенку (Cano G., 2001; Denes A., 2001) и красный костный мозг (Denes A. et al, 2005). Необходимо подчеркнуть, что переднее гипоталамическое ядро, заднее гипоталамическое поле и латеральная гипоталамическая область активируются в первые часы после введения антигенов различной природы, таких как липополисахарид (ЛПС) (Elmquist J.K. et al, 1996; Gaykema R.P.H. et al, 1999; Yi-Hong et al, 2000), столбнячный анатоксин (Корнева ЕА и др., 2001), стафилококковый энтеротоксин В (Gaykema R.P.H. et al, 1998; Goehler L.E. et al, 2001).
Хотя перечисленные факты свидетельствуют в пользу возможного участия орексин-содержащих нейронов и самого орексина в механизмах реализации взаимодействия нервной и иммунной систем, однако прямых доказательств в современной литературе пока не существует. Изучение паттерна активации гипоталамических структур, а также исследование динамики распределения орексин-содежащих нейронов гипоталамуса в первые часы после антигенного воздействия представляется важным этапом для расшифровки этих механизмов на ранней стадии формирования иммунного ответа. Определение уровня экспрессии гена препроорексина в клетках гипоталамуса позволяет проанализировать молекулярные механизмы формирования ответа орексин-содержащих нейронов, вовлекающихся в реакции ЦНС на антигенный стимул.
Цель и задачи исследования
Целью данного исследования явилось изучение реакций орексинэргических нейронов гипоталамуса крыс на введение антигена липополисахарида в различных дозах.
Для реализации этой цели были поставлены следующие задачи:
- Исследовать степень активации клеток и структур гипоталамуса (по выявлению c-Fos белка) через 2 часа после внутривенного введения липополисахарида в дозах 25 и 500 мкг/кг веса животного.
- Исследовать морфо-функциональные характеристики орексин-содержащих нейронов гипоталамуса крыс через 2, 4 и 6 часов после внутривенного введения липополисахарида в дозах 25 и 500 мкг/кг веса животного.
- Исследовать уровень экспрессии гена препроорексина в клетках гипоталамических структур крыс через 2, 4 и 6 часов после внутривенного введения липополисахарида в дозе 25 и 500 мкг/кг веса животного.
Научная новизна работы
Впервые получены данные о степени активации гипоталамических структур в ответ на введение антигена липополисахарида в различных дозах (несептической и субсептической). Показано участие орексин-содержащих нейронов в ответных реакциях ЦНС на антигенное воздействие, а также выявлен дозозависимый характер динамики изменений их морфо-функциональных характеристик. Впервые проведен сравнительный анализ изменений уровня экспрессии гена препроорексина и выявление орексина по иммунореактивности орексин-содержащих нейронов гипоталамических структур после введения антигена.
Теоретическая и практическая значимость работы
Полученные в работе данные значимы для раскрытия центральных механизмов нейроиммунных взаимодействий и являются важным этапом в изучении процесса реализации реакции ЦНС на антигенное воздействие, что создает основу для поиска путей коррекции нарушений процессов взаимодействия нервной и иммунной систем.
Результаты работы расширяют и дополняют сложившиеся в настоящее время представления о морфо-функциональных особенностях системы орексинэргичеких нейронов и могут быть использованы в научной практике, связанной с исследованием клеточных и молекулярных механизмов формирования реакций организма на антигенное воздействие, а также могут быть включены в курс преподавания по физиологии, патофизиологии, нейрофизиологии и иммунологии.
Основные положения, выносимые на защиту
- Внутривенного введение антигена липополисахарида в дозах 25 и 500 мкг/кг веса животного приводит к активации гипоталамических структур (AHN, PVH, VMH, DMH, LHA, PH), паттерн которой различен, что проявляется индукцией синтеза c-Fos белка в клетках этих структур.
- Орексин-содержащие нейроны вовлекаются в ответные реакции ЦНС на введение липополисахарида, что проявляется изменением иммунореактивности этих нейронов, а пространственно-временная динамика изменений их морфо-функциональных характеристик зависит от дозы вводимого антигена.
- Внутривенное введение липополисахарида приводит к активации экспрессии гена препроорексина в клетках гипоталамуса через 2 часа после введения липополисахарида в дозах 25 и 500 мкг/кг веса животного.
Структура и объем работы
Диссертация изложена на 109 страницах машинописного текста и состоит из введения, обзора литературы, описания материала и методов работы, результатов собственных исследований и их обсуждения, выводов и списка цитируемой литературы, из них отечественных — 13 и 214 — зарубежных авторов. Работа проиллюстрирована 25 рисунками и 6 таблицами.
Апробация работы
Материалы исследования изложены в 12 публикациях, в том числе представлены на Российских и Международных конференциях: Х Всероссийский научный форум Дни иммунологии в Санкт-Петербурге (Санкт-Петербург, 29 мая – 1 июня 2006); International Symposium Interaction of the nervous and immune systems in health and disease (Saint-Petersburg, 31 May - 2 June 2007); ХХ съезд физиологического общества имени И.П. Павлова (Москва, 4-8 июня 2007); Объединенный иммунологический форум (Санкт-Петербург, 30 июня – 5 июля 2008); Международная конференция Физиология и патология иммунной системы (Москва, 14-17 сентября 2008).
материалы и методы исследования
Экспериментальные животные и схема эксперимента
Работа выполнена на 126 крысах, взрослых самцах породы Wistar, весом 250-300 г., адаптированных к условиям эксперимента. Животных содержали в условиях вивария при комнатной температуре с 12-часовым циклом свет/темнота, свободным доступом к воде и пище, на стандартной диете в соответствии с нормами содержания лабораторных животных.
В качестве тимус-независимого антигена, обладающего высокой степенью иммуногенности, использовали липополисахарид (ЛПС) (E.coli 055:B5, Sigma, L2880).
Дозы были подобраны так, чтобы в одном случае (25 мкг/кг веса животного) не вызывать синтез антител, определяемый методом пассивной гемагглютинации, а в другом случае (500 мкг/кг веса животного) приводить к достаточному для определения указанным методом синтезу антител (титр 1/64).
Все инъекции проводили в 11 часов утра с целью нивелирования различий, связанных с суточными колебаниями содержания орексина в гипоталамусе (Taheri S. et al, 2000). Крысам внутривенно вводили 200 мкл ЛПС в дозе 25 или 500 мкг/кг веса. Контролем служили животные, которым внутривенно вводили физиологический раствор в том же объеме.
Экспериментальные группы:
- Группа 1. Интактные животные.
- Группа 2. Контрольные животные, которым внутривенно вводили 200 мкл физиологического раствора.
- Группа 3. Животные, которым внутривенно вводили 25 мкг/кг липополисахарида.
- Группа 4. Животные, которым внутривенно вводили 500 мкг/кг липополисахарида.
Выведение животных из эксперимента проводили в 11 часов, а также через 2, 4 и 6 часов после инъекции.
Иммуногистохимическое окрашивание.
Выявление c-Fos- и орексин-позитивных нейронов проводили иммуногистохимичеким методом на фронтальных замороженных срезах мозга (30 мкм). Для выявления c-Fos белка использовали первичные кроличьи поликлональные антитела к семейству c-Fos белков (Santa-Cruz, Biotech.Inc.) и вторичные антитела к кроличьим иммуноглобулинам (IgG), меченые пероксидазой (Sigma). Выявление орексина осуществляли авидин-биотиновым методом. В качестве первичных антител использовали кроличьи антитела к орексину А (Sigma), в качестве вторичных — моноклональные антитела к кроличьим иммуноглобулинам (клон RG-16), конъюгированные с биотином (Sigma), детекцию которых проводили с помощью авидин-пероксидазной метки (Sigma). Визуализацию иммуногистохимической реакции проводили раствором диаминобензидина.
Подсчет количества клеток.
Подсчет c-Fos-позитивных клеток производили, используя систему Иста-Видео-Тест. Срезы мозга исследовали при 40-кратном увеличении светового микроскопа. С помощью компьютерной программы Иста-Видео-Мастер определяли площадь клеток и среза, на которой проводили подсчет клеток и оптическую плотность окраски клеток и фона для каждого среза. При анализе количества c-Fos позитивных клеток учитывали только те клетки, оптическая плотность которых превышала окраску фона, как минимум, в 1,25 раза и выше, а площадь превышала 10 мкм2. Для сопоставления количества c-Fos позитивных клеток, данные количественных подсчетов пересчитывали на унифицированную площадь, равную 10000 мкм2. Сравнительный анализ степени активации структур гипоталамуса по экспрессии c-Fos-подобного белка проводили по оценке относительного коэффициента активации (ОКА), а также по показателю относительной оптической плотности (ООП), которые высчитывали по формулам:
ОКА=
ООП=
Подсчет орексин-позитивных нейронов осуществляли при 10-кратном увеличении светового микроскопа на всей площади срезов 26-32 уровней. Количество орексин-содержащих нейронов широко варьирует у каждого животного на различных срезах мозга, полученных с одного уровня. Для того чтобы минимизировать случайные ошибки, возникающие при изготовлении срезов, в исследовании учитывали количество орексин-содержащих нейронов на всех срезах мозга конкретного животного.
Полимеразно-цепная реакция в режиме реального времени.
Для постановки полимеразно-цепной реакции в режиме реального времени (RT-PCR) животных декапитировали и сразу извлекали гипоталамус.
- Выделение пула РНК клеток гипоталамуса производилось с помощью набора «Aurum Total RNA Fatty and Fibrous Tissue Pack» (Bio-Rad).
- Реакция синтеза к-ДНК/Обратная Транскрипция (ОТ) осуществлялась с использованием реактивов, поставленных компанией «МедиГен».
- Полимеразная Цепная Реакция в Реальном Времени (RT-PCR):
Для проведения реакции использовались праймеры:
— к последовательности, кодирующей препроорексин (Ox):
Прямой: 5’-TGT CGC CCA GAA GAC GTG TTC CTG-3’
Обратный: 5’-AAG ACG GGT TCA CAC TCT GGA TC-3’
Температура отжига: 61°С, длина продукта – 287 пар нуклеотидов.
— к последовательности кодирующей глицеральдегид-3-фосфат дегидрогеназу (GAD):
Прямой: 5’-CCA CTC AGA AGA CTG TGG AT-3’
Обратный: 5’-GTC ATC ATA CTT GGC AGG TT-3’
Температура отжига: 55°С, длина продукта – 224 пары нуклеотидов.
Праймеры были произведены лабораторией «СинТол».
Наблюдение за ходом реакции и регистрацию данных производили с помощью компьютерной программы «Opticon Monitor 3.1».
Уровень экспрессии гена препроорексина определяли относительно уровня экспрессии гена глицеральдегид-3-фосфат дегидрогеназы и высчитывали по следующей формуле:
IOx= EOx^C(t)Ox/EGAD^C(t)GAD
где: IOx – относительный уровень экспрессии гена препроорексина, выраженный в долях от уровня экспрессии гена глицеральдегид-3-фосфат дегидрогеназы.
E – эффективность протекания реакции в конкретной пробе.
C(t) – пороговый показатель циклов (количество циклов необходимое для достижения порогового значения флюоресценции).
Эти параметры были рассчитаны встроенным программным обеспечением амплификатора.
Электрофорез в агарозном геле.
Контроль специфичности полученного после ПЦР продукта осуществляли при помощи электрофореза в агарозном геле. Для постановки электрофореза амплифицированных фрагментов готовили 2% агарозу на 1хТАЕ буфере. В качестве электродного буфера использовали 1хТАЕ буфер. Электрофоретическое разделение проводили в направлении от катода к аноду при напряженности электрического поля 10 В/см геля в течение 30-40 мин. По окончанию разделения гель фотографировали при помощи установки для документации результатов ПЦР-анализа (Gel Imager) с использованием трансиллюминатора с длиной волны 260-340 нм.
Статистическая обработка данных
Для статистической обработки полученных результатов были использованы программы Statistica и SPSS 11.0, а также пакет программ Microsoft Office 2003. Сравнение групп экспериментальных животных проводили при помощи t-критерия Стьюдента. Для сравнения количества орексин-содержащих нейронов на срезах мозга использовали средние взвешенные величины, а также осуществляли ранжирование срезов по количеству клеток и строили кривые распределения для каждой экспериментальной группы животных.
результаты исследования и их обсуждение
Количество c-Fos-позитивных нейронов гипоталамуса после введения липополисахарида.
Активацию гипоталамических структур оценивали по наличию белка c-Fos в нейронах. Количество c-Fos-позитивных клеток определяли в латеральной гипоталамической области (LHA), где локализовано наибольшее количество орексин-содержащих нейронов, а также в структурах с высокой плотностью рецепторов к орексину и орексин-содержащих отростков: паравентрикулярном (PVH), переднем гипоталамическом (AHN), дорзомедиальном (DMH), вентромедиальном (VMH) ядрах и заднем гипоталамическом поле (PH) (рис. 1).
У животных, которым внутривенно вводили антиген (ЛПС) в дозе 25 мкг/кг, происходило увеличение числа активированных нейронов во всех исследуемых структурах гипоталамуса. Инъекции большей дозы ЛПС приводили к увеличению активации нейронов AHN, PVH, LHA и PH; уровень активации в VMH и DMH не отличался от уровня активации этих структур у животных после введения физиологического раствора (рис. 2). Поскольку по абсолютному количеству c-Fos-позитивных клеток нельзя сравнить между собой различные гипоталамические структуры по степени активации, сравнение проводилось по относительному коэффициенту активации (ОКА). Высокий уровень активации нейронов после введения ЛПС в дозе 25 мкг/кг констатирован в AHN, PVH, LHA и PH. Введение 500 мкг/кг ЛПС приводит к более выраженному ответу только в AHN, PVH и LHA (рис. 3, 4). Таким образом, можно предположить, что степень активации клеток гипотоламических структур зависит от дозы вводимого препарата. Как известно, введение ЛПС инициирует развитие комплекса системных ответов организма (активацию гипоталамо-гипофизарно-адреналовой оси, лихорадку, изменение пищевого поведения), в процесс регуляции которых вовлечены указанные гипоталамические структуры. Отличие в паттерне их активации при введении различных доз ЛПС, вероятно, может быть связано с разной интенсивностью иммунных процессов, развивающихся в ответ на введение антигена в разных дозах и возможно, определяющих различную степень и паттерн активации структур ЦНС.
Для выяснения морфо-функциональных особенностей нейронов участвующих в механизмах реализации реакций мозга на антиген проведено ранжирование c-Fos-позитивных клеток, локализованных в LHA согласно их размерам. При введении малой дозы ЛПС происходит в основном активация клеток меньших размеров (10–50 мкм2; класс 1, 2), соответствующих нейронам ассоциативного типа, аксоны которых проецируются на клетки, расположенные внутри данной структуры, в то время как при введении 500 мкг/кг ЛПС наблюдается активация и более крупных клеток (>50 мкм2; класс 3 и выше), в том числе, клеток релейного типа (70–150 мкм2), образующих проекции вне LHA (рис. 5), что обуславливает возможность передачи сигнала к другим структурам мозга, и формированию системного ответа, характерного для реакции на введение ЛПС.
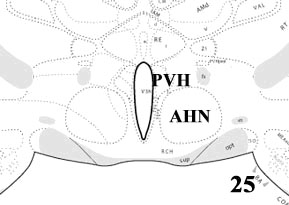
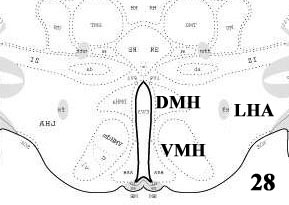
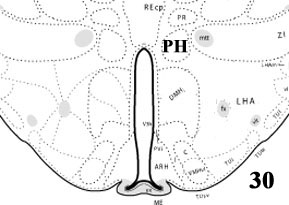
Рисунок 1. Схемы гипоталамуса мозга крысы на 25, 28 и 30 уровнях.
AHN — переднее ядро; PVH — паравентрикулярное ядро; LHA — латеральная гипоталамическая область; DMH — дорзомедиальное ядро; VMH — вентромедиальное ядро;PH — заднее ядро (Swanson, 2004).
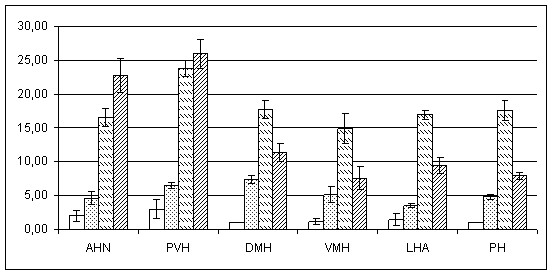
Рисунок 2. Количество c-Fos позитивных клеток в гипоталамаческих структурах мозга крыс после введения ЛПС.
По оси абсцисс — структуры гипоталамуса.
По оси ординат — количество c-Fos-позитивных клеток на 10000 мкм2 среза мозга
Группы животных:
![]() — интактные
— интактные
после введения:
![]() —физиологического раствора
—физиологического раствора
![]() —25 мкг/кг липополисахарида
—25 мкг/кг липополисахарида
![]() —500 мкг/кг липополисахарида
—500 мкг/кг липополисахарида
* — P<0,01; ** — P<0,05 по отношению к их количеству у животных после введения физиологического раствора;
# — P<0,01; ## — P<0,05 по отношению к их количеству у животных после введения 25 мкг/кг ЛПС;
† — P<0,05 по отношению к их количеству у интактных животных.
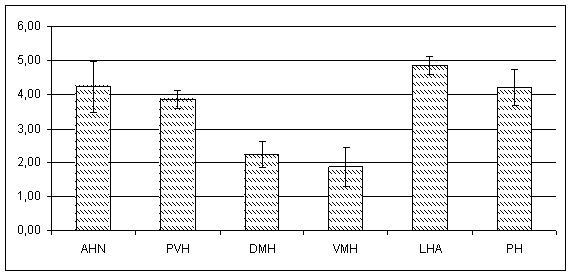
Рисунок 3. Относительные коэффициенты активации гипоталамических структур мозга крыс после введения ЛПС (25 мкг/кг).
По оси абсцисс — структуры гипоталамуса.
По оси ординат — относительный коэффициент активации гипоталамических структур по количеству c-Fos-позитивных клеток на 10000мкм2.
* — P<0,01; ** — P<0,05 по отношению к значению ОКА VMH и DMH;
# — P<0,05 — P<0,05 по отношению к значению ОКА PVH
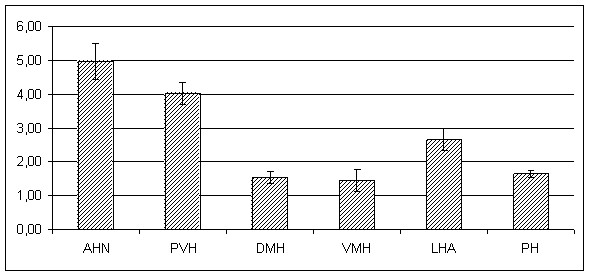
Рисунок 4. Относительные коэффициенты активации гипоталамических структур мозга крыс после введения ЛПС (500 мкг/кг).
По оси абсцисс — структуры гипоталамуса.
По оси ординат — относительный коэффициент активации гипоталамических структур по количеству c-Fos-позитивных клеток на 10000мкм2.
* — P<0,01 по отношению к значению ОКА DMH, VMH, LHA, PH;
# — P<0,05 по отношению к значению ОКА DMH, VMH, PH
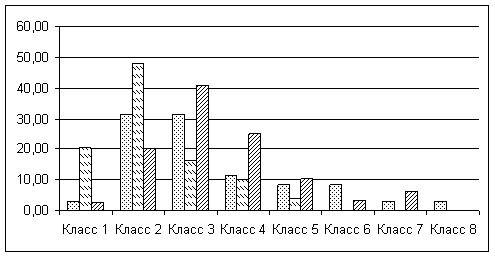
Рисунок 5. Распределение c-Fos позитивных клеток LHA, ранжированных согласно их площади, после введения ЛПС.
По оси абсцисс — классы c-Fos позитивных клеток:
| Класс 1 — 10-30 мкм2 | Класс 5 — 91-110 мкм2 |
| Класс 2 — 31-50 мкм2 | Класс 6 — 111-130 мкм2 |
| Класс 3 — 51-70 мкм2 | Класс 7 — 131-150 мкм2 |
| Класс 4 — 71-90 мкм2 | Класс 8 — 151-170 мкм2 |
По оси ординат — % c-Fos-позитивных клеток определенного класса.
Животные после введения:
![]() — физиологического раствора
— физиологического раствора
![]() — ЛПС (25 мкг/кг)
— ЛПС (25 мкг/кг)
![]() — ЛПС (500 мкг/кг)
— ЛПС (500 мкг/кг)
Орексин-позитивные нейроны гипоталамуса после введения ЛПС.
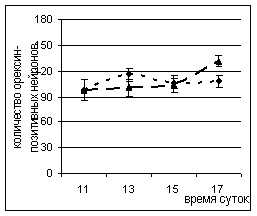
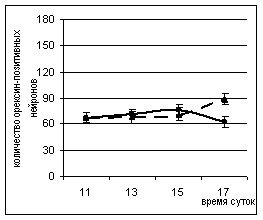
Количество орексин-позитивных нейронов определяли на срезах мозга с 24 по 34 уровень (рис. 6). Так как в литературе имеются данные об изменении количества мРНК препроорексина в орексин-содержащих нейронах гипоталамуса в течение суток (Taheri S. et al, 2000), то предварительно было проведено определение распределения орексин-содержащих нейронов в гипоталамусе интактных крыс в различное время дня (11, 13, 15 и 17 часов), но изменений количества орексин-позитивных нейронов мы не выявили. Для дальнейшего анализа были выбраны срезы 28, 29 и 30 уровней (по атласу Swanson’s), так как на этих уровнях локализовано наибольшее количество клеток, содержащих орексин.
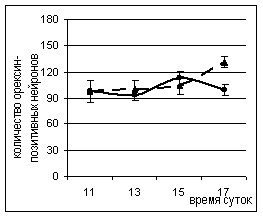
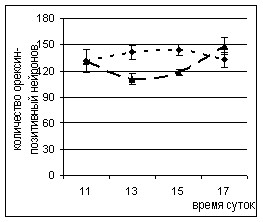
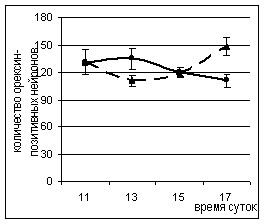
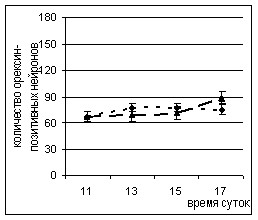
Введение малой дозы ЛПС (25 мкг/кг) привело к изменению количества орексин-позитивных нейронов. Через 2 и 4 часа после введения ЛПС наблюдалось увеличение количества орексин-позитивных нейронов на срезах мозга 29 уровня, а через 6 часов — снижение их числа на срезах мозга 28 уровня (рис. 7). После введения ЛПС в дозе 500 мкг/кг на срезах мозга 29 уровня через 2 часа наблюдалась только тенденция к увеличению количества орексин-позитивных нейронов, и лишь через 6 часов после введения данной дозы антигена было выявлено уменьшение их числа на всех анализируемых уровнях (рис. 7).
Выявленную закономерность подтвердило и сравнение усредненных кривых распределения количества орексин-позитивных нейронов на срезах мозга у животных всех групп (рис 8, 9).
Через 2 и 4 часа после введения ЛПС в дозе 25 мкг/кг кривые распределения количества орексин-позитивных нейронов на срезах мозга 29 уровня сдвигаются в сторону больших величин по сравнению с кривыми их распределения у животных после введения физиологического раствора, что обусловлено преобладанием срезов мозга с большим количеством орексин-позитивных нейронов у животных после введения данной дозы ЛПС (рис 8). После введения ЛПС в дозе 500 мкг/кг также выявлено смещение кривых распределения в сторону больших значений по сравнению с кривыми их распределения у животных после введения физиологического раствора, хотя при сравнивании этих групп животных по средним величинам была выявлена только слабая тенденция (P=0,09) к увеличению количества орексин-позитивных нейронов.
Через шесть часов после введения ЛПС в дозе 25 мкг/кг кривые распределения количества орексин-позитивных нейронов на срезах мозга только 28 уровня, а при введении ЛПС в дозе 500 мкг/кг – 28, 29 и 30 уровней, сдвигаются в сторону меньших величин по сравнению с кривыми их распределения после введения физиологического раствора, что определяется превалированием срезов мозга с меньшим количеством орексин-позитивных нейронов у животных данных экспериментальных групп (рис 9).
Изменения количества орексин-позитивных нейронов отражают различия в содержании орексина в этих клетках, достаточное или недостаточное для иммуногистохимического выявления орексин-содержащих нейронов в гипоталамических структурах на срезах мозга. Изменения содержания орексина в нейронах могут быть обусловлены смещением баланса процессов его синтеза и потребления. Повышение содержания орексина в нейронах может быть следствием как возросшего синтеза этого нейропептида, так и снижением его утилизации. Соответственно уменьшение содержания орексина в нейронах может объясняться либо его сниженным синтезом, либо усилившимся потреблением. Определение уровня экспрессии гена препроорексина дает возможность достаточно определенно судить, какой из указанных механизмов лежит в основе выявленных изменений.

Рисунок 6. Распределение орексин-содержащих нейронов в гипоталамусе крыс Wistar.
Представлены схемы срезов 24-34 уровней мозга. (Swanson’s, 2004).
Точками указаны орексин-содержащие нейроны, цифры на схемах соответствуют уровням срезов.
A B
C D
E F
Рисунок 7. Динамика изменения количества орексин-позитивных нейронов в гипоталамических структурах на срезах мозга через 2, 4 и 6 часов после введения ЛПС.
Введение физиологического раствора и ЛПС проводили в 11.00.

