Дмитриев виктор александрович сравнительная характеристика фармакокинетики, клинической эффективности и безопасности генерических препаратов диклофенака и ибупрофена
НА ПРАВАХ РУКОПИСИ
ДМИТРИЕВ
Виктор Александрович
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА ФАРМАКОКИНЕТИКИ, КЛИНИЧЕСКОЙ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ ГЕНЕРИЧЕСКИХ ПРЕПАРАТОВ ДИКЛОФЕНАКА И ИБУПРОФЕНА
14.00.25 – фармакология, клиническая фармакология
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Москва-2008
Работа выполнена в филиале «Клиническая фармакология» ГУ Научный центр биомедицинских технологий РАМН
Научные руководители:
Доктор фармацевтических наук Кондратенко Светлана Николаевна
доктор медицинских наук Сычев Дмитрий Алексеевич
Официальные оппоненты:
Член - корреспондент РАМН, доктор медицинских наук, профессор
Гуськова Татьяна Анатольевна.
Академик РАМН, доктор медицинских наук, профессор Палеев Николай
Романович.
Ведущая организация: ГОУ ДПО Российская академия последипломного
образования
Защита состоится «__» __________ 2008 года в ___ часов на заседании Диссертационного совета Д 208.040.13 при Московской медицинской академии им. И.М. Сеченова (119991, г. Москва, ул. Трубецкая, д. 8, стр.2)
С диссертацией можно ознакомиться в библиотеке Московской медицинской академии им. И.М. Сеченова (117198, г. Москва, Нахимовский проспект, д.49)
Автореферат разослан «___» _____________2008 года.
Ученый секретарь
Диссертационного Совета Д.208.040.13
кандидат медицинских наук, доцент Архипов Владимир Владимирович
Общая характеристика работы
Актуальность темы
Нестероидные противовоспалительные средства (НПВС) являются наиболее широко назначаемой группой лекарств во всем мире. Ежедневно свыше 30 млн. людей в мире принимают какой-либо НПВС, из них 40% — в возрасте старше 60 лет. Рекомендованый перечень основных (жизненно необходимых) лекарственных средств ВОЗ (Essential Drug List. WHO, 1999) включает в себя два НПВС: диклофенак и ибупрофен.
Эксперты разных стран едины во мнении, что различия в эффективности НПВС, как обезболивающих препаратов относительно невелики (Fries J. F., Williams C. A., Bloch D. A., 1991). Обзоры нескольких десятков клинических испытаний различных НПВС при остеоартрозе и ревматоидном артрите не дают оснований ранжировать эти лекарства по степени их эффективности (Fries J., 1996).
Если эффективность НПВС примерно одинакова, то основанием для их выбора мог бы стать профиль безопасности. Прием НПВС является одной из самых частых причин развития НЛР, прежде всего из-за высокой частоты их применения как по назначению врача, так и в качестве средств самолечения. Так, в Великобритании НПВС составляют 5% всех назначаемых лекарств, однако на их долю приходится 25% всех НЛР, о которых сообщается в Комитет по безопасности медикаментов. В тоже время, по официальным оценкам, в Великобритании 3-4 тыс. смертельных случаев ежегодно обусловлены НЛР НПВС. В США использование НПВС ежегодно приводит к более 70 тыс. госпитализаций и 7 тыс. смертельных случаев. В России рынок НПВС представлен главным образом генерическими препаратами. Таким образом, актуальным предоставляется сравнительное изучение фармакокинетики, клинической эффективности и безопасности именно генерических препаратов ННВС.
Цель исследования
Оценить фармакокинетические параметры, клиническую эффективность и безопасность генерических препаратов диклофенака и ибупрофена у больных с остеоартрозом и ревматоидным артритом.
Задачи исследования
- Изучить биоэквивалентность генерических препаратов диклофенака и ибупрофена по сравнению с оригинальными препаратами.
- Сопоставить клиническую эффективность генерических препаратов диклофенака и ибупрофена у больных с остеоартрозом и ревматоидным артриротом
- Изучить потенциал антиоксидантнго действия генерических препаратов диклофенака и ибупрофена у больных с ревматоидным артритом.
- Сопоставить параметры безопасности в отношении развития гастротоксичности генерических препаратов диклофенака и ибупрофена у больных с остеоартрозом и ревматоидным артриротом
Научная новизна
Впервые были сопоставлены параметры безопасности в отношении развития гастротоксичности при применении генерических препаратов диклофенака и ибупрофена.
Впервые оценен антиоксидантный потенциал генерических препаратов диклофенака и ибупрофена, по результатам анализа изменения концентрации МДА в сочетании с комплексом параметров, характеризующих антиоксидантную систему клетки.
Впервые исследована биоэквивалентность новых генерических препаратов диклофенака и ибупрофена по сравнению с оригинальными препаратами.
Практическая значимость
Полученные результаты позволяют рекомендовать назначение диклофенака больным с остеоартрозом и ревматоидным артритом для лечения болевого синдрома, при отсутствии поражения ЖКТ, как наиболее эффективный обезболивающий препарат. Назначение ибупрофена рекомендуется при сочетанной патологии: остеоартроз и ревматоидный артрит, при сопутствующей патологии ЖКТ, как наиболее безопасный препарат.
На основании полученных результатов биоэквивалентности, исследуемые генерические препараты могут быть рекомендованы к медицинскому применению, что позволит расширить арсенал доступных генерических препаратов из группы НПВС.
Внедрение в практику
Полученные фармакокинетические данные вошли в нормативную документацию на генерические препараты Ортофер и Ибупрофен-Хемафарм, на основании чего препараты были зарегистрированы в РФ и разрешены к применению в клинической практике. Клинические исследования эффективности указанных ЛС позволяют применять в качестве средств симптоматической терапии у больных с деформирующим остеоартрозом и ревматоидным артритом в практическом здравоохранении России.
Личный вклад соискателя
Соискателем лично осуществлялся отбор добровольцев для проведения фармакокинетических исследований, разработана методология исследования клинической эффективности изучаемых препаратов у больных с деформирующим остеоартрозом и ревматоидным артритом, проведено обобщение и статистическая обработка полученных в ходе исследований результатов. Количественный анализ изучаемых ЛС в плазме крови проводился в Филиале «Клиническая фармакология» НЦ БМТ РАМН.
Апробация работы
Результаты проведенных исследований были представлены на XI и XII Российских конгрессах «Человек и лекарство» (Москва, 2004, 2005); апробация работы проведена на совместной научно-практической конференции Филиала «Клиническая фармакология» Научного центра «Биомедицинских технологий» РАМН и ГКБ № 23 им. «Медсантруд» г. Москвы 19 октября 2007 года.
Публикации
Основные положения диссертации опубликованы в 8 работах, 1 из них в журнале, рекомендованном ВАК.
Основные положения, выносимые на защиту
- Генерические препараты ибупрофена (Ибупрофен-Хемофарм) и диклофенака (Ортофер) биоэквиваленты соответствующим оригинальным препаратам.
- Генерический препарат диклофенака превосходит по анальгетической эффективности генерический препарат ибупрофена, но уступает ему по профилю безопасности.
Структура и объем диссертации
Диссертация (123 страницы текста) состоит из введения, обзора литературы, описания материалов и методов исследования, результатов исследования, обсуждения результатов, заключения, выводов, практических рекомендаций, списка литературы, включающего 182 источников (83 на русском и 99 на иностранных языках). Работа проиллюстрирована 30 таблицами и 45 рисунками.
материалы и методы исследования
Проведение исследования одобрено Комитетом по этике при Федеральном органе контроля качества, эффективности, безопасности лекарственных средств (выписки из протоколов №32 от 18.12.2002 и №38 от 09.06.2003).
Для решения поставленных задач проанализированы 278 карт обследования больных. По карте обследования было предусмотрено, что оценка эффективности и безопасности проводимых методов лечения проводилась непосредственно сразу по окончанию терапии, а также через 1, 2 недели, через каждые 4 недели на протяжении 24 недель для больных с ревматоидным артритом, 8 недель – для больных с остеоартрозом коленных суставов.
Проанализированы данные с целью оценки эффективности и переносимости препаратов ибупрофена и диклофенака, у больных остеоартрозом коленных суставов в течение 2-месячного периода наблюдения. Исследовано 160 амбулаторных пациентов (67 мужчин и 93 женщины) в возрасте 45-75 лет. Всем больным проводилась рентгенография суставов для определения стадии остеоартроза, стадия устанавливалась согласно классификации Kellgren-Lawrence. У всех больных был верифицирован остеоартроз коленного сустава I-III рентгенологической стадии, длительность заболевания составляла в среднем 8,5 лет.
Для определения активности ревматоидного артрита использовался комплексный подход, основанный на одновременной регистрации следующих показателей: число болезненных при пальпации суставов, число припухших суставов, продолжительность утренней скованности, оценку выраженности артралгий, общую оценку активности заболевания больным и врачом (тест Lee, опросник состояния здоровья — НАQ), результаты определения функции суставов и лабораторные данные (один из острофазовых показателей). Признаки, входящие в состав объединенных показателей, оценивались суммарно или по отдельности. Так же был использован показатель активности болезни — disease activity score. Наличие и динамику внесуставных проявлений оценивали клинически, а также рентгенологическими и ультразвуковыми методами. Лабораторно определяли уровень С-реактивного белка, биохимические показатели крови, параметры ПОЛ: уровень МДА, ВГ, активности СОД, ГР в сыворотке крови.
Для оценки безопасности препаратов использовали результаты проведенной ранее эзофагогастродуоденоскопии.
Концентрацию НПВС в плазме крови пациентов определяли методом ВЭЖХ с УФ-спектрофотометрическим детектированием. Диклофенак натрия и ибупрофен выделяли из биожидкости методом жидкофазной экстракции с применением хлороформа и дихлорметана соответственно. Полученные экстракты упаривали под вакуумом, сухой остаток растворяли в элюенте, аликвоту наносили на обращеннофазную хроматографическую колонку. В качестве мобильной фазы для диклофенака использовалась смесь ацетонитрила и 0,2М раствора натрия дигидрофосфата в объемном соотношении 40:60, а для ибупрофена – 69% раствор метанола, подкисленный до рН=3,0. Скорость элюирования составляла 1 мл/мин. Детектирование осуществлялось при длине волны 280 и 222 нм соответственно. Количественное определение проводилось методом абсолютной калибровки по площади пиков. В диапазоне терапевтических концентраций калибровочная зависимость имела линейный характер.
Фармакокинетические параметры рассчитывали с помощью программы KineticaTM 2000 модельно-независимым методом.
Исследование биоэквивалентности проводили согласно общепринятым рекомендациям в соответствии с протоколом, утвержденным на заседании специализированной комиссии Фармакологического комитета по клинической фармакологии у 18 здоровых добровольцев (в ГКБ №23 им «Медсантруд» г. Москвы). Прием препаратов осуществлялся однократно перорально в 8 часов утра одного из препаратов. Исследуемые препараты вводили по перекрестной схеме. Концентрацию препаратов в плазме крови добровольцев определяли с помощью методик ВЭЖХ, разработанных в ИКФ ФГУ НЦ ЭСМП Росздравнадзора.
Результаты исследования обрабатывали методами вариационной статистики; достоверность различий показателей между группами оценивали по t-критерию Стьюдента. Полученные фармакокинетические экспериментальные данные были подвержены статистической обработке с помощью дисперсионного анализа (ANOVA).
результаты исследования и их обсуждение
1. Оценка эффективности препаратов диклофенак и ибупрофен.
1.1 Анализ динамики клинических и лабораторных показателей активности воспалительного процесса, полученных при применении диклофенака и ибупрофена для лечения больных ревматоидным артритом.
Анализ карт обследования больных. Оказалось, что при лечении больных ревматоидным артритом 1 и 2 степени активности препаратами диклофенака и ибупрофена на протяжении 24 недель болевой суставной синдром имел регрессионный характер, что является критерием эффективности проводимого лечения. Снижение боли в мм по визуальной аналоговой шкале (ВАШ) в группе применения диклофенака отметили 46% пациентов через 4 недели. Интегральный показатель в эти сроки достиг абсолютного значения 47,4±22,1 мм, снизившись в среднем на 17,4% (р<0,05) от исходного уровня. Сопоставимый результат достигнут в группе применения ибупрофена.
Через 4 недели отмечено снижение уровня боли в мм по ВАШ на 16,1%. В последующем анальгетическое действие препаратов реализовывалось постепенно, с достижением хорошего обезболивающего эффекта в группе применения диклофенака к 12 неделе лечения. Процент снижения к исходному уровню составил в среднем 39,2 (р<0,01). В группе использования ибупрофена в эти же сроки сравниваемый показатель составил 33,2±23,1 мм, снизившись от исходного уровня на 42,2% (р<0,01). К 24 недели проводимой терапии 61% пациентов, принимавших диклофенак, и 65% пациентов, принимавших ибупрофен, отметили субъективно уменьшение боли.
Полученные при анализе показателя боли в мм по ВАШ данные на фоне применения в качестве препаратов лечения исследуемых диклофенака и ибупрофена соответствуют по литературным источникам достижению хорошего эффекта терапии, т.к. уровень 50-70% уменьшения значения этого показателя свидетельствует о хорошем эффекте терапии, с тенденцией к приближению к очень хорошему эффекту - >70%.
Продолжительность утренней скованности составила 143±152 мин. К окончанию первого месяца лечения скованность уменьшилась по продолжительности в группе применения диклофенака у 43% пациентов, в группе применения ибупрофена - у 51%. При этом среднее значение процента снижения продолжительности утренней скованности в группе применения диклофенака составило 41,3% (р<0,05), а в группе применения ибупрофена - 35,7% (р<0,05). В последующем сохранялось умеренное снижение продолжительности утренней скованности линейного характера вплоть до 24 недели исследования. Показатели уровня боли в мм по ВАШ и продолжительности утренней скованности достоверно коррелировали ( r = 0,95; р<0,05). При этом исследуемый параметр, также как и уровень боли по ВАШ, достиг достоверно значимого уровня снижения уже к окончанию 12 недели. На 12 и 24 неделе в группе применения диклофенака 53% и 62% пациентов соответственно отметили уменьшение продолжительности и выраженности утренней скованности суставов. В группе применения ибупрофена в сопоставимые сроки аналогичное улучшение отметили 56% и 66% пациентов.
Анализируя динамику снижения СОЭ выявлено умеренное уменьшение значения этого показателя активности воспалительного процесса у большинства больных ревматоидным артритом. Исходная СОЭ до лечения в среднем составила 37,2 мм/час, что соответствует 2 степени лабораторной активности ревматоидного артрита. При применении диклофенака отмечается снижение СОЭ на 22,7 - 24,5% в первые 4-12 недель лечения и на 32,8-35,5% в последующие 16-24 недели. К окончанию срока исследования у 8 (20,5%) пациентов достигнута нормализация значения показателя СОЭ (<16 мм/час), у 19 (48,7%) - СОЭ снизилась. При этом имели абсолютное значение СОЭ до 25 мм/час 8 (20,5%) пациентов, до 30 - 6 (15,4%). У 4 пациентов СОЭ повысилась. Достоверное снижение СОЭ при применении диклофенака свидетельствует о терапевтической эффективности проводимого лечения, однако средние значения СОЭ в различных сроках исследования: 28,1 - 25,0 - 23,8 - 24,0 мм/час - не позволяют сделать выводы о переходе на фоне лечения диклофенаком активности ревматоидного артрита в категорию с меньшей степенью выраженности лабораторных проявлений воспаления.
При использовании ибупрофена СОЭ снизилась в среднем на 32% (р<0,01) на 12 неделе лечения, и эти уровни значения показателя сохранялись до 24 недели с небольшими (±2,5 3,5%) колебаниями в различные сроки проводимого исследования. У 11 (26,8%) отмечалась уже к 12 недели нормализация СОЭ (<20 мм/час). У 9 (23%) пациентов СОЭ практически не снизилась на протяжении всего исследования с колебаниями каждые 4 недели на ±3-6 мм/час. У 6 (14,6%) мы отметили незначительный рост СОЭ (на 3-5 мм/час) не линейного характера в различные сроки исследования.
В обеих группах большинство больных отметили удовлетворительный эффект. В анализе терапевтической эффективности проводимого лечения ревматоидного артрита в качестве универсального инструмента используют показатель активности болезни - disease activity score (DAS).
При применении в качестве препарата лечения диклофенака достоверно отмечается линейное снижение значения показателя DAS28 до 16 недели: через 4 недели - на 12,9% (р<0,05), через 8 - на 20,1% (р<0,05), через 12 - на 22,8%, через 16 - на 27,8% (р<0,05). В последующие сроки динамика снижения значения показателя DAS28 сохраняет линейный характер, достигая абсолютного значения 4,51±6,2 в конце 24 недели лечения, оказываясь таким образом ниже исходного уровня (6,37±3,16 - значения показателя до лечения) на 29,2% (р<0,01).
При применении в качестве препарата лечения ибупрофена нами выявлено достоверное линейное снижение значения показателя DAS28 до 24 недели: через 4 недели отмечается снижение величины DAS28 на 7,7%, через 8 - на 11,9% (р<0,05), через 12 - на 19,2% (р<0,05), через 16 - на 21% (р<0,05), через 20 - на 24,8%, через 24 - на 27,2% (р<0,05), достигая абсолютного значения 4,64±5,04. Таким образом, на фоне применения в качестве препаратов лечения диклофенака и ибупрофена отмечается достоверное уменьшение активности ревматоидного артрита по показателю DAS28 на 29,2 и 27,2% соответственно, что позволяет сделать вывод о сопоставимой терапевтической эффективности исследуемых лекарственных средств. Однако на фоне применения диклофенака клинико-лабораторное улучшение у пациентов достигнуто на 8 недель раньше, чем при использовании ибупрофена.
При применении в качестве препарата лечения диклофенака достоверно отмечалось линейное снижение значения показателя ПВА до 16 недели: через 4 недели - на 24,6%, через 8 - на 37,8%, через 12 - на 42,9%, через 16 - на 51,5%. DAS 28 и ПВА достоверно коррелировали между собой (r = 0,88, р <0,01). В последующие сроки динамика снижения значения показателя ПВА утрачивает линейный характер, достигая абсолютного значения 98,57±52,14 в конце 24 недели лечения и оказываясь ниже исходного уровня (211,43±100,16) на 53,4% (р<0,01).
При использовании ибупрофена также отмечается достоверное снижение активности ревматоидного артрита по показателю ПВА. Через 4 недели значение исследуемого показателя уменьшилось на 20,5% (р<0,05), через 8 - на 25,2% (р<0,05), через 12 - на 40,3% (р<0,05), через 16 - на 46%(р<0,05), через 20 - на 44,4%, через 24 - на 53,6% (р<0,01), достигая абсолютной величины - 98,4±61,87. Показатели DAS28 и ПВА достоверно коррелировали между собой (r = 0,94, р<0,05).
Содержание С-реактивного белка в сыворотке крови исходно составило 41,7±8,2 мг/л, и оказалось повышенным по отношению к соответствующему показателю у здоровых лиц среднего возраста (до 5 мг/л) в 3-12 раз. Нами отмечается значительное снижение содержания СРБ как в группе применения диклофенака, так и - ибупрофена. Наиболее быстрый эффект снижения СРБ выявлен при использовании диклофенака - процент снижения к 12 недели составил 45,1 (р<0,01) от исходно повышенного уровня. При тенденции к дальнейшему снижению линейный характер регрессии привел к снижению исследуемого показателя к 24 недели - 17,4±10,2 мг/л - и оказался ниже исходного уровня на 58,3% (р<0,05).
Снижение уровня СРБ в группе применения ибупрофена характеризовалось более умеренными сдвигами. Так, величина СРБ на 4 и 8 недели снизилась соответственно на 2,6% и 7,9% соответственно. К 20 неделе лечения ибупрофеном отмечается достоверное снижение значения показателя на 36,5% (р<0,01), а к 24 неделе - на 50,6% (р<0,01), достигая абсолютного значения 20,6±12,3 мг/л. В группе применения ибупрофена нормальные значения СРБ достигнуты у 9 (22,0%) пациентов. У 28 (68,3%) значение СРБ снизилось в 3,5-1,5 раза по отношению к исходным значениям.
Таким образом, установлено значительное уменьшение клинических проявлений и выраженности лабораторных показателей воспаления при ревматоидном артрите 1-2 степени активности на фоне применения диклофенака и ибупрофена.
Редукция основных клинических проявлений имела по большинству показателей линейный характер, однако большинство анализируемых параметров на фоне применения диклофенака имели тенденцию к нормализации в более ранние сроки.
При использовании ибупрофена регистрировалась сопоставимая с диклофенаком по ряду параметров терапевтическая эффективность. В целом к 24 неделе лечения ибупрофеном отмечалось незначительно сниженные по сравнению с использованием диклофенака уровни величин боли в мм по ВАШ, ЧБС, ЧПС, СОЭ, СРБ.
1.2 Анализ динамики выраженности болевого синдрома, полученных при применении диклофенака и ибупрофена
для лечения больных остеоартрозом коленных суставов.
При проведении анализа карт обследования больных оказалось, что на фоне приема исследуемых препаратов у больных ОА отмечалось значительное уменьшение болей уже после недельного курса терапии, при этом в дальнейшем положительная динамика сохранялась.
У больных 1-й группы к 1-ой недели наблюдения уровень боли в коленных суставах в покое (по шкале ВАШ) снизился до 25,7 мм по шкале ВАШ, у пациентов 2-й группы - до 22,3 мм. Ко 2-ой недели наблюдения уровень боли в покое снизился до 24,8 мм в 1-ой группе и до 19,6 мм во 2-ой группе (p<0,05).
У больных 1-й группы ко 2-му месяцу наблюдения уровень боли в коленных суставах в покое (по шкале ВАШ) снизился до 15,26 мм, что соответствует 45,7% (p<0,05), у пациентов 2-й группы его снижение достигло уровня 14,8 мм, что составило 71,9% (p<0,001). На фоне проводимой терапии, у наблюдаемых групп пациентов регистрировалось снижение болей в коленных суставах и при движении, более выраженное у больных ОА 2-й группы, получающих терапию диклофенак (рис. 1).
Рис.1. Динамика болей в коленном суставе при ходьбе
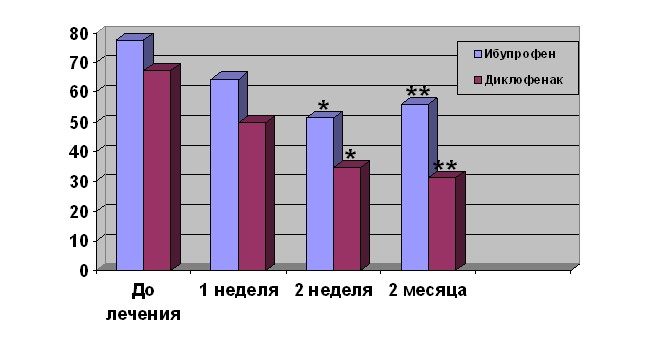
* - достоверность p<0,05, ** - достоверность p<0,01.
Так, уже к концу 2-ой недели лечения были зафиксированы достоверные различия в выраженности болевого синдрома в исследуемых группах (51,3±6,4 мм против 34,8±4,4 по шкале ВАШ, p<0,05), а к концу наблюдения эти показатели составили 55,8±6,1 и 31,2±4,3 мм соответственно (p<0,01).
При изучении динамики индекса WOMAC у исследуемых групп пациентов, характеризующих функциональную активность больных, было получено, что у 2-й группы пациентов, получающих диклофенак, наблюдалась стабилизация данного показателя после 2-недельного курса терапии. У больных остеоартрозом 1-й группы наблюдалась положительная динамика индекса WOMAC.
Уменьшение выраженности болевого синдрома и, соответственно, улучшение функционального состояния на фоне проводимой терапии отмечали больные обеих групп, при этом значимое улучшение ко 2-ой недели наблюдения, по оценке врача, наблюдалось у 10% пациентов 1-й группы и у 20% пациентов 2-й группы, а к концу 2 месяца - у 18% и 22,5% соответственно (p < 0,05). Оценка эффективности терапии пациентами существенно не отличалась от оценки врача.
1.3 Анализ динамики лабораторных показателей, характеризующих антиоксидантный потенциал, диклофенака и ибупрофена
у больных с ревматоидным артритом.
Применение НПВС при ревматоидном артрите в качестве одной из основных фармакотерапевтических групп опасно развитием осложнений в виде язвенно-эрозивных поражений желудочно-кишечного тракта (ЖКТ). Активация ПОЛ рассматривается как один из ведущих механизмов развития этих осложнений. Целью данной главы было изучение состояния ПОЛ и АОС при 24-недельном лечении больных ревматоидным артритом диклофенаком и ибупрофеном.
Уровень МДА в сыворотке крови относительно здоровых людей среднего возраста (n=12) составляет 9,04±1,34 мкмоль/л. Уровень МДА сыворотки крови больных ревматоидным артритом 1-2 степени лабораторной активности изначально составил в среднем 15,07±1,98 мкмоль/л, что оказалось на 66,7% выше сравниваемого показателя у здоровых людей сопоставимого возраста.
При использовании диклофенака максимум снижения зарегистрирован на 8 неделе - снижение от исходного уровня на 34,32% и достижение абсолютного значения 9,72±3,66 мкмоль/л. В последующие сроки наблюдения уровень МДА сыворотки крови претерпевал незначительные изменения, достигая снижения от исходного уровня на 26,69% на 12 неделе наблюдения, 31,69% - на 16 неделе, 28,72% - на 20 неделе. К окончанию срока наблюдения, на 24 неделе лечения зарегистрировано снижение содержания МДА сыворотки на 33,51% от исходного уровня и достижение абсолютного значения 9,84±2,23 мкмоль/л. На 24 неделе лечения диклофенаком достигнуто значение уровня МДА в сыворотке крови, превышающее уровень МДА сыворотки здоровых людей в среднем на 8,85%, что, таким образом, свидетельствует о незначительном уровне вторичного продукта ПОЛ - МДА.
Использование ибупрофена выявило значительное снижение уровня МДА сыворотки уже на 4 неделе, когда зарегистрировано снижение анализируемого показателя от исходного уровня на 33,14% и достижение значения 10,43±4,2 мкмоль/л. После 12 недели отмечается постепенное более значительное снижение уровня МДА сыворотки крови. Так, на 16 неделе достигнуто снижение на 37,56%, на 20 - на 39,55%, на 24 - на 38,14% от исходного уровня и достижение в конце срока наблюдения абсолютного значения 9,65±2,48 мкмоль/л, что лишь на 6,32% выше уровня значения МДА сыворотки крови здоровых людей среднего возраста.
Значение активности СОД в группе здоровых людей среднего возраста составило 0,378±0,042 усл.ед./мин на 1 мг белка. Активность СОД у больных ревматоидным артритом 1-2 степени лабораторной активности составила по нашим данным величину 0,295±0,036 усл.ед./мин на 1 мг белка, что оказалось ниже величины сравниваемого показателя в группе здоровых людей сопоставимого возраста на 21,96%. В группе применения диклофенака на протяжении 12 недель исследования нами не зарегистрировано изменения значения анализируемого показателя. В дальнейшем отмечается постепенное незначительное по выраженности нарастание активности СОД. На 16 и 20 неделе использования в лечении больных диклофенака нами выявлены наиболее высокие значения анализируемого показателя. Активность СОД сыворотки крови возросла до абсолютных значений 0,312±0,047 и 0,311±0,046 усл.ед./мин на 1 мг белка соответственно 16 и 20 неделе наблюдения, увеличившись по сравнению с исходными данными на 9,09 и 8,74%. Уровня значения показателя здоровых людей не было достигнуто.
При использовании ибупрофена отмечается более стремительное нарастание активности этого фермента антиоксидантной защиты. Так, уже на 4 неделе активность показателя увеличилась на 7,97%, а на 12 неделе - на 11,63%, достигнув абсолютного значения 0,336±0,038 усл.ед./мин на 1 мг белка. В последующие сроки наблюдения активность СОД несколько снизилась, но была достигнута относительная стабильность величины показателя. На 12 и 24 неделе значение активности СОД сыворотки крови больных ревматоидным артритом, получавших лечение ибупрофеном, было приблизительно одинаковым, на 9,64 и 9,3% соответственно выше исходного уровня. Но, тем не менее, абсолютные значения СОД в эти сроки оказались ниже величины соответствующего показателя здоровых людей в среднем на 12,7%.
ГР катализирует реакцию восстановления глутатиона с участием НАДФН. Активность ГР сыворотки крови здоровых людей среднего возраста составила 1,320±0,31 мккат/л/мин. Активность ГР сыворотки крови больных ревматоидным артритом средней степени клинико-лабораторной активности оказалась увеличенной в среднем на 113,5% по сравнению со сравниваемым показателем здоровых людей среднего возраста. Практически не отмечалось динамики изменения активности ГР на протяжении 16 недель лечения ни в группе применения диклофенака, ни в группе использования ибупрофена. Применение диклофенака определило статистически значимое снижение активности ГР на 20 неделе лечения - снижение на 5,49% от исходной величины и достижение уровня активности 2,649±0,416мккат/л/мин, и на 24 неделе - снижение на 5,0% от исходной величины и достижение уровня активности 2,663±0,389 мккат/л/мин.
В группе использования ибупрофена динамика активности ГР сыворотки крови аналогична. Вплоть до 20 недели лечения изменение показателя не отмечалось, а в последующем очевидна регрессия величины активности ГР. На 20 неделе наблюдения достигнуто снижение активности ГР на 10,05% от исходной величины и достижение абсолютного значения 2,543±0,371 мккат/л/мин. На 24 неделе активность ГР снизилась значительнее, на 21,68% от исходного уровня и оказалась на 67,73% выше уровня активности ГР у здоровых людей среднего возраста.
Очевидно, что использование диклофенака и ибупрофена в минимальной степени оказало влияние на параметры ПОЛ и ферментативного звена антиоксидантной защиты. Тем не менее, об эффективности проводимой фармакотерапии свидетельствовало как улучшение клинической симптоматики, так и позитивное влияние диклофенака и ибупрофена на лабораторные параметры с наличием отчетливой тенденции к их нормализации. Так, уровень МДА и активность ГР в сыворотке крови снизились, активность СОД повысилась, а абсолютные значения анализируемых параметров к окончанию срока наблюдения за больными - 24 недели - достоверно имели значительно меньшие отклонения от соответствующих нормальных величин группы здоровых людей сопоставимого возраста. Поскольку вторичные и конечные продукты ПОЛ выступают в качестве модуляторов в очаге воспаления, существенно влияя на хемотаксическую и метаболическую активность фагоцитирующих клеток, поддерживая выраженность воспалительных иммунологических реакций, манифестирующихся деструктивными процессами соединительной ткани, сдвиг в системе ПОЛ-АОЗ в сторону активации антиокислительных процессов явился в данном клиническом исследовании свидетельством репаративных процессов.
Глутатион, ГП, глутатион-трансфераза (ГТ), ГР и НАДФН образуют глутатионовую антиоксидантную систему, в которой ГР и НАДФН необходимы для восстановления окисленного глутатиона и, следовательно, его рециклирования. Уменьшение содержания ВГ в сыворотке крови может свидетельствовать об оксидативном стрессе. При этом в печени и плазме накапливается окисленный глутатион. В этих условиях действия ВГ по метаболической биотрансформации ксенобиотиков с помощью ГТ, удалению активных форм кислорода недостаточно. Срыв АОЗ характеризуется развитием свободно-радикальных повреждений разных компонентов клетки и тканей, составляющий синдром пероксидации и включающий следующие изменения: повреждение мембран; инактивация и трансформация ферментов; подавление деления клеток; накопление в клетке инертных продуктов полимеризации. Периодически повторяющийся или текущий синдром пероксидации составляет фактор патогенеза ряда заболеваний, что послужило поводом выделения их в группу свободно-радикальных патологий. Ключевая роль в защите клетки от оксидативного стресса отводится, по-видимому, системе глутатиона.
Уровень ВГ в сыворотке крови больных ревматоидным артритом 1-2 степени лабораторной активности оказался ниже уровня ВГ сыворотки крови здоровых людей среднего возраста в среднем на 13,26%. На фоне 24 недель лечения диклофенаком и ибупрофеном отмечается достоверное увеличение содержания сывороточного ВГ, что, вероятно, объясняется не антиоксидантными свойствами препаратов, а способностью патогенетического противовоспалительного воздействия, выражающегося в том числе в ингибировании биосинтеза медиаторов воспаления (простагландинов). В группе использования диклофенака максимально высокий уровень ВГ выявлен на 20 неделе лечения и составил 238,0±38,4 мкмоль/л, что на 11,95% оказалось выше исходных показателей и лишь на 3,53% ниже уровня ВГ здоровых людей среднего возраста. В целом, устойчивое повышение уровня ВГ в группе использования диклофенака выявлено несколько раньше, на 16 неделе отмечается повышение уровня ВГ на 9,83%. К 24 неделе сохраняется достоверно значимое повышение уровня ВГ сыворотки крови.
В группе использования ибупрофена максимальное увеличение уровня ВГ - увеличение на 7,95% и достижение абсолютной величины 233,6±35,2 мкмоль/л - отмечается на 12 неделе лечения. В последующем уровень ВГ немного снижается [рис. 3.2.4]. В целом, с 8 недели использования ибупрофена отмечается относительно устойчивое увеличение содержания сывороточного ВГ. К окончанию срока наблюдения, на 24 неделе лечения уровень ВГ достиг значения 229,5±38,7 мкмоль/л, что оказалось на 6,05% выше исходного уровня и на 6,97% ниже значения показателя здоровых людей сопоставимого возраста.
Интересным оказался факт того, что у 11 человек в группе использования диклофенака и 8 человек в группе сравнения практически не отмечалось изменения уровней содержания сывороточных МДА, ВГ, активностей ГР, СОД на всех сроках наблюдения или изменения величин изолированы по показателям и незначительны. Именно у этих пациентов выявлены побочные явления используемых НПВС в виде поражения ЖКТ. Очевидно, они оказались "уязвимыми" в плане НПВС-индуцированных поражений ЖКТ. Количество таких пациентов в данном клиническом исследовании оказалось значительно ниже "резистентных", у которых отмечается положительная динамика лабораторных показателей.
Анализируя совокупную динамику клинических и лабораторных показателей выявлено, что подавляющее большинство пациентов чувствовали себя лучше уже с 8-12 недели лечения, но и на 20 - 24 неделе исследования показатели ПОЛ и АОС не достигли значений показателей нормы здоровых людей среднего возраста, что свидетельствует о продолжающихся нарушениях на молекулярном уровне при компенсации проявлений заболевания на уровне целого организма. Вероятно, причиной является недостаточность факторов для устранения интенсивности ПОЛ в виде внутриклеточных и плазменных антиоксидантных механизмов. Наличие изменений окислительного метаболизма у больных ревматоидным артритом на фоне клинического улучшения указывало на молекулярный дисбаланс, что следует учитывать в процессе выработки стратегии реабилитации и, возможно, реконвалесценции, пациентов этого профиля.
1.4 Оценка безопасности применения препаратов
диклофенака и ибупрофена
Влияние НПВС на состояние слизистой оболочки желудка (СОЖ) и 12 перстной кишки оценивалось исходно и после 2 месяцев терапии НПВС.
Была применена рабочая классификация, позволяющая формализовать информацию, как о характере эрозивно-язвенного процесса, так и о выраженности воспаления, состоянии остальной гастродуоденальной слизистой в течение 1-го эндоскопического исследования (Захарченко М.И.)
При контрольной ЭГДС (день терапии ) в 1 группе из 28 ( 82,4%) пациентов с исходно I типом СОЖ у 14 (41,2%) эндоскопическая картина изменений не претерпела, у такого же количества выявлены изменения СОЖ, соответствующие II типу использованной классификации
Из 6 пациентов с исходно умеренными воспалительными изменениями СОЖ у 2-х изменений не было и у 4-х больных (11,8%) отмечено увеличение гиперемии и отека СОЖ, соответствующее III типу СО.
Повреждение слизистой в виде эрозий в этой группе выявлено у 10 больных, что составило 29,4 %.
Во 2-ой группе у 75% пациентов СОЖ исходно соответствовала I типу. Прием ибупрофена более чем у половины из них не привел к каким –либо изменениям. У 21, 9% пациентов состояние СОЖ ухудшилось с развитием изменений II типа. Из 8 пациентов с исходно II типом СОЖ - у половины больных динамики не выявлено и у такого же количества пациентов лечение ибупрофеном привело к появлению выраженной гиперемии и отека СОЖ – III тип изменений (таб.1). Эрозивный гастродуоденит выявлен только у 3 (9,4%) пациентов.
Таким образом, отрицательная динамика проявления воспаления при применении диклофенака в отличие от ибупрофена произошла у большего числа больных. Гастроскопические воспалительные влияния ибупрофена оказалось меньшим, чем у диклофенака, что согласуется с данными метаанализа (Garcia Rodriguez L. A., 1998), где для диклофенака показатель составил 2,3 ± 0,5, а для ибупрофена - 1,0 ± 0.
В исследовании А.Yanagawa и соавт. (1998) изучалось возможное побочное действие диклофенака на слизистую оболочку 12–перстной кишки (по результатам фиброгастродуоденоскопии) в двойном слепом плацебо–контролируемом исследовании [Yanagawa A.,]. Эндоскопические изменения после 2–недельного приема диклофенака и плацебо достоверно чаще наблюдались в группе больных, принимающих диклофенак. При этом было установлено, что у пациентов, получавших диклофенак, содержание гексозамина (фактора, оказывающего цитопротективное действие) и локальный кровоток в слизистой оболочке были значимо снижены.
Терапия диклофенаком значимо чаще, чем ибупрофеном привела к эрозивным повреждениям СОЖ: 29,4% против 9,4%. Подобные результаты меньшей частоты развития НЛР получены и во многих европейских исследованиях. Так, во Франции и Англии с участием 1108 врачей общей практики было проведено рандомизированное исследование 3 анальгетиков: ацетилсалициловой кислоты (АСК), ацетаминофена, ибупрофена. В исследование включили 8677 взрослых пациентов с болями костно–мышечного генеза, горла, ОРЗ [Moore N.]. Лечение проводили в течение 1–7 дней в дозах: АСК и ацетаминофен 3 г/сут., ибупрофен до 1,2 г/сут. Частота значимых неблагоприятных явлений составила при приеме АСК – 18,7%, ибупрофена – 13,7%, ацетаминофена – 14,5%. Общее число ЖКТ осложнений отметили у 5,8% леченных ибупрофеном, у 7,3% – ацетаминофеном и у 10,6% – АСК. ЖКТ кровотечения отсутствовали у больных, получавших ибупрофен, но диагностированы у 4 больных на ацетаминофене (который не ингибирует ЦОГ–1) и у 2 – на АСК.
О высокой безопасности ибупрофена свидетельствует и тот факт, что он более 20 лет является препаратом, отпускаемым без рецепта в стране, где он был создан в 1962 г. S. Adams et al., работавшими в компании Boots (Великобритания).
По данным метаанализа (Garcia Rodriguez L. A., 1998), проведенного для оценки риска возникновения эрозивно-язвенных поражений при приеме ибупрофена и диклофенака, было выявлено, что относительный риск для ибупрофена составляет 1,0±0 (по 11 оцененным работам), а для диклофенака - 2,3±0,5 (по 8 работам). При подсчете индекса гастроинтестинальной токсичности, рассчитанной на основе банка данных ARAMIS было получено, что для ибупрофена он составил 1,13±0,29, при исследовании 577 больных, а для диклофенака 1,81±0,35, при исследовании 415 больных.
2. Исследование фармакокинетики и относительной биодоступности
генерических препаратов диклофенака и ибупрофена
Динамика усредненных концентраций диклофенака натрия и ибупрофена в плазме крови здоровых добровольцев после однократного перорального приема препаратов представлена на рис. 2 и 3 соответственно. Видно, что фармакокинетические кривые генерических и референсных препаратов практически совпадают, а значения концентраций в плазме крови статистически достоверно не различаются на протяжении всего исследования.
Результаты расчетов основных фармакокинетических параметров (в виде среднего значения ± стандартное отклонение) препаратов диклофенака и ибупрофена представлены в таблице 1. Установлено, что значения фармакокинетических параметров генерических и референсных препаратов статистически достоверно не различаются, а средние значения параметров относительной биодоступности и их доверительные интервалы не выходят за допустимые границы [Проведение качественных исследований биоэквивалентности лекарственных средств. Методические указания, 2004].
Рис. 2. Усредненные фармакокинетические кривые препаратов Ортофер (Т) и Вольтарен (R)
Рис. 3. Усредненные фармакокинетические кривые препаратов Ибупрофен-Хемофарм (Т) и Ибупрофен-Тева (R)
Таблица 1
Фармакокинетические параметры препаратов диклофенака и ибупрофена
| Параметры | Ортофер | Вольтарен | Ибупрофен- Хемофарм | Ибупрофен-Тева |
| Cmax, нг/мг1 мкг/мл2 | 1026 ± 440 | 1104 ± 512 | 45,1 ± 20,6 | 47,2 ± 19,2 |
| Tmax, час | 2,2 ± 0,7 | 2,1 ± 0,7 | 1,3 ± 0,5 | 1,4 ± 0,4 |
| AUC0- t, нг*ч/мл1 мкг*ч/мл2 | 2249 ± 995 | 2387 ± 1235 | 136,7 ± 60,1 | 143,5 ± 58,2 |
| Cmax/ AUC0- t | 0,473 ± 0,161 | 0,489 ± 0,148 | 0,347 ± 0,131 | 0,343 ± 0,128 |
| f, %; доверительный интервал | 0,98 ± 0,16; 0,91 – 1,06 | 1,01 ± 0,17; 0,91 – 1,10 | ||
| fII, %; доверительный интервал | 0,96 ± 0,24; 0,85 – 1,08 | 0,99 ± 0,24; 0,89 – 1,11 |
Примечание: 1 – для диклофенака, 2 – для ибупрофена
Результаты дисперсионного анализа значений основных фармакокинетических параметров препаратов Отрофер и Вольтарен, а также Ибупрофен-Хемофарм и Ибупрофен-Тева, представленные в таблице 2, свидетельствуют о том, что все факторы, кроме индивидуальной вариабельности, вносят статистически незначительный вклад в общую вариацию. Поскольку рассчитанные значения критериев статистической достоверности меньше стандартных (критических) значений, нулевая гипотеза об отсутствии статистически значимых различий между значениями показателей биоэквивалентности верна.
Таким образом, не выявлено статистически достоверных различий в процессе всасывания (как по полноте, так и по скорости) диклофенака после приема препаратов Ортофер и Вольтарен, а также ибупрофена после приема препаратов Ибупрофен-Хемофарм и Ибупрофен-Тева.
Таблица 2
Результаты дисперсионного анализа логарифмически
преобразованных фармакокинетических параметров
| Параметр | Факторы вариации | df | SS | MS | F | P |
| препаратов Отрофер и Вольтарен | ||||||
| AUC0- t | Добровольцы | 17 | 6,5333 | 0,38431 | 29,029 | 0,0000<0,001 |
| Периоды | 1 | 0,018213 | 0,018213 | 1,3757 | 0,358>0,3 | |
| Препараты | 1 | 0,0078375 | 0,0078375 | 0,59201 | 0,453>0,3 | |
| Cmax | Добровольцы | 17 | 6,9158 | 0,40681 | 12,806 | 0,0000<0,001 |
| Периоды | 1 | 0,0054319 | 0,0054319 | 0,17099 | 0,68472>0,3 | |
| Препараты | 1 | 0,038399 | 0,038399 | 1,2088 | 0,38784>0,3 | |
| Cmax/ AUC0- t | Добровольцы | 17 | 2,8723 | 0,16896 | 6,2781 | 0,0003<0,001 |
| Периоды | 1 | 0,003752 | 0,003752 | 0,13942 | 0,71376>0,3 | |
| Препараты | 1 | 0,01154 | 0,01154 | 0,42881 | 0,52188>0,3 | |
| препаратов Ибупрофен-Хемофарм и Ибупрофен-Тева | ||||||
| AUC0- t | Добровольцы | 17 | 5,5115 | 0,32421 | 7,7276 | 0,0000<0,001 |
| Периоды | 1 | 0,012325 | 0,012325 | 0,29378 | 0,59528>0,3 | |
| Препараты | 1 | 0,0064999 | 0,0064999 | 0,15493 | 0,69907>0,3 | |
| Cmax | Добровольцы | 17 | 5,9054 | 0,34738 | 18,604 | 0,0000<0,001 |
| Периоды | 1 | 0,00014083 | 0,00014083 | 0,007542 | 0,93187>0,3 | |
| Препараты | 1 | 0,0044297 | 0,0044297 | 0,23723 | 0,63282>0,3 | |
| Cmax/ AUC0- t | Добровольцы | 17 | 1,8069 | 0,10629 | 2,2973 | 0,00517<0,01 |
| Периоды | 1 | 0,015101 | 0,015101 | 0,3264 | 0,57573>0,3 | |
| Препараты | 1 | 0,0001979 | 0,0001979 | 0,00428 | 0,94867>0,3 | |
ВЫВОДЫ
- Генерический отечественный препарат диклофенака – Ортофер (ЗАО «Брынцалов», Россия) является биоэквивалентным препарату сравнения Вольтарен (Новартис Фарма АГ, Швейцария) при исследовании на здоровых добровольцах.
- Генерический препарат ибупрофена – Ибупрофен-Хемофарм (Хемофарм Концерн А.Д., Югославия) является биоэквивалентным препарату сравнения Ибупрофен-Тева (Pharmaceutical Industries Ltd, Израиль) при исследовании на здоровых добровольцах.
- По обезболивающему эффекту генерический препарат диклофенака превосходит генерический препарат ибупрофена у больных ревматоидным артритом и остеоартрозом.
- Генерические препараты диклофенака и ибупрофена обладают антиоксидантным потенциалом у больных с ревматоидным артритом, что соотносится с их клинической эффективностью и безопасностью.
- По параметрам безопасности в отношении развития гастротоксичности, ибупрофен превосходит диклофенак у больных ревматоидным артритом и остеоартрозом.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Генерические препараты Ортофер (ЗАО «Брынцалов», Россия) и Ибупрофен-Хемофарм (Хемофарм Концерн А.Д., Югославия) могут быть рекомендованы для клинического применения, так как являются биоэквивалентными оригинальным препаратам сравнения при исследовании на здоровых добровольцах.
- При лечении остеоартроза и ревматоидного артрита больным без сопутствующей патологии ЖКТ, терапию следует начинать с назначения диклофенака, как препарата с более сильным обезболивающим эффектом. Пациентам с остеоартрозом и ревматоидным артритом, сопровождающимися патологией ЖКТ, терапию следует начинать с ибупрофена, как более безопасного препарата.
СПИСОК работ, опубликованных по теме диссертации
- Дмитриев В.А., Мирчева Ж.Ж. О безрецептурных препаратах за рубежом // Ведомости Научного центра экспертизы и государственного контроля лекарственных средств. – 2000. - № 3. – С. 60-62.
- Дмитриев В.А. Фармакоэпидемиология и фармакоэкономика безрецептурных нестероидных противовоспалительных средств. // Ведомости Научного центра экспертизы и государственного контроля лекарственных средств. – 2001. - № 2. – С. 71-73.
- Дмитриев В.А. Вопросы информирования пациентов при лекарственном самолечении // VIII Российский национальный конгресс «Человек и лекарство»: Тезисы докладов. – Москва, 8-12 апреля 2002. – С. 745.
- Дмитриев В.А. Опыт лекарственного самолечения за рубежом // VIII Российский национальный конгресс «Человек и лекарство»: Тезисы докладов. – Москва, 8-12 апреля 2002. – С. 745.
- Dmitriev V.A., Rosen R, Gotovats S. Economic and Legal Framework for Non-Prescription Medicines, AESGP, Brussels, June 2003. – P. 298-312.
- Dmitriev V.A., Ishmukhametov A. Economic and Legal Framework for Non-Prescription Medicines, AESGP, Brussels, 13th edition -June 2007. – P. 370-382.
- Дмитриев В.А. Тенденции развития фармацевтического рынка воспроизведенных лекарственных средств // Ведомости Научного центра экспертизы средств медицинского применения. – 2007. - № 1. – С. 58-61.
- Дмитриев В.А., Сычев Д.А., Кукес В.Г. Проблема взаимодействия антибиотиков с нестероидными протиовоспалительными средствами (миниобзор) //Антибиотики и химиотерапия.- 2008.- №1-2.- с. 30-32.
Список сокращений
АОС- антикоасидантный статус
АСК- ацетилсалициловая кислота
ВАШ- визуальная аналоговая шкала
ВОЗ- всемирная организация здравоохранения
ГКБ- городская клиническая больница
ГТ - глутатионтрансфераза
ЖКТ- желудочно-кишечный тракт
ИКФ- Институт клинической фармакологии
ЛС- лекарственные средства
МДА- молоновый диальдегид
НПВС- нестероидные противовоспалительные средства
ОА - остеоратроз
ПОЛ- перекисное окисление липидов
РА- ревматоидный артрит
СОД- супероксиддисмутаза
СОЭ- скорость оседания эритроцитов

