Комплексная диагностика и хирургическая коррекция рефлюкс-эзофагита и рефлюкс-гастрита при желчекаменной болезни
На правах рукописи
Абдуллоев
Джамолиддин Абдуллоевич
Комплексная диагностика и хирургическая коррекция рефлюкс-эзофагита и рефлюкс-гастрита при желчекаменной болезни
14.01.17 – хирургия
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук
Душанбе 2010
Работа выполнена на кафедре хирургических болезней №1 Таджикского государственного медицинского универститета имени Абуали ибни Сино
Научный консультант - академик АМН РТ, заслуженный деятель науки и техники РТ,
доктор медицинских наук, профессор Курбонов Каримхон Муродович
Официальные оппоненты:
| академик АН РТ заслуженный деятель науки и техники РТ доктор медицинских наук, профессор | Усманов Негматулло |
| доктор медицинских наук, профессор | Буриев Илья Михайлович |
| доктор медицинских наук, профессор | Борисов Александр Евгеньевич |
Ведущая организация: НИИ Скорой помощи им. Н.В. Склифосовского департамента здравоохранения
г. Москвы
Защита состоится «____» ____________2011 г. в _____ часов на заседании диссертационного совета Д 737.005.01 при Таджикском государственном медицинском университете имени Абуали ибни Сино (Республика Таджикистан, 734003, г Душанбе, проспект Рудаки, 139).
С диссертацией можно ознакомиться в библиотеке Таджикского государственного медицинского университета им. Абуали ибни Сино.
Автореферат разослан «____» _______________ 2011г.
Учёный секретарь диссертационного
совета, кандидат медицинских наук, доцент Рашидов Ф.Ш.
Общая характеристика работы
Актуальность проблемы: Несмотря на значительные достижения в хирургической гепатологии, желчнокаменная болезнь (ЖКБ) остается одной из самых распространенных хирургических и гастроэнтерологических заболеваний [Тотиков В.З., Спелушкин В.Д. и соавт. 2005; Брискин Б.С., Ломидзе О.В., 2005; Орехов Г.И., 2008; Iwase K., Takao T. Et al., 1994]. Следует особо подчеркнуть, что ежегодно в мире проводится более 2,5 млн. операций на желчных путях (преимущественно холецистэктомия при ЖКБ), в России более 100 тыс. холецистэктомий в год, а в США в 5-6 раз больше [ Дадвани С.А., Ветшев П.С. и соавт. 2000; Брюнин А.В. 2000 ]. Неудовлетворительные результаты холецистэктомии (от 10 до 30%) случаев связаны с развитием различных патологических состояний объединенных в понятие постхолецистэктомический синдром (ПХЭС). Среди многочисленных причин, приводящих к развитию ПХЭС особое место отводится несвоевременной диагностики и хирургической коррекции рефлюкс-эзофагита (РЭ) и рефлюкс-гастрита (РГ), которые в отдаленном послеоперационном периоде осложняются постхолецистэктомическим РЭ и РГ [ Григорьев П.Я. и соавт., 2002; Харченко Н.В. и соавт., 2003; Lehman I.V. et al., 1996 ].
Частое сочетание ЖКБ с РЭ и РГ считается патогенетически взаимосвязанным и обусловлены врожденными и приобретенными патологиями пищеводно-желудочного и двенадцатиперстно-еюнального перехода, а также вследствие травматизации блуждающих нервов в пищеводном отверстии диафрагмы [Назаров Б.О., 2004; Курбанов К.М., 2008]. С другой стороны, наличие РЭ и РГ не только отягощают течение ЖКБ, но и могут быть причиной ее развития [Мартынов В.Л., 2003; Репин М.В., 2005].
Необходимо подчеркнуть, что в последние годы публикаций и работ посвященных вопросам, связанных с изучением патогенеза РГ и РЭ ее ранней диагностики освещены в литературе недостаточно [Черноусов А.Ф., и соавт. 1999, Абакумов М.М. и соавт., 2007, Пинчук Т.П., 2007, Бородач А.В., Бородач В.А., 2008; Курбанов К.М., 2008]. До настоящего времени остаются невыясненными, основные причины развития РЭ при наиболее распространенных хронических заболеваниях органов брюшной полости в частности при ЖКБ. Не выработаны научно-обоснованные рекомендаций в определении показаний к выполнению одновременных сочетанных методов коррекции РЭ и РГ при ЖКБ и выбор наиболее оптимального метода операции. Требует более глубокого и всестороннего изучения этиопатогенеза сочетания ЖКБ с РГ и РЭ.
В этом отношении важное значение в развитии нарушений моторно-эвакуаторной функции пищеварительного тракта имеет нарушение гуморальной регуляции [Акимов В.П., Дваладзе Л.Г. и соавт., 2008; Fozard J.R., 1982], что требует глубокого и всестороннего изучения содержания интестинальных гормонов, вырабатываемые АPUD системой при различных степенях тяжести хронического нарушения дуоденальной проходимости (ХНДП) синтезирующего серотонин. Существует точка зрения согласно которой моторно-эвакуаторное нарушение ДПК связано с дисфункцией структур слизистой оболочки, что определяется состоянием местного кровообращения и трофической иннервации (Хаджиев О.Ч.,2001; Акимов В.П., 2007), в основе которых лежат расстройства местной регуляции деятельности слизистой оболочки ДПК, в частности нейромедиаторов, которое оказывают непосредственное влияние на изменение тонуса и моторики ДПК.
Анализ публикаций по рассматриваемой проблеме показывает, что к настоящему времени практически не разработана лечебно - диагностическая тактика при ЖКБ сочетающейся с РЭ и РГ, не уточнены показания к различным методам хирургической и видеолапароскопической коррекции РЭ и РГ при ЖКБ [Дмитриев В.В., 1999 ; Омаров К.Х. и соавт., 2007; Pelligrini G. 1986 ].В связи с отсутствием четко определенных критериев, позволяющих охарактеризовать весь патологический процесс в целом, на сегодняшний день трудно прогнозировать и, следовательно, проводить комплексную профилактику развития осложнений как самой ЖКБ, так и сочетанной с ней РЭ и РГ.
Приведенные аргументы и доводы представляют целесообразность проведения комплексного научного исследования.
Цель исследования. Улучшение результатов хирургического лечения больных с ЖКБ сочетающейся с рефлюкс-эзофагита и рефлюкс-гастрита путем разработки патогенетически обоснованных методов диагностики и дифференцированного выбора оптимального метода хирургического лечения
Задачи исследования
- Определить частоту сочетания РЭ и РГ, а также основные причины их развития при ЖКБ.
- На основании глубокого и всестороннего ретроспективного анализа истории болезни пациентов с постхолецистэктомическим синдромом выяснить причины развития постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита и их клинические проявления.
- Дать сравнительную оценку эффективности современных методов диагностики рефлюкс-эзофагита и рефлюкс-гастрита при желчнокаменной болезни, а также разработать и усовершенствовать новые способы диагностики и хирургического лечения рефлюкс-эзофагита, рефлюкс-гастрита и желчнокаменной болезни.
- Определить роль морфологического состояния гастроэнтериновой системы (ЕС-клеток) в патогенезе хронических нарушений дуоденальной проходимости и желчнокаменной болезни.
- Изучить влияние дуоденогастроэзофагеального рефлюкса, степени хеликобактерной обсемененности желудка и пищевода, а также нарушений процессов перекисного окисления липидов в развитии рефлюкс- эзофагита.
- Разработать и усовершенствовать патогенетически обоснованные методы хирургической и видеолапароскопической коррекции рефлюкс-эзофагита и рефлюкс-гастрита при желчнокаменной болезни.
- Изучить непосредственные и отдаленные результаты хирургического лечения желчнокаменной болезни, сочетающейся с рефлюкс-эзофагитом и рефлюкс-гастритом.
Научная новизна. На большом клиническом материале изучены частота, причины и выраженность клинических симптомов рефлюкс-эзофагита и рефлюкс-гастрита при желчнокаменной болезни. Выявлены и проанализированы основные причины развития постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита и особенности их клинического течения. Дана комплексная оценка существующим и специальным методам комплексного исследования пациентов с рефлюкс эзофагитом и рефлюкс-гастритом при желчнокаменной болезни. Разработан метод эндоскопической ультразвуковой диагностики рефлюкс-эзофагита (Рац. удост №3235/Р-451 от 23.10.09), и холедохолитиаза. Разработан новый способ диагностики эндоскопически негативных форм рефлюкс-эзофагита по показателям повышения уровня продуктов перекисного окисления липидов в слизистой оболочке пищевода (Рац. Удост. №3240/Р-446 от 24.02.2010). Разработаны новые способы ультразвуковой диагностики дуоденостаза (Патент РТ N134 от 23.11.2007) и артериомезентериальной компрессии двенадцатиперстной кишки (Патент РТ N135 от 23.11. 2007). На основании комплексного обследования больных разработаны алгоритмы диагностики и лечения желчнокаменной болезни сочетающейся с рефлюкс-эзофагитом и рефлюкс-гастритом. Впервые проведено глубокое комплексное исследование морфологического состояния ЕС–клеток гастроэнтериновой системы у больных с различными стадиями хронического нарушения дуоденальной проходимости. На основании анализа клинических, биохимических, электронно-микроскопических и люминисцентно-гистохимических данных установлено, что пусковым механизмом в патогенезе хронических нарушений дуоденальной проходимости отводится качественному и количественному уменьшению ЕС-клеток слизистой оболочки двенадцатиперстной кишки, синтезирующих серотонин, способствующее блокаде серотонинсинтезирующих клеток пищеварительного тракта, снижению содержании серотонина и в других структурах двенадцатиперстной кишки приводящее в конечном итоге к снижению уровня серотонина в крови. Впервые выявлена корреляционная связь между тяжестью проявления хронических нарушений дуоденальной проходимости и снижением количества ЕС – клеток и серотонина в крови. Разработана новая концепция патогенеза желчнокаменной болезни.
Доказано, что одним из патогенетических механизмов развития рефлюкс-эзофагита при желчнокаменной болезни является выраженное проявление дуоденогастроэзофагеального рефлюкса, способствующее развитию билиарного рефлюкса, а также высокая степень хеликобактерной обсемененности слизистой пищевода и желудка. Впервые изучено состояние процессов перекисного окисления липидов и антиоксидантной защиты крови и в слизистой оболочке пищевода у больных с недостаточностью нижнего пищеводного сфинктера. При этом установлено, что одним из причин развития недостаточности нижнего пищеводного сфинктера является местное повреждающее действие продуктов перекисного окисления липидов и снижение щелочной буферной емкости слюны.
Углубленный анализ причин развития постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита и данных комплексного обследования больных при желчнокаменной болезни позволил разработать принципы дифференцированного подхода при выборе хирургической тактики. Усовершенствованы способы предоперационной подготовки пациентов с желчнокаменной болезнью, сочетающейся с рефлюкс-эзофагитом и рефлюкс-гастритом. Проведена сравнительная оценка результатов видеолапароскопических и традиционных способов холецистэктомии и коррекции рефлюкс-эзофагита и рефлюкс-гастрита. Показано преимущество видеолапароскопической коррекции рефлюкс-эзофагита при желчнокаменной болезни.
На основании клинического опыта разработана клиническая классификация РГ, дуоденостаза и внедрены новые способы профилактики и лечения осложнений холецистэктомии и билиодигестивных анастомозов получены патенты.
- Способ повышения герметичности холедоходуоденоанастомоза (Патент РТ № 68 от 28. 11. 2006)
- Способ определения жизнеспособности тонкой кишки (Патент РТ № 83 от 29. 06. 2007)
- Способ определения жизнеспособности тканей печени (Патент РТ № 69 от 5.12. 2006)
- Ретрактор печени (Патент РТ № 118 от 29. 01. 2008)
Практическая значимость работы.
Разработанные новые методы ранней диагностики рефлюкс-эзофагита, алгоритмы инструментального обследования пациентов с ЖКБ, сочетающейся с РЭ и РГ, способствуют значительному снижению частоты развития постхолецистэктомического РЭ и РГ. Применение в клинической практике, предложенных методов предоперационной подготовки, разработанные и усовершенствованные способы хирургического лечения ЖКБ и холедохолитиаза в значительной степени уменьшают частоту развития послеоперационных гнойно-септических осложнений.
Основные положения, выносимые на защиту
- Основными причинами развития рефлюкс-эзофагита при желчнокаменной болезни являются недостаточность нижнего пищеводного сфинктера, грыжа пищеводного отверстия диафрагмы и хроническое нарушение дуоденальной проходимости. Причинами развития рефлюкс-гастрита хроническое нарушение дуоденальной проходимости и недостаточность пилорического сфинктера.
- В развитии постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита при желчнокаменной болезни важное значение имеет недостаточная осведомленность врачей о частоте сочетаний желчнокаменной болезни с рефлюкс-эзофагитом и рефлюкс-гастритом и обшности их патогенеза, отсутствие алгоритмов диагностики, а также неадекватный выбор операционного доступа и интраоперационной ревизии.
- Наряду с комплексными инструментальными и специальными исследованиями высокоинформативными методами диагностики тяжести рефлюкс-эзофагита, рефлюкс-гастрита и холедохолитиаза являются определение продуктов ПОЛ и эндоскопическая ультразвуковая сонография, а также разработанные компьютеризованные методики оценки, с использованием спектрального и корреляционного анализа электрических проявлений моторной активности элементов НПС.
- В патогенезе хронических нарушений дуоденальной проходимости и рефлюкс-гастрита ведущее место отводится количественному и качественному уменьшению ЕС-клеток гастроэнтериновой системы и структур клеток слизистой оболочки двенадцатиперстной кишки, синтезирующих серотонин. Имеется тесная корреляционная связь между тяжестью нарушений дуоденальной проходимости и снижением уровня серотонина в крови, которая способствует затруднению оттока желчи в двенадцатиперстную кишку с последующим нарушением метаболизма желчи и развитию ЖКБ.
- Одним из патогенетических механизмов развития рефлюкс-эзофагита при желчнокаменной болезни является выраженное проявления дуоденогастроэзофагеального рефлюкса, способствующее развитию щелочного (желчного) рефлюкса, высокая степень хеликобактерной обсемененности слизистой пищевода и желудка, а также местное повышение продуктов ПОЛ повреждающий нижний пищеводный сфинктер.
- Высокоэффективным методом хирургического лечения рефлюкс-эзофагита при желчнокаменной болезни являются видеолапароскопические комбинированные антирефлюксные вмешательства с холецистэктомией и разработанные и уовершенствованные методы лечения холедохолитиаза.
- Патогенетически обоснованным методом коррекции рефлюкс-гастрита при желчнокаменной болезни являются комбинированные вмешательства на двенадцатиперстной кишке.
Внедрение результатов исследования в практическое здравоохранение и учебный процесс. Разработанные практические рекомендации внедрены и используются при хирургическом лечении больных с желчнокаменной болезнью сочетающейся с РЭ и РГ в хирургических отделениях городской клинической больницы №3, №5 и городской клинической больницы скорой медицинской помощи г. Душанбе. Результаты исследования используются при чтении лекций и проведении практических занятий на кафедрах общей хирургии №1, №2 и хирургических болезней №1 Таджикского государственного медицинского университета им Абуали ибни Сино.
Апробация работы. Материалы диссертационного исследования и основные положения диссертации доложены на Республиканской научно-практической конференции (Душанбе, 2006), VI научно-практической конференции детских хирургов, анестезиологов и реаниматологов РТ (Душанбе, 2006), III Республиканской научно-практической конференции анестезиологов и реаниматологов (Душанбе, 2006), Научно– практической конференции «Медицина XXI - века» (2006), Научно-практической конференции «Актуальные вопросы неотложной хирургии» (Курган-Тюбе, 2007), Республиканской научно – практической конференции «Современная медицина, качество и жизнь пациентов» (Душанбе, 2006), Республиканской научно- практической конференции, посвященной 20-летию организации службы реконструктивно-восстановительной хирургии в Таджикистане (Душанбе, 2007), Юбилейной конференции «Актуальные вопросы герниологии» посвященная 5- ой годовщине со дня образования общества герниологов (Москва, 2006); ХII Международном конгрессе гепатохирургов стран СНГ (Алма-Ата, 2007), международном конгрессе хирургов гепатологов стран СНГ (Алма –Ата, 2007), II городской научно-практической конференции с международным участием «Современные технологии неотложной хирургии органов брюшной полости» (Душанбе, 2007); Республиканской научно-практической конференции «Роль современной медицинской технологии в улучшении качества жизни пациентов » (Турсунзода, 2007) II съезде детских хирургов анестезиологов и реаниматологов Таджикистана (Душанбе, 2008); II съезде Центрально- Азиатских сердечно-сосудистых хирургов (Душанбе, 2008); Всероссийской научно-практической конференции «Актуальные проблемы клинической и экспериментальной медицины (Чита, 2008); Первой международной конференции по торакоабдоминальной хирургии, посвященной 100- летию со дня рождения академика Б. В. Петровского, (Москва, 2008); Международной конференции Современное развитие герниологии (Калининград, 2008); XIV Международном конгрессе хирургов гепатологов стран СНГ (Казань, 2008).Обсуждены на заседании межкафедральной экспертной комиссии по хирургии ТГМУ имени Абуали ибни Сино (2.07.2010).
Публикации. По теме диссертации опубликовано 64 научных работ, одна монография, в том числе 12 публикации в центральных журналах рекомендуемых ВАК РФ. Получено 7 патентов РТ и 8 удостоверений на рационализаторские предложения, 2 удостоверений на авторские свидетельство.
Личное участие автора в получении научных результатов, изложенных в диссертации. При личном участии автора обследовано 287 больных желчнокаменной болезнью сочетающейся с рефлюкс – эзофагитом, рефлюкс – гастритом и больные с ПХЭ РЭ и РГ. Автор в большинстве случаев участвовал в качестве основного хирурга и ассистента при лечении, изучаемых в работе больных. Обработка информации и изучение отдаленных результатов у всех больных также проводилось лично автором. Разработанные при непосредственном участием автора методики диагностики, алгоритмы обследования больных с желчнокаменной болезнью с РЭ, РГ и ПХЭС. Автор получил 7 патентов и 8 рационализаторских предложений по современным методам диагностики и модернизации техники оперативных вмешательств.
Объем диссертации. Диссертации состоит из введения, 7 глав, заключения, выводов, практических рекомендаций, указателя литературы, изложена на 296 страниц машинописного текста. Работа содержит 71 таблиц и 87 рисунков 334 библиографический указатель, в котором представлены 218 отечественных и 115 иностранных литературных источников.
Содержание работы
Характеристика клинического материала и методов исследования
Проанализированный в работе клинический материал, включает комплексное обследование и лечение 3528 больных с желчнокаменной болезнью, находившихся на лечение в 3 городских клиниках г. Душанбе Городских клинических больницах №3 и №5, ГКБ СМП, за последние 15 лет. При этом у 287 (8,1%) пациентов наряду с ЖКБ диагностировали рефлюкс эзофагит – 5,5% (n=195) и рефлюкс-гастрит – 2,6% (n=92).
Следует также отметить, что детально и всесторонне были изучены истории болезни 74 пациентов с постхолецистэктомическим рефлюкс-эзофагитом – 41.9% (n=31) и постхолецистэктомическим рефлюкс гастритом - 58.1% (n=43), которым в указанный период были выполнены различные методы холецистэктомии. Всего были обследованы и пролечены 361 пациента. Согласно Лос-анджеловской классификации больные с РЭ были распределены на 4 группы. Так, РЭ LA стадии А, характеризующая наличием катарального эзофагита длиной не более 5 мм, наблюдался у 57 (33,4%) пациентов. В 72 (42,1%) наблюдениях отмечалось одно или несколько повреждений слизистой оболочки пищевода длиной более 5,0 мм, не сливающихся между собой, ограниченных складками слизистой оболочки, состояние расценивалось как РЭ LA стадия В. РЭ LA стадии С имел место у 32 (18,7%) пациентов и характеризовался выраженным повреждением слизистой оболочки пищевода, занимающее менее 75% окружности пищевода. 10 (5,8%) пациентов с РЭ LA в стадии D, для которой было характерно выраженное повреждение слизистой пищевода по всей его окружности и занимающее более 75%. В 24 наблюдениях эндоскопически отмечали негативные формы заболевания. Следует подчеркнуть, что из 195 пациентов с ЖКБ, сочетающейся с РЭ у 12 пациентов (6,2%) имело место триада Кастена (грыжа пищеводного отверстия диафрагмы+желчнокаменная болезнь+язвенная болезнь двенадцатиперстной кишки), у 7 – триада Сейнта (3,6%) (грыжа пищеводного отверстия диафрагмы+желчнокаменная болезнь+дивертикулез толстой кишки), в 72 случаях (36,9%) наблюдались сопутствующие заболевания органов дыхания у 8 пациентов и сердечно-сосудистая система у 11 больных – 34 (47,2%) с дуоденостазом, 19 больных язвенная болезнь двенадцатиперстной кишки (n =12) и дивертикул толстой кишки (n=7). При неосложненном течении ЖКБ у 35 (20,47%) пациентов наблюдалось РЭ LA стадия А, у 51 (29,82%) РЭ LB стадия В, у 14 (8,19%) РЭ LC стадия С и у 9 (5,26%) РЭ LD стадия D. У пациентов с ЖКБ, осложненной холедохолитиазом без механической желтухи и с наличием механической желтухи в 9 (15.8%) случаях имело место РЭ LА стадия А, в 12(16,7%) – РЭ LВ стадии В, у 11 (34,4%) – РЭ LС стадии С и у 1 (10%) – РЭ LD стадии D. Достаточно большую группу составили 34 (47,2%) пациента, у которых причиной развития РЭ являлись суб- и декомпенсированные стадии дуоденостаза, установленные на основании комплексного обследования. Наличие язвенной болезни двенадцатиперстной кишки (n=12) и дивертикулеза толстой кишки (n=7) наблюдали в 19 случаях.
Больных с ЖКБ, сочетающейся с РГ, составили 92 пациента, при этом, в 71 наблюдениях (77,2%) причиной развития РГ, явились различные варианты функциональной формы ХНДП, в 13 наблюдениях (14,1%) механическая форма ХНДП, и лишь в 8 (8,7%) наблюдениях недостаточность пилорического сфинктера. У пациентов ЖКБ, сочеталась с различными степенями тяжести дуоденостаза. Так, компенсированная стадия дуоденостаза, характеризующаяся нормокинетическим типом моторики, наличием отека слизистой желудка и ДГР 0-I степени имела место у 38 (41,3%) пациентов. В 41(44,6%) наблюдении отмечался субкомпенсированный дуоденостаз, при этом во всех случаях его развитие было обусловлено смешанными причинами с гиперкинетическим типом моторики ДПК и наличием ДГР II-III степени и РГ II степени. Небольшую группу составили 13 (14,1%) пациентов с органическим дуоденостазом, причиной которого явились механические факторы. На электродуоденограммах определялся гипокинетический тип моторики с наличием ДГР III-IV степени и РГ III степени. Следует подчеркнуть, что при суб- и декомпенсированном дуоденостазе в 17 наблюдениях определяли наличие дуоденогастроэзофагеального рефлюкса с выраженными эндоскопическими и морфологическими изменениями в слизистой пищевода и желудка.
Всем больным (n=287) при поступлении и выписке проводились общепринятые клинико-лабораторные и инструментальные исследования Ультразвуковое исследование (УЗИ) проведено с помощью аппаратов ССД-256 и ССД-630 фирмы “Алока” (Япония). Для диагностики артериомезентериальной компрессии ДПК использовали УЗИ с допплерографией мезентериальных сосудов. Эндоскопическую ультразвуковую сонографию (ЭУС) проводили на аппарате ACUSON CV70 фирмы “Siemens”. Полипозиционное рентгенологическое исследование на аппарате STEFANIX фирмы SIMENS. Эзофагогастродуоденоскопию проводили на аппарате “Olimpus” (Япония), и видеогастроскопом “ Pentax - 2930” (Япония). Для оценки степени тяжести РЭ использовалась широко распространенная классификация M. Sovary – G. Miller (1978). Определение концентрации желчных кислот в желудочном соке определена методом газожидкостной хроматографии (ГЖХ), на аппарате “Хром-5” с плазменно-ионизационным детектором. Полученные данные классифицировали по степеням ДГР (0, I, II, III) по Г.И. Рычагову (1986). Кроме этого, о наличии ДГР судили по величине рН желудочного сока, полученного натощак потенциометрическим методом на рН-метре марки “рН-340”. Значения рН от 1 до 4 считали кислой, от 4 до 7 слабокислый, от 7 и выше щелочной (Clemenson, 1972). 24-часовую рН-метрию пищевода проводили с помощью рН метра “Synestic Digitrapper Mis III ”, а результаты обрабатывали на компьютере.
Для определения состояния мышц диафрагмы и нижнего пищеводного сфинктера проводили электромиографию на аппарате ЭМГСТ – 01, при анализе спектров в 2 спектральных диапазонах (0 – 30Гц и 30-500 Гц), анализ спектрально-коррелационных характеристик ЭМГ проводилось по системе MATLAB 6.1. Магнитно-резонансная томография (МРТ) проводилась на аппарате “Magnetom Concerto” – Siemens (Германия). Электродуоденографию проводили на аппарате ЭГС-4М. Электронномикроскопические исследования слизистой оболочки двенадцатиперстной кишки и начального отдела тощей кишки на наличие энтерохроматофильных клеток (ЕС-клеток) гастроэнтериновой системы, а также люминисцентно-гистохимическое исследование проводили в лаборатории электронной микроскопии НИИ общей и неотложной хирургии АМН Украины, согласно договору между ТГМУ им. Абуали ибн Сино и НИИ общей и неотложной хирургии АМН Украины. Для этого каждый препарат фиксировали в 10% нейтральном растворе формалина, и заливали в парафин по стандартной методике. Для выявления биологически активных веществ и полипептидных гормонов в парафиновых срезах толщиной 5 мк проводилась аргирофильная окраска по Масону. Во всех наблюдениях фиксирование препаратов в формалине проводилось по методу Гайдаманина Н.А. и соавт (1974) и исследовали с помощью электронной микроскопии. Ультратонкие срезы контрастировали уранилацетатом и цитратом свинца исследовали с помощью электронного микроскопа JEIM – 100S. Определение уровня серотонина (5-гидроокситриптамина) в крови проводили флюрометрическим методом по реакции с о-фталевым диальдегидом (Камышиков В.С., 2000). Для выявления серотонина в слизистой оболочки ДПК использовали люминисцентно-гистохимический метод Фалька и Хилларна в модификации Е.М. Крохиной (1969). Содержание продуктов перекисного окисления липидов (ПОЛ) в слизистой пищевода и в плазме крови определяли по уровню малонового диальдегида (МДА) и диеновых конъюгат (ДК) по реакции с тиобарбитуровой кислотой и методу Стальной. Комплексное исследование слюны проводили по методике В.К. Леонтьева и соавт (1976). При этом предварительно в слюне измеряли pH, затем к 1мл слюны добавляли 1,0мл 0,01 мл раствора HCl и вновь измеряли pH. После этого к такому же объему слюны добавляли 1,0мл 0,01н NaOH и также измеряли pH.
Оценку отдаленных результатов проводили с учетом жалоб больного и результатов дополнительных методов исследования, тех же, что и до операции. Фактические данные обработаны методами математической статистики в среде электронных таблиц Excel. Для каждого вариационного ряда определяли среднюю арифметическую (х), среднеквадратичное отклонение (б). достоверность различных средних арифметических величин определяли по абсолютному показателю точности (Р) по таблице процентных точек распределения Стьюдента в зависимости от коэффициента достоверности (t) и числа степеней свободы (n). На основании t по таблице Стьюдента определялась вероятность различия (Р). Различие считались достоверным при Р<0,05 т.е в тех случаях, когда вероятность различия составляла больше 95%.
Результаты собственных исследований и их обсуждение
Для ранней диагностики РЭ и РГ при ЖКБ и изучения роли различных патогенетических факторов в развитии сочетанных заболеваний были проведены комплексные исследования. При этом в показателях клинико-лабораторных данных крови существенных нарушений не выявлены. Комплексное УЗИ и ЭУС, проведенное пациентам было направлено не только для выявления ЖКБ и ее осложнений, но и сопутствующего РЭ и РГ. ЭУС эффективно использовали для диагностики различных стадий РЭ. (удостоверение на рацпредложение № 3235/Р-451 от 23.10.09.г. выд. ТГМУ) в 28 наблюдениях. Полученные при ЭУС данные в обязательном порядке сопоставлялись с эндоскопическими находками, а в ряде случаев, и с морфологическим результатом. Проведение УЗИ у больных с ЖКБ сочетающейся с РГ, позволило в 45 случаях выявить косвенные, а в 18 - прямые признаки ХНДП. Для диагностики механических форм ХНДП, способствующих развитию РГ у пациентов с ЖКБ, эффективно проводилось УЗИ сосудов брюшной полости, в частности, верхне-брыжеечной артерии. С целью исключения артериомезентериальной компрессии в 42 наблюдениях измеряли угол и расстояние между аортой и верхнее-брыжеечной артерией на уровне нижне-горизонтальной ветви ДПК натощак и в момент прохождения перистальтической волны. При артериомезентериальной компрессии наблюдалось пристеночное расширение нижней горизонтальной части ДПК, в стадии компенсации у 3 пациентов, а в стадии субкомпенсации у 7 больных. С несколько большей частотой выявлялся острый угол отхождения ВБА и уменьшение расстояния между аортой и ВБА менее 1см. В стадии компенсации и субкомпенсации острый угол был выявлен у 24 пациентов. В стадии декомпенсации вышеперечисленные признаки были практически у всех наблюдаемых пациентов. Для диагностики артерио-мезентериальной компрессии в 12 наблюдениях было эффективно использована разработанная в клинике методика УЗ - допплерографии верхнее - брыжеечной артерии (Патент РТ N135 23.11.2007).с подачей водной нагрузки. Рентгенологическое исследование для выявления РЭ при ЖКБ проведено 140 пациентам из 195. В результате проведенного комплексного рентгенологического исследования у 98 пациентов диагностированы косвенные признаки недостаточности кардии и наличие ГПОД. Прямые рентгенологические признаки недостаточности кардии и РЭ имели место у 42 больных: со стороны средостения (n=8), желудка (n=18) и пищевода (n=16).
Для диагностики моторно-эвакуаторной нарушений ДПК и причин развития РГ, у 92 пациентов были проведены комплексные рентгенологические исследования. В комплекс поэтапного рентгенологического исследования ДПК включались обзорная рентгенография, зондовая рентгенография, без релаксации и в условиях искусственной гипотонии ДПК с двойным контрастированием. Всего было проведено 129 различных методов рентгенологических исследований ДПК. При этом 92 пациента были больные с ХНДП, из которых в 17 (18,4%) наблюдениях диагностировались (различные проявления РЭ (B, C и D стадии). Комплексные рентгенологические исследования были также проведены 34 пациентам с РЭ II-III стадии, у которых причиной эзофагита являлась ХНДП в стадии суб- и декомпенсации.
Комплексные эндоскопические исследования показали, что из 195 пациентов с ЖКБ и РЭ у 171 имелись эндоскопические признаки РЭ. В 24 наблюдениях выявлены эндоскопически негативные ее формы. Недостаточность нижнего пищеводного сфинктера в 25 наблюдениях сопровождалась зиянием кардии, при этом в 7 наблюдениях она сочеталась с рефлюкс-эзофагитом (триада желудочно-пищеводной недостаточности). В 44 наблюдениях прямым эндоскопическим признаком РЭ являлось наличие пролапса слизистой желудка в пищевод. Еще у 48 больных с ГЭРБ в 34 наблюдениях причиной развития гастроэзофагеального рефлюкса являлся дуоденогастроэзофагеальный рефлюкс. Следует также отметить, что тяжесть течения РЭ не имела прямой зависимости от длительности существования заболевания, а определялась, прежде всего, его выраженностью. При эндоскопически негативной форме РЭ (п=24), эндоскопическое исследование в обязательном порядке включало взятие биопсии слизистой оболочки н/3 пищевода. Фиброгастродуоденоскопию проводили также 92 пациентам с ЖКБ, сочетающейся с РГ, в 87 наблюдениях были выявлены воспалительно-дегенеративные изменения в слизистой оболочке желудка и пищевода различной степени выраженности, в 17 наблюдениях, наряду с РГ различной степени тяжести, у больных диагностировали РЭ I-II степени. В 47% наблюдений диагностировано наличие моторно-эвакуаторных нарушений ДПК. Кроме воспалительно-дегенеративных изменений в слизистой желудка, в 23% случаев наблюдались структурные изменения слизистой оболочки ДПК, такие как хронический гастродуоденит, эрозивный бульбит, язвенная болезнь желудка и ДПК.
Для выяснения роли процессов ПОЛ в развитии недостаточности НПС и пилорического сфинктера желудка было изучено состояние антиоксидантной защиты слизистой НПС и зоны пилорического сфинктера желудка. Во время эндоскопии забирали биоптаты в проекции НПС и пилорического сфинктера желудка. Полученные результаты свидетельствовали о повышении уровня продуктов ПОЛ в слизистой НПС и пилорического сфинктера желудка. Так, содержание ДК составило – 1,2±0,28 ЕД.Е, МДА – 2,8±0,3 нм/мг, у пациентов с недостаточностью пилорического сфинктера эти показатели соответственно также были высокими ДК – 1,6±0,32 ЕД.Е, МДА – 2,4±0,5 нм/мг. Для подтверждения роли процессов ПОЛ в патогенезе РЭ и нарушении функции НПС в 12 наблюдениях при эндоскопически негативной форме рефлюксной болезни были исследованы содержания продуктов ПОЛ в слизистой оболочке н/з пищевода. При этом биоптаты были взяты как для морфологического исследования, так и для определения уровня продуктов ПОЛ. В 9 наблюдениях, наряду с повышением содержания ДК (2,4±0,14 ЕД.Е) и МДА (3,9±0,4нм/мг) в слизистой н/з пищевода, наблюдали морфологические изменения вследствие длительного раздражения слизистой пищевода желудочным соком. В результате проведенных исследований и полученных данных о состоянии процессов ПОЛ при РЭ у больных с ЖКБ можно утверждать, что в патогенезе нарушений функции НПС, наряду с повышением внутрибрюшного и интрагастрального давления, ведущее место отводится нарушению процессов ПОЛ в слизистой НПС и в плазме крови. По мере повышения содержания продуктов ПОЛ в слизистой НПС и пилорического сфинктера желудка наблюдается прогрессивное нарушение функции НПС с развитием РЭ, а также нарушение функции пилорического сфинктера желудка. Высокое содержание продуктов ПОЛ, в свою очередь, отрицательно влияют на морфологическую структуру НПС с развитием порочного круга, взаимоусугубляющее друг друга. Подтверждением данного взгляда является выявление у 51 пациента с ЖКБ наличие РЭ и РГ. Наряду с определением продуктов ПОЛ в биоптатах пищевода определяли хеликобактерную обсемененность. Из 68 пациентов, обследованных на наличие НР, у 39 (57,4%) диагностировали различной степени тяжести хеликобактериоз. Наличие у пациентов с ЖКБ различной степени интенсивности хеликобактериоза было особенно выражено при сочетании его с язвенной болезнью (n=11), где в 8 наблюдениях диагностировали НР II-III степени. Исследование показало значимую связь между эндоскопическими проявлениями РЭ и частотой выявления НР. Так при РЭ I стадии у 7 пациентов имело место НР I степени, у 2 – НР++. Значительные и глубокие патоморфологические изменения в слизистой пищевода у 18 пациентов с РЭ II стадии было обусловлено наличием НР++ (n=8) и НР+++ (n=7) у 13 пациентов, лишь у 7 больных наблюдался НР+- легкой степени. Из 9 пациентов с РЭ III стадии в 6 случаях имел место хеликобактериоз II-III степени и лишь в 3 – легкая степень. Важно отметить, что при диагностике НР уреазным, бактериологическим и иммунологическим методами практически во всех обследованных группах больных наблюдалось совпадение. 24 - часовую рН- метрию проводили 89 пациентам с ЖКБ, сочетающейся с РЭ (n=72) и РГ (n-17), для подтверждения диагноза РЭ и получения объективных данных о последствиях нарушения состояния замыкательного механизма кардии и сравнения данных рН-метрии с данными манометрии НПС. В большинстве случаев преобладал кислый рефлюкс желудочного содержимого – у 72 больных (80,89%), а у 17 (19,10%) пациентов – щелочной. Степень поражения слизистой пищевода была напрямую связана с числом продолжительных эпизодов рефлюкса в ночное время. Так же при РЭ II-IV степени наблюдалась выраженная экспозиция желудочного содержимого в пищеводе во время сна.
Наряду с моторикой пищевода, и связочного аппарата НПС, важное значение в самоочищении пищевода имеют “химические” факторы защиты слизистой НПС, такие как бикарбонаты слюны. Учитывая, что важной составной частью преэпителиальной защиты слизистой оболочки пищевода являются бикарбонаты слюны, обеспечивающие химическую нейтрализацию рефлюктанта, по определению буферной емкости слюны можно судить о ее способности к химической нейтрализации РЭ. Известно, что бикарбонаты слюны составляют 80% буферной емкости слюны. Результаты исследования показали, что при тяжелых и глубоких морфологических изменениях в слизистой пищевода отмечается тенденция к снижению щелочной буферной емкости слюны по щелочи (46,3±1,7 мэкв/л до 40,2±3,6 мэкв/л), что указывает на недостаточную секрецию слюны и снижение содержания бикарбонатов в составе слюны. Наоборот при РЭ II-IV степени наблюдается тенденция к повышению буферной емкости слюны по кислоте, которая увеличивает повреждающее действие рефлюктанта на слизистую пищевода. Интересные данные были получены при исследовании буферной емкости слюны у 8 пациентов с эндоскопически негативной формой РЭ. У этих пациентов наблюдалось повышение значений буферной щелочной емкости слюны (53,4±1,2 мэкв/л) по сравнению о значениями кислотной емкости (7,8±0,8 мэкв/л). Наличие достаточного количества слюны с нормальным содержанием ее компонентов обеспечивают эффективную нейтрализацию кислого рефлюкса. При РЭ наблюдается не только глубокое нарушение моторной функции пищевода, сопровождающееся кислым РЭ, но и снижение проэпителиальной защиты слизистой пищевода.
Исследование моторной функции пищевода до операции осуществляли у 209 пациентов с ЖКБ, сочетающейся с РЭ (n=192) и РГ (n=17). Практически во всех случаях выявляли нарушение замыкательной функции кардии. Длина кардиального отдела у больных ЖКБ с ГПОД (n=42) в среднем была короче более, чем в 2,5 раза по сравнению с нормой, также эти параметры были намного ниже чем у пациентов с ЖКБ, сочетающейся с РЭ, РЭ (А) и РЭ (В). Тонус НПС у этого контингента больных отличался от такового при других нозологиях своими высокими показателями. Еще одной отличительной особенностью манометрических данных больных с ГПОД было повышенное внутригрудное давление, которое было выше нормы в 1,7 раза и достоверно выше, чем в других группах больных. Вследствие вышеуказанных изменений пищеводно-желудочный градиент давления и коэффициент характеризующий отношение тонуса НПС к внутрижелудочному, был ниже нормы почти в 2,3 раза. Основной причиной недостаточности кардии у больных с ГПОД было укорочение длины НПС и повышение интрагастрального давления. При ЖКБ, сочетающейся с РЭ, на фоне недостаточности кардии (n=56) значительного укорочения длины кардии не отмечено, она составляла 2,65±0,04 см. Однако наблюдалось снижение тонуса НПС (1733±0,36 мм рт.ст.), более выраженное при сочетании с дуоденогастроэзофагеальным рефлюксом (14,26±0,2 мм рт.ст.) у 34 пациентов. Небольшое уменьшение длины кардии у пациентов с ЖКБ, сочетающейся с РЭ, РЭ и РГ, обусловлено низким тонусом НПС, когда подъем и снижение давления в начале и в конце регистрации мало отличается от давления в желудке и пищеводе. Сопоставление данных манометрии пищеводно-желудочного перехода, показало, что снижение тонуса НПС, укорочение пищевода, а также повышение интрагастрального давления, способствовали развитию более тяжелых морфологических изменений в слизистой оболочке пищевода. При снижении тонуса НПС у пациентов с тяжелыми формами РЭ свидетельствует о том, что в области НПС у 90% больных наблюдали тяжелые проявления РЭ и наличие выраженной слабости НПС, способствовающее беспрепятственному забросу кислого желудочного содержимого в пищевод. Полученные в ходе исследования новые данные свидетельствуют о том, что именно гипотензия НПС, обусловленное в том числе повреждающим действием продуктов ПОЛ и снижением бикарбонатной защиты слюны, способствует развитию глубоких морфологических изменений в слизистой пищевода. Для диагностики степени тяжести ХНДП при ЖКБ, сочетающейся с РГ (n=92) и РЭ (n=37), в 127 наблюдениях проводили поэтажную манометрию и электродуоденографию, при этом в 21 наблюдении диагностировали компенсированную стадию ХНДП, в 44 - суб- и в 12 - декомпенсированную стадию. При сопоставлении стадии ХНДП с тяжестью дуоденогастрального рефлюкса (ДГР) установлено, что компенсированной стадии соответствует ДГР I-II степени, субкомпенсированной и декомпенсированной ДГР II-III степени. У 51 пациента с ЖКБ, имело место наличие РЭ и РГ, при этом, у 39 больных причиной морфологических изменений в слизистой пищевода являлось дуоденогастроэзофагеальный рефлюкс. Для более объективной оценки состояния моторной функции ДПК у 54 пациентов были проведены электрофизиологические исследования моторной функции ДПК. Во время изучения данных электродуоденографии (ЭДГ), нами как и при гастрографии обнаружено 3 типа ЭДГ. Наличие гиперкинетического типа ЭДГ выявили у 38, (70,37%) пациентов из 54 гипокинетический тип ЭДГ – у 5(9,26%) и нормокинетический тип ЭДГ у 11 (29,37%) пациентов.
Для более глубокого и всестороннего изучения состояния НПС и факторов, влияющих на его функцию, нами у 56 больных проведены электроэзофагография и электромиографии НПС. Результаты электрофизиологических методов исследования пищевода у пациентов с ЖКБ показали, что в подавляющем большинстве случаев, по мере снижения амплитуды и продолжительности сокращения пищевода, наблюдаются глубокие морфологические нарушения в слизистой оболочке пищевода. Комплексное дооперационное рентгенологическое и интраоперационное исследование величины угла Гиса было проведено у 128 пациентов с ЖКБ, сочетающейся с РЭ и РГ. Полученные результаты исследования показали, что наличие острого угла Гиса имело место у 53 пациентов (41,41%) из 128. Чаще всего наличие острого угла Гиса определялось у пациентов с ЖКБ, у которых причиной РЭ являлась недостаточность НПС (n=21) и ГПОД (n=20), несколько реже (n=12) при наличии дуоденогастроэзофагеального рефлюкса. Прямой угол Гиса был обнаружен у 39 (30,47%) больных, при этом, в 29(22,66% ) случаях он имелся у пациентов с ЖКБ+недостаточность НПС в 10 у больных с ЖКБ+ГПОД (n=5) и ЖКБ+РЭ+РГ (n=5). Наличие тупого угла Гиса имело место в 36 (28,13%) наблюдениях при ЖКБ+недостаточность НПС (n=18), ЖКБ+РЭ+РГ (n=11) и ЖКБ+ГПОД (n=7). Следует подчеркнуть, что между размерами ГПОД и величиной угла Гиса корреляционной связи не выявлено. При наличии РЭ С и РЭ D у 27 пациентов из 90, острый угол Гиса наблюдался у 13 больных, у 5 больных угол Гиса была прямой, и у 9 – тупой. Пациенты с РЭ А и РЭ В (n=63) в 29 (32,22%) наблюдениях имели острый угол Гиса в 21 случае угол Гиса оказался тупым и в 13 случаях – прямым. Наличие острого угла Гиса в 29 наблюдениях не дало возможности развития тяжелых форм РЭ, а еще у 21 пациента с тупым углом Гиса не наступило прогрессирования РЭ А и РЭ В. Полученные в результате исследования данные убедительно доказывают, что не величина угла Гиса определяет замыкательную функцию кардии, а недостаточность функции кардии способствует ее притуплению. Наряду с измерением величины угла Гиса, нами проведено исследование расстояния между ножками диафрагмы у 128 пациентов с ЖКБ, сочетающейся с РЭ. При этом, в 87 наблюдениях (62,97%) измерения проводили во время открытых операций, в 41 (32,03%) - при эндовидеохирургических вмешательствах. В 103 (80,47%) наблюдениях расстояние между ножками диафрагмы не было изменено и соответствовало 3,5-4,0 см. при норме 3,5-4 см. Расширение пищеводного отверстия диафрагмы было обнаружено у 12 пациентов и оно не превышало 4-7 см. Расширение расстояния между ножками диафрагмы более 7 см имело место у 13 больных и было характерно для больных с ГПОД. Сопоставление морфологических и эндоскопических данных с величиной расстояния между ножками диафрагмы у 90 пациентов на какую либо взаимосвязь не указало. Таким образом, величина угла Гиса и расстояния между ножками диафрагмы не оказывают существенного влияния на развитие РЭ, а лишь подчеркивают признак ГПОД.
Неудовлетворительные результаты холецистэктомии в большинстве случаев связаны с развитием различных патологических состояний, объединенных в понятие постхолецистэктомический синдром (ПХЭС). Среди многочисленных причин, приводящих к развитию ПХЭС, особое место отводится несвоевременной диагностики и хирургической коррекции РЭ и РГ, которые в отдаленном послеоперационном периоде осложняются постхолецистэктомическим РЭ и РГ. Для выявления причин развития ПХЭ РЭ и ПХЭ РГ нами проведено глубокое, тщательное и всестороннее изучение и анализ возникновения ПХЭ РЭ и ПХЭ РГ у 74 пациентов, оперированных в различных лечебных учреждениях Республики Таджикистан с 1995 по 2000 годы. Непосредственными причинами развития ПХЭ РГ и РЭ являются: 1) игнорирование факта сочетания ЖКБ с ГПОД, ХНДП и значения нарушений функций НПС и моторных нарушений ДПК в развитии ЖКБ РЭ и РГ, а также неосведомленность практических врачей о патогенетической связи ЖКБ+ГПОД и РЭ; 2) отсутствие рациональной схемы обследования больных с ЖКБ с учетом нарушений моторной функции НПС и ДПК и включения в комплекс исследований рН–метрии, поэтажной манометрии, эндоскопических и рентгенологических исследований по показаниям; 3) нерациональный выбор способа холецистэктомии и доступа при наличии клинических и инструментальных признаков РЭ и РГ; 4) неадекватная, неполноценная ревизия пищевода, желудка, двенадцатиперстной кишки и начального отдела тонкой кишки; 5) отказ от проведении интраоперационных методов диагностики РЭ и РГ при наличии спаечных процессов в зоне пищеводно-желудочного перехода и дуоденоеюнального изгиба, либо при умеренном расширении ДПК и пищеводного отверстия диафрагмы; 6) отказ от выполнения сочетанных оперативных вмешательств при холецистэктомии на пищеводном отверстии диафрагмы, Трейтцовой связке и перипроцессах в области ДПК; 7) развитие ранних послеоперационных осложнений (желчеистечения, кровотечения, подпеченочные абсцессы) на фоне имеющихся нарушений моторной функции ДПК, которые способствуют прогрессированию заболевания в отдаленном периоде; 8) отсутствие опыта для выполнения сочетанных (симультанных) операций на желчевыводящей системе, пищеводе, желудке и ДПК.
Полученные в процессе комплексного клинико-инструментального и специального методов исследования, а также ретроспективный анализ развития ПХЭ РЭ и РГ у 74 больных, позволили нам провести глубокое изучение патогенетических механизмов развития и связей ЖКБ с РЭ и РГ. Наряду с механическими факторами в патогенезе ХНДП ведущее место отводится нарушению моторной функции ДПК, обусловленной гуморальными факторами. Эффективность сократительной способности ДПК обусловлена не только активностью вегетативной нервной системы и ауэрбаховской иннервации, но и гуморальными факторами. На нервные механизмы регуляции моторики ДПК оказывают положительное влияние также биологически активные вещества серотонин, гистамин, кишечное вещество, субстанция Р и ангиотензин. В этой связи изучение гуморальной регуляции ДПК интестинальными гормонами, вырабатываемыми APUD (Amine Precursor Uptake and Decarboxyiontien) системой, которые в свою очередь вырабатывают серотонин, позволяет выяснить теневые стороны патогенеза ХНДП и развития ЖКБ.
Учитывая связь между содержанием серотонина в крови и состоянием гастроэнтериновой системы была поставлена задача на основании электронно-микроскопических исследований изучить морфологическое состояние ЕС-клеток энтериновой системы ДПК у 38 пациентов с различными стадиями ХНДП и содержанием серотонина в крови. При этом 14 пациентов были с компенсированной стадией ХНДП, 16 с субкомпенсированной и 8 больных были с ХНДП декомпенсированной стадии. Следует подчеркнуть, что из 38 пациентов с различными стадиями ХНДП у 17 имел место дуоденогастроэзофагеальный рефлюкс, в связи с чем у этих пациентов биоптаты для морфологического исследования брали из слизистой пилорического отдела желудка и области НПС. Результаты электронномикроскопических исследований показали, что прогрессирование ХНДП сопровождается глубокими дисторофическими и деструктивные изменениями ЕС-клеток. Наблюдается очаговый лизис внутриклеточных мембранных цитоплазматических структур. Разрушение наружных мембран и крист митохондрий свидетельствует о глубоких нарушениях окислительно-восстановительных процессов. Следствием этих нарушений является и резкое снижение секреторной активности ЕС-клеток. Подтверждением этого положения могут служить обнаруженные участки фрагментации мембран гранулярного эндоплазматического ретикулума, уменьшение количества рибосом на поверхности его мембран, а также общее снижение числа свободно лежащих в цитоплазме рибосом, редукция пластинчатого цитоплазматического комплекса Гольджи с появлением в области его локализации вторичных лизосом, и резкое сокращение количества секреторных гранул в цитоплазме. Все это вместе взятое дает возможность утверждать, что при терминальных стадиях ХНДП снижается количество синтезируемого серотонина. Выявленные нарушения ультраструктурной организации органелл ЕС-клеток в стадии декомпенсации указывают на превалирование катаболических реакций над синтетическими. Следует отметить, что глубина и степень выраженности субмикроскопических перестроек ЕС-клеток являются обратимыми у пациентов с компенсированной стадией ХНДП. Выявленые в результате электронно-микроскопического исследования ультраструктурные изменения органелл клеток, синтезирующих серотонин, у больных с компенсированной стадией ХНДП указывают на снижение уровня синтеза этого фермента. По степени выраженности и глубине обнаруженных нарушений ультраструктур их можно отнести к компенсаторно-адаптационным. Вместе с тем, при ХНДП в компенсированной стадии наблюдается умеренное снижение количества синтезируемого серотонина ЕС- клетками ДПК. Параллельно с этим, в отдельных клетках наблюдаются и процессы функционального напряжения, усиления репаративных и синтетических процессов. Это можно объяснить включением резервных внутриклеточных механизмов компенсации в ответ на негативное воздействие ХНДП. В группе больных с ХНДП в субкомпенсированной стадии наблюдается углубление дистрофического процесса и переход его в деструктивную фазу. В группе больных с ХНДП в декомпенсированной стадии глубина дистрофических нарушений в ЕС-клетках еще более сдвигается в сторону превалирования деструктивных нарушений. Структурно это выражается в лизисе участков ядерной мембраны, наружной мембраны и крист митохондрий, очаговой деструкции мембран гранулярной эндоплазматической сети, резком снижении количества секреторных гранул. Часть ЕС-клеток этой группы больных подвержена очаговому разрушению внутриклеточных мембранных систем, что приводит к значительному снижению активности синтеза серотонина. Изучение биопсийного материала слизистой оболочки ДПК у больных с различными стадиями ХНДП с помощью люминисцентно-гистохимического метода показало, что по мере прогрессирования патологического процесса в слизистой оболочке ДПК наблюдается прогрессивное ее снижение (табл. 1). При этом установлено, что прогрессирование патологического процесса в слизистой оболочке ДПК сопровождается снижением уровня серотонина во всех структурах слизистой оболочки, особенно в стадии суб - и декомпенсации. Снижение синтеза серотонина в слизистой оболочке ДПК, в свою очередь, приводит к уменьшению его количества в крови.
Таблица 1
Уровень серотонина (в усл. ед.) в структурах ДПК при ХНДП (M±m;n=28)
| Группы обследованных | Структуры | |||
| Энтерохромофильные клетки | Железистый эпителий | Соединительная ткань | Межклеточное вещество | |
| здоровые (n=25) | 5,2±0,3 | 4,7±0,3 | 3,5±0,7 | 3,1±0,3 |
| с компенсированной стадией ХНДП (n=14) | 4,9±0,2 | 9,7±0,5 Р<0,001 | 9,2±0,3 Р<0,001 | 8,4±0,5 Р<0,001 |
| с субкомпенсированной стадией ХНДП (n=10) | 3,2±0,5 Р<0,05 | 4,2±0,4 | 3,1±0,7 | 2,9±0,1 |
| с декомпенсированной стадией ХНДП (n=4) | 1,3±0,4 Р<0,001 | 3,0±0,7 | 2,8±0,4 | 2,1±0,4 |
Примечание: Р-значимость различих средных показателей со средным значениям здоровых
Исследование содержания уровня серотонина в крови у пациентов с различной степенью тяжести ХНДП подтвердилась уменьшением количества ЕС-клеток слизистой ДПК, полученных при электронной микроскопии (табл.2).
Таблица 2
Соотношение содержания серотонина в крови в зависимости от стадии ХНДП у больных с ЖКБ (M±m; n=38)
| Показатель | Стадии ХНДП | ||
| Компенсиро- ванная (n=14) | Субкомпенсиро- ванная (n=16) | Декомпенси- рованная (n=8) | |
| Содержание серотонина в крови, мкмоль/л | 0,7±0,13 | 0,5±0,18 | 0,3±0,23 |
Электронно-микроскопическое исследование ЕС-клеток в биоптатах из слизистой оболочки ДПК, пилорического отдела желудка и НПС, проведенное у 17 пациентов с ЖКБ, имеющих суб- и декомпенсированную стадии ХНДП с выраженным явлением дуоденогастроэзофагеального рефлюкса, показало, что по мере прогрессирования нарушений моторной функции ДПК наблюдается уменьшение количества ЕС-клеток, что очевидно, обусловлено блокадой секреторной активности серотонинпродуцирующих клеток НПС и пилорического отдела желудка. Блокада секреторной активности серотонин-продуцирующих клеток сопровождалась выраженной активностью процессов ПОЛ в слизистой НПС и в крови, что способствовало прогрессированию дистрофических процессов в области НПС (табл.3)
Таблица 3
Содержание серотонина и продуктов ПОЛ в крови и в слизистой у пациентов с ЖКБ и РЭ (M±m; n=18)
| Показатели ПОЛ | Рефлюкс эзофагит | |||
| РЭ А (n=6) | РЭ В (n=4) | РЭ С (n=5) | РЭ D (n=2) | |
| В крови: ДК, ед.Е | 2,3±0,8 | 2,4±0,34 | 2,5±0,24 | 2,6±0,12 |
| МДА, нм/мг | 3,1±0,2 | 3,3±0,9 | 3,8±0,6 | 4,0±0,7 |
| Витамин Е, мг% | 0,84±0,3 | 0,76±0,14 | 0,61±0,21 | 0,42±0,38 |
| В слизистой НПС: ДК, ед.Е | 1,1±0,12 | 1,4±0,16 | 1,7±0,21 | 1,9±0,34 |
| МДА, нм/мг | 2,4±0,2 | 2,6±0,3 | 2,7±0,5 | 2,8±0,3 |
Полученные данные свидетельствуют, что нарушение выработки серотонина в ДПК уже в ранних сроках своего развития приводит к блокаде активности серотонин-продуцирующих эндокринновых клеток (ЕС-клеток) ДПК, пилорического отдела желудка и НПС. На основании проведенного исследования разработана схема патогенеза ХНДП (рис.1).
Рис.1. Схема патогенеза ХНДП
Согласно разработанной схеме патогенеза ХНДП, вследствие многообразных причин локализующих в слизистой оболочке ДПК, происходит уменьшение количества функционирующих ЕС-клеток, продуцирующих серотонин. Уменьшение количества ЕС-клеток в ДПК приводит к снижению синтеза серотонина и его концентрации в крови, которое сопровождается нарушением, а точнее, снижением моторно-эвакуаторной функции ДПК. Различной степени выраженности нарушения двигательной функции ДПК приводят к развитию или усугублению воспалительного процесса в слизистой оболочке ДПК и блокированию серотонин-секретирующих клеток желудочного кишечного тракта с развитием порочного патологического круга, способствующего прогрессивному уменьшению ЕС-клеток и синтеза серотонина. Длительное нарушение моторной функции ДПК, обусловленное дефицитом серотонина, в последующем приводит к расширению ДПК и глубоким морфологическим изменениям в нервном аппарате ДПК с развитием ХНДП. Следует отметить, что нарушение моторной функции ДПК сопровождающееся повышением давления в просвете ДПК и желудка, которая способствует развитию дисфункции НПС. Кроме этого, наблюдавщаяся при ХНДП блокада серотонин-секретирующих клеток ЖКТ, охватывает и слизистую пищевода, нарушая ее моторику, что в последующем приводит к нарушению процессов ПОЛ в слизистой пищевода и НПС с развитием дистрофических изменений в ней и развития РЭ.
Результаты электронно-микроскопических исследований ЕС-клеток слизистой ДПК, пищевода и желудка, а также данных инструментального исследования 51 пациента с ЖКБ, сочетающейся с РЭ и РГ, и 17 пациентов с ПХЭ РЭ и ПХЭ РГ подтверждают приведенную концепцию развития РЭ при ХНДП. Нарушения моторно-эвакуаторной функции ДПК могут явиться одним из патогенетических факторов развития ЖКБ. Для определения роли нарушения двигательной функции ДПК в патогенезе ЖКБ у 46 пациентов с различной степенью тяжести ХНДП нами проведено комплексное исследование биохимического состава желчи и крови.
Исследования показали, что, по мере прогрессирования нарушений моторной функции ДПК наблюдается нарушение коллоидного равновесия желчи, перенасыщение холестерином, снижение концентрации желчных кислот и т.д. У пациентов с ХНДП в стадии декомпенсации показатели физико-химических свойств желчи прогрессивно ухудшались по сравнению с таковыми у пациентов с ХНДП в стадии компенсации и субкомпенсации. Так, повышалось содержание общего билирубина (0,84±0,9ммоль/л) и (10,82±0,32ммоль/л), наблюдалось снижение суммарного количества желчных кислот (СЖК) (25,8±0,68 ммоль/л) как в порции “В”, так и “С”. Таким образом, у пациентов с суб- и декомпенсированной стадиями ХНДП, наблюдаются нарушения дренажной функции желчевыводящих путей, повышение литогенности желчи и риск развития ЖКБ. Проведенное электронно-микроскопическое исследование ЕС-клеток слизистой оболочки ДПК, а также изучение содержания серотонина в крови, изменения биохимического состава желчи при различных степенях тяжести моторно-эвакуаторной нарушении ДПК, позволили разработать схему патогенеза ЖКБ. (Рис.2)
Рис. 2. Схема патогенеза ЖКБ.
Одним из пусковых моментов в патогенезе ЖКБ является снижение количества ЕС-клеток ДПК, способствующее снижению выработки серотонина, что приводит к снижению моторно-эвакуаторной функции ДПК. Процесс сопровождается интрадуоденальными гипертензиями, и препятствует нормальной эвакуации желчи из дистальных отделов желчных протоков в ДПК. По мере прогрессирования заболевания происходит нарушение метаболизма желчи и желчных кислот со снижением бактериоцидности желчи и дисфункцией терминального отдела тонкой кишки и БДС. Нарушение метаболизма желчи и транслокаций бактерий, а также дисбактериоз в последующем приводят к камнеобразованию.
Показанием к коррекции РЭ и РГ при ЖКБ является неэффективность консервативных методов лечения при наличии глубоких морфологических изменений в пищеводе, желудке и ДПК, а также при экстрапищеводных проявлениях РЭ. В наших наблюдениях показаниями к выполнению корригирующих операций при ЖКБ с РЭ и РГ являлись: 1) осложненное течение РЭ и РГ; 2) сохранение симптомов заболевания и частый рецидив РЭ и РГ; 3) грыжа пищеводного отверстия диафрагмы и ХНДП; 4) стойкая гипотония НПС. Основной и главной целью операции при ЖКБ с РЭ и РГ является не только удаление желчного пузыря, восстановление нормального желчеоттока по внепеченочным желчным путям, но и выполнение патогенетически обоснованных антирефлюксных вмешательств, способствующих восстановлению нарушенных анатомических позиций дуоденоеюнального и эзофаго-гастрального переходов, а также НПС. При выполнении корригирующих вмешательств направленных на ликвидацию причин РЭ, независимо от выбора метода оперативного вмешательства мы придерживались следующих принципов:1) восстановление зоны высокого давления в области пищеводно-желудочного перехода; 2) восстановление абдоминальной позиции дистального отдела пищевода (не менее 2,0 см); 3)восстановление длины нижнего пищеводного сфинктера (не менее 3 см); 4) сохранение проходимости дистального отдела пищевода и кардии; 5) устранение дефектов диафрагмальных ножек; 6) устранение высокого интрадуоденального давления. Следует отметить, что в своих исследованиях мы дополняли предложенное Tom De Meester дополнительных принципов. Показаниями к проведению хирургической коррекции РГ при ЖКБ в наших наблюдениях являлись: 1) наличие механических форм ХНДП, способствующих развитию РГ; 2) РГ, осложненное РЭ; 3) сочетание язвенной болезни+ РЭ+ РГ на почве ХНДП; 4) суб- и декомпенсированные формы функционального дуоденостаза. При наличии РГ и осложненных форм ЖКБ, когда возникает необходимость в выполнении корригирующих вмешательств на внепеченочных желчных путях, практически во всех ситуациях выполняли вмешательства, направленные на выключение ДПК из желчеоттока. Показания к операции по поводу РГ определяли строго индивидуально с учетом причин возникновения РГ, тяжести течения заболевания и характера патологических изменений во взаимосвязанных органах. Учитывая тот факт, что в наших наблюдениях РГ сочетался с ЖКБ во всех случаях, независимо от стадии выраженности ХНДП, производили коррекцию выявленных нарушений. Дренирующие ДПК операции, направленные, главным образом, на опорожнение ДПК, выполняли при ХНДП в стадии компенсации и субкомпенсации. В этих случаях предпочтение отдавали операции Стронга и различным вариантам дуоденоеюностомии. В стадии декомпенсации, учитывая неэффективность шунтирующих ДПК оперативных вмешательств, помимо выполнения шунтируюущих ДПК операций, выполняли оперативные вмешательства эффективно коррегирующие дуоденогастральный рефлюкс, предупреждающие развитие нарушений типа «порочного круга» и возможного возникновения пептической язвы и рака культи желудка. В этом отношении наиболее эффективным методом операции являлись комбинированные вмешательства на ДПК. Выбор метода и объем хирургической коррекции РЭ и РГ при ЖКБ, основывалось на результатах специальных методов исследования (24-часовой рН - метрии, ЭЭГ, ЭГГ, манометрии пищевода, желудка и ДПК, а также рентгенологических данных), и характера осложнений ЖКБ, сопутствующей патологией и возраста пациентов. Следует отметить, что результаты дооперационных клинико-инструментальных и специальных методов исследования во всех случаях ориентировали нас на выбор корригирующей антирефлюксной операции. Однако окончательный объем и характер коррегирующей операции выбирался во время лапаратомии или видеолапараскопии.
В предоперационном периоде больным с РЭ В и С и РЭ Д назначали медикаментозную терапию, включающую следующие группы препаратов: 1) блокаторы желудочной секреции; 2) прокинетики; 3) антациды; 4) лекарственные средства, обладающие защитным и восстанавливающим действием на слизистую желудка и пищевода; 5) антихеликобактерную терапию. С целью комплексной, патогенетически обоснованной, предоперационной подготовки широко использовали терапию второй линии: ингибитор протоновой помпы (омепрозол) в стандартной дозе 2 раза в день + висмута субсалицилат субцитрат (Де–нол) - 120 мг 4 раза в день +метронидазол - 500 мг 3 раза в день + кларитромицин - 500 мг х 2 раза в течение 7 дней. На основании разработанной концепции патогенеза ЖКБ, РЭ и РГ и выявления роли нарушения обмена серотонина, для проведения предоперационной консервативной терапии, а также комплексного лечения нарушений моторно-эвакуаторной функции ДПК, в 34 наблюдениях эффективно применяли препарат серотонин–адипинат по 2 мл внутривенно 2 раза в сутки на 20 мл физиологического раствора в течение 6-7 дней. Следует подчеркнуть, что после проведенного консервативного лечения серотонин–адиптином в значительной степени наблюдалось улучшение моторной функции ДПК у 29 пациентов, выражающееся в существенном изменении показателей функциональной пробы ДПК.
Применение серотонин-адиптина в качестве препарата, повышающего содержание серотонина, способствовало на 7-8 сутки восстановить моторно-эвакуаторную функцию ДПК, о чем свидетельствовали результаты специальных методов исследования приведенных в таблице.
Для лечения больных с ЖКБ, сочетающейся с РЭ, выполнялись как традиционные открытые методы лечения ЖКБ и РЭ, так и видеолапароскопические. Так, открытая традиционная холецистэктомия с коррекцией РЭ проведена 125 (64,1%) пациентам из 195. В 70 (35,9%) наблюдениях мы прибегали к одновременной видеолапароскопической холецистэктомии и коррекции РЭ (табл 4).
Таблица 4
Характер открытых и видеолапароскопических вмешательств при ЖКБ и РЭ (n=195)
| Характер оперативных вмешательств | Кол. | % |
| Фундопликация по Ниссен+холецистэктомия | 19 | 9,7 |
| Гемифундопликация по Dor+ холецистэктомия | 7 | 3,6 |
| Комбинированная гемифундопликация по Тупэ+ холецистэктомия | 13 | 6,7 |
| Комбинированная фундопликация по Ниссен+холецистэктомия + холедохолитотомия +Дренирование холедоха по Робсону | 8 | 4,1 |
| Комбинированная гемифундопликация по Тупэ+ холецистэктомия+ холедохолитотомия+ХДА по Юрашу-Виноградову | 9 | 4,6 |
| Комбинированная гемифундопликация по Тупэ+ холецистэктомия+ холедохолитотомия+ХДА по методике клиники | 7 | 3,6 |
| СПВ с фундопликацией по А.Ф. Черноусову+иссечение язвы с пилородуоденопластикой+ холецистэктомия | 10 | 5,1 |
| СПВ с комбинированной фундопликацией по Ниссену+ холецистэктомия +иссечение язвы+пилородуодено-пластика | 8 | 4,1 |
| Холецистэктомия+резекция желудка по Ру с фундопликацией по Ниссену | 24 | 12,3 |
| Гемифундопликация по Тупэ+ холецистэктомия+дуоденоеюноанастомоз по Грегуара | 13 | 6,7 |
| Фундопликация по Ниссен+холецистэктомия+резекция толстой кишки | 7 | 3,6 |
| Видеолапароскопическая фундопликация по Ниссен+ холецистэктомия | 34 | 17,5 |
| Видеолапароскопическая гемифундопликация по Тупэ | 12 | 6,1 |
| Видеолапароскопическая гемифундопликация по Dor | 10 | 5,1 |
| Видеолапароскопическая фундопликация по Ниссен+ холецистэктомия+холедохолитотомия с дренированием по Холстеду - Пиковскому | 8 | 4,1 |
| Видеолапароскопическая пластика пищеводного отверстия диафрагмы эндопротезом+холецистэктомия | 6 | 3.1 |
| Всего | 195 | 100 |
Так, при наличии РЭ и ЖКБ в 47 наблюдениях выполняли фундопликацию по Ниссену (n=19) и гемифундопликацию (n=20), в том числе по Dor (n=7) и комбинированный метод Тупэ (n=13). Следует подчеркнуть, что в 8 наблюдениях была выполнена разработанная нами совместно с кафедрой торакоабдоминальной хирургии ХМАПО методика хирургической коррекции недостаточности кардии путем двусторонней фундокрурофренопексии (ФКФП) комбинированной фундопликации по Ниссену ( автор. свидет.№0269) в сочетании с холедохолитотомией и дренированием холедоха по Робсону Методика отличается от фундопликации по Ниссену тем, что накладывают 2-3 шва на ножки диафрагмы, по очереди завязывают швы, суживая пищеводное отверстие диафрагмы так, чтобы можно было провести кончик указательного пальца в пищеводное отверстие рядом с пищеводом. Нити, которыми выполнена крурорафия, несрезают. Левым рядом несрезанных нитей проводят заднюю фундокрурорафию с вовлечением задней стенки дна желудка, завязывают и срезают швы. Вторым рядом нитей проводят переднюю фундокрурорафию: захватывают переднюю стенку дна желудка и подшивают ее к задней стенке последнего, завязывают второй ряд швов. Таким образом, пищевод на протяжении 3-5 см на 3600 окутывают дном желудка и фиксируют к сведенным ножкам диафрагмы (рис. 3). Показанием к комбинированной фундопликации с двухсторонней крурофундоэзофагофренопексией считали выраженную гипотонию НПС, наличие эрозивно-язвенного поражения слизистой оболочки пищевода
Показанием к комбинированной фундопликации с двухсторонней крурофундоэзофагофренопексией считали выраженную гипотонию НПС, наличие эрозивно-язвенного поражения слизистой оболочки пищевода.
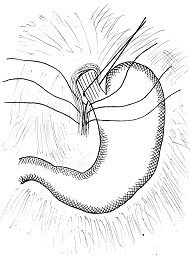
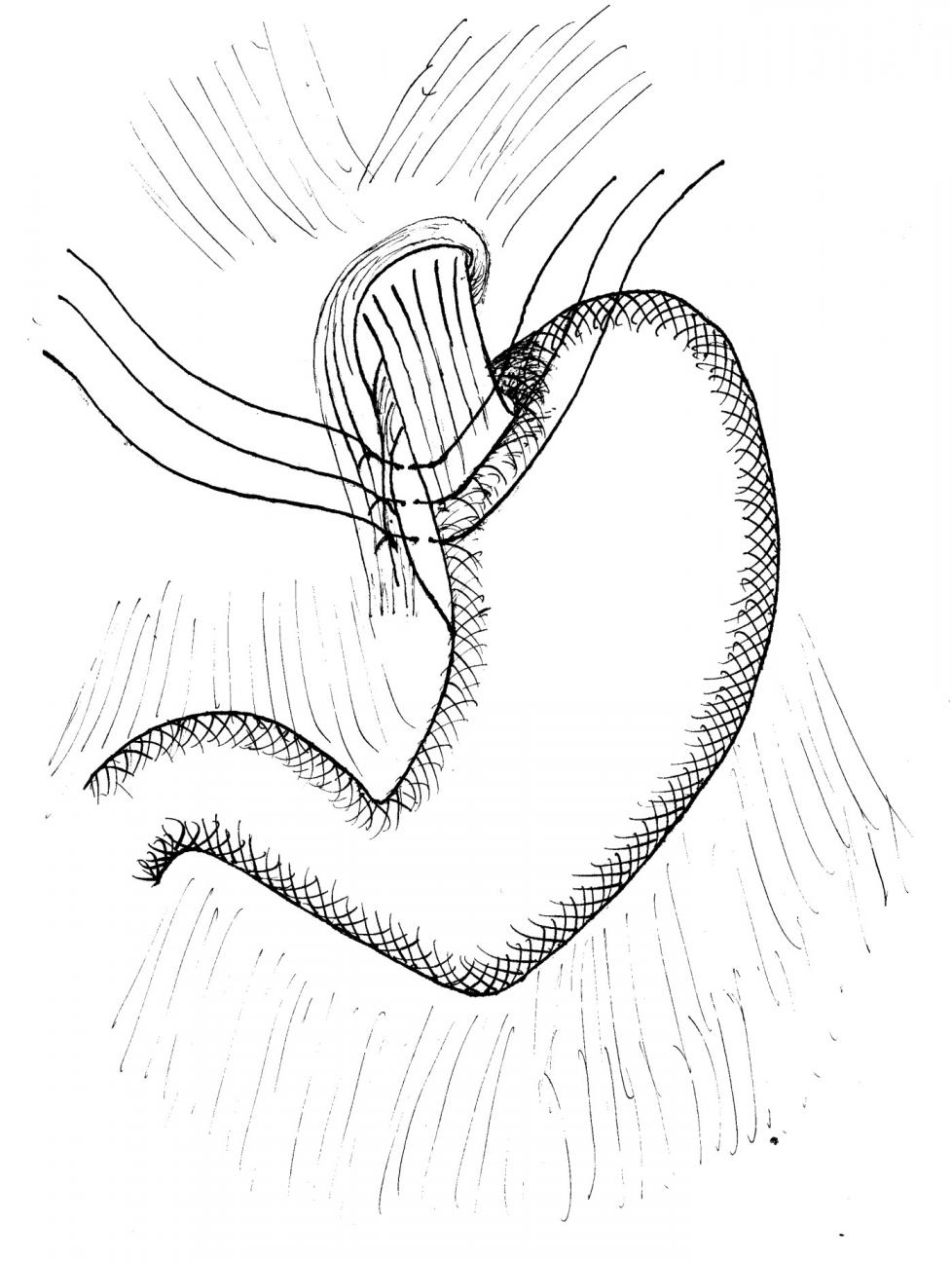


Рис.3. Способ комбинированной фундопликации. Двусторонняя крурофундоэзофагофренопексия
В 16 наблюдениях у пациентов с холедохолитиазом c механической желтухой (n=11) комбинированную гемофундопликацию по Тупэ (автор. свидет.№0270) сочетали с холедохолитотомией и формированием холедоходуоденоанастомоза по Юрашу-Виноградову (n=9) и холедоходуоденоанастомозом по методике клиники (n=7). Особенностью комбинированной фундопликации (аналог – фундопликация Toupet) является то, что проводят заднюю ФКФП с увлечением задней стенки дна желудка и пищевода, завязывают и срезают швы. Таким образом, пищевод на протяжении 3-5 см на 240-2700 окутывают дном желудка и фиксируют к сведенным ножкам диафрагмы(рис.4).
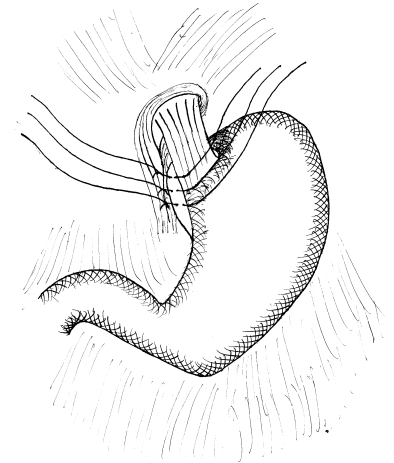
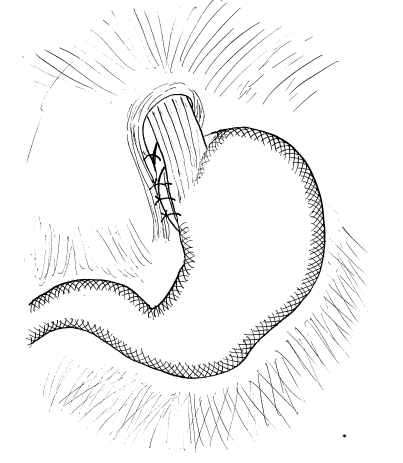
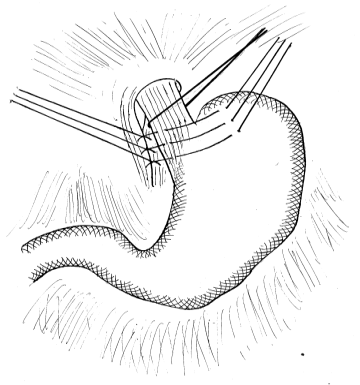
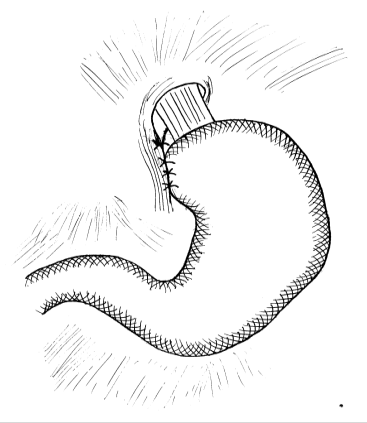
Рис.4 Комбинированная задняя и передняя гемифундопликация
Показаниям к выполнению различных вариантов гемифундопликации с крурорафией являлись: а) незначительные нарушения тонуса НПС (>15 мм рт.ст.), которые ведут к РЭ только при значительных повышения интрагастрального давления (10-15 мм рт.ст.) б) первичные нарушения перистальтики пищевода с наличием гипотонии НПС (<15 мм рт.ст.). Для профилактики регургитационного холангита нами разработан способ формирования холедоходуоденоанастомоза, в значительной степени уменьшающий частоту дуоденобилиарного рефлюкса и его несостоятельности (Патент РТ № 70 от 13.12.2006), а для облегчения оперативных вмешательств на печени и желчных протоках разработан ретрактор печени (Патент РТ № 118 от 21.09.2008). В 18 наблюдениях при наличии триады Кастена (n=12) (ЖКБ+ГПОД+язвенная болезнь ДПК), а также при высоких показателях желудочной секреции в I фазе (n=6), коррекцию РЭ производили путем выполнения СПВ и фундопликации по методике А.Ф. Черноусова (n=10), а также выполняли комбинированную фундопликацию по Ниссену (n=8). Следует подчеркнуть, что в 44 наблюдениях у пациентов с ЖКБ и РЭ наблюдалось наличие ХНДП в стадии суб- и декомпенсации (n=34), что требовало соответствующей хирургической коррекции. Для этого в 21 наблюдении выполняли холецистэктомию с резекцией желудка по Ру, с фундопликацией по Ниссену, в 13 случаях выполняли заднюю гемифундопликацию по Тупэ в сочетании с крурорафией по Харрингтону с последующим выполнением холецистэктомии с модифицированным дуоденоеюноанастомозом по Грегуару. В 7 наблюдениях, при наличии у пациентов триады Сейнта (ГПОД+ЖКБ+дивертикулез толстой кишки), прибегали к фундопликации по Ниссену, холицистэктомии и субтотальной резекции толстой кишки. Арефлюксные эндовидеохирургические вмешательства на кардии в сочетании с холецистэктомией выполнены 70 больным. При этом, у 6 пациентов с целью коррекции ГПОД и РЭ, эффективно применяли эндопротез. Следует подчеркнуть, что во всех случаях операцию начинали с антирефлюксного вмешательства, после чего выполняли холецистэктомию. Пластику пищеводного отверстия диафрагмы сетчатым трансплантантом выполнили 6 больным с ЖКБ, сочетающейся с РЭ. Показанием к применению сетчатого трансплантанта в наших наблюдениях являлось расширение пищеводного отверстия диафрагмы более 5 см с выраженной слабостью тканей диафрагмы, а также при наличии факторов, предрасполагающих к повышению внутрибрюшного давления. В своих исследованиях в качестве трансплантатамы эффективно применяли полипропиленовые сетки – наиболее длительно и широко используемые. Фиксацию сетки позади пищевода поверх задней крурорафии осуществляли у 4 пациентов. При этом фиксировали лоскут в виде прямоугольника в перпендикулярном направлении, перекрывая частично ножки диафрагмы. В 2 наблюдениях трансплантанты фиксировали к ножкам диафрагмы без крурорафии. Данную методику использовали при больших скользящих грыжах пищеводного отверстия диафрагмы. Во всех случаях в конце операции, операционное поле тщательно промывается и проводится контроль гемостаза. После чего приступают к выполнению видеолапароскопической холецистэктомии. В 2 наблюдениях, при наличии у пациентов холедохолитиаза выполняли лапароскопическую холедохолитотомию с проведением интраоперационной холангиографии. После завершении всех этапов эндоскопических вмешательств завершали операцию подведением страховочного дренажа. Выполнение различных антирефлюксных вмешательств на кардии в сочетании с холецистэктомией у 195 пациентов сопровождалось в 27 (13,8%)случаях ранними осложнениями. При этом после традиционных открытых сочетанных оперативных вмешательств осложнения наблюдались у 19 (9,7%) пациентов, а после видеолапароскопических вмешательств у 8 больных. Во время выполнения открытых традиционных антирефлюксных вмешательств (n=2), а также при выполнении видеолапароскопических операции (n=2) у 4 пациентов наблюдалось кровотечение из сосудов пищеводно-диафрагмальной связки. При этом в 2 наблюдениях прибегали к конверсии и остановке кровотечения. Еще в 2 случаях во время выполнения, как традиционного, так и видеолапароскопического антирефлюксных вмешательств имело место перфорация пищевода. Зона перфорации была ушита, формировалась фундопликационная манжетка (n=2). При интраоперационном повреждении селезенки (n=2) прибегали к спленэктомии. Наиболее частым ранним послеоперационным осложнением традиционного (n=2) и видеолапароскопических антирефлюксных вмешательств (n=3) являлась дисфагия. Причиной послеоперационной дисфагии являлось наличие узкой и тугой фундопликационной манжетки в 3 случаях. Еще в 2 наблюдениях причиной дисфагии являлось раздражающее действие сетчатых трансплантатов. Проведенное консервативное лечение у этих больных оказалось эффективным. Миграцию фундопликационной манжетки мы наблюдали в 2 случаях, вследствие несостоятельности швов фундопликационной манжетки (n=1) и широкой фундопликационной манжетки (n=1) после традиционных открытых вмешательств по Ниссену. Во всех наблюдениях на 8-9 сутки нам пришлось выполнить повторные оперативным вмешательства. Следует подчеркнуть, что в большинстве наблюдений эти осложнения были связаны с интраоперационными техническими ошибками. К таким ошибкам, на наш взгляд, следует отнести игнорирование тщательной ревизии величины диастаза диафрагмальных ножек, обязательной фиксации манжетки к пищеводу и правой диафрагмальной ножке, использование нерассасывающегося шовного материала при сшивании диафрагмальных ножек. В 9 наблюдениях, после выполнения традиционных сочетанных оперативных вмешательств отмечали осложнения связанные с операциями на желчных путях. Так, у 3 пациентов были отмечены послеоперационные внутрибрюшные желчеистечения из ложа желчного пузыря (n=2) и соскальзывания лигатуры из пузырного протока (n=1), при этом в 2 случаях были выполнены релапаротомии, ушивание ложа желчного пузыря (n=1) и культи пузырного протока. Еще в 3 случаях релапаротомию проводили по поводу ранней спаечной тонкокишечной непроходимости. Релапаротомия была выполнена еще у 3 больных при наличии множественных внутрибрюшных абсцессов (n=2) и несостоятельности толстокишечного анастомоза (n-1), прежде перенесены сочетанные операции по поводу триады Сейнта. В послеоперационном периоде 1 больной умер от интоксикации. Таким образом, после выполнения 125 сочетанных открытых оперативных вмешательств послеоперационные осложнения имело место в 19(15,2%) наблюдениях с одним (0,8%) летальным исходом. Тогда как после 70 видеолапароскопических антирефлюксных вмешательств, сочетанных с холецистэктомией, осложнения имели место у 8(11,4%) больных.Летальных исходов не было. Длительность пребывания пациентов в стационаре после открытых оперативных вмешательств составила 10,8±3,6 суток, после видеолапароскопических вмешательств 5,1±1,4 суток.
При хирургическом лечении 92 пациентов с ЖКБ, сочетающейся с РГ нами были выполнены самые различные по характеру и объему оперативные вмешательства (таб 5).
Таблица 5
Характер сочетанных оперативных вмешательств при ЖКБ и РГ (n=92)
| Характер оперативных вмешательств | Кол. | % |
| Холецистэктомия. Операция Стронга. Закрытая пилоропластика | 42 | 45,65 |
| СПВ. Холецистэктомия. Дуоденоеюностомия по Грегуару | 1 | 1.09 |
| СПВ. Холецистэктомия. Еюнодуоденопластика по Боппе | 3 | 3,26 |
| Холецистэктомия. Комбинированное вмешательство на ДПК | 6 | 6,52 |
| Холецистэктомия. Резекция желудка по Ру | 6 | 6,52 |
| Комбинированная фундопликация по Ниссену+ холецистэктомия+ дуоденоеюностомия по Робинсону конец в бок | 9 | 9,78 |
| Комбинированная гемифундопликация по Тупэ+ холецистэктомия+ двустороннее выключение ДПК | 8 | 8,69 |
| Холецистэктомия. Операция Стронга с арефлюксным холедоходуоденоанастомозом по методике клиники | 3 | 3,26 |
| Холецистэктомия. Резекция желудка по Ру с холедохоеюноанастомозом бок в бок с приводящей петлей | 6 | 6,52 |
| Холецистэктомия с холедохолитотомией. Резекция желудка по Ру с формированием холедохоеюноанастомоза с межкишечным анастомозом и заглушка по Шалимову | 4 | 4,35 |
| Холецистэктомия. СВ. Еюнодуоденохоледохостомия с анастомозом по Ру | 2 | 2,17 |
| Холецистэктомия с холедохолитотомией. Резекция желудка по Ру с холедохоеюноанастомозом с приводящей петлей | 2 | 2,17 |
| Всего | 92 | 100 |
Выбор методов оперативного вмешательства был обусловлен степенью выраженности РГ, ДГР, моторно-эвакуаторных нарушений ДПК. Наиболее частым вмешательством на ДПК при ЖКБ, сочетающейся с РГ, являлась операция Стронга (n=42). Следует подчеркнуть, что во всех случаях при наличии острого угла отхождения тощей кишки, либо наличия периеюнита наблюдалась недостаточность замыкательной функции пилорического сфинктера. Для коррекции этой недостаточности во всех случаях операцию дополняли формированием дополнительной антирефлюксной закрытой пилорической, а при наличии высокой кислотоагрессии, и селективной проксимальной ваготомии (СПВ). Следует подчеркнуть, что в 17 наблюдениях ЖКБ сочеталась с РГ и РЭ. При этом в 14 наблюдениях отмечался выраженный дуоденогастроэзофагеальный рефлюкс с недостаточностью НПС, что требовало выполнения соответствующей хирургической коррекции. В 9 наблюдениях выполняли комбинированную фундопликацию по Ниссену с созданием двухуровневой манжетки, с захватом пищевода в нижней части на 360о, а в верхнем на 180о.
В 8 случаях для коррекции недостаточности НПС прибегали к гемофундопликации по Тупэ. Во всех случаях (n=17) после выполнении антирефлюксных вмешательств проводили холецистэктомию с последующим выполнением дуоденоеюностомии конец в бок по Робинсону (n=9), а также двустороннее выключение ДПК (n=8). У 15 пациентов ЖКБ с РГ II-III степени сочеталась с язвенной болезнью желудка (n=9) и двенадцатиперстной кишки. При наличии ЖКБ, РГ и язвенной болезни желудка в 6 случаях мы выполняли холецистэктомию с резекцией желудка по Ру, а при наличии дуоденальной язвы (n=3) и язвенной болезни желудка (n=3) прибегали к комбинированному вмешательству на ДПК. Суть операции заключалась в выполнении резекции желудка по Ру с анастомозом конец в конец, формированием дуоденоеюноанастомоза на длинной петле с межкишечным анастомозом и стволовой ваготомией. У 3 больных при язвенной болезни ДПК СПВ сочетали с еюнодуоденопластикой по Боппе. В 1 случае производили СПВ, холецистэктомию с дуоденоеюностомией по Грегуару. Особые трудности возникали при ЖКБ,осложненной холедохолитиазом (n=8) и стенозом БДС (n=1). В этих случаях прибегали к нестандартным оперативным вмешательствам направленны прежде всего на профилактику регургитационного холангита. Так, в 4 наблюдениях после выполнения холецистэктомии, холедохолитотомии, выполняли резекцию желудка по методике Ру с формированием холедохоеюноанастомоза на длинной петле с межкишечным анастомозом с заглушкой по Шалимову. В 2 случаях, после резекции желудка по Ру, формировали холедохоеюноанастомоз по Ру с приводящей петлей на тонкой кишке. В 3 наблюдениях при ЖКБ с холедохолитиазом (n=2) и стенозом БДС (n=1) проводили холецистэктомию с холедохолитотомией и формированием арефлюксного холедоходуоденоанастомоза. Желчнокаменная болезнь в 8 наблюдениях сочеталась с билиарным панкреатитом и РГ II-III степени, у этих пациентов в 6 случаях мы прибегали к холецистэктомии, резекции желудка по Ру с формированием холедохоеюноанастомоза бок в бок с приводящей петлей, а в 2 случаях холецистэктомию сочетали с СВ и формированием еюнодуоденохоледохеального анастомоза типа Ру. Таким образом,при суб- и декомпенсированной стадии хронических нарушений дуоденальной проходимости, независимо от ее природы выполнялись комбинированные вмешательства на ДПК, позволяющие эффективно коррегировать дуоденогастральный рефлюкс и устранять риск развития отдаленных послеоперационных осложнений. После выполнения сочетанных оперативных вмешательств по поводу ЖКБ и РГ в раннем послеоперационном периоде у 13 пациентов отмечались послеоперационные осложнения с 2 летальными исходами. Так в 4 случаях наблюдались внутрибрюшные абсцессы, по поводу которых выполнялись вскрытия и дренирование гнойников. У 3 пациентов при желчеистечении из ложа желчного пузыря (n=2) и несостоятельности швов культи пузырного протока прибегали к релапаротомии, ушиванию ложа желчного пузыря (n=2) и культи пузырного протока (n=1) с санацией и дренированием брюшной полости. Релапаротомия также была выполнена 3 пациентам, которым выполнялась комбинированная фундопликация по Ниссену с холецистэктомией и дуоденоеюностомии. При этом источниками кровотечения в 2 наблюдениях являлись сосуды пищеводно-диафрагмальной связки, а в одном сосуды большого сальника. Несостоятельность холедохоеюноанастомоза имела место в 2 наблюдениях. После релапаротомии, санации и дренирования подпеченочного пространства и брюшной полости умер один больной от выраженной интоксикации. Еще один больной умер от острого инфаркта миокарда на 7 сутки послеоперационного периода. Таким образом, после выполнения 92 пациентам различных по характеру и объему оперативных вмешательств послеоперационные осложнения имели место у 13 (14,1%) больных с 2 (2,2%) летальными исходами.
Об эффективности результатов хирургического лечения больных с ЖКБ, сочетающейся с РЭ и РГ, судят по отдаленным результатам и частоте развития ПХЭРЭ и ПЭХРГ. Отдаленные результаты хирургического лечения пациентов с ЖКБ, РЭ и РГ изучены в сроки 12-60 месяцев у 188 пациентов из 287, при этом 120 (63,8%) пациентов были с ЖКБ и РЭ, 68 (36,7%) с ЖКБ с РГ. Детальное и всестороннее изучение отдаленных результатов хирургического лечения ЖКБ и РЭ у 120 пациентов показало, что в большинстве случаев результаты лечения были обусловлены характером выполненных оперативных вмешательств. В отдаленном послеоперационном периоде после выполнения традиционных антирефлюксных открытых оперативных вмешательств отличные и хорошие результаты отмечены у 51 (72,8%) пациента из 70 пациентов, удовлетворительные результаты - у 12 (17,2%), неудовлетворительные – у 7 (10%). Тогда как после выполнения антирефлюксных видеолапароскопических вмешательств отличные и хорошие результаты наблюдались у 46 (92%) пациентов из 50, удовлетворительные – у 2 (4%) и неудовлетворительные - также у 2 (4%) больных.
Комплексное всестороннее изучение отдаленных результатов лечения ЖКБ и РГ проведено у 68 больных. Отдаленные результаты были изучены в сроки от 6 месяцев до 5 лет, в зависимости от характера выполненных, корригирующих РГ, оперативных вмешательств. Эффективность полученных данных во многом зависит от выбора наиболее рационального оперативного вмешательства и степени выраженности ХНДП.
Таким образом, в отдаленном послеоперационном периоде при обследовании 48 пациентов перенесших традиционные вмешательства (п=28), и одностороннее выключение ДПК (п=20), отличные и хорошие результаты были получены в 73%, удовлетворительные в 12,5 % и неудовлетворительные в 14,5%. Тогда как после комбинированных оперативных вмешательств в отдаленном периоде отличные и хорошие результаты составили 90 %, удовлетворительные- 10%. В общей сложности в 52 случаях (76,5%) получены отличные и хорошие результаты. В 9 (13,2%) – удовлетворительные и у 7 (10,3%) пациентов – неудовлетворительные результаты.
ВЫВОДЫ
- Желчнокаменная болезнь в 5,5% случаев сочетается с рефлюкс-эзофагитом в 2,6% с рефлюкс-гастритом. При этом в 55,4% причинами РЭ явились недостаточность нижнего пищеводного сфинктера, в 27,2%-грыжа пищеводного отверстия диафрагмы в 17,4% - хроническое нарушение дуоденальной проходимости. Причинами РГ в 77,2% функциональные, в 14,1% -органические нарушения дуоденальной проходимости,а в 8,7% -недостаточность пилорического сфинктера желудка.
- Основаными причинами развития постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита, является недостаточная осведомленность о частоте сочетания желчнокаменной болезни с рефлюкс-эзофагитом и рефлюкс-гастритом и общностью их патогенеза, отсутствием рациональных алгоритмов, а также неадекватным выбором операционного доступа и в связи с этим эффективной ревизии пищеводно-желудочного и дуоденоеюнального переходов.
- Наряду с рентгенологическими, эндоскопическими и специальными методами исследования (манометрия пищевода, 24 – часовой pH мониторинг, поэтажная манометрия) ведущими современными методами диагностики рефлюкс-эзофагита и рефлюкс-гастрита и их причин и холедохолитиаза является эндоскопическая ультрасонография, ультразвуковое дуплексное сканирование мезентериальных сосудов, а также электрофизиологические исследования пищевода, и двенадцатиперстной кишки.
- Одним из высокоинформативных маркеров, характеризирующий морфологические изменения в слизистой пищевода при эндоскопически негативной форме рефлюкс-эзофагита и слизистой желудка, способствующее развитию недостаточности НПС и пилорического сфинктера желудка, является повышенное содержание продуктов ПОЛ (МДА, ДК).
- Ведущим патогенетическим механизмом развития хронических нарушений дуоденальной проходимости является количественное и качественное нарушение в ультраструктурах органелл EC – клеток гастроэнтериновой системы, синтезирующих серотонин. Прогрессирование патологического процесса при хроническом нарушении дуоденальной проходимости сопровождается снижением количество ЕС – клеток, не только в слизистой ДПК, но и в других серотонинсодержащих структурах ДПК с блокадой серотонинсинтезирующих клеток пищеварительного тракта и прогрессирующего снижения уровня серотонина в крови.
- Одним из патогенетических механизмов развития желчнокаменной болезни является нарушение моторно-эвакуаторной функции двенадцатипрестной кишки, способствующее развитию дуоденальной гипертензии, нарушении нормальной эвакуации желчи из дистальных отделов желчных протоков и расстройством метаболизма составных частей желчи.
- У 13,2% пациентов с рефлюкс-эзофагитом обусловленное недостаточностью НПС с развитием дистрофических нарушений в сфинктере, патоморфологических изменений в слизистой оболочке пищевода, наряду с дуоденогастроэзофагеальным рефлюксом, высокой степенью хеликобактерной обсемененности, повышении уровня интрагастрального давления, важное значение имеет снижение местной и общей антиоксидантой защиты и щелочной буферной емкости слюны.
- При выраженной гипотонии НПС, грыжах пищеводного отверстия диафрагмы, сопровождающихся рефлюкс-эзофагитом С и D патогенетически обоснованным методом антирефлюксных вмешательств, способное противостоять высокому внутрибрюшному и внутрижелудочному давлению и препятствующей эпизодам желудочно-пищеводного рефлюкса является комбинированная фундопликация, а при не выраженных нарушениях моторики пищевода и рефлюкс-эзофагите предпочтения следует отдавать комбинированной гемофундопликации по Toypet.
- Видеолапароскопическая холецистэктомия в сочетании с антирефлюксными вмешательствами на кардии, являются альтернативой традиционным открытым антирефлюксным вмешательствам. Непосредственные и отдаленные результаты сочетанных видеолапароскопических вмешательств в значительной степени лучше, по сравнению с традиционными открытыми операциями.
- При желчнокаменной болезни сочетающейся с хроническим нарушением дуоденальной проходимости в стадии компенсации, эффективным методом коррекции является шунтирующие двенадцатиперстную кишку вмешательства, а при суб и декомпенсированной стадии хронической нарушении дуоденальной проходимости патогенетически обоснованной операцией является одностороннее выключение двенадцатиперстной кишки и комбинированные вмешательства, позволяющее устранить дуоденогастральный рефлюкс и восстановить адекватный пассаж по желудочно-кишечному тракту.
- Отдаленные результаты хирургического лечения желчнокаменной болезни сочетающейся с рефлюкс-эзофагитом и рефлюкс-гастритом показали высокую эффективность видеолапароскопических антирефлюксных вмешательств в сочетании с холецистэктомией. Отличные и хорошие результаты отмечены у 92%, удовлетворительные у 4% неудовлетворительные у 4% больных, тогда как после традиционных сочетанных вмешательств отличные и хорошие результаты составили 72,8%, удовлетворительные 17,2%, и неудовлетворительные - 10%. Выполнение комбинированных оперативных вмешательств для коррекции рефлюкс-гастрита при желчнокаменной болезни способствовали улучшению отдаленных результатов. Отличные и хорошие результаты отмечены у 90 % удовлетворительные у 10 %.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Для снижения частоты развития постхолецистэктомического рефлюкс-эзофагита и рефлюкс-гастрита рекомендуется в клинической практике использовать разработанные алгоритмы диагностики рефлюкс-эзофагита и рефлюкс-гастрита.
- Диагностика рефлюкс-эзофагита и рефлюкс-гастрита при желчнокаменной болезни должна быть комплексной и основываться не только на данных существующих традиционных методов исследования, но и на основании проведение эндоскопической ультразвуковой сонографии, ультразвукового дуплексного сканирования мезентериальных сосудов, а также электрофизиологических исследований функции пищевода и двенадцатиперстной кишки.
- Пациентам с желчнокаменной болезнью сочетающейся с рефлюкс-эзофагита и рефлюкс-гастрита в комплекс предоперационной подготовки рекомендуется включение проведение антихеликобактерной терапии и назначении препарата серотонин адиптина с целью восстановления моторики пищевода, желудка и двенадцатиперстной кишки и снижения морфологических изменений в слизистой оболочки пищевода.
- Сочетанные антирефлюксные вмешательства с холецистэктомией целесообразно выполнять с использованием видеолапароскопических технологий, которые позволяют добиться более большого количества отличных и хороших результатов по сравнению с традиционными открытыми вмешательствами с меньшей травматичностью и быстрой реаблитацией больных.
- При сочетании желчнокаменной болезни с хроническим нарушением дуоденальной проходимости в стадии суб - и декомпенсации рекомендуется выполнение комбинированных вмешательств на двенадцатиперстной кишке, а при компенсированной стадии - шунтирующие операции.
Cписок работ, опубликованных по теме диссертации:
- Абдуллоев Д.А. Профилактика рефлюкс – гастрита у больных с желчекаменной болезнью /Д.А.Абдуллоев, К.М. Курбонов// Материалы научно-практической конференции детских хирургов, анестезиологови реаниматологов Республики Таджикистан с международным участием «Проблемы перитонита у детей», Душанбе, 2006. С.182-183.
- Абдуллоев Д.А. Бронхолегочной синдром при гастроэзофагеальной рефлюксной болезни/Д.А.Абдуллоев, К.М. Курбонов// Материалы III – республиканской научно-практической конференции анестезиологов и реаниматологов Республики Таджикистан с международным участием «Современные аспекты медицины критических состояний » Душанбе, 2006. С.47-50.
- Абдуллоев Д.А. Атипичное проявление гастроэзофагеальной рефлюксной болезни/ Абдуллоев Д.А., Курбонов К.М.// Ежегодная ХII научно-практическая конференция Таджикского института последипломной подготовки медицинских кадров с международным участием «Медицина 21 века. Актуалные вопросы и пути их решения».(cборник статей) Душанбе-2006 c. I86-187.
- Абдуллоев Д.А. Диагностика хронической недостаточности дуоденальной проходимости у больных с желчекаменной болезнью /Д.А.Абдуллоев, К.М. Курбонов// Материалы 55 научно-практической конференции ТГМУ им.Абуали ибни Сино с международным участием Душанбе, 2006. С.8-9.
- АбдуллоевД.А.,Сердечно-сосудистые расстройства при гастроэзофагеальном рефлюксе/ Абдуллоев Д.А., КурбоновК.М., Б.Д.Азизов //Вестник Авиценны, №3-4.2006.С.18-21.
- Абдуллоев Д.А. Лечение холангиогенных панкреатитов /АбдуллоевД.А. КурбоновК.М.. “Современная медицина и качество жизни пациента” Душанбе 2006. С.9-10.
- Абдуллоев Д.А.Особенности диагностики и лечения грыжи пищеводного отверстия диафрагмы, сочетающейся с заболеваниями органов брюшной полости/ Абдуллоев Д.А., Курбонов К.М. //Материалы юбилейной конференции «Актуальные вопросы герниологии» посвященной пятой годовщины со дня образования «общества герниологов», Москва. 2006. С.5-6.
- Абдуллоев Д.А.Новый способ диагностики дуоденостаза при калькулёзном холецистите / Абдуллоев Д.А. Курбонов К.М..//Анналы хирургической гепатологии- Москва №3.Т11.2006.С. 175-
- Курбонов К.М.,Cпособ лечения холецистодуоденального свиша при желчнокаменной болезни/ Курбонов К.М., Абдуллоев Д.А/ Анналы хирургической гепатологии - Москва №3.Т11.2006.С.9.
- Курбонов К.М.,Выбор методов хирургического лечения «трудного»желчного пузыря// Анналы хирургической гепатологии - Москва №3.Т11.2006.С.9.
- Абдуллоев Д.А. Хирургическая коррекция дуоденогастрального рефлюкса при хроническом калькулёзном холецистите /Д.А.Абдуллоев, К.М. Курбонов// Материалы республиканской научно-практической конференции с международным участием «Роль современной медицинской технологии в улучшении качества жизни пациента» Турсунзода, 2007. С.5-6.
- Абдуллоев Д.А. Диагностика и хирургическое лечение сочетанного постхолецистэктомического синдрома /Д.А.Абдуллоев и др. // Материалы республиканской научно-практической конференции с международным участием «Роль современной медицинской технологии в улучшении качества жизни пациента» Турсунзода, 2007. С - 69.
- Абдуллоев Д.А. Хирургическая тактика при синдроме Мириззи /Д.А.Абдуллоев, К.М. Курбонов, Х.Ш. Шоймардонов// Материалы республиканской научно-практической конференции с международным участие « Роль современной медицинской технологии в улучшении качества жизни пациента» Турсунзода, 2007. С. 170.
- Абдуллоев Д.А. Диагностика и лечение хронической дуоденальной непроходимости /Д.А.Абдуллоев, К.М. Курбонов, К.М. Саидов // Материалы 56 научно-практической конференции ТГМУ им.Абуали ибни Сино с международным участием Душанбе, 2007. С.171
- Холов К.Р. Послеоперационный холедохолитиаз / Холов К.Р., Абдуллоев Д.А., Курбонов К.М., Даминова Н.М. //Материалы II городской научно-практической конференции с международным участием« Современные технологии в неотложной хирургии органов брюшной полости». Душанбе, 2007.C.53-54
- Абдуллоев Д.А. Профилактика и диагностика постхолецистэктомического рефлюкс гастрита при остром холецистите /АбдуллоевД.А., Курбонов К.М. //Материалы научно-практической конференции хирургов Хатлонской области. Актуалные вопросы неотложной хирургии. Курган-тюбе 2007 с. 17-19.
- Курбонов К.М., Реконструктивные и восстановительные операции на желчных путях/ Курбонов К.М., Абдуллоев Ч.А., Даминова Н.М., Холов К.Р. //Актуальные вопросы реконструктивной и пластической хирургии. Материалы республиканской научно-практической конференции с международным участием, посвященной 20-летию организации службы реконструктивной и пластической хирургии в Таджикистане.-Душанбе. 2007. С.83-84.
- Абдуллоев Д.А. Хирургическое лечение больных с осложнёнными формами желчнокаменной болезни / Абдуллоев Д.А., Курбонов К.М., Н.М.Даминова.,А.О.Исоев//Вестник хирургии- Санкт-Петербург №2,Т. 166.2007.С.5-8
- Курбонов К.М., Сочетанные постхолецистэктомические синдромы/ Курбонов К.М., Абдуллоев Д.А., К.Холов//Вестник Авиценны №4,Душанбе.2007. С.9-14
- Курбонов К.М.,Антарефлюксные вмешательства на кардии при хирургическом лечении желчнокаменной болезни/ Курбонов К.М., Абдуллоев Д.А.,Кабилов И.И.//Журнал Проблемы гастроэнтерологии №4-2007. Душанбе-Москва. С 237-239.
- Абдуллоев Д.А.,Результаты хирургической коррекции рефлюксов пищеварительного тракта при желчекаменной болезни / Абдуллоев Д.А., Курбонов К.М.,//Анналы хирургической гепатологии –Москва 2007 №3.Т12. С.32.
- Холов К.Р. Новые аспекты в диагностике и лечении резидуального холедохолитиаза. /Холов К.Р., Абдуллоев Д.А., Курбонов К.М.,//Анналы хирургической гепатологии №3.Т12.2007. - Москва. С.121.
- Абдуллоев Д.А. Реконструктивные операции на пищеварительном тракте при желчекаменной болезни/ Абдуллоев Д.А., Курбонов К.М. //Актуальные вопросы реконструктивной и пластической хирургии. Материалы республиканской научно-практической конференции с международным участием, посвященной 20-летию организации службы реконструктивной и пластической хирургии в Таджикистане. Душанбе 2007.С32-34.
- Д.А.Абдуллоев.,Диагностика и лечение рефлюкс-энтерита при желчекаменной болезни /АбдуллоевД.А., К.М.Курбонов, К.М.Саидов. //II-Съезд детских хирургов, анестезиологов и реаниматологов Таджикистана.Душанбе-2008.С. 308-309.
- Д.А.Абдуллоев. Недостаточность баугиневой заслонки при желчнокаменной болезни/АбдуллоевД.А., К.М.Курбонов, К.М.Саидов. II-Съезд детских хирургов, анестезиологов и реаниматологов Таджикистана.Душанбе-2008.С. 309.
- Курбонов К.М. Диагностика и лечение артериомезентериального компрессионного синдрома /Курбонов К.М.,Абдуллоев Д.А., Даминова Н.М. Центрально-Азиатский журнал. сердечно-сосудистый хирургии – Душанбе №2.2008. с. 131-132.
- Даминова Н.М.Видеопароскопические санации брюшной полости в комплексном лечении послеоперационного желчного перитонита /Даминова Н.М., Курбонов К.М., Абдуллоев Д.А. //Актуальные проблемы клиничекой и экспериментальной медицины.Чита-2008. С.314-315.
- К.М.Курбонов Оптимизация хирургического лечения больных желчнокаменной болезнью в хронической стадии заболевания /К.М.Курбонов, Д. А. Абдуллоев, Ш.Ш.Сайдалиев, Д.С.Шоев. //Харковская хирургическая школа.- Харьков №1, 2009. С. 14-16.
- Абдуллоев Дж.А.,Возможности видеолапароскопической коррекции пищеварительных рефлюксов при желчнокаменной болезни/ Абдуллоев Дж.А.,и др. //Первая международная конференция по торако-абдоминальной хирургии. Москва. 2008. С 77-78.
- Абдуллоев Дж.А., Хирургическое лечение грыж пищеводного отверстия диафрагмы, сочетающейся с заболеваниями органов брюшной полости /Абдуллоев Дж.А., Курбонов.К.М. //Материалы межрегиональной конференции “Современное состояние и перспективы герниологии” Калининград 2008. С.4.
- Абдуллоев Дж. А.,Функциональный дуоденостаз как причина хронического панкреатита/ Абдуллоев Дж.А., К.М.Курбонов.,Даминова Н.М.// Анналы хирургической гепатологии. – Москва №3.Т13.2008.С150
- Абдуллоев Дж. А.,Бронхолегочной и сердечно-сосудистый синдром при гастроэзофагеальный рефлюксном болезни/ Абдуллоев Дж.А., Курбонов.К.М.//Здравоохранение Таджикистана. - Душанбе 2008 №3. С.100-101.
- Абдуллоев Д.А. Патогенез функционального дуоденостаза/ Абдуллоев Д.А., Курбонов. К.М. //Вестник Авиценны №3. Душанбе. 2009. С. 48-50.
- Курбонов.К.М. Биэндоскопические вмешательства при механической желтухе. / Курбонов К.М., Даминова Н.М., Абдуллоев Д.А., Рустамова Л.С. //Актуальные проблемы хирургии. Материалы республиканской научной конференции. Ташкент 2009.С 103-104.
- Абдуллоев Д.А. Значение нарушений гастроэнтериновой системы в патогенезе дуоденостаза /Д.А.Абдуллоев, К.М. Курбонов// Материалы 57 научно-практической конференции ТГМУ им.Абуали ибни Сино с международным участием Душанбе, 2009. С.277-278
- Абдуллоев Д.А. Комплексная диагностика и лечение хронических нарушений дуоденальной проходимости при калькулёзном холецистите/ Абдуллоев Д.А., Курбонов.К.М. //Вестник Авиценны №1 Душанбе. 2009. С. 29-35.
- Курбонов.К.М. Совершенствование диагностики и лечения больных с желчекаменной болезнью в хронической стадии заболевания/ Курбонов.К.М., Абдуллоев Д.А., Ш.Ш. Сайдалиев, Д.С. Шоев//журнал Педиатрия и детская хирургия Таджикистана. Душанбе. 2009. С. 54-56.
- Курбонов.К.М. Наружные свищи печени и желчных протоков /К.М.Курбонов, Н.М. Даминова,Ф.И. Махмадов,Д.А. Абдуллоев // Харковская хирургическая школа. –Харьков 2009№2.1,. С. 135-137..
- Курбонов.К.М. Диагностика и лечение несостоятельности швов желчеотводящих анастомозов / Курбонов.К.М. Н.М. Даминова, Абдуллоев Д.А.//Клиническая хирургия – Киев. 2009.№1,.С.18-22
- Д.А. Абдуллоев. Особенности диагностики и лечения хронических нарушений дуоденальной проходимости при калькулёзном холецистите / Д.А. Абдуллоев. К.М. Курбонов //Второй конгресс врачей ЮФО г.Ростов- на –Дону 2009.С.157-161я
- Курбонов.К.М.Несостоятельность швов билиодигестивного анастомоза/ К.М. Курбонов, Н.М. Даминова, Д.А. Абдуллоев //Анналы хирургической гепатологии.- Москва 2009№3Т.14..С.36-40.
- Абдуллоев Д.А. Современный взгляд на патогенез дуоденостаза /Абдуллоев Д.А. и др. //Харковская хирургическая школа.- Харьков №4.1, 2009. С. 142-143.
- Абдуллоев Д.А. Современный взгляд на патогенез дуоденостаза К.М.Курбонов, Невзоров В.П. Харковская хирургическая школа.- Харьков №2.1, 2009. С. 135-137.
- Абдуллоев Д.А. Диагностика и лечение хронического калькулёзного холецистита, сочетающегося с рефлюкс эзофагитом / Абдуллоев Д.А., Курбонов. К.М. // Вестник Авиценны №2 Душанбе. 2010. С. 34-37.
- Абдуллоев Д.А. Выбор тактики лечения осложнений желчекаменной болезни с учётом функционального состояния двенадцатиперстной кишки/ Абдуллоев Д.А., Курбонов. К.М., Темуров Дж.А. //Здравоохранение Таджикистана. - Душанбе 2010. №1. С.102-105.
- Абдуллоев Д.А. Патогенез, диагностика и тактика лечения хронической дуоденальной непроходимости/ Абдуллоев Д.А., Курбонов. К.М. //Педиатрия и детская хирургия Таджикистана. - Душанбе 2010. №3. С.175-178.
Патенты
- Курбонов К.М., Абдуллоев Д.А., Раджабов А.М.,Улаев Н.А. Способ диагностики артериомезентериальной компрессии двенадцатиперстной кишки. Патент № ТJ-135.2008
- Абдуллоев Д.А., Курбонов К.М.,Раджабов А. Способ определения жизнеспособности кишки. Патент № ТJ-83.2007
- Даминова М.Н., Абдуллоев Д.А., Курбонов К.М., Способ формирования холедоходуоденоанастомоза. Патент № ТJ-70.2007
- Даминова М.Н., Абдуллоев Д.А., Курбонов К.М., Способ послеоперационного определения жизнеспособности ткани печени. Патент № ТJ-69.2007
- Курбонов К.М.,Сайдалиев Ш.Ш.,Шоев Д.С.Ретрактор печени. Патент № ТJ-118.2008
- Даминова М.Н., Абдуллоев Д.А., Курбонов К.М., Способ повышения герметичности швов билиодигестивных анастомозов.Патент № ТJ-68.2007
- Курбонов К.М., Абдуллоев Д.А., Раджабов А.М.,Улаев Н.А. Способ диагностики дуоденального стаза. Патент № ТJ -134. 2008.
Авторские свидетельство
1. Абдуллоев Д.А., Курбонов К.М., Велигоцкий Н.Н. Способ двухсторонней крурофундоэзофагорафии при хирургической коррекции недостаточности кардии. № 0269 РТ. 21.07.2010.
2.Абдуллоев Д.А., Курбонов К.М., Велигоцкий Н.Н. Способ комбинированной гемифундопликации при хирургической коррекции недостаточности кардии. № 0270 РТ. 21.07.2010.
Рационализаторские предложение
- Абдуллоев Д.А., Курбонов К.М., Исоев А.О. Способ лечения холецистодуоденальных свищей у больных с желчекаменной болезнью. Рац. Предложения №3122/Р- 424, выданное ТГМУ от 04.01.2006
- Абдуллоев Д.А., Курбонов К.М.,Азимшоеву М.А. Способ лечения перфорации язвы двенадцатиперстной кишки сочетаюшейся с хронической дуоденальной непроходимостью. Рац. Предложения №3128/Р-430, выданное ТГМУ от 9.02.2006
- Абдуллоев Д.А.,Шодиев Э.Ф., Курбонов К.М., Способ ранней диагностики хронической дуоденальной непроходимостью. Рац. Предложения №3115-Р-417, выданное ТГМУ от 7.12.2005
- Абдуллоев Д.А.,Шодиев Э.Ф., Курбонов К.М., Способ УЗИ диагностики хронической дуоденальной непроходимостью у больных с желчекаменной болезнью. Рац. Предложения №3114-Р-416, выданное ТГМУ от 7.12.2005
- Абдуллоев Д.А., Даминова М.Н., Курбонов К.М.,Cпособ лечения несостоятельности холедоходуоденоанастамоз. Рац. Предложения №3143/Р-445, выданное ТГМУ от 16.10.06
- Абдуллоев Д.А., Курбонов К.М.,Даминова М.Н., Cпособ билиодигестивное шунтирование несостоятельности холедоходуоденоанастамоза. Рац.Предложения№3144/Р-446,выданное ТГМУ от 16.10.06
- Абдуллоев Д.А., Курбонов К.М.,Саидову К.М., Способ диагностики рефлюкс эзофагита. Рац.Предложения№3235/Р-451,выданное ТГМУ от 23.10.09.
- Абдуллоев Д.А., Курбонов К.М., Саидову К.М., Способ диагностики негативных форм рефлюкс-эзофагита. Рац.Предложения№3240/Р-446. Выданное ТГМУ от 24.02.10.
Монография
- Курбонов К.М.,Даминова М.Н., Абдуллоев Д.А. Трудный желчный пузырь. Душанбе. 2006. 379 с.
Список сокращенных слов, использованных в автореферате
АМК артериомезентериальная компрессия
ГПОД грыжа пищеводного отверстия диафрагмы
ГЭРБ гастроэзофагеальная рефлюксная болезнь
ДГХК дегидрохолевая кислота
ДЕС дуоденоеюностомия
ДПК двенадцатиперстная кишка
ДХК дезоксихолевая кислота
ЖКБ желчекаменная болезнь
ЖКТ желудочно-кишечный тракт
МЭФ моторно-эвакуаторная функция
НК недостаточность кардии
НПС нижний пищеводный сфинктер
ПОЛ перекисное окисление липидов
РГ рефлюкс-гастрит
РЭ рефлюкс-эзофагит
СОЖ слизистая оболочка желудка
СПВ селективная проксимальная ваготомия
УЗИ ультразвуковое исследование
ФГДС фиброгастродуоденоскопия
ХДХК хенодезоксихолевая кислота
ХК холевая кислота
ХКХ хронический калькулезный холецистит
ХНДП хроническое нарушение дуоденальной проходимости
ЭУС эндоскопическая ультразвуковая сонография
ЭЭГ электроэзофагография
ЭМГ электромиография
ЯБДК язвенная болезнь двенадцатиперстной кишки
Хулоса
Абдуллоев Ч.А.
Ташхиси комплекси ва бартарафкунии чаррохии эзофагити рефлюкси ва гастрити рефлюкси хангоми бемории санги сафро
Рис.докт.14.01.17 - чаррох
Натичаи ташхис ва табобати комплексии 287 бемор бо бемории санги сафро бо хамрохии эзофагити рефлюкси ва гастрити рефлюкси, маълум гашт, ки дар асоси ин бемори накши асосиро пастшавии вазифаи харакатии рудаи 12-ангушта дар натичаи пастшавии сатхи сератонин дар хун ва пардахои луобии роххои хозима, ва хамчунин баландшавии махсулоти туршшавии перекисии липидхо мебозанд. Исбот шудааст, ки дар катори усулхои маъмули ташхиси эзофагити рефлюкси ва гастрити рефлюкси усули баландахбори ташхис ултрасонографияи даруннигори, ангиосканиронии дуплексии шараёнхои мезентриали ба хисоб меравад.
Муайян шуд, ки натичахои холнсистэктомияи видеолапароскопи дар якчояги бо амалиётхои чаррохии зиддирефлюкси хангоми эзофагити рефлюкси ва амалиётхои якчоягии анъанави хангоми бемории санги сафро бо гастрити рефлюкси бештар натичабахштаранд.
Сах. – 296; накша - 71; расм - 87; адаб. - 334
Summary
Abdulloev Djamoliddin Abdulloevich
Complex diagnosis and surgical correction refluxe-oesophagitis and refluxe-gastritis on cholelitiasis
Doctoral dissertation 14.01.17-surgery
Results of complex investgation and treatment of 287 patients with cholelitiasis combined with refluxe-oesophagitis and refluxe-gastritis. It is established that in patogenesis these diseases the leading place is taken away to infringement of motor function duodenum because of decrease level of serotonine in mucous of gastrointestinal tract and in blood and also increase of products perhydrate oxidations of lipids. It is proved that along with well-known methods of diagnostics methods of refluxe-oesophagitis and refluxe-gastritis one of the high informative method is endoscopic ultrasonography and duplex angioscan of mesenteric vessels.
It is established that results videolaparoscopic cholecystectomy in a combination with antirefluxe tehnic at refluxe-oesophagitis and combined traditional interventions at a combination cholelitiasis with refluxe-oesophagitis it is rather effective.
Pages-296; Tables-71; Figures-87; Bibliography-334

