Физико – химический анализ систем с наличием окислительно - восстановительных процессов
- На правах рукописи
- КАСТЕРИНА Татьяна Витальевна
ФИЗИКО – ХИМИЧЕСКИЙ АНАЛИЗ
СИСТЕМ С НАЛИЧИЕМ
ОКИСЛИТЕЛЬНО - ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ
02.00.04 – физическая химия
А В Т О Р Е Ф Е Р А Т
диссертации на соискание ученой степени
кандидата химических наук
Саратов - 2008
Работа выполнена в Самарском государственном техническом университете.
Научный руководитель: доктор химических наук, профессор,
Заслуженный деятель науки РФ
Трунин Александр Сергеевич.
Официальные оппоненты: доктор физико-математических наук,
профессор Кленин Виталий Иосифович
кандидат химических наук
Герасимова Галина Викторовна
Ведущая организация: Московский государственный университет им. М.В.Ломоносова
Защита состоится «9» октября 2008 года в 16.00 часов на заседании диссертационного совета Д 212.243.07 по химическим наукам при Саратовском государственном университете им. Н.Г.Чернышевского по адресу: 410012, г. Саратов, ул. Астраханская, 83, 1 корпус, химический факультет.
С диссертацией можно ознакомиться в библиотеке Саратовского государственного университета.
Автореферат разослан «4» сентября 2008 г.
Ученый секретарь
диссертационного совета В. В. Сорокин
- ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Физико-химический анализ является наиболее общим методом исследования превращения веществ и широко применяется в химии и химической технологии. Физико-химический анализ многокомпонентных систем рассматривается как основа современного материаловедения.
До настоящего времени с использованием физико-химического анализа исследовались системы с обменными реакциями, реакциями соединения. Одним из распространенных реакций, окислительно-восстановительным (ОВР), при изучении фазовых диаграмм внимание практически не уделялось. Так, в доступной нам литературе отсутствуют диаграммы, на которых представлены области ОВР. В тоже время разработка энергонасыщенных композиций с использованием ОВР является перспективным направлением современной физической химии.
В связи со значительным увеличением энергопотребления, а также сокращением углеводородных невозобновляемых источников энергии возникла необходимость поиска новых источников энергии. В качестве перспективного подхода нами рассматриваются химические системы типа «окислитель – восстановитель - вода». Окислители и восстановители, взаимодействуя между собой, могут выделять значительное количество энергии, которую можно превратить в механическую работу. Компоненты ОВР могут вступать в реакцию, как в присутствии воздуха, так и без него. Ингредиенты должны обладать следующими свойствами: возобновляемость, дешевизна, безопасность при хранении и эксплуатации. Такие композиции могут применяться в разнообразных отраслях промышленности, в том числе и военных. Фундаментальной основой для разработки энергонасыщенных композиций является фазовые диаграммы систем типа «окислитель – восстановитель - вода». Таким образом, исследование фазовых диаграмм с наличием ОВР является важным для решения ряда теоретических и прикладных задач, связанных с разработкой энергонасыщенных композиций.
Цель работы. Получение физико-химических характеристик систем с наличием окислительно-восстановительных процессов для разработки неуглеводородных энергонасыщенных композиций.
Задачи исследования:
- Проанализировать современное состояние проблемы поиска альтернативных источников энергии.
- Обосновать выбор ингредиентов и формирование двух-, трех-, четырехкомпонентных систем для разработки энергонасыщенных композиций.
- Установить характеристики эвтоник двухкомпонентных систем: CO(NH2)2 * НNO3 – H2O, NH4СlO4 – H2O, NaСlO4 – H2O и эвтектик в системах NH4NO3 – NaСlO4, NH4NO3 – NH4СlO4.
- Построить политермы кристаллизации трехкомпонентных систем NH4NO3 – NH4СlO4 – H2O, NaСlO4 – CO(NH2)2 – H2O, NH4СlO4 – CO(NH2)2 – H2O, CO(NH2)2 *НNO3 – С2Н5NО – H2O, NH4NO3 – С6Н12N4 – H2O с использованием современных методов моделирования и аппаратуры физико-химического анализа.
- Моделирование и экспериментальное подтверждение характеристик эвтоник четырехкомпонентных систем: NH4NO3 – NH4СlO4 – CO(NH2)2 – H2O, NH4NO3 – NaСlO4 – CO(NH2)2 – H2O, NH4NO3 – CO(NH2)2 – С2Н5NО – H2O.
Методы исследования:
Для решения поставленных задач использовалось компьютерное моделирование и экспериментальные методы физико-химического анализа: визуально-политермический анализ (ВПА), дифференциальный термический анализ (ДТА).
Научная новизна:
- Показано наличие на фазовых диаграммах областей окислительно-восстановительных процессов в двухкомпонентных системах: CO(NH2)2 *НNO3 – H2O, NH4СlO4 – H2O, NaСlO4 – H2O, NH4NO3 – NaСlO4, NH4NO3 – NH4СlO4.
- Построены политермы кристаллизации трехкомпонентных систем: NH4NO3 – NH4СlO4 – H2O, NaСlO4 – CO(NH2)2 – H2O, NH4СlO4 – CO(NH2)2 – H2O, CO(NH2)2 *НNO3 – С2Н5NО – H2O, NH4NO3 – С6Н12N4 – H2O.
- На фазовых диаграммах трехкомпонентных систем выделены области и температуры начала окислительно-восстановительных реакций.
- Рассчитаны и экспериментально подтверждены характеристики эвтоник четырехкомпонентных систем: NH4NO3 – NH4СlO4 – CO(NH2)2 – H2O, NH4NO3 – NaСlO4 – CO(NH2)2 – H2O, NH4NO3 – CO(NH2)2 – С2Н5NО – H2O.
Практическая ценность работы. Результаты диссертационного исследования предложены для разработки энергоемких композиций, в том числе позволяющих снижать расход дефицитного углеводородного сырья.
На защиту автор выносит. Новые данные по диаграммам состояния двух-, трех-, четырехкомпонентных эвтонических систем, в том числе с наличием окислительно-восстановительных процессов между компонентами.
Апробация работы и публикации. Основные результаты работы докладывались и обсуждались на: 5-ой Международной конференции молодых учёных «Актуальные проблемы современной науки» (Самара, 2004); 1-3 Международных форумах (6 - 8 Международных конференциях молодых учёных) «Актуальные проблемы современной науки» (Самара, 2005 – 2007); Международной научной конференции «Фундаментальные и прикладные проблемы современной химии в исследованиях молодых ученых» (Астрахань, 2006). По материалам диссертации опубликовано 15 статей, в том числе в изданиях, рекомендованных ВАКом.
Личный вклад соискателя: участие в постановке задач исследования, интерпретации полученных результатов. Проведение эксперимента и его обработка.
Структура и объём работы. Диссертационная работа состоит из введения, трёх глав, выводов, списка литературы (111 наименований). Общий объем работы составляет 142 страницы, содержит 43 таблицы и 79 рисунков.
- ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обоснована актуальность работы, сформулирована цель, определены задачи исследования, научная новизна и практическая ценность исследований.
В первой главе приводится обзор литературы по проблемам современной энергетики. С каждым годом уровень потребляемой энергии заметно растет, в то время как запасы органического топлива сокращаются. Производство и использование энергии всегда сопровождалось рассмотрением экологических проблем. Огромные выбросы продуктов сгорания отрицательно влияют на биосферу в целом.
Настоящая работа посвящена исследованию физико-химических систем с наличием окислительно-восстановительных процессов. Приводится обоснование и анализ выбора компонентов данных систем.
В отличие от привычных представлений о "топливе", в качестве которого до сих пор рассматривались лишь горючие вещества минерального, синтетического или биологического происхождения, предложен для исследования ряд систем, на основе недефицитных ингредиентов, молекулярный состав которых основан на сочетаниях (Н,N,О) – атомов, для последующей разработки на их основе энергонасыщенных композиций.
Новым видом энергонасыщенных композиций, в частности, являются растворы неагрессивных азотных соединений, реализуемых по принципу совместного присутствия окислителей, горючих веществ и воды. В качестве окислителей топливных систем были исследованы нитраты и перхлораты натрия и аммония, а в качестве сорастворимых восстановителей – некоторые амины, богатые химически связанным водородом. Общим растворителем водо-нитратных смесей является вода, что в обычных условиях исключает горючесть и неспособность к взрыву энергонасыщенных смесей. Выбранные ингредиенты характеризуются возобновляемой сырьевой базой при высоком уровне эксплуатационной безопасности образуемых энергонасыщенных композиций, с эффектом снижения температур плавления образуемых эвтектик, а в присутствии воды – эвтоник.
Окислительно-восстановительные реакции в предлагаемых композициях характеризуются высоким тепловым эффектом, достаточным для испарения всей присутствующей воды - растворителя. Образуется перегретая парогазовая фаза, что необходимо для совершения полезной механической работы при расширении газовых продуктов.
Многообразие возможных сочетаний компонентов позволило сформировать ряд перспективных энергонасыщенных систем, состоящих из двух-, трёх- и четырёх компонентов.
Наибольший интерес представляют системы с недефицитными окислителями и восстановителями богатыми химически связанным водородом.
Исследование систем является трудоемким процессом, поэтому оно проводилось на основе общего алгоритма оптимизации исследования многокомпонентных систем. Он предполагает наличие трёх информационных уровней (табл. 1) и их реализацию с целью минимизации трудозатрат на исследование систем.
Таблица 1
Общий алгоритм комплексной методологии исследования
многокомпонентных систем
| Уровень | Содержание уровня |
| |
| 0. | Нулевой информационный уровень – база данных |
| 0.1. | Формирование и моделирование физико-химической системы |
| 0.2. | Обзор литературы по состоянию изученности системы |
| 0.3. | Кодирование информации на модели системы |
| 1.0. | Первый информационный уровень - качественное описание системы |
| 1.1. | Дифференциация системы на фазовые единичные блоки; формирование древа фаз |
| 1.2. | Формирование древа кристаллизации |
| 1.3. | Описание химического взаимодействия в системе |
| 2.0. | Второй информационный уровень - количественное описание системы |
| 2.1. |
|
| 2.2. | Определение характеристик моновариантных равновесий |
| 2.3. | Определение характеристик поливариантных равновесий |
Постановка задачи исследования определяется тем реализуемым высшим информационным уровнем и его этапом, который отвечает конечной цели исследования. Из содержания каждого уровня вытекает задача построения алгоритмов использования и получения информации при минимальном ее избытке. Однако, несмотря на совершенствование экспериментальных методов и использование ПК, эксперимент остается самым трудоемким и длительным этапом исследования фазовых диаграмм.
Во второй главе приводится описание методов исследования, использованных в работе. Описаны методы моделирования эвтектик, а также экспериментальные методы исследования (визуально-политермический анализ, дифференциальный термический анализ) и их инструментальное обеспечение.
Третья глава посвящена экспериментальным исследованиям. Приведены исходные вещества с указанием основных термодинамических свойств, которые в свою очередь являются основой для формирования двух-, трёх- и более сложных систем. Данные соединения используются для разработки различных составов энергоемких композиций.
Были рассчитаны термохимические эффекты основных окислителей, которые использовались в работе. Наиболее эффективные окислители – те, которые имеют максимальное содержание кислорода при минимальных теплозатратах на разложение единицы массы вещества. При разложении аммиачных солей-окислителей теплота выделяется, а при разложении нитратов металлов (нитрата натрия) – поглощается. Таким образом, перхлораты являются более сильными окислителями (табл. 2).
- Таблица 2
Термохимические эффекты окислителей
| Вещество | КБ (содержание активного кислорода) | Теплота разложения чистого окислителя, Дж/г | Тепловой эффект выделения 1 г О2, кДж/г |
| NH4NO3 | 20 | +1481 | +7,4 |
| NH4ClO4 | 34 | +1457 | +4,29 |
| NaNO3 | 47 | -3031 | -6,44 |
| NaClO4 | 52,3 | +222,3 | +0,43 |
Исследован ряд двухкомпонентных систем с ингредиентами энергонасыщенных композиций. Анализ имеющихся справочных данных показал, что ряд систем ранее исследован в узком диапазоне концентраций. В связи с этим были исследованы фазовые диаграммы кристаллизации систем NH4СlO4 – H2O, NaСlO4 – H2O, определены составы и температуры двухкомпонентных эвтоник.
Впервые изучены двухкомпонентные системы: С2Н5NО – H2O, CO(NH2)2 *НNO3 – H2O, NH4NO3 – NaСlO4, NH4NO3 – NH4СlO4. Характеристики нонвариантных точек исследованных двухкомпонентных систем представлены в табл. 3.
При рассмотрении вышеприведенных систем было установлено наличие окислительно-восстановительных процессов между компонентами. В ходе исследований было установлено, что при концентрации CO(NH2)2*НNO3 в системе CO(NH2)2 *НNO3 – H2O, начиная с 70 % масс., наблюдается газообразование. Это свидетельствует о протекании окислительно-восстановительной реакции (ОВР). Области ОВР выявлены также в системе NaСlO4 – H2O, начиная с 83 % NаClO4 (масс.), и в системе NH4СlO4– H2O, начиная с 70 % NH4СlO4 (масс.).
В результате проведенных исследований было установлено, что перхлораты образуют эвтектики при содержании около 10 % масс. перхлоратов: для системы NH4NO3 – NаСlO4 при 129 0С, а для системы NH4NO3 – NH4СlO4 при 146 0С.
- Таблица 3
Характеристики эвтектик и эвтоник двухкомпонентных систем
| Система | Характер точек | Состав | Температура | |||||
| А | В | масс. % | мол. % | |||||
| А | В | А | В | °С | К | |||
| NH4NO3 | NaClO4 | е | 90 | 10 | 93,3 | 6,7 | 129 | 402 |
| NH4NO3 | NH4ClO4 | е | 90 | 10 | 92,9 | 7,1 | 146 | 419 |
| CO(NH2)2 *HNO3 | H2O | е | 10 | 90 | 1,6 | 98,4 | -4,5 | 268,5 |
| C2H5NO | H2O | е | 48 | 52 | 21,97 | 78,03 | -36,2 | 236,8 |
| NaClO4 | H2O | е | 57,5 | 42,5 | 16,6 | 83,4 | -31,4 | 241,6 |
| NH4ClO4 | H2O | е | 11 | 89 | 1,86 | 98,14 | -3,2 | 269,8 |
Сплавы NH4NO3 с перхлоратами интенсивно разлагаются выше 180 0С с газообразованием (выделением продуктов реакции). Для системы NH4NO3 - NH4ClO4 ОВР наблюдается при содержании NH4ClO4 более 20 % масс. Для системы NH4NO3 - NaClO4 ОВР - при содержании NаClO4 более 30 % масс.
Данный эффект связан с окислительно-восстановительными реакциями, протекающими между компонентами:
NH4NO3 + 2NH4ClO4 = 2N2 + 2HCl + 5H2O + 3O2
NH4NO3 + 2NaClO4 = N2 + 2NaCl + 2H2O + 4,5O2
Возможен также термолиз перхлората аммония, который заметно возгоняется и разлагается выше 150 0С по схеме:
4NH4ClO4 = 2Cl2 + 2N2O + 3NO2 + 8H2O
Для систем NH4ClO4 - CO(NH2)2 и NaClO4 - CO(NH2)2 экспериментально определены составы и температуры двойных эвтектик, соответственно: 50 % масс. NH4ClO4 при 55 0С и 37,5 % масс. NaClO4 при 60 0С.
Протекание ОВР наблюдается при содержании более 80 % масс. NH4ClO4 для системы NH4ClO4 - CO(NH2)2, и более 80% масс. NaClO4 для системы NаClO4 - CO(NH2)2.
Модели химических реакции в рассматриваемых системах:
5CO(NH2)2 + 6NH4ClO4 = 8N2 + 6HCl + 19H2O + 5CO2
4CO(NH2)2 + 3NaClO4 = 4N2 + 3NaCl + 8H2O + 4CO2
Было установлено, что перхлораты натрия и аммония образуют легкоплавкие эвтектики с карбамидом и нитратом аммония. Добавки перхлоратов к нитратным окислителям могут повышать энергоёмкость и легкоплавкость синтезируемых систем.
Наличие окислительно-восстановительных реакций выявлено также в ранее исследованных системах: NH4NO3 - C6H12N4, CO(NH2)2*HNO3 - C2H5NO. В системе NH4NO3 - C6H12N4 эвтектика содержит 20 % масс. C6H12N4 при 122 0С; а для системы CO(NH2)2*HNO3 - C2H5NO 70 % масс. C2H5NO при 42 0С.
Для системы NH4NO3 - C6H12N4 эффект ОВР наблюдается при содержании C6H12N4 более 30 % (масс.), для системы CO(NH2)2*HNO3 - C2H5NO - при содержании CO(NH2)2*HNO3 более 70 % (масс.).
С помощью методов моделирования были рассчитаны и экспериментально подтверждены характеристики эвтоник ряда трехкомпонентных систем: NH4NO3 – NH4СlO4 – H2O, NaСlO4– CO(NH2)2 – H2O, NH4СlO4 – CO(NH2)2 – H2O, CO(NH2)2*НNO3 – С2Н5NО – H2O, NH4NO3 – С6Н12N4 – H2O (табл. 4). Расхождение данных моделирования и эксперимента не превышает 5%.
Таблица 4
Характеристики эвтоник трехкомпонентных систем
| Система | Состав, % мас. | Температура | |||||
| А | В | С | А | В | С | оС | К |
| NH4NO3 | NH4СlO4 | Н2О | 39,41 | 6,29 | 54,30 | -18 | 255 |
| NaСlO4 | CO(NH2)2 | Н2О | 48,13 | 16,32 | 35,55 | -41,7 | 231,3 |
| NH4СlO4 | CO(NH2)2 | Н2О | 4,41 | 30,09 | 65,5 | -11,6 | 261,4 |
| CO(NH2)2 *НNO3 | С2Н5NО | Н2О | 6,87 | 44,73 | 48,4 | -37,3 | 235,7 |
| NH4NO3 | С6Н12N4 | Н2О | 39,86 | 9,49 | 50,65 | -18 | 255 |
В ходе исследований была установлена особенность этого ряда систем: наличие процессов с выделением газов. Это явление при построении диаграмм установлено впервые и в доступной нам литературе по физико-химическому анализу ранее не отражалось.
Эксперимент выявил наличие эвтоник в исследованных тройных системах. Области окислительно-восстановительных реакций, идущих с выделением газов, на фазовых диаграммах расположены около сильных окислителей или нестойких соединений, таких как, перхлораты аммония и натрия, нитрат карбамида, уротропин и др.
Был проведен ряд экспериментов, заключающихся в дополнительном исследовании серии внутренних разрезов трехкомпонентных систем.
Совокупностью аналитических, проекционных и экспериментальных методов построены полные поверхности кристаллизации систем. Определены температурные и концентрационные кривые границ окислительно-восстановительных реакций (рис. 1-5).
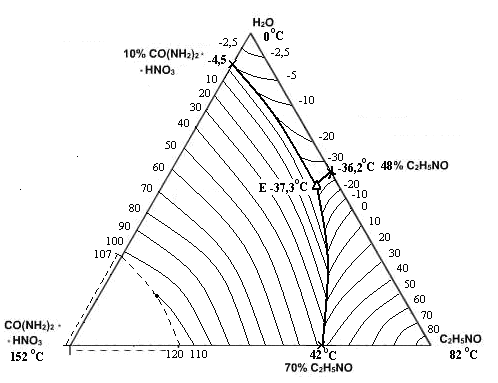
Рис. 1. Политерма кристаллизации системы CO(NH2)2 *НNO3 – С2Н5NО – H2O
(области ОВР пунктиром) (масс. %, t0С)
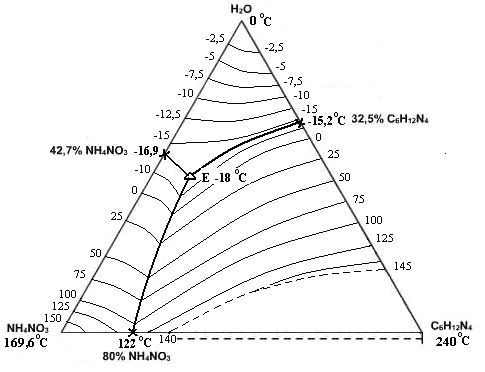
Рис. 2. Политерма кристаллизации системы NH4NO3 – С6Н12N4 – H2O
(области ОВР пунктиром) (масс. %, t0С)
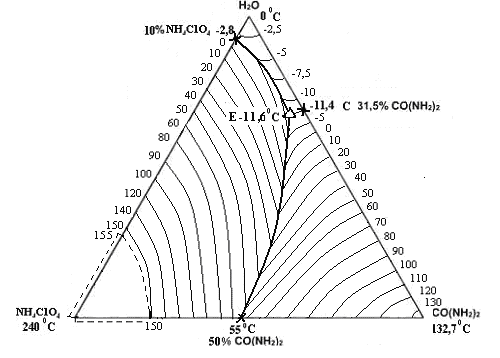
Рис. 3. Политерма кристаллизации системы NH4СlO4 – CO(NH2)2 – H2O
(области ОВР пунктиром) (масс. %, t0С)
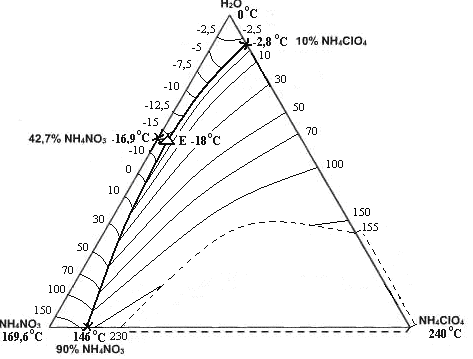
Рис. 4. Политерма кристаллизации системы NH4NO3 – NH4СlO4 – H2O
(области ОВР пунктиром) (масс. %, t0С)
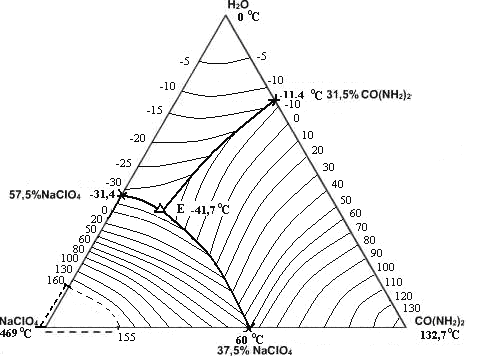
Рис. 5. Политерма кристаллизации системы NaСlO4 – CO(NH2)2 – H2O
(области ОВР пунктиром) (масс. %, t0С)
Для исследованных систем были рассчитаны тепловые эффекты химических реакций на 1 г безводных смесей, где вода - пар.
5CO(NH2)2 + 6NH4ClO4 8N2 + 6HCl + 19H2O + 5CO2
Н = -3,77 кДж/г
4CO(NH2)2 + 3NaClO4 4N2 + 3NaCl + 8H2O + 4CO2
Н = -3,76 кДж/г
13NH4NO3 + NH4ClO4 13,5N2 + HCl + 7,5O2 + 27,5H2O
Н = -1,51 кДж/г
7NH4NO3 + C6H12N4 + 11/2{4N2 + O2} 31N2+ 20H2O + 6CO2
Н = -6,51 кДж/г
CO(NH2)2*HNO3 + 6C2H5NO + 16,75{4N2 + O2} 38N2+ 17,5H2O +
+ 13CO2
Н = -14 кДж/г
Впервые рассчитаны и экспериментально подтверждены характеристики эвтоник четырехкомпонентных систем: NH4NO3 – NH4СlO4 – CO(NH2)2 – H2O, NH4NO3 – NaСlO4 – CO(NH2)2 – H2O, NH4NO3 – CO(NH2)2 – С2Н5NО – H2O.
Понижение температуры эвтоники при добавлении четвертого компонента важно для технологических целей, например, для получения составов, характеризующихся пониженной температурой замерзания. При этом существенно расширяются низкотемпературные области кристаллизации составов.
В табл. 4. представлены данные по составам и температурам эвтоник исследованных четырёхкомпонентных систем.
Таблица 4
Характеристики эвтоник четырёхкомпонентных систем
| Состав компонентов, % мас. | Температура эвтоники | ||||||
| NH4NO3 | NH4СlO4 | CO(NH2)2 | NaСlO4 | С2Н5NО | H2O | Т, К | t, 0C |
| 27,77 | 5,05 | 21,04 | - | - | 46,14 | 244 | -29 |
| 17,91 | - | 13,73 | 38,12 | - | 30,24 | 230 | -43 |
| 23,44 | - | 8,17 | - | 32,85 | 35,54 | 200 | -73 |
На рис. 6 представлена модель четырехкомпонентной системы NH4NO3 - С2Н5NО - CO(NH2)2 - H2O с нанесенной эвтонической точкой и объемами кристаллизации компонентов.
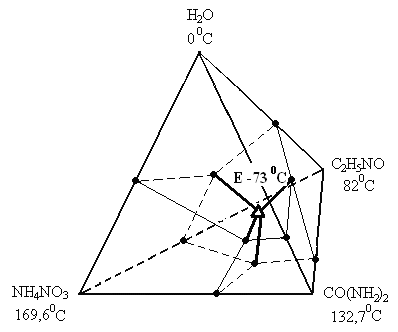
Рис. 6. Модель четырёхкомпонентной системы
NH4NO3 - С2Н5NО - CO(NH2)2 - H2O
Полученные данные по четырёхкомпонентным системам являются важными физико-химическими характеристиками для разработки энергонасыщенных композиций.
Проведенный цикл исследований позволяет сделать следующие выводы.
Выводы:
- Анализ современного состояния проблемы поиска альтернативных источников энергии показал, что перспективными являются растворы азотно-водородных соединений. Выбранные ингредиенты характеризуются значительной реакционной способностью, а их взаимодействие – высокими значениями энтальпий окислительно-восстановительных реакций и минимальным содержанием углерода.
- Построены фазовые диаграммы двухкомпонентных систем: CO(NH2)2 *НNO3 – H2O, NH4СlO4 – H2O, NaСlO4 – H2O, NH4NO3 – NaСlO4, NH4NO3 – NH4СlO4, экспериментально установлены характеристики эвтектик (эвтоник) систем, обозначены области окислительно-восстановительных реакций.
- В трехкомпонентных системах: NH4NO3 – NH4СlO4 – H2O, NaСlO4 – CO(NH2)2 – H2O, NH4СlO4 – CO(NH2)2 – H2O, CO(NH2)2 *НNO3 – С2Н5NО – H2O, NH4NO3 – С6Н12N4 – H2O осуществлено моделирование эвтоник, построены политермы кристаллизации фазовых диаграмм с выделением полей окислительно-восстановительных реакций. Показано, что реакции протекают при температуре ниже температуры плавления чистых компонентов, и сопровождаются выделением тепла, что важно для разработки альтернативных энергоносителей.
- Полученные характеристики эвтоник четырехкомпонентных систем: NH4NO3 – NH4СlO4 – CO(NH2)2 – H2O, NH4NO3 – NaСlO4 – CO(NH2)2 – H2O, NH4NO3 – CO(NH2)2 – С2Н5NО – H2O существенно расширяют низкотемпературные области кристаллизации составов, что является важным для разработки энергонасыщенных композиций.
- Результаты диссертационного исследования показывают принципиальную возможность осуществления окислительно-восстановительных реакций между реагентами типа "окислитель + восстановитель" в фазе совместных водных растворов, что, с учётом тепловыделения и образования газовых продуктов, может быть использовано при разработке энергонасыщенных композиций.
Основное содержание диссертации опубликовано:
- Трунин А.С., Кастерина Т.В., Юлина И.В. Исследование водонитратных систем как компонентов альтернативных энергоносителей // Вестник АГТУ. № 6. 2006. С. 143-149.
- Трунин А.С., Кастерина Т.В., Бодня М.С. Физико-химический анализ систем как компонентов неуглеводородных энергонасыщенных композиций // «Известия вузов. Химия и химическая технология». Т.51. Вып.5. 2008. С. 68-70.
- Трунин А.С., Юлина И.В., Макаров А.Ф., Кастерина Т.В., Зипаев Д.В. Исследование физико-химических систем с ингредиентами альтернативных энергоносителей // Аспирантский вестник Поволжья. №1(11). 2006. С. 66-70.
- Трунин А.С., Кастерина Т.В. Исследование многокомпонентных систем, как составляющих альтернативных топлив // Современные проблемы науки и образования. № 3. 2006. С. 108-110.
- Трунин А.С., Кастерина Т.В. Исследование водносолевых систем, как составляющих альтернативных топлив // Материалы междунар. научной конференции «Фундаментальные и прикладные проблемы современной химии». АГУ. Астрахань. 2006. С. 156-158.
- Трунин А.С., Кастерина Т.В., Юлина И.В. Исследование системы перхлорат натрия – вода как составляющей альтернативных топлив // Тр. 1-го Междунар. форума «Актуальные проблемы современной науки». Ч.19. Альтернативные энергоносители на возобновляемых ресурсах. Самара. 2005. С. 70-73.
- Трунин А.С., Кастерина Т.В., Юлина И.В. Исследование системы перхлорат аммония – вода как составляющей альтернативных топлив // Тр. 1-го Междунар. форума «Актуальные проблемы современной науки». Ч.19. Альтернативные энергоносители на возобновляемых ресурсах. Самара. 2005. С. 50-54.
- Трунин А.С., Юлина И.В., Кастерина Т.В. Исследование системы нитрат карбамида - вода как составляющей альтернативных топлив // Тр. 1-го Междунар. форума «Актуальные проблемы современной науки». Ч.19. Альтернативные энергоносители на возобновляемых ресурсах. Самара. 2005. С. 54-57.
- Трунин А.С., Юлина И.В., Кастерина Т.В. Исследование двухкомпонентной системы ацетамид – вода // Тр. 1-го Междунар. форума «Актуальные проблемы современной науки». Ч.19. Альтернативные энергоносители на возобновляемых ресурсах. Самара. 2005. С. 57-60.
- Трунин А.С., Юлина И.В., Кастерина Т.В., Макаров А.Ф. Исследование системы карбамид – перхлорат аммония как окислительной фазы неуглеводородных топлив // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 56-59.
- Трунин А.С., Кастерина Т.В., Моргунова О.Е. Политерма кристаллизации системы NH4NO3 – NH4СlO4 – H2O // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 116-125.
- Трунин А.С., Кастерина Т.В., Моргунова О.Е. Политерма растворения системы NH4СlO4 – CO(NH2)2 – H2O // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 125-134.
- Трунин А.С., Кастерина Т.В., Моргунова О.Е. Политерма кристаллизации системы NаСlO4 – CO(NH2)2 – H2O // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 134-143.
- Трунин А.С., Кастерина Т.В., Моргунова О.Е. Политерма кристаллизации системы NH4NO3 – С6Н12N4 – H2O // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 143-153.
- Трунин А.С., Кастерина Т.В., Моргунова О.Е. Политерма кристаллизации системы CO(NH2)2 *НNO3 – С2Н5NО – H2O // Тр. 3-го Междунар. форума «Актуальные проблемы современной науки». Ч.9. Физико-химический анализ. Вып. 2. Самара. 2007. С. 153-164.
- КАСТЕРИНА Татьяна Витальевна
ФИЗИКО-ХИМИЧЕСКИЙ АНАЛИЗ
СИСТЕМ С НАЛИЧИЕМ
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССОВ
02.00.04 – физическая химия
А в т о р е ф е р а т
Диссертации на соискание учёной степени
кандидата химических наук
____________________________________________________
Подписано в печать
Формат 60x84 1/16. Объем 1,25 п.л. Тираж 100 экз. Заказ №
__________________________________________________
Отпечатано в типографии
ООО ПКФ «Триада»

