Биологически активные аминокислотные производные поли-n-винилпирролидона и их металлокомплексы
На правах рукописи
Ташмухамедов Равшан Иркинович
Биологически активные аминокислотные производные поли-N-винилпирролидона и их металлокомплексы
02.00.06 – Высокомолекулярные соединения
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора химических наук
Москва – 2007
Работа выполнена в Российском химико-технологическом университете имени Д.И.Менделеева (Москва, Россия) и на фирме «Фармед» (Ташкент, Республика Узбекистан)
| Научный консультант | доктор химических наук, профессор Штильман Михаил Исаакович |
| Официальные оппоненты | доктор химических наук профессор Коршак Юрий Васильевич |
| доктор химических наук профессор Паписов Иван Михайлович | |
| доктор химических наук, профессор Телешов Эдуард Никанорович | |
| Ведущая организация | Институт нефтехимического синтеза им.А.В.Топчиева РАН |
Защита состоится «01» ноября 2007 г. в 15.00 час. на заседании Диссертационного совета Д 212.120.04 при ФГОУ ВПО Московская академия тонкой химической технологии им. М.В.Ломоносова (МИТХТ) (119571 Москва, пр.Вернадского, д.86) в ауд._________
С диссертацией можно ознакомиться в библиотеке МИТХТ им. М.В.Ломоносова
Автореферат размещен на сайте www.mitht.ru
Автореферат разослан «_____»____________ 2007 г.
Ученый секретарь диссертационного совета Д 212.120.04,
доктор химических наук, профессор И.А.Грицкова
1. ВВЕДЕНИЕ
Актуальность выбранной темы. Макромолекулярные системы, обладающие различной биологической активностью, в частности, оказывающие лекарственное действие, обладают существенными преимуществами перед низкомолекулярными аналогами, а в ряде случаев определенные виды активности характерны только для макромолекулярных систем.
К настоящему времени описано большое количество полимерных соединений различного химического строения, проявляющие биологическую активность как за счет макромолекулярной природы (полимеры с собственной биологической активностью), так и за счет определенного фрагмента, который может постепенно выделяться из полимера и поступать в биологический объект (системы с контролируемым выделением активного вещества).
В последнем случае определяющее значение имеет не только тип выделяющегося активного вещества и характер связи его с полимерным носителем, определяющей скорость выделения, но и строение самого полимерного носителя, который должен обладать высоким уровнем безвредности (особенно для систем, вводимых инъекционно).
Поэтому во многих случаях в качестве основы для создания полимерных носителей лекарственных веществ используются полимеры, хорошо изученные как компоненты кровезаменителей, взаимодействие которых с организмом исследовано достаточно глубоко, в том числе поли-N-винпилпирролидон, входящий в состав кровезаменителей дезинтоксикационного назначения.
Важнейшим элементом создания лекарственных полимеров с контролируемым выделением активного вещества является выбор иммобилизуемого объекта, определяющего характер и уровень биологической активности, что отражено в громадном числе публикаций.
В то же время, такая важная группа биологически активных полимеров как макромолекулярные производные биогенных металлов, в первую очередь переходных групп, которые могут явиться основой целого ряда терапевтических систем, исследована явно недостаточно.
При этом существенно, что успешное использование таких систем связано с обеспечением постепенного поступления активного агента в организм в оптимальных дозах и исключение возможной токсичности, проявляющейся при повышенных концентрациях. Это подразумевает использование для иммобилизации металлов оптимальных по своим характеристикам носителей, как с точки зрения полной выводимости из организма, так и с точки зрения отсутствия острой и длительной токсичности.
Таким образом, весьма актуальным является разработка полимерных металлокомплексов, содержащих различные металлы, а в качестве макромолекулярных носителей используются полимеры с высоким уровнем биологической безвредности.
Цель работы состояла в разработке нового типа полимерных носителей для биологически активных веществ на основе эпоксидсодержащего поли-N-винилпирролидона, содержащего боковые комплексообразующие аминокислотные группы, получение на их основе макромолекулярных комплексов переходных металлов и исследование их в качестве макромолекулярных систем, обладающих различными типами биологической активности.
Научная новизна работы. Разработаны новые биологически активные аминокислотные производные поли-N-винилпирролидона и их металлокомплексы, характеризующиеся низкой токсичностью и проявляющие биологическую активность различного типа.
Предложен новый метод функционализации поли-N-винилпирролидона, в том числе его промышленных образцов медицинского назначения, путем введения в него эпоксидных групп с использованием модифицированной реакции Дарзана, что позволяет получать реакционноспособные полимерные производные этого полимера с заранее заданным молекулярно-массовым распределением.
Получен ряд новых полимерных соединений низших,-аминокислот путем их реакции с эпоксидсодержащим поли-N-винилпирролидоном и металлокомплексов ряда переходных металлов на их основе.
Впервые получены аминокислотные производные поли-N-винилпирролидона и их металлокомплексы с использованием в качестве носителя амфифильного полимера N-винилпирролидона, способного к образованию наноразмерных агрегатов в водных растворах, и изучены их свойства.
Показано, что аминокислотные производные эпоксидсодержащих полимеров N-винилпирролидона и металлокомплексов на их основе обладают различными типами биологической активности. Выявлена взаимосвязь между биологической активностью полимеров и их химическим строением.
Практическая значимость работы. В модельных условиях в опытах на клетках и в опытах на животных in vivo показано, что синтезированные полимеры и металлокомплексы на их основе обладают низкой токсичностью, и проявляют высокую иммуностимулирующую, иммуноадъювантную, антвирусную, гемостимулирующую активность, а также усиливают продуцирование интерферона, подавление репликации микроорганизмов под действием антибиотиков.
Эти данные указывают на перспективность использования синтезированных полимеров и их металлокомплексов в качестве основы лекарственных препаратов.
Объем и структура диссертации. Диссертационная работа изложена на 220 стр. машинописного текста и включает введение, обзор литературы, обсуждение результатов, основные выводы и список цитированной литературы из 243 наименования. Работа содержит 53 таблиц и 68 рисунков.
2. ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
2.1. Выбор метода синтеза полимерных носителей и полимерных металлокомплексов
Cоздание макромолекулярных систем, содержащих атомы переходных металлов, способных оказывать тот или иной терапевтический эффект, требовало выбора полимерных носителей, обладающих оптимальными характеристиками.
В случае лекарственных полимеров такая оптимизация подразумевает придание системе биосовместимости, обеспечение требуемого уровня прочности связи между полимерным носителем и группировкой, определяющей биологическую активность. Наконец, в случае использования полимера в виде водного раствора, например, при инъекционном введении, строение полимерного носителя должно обеспечить растворимость системы в воде.
С учетом этих требований в качестве основы использовавшихся полимерных носителей был выбран поли-N-винилпирролидон (далее – ПВП), допущенный для инъекционного введения в организм как компонент кровезаменителей дезинтоксикационного действия.
Для введения в состав полимера атомов металлов был использован метод комплексообразования. В этом случае в боковые группы полимеров были введены группировки, способные к комплексообразованию. В качестве таких группировок были использованы остатки низших,-алканаминокислот. Использование в качестве комплексообразующего фрагмента аминокислот позволяло получать системы с высокой биосовместимостью.
В качестве исходных полимеров, на основе которых были получены полимерные производные аминокислот, были использованы полимеры N-винилпирролидона, содержащие боковые эпоксидные группы. При синтезе таких полимеров были использованы подходы, позволяющие получить полимеры с оптимизированным молекулярно-массовым распределением.
2.2. Синтез эпоксидсодержащих носителей
В качестве эпоксидсодержащего полимера N-винилпирролидона в работе был использован специально синтезированный эпоксидированный поли-N-винилпирролидон (далее - ЭПВП), в том числе содержащий концевой гидрофобный фрагмент. В ряде исследований для сравнения был рассмотрен также сополимер N-винилпирролидона и аллилглицидилового эфира.
Для получения ЭПВП был использован новый подход, заключающийся во введении в ПВП эпоксидных групп в условиях модифицированной реакции Дарзана.
Классическая схема реакции образования эпоксидов по Дарзану описана для взаимодействия эфиров хлоруксусной кислоты с карбонильными соединениями в щелочной среде, в первую очередь с кетонами. В данном случае был использован нестандартный подход – взаимодействие с производным хлоруксусной кислоты – хлорацетамидом – карбонила пирролидонового кольца, т.е. карбонила циклического амида:
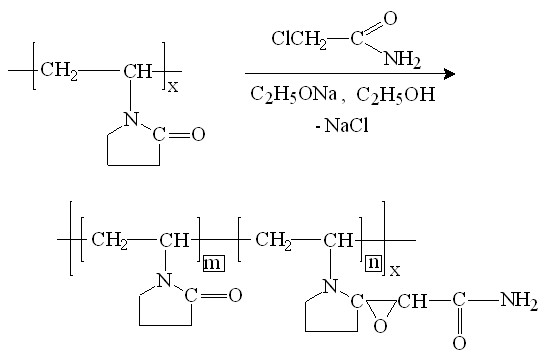
Введение в ПВП эпоксидной группы, обладающей высокой реакционной способностью без дополнительного активирования позволяет рассматривать получаемый полимер в качестве потенциального носителя различных лигандов. Синтезированный в данном случае эпоксидсодержащий полимер (ЭПВП) содержит в реакционноспособном звене амидную группу, что позволяет обеспечить высокую общую полярность полимера.
Это существенно с точки зрения возможности использования его в качестве носителя гидрофобных веществ, при сохранении растворимости всей системы в воде.
Образование эпоксидсодержащего продукта при взаимодействии пирролидонового цикла с хлорацетамидом в условиях модифицированной реакции Дарзана, было подтверждено синтезом модельного соединения - эпоксидированного N-метилпирролидона (4-метил-1-окса-4-азаспиро[2,4]гептан-2-карбоксамида):
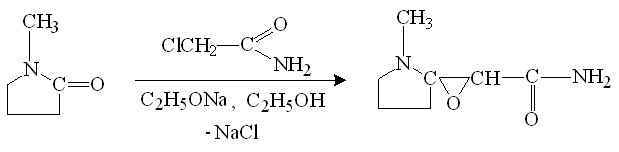
Ход протекания реакции и чистоту полученного продукта контролировали методом тонкослойной хроматографии (элюент - диоксан : вода = (5:2), пластинки фирмы «Silufol UV-254», Rf=0,57), а также методом высокоэффективной жидкостной хроматографии (хроматограф HP 1090, колонка ODS Hipersyl 1002 мм, элюент – фосфатный буфер, скорость потока 0,25 мл/мин). Как было показано, продукт реакции является индивидуальным веществом без примесей исходных веществ или побочных продуктов.
Реакцию проводили в среде этанола при 10оС. Бесцветные кристаллы эпоксидированного N-метилпирролидона плавились при 171оС. Его строение было подтверждено элементным анализом и данными ИК- и ЯМР- спектроскопии (ИК спектр: 1250 см -1, 1114 см-1, 930 см –1, 770 см -1 (оксирановый цикл); 3400 см -1 (NH), 1650 см -1 и 1440см -1 (C=O амидной группы). ПМР спектр: (, м.д.): 2,04 (м, 2Н, СН2); 2,42 (т, 2Н, СН2); 2,82 (с, 3Н, СН3); 3,50 (т, 2Н, СН2); 4,67 (NН2); 4,90 (с, 1Н, СН) ).
Для исследования особенностей протекания реакции с участием ПВП и нахождения оптимальных условий получения его эпоксидированного производного (ЭПВП), содержащего требуемое количеством эпоксидных групп, было исследовано влияние на протекание процесса различных факторов (концентрации и соотношения реагентов, температуры и времени реакции, а также строения используемого в качестве среды спирта и молекулярных масс ПВП).
В работе использовали ПВП с Mn= 9,0103, 25,4 (25)103 и 39,8 (40) 103.
Строение полученного полимера было подтверждено функциональным анализом (потенциометрическое титрование), ИК спектральным анализом и ПМР-спектроскопией.
Проведённые исследования показали, что взаимодействие хлорацетамида с ПВП проходит в мягких условиях (Т=10-12оС). При этом в оптимальных условиях образуется продукт с достаточно высоким содержанием эпоксидных групп (20-25 мол.%).
В качестве примера на рис.1,2 приведены зависимости, характеризующие влияние на содержание в полимере ВП эпоксидных групп температуры реакции и соотношения хлорацетамид:ПВП времени процесса для полимеров с различной молекулярной массой.
Рис.1. Зависимость количества эпоксидных групп от температуры (соотношение ПВП:Хлорацетамид:Na – 1:1:1 осново-моль/моль/моль, концентрация полимера в растворителе 12,5 %, время проведения реакции 4 часа. Молекулярная масса ПВП: 1 - 40 тыс. 2 - 25 тыс.; 3 - 9 тыс.)
Как видно, повышение температуры реакции выше 20оС не приводит к повышению количества эпоксидных групп, что, возможно связано с их возможным гидролизом в щелочной среде.
При этом было обнаружено, что во всех случаях при одинаковых условиях степени замещения пирролидоновых циклов спиро-циклами с эпоксидными группами определенным образом зависят от молекулярных масс полимеров. Количество эпоксидированных звеньев повышается с уменьшением молекулярной массы полимеров, что, вероятно, определяется пространственными причинами.
Рис. 2. Зависимость количества эпоксидных групп от соотношения ПВП : Хлорацетамид (концентрация полимера в растворе 12,5 %, температура t=100C, время проведения реакции 4 часа. Молекулярная масса ПВП: 1 - 40 тыс. 2 - 25 тыс.; 3 - 9 тыс.).
Полученный ЭПВП представляет собой бесцветный порошок, растворимый в воде и полярных органических растворителях.
Для получения его аминокислотных производных и затем полимерных металлокомплексов в работе был использован ЭПВП с содержанием эпоксидсодержащих звеньев 10,31 мол.% (10 мол.%) и молекулярной массой около Mn = 9103 (полимер, являющийся основой препарата «Неогемодез».
Для синтеза амфифильных полимеров ВП, содержащих боковые аминокислотные группы в качестве эпоксидированного носителя был использован ПВП, содержащий одну концевую гидрофобную алифатическую группу –С17Н35. (Mn2000).
Эпоксидные группы вводили в этот полимер с использованием модифицированной реакции Дарзана. Содержание эпоксидных групп в полимере, использовавшемся для дальнейших превращений было 9 мол.%. Наличие в полученных водорастворимых амфифильных полимерах гидрофобной концевой группы определяло их склонность к образованию наноразмерных агрегатов в водной среде.
В сравнительных опытах для реакции с аминокислотами и далее для получения металлокомплексов в работе был также использован сополимер N-винилпирролидона и аллилглицидилового эфира с содержанием эпоксидсодержащих звеньев 9,86 мол.% (10 мол.%) и молекулярной массой Mn = 17103D (паровая осмометрия) и Mw = 24103D (седиментация).
2.3. Синтез полимеров, содержащих аминокислотные остатки
Синтез полимеров, содержащих боковую группировку, способную образовывать хелатные комплексы с переходными металлами, проводили взаимодействием эпоксидсодержащих полимерных носителей, с низшими,-аминокислотами.
Проходящая в этом случае реакция N-алкилирования аминогруппы аминокислоты принципиально не препятствовала последующему образованию комплексов как с участием карбоксильной группы, так и с участием аминогруппы (за счет свободной пары электронов). Реакцию полимерных эпоксидов с аминокислотами проводили pH > 7, когда разрушается цвиттер-ион аминокислот и их аминогруппа приобретает основные свойства и способность вступать в реакции алкилирования, в том числе, присоединяться к оксирановому циклу.
В случае сополимера N-винилпирролидона и аллилглицидилового эфира, содержащего монозамещенный оксирановый цикл, присоединение кислоты протекает в соответствии правилом Красуского, когда аминогруппа направляется к СН2-группе.
С другой стороны, в случае ЭПВП, когда в реакцию с аминокислотой вступал 1,2-дизамещенный оксиран, реакция могла протекать в двух направлениях – с присоединением остатка аминокислоты к атому углерода, входящему в цикл, и с присоединением остатка аминокислоты к атому углерода, связанному с карбонилом амидной группы:
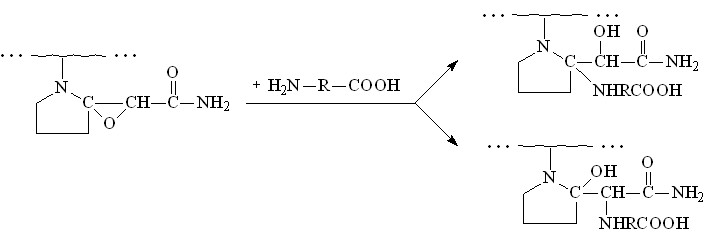
Поэтому, требовались дополнительные исследования для выявления строения продукта. Для выяснения направления протекания этой реакции было исследовано строение продукта присоединения аминокислоты в модельной реакции ее взаимодействия с эпоксидсодержащим N-метилпирролидоном с глицином.
Реакцию взаимодействия ЭМП с глицином проводили при температуре 25оС в щелочной среде в течение 4 часов. Полученный продукт, выделенный после нейтрализации раствора, перекристаллизовывали из этанола.
Ход протекания реакции и чистоту полученного продукта контролировали методом тонкослойной хроматографии (элюент – метанол : 10% аммиачный раствор = (4:1), пластинки фирмы «Silufol UV-254», Rf=0,67), а также методом высокоэффективной жидкостной хроматографии (хроматограф HP 1090, колонка ODS Hipersyl 1002 мм, элюент – фосфатный буфер, скорость потока 0,25 мл/мин).
Полученный продукт представлял собой бесцветные кристаллы (tпл = 196оС), растворимые в воде, диметилсульфоксиде. Строение полученного продукта было определено методом ИК, ПМР спектроскопии.
Анализ ИК-спектра ЭМП-глицин, снятого с таблеток KBr с исследуемым веществом с помощью микрофокусировочной приставки на ИК-Фурье спектрометре «Paragon 1000РС», показывает, что происходит исчезновение полос, принадлежащих эпоксидной группе: 1250 см -1, 930 см -1 и 770 см -1, а также появление ряда других полос, соответствующие присоединению аминокислоты: 1610 см -1, 1335 см-1 (колебания карбоксильной группы), 1180 см-1 – участие образующейся С-N связи в скелетных колебаниях молекулы. Также в спектре наблюдаются полосы 3400 см -1 (NH-группа), 1650 см -1 и 1410 см -1 (колебания C=O амидной группы).
На ПМР спектре ЭМП-глицин (снят на приборе «Bruker spectrometer 200 MHz», c использованием D2O в качестве растворителя и тетраметилсилана в качестве эталона.) наблюдаются следующие сигналы (, м.д.): 1,88 (м, 2Н, СН2); 2,17 (т, 2Н, СН2); 2,67 (с, 3Н, СН3); 3,02 (т, 2Н, СН2-глицина); 3,36 (т, 2Н, СН2); 4,05 (с, 1Н, СН).
При этом сигнал протонов с химическим сдвигом 3,02 м.д. соответствует СН2 группе от глицинового остатка (смещается в высокочастотную область по сравнению с самим глицином, который имеет сигнал протонов СН2 группы с химическим сдвигом 3,42 м.д.), а сигнал протона СН группы при раскрытии эпоксидного кольца с химическим сдвигом 4,02 м.д. незначительно смещается в область слабого поля с химическим сдвигом 4,05 м.д.
Учитывая, что в данной реакции возможно образование двух изомеров продукта реакции в зависимости от места присоединения остатка глицина в или положении по отношению к амидной группе при раскрытии оксиранового кольца, для определения места присоединения остатка глицина был проведен анализ ПМР спектра полученного соединения, а также анализ теоретически предполагаемых ПМР спектров возможных изомеров (компьютерная программа ACDLab):
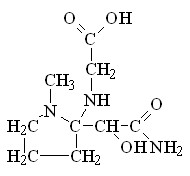 | 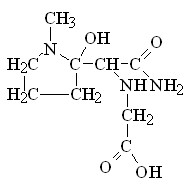 |
| 1 (-положение к амидной группе) | 2 (-положение к амидной группе) |
Было установлено, что различить изомеры 1 и 2 можно по сигналу протонов (СН) при раскрытии эпоксидного кольца, а также по сигналу протонов СОСН2 пирролидонового кольца. Сигнал протона СН изомера 1 имеет такой же практически химический сдвиг 4,05 м.д., как и в случае исходного вещества ЭМП (4,02 м.д.), если бы остаток глицина присоединялся в - положение к амидной группе, то сигнал протона СН группы (при эпоксидном кольце) сместился бы в более сильное поле. Сигнал протонов СОСН2 пирролидонового кольца незначительно смещается в более сильное поле с химическим сдвигом 2,17 м.д.
Таким образом, присоединение остатка аминокислоты к эпоксидсодержащему звену полимера, очевидно, протекает, по атому углерода, являющимся центральным в исходном спиросоединении.
Присоединение остатка глицина в -положение к амидной группе не противоречит теоретическим представлениям, что может быть, таким образом, представлено как:
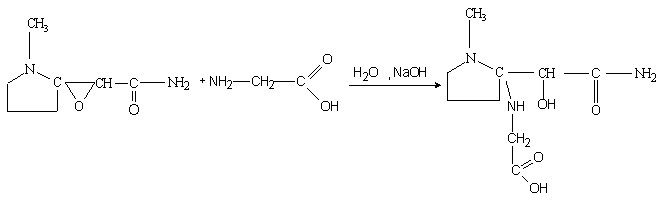
Для создания в полимерах боковых комплексообразующих групп был использован ряд,-аминокарбоновых кислот, содержащих между аминной и карбоксильной группой линейный алкиленовый радикал. Это, с одной стороны позволяло выявить влияние длины этого радикала на все протекающие реакции и строение образующихся металлокомплексов, а с другой выявить границы размеров циклов комплексов, позволяющие участвовать в их образовании и карбоксильной и аминной групп.
Поэтому в работе для получения боковых комплексообразующих групп были использованы аминокислоты глицин, -аланин, -аминомасляная и -аминокапроновая кислоты, а протекание их реакций с ЭПВП может быть представлено следующим образом:
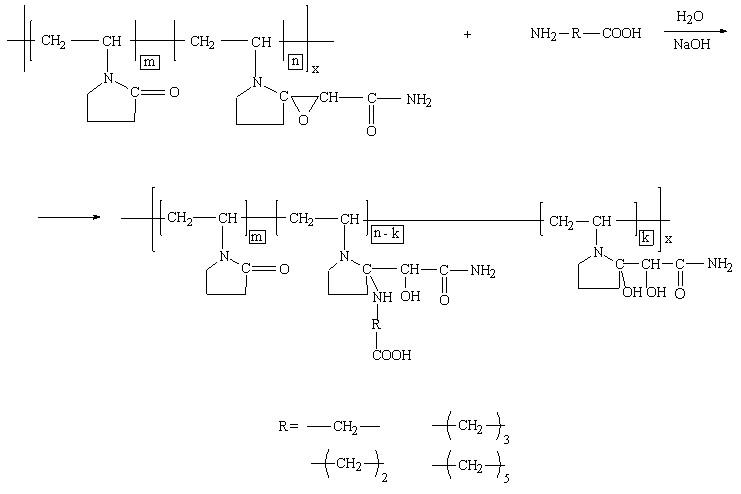
Для уточнения условий проведения реакции эпоксидсодержащих полимерных носителей с аминокислотами было исследовано влияние на глубину протекания процесса ряда факторов – рН среды, температуры реакции, соотношения реагентов.
При проведении реакции при различных рН среды (рН создавался использованием различных фосфатных буферов) наблюдалось определенное повышение степени превращения эпоксидных групп при увеличении значения рН (исследовавшийся диапазон рН 7,6, 9,0 и 10,0). Поэтому в дальнейшем в реакцию вводили натриевые соли кислот при рН=10,0.
Повышение степени превращения наблюдалось при снижении температуры реакции с 343 до 298К, что, вероятно, объясняется побочным гидролизом эпоксидных групп при повышенной температуре. Дальнейшее снижение температуры не приводило к заметному возрастанию количества присоединившейся аминокислоты. Реакцию проводили в течение 4 часов.
Степень превращения зависела также от количества введенной в реакцию аминокислоты. Так, в этой же паре реагентов (температура 298 К) при соотношениях аминокислоты и эпоксидных групп 2:1, 10:1 и 20:1 удалось повысить степень превращения с 80 % до 85%. Конечные продукты очищали диализом, сушили лиофильно и исследовали.
Производные аминокислот, растворялись в воде, амидных растворителях и диметилсульфоксиде. В то же время, полимеры с аминокислотными остатками, полученные на основе ЭПВП, не растворялись или плохо растворялись (в зависимости от содержания в исходном полимере звеньев с оксирансодержащих звеньев) в спиртах и кетонах. С другой стороны, полимеры, полученные на основе сополимера N-винилпирролидона и аллилглицидилового эфира, растворялись также в спиртах и кетонах. Эта различие в растворимости определяется наличием в полимерах, полученных на основе ЭПВП боковых амидных групп, определяющим достаточно сильное межмолекулярное взаимодействие за счет водородной связи.
Строение полимеров, содержащих аминокислотные группировки, было подтверждено исследованием их ИК спектров (ИК-Фурье спектрометр "Paragon 1000РС").
Как и следовало ожидать, спектры полученных полимеров были менее дифференцированы, чем спектры низкомолекулярного модельного соединения. Тем не менее на них четко различимы области полос поглощения С=О группы (от амида в пирролидоновом кольце, амида эпоксидсодержащего звена, а также от карбоксильной группы аминокислоты). Поглощение эпоксидных групп в полимерах обнаружено не было. Подтверждают строение полимеров с боковыми аминокислотными группировками и спектры ПМР.
Так, в спектре ПМР раствора ЭПВП-глицин (D2O) наблюдаются изменения в области от 3,66 до 4,01 м.д. с увеличением относительной интенсивности пиков по сравнению с исходным ЭПВП, что может свидетельствовать о присоединении аминокислоты. В спектре ПМР раствора ЭПВП-глицин в хлороформе-d1 наблюдаются два положения сигналов связанной воды при 4,90 м.д. и 2,85 м.д., которые находятся в более высокочастотной области по сравнению с ПВП и ЭПВП.
В спектре ПМР раствора ЭПВП--аланин наблюдаются те же характерные, что и для предыдущего соединения, особенности: увеличение относительной интенсивности низкочастотного широкого пика 3,66 м.д. и изменения в области от 3,66 до 4,01 м.д. Положение пика воды в спектре ПМР раствора ЭПВП--аланин в хлороформе-d1 находится в области 2,77 м.д., при этом молекулы воды присоединяются почти к каждому звену полимера.
Таким образом, в результате проведенных реакций образуются полимеры ЭПВП с аминокислотными остатками в боковой цепи. В модифицированных полимерах аминокислоты связаны с эпоксидными звеньями исходного полимера по аминным группам. Причем присоединение к оксирановому циклу идет по углероду, находящемуся в азотсодержащем цикле.
Степень превращения в полимерах ЭПВП с аминокислотными остатками определяли функциональным анализом по аминной и карбоксильной группам.
В таблице 1 приведены также данные по рассмотренным полимерам на основе сополимера N-винилпирролидона и аллилглицидилового эфира.
Таблица 1
Характеристики эпоксидсодержащих полимеров ВП, модифицированных
аминокислотными остатками
| ПОЛИМЕР | Степень превращения,* масс. % | |
| По NH-группам | По СOOH-группам | |
| ЭПВП-глицин | - | 78,2 |
| ЭПВП--аланин | 82,2 | 83,1 |
| ЭПВП –-аминомасляная кислота | 83,4 | 84,5 |
| ЭПВП--амино-капроновая кислота | 85,3 | 86,7 |
| СПЛ ВП-АГЭ – глицин | 79,2 | |
| СПЛ ВП-АГЭ - -аланин | 85,9 | 81,5 |
| СПЛ ВП-АГЭ - -аминомасляная кислота | 87,2 | 86,0 |
| СПЛ ВП-АГЭ - -аминокапроновая кислота | 88,4 | 87,2 |
* По результатам потенциометрического титрования
Как видно из данных таблицы 1, функциональные анализы по двум различным группам дают сходные результаты для модифицированных полимеров с -аланином, -аминомасляной и -аминокапроновой кислотами. Из таблицы также видно, что степень превращения несколько увеличивается в ряду от полимеров, содержащих остатки глицина, до полимеров с -аминокапроновой кислотой.
На основе эпоксидированного амфифильного ЭПВП (Mn = 2060, содержание эпоксидных групп 9,1 мол.%) с использованием вышеописанной стандартной методики были получены продукты, содержащие остатки -аланина и -аминомасляной кислоты. Степени замещения эпоксидных групп в этих реакциях были соответственно 78,1 и 81,3%, т.е. эти полимеры содержали 7,1 и 7,4 мол.% звеньев с остатками аминокислот.
Они хорошо растворялись в воде и их критическая концентрация образования агрегатов, найденная стандартным флуоресцентным методом по солюбилизации пирена, была близка 6,1 мкМ.
Кислотно-основные свойства модифицированного ЭПВП, содержащего аминокислотные остатки
При исследовании кислотно-основных свойств полученных полимеров ЭПВП с фрагментами глицина, -аланина, -аминомасляной и -аминокапроновой кислот было показано, что они ведут себя в растворе как типичные полиэлектролиты.
Определение констант основной (pKb) и кислотной (pKa) диссоциации проводили методом потенциометрического титрования с расчетом по уравнению Гендерсона-Хассельбаха.
При сравнении абсолютных значений констант диссоциации для полимеров с аминокислотными остатками и их низкомолекулярных аналогов видно, что во всех случаях наблюдается незначительная тенденция к уменьшению значений pKb и увеличению pKa для полимерных производных (в таблице 2 приведены соответствующие данные).
Таблица 2
Сравнение pKb и pKa модифицированных полимеров и их
низкомолекулярных аналогов
| Соединение | pKb | pKa |
| ЭПВП-глицин | 9,9 | 3,18 |
| ЭПВП--аланин | 10,06 | 3,37 |
| ЭПВП--аминомасляная кислота | 10,1 | 4,00 |
| ЭПВП--аминокапроновая кислота | 10,19 | 4,43 |
| Глицин | 9,98 | 2,35 |
| -аланин | 10,15 | 3,28 |
| -аминомасляная кислота | 10,38 | 3,90 |
| -аминокапроновая кислота | 10,72 | 4,39 |
Т.е. гидроксильная группа, образующаяся после раскрытия оксиранового цикла, снижает основные свойства аминокислот, связанных с полимером. Снижение основности аминогрупп уменьшает ионизацию карбоксильной группы аминокислотного остатка модифицированного полимера, вследствие чего значения кажущихся констант кислотной диссоциации (pKa) увеличиваются. При этом, по мере удаления аминной группы от карбоксильной, значения pKa для модифицированных полимеров приближаются к значениям pKa их низкомолекулярных аналогов.
Таким образом, были получены полимеры ЭПВП с аминокислотными остатками, строение которых было подтверждено методами ИК- и ПМР-спектроскопии, функциональным и элементым анализами. Установлено, что степень превращения в модифицированных полимерах зависит от природы модифицирующих аминокислот и увеличивается с повышением их основных свойств. Аналогичная картина наблюдалась в случае полимерных производных аминокислот, полученных на основе сополимера N-винилпирролидона и аллилглицидилового эфира.
Исследование светорассеяния растворов
аминокислотных производных
Как известно, на уровень биологической активности водорастворимых полимеров, вводимых в организм, существенное влияние оказывает их конформация в растворе, влияющая как на взаимодействие с мембранами и мембранными рецепторами клеток, так и на проникновение в клетку за счет процесса эндоцитоза. В этих процессах значительное влияние оказывают как минимум размер макромолекулярного объекта.
Для исследования поведения синтезированных полимеров в водном растворе было проведено изучение их светорассеяния. При этом были рассмотрены полимеры с аминокислотными остатками на основе ЭПВП (Mn = 9103, 9,9% эпоксидных групп) и сополимера N-винилпирролидона и аллилглицидилового эфира (Mn = 12103, 9,7% эпоксидных групп) и.
Экспериментальная автокорреляционная функция была найдена с использованием прибора, снабженного диодным лазером (Coherent Radiation Model Innova) с длиной волны 532 нм.
На рис.3 показаны распределения времен релаксации для полимера ЭПВП-глицин, ПВП и глицинового производного сополимера N-винилпирролидона и аллилглицидилового эфира (СПЛ ВП-АГЭ-глицин) при различных углах рассеяния.
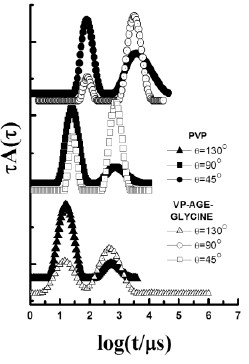  | 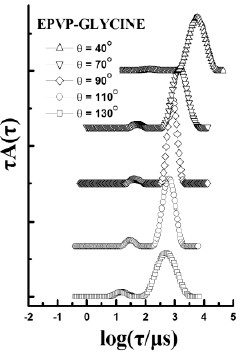  |
Рис.3. Распределение времен релаксации в виде зависимостей функции A() = f(log ) для растворов ПВП, (СПЛ ВП-АГЭ)-глицин, ЭПВП-глицин
Как видно, на этих зависимостях хорошо различимы два пика (две моды – «медленная» и «быстрая»), показывающие, что в системе имеются группы частиц двух размеров – обладающие более быстрой и более медленной скоростью диффузии в растворе.
По видимому, в этом случае «быстрая» мода соответствует диффузии макромолекулярных клубков неассоциированных молекул, а «медленная» мода – их ассоциатам. Отнесение этих пиков к клубкам единичных макромолекул и ассоциатам подтверждено определением величин их средних гидродинамических радиусов.
Как было найдено, гидродинамический радиус Rh для исходного полимера ПВП и полимерных производных аминокислот находился в диапазоне 3,2-3,7 нм, а для объектов, соответствующих «медленной» моде, равнялся 93 нм.
Соотношение количеств ассоциатов и макромолекулярных клубков может быть оценено из соотношения площадей под модами. Хотя при рассмотрении интенсивности светорассеяния должно быть учтено, что молекулярные массы ассоциатов заметно выше, чем молекулярные массы макромолекулярных клубков единичных макромолекул.
Тем не менее, сравнение параметров мод корректно показывают тенденцию соотношения различных частиц в растворе для различных полимеров. Значения этих соотношений приведены в таблице 3.
Как видно, сам ПВП обладает слабой склонностью к ассоциации в растворе, что известно из литературы. С другой стороны, в случае аминокислотных производных площади под «медленной» модой значительно больше.
Таблица 3
Соотношение площадей (А) под модами, отражающими медленную и быструю диффузию, на кривых распределения экспериментальных корреляционных функций для различных полимеров
| Тип полимера | А* |
| Поли-N-винилпирролидон (ПВП) | 0,192 |
| Глицин – [Сополимер ВП-АГЭ] | 0,558 |
| Глицин - [ЭПВП] | 0,921 |
А* - доля площади под пиком медленной диффузии к суммарной площади под пиками (определены для угла рассеяния =90оС).
При переходе от полимерного производного глицина, полученного на основе сополимера N-винилпирролидона и аллилглицидилового эфира, к полимерному производному, полученному на основе ЭПВП наблюдается значительное увеличение количества асcоциатов, причем в данном случае агрегаты образуются даже в разбавленных растворах.
Вероятно, это явление связано с наличием в полимерных производных аминокислот боковых функциональных групп, склонных к образованию водородных связей, а наличие в производных боковой первичной аминогруппы, по-видимому, повышает возможность межмолекулярного взаимодействия макромолекул полимеров в растворе.
Как видно из данных рис.3, положение пиков для различных полимеров соответствует близким временам диффузии, что также указывает на близкие значения размеров макромолекулярных клубков различных полимеров, в том числе ПВП. Т.е. введение в полимеры аминокислотных групп не оказывает значительного влияния на размер их макромолекулярных клубков в водном растворе по сравнению с самим ПВП.
В случае амфифильных полимерных производных аминокислот -аланина и -аминомасляной кислоты размер агрегатов, определенный методом динамического светорассеяния, находился в диапазоне 150-200 нм. Т.е. эти полимеры имели высокую склонность к образованию наноразмерных агрегатов в растворе, также как другие известные амфифильные полимеры винилпирролидона.
Таким образом, исследования светорассеяния растворов полимерных производных аминокислот показали, что эти полимеры в отличие от самого ПВП имеют определенную склонность к образованию ассоциатов, в том числе в в разбавленных растворах. При этом эта склонность к ассоциации в большей степени выражена для аминокислотных производных ЭПВП.
3.4. Синтез полимерных металлокомплексов и их исследование
Для получения полимерных металлокомплексов был выбран ряд переходных металлов, производные которых обладают биоактивностью – кобальт (II), германий (II), медь (II), цинк (II) и марганец (II), платина (II).
Полимерные металлокомплексы получали смешением ацетоновых или диоксановых растворов хлоридов металлов с растворами полимеров в смеси растворителей метанол-ацетон (3:1). Смесь перемешивали и концентрировали на роторном испарителе до выпадения осадка, который очищали экстракцией ацетоном и высушивали в вакууме.
Взаимодействие металла с лигандом изучали с помощью фотометрии, комплексонометрии, потенциометрии, вискозиметрии, а для определения характера донорных атомов, взаимодействующих с ионами металлов проведены исследования полученных полимерных металлокомплексов методами ИК-, ПМР, и ЭПР-спектроскопии.
При растворении в воде систем ЭПВП-глицин-CoCl2 и ЭПВП--аланин-CoCl2 образуются растворы розового цвета, тогда как растворы исходных солей имели голубую окраску. Максимум полосы поглощения находился при 520 нм. Аналогичное изменение цвета наблюдается при растворении системы ЭПВП--аланин-CuCl2, в сухом виде этот комплекс имеет светло-зеленую окраску, а в растворе бледно-зелено-голубую. В спектре раствора ЭПВП--аланин-CuCl2 наблюдается широкая полоса поглощения в области 520-850 нм, с несколькими максимумами. Изменение окраски при растворении свидетельствует об образовании аква-комплексов.
Исследование ИК-спектров полимерных металлокомплексов на основе ЭПВП с аминокислотными группировками и CoCl2 и GeCl2 показало, что взаимодействие кобальта (II) и германия (II) с модифицированными полимерами сопровождается характерными изменениями полос as(COO) и s(COO) для остатков аминокислот.
Так, при образовании металлокомплексов наблюдается исчезновение полос ассиметричных валентных колебаний карбоксильной группы (1560 см-1) и уширение полосы 1600 – 1650 см-1 за счет появления полос поглощения в области 1600-1605 см-1, которая относится к ассиметричным валентным колебаниям карбоксилатного иона. Также наблюдается появление полос в области 1340 см-1, соответствующих симметричным валентным колебаниям карбоксилатного иона. Это свидетельствует о замещении водорода карбоксильной группы на ионы металла с образованием связи Ме-О.
При исследовании ПМР-спектров полимерных металлокомплексов, содержащих аминокислотные остатки с GeCl2, было показано, что для производных модифицированного ЭПВП имеет место изменение в области от 3,4 м.д. до 3,9 м.д., Низкочастотная линия дифференцируется в низкочастотную область, что особенно характерно для комплекса соединения ЭПВП-глицин с GeCl2, а также изменение интенсивностей сигналов протонов и появление других сигналов в области от 1 м.д. до 1,4 м.д., что характеризует образование нового соединения.
Низкочастотные области ПМР-спектров для систем, образованных производными глицина и -аланина (ЭПВП-глицин-GeCl2 и ЭПВП--аланин-GeCl2) заметно отличаются от низкочастотных областей производных -аминомасляний и --аминокапроновая кислот (ЭПВП--аминомасляная кислота-GeCl2 и ЭПВП--аминокапроновая кислота-GeCl2). Это дало основание предположить различное строение металлокомплексов в этих системах.
Для определения методом ЭПР координационной сферы ионов меди в комплексах были изучены полимерные металлокомплексы на основе ЭПВП, модифицированного аминокислотными остатками, и их низкомолекулярные аналоги в замороженных водных растворах при 77К.
Спектры регистрировали на спектрометре “ER-200 DSRC-Bruker”. В качестве растворителя использовали смесь D2O:CD3OD=1:1. Концентрация иона металла в исследованных образцах составляла 110-2 моль/л. Значения параллельной и перпендикулярной составляющих спина (g) и (g), константы сверхтонкого взаимодействия неспаренного электрона с ядрами меди (А) и азота (аN) рассчитывали согласно известным методам.
С целью выяснения состава и структуры полимерных комплексов были изучены их спектры ЭПР при постоянной концентрации ионов меди (II) и различных концентрациях и степени нейтрализации лигандов. Идентификацию образующихся комплексов проводили путем предварительного исследования комплексообразования соответствующих низкомолекулярных аминокислот с медью (II).
Было выяснено, что характер зависимости состава комплексов от соотношения компонентов системы для низкомолекулярных металлокомплексов отличаются от таких зависимостей для полимерных металлокомплексов.
Так, при десятикратном избытке металла в отличие от медных комплексов глицина типа CuL+ и CuL2 в случае полимерного производного были обнаружены только комплексы состава CuL2.
Такая склонность макромолекулярных лигандов к образованию полимерных комплексов состава CuL2 наблюдается и в случае полимерных производных других исследуемых аминокислот. По-видимому, это является результатом возможности в случае гибкой полимерной цепи контакта двух аминокислотных групп, образующих комплекс.
В то же время сохранение растворимости систем при образовании металлокомплексов указывает на наличие внутримолекулярного хелатирования, а не на образование межцепных хелатных группировок.
Определение условий существования медных комплексов показывает, что если для полимерных производных глицина и -аланина комплексы состава CuL2 образуются при эквивалентных соотношениях реагирующих компонентов (=1, степень нейтрализации лиганда =1), то для -аминомасляной кислоты уже необходим избыток металла (=10) при степени нейтрализации лиганда (=0,1).
В случае полимерного производного -аминокапроновой кислоты при увеличении соотношения металл / лиганд (>10) вязкость растворов сильно возрастала. препятствует проведению исследований.
Возможно, в этом случае, когда карбоксильная группа значительно удалена от основной цепи полимера, имеет место межмолекулярное образование металлокомплекса, а комплекс состава CuL2 образуется только при значительном избытке ионов металла (>100).
В первую очередь это связано с переходом от типа комплекса, образующегося в случае глицина и -аланина за счет участия в комплексообразовании и аминной, и карбоксильной групп, к системам, образующимся в случае -аминомасляной и -аминокапроновой кислот только за счет взаимодействия металла и удаленной карбоксильной группы.
И действительно, в спектрах медных комплексов глицина и -аланина и их полимерных производных в области (g) разрешена дополнительная сверхтонкая структура (СТС). Это свидетельствует об образовании координационной связи между ионом металла и атомом азота аминокислоты.
Для комплексов состава CuL+ дополнительная СТС состоит из трех линий разной интенсивности, что указывает на взаимодействие неспаренного электрона с одним ядром азота (g = 2,066, аN= 22,0).
В комплексах типа CuL2 дополнительная СТС разрешена в виде пяти линий, что служит доказательством участия в координации двух ядер атомов азота (g = 2,070, аN= 14,1). Т.е. в комплексах с полимерами, содержащими остатки глицина и -аланина ионы металла связываются с участием и карбоксильных и аминных групп, образуя, соответственно, пяти и шестичленные хелатные циклы.
С другой стороны, на ЭПР-спектрах комплексов полимерных производных -аминомасляной и -аминокапроновой кислот и их низкомолекулярных аналогов в области g дополнительная СТС не разрешена. Это указывает на отсутствие в этих случаях координации иона Cu2+ с атомом азота аминокислоты и указывает на образование только карбоксилатных комплексов.
Это отличие, очевидно, связано с различием в строении комплексов, которые в случае аминокислот с короткой углеродной цепью образуются за счет взаимодействия иона меди с кислородом и азотом с образованием пространственно выгодных пяти- и шестичленных хелатных комплексов, а в случае аминокислот с более длинным углеводородным фрагментом, когда семи- и девятичленные хелатные комплексы стерически не выгодны – за счет взаимодействия только с карбоксильной группой.
Можно было предположить, что в случаях с ЭПВП-глицин-GeCl2 и ЭПВП--аланин-GeCl2 образуются хелатные структуры с участием атомов кислорода и азота аминокислотного остатка и формируется координационная сфера вокруг центрального иона (Ge2+), а в полимерных металлокомплексах с -аминомасляной и -аминокапроновой кислотами происходит образование карбоксилатных комплексов, которые объясняются более длинными углеводородными радикалами - (СН2)3,5.
На основании проведенных исследований можно сделать вывод, что во всех комплексах ионы металлов связаны с атомом кислорода карбоксилатной группы аминокислотного остатка. При этом в отличие от полимеров с -аминомасляной и -аминокапроновой кислотами в комплексах полимеров, содержащих глициновые и -аланиновые остатки, ионы металлов координированы и с двумя атомами азота аминокислотного остатка.
Расчет констант устойчивости в системе металл-лиганд проводили на основании результатов потенциометрического титрования раствора макромолекулярного лиганда в присутствии соли кобальта (мольное соотношение полимер:металл составляет 1:10) 0,1 н. раствором едкого натра, освобожденным от карбонатов при 298К (ионная сила J=0,1).
В таблице 4 приведены данные по константам устойчивости К и константам равновесного обмена В комплексов с участием макромолекулярных лигандов с аминокислотными остатками и их низкомолекулярных аналогов.
Как видно, устойчивость комплексов зависит от природы аминокислотного остатка в модифицированном полимере и устойчивость комплексов уменьшается в ряду от полимера с глицином до полимера с -аминокапроновой кислотой.
Таким образом, проведенные исследования устойчивости модифицированных полимеров с аминокислотными остатками показали заметные отличия их от низкомолекулярных производных. Полимеры, вследствие концентрационного эффекта образуют с ионами металлов более устойчивые комплексы, чем низкомолекулярные N-производные аминокислот.
Таблица 4
Комплексообразующие свойства аминокислот, их пептидов и полимерных аминокислотных производных
| Соединение | Со2+ | |
| lgK | lgB | |
| Глицин* | 8,99 | - |
| Глицилглицин* | 5,88 | - |
| Глицилглицилглицин* | 5,44 | - |
| -Аланин* | 6,14 | - |
| ЭПВП-глицин | 7,1 | -7,5 |
| ЭПВП--аланин | 5,2 | -7,2 |
| ЭПВП--аминомасляная кислота | 2,3 | -3,2 |
| ЭПВП--аминокапроновая кислота | 1,5 | -2,1 |
* Литературные данные
Для исследования свойств полимерных металлокомплексов был использован вискозиметрический метод, с помощью которого исследовали растворы ЭПВП, содержащего аминокислотные остатки, в смеси растворителей метанол:ацетон (массовое соотношение 3:1) в присутствии ионов металла Co (II).
Анализ зависимостей уд./С от мольного отношения [Co (II)]/[полимер] при постоянной концентрации полимера (0,05 моль/л) показал, что повышение количества добавленного иона металла уменьшает вязкость раствора. Это, по-видимому, означает, что вследствие внутрицепного хелатирования имеет место уплотнение макромолекулярного клубка.
Характеристики полимерных металлокомплексов, использовавшихся при биологических исследованиях приведены в таблице 5.
Как видно, в этом случае степень превращения в реакции комплексообразования достигала 80-90%.
Таким образом, на основании проведенных исследований можно заключить, что полимеры с аминокислотными остатками образуют с переходными металлами с высоким выходом комплексы двух типов – хелатные с участием атомов азота и кислорода (более характерные для низших аминокислот) и карбоксилатные с участием атомов кислорода (для аминокислот с более длинным радикалом между аминной и карбоксильной группами).
Таблица 5
Содержание металла в полимерных металлокомплексах
| Полимерный металлокомплекс | Содержание Co2+ | Cодержание Ge2+ | ||||
| Масс.% | Моль. % | Степень превраще-ния, % | Масс.% | Моль. % | Степень превра-щения, % | |
| ЭПВП – глицин | 16,3 | 6,9 | 88,4 | 15,6 | 6,3 | 80,7 |
| ЭПВП - -аланин | 18,1 | 7,4 | 89,9 | 17,2 | 7,1 | 86,3 |
| ЭПВП - -аминомасляная кислота | 19,1 | 7,6 | 91,1 | 18,1 | 7,3 | 87,5 |
| ЭПВП - -аминокапроновая кислота | 20,6 | 7,7 | 90,4 | 19,2 | 7,4 | 86,8 |
3.5. Биологическая активность производных ПВП с аминокислотными боковыми группами и их металлокомплексов
Наличие в синтезированных полимерах фрагментов цепи ПВП и боковых аминокислотных группировок при оптимальных молекулярных массах позволило при высоком уровне биосовместимости обеспечить наличие у полимеров различных типов биологической активности, характерных для ионогенных макромолекулярных соединений, т.е систем с собственной биологической активностью. С другой стороны, связывание с полимерами комплексной связью биогенных металлов, позволило обеспечить их постепенное включение в биологические процессы, что характерно для систем с контролируемым выделением биологически активного агента.
При исследования биологической активности синтезированных в работе полимеров были рассмотрены образцы, содержащие аминокислотные остатки, полученные на основе эпоксидированного ПВП (ЭПВП) с Мn 9000 и содержанием эпоксидных групп 9,9 мол.%, и его амфифильного производного с Мn 2000 и содержанием эпоксидных групп 9,0 мол.%. В ряде экспериментов также были исследованы полимеры, синтезированные на основе сополимера N-винилпирролидона с аллилглицидиловым эфиром с Мn 12000 и содержанием эпоксидных групп 9,7 мол.%. Также были исследованы металлокомплексы на основе этих модифицированных аминокислотами полимеров.
3.5.1. Общая токсикологическая характеристика
Низкая острая токсичность синтезированных полимеров была подтверждена в опытах на культурах клеток и на опытных животных.
Так, с использованием ряда культур клеток было показано, что при введении в клеточную суспензию (концентрации 2106 клеток/мл) полимерных производных аминокислот глицина, -аланина, -аминомасляной кислоты, -аминокапроновой кислоты, полученных на основе ЭПВП в концентрациях до <2,0 мг/мл, токсического действя не наблюдалось.
Такой же низкий уровень токсичности в этих опытах наблюдался при введении в клеточные суспензии комплексов этих полимеров и СоCI2. Цитотоксическое действие полимеров определяли, исходя из минимальной концентрации препарата, которая оказывала цитодеструктивное действие (лизис клеток, нарушение их морфологии).
Низкая острая токсичность полимеров и их металлокомплексов была подтверждена также в опытах на животных (белые беспородные мыши) при внутривенном введении. В этом случае ЛД50 для производных всего ряда аминокислот была не ниже 4000 мг/кг. В случае комплексов Со2+ значения ЛД50 были несколько ниже, но во всех случаях выше 1000 мг/кг (1050-2500 мг/кг). Причем, при этом значения ЛД50 понижались со снижением константы устойчивости металлокомплекса.
Исследование скорости выведения кобальтовых металлокомплексов из организма путем почечной фильтрации исследовали на самцах крыс после однократного внутривенного. Как было установлено, при внутривенном введении через 6 часов с мочой выводилась большая часть введенных полимеров (до 95%).
То есть, синтезированные полимеры с аминокислотными остатками в этих исследованиях показали достаточно высокий уровень биологической безвредности.
3.5.1. Примеры биологической активности.
Как было установлено, полученные полимерные производные аминокислот и их металлокомплексы обладают различными типами биологической активности.
Некоторые примеры результатов этих исследований в виде кратких описаний приводятся ниже в автореферате. Подробное описание экспериментов и ряд других исследований приведено в тексте диссертации.
Иммунная активность аминокислотных производных ЭПВП была изучена для случая ангигенной стимуляции пролиферации (деления) лимфоцитов периферической крови (ЛПК) человека при использовании в качестве антигена столбнячного токсина. Наблюдаемое адъювантное (усиливающее) действие полимеров различного строения, выраженное в количестве клеток ЛПК в объеме культивирования, показано на рис.4.
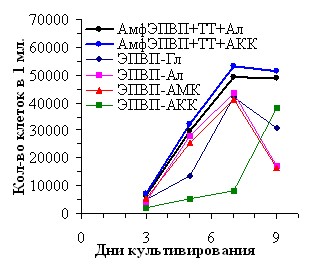

Рис.3. Антиген-специфическая активность производных ЭПВП с аминокислотными заместителями, оцененная по пролиферационному ответу ПЛК человека в присутствии антигена - столбнячного токсина (приведено число клеток на мл в зависимости от продолжительности культивирования).
Как видно, все рассмотренные полимеры обладают способностью усиливать образование иммунокомпетентных клеток. При этом активность производных сополимера N-винилпирролидона с аллилглицидиловым эфиром была значительно ниже, чем активность аминокислотных производных ЭПВП (данные приведены в диссертации).
Обращает на себя внимание более высокая активность амфифильных производных, которая, возможно, объясняется их склонностью к образованию ассоциированных структур в водной среде, что способствует взаимодействию полимеров с иммунными клетками как за счет интенсификации процессов эндоцитоза, так и гидрофобного взаимодействия с клеточными мембранами иммунных клеток.
Противовирусная активность аминокислотных производных ЭПВП в отношении вируса энцефаломиокардита (штамм «Колумбия SK-Col-SK») была исследована на клетках человека (J-41, J-96, гипер-нефрома, HeLa). Было установлено, что Все полимеры с аминокислотными остатками оказывают более высокую противовирусную активность по сравнению с препаратом Ридостин.
Противовирусная активность в отношении вируса гриппа (штамм A/Aichi/68 H3N2) была исследована на мышах линии СВА с применением системы ЭПВП-–аминокапро-новая кислота. Препарат вводили внутрибрюшинно в дозе 10 мг/кг за 24 часа до заражения мышей и через 24 часа после заражения. Выживаемость при введении препарата – 45-50% по сравнению с полной летальностью в отсутствии препарата.
Антихламидийное действие системы (ЭПВП + -аланин) + GeCI2 исследовали на мышах линии СВА. Инъекция 10 мг/кг внутри-брюшинно через 24 часа после инфицирования C.trachomatis привела к стимуляции образование в крови, легких и лимфатических узлах эндогенных интерферонов (- и -интерфероны), являющихся одним из основных факторов подавления размножения хламидий. Препарат, в отношении подавления хламидиоза превосходил тетрациклин гидрохлорид в 2-2,2 раза.
Усиление антихламидийного действия антибиотика (тетрациклин гидрохлорид) исследовали при с использованием системы (ЭПВП + -аланин) + CuCI2, вводимой внутрибрюшинно через 24 часа после инфицирования C.trachomatis. По результатам цитоскопии индекс эффективности в лимфатических узлах и легких был, соответственно, в 3,2 и 2,5 раза выше, чем при лечении только антибиотиком.
Повышение чуствительности клеток к интерферону исследовали на культуре мышиных клеток L929 с использованием системы (ЭПВП + глицин) + PtCI2. Было показано, что введение препарата в среду с клетками (доза 250 мкг/1105 клеток/мл Повышало чувствительность клеток к интерферону в 32 раза
Повышение радиозащитного действия препарата препарата Рефнолин (фактор некроза опухолей). Исследования проводили на мышах линии (СВАхС57В16) Fj при дозе 25 мкг/мышь при облучении в дозе 6,0 Гр. В контрольной группе наблюдалась гибель всех животных. В опытной группе количество выживших животных составило: при использовании только Рефнолина – 60%, при использовании препарата 75%, при совместном использовании препарата и Рефнолина – 90%.
Стимулирование процесса кроветворения исследовали на белых беспородных крысах и мышах с использованием кобальтовых комплексов полимеров с аминокислотными остатками. Наблюдалось восстановление количества эритроцитов и гемоглобина, а также по выживаемости животных на фоне экспериментальной анемии, вызванной путем трехкратного подкожного введения солянокислого фенилгидразина.
____________
Таким образом, показано, что синтезированные полимеры с аминокислотными остатками характеризуются, как и ПВП, хорошими токсикологическими характеристиками. При этом введение ионов металлов в состав полимеров незначительно повышает их токсичность и придает им новые биологические свойства.
4. ВЫВОДЫ
- Впервые синтезированы аминокислотные производные эпоксидсодержащего поли-N-винилпирролидона и их комплексы с переходными металлами, изучены их свойства и показано, что они характеризуются низкой токсичностью и проявляют биологическую активность различного типа.
- Выявлен новый путь протекания реакции Дарзана с участием карбонила циклических амидов и хлорацетамида, и с использованием этой реакции синтезирован эпоксидсодержащий полимер N-винилпирролидона. Исследованием влияния на протекание реакции различных факторов найдены оптимальные условия ее проведения, позволяющие получать модифицированный поли-N-винилпирролидон с содержанием эпоксидных групп до 25 мол.%.
- Взаимодействием эпоксидсодержащего поли-N-винилпирролидона с рядом низших,-аминоксилот получены их N-замещенные полимерные производные. С использованием модельной реакции с участием низкомолекулярных соединений установлено, что реакция аминокислот с дизамещенным эпоксидом 4-метил-1-окса-4-азаспиро[2,4]гептан-2-карбоксамидом протекает с присоединением остатка аминокислоты к атому углерода, входящему в пирановый цикл.
- Показано, что аминокислотные производные эпоксидсодержащего поли-N-винилпирролидона образуют комплексы с переходными металлами, в которых металл связан с фрагментом аминокислоты или с участием атомов кислорода и азота или в виде карбоксилатного комплекса в завивисимости от длины углеводородного радикала аминокислоты.
- Показано, что аминокислотные производные эпоксидсодержащего поли-N-винилпирролидон в большей мере склонен к образованию ассоциатов в водном растворе, чем аминокислотные производные сополимера N-винилпирролидона и аллилглицидилового эфира.
- Впервые синтезированы эпоксидное и аминокислотные производные амфифильного полимера N-винилпирролидона. Показано, что эти полимеры склонны к образованию наноразмерных агрегатов в водном растворе.
- В опытах на животных in vivo и клетках in vitro установлено, что синтезированные полимерные производные аминокислот и их металлокомплексы при низкой острой токсичности проявляют различные типы активности – иммуностимулирующую, иммуноадъювантную, интерферонстимулирующую, антивирусную, антимикробную; способствуют антиген-специфичной стимуляции лимфоцитов, стимулируют процесс гемопоэза. В ряде исследований биологической активности синтезированных полимеров установлено, что она повышается с увеличением способности полимеров к агрегации в водном растворе.
Научные труды по теме диссертации
- Ташмухамедов Р.И., Ли В.А., Брудзь С.П., Штильман М.И., Рашидова С.Ш. Сополимеры ВП с аминокислотными остатками. // Высокомолекул.соедин., 1989, В31, №5, 353-355.
- Ташмухамедов Р.И., Ли В.А., Мусин Р.И., Рашидова С.Ш., Туляганов Р.Т., Штильман М.И. Синтез и свойства комплексов металлов переходного ряда и полимеров с аминокислотными остатками.// Хим.-фарм.журнал.-1989.-N 12.-С.1447-1450.
- Ташмухамедов Р.И., Ли В.А., Турганов М.М., Рашидова С.Ш. ЭПР исследование медных комплексов сополимеров винилпирролидона с аминокислотными остатками.// Высокомолекул.соедин., 1990, А32, №5, 1027-1031.
- Lee V.A., Musin R.I., Tashmukhamedov R.I., Shtilman M.I., Rashidova S.Sh. Metal complexes of polymers with amino acid residues. Formation, stability and controlled biological activity.// J.Controled Release. – 1990.-V.14.-P.61-70.
- Ли В.А., Разиков Р.К. Ташмухамедов Р.И., Батырбеков А.А., Муратходжаев Ф.Н. Иммунологические свойства металлокомплексов сополимеров винилпирролидона с аминокислотными остатками в боковой цепи. // Иммунология, 1997, N1, с.35-37.
- Штильман М.И., Хвостова В.Ю., Ташмухамедов Р.И., Головкова Т.А., Tsatsakis А.М., Эпоксидсодержащий поли-N-винилпирролидон. // Пластмассы.- 2001. – N.7. – С.5-9.
- Baritaki S., Baritaki S., Tzanakakis GN, Alifragis J., Zafiropoulos A., Tashmukhamedov, RI, Tsatsakis, A., Shtilman, MI, Rizos, AK, Krambovitis, E. Light scattering and in vitro biocompatibility studies of poly (vinyl pyrrolidone) derivatives with amino-acid-dependant groups. // J. Biomed. Mater. Res., 2002, V.63, N.3, P.830-837.
- Ташмухамедов Р.И., Штильман М.И., Хвостова В.Ю., Клягина М.В., Tsatsakis A.M., Шашкова И.М. Поли-N-винилпирролидон с боковыми аминокислотными группами. // Высокомолекул.соедин., 2005, Серия А, т.47, №6, С.1-4. (Tashmuhamedov R.I., Shtilman M.I., Khvostova V.Yu., Klyagina M.V., Tsaysakis A.M., Shashkova I.M. Poly(N-vinylpyrrolidone) with amino acid side groups. // Polymer Science, Ser.B, 2005, Vol.47, N.5-6, PP.167-169.
- Ташмухамедов Р.И., Клягина М.В., Хвостова В.Ю., Штильман М.И. Реакция дизамещенных эпоксидов с аминокислотами. // ИзвВУЗов. Химия и хим.технол., 2006, Т.49, № 1, С.93-95.
- Ташмухамедов Р.И., Штильман М.И., Хвостова В.Ю., Клягина М.В. Присоединение аминокислот к дизамещенным эпоксидам. // ИзвВУЗов. Хими и хим.техн., 2006, Т.49, № 1, С.93-95.
- Ташмухамедов Р.И., Крамбовитис Е., Тсатсакис А.М., Батырбеков А.А. Иммунореактивные свойства производных поли-N-винилпирролидона с аминокислотными группами и их металлокомплексов. // Журнал теоретической и клинической медицины, 2007, №1, С.10-19.
- Kuskov A.N., Shtilman M.I., Goryachaya A.V., Tashmuhamedov R.I., Yaroslavov A.A., Torchilin V.P., Tsatsakis A.M., Rizos A.K. Polymeric Nanoscaled Drug Carriers Composed of Amphiphilic Poly-N-vinylpyrrolidones. // Journal of Non-Crystalline Solids, 2007, (accepted).
- Штильман М.И., Рашидова С.Ш., Ташмухамедов Р.И., Ли В.А. и др. Сополимеризация аллилглицидилового эфира с N-винилпирролидоном. // Хим.технол., свойства и примен.пластмасс./ Ред. А.Ф.Николаев.- Л: ЛТИ им.Ленсовета.- 1986.- С.111-120; Chem.Abstr.- 1987.- V.107.- 78350m.
- Штильман М.И., Брудзь С.П., Рашидова С.Ш., Ташмухамедов Р.И. Радикальная полимеризация и сополимеризация моноаллильных соединений. МХТИ, М.1985. 73с.
- Рашидова С.Ш., Ташмухамедов Р.И. Сополимеризация N-винилпирролидона и N-винилкапролактама с аллилглицидиловым эфиром.// Сборник. Синтез, свойства и применение полимеров на основе N-виниллактамов, 1990, 50-63.
- Клагина М.В., Майборода С.Б., Ташмухамедов Р.И., Штильман М.И. Металлокомплексы полимеров с аминокислотными остатками. // Успехи в химии и химической технологии.- М.: Минобразования России.- 2002.- Т.16.- N.3(20).- С.56.
- Клягина М.В., Ловягин Ден.А., Ловягиен Дм.А., Ташмухамедов Р.И., Штильман М.И. Водорастворимые металлокомплексы на основе производных поливинилпирролидона. // Успехи в химии и химической технологии.- М.: Минобразования России.- 2003.- Т.17.- N.5 - С.68-71.
- Ташмухамедов Р.И., Клягина М.В., Хвостова В.Ю., Штильман М.И. Взаимодействие глицина с 4-метил-1-окса-4-азаспиро[2,4]гептанкарбоксамидом. // Вестник РУДН: Серия – Экология и природоведение, 2005, С.75-78.
- Ташмухамедов Р.И., Клягина М.В., Хвостова В.Ю., Штильман М.И. Комплексы переходных металлов на основе аминокислотных производных эпоксидсодержащего поли-N-винилпирролидона. // Вестник РУДН: Серия – Экология и природоведение, 2005, С.79-85.
- Ташмухамедов Р.И., Клягина М.В., Хвостова В.Ю., Штильман М.И. Эпоксидсодержащий поли-N-винилпирролидон, модифицированный аминокислотами. // Вестнике РУДН: Серия – Экология и природоведение, 2005, С.86-88.
- Shtilman M.I., Voskanyan P.S., Tashmuhamedov R.I. Polymers in bioactive systems. // New Polymer Systems for Biotechnological and Biomedical Application [8th International Seminar ISTC. [Erevan, Armenia]. 2005, P.159-164.
- Kuskov A.N., Tashmukhamedov R.I., Shtilman M.I. Amphiphilic polymers as the drugs carriers. // New Polymer Systems for Biotechnological and Biomedical Application [8th International Seminar ISTC. [Erevan, Armenia]. 2005, P.91.
- Kuskov A.N., Tashmukhamedov R.I., Vilemson A.L., Shtilman M.I., Larionova N.I., Tsatsakis A.M. Polymeric nano-sized carriers for creation of new systems for drug delivery. // New Polymer Systems for Biotechnological and Biomedical Application [8th International Seminar ISTC. [Erevan, Armenia]. 2005, P.92-103.
- Tashmuhamedov R.I., Klyagina M.V., Shtilman M.I. Metal complexes on the base of new polymer carriers. // New Polymer Systems for Biotechnological and Biomedical Application [8th International Seminar ISTC. [Erevan, Armenia]. 2005, P.176.
- Shtilman M.I., Voskanyan P.S., Tashmuhamedov R.I. Polymers in bioactive systems. // New Polymer Systems for Biotechnological and Biomedical Application [8th International Seminar ISTC. [Erevan, Armenia]. P.30-35.
- Кусков А.Н., Виллемсон А.Л., Ташмухамедов Р.И., Штильман М.И. Амфифильные производные поли-N-винилпирролидона и их взаимодействие с компонентами крови. // Успехи в химии и химической технологии.- М.: Минобразования России.- 2005.- Т.19.- N.6(54)- С.71-72.
- Ташмухамедов Р.И., Разиков Р., Ли В.А., Рашидова С.Ш. Устойчивость комплексов кобальта (II) и меди (II) с сополимером N-винилпирролидона в растворе.// Тезисы доклада III съезда фармацевтов Узбекистана, г.Ташкент, 1987, 164с.
- Ташмухамедов Р.И., Разиков Р.К., Ли В.А., Новые водорастворимые полимеры с аминокислотными остатками.//Тез.докл.III Всес.конф. «Водораствориые полимеры и их применение», г.Иркутск.- 1987.-С.55.
- Lee V.A., Tashmukhamedov R.I., Turganov M.M., Rashidova S.Sh. An ESR-study of copper (II) complexes of vinylpyrrolidone with aminoacids residues copolymers.//Abstracts of XXIY-th AMPERE Congress on magnetic resonance and related phenomena. Poznan, Poland.-1988.
- Lee V.A., Musin R.I., Razikov R.K., Tashmukhamedov R.I. Polymer metal complexes as biometal delivery systems.// Abstracts of 33-rd IUPAC International Symposium on Macromolecules. Montreal, Canada.- 1990.-Session 3.4.4.
- Ли В.А., Разиков Р.К., Ташмухамедов Р.И., Батырбеков А.А. Полимерметаллокомплексы: Структура, устойчивость и иммунологические свойства.// Тез.докл. 1 Респ.научн.конф.по химии ВМС «Узбекистон МАКРО-92», Ташкент.-1992-С.162.
- Штильман М.И., Tsatsakis A.M., Ташмухамедов Р.И., Хвостова В.Ю., Цветкова Л.С., Чеботарь М.И., Hatzidakis G., Шашкова И.М. Полимеры N-винилпирролидона, содержащие гидролизуемые группы. // Всеросс.конфер.«Конденсационные полимеры: Синтез, структура, свойства» [Янв.12-14, Москва.].- М.1999- ИНЭОС.- С. С1-31.
- Sztilman M.I., Tsatsakis A.M., Szaszkova I.M., Woskanian P.S., Brudz S.P., Taszmuchamedow R.I. Biologicznie aktywne polimery: problemy I perspektywy.// Modyfikacja polimerow. XIV konferencja naukowa [Kudowa Zdroj, 26-30 Sept.,1999].- Wroclaw.- 1999. – P.120.
- Shtilmanm M.I., Tashmuhamedov R.I., Tsatsakis A.M., Hvostova V.Yu., Hadzidakis G., Assithinakis P., Rashidova S.Sh., Shashkova I.M. // 27th Intern.Symp.on Contr.Release of Bioact. Materials (Paris, 2000).- CRS.- 2000.- P.7009.
- Еrshov F.I., Shtilman M.I., Narovlyansky A.N., Mezentseva M.V., Tashmuhamedov R.I., Hvostova V.Yu., Tsatsakis A.M. Polymeric formulation with antiviral activity.// Intern.confer. “Biologically active polymers” (Prague, 2000).- P. 35.
- Shtilman M.I., Tashmuhamedov R.I., Hvostova V.Yu., Tsatsakis A.M., Hadzirakis J., Rashidova S.Sh., Golovkova T.A., Shashkova I.M. Metal complexes of amino acid derivatives of epoxide-cjntaining poly-N-vinylpyrrolidone.// Intern.confer. “Biologically active polymers” (Prague, 2000).- P. 36.
- Maiboroda S.B., Loseva S.V., Klyagina M.B., Tashmuhamedov R., Kosharnaya O.P., Shtilman M.I. Биодеструктируемые полимеры N-винилпирролидона. // Modifikacja polimerow. XV Konferencja naukowa [Wroclaw, 2001].- N50.
- Klyagina M.V., Tashmuhamedov R.I., Tsatsakis A.M., Hvostova V.Yu., Maiboroda V.B., Shtilman M.I. Metal immobilization on the polymer carriers containing complex-forming groups. // Biomed 2002 (IXth International Symposium on Biomedical Science and Technology [19-22 Sept. 2002, Kemer-Antalya, Turkey], 2002, P-49.
- Штильман М.И., Кусков А.Н., Ташмухамедов Р.И., Torchilin V.P., Tsatsakis A.M. Амфифильные производные поливинилпирролидона – новые материалы для лекарственных систем. // XVII Менделеевский съезд по общей и прикладной химии. Тезисы докладов [Казань, 21-26 сентября 2003].- 2003, С.467.
- Klyagina M.V., Tashmuhamedov R.I., Shtilman M.I., Lovyagin Den.A., Lovyagin Dm.A. Water-soluble metal complexes based on derivatives of poly-N-vinylpyrrolidone. // European Material Research Society. Fall Meeting [Warshaw, 15-19 September, 2003].- 2003, P.169.
- Klyagina M.V., Tashmuhamedov R.I., Shtilman M.I., Mezenceva M.V., Semernina V.V., Narovlyansky A.N. Polymeric water-soluble metal complexes with biological activity. // Biotechnology: State of art and prospects of development [3rd Moscow International congress], 2005, P.48.
- Shtilman M.I., Kuskov A.N., Tashmuhamedov R.I. Microaggregates of N-vinylpyrrolidone amphiphilic polymers. // XVII Int.Conf “Modification of Polymers [Kudowa Zdroj, Poland, 12-15 Sept.2005], P.15.
- Tashmuhamedov R.I., Klyagina M.V., Hvostova V.Yu., Shtilman M.I. Epoxycontaining poly-N-vinylpyrrolidone modified of aminoacids. // XVII Int.Conf “Modification of Polymers [Kudowa Zdroj, Poland, 12-15 Sept.2005], P.26.
- Tashmuhamedov R.I., Klyagina M.V., Hvostova V.Yu., Shtilman M.I. Complecex 0f metals on the base of aminoacid derivatives of poly-N-vinylpyrrolidone. // XVII Int.Conf “Modification of Polymers [Kudowa Zdroj, Poland, 12-15 Sept.2005], P.27.
- Штильман М.И., Кусков А.Н., Ташмухамедов Р.И., Тсатсакис А.М. Амфифильные полимеры - основа новых наноразмерных носителей лекарственных веществ. // Тезисы докл. Международной конференции «Биотехнология и медицина» [Москва,2006], С.37.
- Штильман М.И., Ташмухамедов Р.И., Кусков А.Н., Горячая А.В. Амфифильные полимеры – новые материалы для медицины. // Actual problems of polymer chemistry and physics [Tashkent, 17-18 Oct.2006], C.23-27.
- Shtilman M.I., Kuskov A.N., Tsatsakis A.M., Tashmuhamedov R.I. Self-assembly hydrophobically end-capped poly-N-vinylpyrrolidones in aqueous solutions. // 33rd Annual Meeting of Controlled Release Society [Vienna, Austria, July,21-27, 2006].P.723.
- Горячая А.В., Штильман М.И., Кусков А.Н., Ван Дуань, Ташмухамедов Р.И. Полимерные мицеллы – новое поколение носителей лекарственных веществ. // Биотехнология: Состояние и перспективы развития [Москва, март 2007], 2007, С.59. (Goryachaya A.V., Shtilman M.I., Kuskov A.N., Wang Duan, Tashmuhamedov R.I. Polymeric micells – new generation of drug carriers. // Biotechnology: State of the art and prospects of development [Moscow, March 2007]. 2007, P.59.
- Штильман М.И., Ташмухамедов Р.И., Кусков А.Н., Артюхов А.А., Брудзь С.П. Полимеры для создания биологически активных и лекарственных систем. // Биотехнология: Состояние и перспективы развития [Москва, март 2007], 2007, С.111. (Shtilman M/I/, Tashmuhamedov R.I., Kuskov A.N., Artyukhov A.A, Brudz S.P. Polymers for creation of biologically active and drug systems. // Biotechnology: State of the art and prospects of development [Moscow, March 2007]. 2007, P.58.
- Ершов Ф.И., Наровлянский А.Н., Ташмухамедов Р.И. и.др. Полимерные металлокомплексы с терапевтической активностью. // Решение о выдаче патента РФ по заявке № 2002128394 (2003).

