Синтез и реакции мезо -фенилзамещенных порфиринов
На правах рукописи
СЫРБУ Сергей Александрович
СИНТЕЗ И РЕАКЦИИ
МЕЗО-ФЕНИЛЗАМЕЩЕННЫХ ПОРФИРИНОВ
02.00.03 – Органическая химия
Автореферат
диссертации на соискание ученой степени
доктора химических наук
Иваново 2008
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Ивановский государственный химико-технологический университет»
Научный консультант: доктор химических наук, профессор Семейкин Александр
Станиславович
Официальные оппоненты:
член-корреспондент РАН Кукушкин Вадим Юрьевич,
доктор химических наук Пономарев Гелий Васильевич,
доктор химических наук, профессор Ломова Татьяна Николаевна.
Ведущая организация:
Московский государственный университет им. М.В. Ломоносова
Защита диссертации состоится 20 октября 2008 г. в 10.00 часов на заседании совета по защите докторских и кандидатских диссертаций Д 212.063.01 в ГОУ ВПО «Ивановский государственный химико-технологический университет» по адресу: 153000, г.Иваново,
пр-т. Ф.Энгельса, 7.
С диссертацией можно ознакомиться в Информационном центре в ГОУ ВПО «Ивановский государственный химико-технологический университет» по адресу: 153000, г.Иваново,
пр-т. Ф.Энгельса, 10.
Автореферат разослан «___»________ 2008 г.
| Ученый секретарь совета по защите докторских и кандидатских диссертаций | Хелевина О.Г. |
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Тетрапиррольные макрогетероциклы, к числу которых относятся порфирины и металлопорфирины, широко распространены в природе и имеют большое биологическое значение. Важнейшими их представителями являются хлорофиллы и бактериохлорофилы, осуществляющие растительный и бактериальный фотосинтез и гем крови, который в ансамбле с белком глобином осуществляет обратимое связывание и транспортировку молекулярного кислорода во все органы и ткани живых существ и перенос углекислого газа от периферических тканей к дыхательным органам для последующего выведения из организма. Металлопорфирины входят также в состав многих биокатализаторов (ферментов) на основе хромопротеинов – каталаз, пероксидаз, цитохрома-Р450 и других.
В настоящее время известны более 30 областей практического использования порфиринов. Порфирины, металлпорфирины и их аналоги применяются в качестве сверхпрочных красителей и пигментов, эффективных катализаторов и биокатализаторов различных процессов, лекарственных препаратов особенно для фотодинамической и нейтроно-захватной терапии рака, а также в качестве модельных соединений при исследовании ряда биологических процессов. Успешное развитие перечисленных направлений зависит от наличия надежных высокоэффективных методов синтеза и модификации порфиринов, обладающих самыми разнообразными физико-химическими свойствами, устойчивых к действию агрессивных сред и реагентов, хорошо растворимых в растворителях различной природы, в том числе водных растворах.
Широкое применение природных порфиринов и их аналогов в технике, технологии и медицине сдерживается сложностью их выделения из природного сырья. Выход порфиринов при этом, как правило, довольно низкий (<5%). Синтез наиболее близких к природным -алкилзамещенных порфиринов (особенно несимметрично-замещенных порфиринов) также достаточно сложен и включает большое число стадий. Кроме того в -алкилпорфиринах отсутствуют заместители, которые в дальнейшем можно модифицировать или использовать для «привязки активных групп» или иммобилизации на различные носители. В связи с этим особый интерес и актуальность приобретают вопросы химии синтетических порфиринов, содержащих в мезо-положениях фенильные заместители, для которых разработаны достаточно эффективные методы синтеза и заместители в фенильных кольцах, которые можно подвергать разнообразным химическим превращениям, таким образом, изменяя свойства этих соединений.
Цель работы. Разработка новых целенаправленных подходов к высокоэффективному синтезу замещенных по фенильным кольцам мезо-фенилпорфиринов различной структуры, химическая модификация реакционноспособных заместителей и изучение физико-химических свойств полученных соединений.
Научная новизна. На основе анализа и обобщения литературных данных и механизмов реакций конденсации пиррола и полиметиленпирролов с альдегидами разработаны удобные и высокоэффективные методы синтеза мезо-фенилзамещенных порфиринов, имеющих в фенильных кольцах заместители, способные к дальнейшей химической модификации, позволяющей получать из небольшого набора порфиринов соединения с самыми разнообразными физико-химическими свойствами. С помощью разработанных методов получены различные порфирины, в том числе с несимметричной структурой (тетрафенилпорфины с асимметричной системой заместителей в фенильных кольцах, монофенил-, 5,10-дифенил-, 5,10,15-трифениоктаалкиллпорфирины), а также пространственно искаженные порфирины. На способ получения монооксифенилтрифенилпорфинов получено АС СССР, на способ получения безметального фталоцианина получен патент РФ.
На примере реакции нитрования впервые изучена реакционная способность различных положений свободных оснований мезо-фенилпорфиринов в реакциях электрофильного замещения.
Изучены реакции модификации заместителей в фенильных кольцах мезо-фенилзамещенных порфиринов, позволяющие получать из небольшого набора порфиринов соединения с самыми разнообразными физико-химическими свойствами. На способ получения оксифенилзамещенных порфиринов получено АС СССР, на способы получения тетра(3-амино-5-трет-бутил)фталоцианина меди получен патент РФ. Получены 8 патентов РФ на новые соединения.
Практическая значимость. Разработаны удобные и высокоэффективные методы синтеза мезо-фенилзамещенных порфиринов содержащих в фенильных кольцах активные группы, дальнейшая модификация которых, позволяет получать соединения с заранее заданными свойствами. С помощью этих методов получены порфирины различных структур, включая порфирины с несимметричной системой замещения, а также пространственно искаженные порфирины.
Разработаны высокоэффективные методы модификации заместителей в фенильных кольцах мезо-фенилпорфиринов реакций электофильного и нуклеофильного замещения: гидролиза, алкилирования, ацилирования, этерификации, аминирования, диазотирования, замены диазогруппы, азосочетания, восстановления. Комбинацией разработанных методов синтезирован большой набор порфиринов (в том числе с активными группами) с разнообразными физико-химическими свойствами. Изучена возможность иммобилизации мезо-фенилзамещенных порфиринов с активными группами в фенильных кольцах на полимеры-носители различной природы. Получено 8 патентов РФ на новые соединения, которые могут использоваться в качестве красящих веществ для оптических фильтров.
Апробация работы. Различные разделы работы докладывались и обсуждались на IV Всесоюзной конференции по химии макроциклов (Одесса, 1984), IV Всесоюзной конференции по химии и применению порфиринов (Ереван, 1984), Всесоюзной конференции по химии и технологии органических красителей и промежуточных продуктов (Ленинград, 1985), VI Международной конференции по органическому синтезу (Москва, 1986), I Всесоюзной конференции по химии и применению неводных растворов (Иваново, 1986), V Всесоюзной конференции по координационной и физической химии порфиринов (Иваново, 1988), III Всесоюзной конференции по химии и биохимии макроциклических соединений. (Иваново,1988), Международных конференциях “Проблемы сольватации и комплексообразования в растворах” (Иваново,1989, Плес, 2004, Суздаль, 2007), Международных Чугаевских конференциях по координационной химии (Минск, 1990, Иваново, 1999, Кишинев, 2005, Одесса, 2007), Всесоюзных семинарах по химии порфиринов и их аналогов (Самарканд, 1991), I-й Международной конференции по бикоординационной химии (Иваново, 1994), Международных конференциях по химии порфиринов и их аналогов (С.-Пб, 1995; Суздаль, 2003), Международных конференциях “Актуальные проблемы химии и хим. технологии” (Иваново, 1997), III Междуна-родной конференции по лиотропным жидким кристаллам (Иваново, 1997), International Conference on Porphyrins and Phthalocyanines (Dijon, 2000; Rome, 2006; Moscow, 2008), I Международной конференции «Химия и биологическая активность гетероциклов и алкалоидов» (Москва, 2001), Международной конференции «Органическая химия от Бутлерова и Бейльштейна до современности» (С-Пб., 2006), Всероссийской научной конференции «Природные макроциклические соединения и их синтетические аналогии» (Сыктывкар, 2007), XVIII Менделеевском съезде по общей и прикладной химии (Москва, 2007).
Публикации. Основное содержание диссертации изложено в 106 научных публикациях, в том числе 39 статьях, 54 тезисах докладов совещаний и конференций, 2 авторских свидетельствах СССР и 11 патентах РФ.
Структура работы. Работа состоит из введения, трех глав, экспериментальной части, основных результатов и выводов и списка цитируемой литературы.
Вклад автора. Личный вклад автора состоит в постановке проблемы, формулировке целей и задач исследования, определении путей и методов их решения, проведении ключевых экспериментов по синтезу новых соединений, изучению их физико-химических свойств, в анализе, теоретическом обобщении и интерпретации полученных данных.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Глава 1. Синтез мезо-фенилзамещенных порфиринов. Глава посвящена синтезу мезо-фенилпорфиринов реакцией конденсации пирролов и его линейных производных (дипиррометанов и биладиенов-а,с) с бензальдегидами и состоит из трех разделов: синтез мезо-тетрафенилпорфинов, синтез 5,15-дифенилпорфиринов и синтез 5-фенилпорфиринов.
1.1. Синтез мезо-тетрафенилпорфинов (H2ТФП). Наиболее простые полностью симметричные порфирины, к которым относятся и тетрафенилпорфирины (1), обычно получают конденсацией 2,5-незамещенных пирролов с бензальдегидами (1-1).
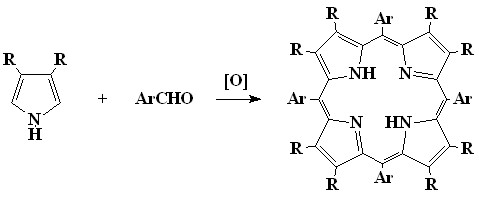 | (1-1) |
| 1 |
В диссертации обобщены литературные данные по трем основным методам проведения данной реакции – метод Ротмунда, метод Адлера и метод Линдсея, а также влиянию на выход тетрафенилпорфинов электронной природы и стерических факторов заместителей в бензальдегидах, используемых в реакции.
Реакция конденсация пирролов с бензальдегидами использовалась нами для синтеза как собственно тетрафенилпорфина и его замещенных по фенильным кольцам, так и более сложных порфириновых структур: тетрафенилпорфинов с асимметричной системой заместителей (А) и пространственно искаженных порфиринов (Б) – мезо-фенил--октаалкилпорфиринов, а также «сэндвичевых» димерных порфиринов и «перекрытых» порфиринов.
(А) Синтез тетрафенилпорфинов с ассиметричной системой заместителей в фенильных кольцах (2). Такие порфирины представляют интерес, так как симметричная система заместителей тетрафенилпорфинов (1) ограничивает возможности их практического использования для решения ряда задач. Одним из наиболее простых подходов к синтезу таких порфиринов, является, так называемая, смешанно-альдегидная конденсация (1-2), при которой в реакции пиррола со смесью двух альдегидов образуется смесь порфиринов, которую, в случае наличия в одном из альдегидов полярной группы можно разделить с помощью колоночной хроматографии.
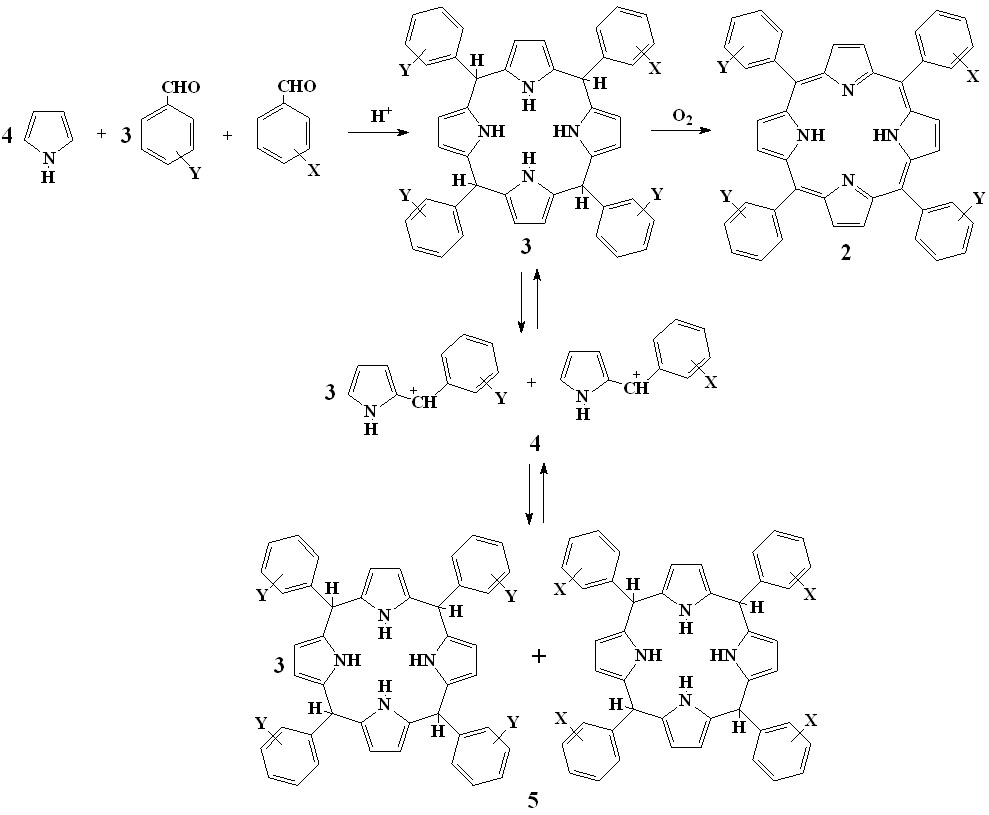 | (1-2) (1-3) (1-4) |
Выход тетрафенилпорфина с ассиметричной системой заместителей (2) максимален при соотношении реагирующих альдегидов 3:1 и обычно низок (<10%) в следствии различной активности альдегидов. Нами разработан метод, позволяющий получать асимметричные тетрафенилпорфирины с выходами, сопоставимыми с таковыми для симметричных тетрафенилпорфиринов (более 20%). Методика отрабатывалась на примере получения наиболее интересных монооксифенилтрифенилпорфинов (2, Х = OH, Y = H), так как эти соединения способны к дальнейшим многочисленным химическим превращениям. Такие порфирины образуются при конденсации пиррола со смесью бензальдегида и оксибензальда в соотношении 3:1, однако проведение реакции в условиях аналогичных синтезу симметричных тетрафенилпорфинов приводит низкому выходу монооксифенилтрифенилпорфинов (около 5%), а основным продуктом реакции является тетрафенилпорфин. Основываясь на факте, что скорость реакции конденсации уменьшается с ростом электронодонорных свойств заместителей в фенильном кольце бензальдегида нами было выдвинуто предположение, что при конденсации пиррола со смесью бензальдегида и оксибензальдегида, бензальдегид быстрее реагирует с пирролом, чем оксибензальдегид, что приводит к накоплению в реакционной среде преимущественно тетрафенилпорфина. Реакция конденсации пиррола с бензальдегидами проходит через стадию образования порфириногена (3), который далее окисляется кислородом воздуха до порфирина (1-2). Порфириноген в кислой среде существует в равновесии с соответствующим карбкатионами (4) (1-3), но это свойство исчезает при его окислении. Таким образом, если исключить окисление на первых стадиях реакции, то можно добиться накопления в реакционной среде порфириногена (3), имеющего в фенильных кольцах систему заместителей, создаваемую соотношением участвующих в реакции бензальдегидов. При окислении такого порфириногена должен образоваться преимущественно нужный порфирин (2). С целью реализации указанных условий, первая стадия реакции конденсации в смеси ксилол-монохлоруксусная кислота, нами проводилась в инертной атмосфере (азот), а затем реакционную смесь окисляли кислородом воздуха.
Для подтверждения вышеизложенных предположений нами был синтезирован 5-(4’-оксифенил)-10,15,20-трифенилпорфин (3, Х = OH, Y = H, пара-изомер) из смеси порфириногенов (5, Х =O H, Y = H, пара-изомер), полученной восстановлением смеси тетрафенилпорфина и тетра(4-оксифенил)порфина при молярном соотношении 3 : 1 (1-4). После кипячения смеси порфириногенов в присутствии кислоты в атмосфере азота и последующем окислении реакционной смеси кислородом воздуха был выделен с небольшим выходом (около 3%) порфирин (2, Х = OH, Y = H, пара-изомер), образование которого подтверждают вышеизложенные предположения.
При изучении условий реакции (1-2), установлено, что оптимальное время проведения реакции в инертной атмосфере 40 минут, с последующим окислением образующегося порфириногена (3) в течение 1 часа.
Разработанный нами метод для синтеза монооксифенилтрифенилпорфинов был использован для синтеза других асимметрично замещенных тетрафенилпорфинов как с электронодонорными, так и с электроноакцепторными заместителями, а именно мононитрофенил- (2, Х = NО2, Y = H), моноаминофенил- (3, Х = NН2, Y = H), монодиметиламинофенил- (2, Х = NМе2, Y = H), монопиридилтрифенилпорфинов, моно(4-оксифенил)-трис(3,5-ди-трет-бутил-4-оксифенил)порфина (выход и физико-химические свойства приведены в диссертации).
Таким образом, разработанная нами методика для синтеза тетрафенилпо-рфиринов с асимметричной системой заместителей в фенильных кольцах является общей для синтеза монозамещенных тетрафенилпорфиринов как с электронодонорными, так и с электроноакцепторными заместителями.
(Б) Синтез пространственно искаженных порфиринов. Искажение порфиринового цикла может играть значительную роль в фотосинтетических и окислительно-восстановительных биологических системах, и кроме того, конформационные искажения порфиринового хромофора могут служить инструментом тонкой подстройки их физико-химических свойств. Наиболее известным и основным методом искажения порфиринового цикла является введение на его периферию заместителей в соседние мезо- и -положения, причем искажение растет с увеличением их числа и размеров.
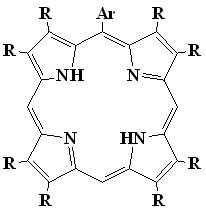
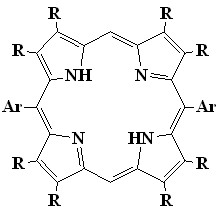
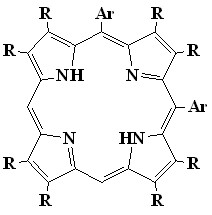
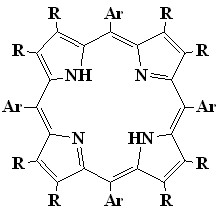
Наиболее сильно искаженные додеказамещенные порфирины (13) были получены нами конденсацией альдегидов с 3,4-дизамещенными пирролами, причем методы их синтеза мало отличаются от таковых для наиболее известных синтетических мезо-тетрафенилпорфиринов (выход 30-50%). С целью изучения влияния последовательного мезо-фенильного замещения в -октаалкилпорфиринах на плоскостное искажение порфиринового цикла, нами разработан метод синтеза серии мезо-фенилзамещенных октаалкилпорфиринов с различным числом и положением мезо-фенильных групп (общий выход 70%). Синтез проводился катализируемой кислотой конденсацией смеси 3,4-диалкилпирролов (6) и 2-гидроксиметил-3.4-диалкилпирролов (7) с бензальдегидами с последующим окислением образовавшейся смеси порфириногенов п-хлоранилом (1-5). Полученная смесь порфиринов достаточно легко и полно разделяется последовательной колоночной хроматографией на оксиде алюминия и силикагеле. Этот метод позволил нам получить все возможные замещенные порфирины с различной степенью искажения макрокольца. Особый интерес метод представляет для синтеза мало изученных 5,10-ди- (11) и 5,10,15-трифенилзамещенных (12) -октаалкилпорфиринов которые сложно получить прямым синтезом в индивидуальном виде. Тем более что состав смеси синтезируемых порфиринов можно регулировать в широких пределах соотношением исходных реагентов.
Квантово-химическое оптимизирование структур синтезированных порфиринов (программа HyperChem, метод PM3), показало, что -октаметил-порфин (8), а также мезо-монофенил (9) и транс-дифенил--октаметил-порфины (10) имеют почти плоское строение (24=0.012 и 0.010 для порфиринов 9 и 10 соответственно). Молекулы цис-дифенил (11), мезо-трифенил (12) и мезо-тетрафенилзамещенных (13) -октаметилпорфиринов значительно искажены (24=0.30, 0,44 и 0,63 для порфиринов 11, 12 и 13 соответственно), причем искажение порфиринового кольца нарастает с увеличением количества замещающих фенильных групп (8<9<10<11<12<13).
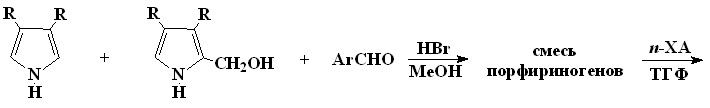 | ||
| 6 7 | ||
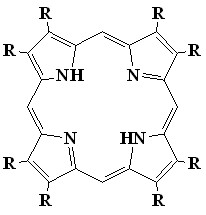 |  |  |
| 8 | 9 | 10 (1-5) |
 | 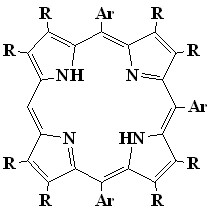 |  |
| 11 | 12 | 13 |
Данные РСА синтезированных нами порфиринов (11, R = Me) и (12, R = Me) показали, что молекула мезо-трифенил--октаметилпорфина (12), как и ожидалось, сильно искажена, а цис-дифенил--октаметилпорфина (11) почти плоская (24=0.040) (рис. 1), что расходится с данными квантово-химического расчета. О наличии искажения в цис-замещённом порфирине (11) в растворах свидетельствуют данные ЭСП и комплексообразования (приведены в диссертации). Таким образом, отсутствие плоскостной деформации в цис-замещённом порфирине (11, R = Me) в твердом состоянии, в отличие от теоретических данных для газовой фазы и экспериментальных данных в растворах, можно объяснить эффектами упаковки и межмолекулярных взаимодействий в кристалле. Молекулярная упаковка мезо-цис-дифенилзамещенного -октаметилпорфина (11, R = Me) характеризуется слоистой структурой, в отличие от паркетной структуры мезо-трифенилзамещенного -октаметилпорфина (12, R = Me) (рис. 2).
Другим методом искажения порфиринового цикла является напряжение связей, обычно между фенильными кольцами в мезо-положениях и макроциклом. К порфиринам такого типа относятся так называемые «циклофановые димерные» (14), «перекрытые» (15) и «перепоясанные» (16) порфирины, которые мы получали конденсацией пиррола с димерными бензальдегидами в которых фенильные кольца соединены достаточно короткими связками (О(СН2)nО) (1-6). Димерные порфирины (14) получаются при проведении реакции конденсации при высоком разбавлении в толуоле с добавкой 0,5% монохлоруксусной кислоты (выход до 10%). Использование других реакционных сред (ксилол-монохлоруксусная кислота, хлороформ-трифторуксусная кислота, пропионовая кислота) приводит к получению с димерных порфиринов с выходом менее 1%.
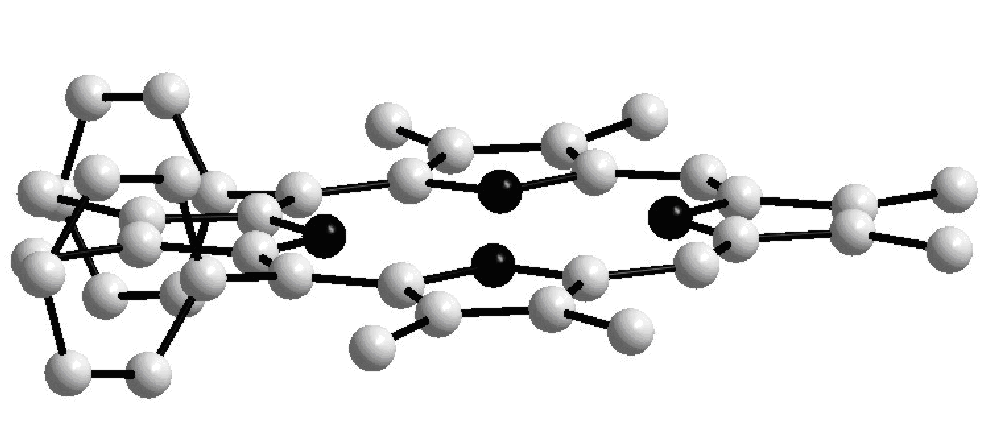 | 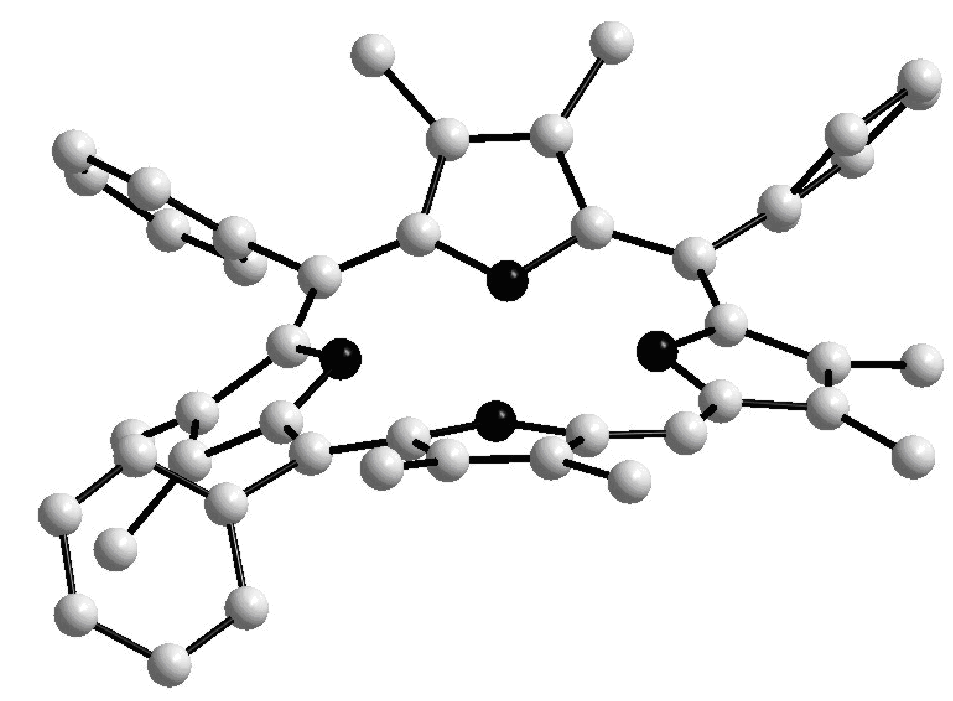 | |
| 11, R = Me, Ar = Ph | 12, R = Me, Ar = Ph | |
| Рисунок 1. Влияние мезо-фенильного замещения на плоскостное искажение порфиринов (11) и (12) (данные РСА). | ||
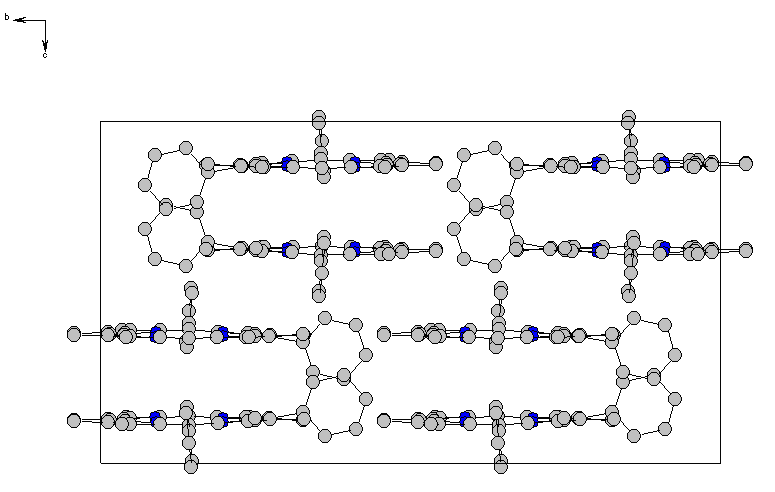 а а | 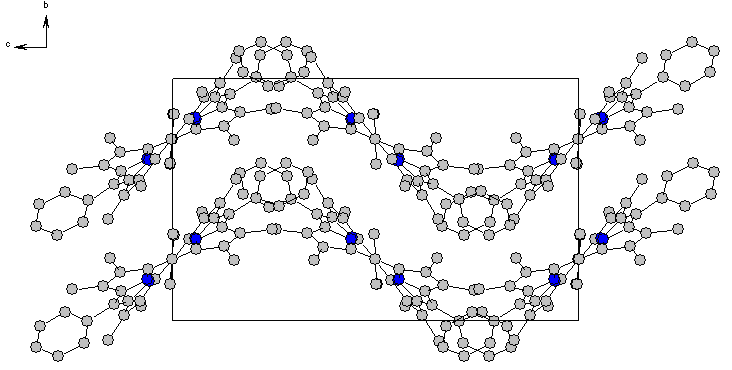 б б | |
| Рисунок 2. Молекулярная упаковка порфиринов (11) - (а) и (12) – (б). | ||
Нами установлено, что димерные порфирины (14), у которых порфириновые фрагменты соединяются диоксиметиленовыми мостиками (n = 1), в реакции конденсации не образуются, так как соответствующие диальдегиды в условиях кислотного катализа разрушаются с образованием формальдегида и исходных оксибензальдегидов. Не образуются димеры (14) и при конденсации пара-серии диальдегидов. В этом случае, по-видимому, идут в основном процессы полимеризации.
В случае орто-серии диальдегидов в реакции конденсации образуются димерные порфирины (14) при длине связующей полиметиленовой цепочки (n) 2-3 углеродных атома (для мета-серии n = 2-4). В случае n > 3 (для мета-серии n > 4) вместо димера (14) образуется смесь трех изомерных «перекрытых» и «перепоясанных» порфиринов (15 - 17) (выход 1-4%), так как в данном случае длины цепи хватает для образование связи между соседним фенильными фрагментами.
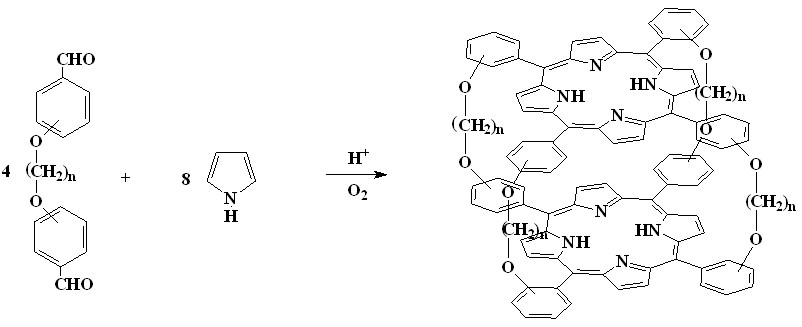 | (1-6) | ||||
| 14 | |||||
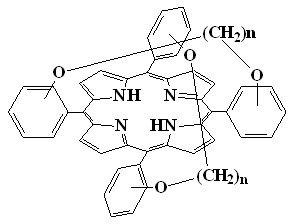 | 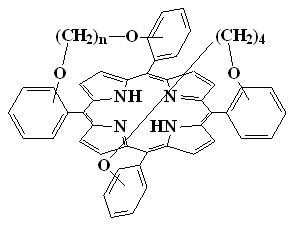 | 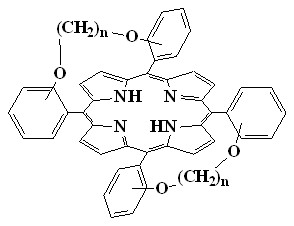 | |||
| 15 | 16 | 17 | |||
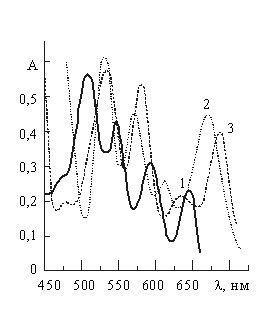 | Данные ЭСП и спектров 1Н ЯМР димерных порфиринов (14) (приведены в диссертации), а также квантово-хими-ческие расчеты (метод РМ3), показали, что в составе димера (14) соседние порфириновые макроциклы оказывают взаимное поляризующее действие и сильно искажены. В частности, в электронных спектрах поглощения димеров (14) имеет место батохромный сдвиг на 20-50 нм всех полос поглощения по сравнению с ЭСП мономерными тетра-(отро- и мета- фенил)порфинами (рис. 3), свидетельствующий о взаимном поляризующем действии двух порфириновых фрагментов. | ||||
| Рисунок 3. ЭСП порфиринов: 1- H2N(м-BuOФ)П; 2- 14 (м-С3); 3 -14 (м-С4) | |||||
Однако этот сдвиг не имеет монотонного характера при укорочении полиметиленовых цепочек, что свидетельствует о различной степени искажения димеров (14) с четным и нечетным числом метиленовых звеньев. Димер с нечетным числом метиленовых звеньев (n = 3, орто-, мета-) практически не имеют пространственных искажений и сохраняют практически плоское строение. Напротив, димеры с четным числом метиленовых звеньев (n = 2 орто-, мета-; n = 4 мета-) имеют «жесткую» структуру с сильно деформированными рифлеными порфириновыми макроциклами в которых два противоположных пиррольных ядра повернуты вверх, а два других вниз. Это характерным образом проявляется в 1Н ЯМР спектрах соединений (14). Сочетание наклона бензольных ядер по отношению к средней плоскости макроцикла с рифлением последнего является причиной магнитной неэквивалентности внешних и внутренних орто-протонов бензольных ядер, химические сдвиги которых составляют 7,62 м.д. и 8,6 м.д. соответственно, а также -протонов соседних пиррольных колец: 8,37 и 9,02 м.д.
1.2. Синтез 5,15-дифенил--октаалкилпорфинов. 5,15-Дифенил--октаалкилпорфирины (18) интересны тем, что эти соединения объединяют некоторые особенности мезо-тетрафенилпорфирина (1, R = H), а именно наличие мезо-арильных групп, с некоторыми особенностями -алкилпорфиринов (8), благодаря наличию незамещенных мезо-положений.
Наиболее распространенный способ синтеза 5,15-дифенилпорфиринов (18) заключается в конденсации,-незамещенных дипирролилметанов (19) с альдегидами в присутствии кислоты (1-7) и сходен с таковым для синтеза мезо-тетрафенилпорфинов.
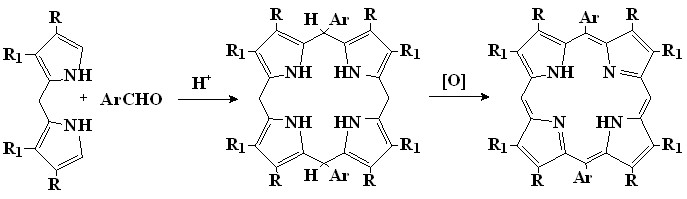 | (1-7) |
| 19 18 |
Нами был получен ряд 5,15-дифенилпорфиринов (18) (выход 30-60%, физико-химические свойства приведены в диссертации) и изучено влияние условий проведения реакции конденсации (1-7), а также стерических факторов заместителей в дипирролилметанах (19) и альдегидах и электронной природы заместителей в альдегидах на выход 5,15-дифенилпорфиринов (18).
Установлено, что лучшими растворителями для проведения реакции конденсации (1-7) являются хлороформ и хлористый метилен, а в качестве кислотного катализатора сильные органические кислоты (хлоруксусная и трихлоруксусная). В качестве окислителя промежуточного порфириногена можно с равным успехом использовать как традиционно применяемый дихлордицианбензахинон (ДДХ), так и более доступные и дешевые орто- и пара-хлоранилы (ХА).
Наличие небольших по размеру заместителей в 3,3'-положениях дипирролилметана (19, R1 = Н, Me, Et; R = H, Me) мало влияет на выход порфиринов, однако присутствие более объемистых групп (R1 = Pr, н-Bu, н-Am, н-Hex, и особенно сильно Bz; R = Me) значительно снижает его. Эти факты указывают на то, что наличие объемных заместителей в 3,3'-положениях дипирролилметанов препятствует образованию конформации (19a), которая требуется для осуществления реакции конденсации. В данном случае они находятся в основном в энергетически более выгодной трансоидной форме (19b), что приводит к снижению выхода порфирина.
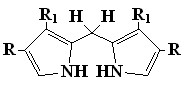 | 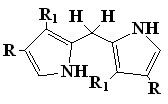 | Увеличение размеров заместите-лей в 4,4'-положениях дипирролилме-танов (19, R = Et, Bu) резко уменьшает выход порфиринов, что связано со сте- | |
| 19a | 19б | ||
рическими препятствиями заместителей реакции конденсации (1-7).
Электронная природа заместителей и их положение в исходных бензальдегидах мало влияют на выход порфиринов (18), и только наличие двух заместителей в 2,6-положениях фенильного кольца бензальдегида сильно снижает выход, что связано с неблагоприятными стерическими факторами.
Использование в конденсации (1-7) в качестве альдегида медного комплекса 2-формилтетрафенилпорфина (20) позволило нам получить смесь двух атропизомеров тримерного порфирина (21) (выход 11%) (1-8).
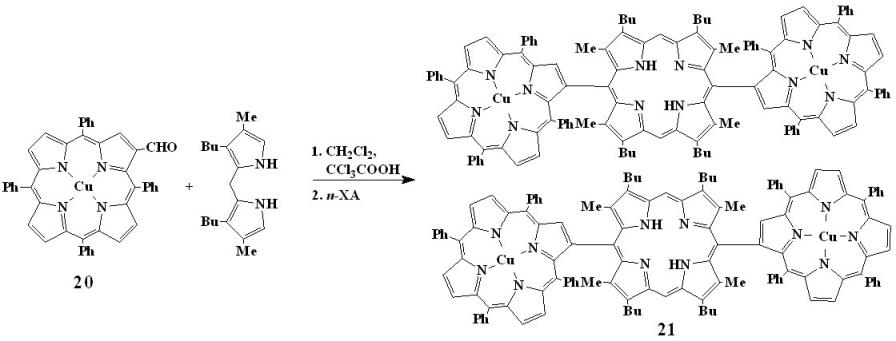 | (1-8) | ||
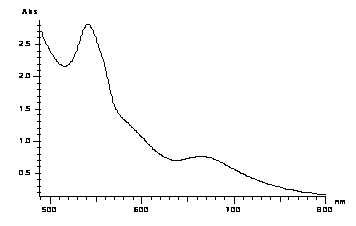 Рисунок 4. ЭСП порфирина (21) Рисунок 4. ЭСП порфирина (21) | ЭСП тримерного порфирина (21) представляет собой суперпозицию пиков боковых фрагментов CuТФП и центрального фрагмента свободного основания октаалкилпорфина (рис. 4). | ||
Таким образом, основное влияние на выход 5,15-дифенилпорфиринов (18) оказывают стерические факторы замещающих групп, как в исходных дипирролилметанах, так и в альдегидах, причем имеются оптимальные размеры замещающих групп.
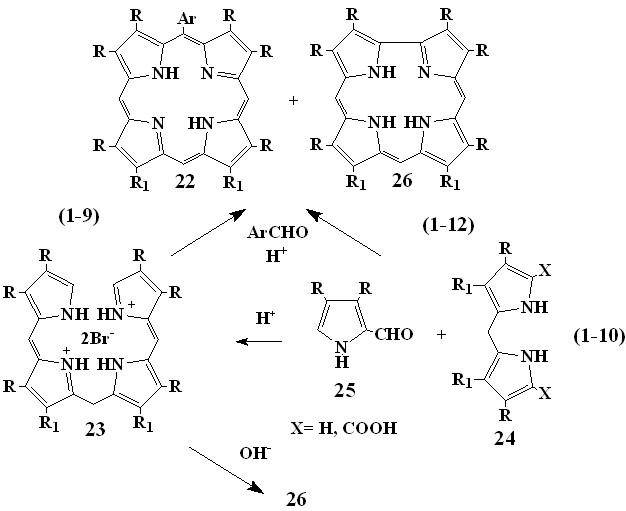
1.3 Синтез 5-фенил--октаалкилпорфинов. 5-Фенил--октаалкилпорфи-рины (22) как и 5,15-дифенил--октаалкилпорфирины (18) благодаря наличию арильных групп и свободных мезо-положений объединяют некоторые особенности мезо-тетрафенилпорфинов (1), с особенностями -алкилпорфиринов (8). Одним из наиболее распространенных методов синтеза 5-фенил--октаалкилпорфиринов (22) в настоящее время является катализируемая кислотой конденсация бензальдегидов с 1,19-динезамещенными биладиенами-а,с (23) в спиртах при кислотном или основном катализе (1-9).
Нами найдены оптимальные условия проведения конденсации биладиенов-а,с (23) с бензальдегидами для синтеза 5-фенил--октаалкилпорфиринов (22) (1-9). Установлено, что конденсация биладиенов-а,с (23) с бензальдегидами лучше всего проходит в спиртах. Добавка минеральной кислоты (HBr), которая должна подавлять образование порфирина, напротив, несколько увеличивает выход порфиринов (22), в то время как присутствие основания (пиридин), снижает выход (22), и всегда, одновременно с ним, образуется соответствующий коррол (26). По-видимому, соотношение выходов порфирина (22) и коррола (26) определяется относительными скоростями этих конкурирующих реакций ((1-9)-(1-11)).
 |
На выход 5-фенил--октаалкилпорфиринов (22) также оказывает электронная природа заместителей в бензальдегидах, в частности, использование бензальдегидов с электроноакцепторными заместителями приводит резкому уменьшению выхода порфиринов (22) и образованию побочных корролов (26).
Таким образом, оптимальными условиями для синтеза 5-фенил--окта-алкилпорфиринов (22) являются проведение реакции конденсации биладиена-а,с (23) с 12 кратным избытком бензальдегида в спиртах (метаноле в случае бензальдегидов с электронодонорными заместителями или бутаноле в случае бензальдегидов с электроноакцепторными заместителями) в течении 4-х часов с добавкой бромистоводородной кислоты и эквимолярного количества иода в качестве окислителя по отношению к используемому биладиену-а,с (23).
Нами получен ряд 5-фенил--октаалкилпорфиринов (22) с различными -алкильными заместителями (R = Me, R1 = H, Me, Et, Pr, Bu) и заместителями различной природы а фенильных кольцах (Ar = Ph, MeOC6H4, NO2C6H4, BrC6H4, 4-OH-3,5-(t-Bu)C6H2, Py, H, Hex) (выход 14-70%, некоторые физико-химические свойства приведены в диссертации).
Нам удалось также значительно упростить вышеописанную методику синтеза 5-фенил--октаалкилпорфиринов (22) при сохранении высокого выхода (22). Так как реакция синтеза дигидробромидов биладиена-а,с (23) и их дальнейшая конденсация с бензальдегидами проходит в сходных условиях (спиртовой растворитель), нами был осуществлен одноколбовый синтез 5-фенилпорфинов (22) из дипирролилметанов (24) и формилпирролов (25) без выделения промежуточных биладиенов-а,с (23) (1-12).
Глава 2. Введение заместителей в мезо-фенилзамещенные порфирины. Глава посвящена методам введения заместителей в мезо-фенилпорфириновую систему и изучению сравнительной активности мезо-, -положений порфиринового цикла и мезо-фенильных фрагментов в реакциях электрофильного замещения.
Не всегда удается получить с высокими выходами мезо-фенилзамещен-ные порфирины (9)-(13) реакцией конденсации пиррола или его линейных производных с бензальдегидами. Поэтому большой интерес представляет изучение и разработка методов введения заместителей в готовую мезо-фенилпорфириновую молекулу.
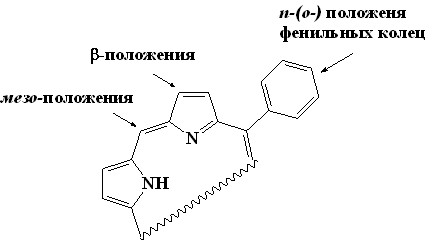 | Сам мезо-фенилпорфириновый фрагмент (27) имеет 3 возможных потенциальных центра для атаки реагентами: фенильные кольца (для порфиринов (9-13, R = Alk)), -положе-ния (для порфиринов (9-13, R = H)) и мезо-положения (для моно-, ди- и три-мезо-фенилпрофиринов (9-12 R = Alk)). |
| 27 |
В настоящей главе проведен анализ и обобщение современных литературных данных по реакциям сульфирования, галогенирования (хлорирования, бромирования, йодирования), формилирования, ацилирования, нитрования как свободных мезо-фенилпорфиринов, так и их металлокомплексов. Рассматривая все эти реакции, можно выделить реакции электрофильного замещения, -катионрадикальные реакции металлокомплексов, нуклеофильные реакции и некоторые другие. На наш взгляд, особый интерес представляют реакции электрофильного замещения, которые проходят в ароматическом порфириновом цикле. Большой интерес представляет изучение сравнительной активности мезо- и -положений порфиринового цикла, а также относительной активности мезо-фенильных заместителей, которые испытывают на себе влияние порфиринового цикла. Введение металла во внутренний реакционный центр макроцикла значительно изменяют активность различных положений в порфириновом цикле, что искажает картину их реакционной способности. Поэтому, большой интерес вызывают реакции электрофильного замещения на свободных основаниях мезо-фенилпорфиринов.
Для изучения сравнительной активности мезо- и -положений порфиринового цикла и мезо-фенильных заместителей мезо-фенилпрофиринов в реакциях электрофильного замещения нами была выбрана реакция нитрования, которая является классической реакцией электрофильного замещения в большинстве ароматических соединениях. В качестве объектов исследования были выбраны 5-фенил--октаалкилпорфин (22), 5,15-дифенил--октаалкилпорфин (18), имеющие свободные мезо-положения и фенильные кольца, мезо-тетраэ-тилпорфин (28), имеющий свободные -положения и не имеющий фенильных колец и Н2ТФП, имеющий свободные -положения и фенильные кольца.
Установлено, что наиболее эффективными нитрующими агентами для электорфильного нитрования мезо-фенилпорфиринов являются азотная кислота в хлороформе и нитрит натрия в трифторуксусной кислоте Нитрование 5-фенил--октаалкилпорфина (22) (2-1) приводит к смеси двух нитропорфиринов (появление в ИК-спектре двух полос деформационных колебаний нитрогруппы при 1529 и 1361 см-1), имеющих очень близкую подвижность на силуфоле (ТСХ, соотношение 1:1) и не разделяемых колоночной хроматографией или перекристаллизацией. Данные элементного анализа, масс-спектр (МАЛДИ) и анализ спектра 1Н ЯМР (рис. 5) позволил сделать вывод, что смесь состоит из мезо-динитропорфиринов (цис- (28) и (транс- (29) изомеры). Попытки получить мононитропорфирин не привели к положительным результатам даже при недостатке нитрующего агента и при использовании более мягких нитрующих систем. Это связано с искажением порфиринового цикла при первичном нитровании и, тем самым, облегчением реакции повторного нитрования за счет снижения ароматичности порфиринового цикла. Об искажении порфиринового цикла говорит батохромный сдвиг и уширение полос в ЭСП полученной смеси мезо-динитропорфиринов, а также квантово-химическое оптимизирование структуры монониропорфирина. (Данные ЭСП и квантово-химических расчетов (программа HyperChem, метод PM3) приведены в диссертации). Дальнейшее нитрование смеси мезо-динитропорфиринов приводит к мезо-тринитропорфирину (30), который далее (в фенильный фрагмент) не нитруется даже в более жестких условиях.
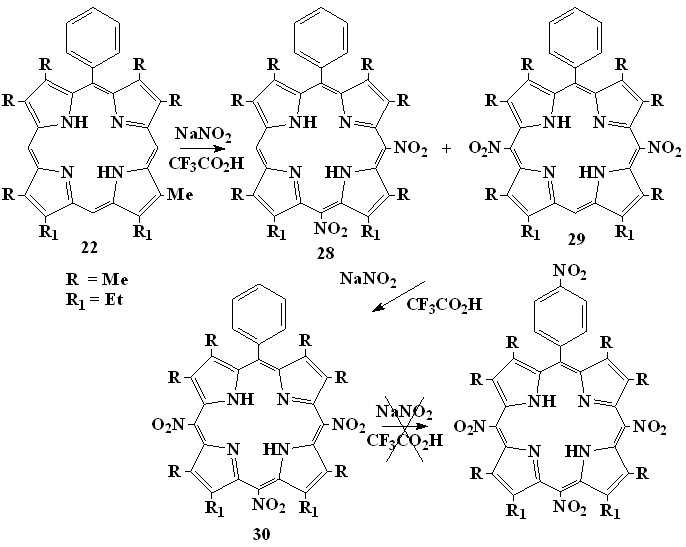 | (2-1) | |
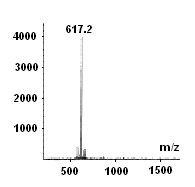 а а | 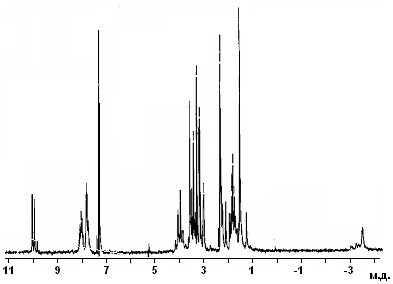 б б | |
| Рисунок 5. Масс-спектр (МАЛДИ) (а) и спектр 1Н ЯМР (б) смеси динитропорфиринов 28 и 29. | ||
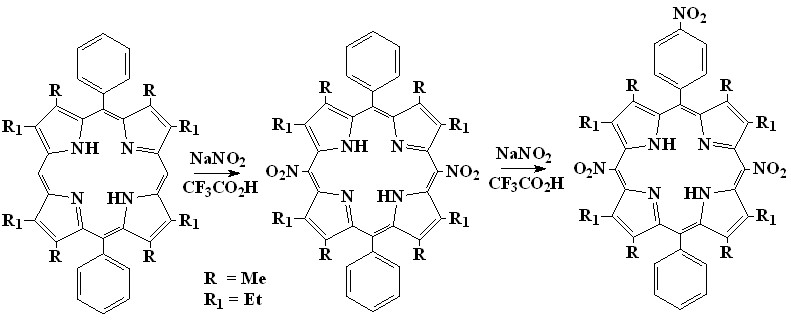
Аналогичным образом, нитрование 5,15-дифенил--октаалкилпорфина (18) сразу приводит к мезо-динитропорфирину (31). Дальнейшее нитрование мезо-динитропорфирина (31) идет в одно из фенильных колец (2-2). Нитрование второго фенильного кольца не происходит, что вероятно связано с дезактивацией мезо-фенилпорфириновой молекулы (32) тремя электроноакцепторнымих нитро-группами.
 | (2-2) |
| 18 31 32 |
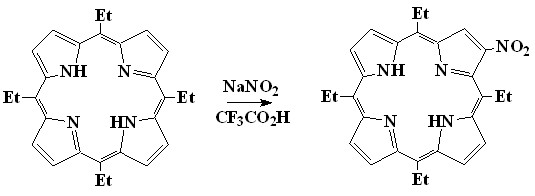
Нитрование порфирина (29) не имеющего фенильных колец и свободных мезо-положений идет с трудом в свободное -положение (2-3).
 | (2-3) |
| 29 |
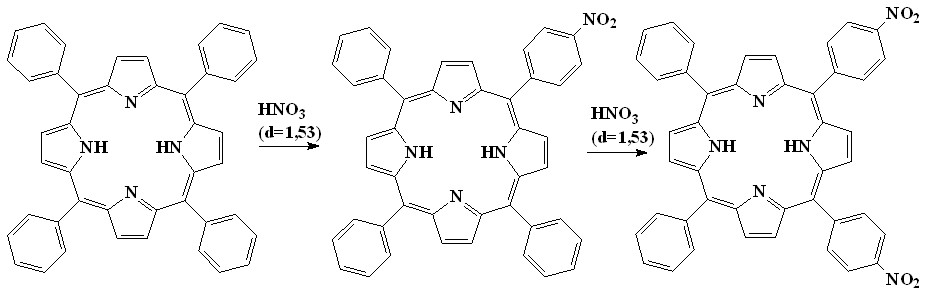
Нитрование Н2ТФП, как описано в литературе, приводит к мононитрофенилтрифенилпорфину (33, п-изомер). Увеличение концентрации нитрующего реагента и времени реакции приводит к 5,10-ди(п-дитрофенил)-15,20-ди-фенилпорфину (34).
 | (2-3) |
| 33 34 |
Таким образом, мы пришли к выводу, что существующее в литературе утверждение о влиянии протонирования по внутрициклическим атомам азота на реакционную способность различных положений порфиринового цикла в реакции электрофильного замещения является не совсем правомочным. Наиболее легко подвергаются электрофильной атаке мезо-положения, далее идет замещение в фенильных кольцах. Реакция в -положение идет с большим трудом только при отсутствии свободных мезо-положений и фенильных колец.
Кроме этого, нами изучено влияние природы заместителей в фенильных кольцах на реакцию нитрования Н2ТФП. Установлено, что тетра(м-фенил)порфины, независимо от электронной природы заместителей, всегда нитруются в пара-положения по отношению к порфириновому циклу. Как и следовало ожидать, порфирины с электронодонорными заместителями в фенильных кольцах нитруются намного легче, чем порфирины с электроноакцепторными заместителями. В последнем случае нитрование идет медленнее и с более низким выходом. При наличие электронодонорных заместителей в орто-положениях бензольных ядер нитрование, как и следовало ожидать, идет в положение 5 того же фенильного фрагмента, что объясняется ориентирующим влиянием заместителей. При наличие в орто-положениях фенильных колец электронакцепторных заместителей реакция не идет. Наличие заместителей в пара-положениях фенильных колец приводит, в условиях реакции, в основном, к окислительной деструкции порфиринового цикла.
Выход и физико-химические свойства нитропорфиринов, полученных в результате нитрования мезо-фенилпорфиринов, приведены в диссертации.
Глава 3. Модификация заместителей в мезо-фенилзамещенных порфиринах. Глава посвящена методам модификации заместителей в мезо-фенилпорфиринах и состоит из 2-х разделов: модификации заместителей в мезо- и -положениях мезо-фенилпорфиринов и модификации заместителей в фенильных фрагментах мезо-фенилпорфиринов. Следует отметить, что эти методы во многом схожи, поэтому по модификации заместителей в мезо- и -положениях в диссертации приведены литературные данные, а основное внимание уделено разработке и изучению методов модификации заместителей в фенильных фрагментах порфиринов наиболее доступных, получаемых с высокими выходами в реакциях конденсации ((1-1), (1-7), (1-9) см. выше) функционально замещенных по фенильным кольцам мезо-фенилпорфиринах (9-13). Эти методы позволяют получать порфирины, имеющие самые разнообразные физико-химические свойства и содержащие заместители с активными группами, из небольшого числа доступных предшественников.
Из известных в настоящее время мезо-фенилзамещенных порфиринов с активными группами в фенильных кольцах, с точки зрения возможности их дальнейшей химической модификации, наибольший интерес представляют оксифенил-, аминофенил-, карбоксифенил- и галогенфенилзамещенные мезо-фенилпорфирины.
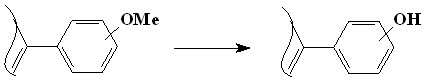
3.1. Мезо-оксифенилпорфирины. Мезо-тетраоксифенилпорфирины (1, R = H, Ar = C6H(5-n)OHn) образуются в реакциях конденсации пиррола с бензальдегидами с низкими выходами и большим количеством трудноотделимых примесей, а в случае использования в этих реакциях салицилового альдегида порфирины вообще не образуются. Наиболее перспективным методом синтеза мезо-оксифенилпорфиринов в настоящее время является деметилирование легко доступных мезо-метоксифенилпорфиринов (3-1).
 | (3-1) |
Хорошие результаты достигаются при использовании в качестве деметилирующих агентов гидрохлоридов пиридина или анилина при кипении. Однако этот метод применим лишь для синтеза наиболее устойчивых мета- и пара- тетраоксифенилпорфинов (выход около 90%) и мало пригоден для синтеза орто- оксифенилзамещенных порфиринов, а также для тетра(диоксифенил)-порфиринов, 5,15-диокифенилоктаалкилпорфинов и 5-оксифенилоктаалкил-порфинов. Нами было показано, что для синтеза тетра(орто-оксифенил)-порфинов и тетра(диоксифенил)порфиринов более подходящим деметилирующим агентом является 60%-ная бромистоводородная кислота в инертной атмосфере. В настоящее время для гидролиза метоксифенилпорфиринов используется мягкий деметилирующий агент – трибромид бора (реакция идет в хлористом метилене при –800С в инертной атмосфере в течение 24 ч). Однако нами было установлено, что реакцию деметилирования можно без снижения выхода проводить при комнатной температуре на воздухе в хлороформе. Были определены оптимальные условия проведения данной реакции, которые позволяют получать с высокими выходами (90-98%) не только гидроксипроизводные тетрафенилпорфинов, но и менее устойчивые 5,15-диокифенилокта-алкил- и 5-оксифенилоктаалкилпорфирины.
Мезо-оксифенилпорфирины, имея в своем составе активную окси- группу, легко подвергаются дальнейшим химическим превращениям, среди которых наиболее интересны реакции алкилирования и ацилирования.
Реакция алкилирования мезо-оксифенилпорфиринов (3-2) является типичной реакцией нуклеофильного замещения (SN2) аналогичной, алкилированию фенолов. Она идет в полярных растворителях в присутствии основного агента необходимого для активации фенола.
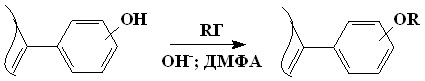 | (3-2) |
| 35 |
Проведение алкилирования мезо-оксифенилпорфиринов в спиртах в присутствии твердой щелочи или карбоната калия малоэффективно в виду длительности процесса и неполноты превращения из-за плохой растворимости как исходных мезо-оксифенилпорфиринов, так и получаемых мезо-алкоксифенилпорфиринов (35). Использование в качестве растворителя ДМФА, позволило значительно увеличить выход (35) (80-95%), однако реакция при комнатной температуре идет очень медленно (12-24 ч). Исходя из высокой химической устойчивости большинства мезо- алкоксифенилпорфиринов (35) нами была проведена реакция алкилирования в кипящем ДМФА, в присутствии карбоната калия, что позволило значительно сократить время реакции (до 1 ч) при неизменно высоком выходе мезо- алкоксифенилпорфиринов (35). Интересен тот факт, что в реакцию алкилирования вступают только первичные галогеналканы. Нам не удалось провести реакцию с вторичными галогеналканами. Вероятно, в условиях реакции вместо нуклеофильного замещения галогена идет элиминирование с образованием соответствующих алкенов.
Таким образом, в настоящее время реакция алкилирования проводится первичными галогеналканами, в основном, в ДМФА в присутствии в качестве основного агента карбоната калия при кипении для устойчивых мезо-оксифенилпорфиринов или при комнатной температуре для лабильных мезо-оксифенилпорфиринов.
Приведенным методом нами синтезированы различные тетраалкоксифенил (36) замещенные порфирины, хорошо растворимые в неполярных органических растворителях, тетрааллилокси- (37) и тетрапропаргилоксифенилпорфины (38), которые могут быть использованы в качестве мономеров в реакции полимеризации, этиловые эфиры тетракис(карбоксиметиленоксифенил)-порфирины (39), при гидролизе которых образуются растворимые в щелочных растворах тетракис(карбоксиметиленоксифенил)порфирины (40), а также проведена иммобилизация на эпоксиактивированные полимеры.
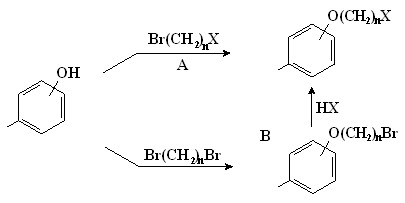
Алкилированием монооксифенилтрифенилпорфинов нами синтезирован ряд порфиринов, содержащих на периферии молекулы остатки с активными группами (43). «Привязка» остатков с активными группами к порфирину может проводиться двумя путями (3-3): алкилированием оксифенилпорфирина галогеналканом с активной группой (путь A), или предварительным алкилированием оксипорфирина избытком,-дибромалкана с образованием -бромалкоксифенилпорфирина с последующим его взаимодействием в аналогичных условиях с соединением, имеющим активную группу (путь B).
Путь A предпочтительнее, так как короче и дает более высокий выход целевого продукта (на исходный оксифенилпорфирин). Однако не всегда можно получить и очистить галогеналкан, имеющий активную функциональную группу. В связи с этим, в основном, используется путь B. Выход синтезированных таким путем соединений составляет 40-60%, их физико-химические свойства приведены в диссертации.
 | (3-3) | |
| Х – остаток с активной группой | ||
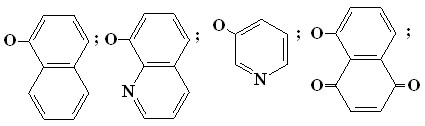
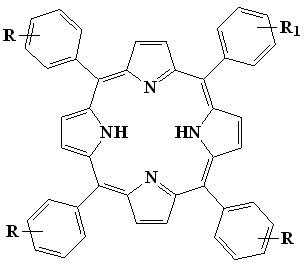 | 36 R = R1 = OCnH2n+1, n=216; 37 R = R1 = OCH2CH=CH2; 38 R = R1 = OCH2CCH; 39 R = R1 = OCH2COOEt; 40 R = R1 = OCH2COOH 41 R = H, R1 = OCH2COOH 42 R = H, R1 = OC16H33; 43 R = H, R1 = O(CH2)4X, X = Br; OH; N(CH2COOH)2; | |
 | ||
 | ||
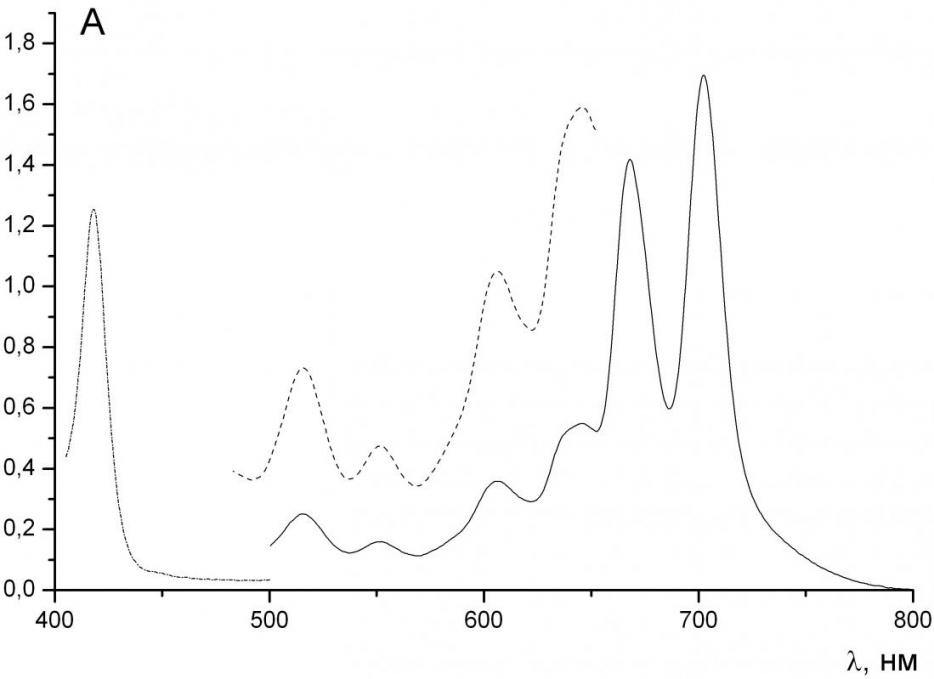
ЭСП порфирин-фталоцианинового димера являются комбинацией порфириновой и фталоцианиновой составляющих (рис. 6). Тоже самое можно сказать о спектре ЯМР 1Н этого соединения, который содержит сигналы протонов как порфиринового, так и фталоцианинового фрагментов (рис. 6).
 а а | 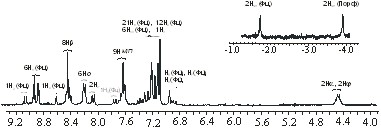 б б |
| Рисунок 6. ЭСП (а) и спектр ЯМР 1Н (б) порфирин-фталоцианинового димера | |
Нами проведено ацилирование 5-оксифенил-10,15,20-трис(2’,6’-ди-трет-бутил-4’-оксифенил)порфина (44) хлорангидридами пальмитиновой, олеиновой и акриловой кислот (3-4) в условиях реакции Айнхорна (выход 86%, физико-химические свойства приведены в диссертации). Химизм данного процесса приведен на схеме (3-5).
Преимущества ацилирования в условиях метода Айнхорна состоит в высокой ацилирующей способности образующейся пиридиниевой соли (46) и мягких условиях проведения синтеза. Полученный 5-пальмитоилоксифенил-10,15,20-трис(2’,6’-ди-трет-бутил-4’-оксифенил)порфин (45, R = C15H31) является полифункциональным порфирином, сочетающим в одной молекуле остатки 2,6-ди-(трет-бутил)фенола в качестве заместителей антиоксидантов и липофильный фрагмент, обеспечивающий возможность встраивания порфирина в липидный бислой клеточной мембраны.
 | (3-4) |
| 44 45 | |
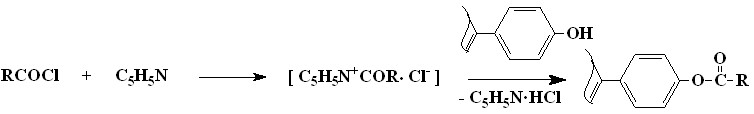 | (3-5) |
| 46 |
Для изучения антиоксидантной активности порфина (45, R = C15H31) проведено его окисление PbO2 и изучена устойчивость образующихся радикальных частиц методом ЭПР.
Спектр ЭПР образующихся радикалов (рис. 7) представляет триплет, характеризующийе взаимодействие спина неспаренного электрона с двумя эквивалентными мета- протонами феноксильного остатка. Образующиеся радика-
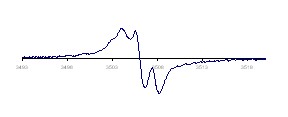 | лы устойчивы в растворе в отсутствии кислорода при комнатной температуре в течение нескольких суток. Величина изотопного g-фактора составляет 2,0040, а величина константы сверхтонкого вза имодействия с ядрами аН (1Н) равна 0,18 мТл |
| Рисунок 7. Спектр ЭПР радикала (толуол, 295К). |
3.2. Мезо-аминофенилпорфирины. Подобно мезо-оксифенилпорфиринам, мезо-аминофенилпорфирины (1, R = H, Ar = C6H5NH2) невозможно получить конденсацией аминобензальдегидов с пирролом или его производными. Наиболее перспективным методом синтеза мезо-аминофенилпорфиринов в настоящее время является восстановление мезо-нитрофенилпорфиринов (3-6)
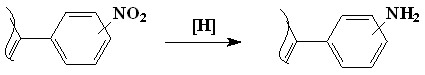 | (3-6) |
Восстановление тетра(нитрофенил)порфинов нами проводилось в 1,5-кратном избытке дигидрата двухлористого олова в концентрированной соляной кислоте при температуре 70-800С, что позволяет получить почти количественный выход тетра(аминофенил)порфиринов.
Ди- (18, Ar = C6H4NO2) и моно- (22, Ar = C6H4NO2) замещенные нитрофенилпорфирины требуют более мягких условий восстановления, т.к. в условиях, описанных выше, возможно хлорирование более реакционноспособных свободных мезо-положений. В данном случае реакцию восстановления проводили при комнатной температуре и в среде метанола, который переводит получаемые аминофенилпорфирины в раствор и способствует полному восстановлению исходных нитрофенилпорфиринов.
Кроме того, нами предложен более удобный метод восстановления нитрофенилпорфиринов с использованием в качестве восстановителя гидразин гидрата при катализе палладием на угле в смеси бензол – метанол. Этот метод позволяет проводить реакцию с почти количественным выходом и избежать трудоемкого отделения неорганических солей от аминофенилпорфирина. Данный метод применим для восстановления не только нитрофенилпорфиринов, но и их аналогов нитрофталоцианинов (выход 97%). Однако, следует отметить, что этот метод эффективен лишь при восстановлении мезо-нитрофенил--октаалкилпорфиринов, так как образующийся диимид, выполняющий роль восстановителя, в случае -незамещенных мезо-нитрофенилпорфиринов кроме нитро- группы частично восстанавливает порфириновый цикл до соответствующих хлоринов.
Выход и физико-химические свойства полученных нами мезо-аминофенилпорфиринов приведены в диссертации.
Аминогруппа мезо-аминофенилпорфиринов очень активна и легко модифицируется.
Метилирование тетра(аминофенил)порфинов иодметаном в ДМФА в присутствии 2,6-лутидина позволило нам получить катионные триметиламинофенилпорфирины (47) (выход 70%). Тетракис(п- и м-триметиламинофенил) порфины растворимы в воде в широком интервале рН. При использовании в качестве оснований К2СО3 реакция останавливается на стадии образования диметиламинофенилпорфиринов (48) (3-7) (выход 80%). Физико-химические свойства полученных нами алкилированных мезо-аминофенилпорфиринов приведены в диссертации.
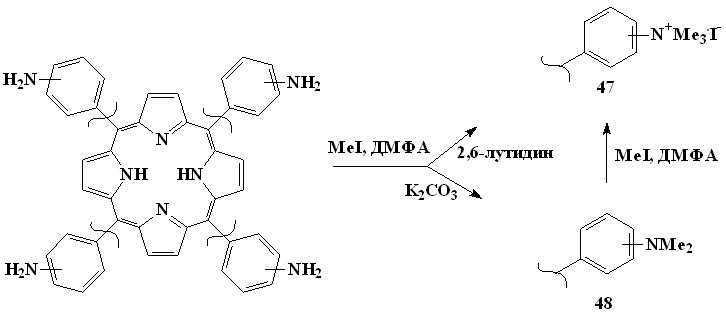 | (3-7) |
С целью получения порфириновых мономеров нами было проведено ацилирование ряда мезо-аминофенилпорфиринов хлорангидридом акриловой кислоты в условиях реакции Айнхорна (3-8). Реакция проводилась в хлороформе, в качестве основного катализатора использовался пиридин. Выход и физико-химические свойства ацилированных мезо-аминофенилпорфиринов (49) приведены в диссертации.
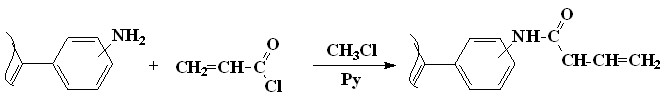 | (3-8) |
| 49 |
Особый интерес с точки зрения модификации аминогруппы представляет реакция диазотирования, которая широко используется для синтеза ароматических соединений с различными функциональными группами. С применением реакции диазотирования получают интересный и важный класс органических соединений - азокрасители.
Тетра(аминофенил)порфины легко диазотируются нитритом натрия в водных растворах минеральных кислот (3-9). Полученные соли диазония (50) довольно устойчивы. Их заметное разложение с выделением азота наблюдается только при температуре выше комнатной. Порфириновый цикл в условиях реакции диазотирования устойчив, однако диазотированный тетра(2-аминофенил)порфин при нагревании дает соединения непорфиринового характера. Вследствие этого орто-замещенные тетрафенилпорфины образуются с низкими выходами и большим количеством трудноотделимых примесей. Однако, реакция азосочетания диазотированного тетра(2-аминофенил)порфина с фенолом успешно проходит на холоду с образованием тетра(2-оксифенил-азофенил)порфина. Диазотированные тетра(3- и 4-аминофенил)порфины при нагревании дают тетра(оксифенил)порфины, а также вступают в реакцию Зандмеера и реакцию азосочетания, что позволяет получать тетра(галоген-фенил)порфины и азокрасители на основе порфиринов, которые невозможно получить другим путем. Диазотирование моно- (22, Ar = C6H4NН2) и дизамещенных аминофенилпорфиринов (18, Ar = C6H4NН2) с последующим превращением полученных солей диазония позволяет синтезировать замещенные порфирины которые недоступны при использовании других путей синтеза. Использование в качестве диазотирующего агента нитрита натрия в водных растворах кислот в данном случае не приводит к положительным результатам, так как такие аминофенилпорфирины не растворимы в этих условиях. Однако аминофенилпорфирины диазотируются амилнитритом в смеси хлороформ – уксусная кислота. Полученные растворы солей диазония вступают в реакцию Зандмеера и реакцию азосочетания, причем для создания нужной основности среды в данном случае использовался триэтиламин.
Выход и физико-химические свойства полученных нами порфиринов (схема (3-9)) приведены в диссертации.
Анализ ЭСП (рис. 8) «порфирин-азокрасителей» не позволяет сделать однозначных выводов о возможности взаимодействия -систем азокрасителей с -системой порфиринового макроцикла. Полоса Соре тетрафенилпорфинов (max 420 нм, 5.105) находится рядом с широкой полосой поглощения
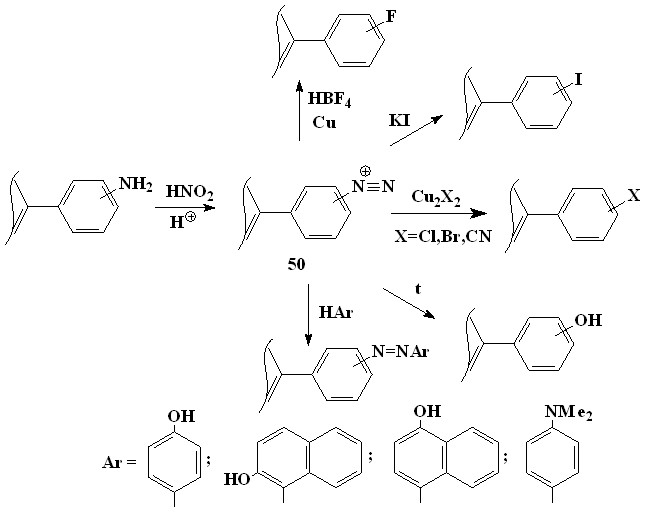 | (3-9) |
остатка азокрасителя (max 500 нм, 2,5.104), поэтому трудно судить имеет
| ли место «перекачка» -электронной плотности с остатков азокрастелей на порфириновый цикл. Однако сильное снижение интенсивности полосы Соре в ЭСП «порфирин-азокрастителей» и рост полос электронных переходов, а также их батохромный сдвиг по сравнению с ЭСП H2TФП указывает на существования такого взаимодействия. | |
| Рисунок 8. ЭСП порфирин-азокрасителя с остатком -нафтола. |
3.3. Мезо-карбоксифенилпорфирины. В данном разделе проведен анализ и обобщение литературных данных по модификации карбоксильной группы в мезо-карбоксифенилпорфиринах. Кроме этого, с целью получения порфириновых мономеров и изучения возможности иммобилизации порфиринов на полимерные носители, содержащие гидроксильные группы, нами была предпринята попытка этерификации мезо-карбоксифенилпорфиринов спиртами в присутствии серной кислоты в качестве катализатора. Установлено, что реакция идет только с простыми спиртами, такими как метанол и этанол. С другими спиртами, такими как циклогексанол, аллиловый, амиловый, реакция не идет. Поэтому, из соответствующих мезо-карбоксифенилпорфиринов, действием на них тионилхлорида в хлороформе в присутствии ДМФА получены хлорангидриды, которые далее реагировали со спиртами в условиях реакции Айнхорна (3-10). Реакция проводилась в хлороформе, в качестве основного катализатора использовался пиридин. Кроме того, с помощью этой реакции проведена иммобилизация мезо-карбоксифенилпорфиринов на эпоксиактивированные полимеры. Выход и свойства полученных мезо-алкилкарбоксифенилпорфиринов (51) приведены в диссертации.
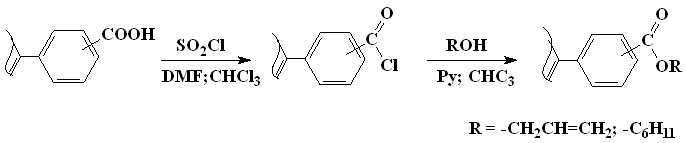 | (3-10) |
| 51 |
3.4. Мезо-галогенфенилпорфирины. В данном разделе проведен анализ и обобщение литературных данных по использованию мезо-галогенфенил-порфиринов в качестве исходных соединений в палладий катализируемых реакциях таких как реакция Хека, Соногашира, кросс-сочетания Сузуки, а также реакциях аминирования и амидирования.
Кроме того, в нашей совместной работе с группой И.П. Белецкой проведено палладий катализируемое аминирование 5,15-дибромфенил--окта-алкилпорфинов (18, Ar = C6H4Br) анилином и изучены условия реакции аминирования 5,15-дибромфенил--октаалкилпорфинов (18, Ar = C6H4Br) и 5-бромфенил--октаалкилпорфинов (22, Ar = C6H4Br) вторичными аминами различной природы, включая гидроксипиперидины в присутствии различных фосфиновых лигандов (L) (3-11). Реакция мезо-бромфенилпорфиринов с гидроксипиперидинами осложняется тем, что последние содержат вторичную спиртовую группу и потенциально могут восстанавливать исходный мезо-бромфенилпорфирин.
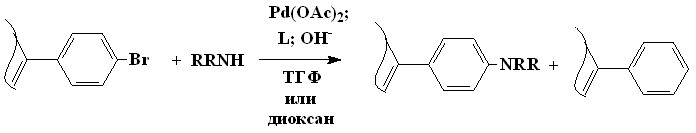 | (3-11) |
| 52 53 | |
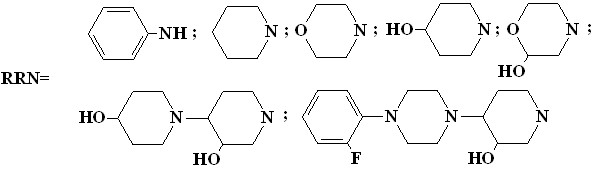 | |
Было установлено, что наиболее подходящими фосфиновыми лигандами (L) в реакциях аминирования мезо-бромфенилпорфиринов являются 2-(ди-трет-бутилфосфино)бифенил (54), 2-(дициклогексилфосфино)-2’- диметил-амино)бифенил (55), 1-[2-(дифенилфосфино)-ферроценил]-этилметиловый эфир (56), причем они проявляют приблизительно одинаковую активность.
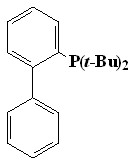 | 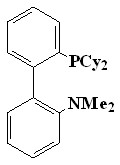 | 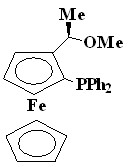 | В качестве растворителя можно использовать как ТГФ, так и диоксан, но из-за удобства работы предпочтение было отдано диоксану. Оптимальная температура реакции 80-100°С. |
| 54 | 55 | 56 |
В качестве основания лучше использовать трет-бутилат натрия. Реакции мезо-бромфенилпорфиринов с гидроксипиперидинами сопровождаются образованием значительных количеств продуктов восстановления ((53).
В этом случае для увеличения выхода продуктов аминирования необходимо использовать большой избыток фосфинового лиганда и основания. Выход и свойства продуктов аминирования (52) приведены в диссертации.
Таким образом, модификация заместителей в мезо-фенилпорфиринах позволяет получать соединения с практически любыми заданными физико-химическими свойствами и требуемым набором заместителей.
В заключение следует отметить, что для ряда синтезированных мезо-фенилпорфиринов исследованы кислотно-основные свойства, кинетика таутомерных переходов, обусловленных наличием 2-х атомов водорода и 4-х внутрициклических атомов азота, кинетика комплексообразования и дальнейшей экстракоординации полученных металлокомплексов, а также кинетика их диссоциации. Кроме этого некоторые полученные порфирины были переданы для исследования в качестве термотропных и лиотропных жидких кристаллов, катализаторов радикальной полимеризации метилметакрилата, модификаторов различных полимерных материалов.
Основные результаты и выводы:
- На основе анализа и обобщения литературных данных и механизмов реакции конденсации пиррола и полиметиленпирролов с альдегидами разработаны удобные и эффективные методы синтеза мезо-фенилзамещенных порфиринов симметричной и несимметричной структуры имеющих в фенильных кольцах заместители, способные к дальнейшей химической модификации, а также пространственно-искаженные порфирины.
- Исследовано влияние электронной природы заместителей и стерических факторов в бензальдегидах и пиррольных соединениях на выход мезо-фенилпорфиринов. Установлено, что электронная природа заместителей в бензальдегидах оказывает существенное влияние на выход порфиринов только в случае тетрафенилпорфинов (выход порфиринов с электроноакцепторными заместителями выше, чем с электронодонорными). В случае ди- и моно-фенилпорфиринов природа заместителей в бензальдегидах мало влияет на выход порфиринов. В случае орто-замещенных бензальдегидов, во всех случаях заместитель препятствует реакции конденсации, следовательно, превалирует действие стерических факторов над действием электронных эффектов.
- Разработанная методика синтеза тетрафенилпорфиринов с асимметричной системой заместителей в фенильных кольцах является общей для синтеза монозамещенных тетрафенилпорфиринов как с электронодонорными, так и с электроноакцепторными заместителями.
- Изучено влияние последовательного мезо-фенильного замещения в -октаалкилпорфиринах на степень искажения порфиринового кольца. Установлено, что искажение порфиринового кольца нарастает с увеличением количества замещающих фенильных групп. Мезо-цис-дифенилпорфин оказался почти плоским в твердом состоянии и искаженным в газовой фазе и в растворах, что объясняется эффектами упаковки и межмолекулярных взаимодействий в кристалле.
- Сэндвичевые димеры с нечетным числом метиленовых звеньев практически не имеют пространственных искажений и сохраняют практически плоское строение, напротив, димеры с четным числом метиленовых звеньев имеют «жесткую» структуру с сильно деформированными рифлеными порфириновыми макроциклами в которых пиррольные циклы имеют седловидную конформацию.
- На примере реакции нитрования изучена реакционная способность различных положений мезо-фенилпорфиринов в реакциях электрофильного замещения. Установлено, что существующее в литературе утверждение о влиянии протонирования на реакционную способность различных положений порфиринового цикла в реакции электрофильного замещения является не совсем правомочным. Наиболее легко подвергаются электрофильной атаке мезо-положения, далее идет замещения в фенильных кольцах. Реакция в -положение идет с большим трудом только при отсутствии свободных мезо-положений и фенильных колец.
- Предложены удобные и эффективные методы синтеза мезо-фенилзамещенных порфиринов с активными группами в фенильных кольцах, в том числе оксифенилпорфиринов деметилированием метоксифенилпорфиринов, аминофенилпорфиринов восстановлением нитрофенилпорфиринов.
- Изучены реакции модификации активных заместителей в фенильных кольцах мезо-фенилзамещенных порфиринов, позволяющие получать из небольшого набора порфиринов, соединения с самыми разнообразными физико-химическими свойствами, в том числе алкилирование и ацилирование оксифенилпорфиринов; этерификация карбоксифенилпорфиринов; алкилирование, ацилирование и диазотирование аминофенилпорфиринов, с дальнейшей заменой диазогруппы на Cl, Br, I, OH; а также реакция азосочетания, в результате которой получены порфирины с остатками азокрасителя. Проведено аминирование галогенфенилпорфиринов вторичными аминами.
- Комбинацией разработанных методов синтезирован большой набор порфиринов с разнообразной структурой и разнообразными физико-химическими свойствами, в том числе водо- и органорастворимые.
- Изучена возможность иммобилизации мезо-фенилзамещенных порфиринов с активными группами в фенильных кольцах на полимеры-носители различной природы.
- Изучены физико-химические свойства вновь полученных порфиринов и их металлокомплексов.
Автор признателен коллективу кафедры органической химии и руководству Ивановского государственного химико-технологического университета за многолетнюю поддержку данной работы. Автор благодарит всех соавторов и коллег, без участия которых выполнение данной работы было бы невозможным. Особая благодарность – член-корреспонденту РАН О.И. Койфману за неоценимую помощь и поддержку данной работы.
Основное содержание работы опубликовано в следующих работах:
- Семейкин А.С., Койфман О.И., Березин Б.Д. Сырбу С.А. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 2. Получение тетра(оксифенил)порфинов. // Химия гетероцикл. соед. 1983. №10. С.1359-1361.
- Койфман О.И., Семейкин А.С., Шляпова А.Н., Сырбу С.А. Исследование кинетики реакции координации Cd2+ и Zn2+ с алкоксизамещенными тетрафенилпорфинами в ДМФА. // Изв.вузов. Химия и хим. технология. 1986. Т.29. №9. С.125-127.
- Сырбу С.А., Семейкин А.С., Березин Б.Д., Койфман О.И. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 4. Функционально замещенные монооксипроизводные тетрафенилпорфина. // Химия гетероцикл. соед. 1987. №6. С. 781-786.
- Голубчиков О.А., Коровина С.Г., Сырбу С.А. и др. Синтез, спектральные характеристики и строение циклофанового димера тетрафенилпорфина. // Журн. орг. химии. 1988. Т.24. №11. С. 2378-2383.
- Сырбу С.А., Семейкин А.С., Березин Б.Д., Койфман О.И. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 5. Тетра(карбоксиметиленоксифенил)порфины и их этиловые эфиры. // Химия гетероцикл. соед. 1989. №10. С. 1373-1377.
- Голубчиков О.А., Кувшинова Е.М., Коровина С.Г., Сырбу С.А. и др. Кинетика координации циклофанового и линейного порфиринов ацетатами Сu, Zn и Сd. // Журн. физич. химии, 1989. Т. 63.№ 4. С. 912-918.
- Сырбу С.А., Семейкин А.С., Березин Б.Д., Койфман З.Ц. Кинетические особенности образования комплексов Zn2+ с монозамещенными тетрафенилпорфинами. // Изв.вузов. Химия и хим. технология. 1990. Т.33. №5. С.29-32.
- Сырбу С.А., Семейкин А.С., Березин Б.Д. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 6. Применение реакции диазотирования для синтеза монозамещенных тетрафенилпорфинов. // Химия гетероцикл. соед. 1990. №11. С.507-509.
- Сырбу С.А., Семейкин А.С., Березин Б.Д. Способ получения оксифенилзамещенных порфиринов. // А.С. №1684284 СССР МКИ 5 С 07 D 478/22. Опубл. БИ №38 от 15.10.91.
- Сырбу С.А., Семейкин А.С., Сырбу Т.В. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 7. Соли тетра(N,N,N-три-метиламинофенинил)порфинов.// Химия гетероцикл.соед. 1996. №5. С. 668-671.
- Сырбу С.А., Семейкин А.С., Сырбу Т.В. Синтез тетрафенилпорфинов с активными группами в фенильных кольцах. 9. Азокрасители на основе тетрафенинилпорфинов.// Химия гетероцикл.соед. 1996. №8. С. 1045-1049.
- Хализов О.И., Семейкин А.С., Сырбу С.А., Березин Б.Д. Применение реакции диазотирования для синтеза замещенных фталоцианинов. // Изв. вузов. Химия и хим. технол. 1999. Т. 42. В. 3. С. 23-27.
- Сырбу С.А., Семейкин А.С. Синтез (гидроксифенил)порфиринов. // Журн. орг. химии. 1999. Т. 35. В. 8. С. 1262-1265.
- Syrbu S., Semeikin A., Lyubimova T., Stuzhin P. Unsymmetrical meso-phenyl sabstituted octamethylporphyrins: synthesis by mixed condensation and chromatographic separation. // First International Conference on Porphyrins and Phthalocyanines (ICPP-1). Dijon. France. 2000. P. 576.
- Голубчиков О.А., Власова Е.К., Кувшинова Е.М., Сырбу С.А. Структура и координационные свойства некоторых пространственно искаженных производных тетрафенилпорфина. // Изв. вузов. Химия и хим. технол. 2000. Т. 43. В. 6. С. 120-123.
- Петров О.А., Чижова Н.В., Сырбу С.А., Березин Б.Д. Роль кислотно-основных взаимодействий в реакции комплесообразования тетрагалогентетраазапорфиринов с ацетатом магния в системе ДМСО – хлорбензол. // Журн. общ. химии. 2000. Т. 70. В. 5. С. 825–831.
- Семейкин А.С., Сырбу С.А., Любимова Т.В. Влияние стерических и электронных эффектов заместителей на выход 5,15-замещенных октаалкилпорфинов.// Журн. общ. химии. 2001. Т.71. №10. С.1747-1750.
- Карманова Т.В., Громова Т.В., Березин Б.Д., Сырбу С.А., Семейкин А.С. Влияние структурных особенностей -замещенных производных порфиринов на их физико-химические свойства. // Журн. общ. химии. 2001. Т.71. №5. С. 856-861.
- Сырбу С.А., Семейкин А.С., Буряева И.В., Кумеев Р.С., Альпер Г.А. ЯМР-спектры мезо-фенилзамещенных порфиринов с различной степенью искажения порфиринового макрокольца. // Изв.вузов. Химия и хим.технология. 2002. Т.45. №7. С. 141-142.
- Березин Б.Д., Карманова Т.В., Громова Т.В., Сырбу С.А., Семейкин А.С. Исследование экстракоординации бромзамещенных порфиринов с органическими основаниями.// Координац. химия. 2002. Т.28. №9. С.648-653.
- Семейкин А.С., Березин М.Б., Чернова О.М., Антина Е.В., Сырбу С.А., Любимова Т.В., Кутепов А.М. Взаимосвязь строения и сольватационных характеристик алкилзамещенных дипирролилметенов. // Изв. РАН. Сер. химическая. 2003. В. 8. С. 1712-1718.
- Березин М.Б., Чернова О.М., Сырбу С.А., Березин Д.Б., Кумеев Р.С., Альпер Г.А., Семейкин А.С., Вьюгин А.И. Спектральные характеристики метилзамещенных дипирролилметенов и их структурных аналогов. // Изв.вузов. Химия и хим.технология. 2003. Т.46. № 8. С. 30-34.
- Семейкин А.С., Сырбу С.А., Березин М.Б., Любимова Т.В. Синтез алкилзамещенных дипирролилметанов. // Изв.вузов. Химия и хим. технология. 2004. Т.47. № 4. С. 10-14.
- Сырбу С.А., Семейкин А.С., Койфман О.И. Мезо-фенилзамещенные порфирины. Модификация в арильных группах. // Изв. вузов. Химия и хим. технол. 2004. Т. 47. № 5. С. 46-55.
- Сырбу С.А., Любимова Т.В., Семейкин А.С. Фенилзамещенные порфирины. 1. Синтез мезо-фенилзамещенных порфиринов. // Химия гетероцикл. соед. 2004. № 10. С. 1464 -1472.
- Трифонова И.П., Бурмистров В.А., Сырбу С.А., Койфман О.И. Координация азагетероциклов макрогетероциклическими металлокомплексами в амфипротонных средах. I. Взаимодействие имидазола с (ацетат) тетра-фенилпорфинатом хрома III. // Журн. общ. химии. 2005. Т.75. № 8. С. 1360-1364
- Syrbu S., Semeikin A. Synthesis and modification of meso-monosubstituted porphyrins. // J.Porphyrins.Phtalocyanines. 2006. V.10. №6. Р.884
- Сырбу С.А., Семейкин А.С., Корженевский А.Б., Койфман О.И. 5-(3’-аллилоксифенил)-2,3,7,8,12,18-гексаметил-13,17-дибутилпорфин и 5-(2’-аллилоксифенил)-2,3,7,8,12,18-гексаметил-13,17-дибутилпорфин в качестве красящего вещества оптических фильтров. // Патент РФ № 2281301 Б.И. №22 от 10.08.2006.
- Сырбу С.А., Семейкин А.С., Корженевский А.Б., Койфман О.И. 5-(4’-акриламидофенил)-10,15,20-трифенилпорфин и 5-(3’-акриламидофе-нил)-10,15,20-трифенилпорфин в качестве красящего вещества оптических фильтров. // Патент РФ № 2277557 Б.И. №16 от 10.06.2006.
- Глазунов А.В., Сырбу С.А., Семейкин А.С. Способ получения тетра(3-амино-5-трет-бутил)фталоцианина меди. // Патент РФ № 2272038 Опубл. Б.И. №8 от 20.03.2006.
- Сырбу С.А., Семейкин А.С., Корженевский А.Б., Койфман О.И. 5-(4’-акриламидофенил)-2,8,12,13,17,18-гексаметил-3,7-дибутилпорфин и 5-(3’-акриламидофенил)-2,8,12,13,17,18-гексаметил-3,7-дибутилпорфин в качестве красящего вещества оптических фильтров. // Патент РФ № 2281304 Б.И. №22 от 10.08.2006.
- Сырбу С.А., Глазунов А.В., Семейкин А.С. Новый подход к восстановлению нитрофенилпорфиринов. // Изв. вузов. Химия и хим. технология. 2006. Т.49. №4. С. 122-123.
- Syrbu S., Semeikin A., Ageeva T., Kolodina E. Koifman O. Strategies for the synthesis of porphyrin monomers. // J.Porphyrins.Phtalocyanines. 2006. V.10. №6. Р.885.
- Герасимова О.А., Милаева Е.Р., Шпаковский Д.Б., Семейкин А.С. Синтез 5-(4-гидроксифенил)-10,15,20-трис[3,5-ди(трет-бутил)-4-гидрокси-фенил]порфина и 5-(4-пальмитилоксифенил)-10,15,20-трис[3,5-ди-(трет-бутил)-4-гидроксифенил] порфина и феноксильные радикалы на их основе. // Изв. РАН Серия химическая. 2007. № 4. С. 800-303.
- Сырбу С.А., Агеева Т.А., Семейкин А.С., Койфман О.И. Стратегия синтеза мономеров на основе фенилзамещенных порфиринов для порфиринсодержащих полимеров различной структуры. // Изв. РАН. Серия химическая. 2007. № 4. С. 680-703.
- Семейкин А.С., Кувшинова Е.М., Сырбу С.А., Голубчиков О.А. Синтез и кинетика координации биядерного медного комплекса порфиринового триммера ацетатом меди в уксусной кислоте. // Изв. вузов. Химия и хим. технология. 2007. Т.50. №6. С.18-20.
- Белокурова А.П. Щербина А.А. Исляйкин М.К. Ершова Ю.Н. Сырбу С.А., Бурмистров В.А. Набухание диацетата целлюлозы, модифицированного макроциклическими соединениями, в воде и разбавленных растворах азотной кислоты. // Пластические массы. 2007. №7. С.17-19.
- Lyubimtsev A., Syrbu S., Vagin S., Hanack M. Synthesis of novel covalently linked dimeric phthalocyanines. // Eur. J. Org. Chem. 2007 Р. 2000–2005.
- Milaeva E.R., Gerasimova O.A., Jingwei Zhang, Shpakovsky D.B., Syrbu S.A., Semeykin A.S., Koifman O.I., Kireeva E.G., Shevtsova E.F., Bachurin S.O., Zefirov N.S. Synthesis and antioxidative activity of metalloporphyrins bearing 2,6-di-tert-butylphenol pendants. // J.Inorg.Biochem. 2008. V. 102. P.1348-1358.
- Исламова Р.М., Садыкова Г.Р., Ионова И.А., Сырбу С.А., Койфман О.И., Монаков Ю.Б. Влияние металлокомплексов порфиринов в присутствии пероксида бензоила и азодиизобутиронитрила на радикальную полимеризацию метилметакрилата. // Изв. вузов. Химия и хим. технология. 2008. Т.51. №3. С.65-68.
- Александрийский В.В., Кононов В.Д., Бурмистров В.А. Трифонова И.П., Сырбу С.А., Исляйкин М. К., Койфман О.И. Сольватационное состояние тетра(3,5-ди-третбутилфенил) порфина в смесях хлороформ-этанол по данным ЯМР и квантовохимических расчетов. // Изв. вузов. Химия и хим. технология.2008. Т.51. №7. С.53-55.
- Артамкина Г.А., Сазонов П.К., Штерн М.М., Гришина Г.В., Веселов И.С., Сырбу С.А., Семейкин А.С. Койфман О.И., Белецкая И.П. Аминирование мезо-бромфенил(полиалкил)порфиринов: синтез порфиринов, содержащих гидроксипиперидиновый фрагмент. // Журн. орг. химии. 2008. Т.44. №3. С. 423-433.
- Artamkina G.A., Sazonov P.K., Shtern M.M., Grishina G.V., Veselov I.S., Semeikin A.S., Syrbu S.A., Koifman O.I., Beletskaya I.P. Palladium-Catalyzed N-Arylation of Hydroxypiperidines with meso-Bromophenyl(polyalkyl)porphyrins. // Synlett. 2008. №1. P.45-48.

