Синтез и свойства диамино -1,2,4- и -1,3,4-тиадиазолов и макрогетероциклических соединений на их основе
На правах рукописи
МЕЛЕНЧУК ТАТЬЯНА ВЛАДИМИРОВНА
Синтез и свойства
диамино-1,2,4- и -1,3,4-тиадиазолов
и макрогетероциклических соединений
на их основе
02.00.03 – Органическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Иваново 2009
Работа выполнена на кафедре технологии тонкого органического синтеза Государственного образовательного учреждения высшего профессионального образования «Ивановский государственный химико-технологический университет»
Научный руководитель: кандидат химических наук, доцент
Данилова Елена Адольфовна
Официальные оппоненты: доктор химических наук, профессор
Абрамов Игорь Геннадьевич.
доктор химических наук, профессор
Андрианов Владимир Геннадьевич
Ведущая организация: Институт химии Коми
НЦ УрО РАН
Защита состоится «9» ноября 2009 г. в 1000 часов на заседании совета по защите докторских и кандидатских диссертаций Д 212.063.01 в ГОУВПО «Ивановский государственный химико-технологический университет» по адресу: 153000, г. Иваново, пр. Ф.Энгельса, д. 7.
С диссертацией можно ознакомиться в информационном центре ГОУ ВПО «Ивановский государственный химико-технологический университет» по адресу: 153000, г. Иваново, пр. Ф.Энгельса, д. 10.
Автореферат разослан « 28 » сентября 2009 г.
Ученый секретарь совета по защите
докторских и кандидатских диссертаций Кувшинова Е.М.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Макрогетероциклические соединения (Мс) можно рассматривать как аналоги фталоцианина, у которого один или два изоиндольных фрагмента заменены карбо- или гетероциклическими остатками диаминов. Особый интерес представляют соединения, имеющие в структуре пятичленный гетероцикл с атомом серы. Это обусловлено биологической активностью и широким разнообразием других аспектов практического применения прекурсоров синтеза Мс – 2,5-диамино-1,3,4-тиадиазола и 3,5-диамино-1,2,4-тиадиазола. На их основе созданы многие эффективные лекарственные препараты. 3,5-Диамино-1,2,4-тиадиазол - «Амтизол», 2-имино-4-тиобиурет, из которого он получается - «Гутимин», являются эффективными антигипоксантами. Диакарб, этазол, тизанидин содержат в своем составе 1,3,4-тиадиазольный фрагмент.
На момент постановки данной работы способы получения этих соединений не удовлетворяли химиков-органиков, как по качеству, так и по выходу целевых продуктов. Поэтому разработка новых подходов к созданию компактных методик, базирующихся на сокращении числа стадий и повышении выхода целевых продуктов, является актуальной задачей.
К началу наших исследований тиадиазолсодержащие Мс были представлены соединениями АВАВ типа с 1,2,4-тиадиазольными фрагментами и АВАВАВ типа с 1,3,4-тиадиазольными фрагментами (А-тиадиазольный, В-изоиндольный циклы). Единственная публикация по синтезу безметального трет-бутилзамещенного Мс с фрагментом 1,3,4-тиадиазола АВВВ типа, названного тиадиазолофталоцианином, появилась в 2001 году. Введение тиадиазольного цикла сопровождается включением атома серы в макроциклическую структуру. Изучение реакционной способности и геометрического строения диаминов позволит объяснить различия в строении тиадиазолсодержащих Мс.
Фактором, ограничивающим углубленное изучение Мс, является их низкая растворимость в органических растворителях, вместе с тем одним из возможных путей повышения растворимости могло бы быть введение алкильных заместителей в 1,3,4-тиадиазольный фрагмент. На момент постановки данной работы в литературе отсутствовали сведения о синтезе Мс с N-алкил-1,3,4-тиадиазолиновыми фрагментами.
Таким образом, постановка исследования, направленного на получение и изучение свойств диаминотиадиазолов и макрогетероциклических соединений на их основе, актуальна и научно обоснована.
Цель работы: синтез и свойства диамино-1,2,4- и -1,3,4-тиадиазолов и макрогетероциклических соединений на их основе. Для достижения поставленной цели предполагается решить следующие задачи:
- Провести научное и экспериментальное обоснование создания новых и усовершенствование известных способов синтеза исходных соединений: 2-имино-
-4-тиобиурета, 3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола и его
3-N-алкилзамещенных тиадиазолинов. - Разработать новые подходы к созданию компактных методик, базирующихся на сокращении числа стадий и повышении выхода целевых продуктов, которые позволили бы решить проблемы ресурсосбережения и повысить экологическую безопасность.
- Изучить реакционную способность новых 3-N-алкилзамещенных тиадиазолинов и влияние природы тиадиазольного цикла на формирование макроциклических систем;
- Осуществить направленный синтез новых органорастворимых макрогетероциклических соединений на основе 3,5-диамино-1,2,4-тиадиазола и
3-N-алкилзамещенных 1,3,4-тиадиазолинов и их комплексов с металлами. - Изучить особенности электронного и геометрического строения полученных соединений с использованием методов квантовой химии и с применением комплекса физико-химических методов: масс--спектрометрии, электронной, колебательной, 1Н ЯМР спектроскопии, элементного анализа.
- Изучить свойства синтезированных соединений с целью определения возможного их практического применения.
Научная новизна. Впервые синтезированы органорастворимые макрогетероциклические соединения на основе 3,5-диамино-1,2,4-тиадиазола АВАВ-типа.
Синтезированы новые трехзвенные продукты (ТЗП) АВА-типа и новые макрогетероциклические соединения АВВВ – типа, содержащие
3-N-алкилзамещенные тиадиазолины. Методом рентгеноструктурного анализа (РСА) доказано, что алкилирование проходит по циклическому атому азота N(3). Показана возможность образования никелевых комплексов на основе Мс.
Впервые измерены квантовые выходы безметальных серусодержащих Мс АВВВ-типа и ТЗП АВА-типа. Показано, что ТЗП с N-пентил-1,3,4-тиадиазолиновыми фрагментами имеет наибольший квантовый выход люминесценции, что позволяет расценивать его как потенциально практически применимый объект.
Научная и практическая значимость. Проведено научное и экспериментальное обоснование создания новых и усовершенствование известных способов синтеза исходных соединений: 2-имино-4-тиобиурета,
3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола и его
3-N-алкилзамещенных тиадиазолинов. Разработанные способы получения 2-имино-
-4-тиобиурета, 3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола имеют патентную защиту.
Разработаны новые подходы к созданию компактных методик, базирующихся на сокращении числа стадий и повышении выхода 2-имино-4-тиобиурета,
3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола, которые позволили повысить экологическую безопасность процессов.
Изучены влияние природы тиадиазольного цикла на формирование макроциклических систем и реакционная способность новых
N-алкилзамещенных тиадиазолинов.
Изучены особенности электронного и геометрического строения полученных соединений с использованием методов квантовой химии и с применением комплекса физико-химических методов: масс-спектрометрии, электронной, колебательной,
1Н ЯМР спектроскопии, элементного анализа.
ТЗП с N-пентил-1,3,4-тиадиазолиновыми фрагментами запатентован в качестве жирорастворимого красителя для крашения полистирола и парафина.
Изучены свойства синтезированных соединений с целью определения возможного их практического применения.
Часть настоящей работы выполнена при поддержке гранта Российского фонда фундаментальных исследований № 05-03-33003а
Апробация работы. Результаты были представлены и обсуждались на 10ой Международной конференции по физической и координационной химии порфиринов и их аналогов (Иваново, 2009), XXIV Международной Чугаевской конференции по координационной химии (Санкт-Петербург, 2009), Международной конференции «Новые направления в химии гетероциклических соединений» (Кисловодск, 2009), 23ем Международном симпозиуме по органической химии серы (Москва, 2008), Fifth International Conference on Porphyrins and Phthalocyanines (ICPP-5) (Moscow, 2008), XXIII Международной Чугаевской конференции по координационной химии (Одесса, 2007), Всероссийской научной конференции «Природные макроциклические соединения и их синтетические аналоги» (г. Сыктывкар, 2007), научных конференциях фестивалей студентов, аспирантов и молодых ученых «Молодая наука в классическом университете» (Иваново, 2006-2009), XXVII научной сессии Российского семинара по химии порфиринов и их аналогов «Проблемы бионеорганической химии в России» (Иваново, 2006), XXIX научной сессии Российского семинара по химии порфиринов и их аналогов «Достижения и перспективы развития координационной химии порфиринов. Итоги 50-летних исследований» (Иваново, 2006), 61ой региональной конференции студентов, магистрантов и аспирантов, посвященной 1000-летию Ярославля (Ярославль, 2008).
Публикации. По материалам диссертации опубликовано 6 статей (из них 3 в журналах, рекомендованных ВАК), 18 тезисов докладов и 3 патента РФ.
Объем и структура диссертации. Диссертация изложена на 140 страницах машинописного текста и состоит из введения, литературного обзора, экспериментально-методической части, обсуждения результатов и основных результатов и выводов. Работа содержит 27 схем, 51 рисунок, 18 таблиц, список литературы, включающий 184 наименований.
Автор выражает глубокую признательность своему научному руководителю к.х.н., доц. Даниловой Е.А.; д.х.н., проф. Исляйкину М.К. за всестороннюю помощь и поддержку на всех этапах работы и помощь в проведении квантово-химических расчетов; д.х.н., проф. Нефедову С.Е. за помощь в проведении рентгенодифракционного эксперимента; д.х.н., проф. Горбуновой Ю.Г. за помощь в проведении масс-спектрометрических исследований синтезированных соединений; д.биол.н., проф. Кузнецову О.Ю. за совместную работу по исследованию биологических свойств; ведущему инженеру отдела химии лантанидов Семенишину Н.Н. и д.х.н. Коровину Ю.В. за помощь в проведении исследований люминесцентных свойств синтезированных соединений, а также д.х.н.
Усольцевой Н.В. и к.х.н. Быковой В.В. за совместную работу по исследованию жидкокристаллических свойств.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении дано обоснование актуальности работы, сформулирована ее цель, отмечена научная новизна и практическая значимость.
1. Литературный обзор
Литературный обзор состоит из 4 разделов. В первых двух разделах рассмотрены методы получения исходных соединений в синтезе Мс и непосредственно самих тиадиазолсодержащих макрогетероциклических соединений, отмечены особенности строения макроциклов АВАВ- и АВВВ – типов. Третий раздел посвящен рассмотрению спектральных и физико-химических свойств тиадиазолсодержащих макрогетероциклических соединений. Четвертый раздел содержит сведения о свойствах макрогетероциклических соединений, определяющих перспективы их практического применения.
2. Экспериментально-методическая часть
В данной главе описаны использованные экспериментальные методики и приведены оригинальные методики синтеза новых соединений и данные по их идентификации: результаты изучения строения полученных соединений с помощью ИК, электронной, 1Н ЯМР спектроскопии, масс-спектрометрии и элементного анализа, характеристики приборов, использованных для изучения строения и физико-химических свойств (элементный анализ, ИК, 1Н ЯМР и электронная адсорбционная и эмиссионная спектроскопии, масс-спектрометрия, рентгеноструктурный анализ), а также особенности проведения квантово-химических расчетов.
Описаны методики исследования биологических, люминесцентных и жидкокристаллических свойств.
3. Обсуждение результатов
3.1. Синтез исходных веществ
Были разработаны новые методы синтеза 2,5-диамино-1,3,4-тиадиазола 2,
3,5-диамино-1,2,4-тиадиазола 4 и 2-имино-4-тиобиурета 3, которые являются важными лекарственными препаратами так и биологически активными веществами.
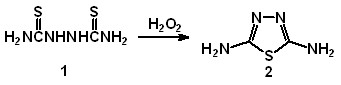 | 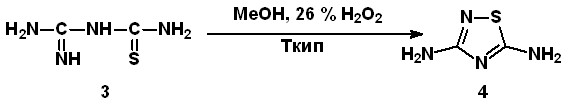 |
| Схема 1 | Схема 2 |
В основе предложенных нами методик синтеза 2 и 4 лежит окислительная конденсация 26 %-ым H2O2 производных мочевины, что позволяет увеличить выход целевых продуктов в сравнении с литературными данными с 43 % до 98 %, с 50 % до 86 % соответственно (схема 1, 2) и существенно сократить число технологических стадий.
С помощью квантово-химических расчетов, выполненных методом DFT с использованием гибридного функционала B3LYP с базисным набором
6-31G(d, p) с помощью программного комплекса GAMESS V.7, проведено изучение геометрического строения и конформационных свойств исходных соединений и возможных конформеров. На основании полученных результатов предложен вероятный механизм образования циклического соединения 4 (схема 3).
Схема 3
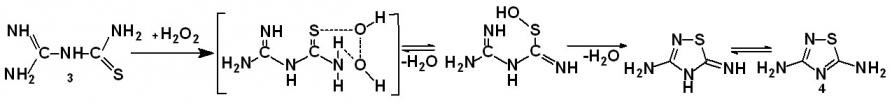
Нами предложен новый способ получения 2-имино-4-тиобиурета, заключающийся во взаимодействии дициандиамида с тиосульфатом натрия в присутствии 25 %-ой серной кислоты (схема 4), который исключает применение газообразного сероводорода. На данный способ получен приоритет по выдаче патента РФ.
Схема 4
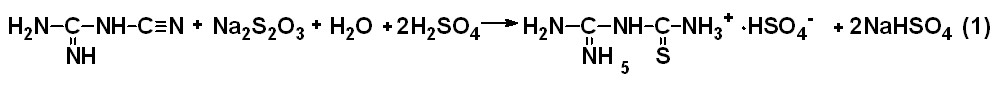
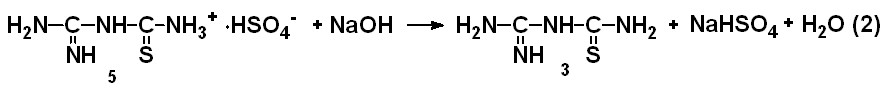
Предложенные способы получения 2,5-диамино-1,3,4-тиадиазола, 3,5-диамино-1,2,4-тиадиазола и 2-имино-4-тиобиурета прошли испытание и получили положительную рекомендацию к применению в лабораторном и полупромышленном синтезе.
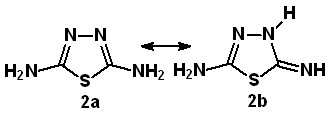
2,5-Диамино-1,3,4-тиадиазол может существовать в виде двух таутомерных форм: тиадиазольной 2а и тиадиазолиновой 2b. Сведения о 3-N-алкилзамещенных тиадиазолинах в литературе ограничены синтезом 5-амино-3-бутил-2-имино-1,3,4-тиадиазолина. Нами получен ряд новых алкилзамещенных тиадиазолинов с пентильным, децильным и додецильным фрагментами (схема 5). Строение установлено на основании данных элементного анализа, масс-спектрометрии, электронной, ИК и Н1 ЯМР спектроскопии.
| Схема 5 |
 |
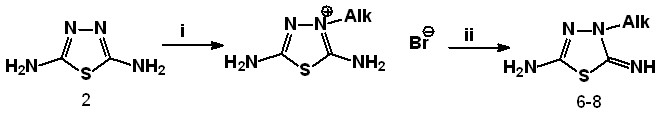 6 – Alk -C5H11, 7 – Alk -C10H21, 8 – Alk -C12H25, i – AlkВг, МеОН, 24 час, кип. ii - NH3 водн. 6 – Alk -C5H11, 7 – Alk -C10H21, 8 – Alk -C12H25, i – AlkВг, МеОН, 24 час, кип. ii - NH3 водн. |
Алкилированные продукты 6-8 растворяются в спиртах, в бензоле, хлороформе, дихлорметане, не растворяются в воде.
Разработка удобных способов получения сделала доступными соединения 2-4, 6-8, которые послужили основой для синтеза новых Мс.
3.2. Синтез тиадиазолсодержащих макрогетероциклических соединений
3.2.1. Синтез макрогетероциклических соединений АВАВ-типа
Из литературы известно, чтопри использовании соединения 2 образуется Мс АВАВАВ-типа, а в случае 4 - АВАВ-типа. Однако объяснения данному факту отсутствуют. Нами проведены квантово-химические расчеты исходных диаминов и дано объяснение влияния строения тиадиазольного цикла на формирование макроциклических систем.
На момент постановки данной работы в литературе имелась единичная публикация по синтезу незамещенного Мс с фрагментами 1,2,4-тиадиазола
АВАВ-типа. Это соединение практически не растворяется в органических растворителях, что затрудняет его очистку и исследование.
Нами впервые получены органорастворимые Мс 13, 14 в соответствии со схемой 6. Контроль за ходом реакции осуществляли с помощью тонкослойной хроматографии и ЭСП. Очистку Мс 13, 14 проводили в аппарате Сокслета, элюируя примеси бензолом, целевой продукт вымывали метанолом. При использовании трет-бутилзамещенного 1,3-дииминоизоиндолина выход соединения 13 оказался почти в два раза выше и составил 68 %, в пересчете на 3,5-диамино-1,2,4-тиадиазол. Полученные соединения охарактеризованы данными ИК, электронной, Н1 ЯМР спектроскопии, масс-спектрометрии, а также данными элементного анализа.
Схема 6. 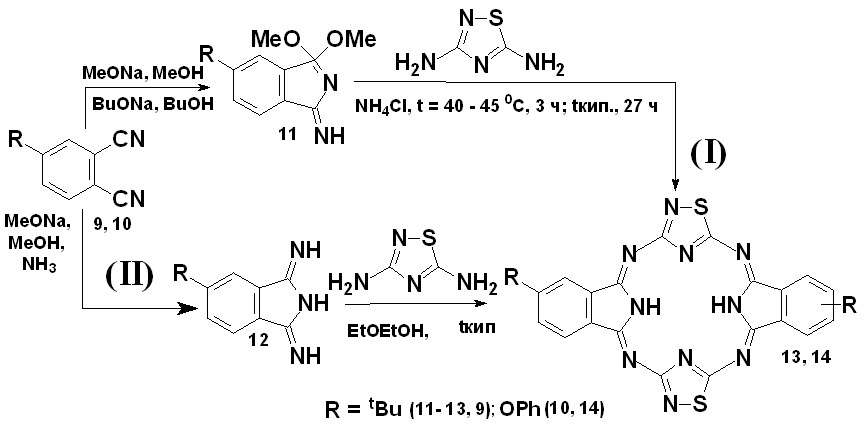 |
В масс-спектре соединения 13 (MALDI-TOF) обнаружен пик молекулярного иона m/e 561 [М-4H]+, что соответствует Мс АВАВ-типа, а его изотопное распределение находится в соответствии с теоретически вычисленным.
В спектре ЯМР 1H соединения 13, измеренном в ДМСО-D6, обнаружены синглет в области 1.27 м.д., характеризующий резонанс протонов алкильных групп и мультиплет в области 7.80 – 7.17 м.д, вызванный резонансом протонов бензольных ядер. Сигнал протонов иминогрупп, наблюдаемый в слабом поле (9.84 м.д.), свидетельствует о неароматическом характере макрокольца. Положение сигналов и сделанное отнесение находятся в соответствии с литературными данными, приведенными для ряда трет-бутилзамещенных Мс.
Соединение 13 растворимо в метаноле, мало растворимо в хлороформе, дихлорметане, ацетоне, очень мало растворимо в бензоле. В электронном спектре поглощения 13 (рис.1) присутствует интенсивная полоса при 423 нм (MeOH), в ДМФА она сдвинута на 5 нм в длинноволновую область (428 нм), что согласуется с литературными данными для незамещенного Мс.
В электронном спектре 14 наблюдается интенсивная полоса поглощения в области 348 нм, присущая -*-электронным переходам в макроциклической системе. В отличие от трет-бутилзамещенного Мс 13 эта полоса сдвинута гипсохромно на 75 нм. Вероятно, введение объемных феноксильных групп приводит к нарушению плоскостности строения молекулы.
За счет введения оксифенильных групп соединение 14 растворимо в ацетоне, ДМФА, метаноле, мало растворимо в хлороформе, не растворимо в воде.
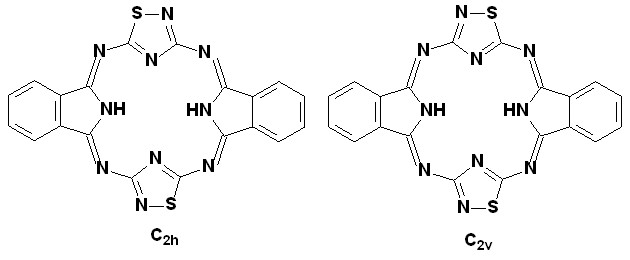 |
| Рис.1. Модели Мс АВАВ-типа точечной группы симметрии С2v и C2h. |
Полученные соединения, по всей вероятности, представляют собой смесь региоизомеров, которую в условиях эксперимента разделить не удалось. Чтобы выявить различия в свойствах двух возможных таутомерных форм нами проведены расчеты электронных спектров поглощения моделей Мс АВАВ-типа точечной группы симметрии С2v и C2h методом DFT B3LYP 6-31G(d,p) с полной оптимизацией геометрических параметров. Полученные данные показывают, что экспериментальный спектр поглощения соединений 13, 14 в большей степени согласуется с расчетным спектром модели молекулы симметрии C2h. По-видимому, в полученных соединениях региоизомер симметрии C2h преобладает.
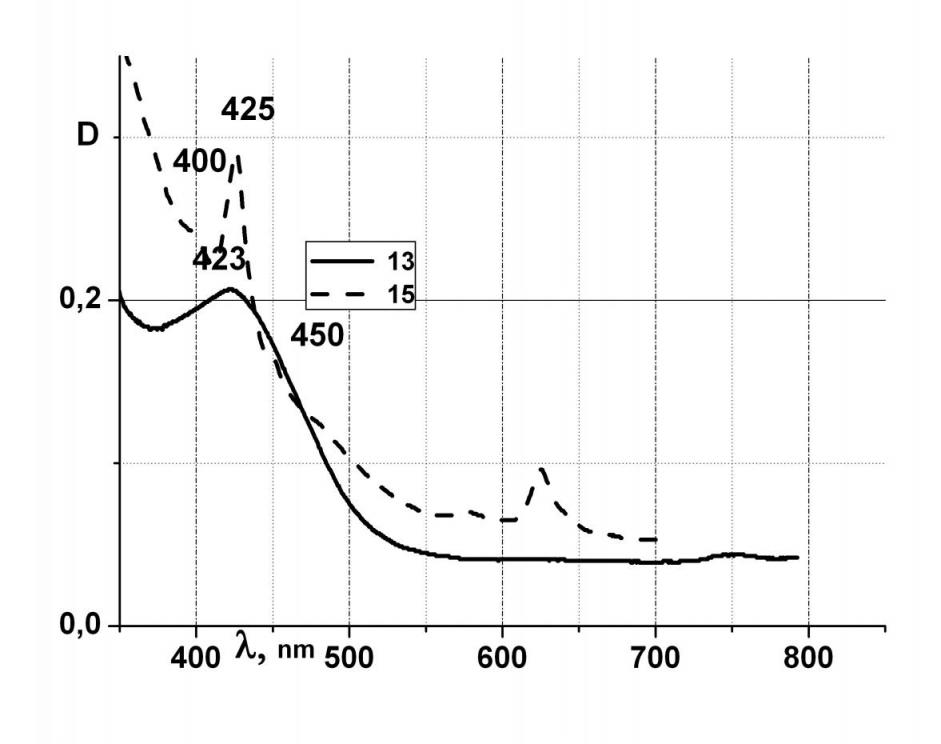 |
| Рис.1. ЭСП в MeOH: 13 - с= 4.17·10-5 моль л-1; 15 - с= 3.38·10-5 моль л-1 |
Взаимодействием Мс 13 с ацетатом никеля
(Ni(OAc)2· 4H20) в бутаноле показана возможность проведения реакции комплексообразования. Подтверждением вступления металла в координационную полость является отсутствие полосы валентных колебаний связи N-H иминогрупп в области 3225 см-1, характерной для Мс. В целом характер спектров металлокомплекса 15 и безметального Мс подобен. В области 2957–2851 см-1 обнаруживаются полосы, отвечающие различным колебаниям связей С-Н в трет-бутильных группах.
В электронном спектре поглощения (рис.1) соединения 13 наряду с интенсивной полосой поглощения в области 425 нм, присущей 15, наблюдается появление полосы при 450. Такое изменение характера спектра находится в соответствии с литературными данными для металлокомплексов незамещенного Мс с фрагментами 1,2,4-тиадиазола.
3.2.2. Синтез макрогетероциклических соединений АВВВ-типа
Первым представителем тиадиазолсодержащих макрогетероциклических соединений АВВВ-типа является трет-бутилзамещенное Мс с 1,3,4-тиадиазольным фрагментом. Обычно соединения такого состава получают взаимодействием ТЗП ВАВ-типа с 1,3-дииминоизоиндолином. Поэтому, первоначально планировалось провести синтез соответствующих трехзвенных продуктов, у которых в тиадиазолиновом фрагменте имелись бы алкильные заместители.
Взаимодействием 5-амино-2-имино-3-пентил-1,3,4-тиадиазолина 6 с
1,1-диметокси-3-иминоизоиндолином 16 в соотношении 1:2 в среде метанола при 40 - 45 0С была получена реакционная масса и при хроматографическом разделении выделены пять ярко-окрашенных зон. После удаления растворителя соединения охарактеризованы данными элементного анализа, масс-спектрометрии, электронной и ИК спектроскопии. Наличие большого количества соединений различной структуры, вероятно, связано с низкой температурой реакции конденсации (т.к. образуются как циклические АВВВ, так и нециклические продукты – АВ, АВА, АВАВАВА) и высокой реакционной способности пентилтиадиазолина 6. При этом, в реакционной массе мы не обнаружили классический трехзвенный продукт ВАВ-типа, но выделили соединение АВА-типа. Нами проведен ряд экспериментов для выбора оптимального температурного режима реакции, что позволило подобрать условия для направленного синтеза Мс АВВВ-типа и трехзвенных продуктов АВА-типа.
Взаимодействием соответствующих 3-N-алкилтиадиазолинов 6-8 с
1,1-диметокси-3-иминоизоиндолином 16 в соотношении 2:1 в метаноле при
40 - 45 0С в течение 15 часов впервые получены трехзвенные продукты
АВА-типа с различными алкильными заместителями 17 - 19 (схема 7). Очистку соединений проводили хроматографированием на колонке, заполненной оксидом алюминия.
Строение полученных соединений установлено на основании данных элементного анализа, масс-спектрометрии, электронной, ИК и Н1 ЯМР спектроскопии, РСА.
Схема 7. 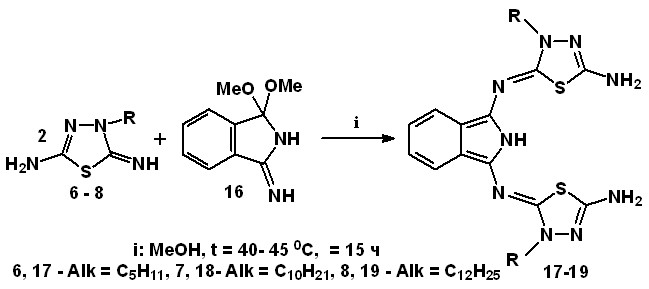 |
Электронные спектры поглощения соединений 17-19 подобны. В них наблюдаются две полосы с максимумами поглощения в области 384 и 493-498 нм.
В спектре 1Н ЯМР соединений 17-19 присутствует ряд сигналов (0.91, 1.28, 1.58, 4.54, 4.7, 5.32 м.д.), характеризующих резонанс протонов алкильной цепочки, и мультиплет 7.59 – 7.89 м.д., вызванный резонансом протонов ароматического кольца. Полученные данные находятся в соответствии с литературными, приведенными для соединений АВА-типа с 1-додецил-1,2,4-триазольным фрагментом.
 | 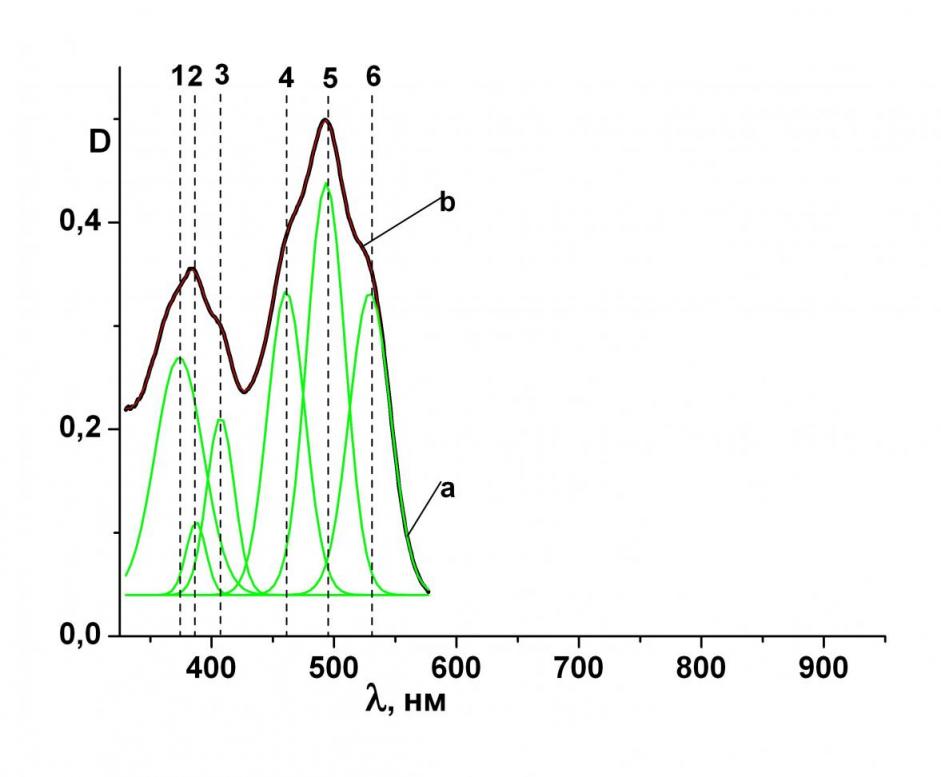 |
| Рис.2. Структура молекулы 17a по данным РСА | Рис.3. Экспериментальный спектр (с= 1.66·10-5 моль·л-1) 17 в MeOH (a), разложенный на функции Гаусса (b) |
Медленным испарением растворителя нам удалось вырастить монокристалл продукта 17a и изучить методом РСА. Фрагмент кристаллической решетки приведен на рис. 2. В структуре полученного кристалла присутствует атом натрия, наличие которого было подтверждено и аналитическими методами исследования. Вступление этого металла в координацию с ТЗП возможно из-за присутствия последнего в
1,1-диметокси-3-иминоизоиндолине, который получают при избытке метилата натрия. Тиадиазолины расположены таким образом, что алкильные группы находятся вблизи изоиндольного фрагмента.
Данные РСА однозначно говорят о том, что алкилирование 2,5-диамино-
-1,3,4-тиадиазола проходит по атому азота N(3) тиадиазольного цикла и подтверждает предлагаемое строение трехзвенного продукта АВА-типа.
Нами выполнены квантово-химические расчеты молекулы 1,3-бис(5-амино-
-2-имино-3-пентил-1,3,4-тиадиазолин)изоиндолина 17 симметрии C2v с помощью пакета программ GAMESS (PC) методом DFT B3LYP 6-31G(d,p) с полной оптимизацией геометрических параметров. Остов молекулы имеет плоскостное строение, атомы серы удалены друг от друга на расстояние 4.301. Алкильные заместители находятся при атомах азота, соседствующих с изоиндольным фрагментом. Рассчитанные длины связей находятся в соответствии с данными РСА.
Экспериментальный спектр поглощения 17, в котором наблюдаются две полосы поглощения с максимумами в области 384 и 495 нм с инфлексиями при 404, 462 и 527 нм, был разложен на гауссовы составляющие (рис. 3) и рассчитан ЭСП с помощью квантово-химических методов. Проведенные расчеты ЭСП 17 коррелируют с экспериментальными данными, что подтверждает предлагаемое строение соединения АВА-типа.
Взаимодействием соответствующих 3-алкил-5-амино-2-имино-1,3,4-тиадиазолинов (6-8) и 1,1-диметокси-3-иминоизоиндолина в соотношении 1:3 в среде метанола при постепенном повышении температуры до кипения реакционной массы в течение 15 часов нами впервые целенаправленно были получены макрогетероциклические соединения 20-22 (схема 8).
Схема 8. 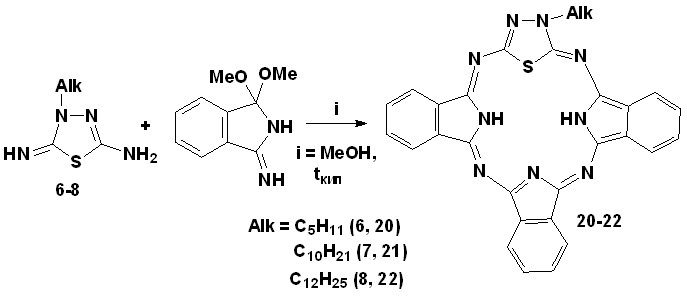 | 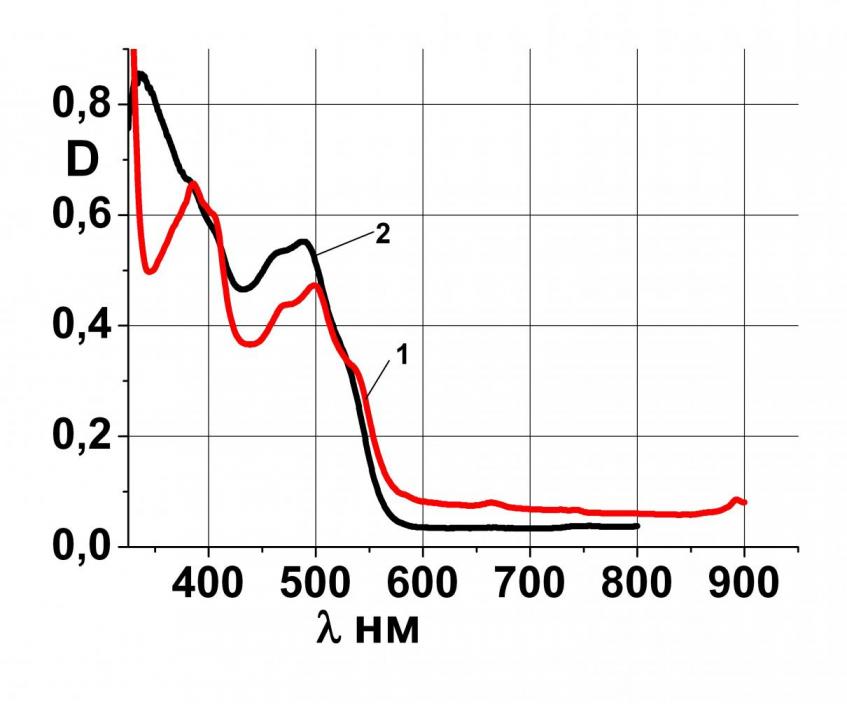 | |
| Рис.4. ЭСП MeOH 1-20 (с = 1,25 10 -4 моль·л-1); 2-22 (с = 1,14 10 -4 моль·л-1). | Рис.5. ЭСП 22 в различных растворителях: 1 - C6H6; 2 – CHCl3; 3 – MeOH; 4 –ДМФА. |
Очистку проводили методом колоночной хроматографии на оксиде алюминия. При этом выход 20-22 после очистки составляет 30 - 35 %. Соединения охарактеризованы данными электронной, ИК, 1Н спектроскопии, масс-спектрометрии, элементного анализа.
В спектре 1Н ЯМР соединений 20-22 присутствует ряд сигналов (0.91, 1.25, 1.90, 4.50 м.д.), характеризующих резонанс протонов алкильной цепочки, и наблюдается мультиплет 7.78 – 7.25 м.д., соответствующий протонам ароматического кольца. Сигнал, вызванный резонансом протонов циклических иминогрупп, расположен в области слабого поля (9.59 м.д.), что свидетельствует о неароматическом характере макрокольца, и находится в соответствии с литературными данными.
| Схема 9 |
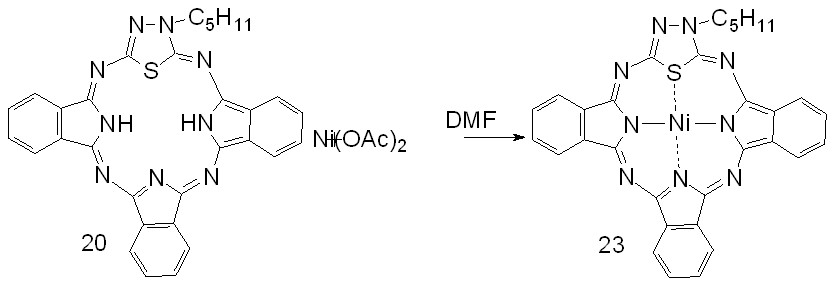 |
В ЭСП (рис.4) имеются интенсивные полосы в видимой части спектра при 499 нм с плечами при 538 нм и 490 нм соответственно для 20 и 22, а также интенсивные полосы поглощения при 386 и 337 нм. С переходом от неполярного растворителя (бензол) к полярному (например, хлороформ) наблюдается гипсохромный сдвиг длинноволновой полосы поглощения с 504 нм до 497 нм, как это показано на рис. 5 для Мс 22. Характер спектров макроциклических лигандов аналогичен спектру трет-бутилзамещенного макрогетероциклического соединения несимметричного строения АВВВ-типа описанного в литературе.
В масс-спектрах соединений 20-22 присутствуют пики молекулярных ионов [М]+, что отвечает соединениям, в состав которых входят один алкилтиадиазолиновый и три изоиндольных фрагмента.
На примере несимметричного Мс с пентильным фрагментом 20 нами показана возможность проведения реакции комплексообразования в осушенном ДМФА
(схема 9). Доказательством вступления металла в координационную полость являются изменения как в ЭСП, так и в ИК спектрах.
Например, в ЭСП 23 интенсивная полоса поглощения в области 386 нм с инфлексией при 404 нм, наблюдаемая для 20, сливается в одну широкую полосу при 394 нм, а в видимой части спектра - при 490 нм, вместо двух полос при 469 и 499 нм для Мс.
3.4. Исследование свойств синтезированыых соединений,
определяющих их возможное практичекое применение
Для поиска перспектив возможного практического применения синтезированных соединений нами были исследованы следующие свойства.
Исследование колористических свойств. Синтезированные нами соединения обладают повышенной растворимостью в органических растворителях и образуют ярко-окрашенные растворы. На примере соединения 17 показана возможность его использования в качестве жирорастворимого красителя для крашения полистирола и парафина. Образцы окрасок имеют равномерное крашение и яркие цвета. Полученные результаты защищены патентом РФ.
Исследование антимикробных свойств. Первые систематические исследования в этой области были начаты на примере ряда трет-бутилзамещенных Мс и их металлокомплексов, содержащих 1,2,4-триазольные и 1,3,4-тиадиазольные фрагменты. Нами продолжено изучение в этой области и проведена оценка противомикробной активности исходных новых 3-N-алкилированных тиадиазолинов, а также ТЗП и Мс, полученных на их основе. Антимикробное воздействие изучалось на стандартном штамме Staphylococcus alb. и Bacillus sp. методом нанесения стандартных дисков. Установлено, что бактериостатическое действие по отношению к исследуемому штамму проявляют лишь тиадиазолины, содержащие децильные и додецильные фрагменты. По отношению к штамму Bacillus sp. все соедиениня не активны. Исследования биологических свойств синтезированных ТЗП и Мс показали отрицательный результат. Таким образом, соединения являются нетоксичными.
Исследование жидкокристаллических свойств. Мезоморфные свойства
3-N-алкилзамещенных тиадиазолинов были исследованы методом оптической поляризационной микроскопии. Установлено, что данные соединения жидкокристаллических свойств не проявляют.
Исследование спектрально-люминесцентных свойств.
Таблица 1
Спектрально-люминесцентные характеристики исследуемых соединений*
| Соединение | Максимум полосы возбуждения max., нм | Максимум полосы люминесценции max., нм | Квантовый выход люминесценции отн., абс. ед.** |
| 17 | 367 | 534 | 0.18 |
| 18 | 367 | 564 | 0.025 |
| 19 | 364 | 566 | 0.026 |
| 20 | 364 | 586 | 0.013 |
| 22 | 358 | 582 | 0.016 |
* Все растворы в метаноле (х.ч.), Т=298К., ** Ошибка определения составляет 10 %.
Люминесцентные свойства довольно широко используются в биологии, медицине и прикладной спектроскопии. По сравнению с порфиринами и фталоцианинами сведения о проявлении люминесцентных свойств Мс и их металлокомплексов в литературе весьма ограничены. Нами проведено исследование спектрально-люминесцентных свойств ТЗП 17-19 и Мс 20, 22.
Впервые для синтезированных ТЗП и Мс обнаружена люминесценция. Показано, что при циклизации соединений происходит снижение квантового выхода. Из всего ряда изученных соединений, 17 имеет самый высокий квантовый выход, что позволяет расценивать его как потенциально практически применимый объект.
Основные результаты и выводы
- Проведено научное и экспериментальное обоснование создания новых и усовершенствование известных способов синтеза исходных соединений: 2-имино-4-тиобиурета, 3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола и его
3-N-алкилзамещенных тиадиазолинов. Разработанные способы получения 2-имино-
-4-тиобиурета, 3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола имеют патентную защиту. - Разработаны новые подходы к созданию компактных методик, базирующихся на сокращении числа стадий и повышении выхода 2-имино-4-тиобиурета,
3,5-диамино-1,2,4-тиадиазола, 2,5-диамино-1,3,4-тиадиазола, которые позволили повысить экологическую безопасность процессов. Предложенные способы получения прошли испытание и получили положительную рекомендацию к применению в лабораторном и полупромышленном синтезе. - Впервые получены 3-N-алкилзамещенные (С5, С10, С12) 1,3,4-тиадиазолины. Изучены влияние природы тиадиазольного цикла на формирование макроциклических систем и реакционная способность новых N-алкилзамещенных тиадиазолинов.
- Взаимодействием 4-трет-бутилфталонитрила или 5-трет-бутил-
-1,3-дииминоизоиндолина и 4-феноксифталонитрила с 3,5-диамино-1,2,4-тиадиазолом синтезированы новые органорастворимые макрогетероциклические соединения АВАВ-типа. - Впервые взаимодействием соответствующих 3-алкил-5-амино-2-имино-1,3,4-тиадиазолинов и 1,1-диметокси-3-иминоизоиндолина осуществлен синтез новых трехзвенных продуктов АВА-типа и Мс АВВВ-типа.
- Изучены особенности электронного и геометрического строения полученных соединений с использованием методов квантовой химии и с применением комплекса физико-химических методов: масс-спектрометрии, электронной, колебательной,
1Н ЯМР спектроскопии, элементного анализа. - С помощью данных РСА установлено, что молекула 1,3-бис(5-амино-2-имино-3-пентил-1,3,4-тиадиазолин)изоиндолина плоская, тиадиазолиновые фрагменты расположены таким образом, что алкильные группы находятся вблизи изоиндольного фрагмента. Доказано, что алкилирование 2,5-диамино-1,3,4-тиадиазола проходит по атому азота N(3) тиадиазольного цикла.
- 1,3-Бис(5-амино-2-имино-3-пентил-1,3,4-тиадиазолин)изоиндолин запатентован в качестве жирорастворимого красителя для крашения полистирола и парафина;
- Впервые для синтезированных ТЗП и Мс обнаружена люминесценция, а также представлены квантовые выходы для этих соединений. Обнаружено, что замыкание цикла уменьшает квантовый выход. Показано, что 1,3-бис(5-амино-2-имино-
-3-пентил-1,3,4-тиадиазолин)изоиндолин имеет самый высокий квантовый выход люминесценции, что позволяет расценивать его как потенциально практически применимый объект. - Синтезировано 13 новых соединений, строение которых установлено с привлечением комплекса физико-химических методов исследования (элементный анализ, ИК-, электронная абсорбционная и Н1 ЯМР - спектроскопия, масс-спектрометрия).
Основное содержание работы изложено в следующих публикациях:
- Патент 2313523 Российская Федерация, МПК6 C07D285/135. Способ получения 2,5-диамино-1,3,4-тиадиазола [Текст] / Меленчук Т.В., Данилова Е.А., Исляйкин М.К., Колесников Н.А.; заявитель Государственное образовательное учреждение высшего профессионального образования «Ивановский государственный химико-технологический университет», патентообладатель Государственное образовательное учреждение высшего профессионального образования «Ивановский государственный химико-технологический университет» – 2006130439/04; заявл. 24.08.2006; опубл. 27.12.2007, Бюл. № 36.
- Патент 2348623 Российская Федерация, МПК6 C07D285/08. Способ получения 3,5-диамино-1,2,4-тиадиазола [Текст] / Меленчук Т.В., Данилова Е.А., Исляйкин М.К., Судьина Е.Е.; заявитель Государственное образовательное учреждение высшего профессионального образования «Ивановский государственный химико-технологический университет», патентообладатель Государственное образовательное учреждение высшего профессионального образования «Ивановский государственный химико-технологический университет» – 2007118789/04; заявл. 21.05.2007; опубл. 10.03.2009, Бюл. № 7.
- Меленчук Т.В., Данилова Е.А., Исляйкин М.К., Судьина Е.Е. Решение о выдаче патента на изобретение «N1, N3-Бис(5-амино-3-пентил-1,3,4-тиадиазол-2-илиден)-2Н-изоиндол-1,3-диамин» по заявке № 2008128228/04 (034752) от 08.06.2009 г.
- Меленчук, Т.В Синтез и свойства трет-бутилзамещенного макрогетероциклического соединения с фрагментами 1,2,4-тиадиазола / Т.В. Меленчук, Е.А. Данилова, А.А. Воронцова, М.К. Исляйкин, Ю.Ю. Енакиева, ЮГ. Горбунова // Изв. вузов. Химия и химическая технология. 2009. Т.52. Вып. 8. С. 113-116.
- Меленчук, Т.В. Диаминотиадиазолы. Синтез и свойства / Т.В. Меленчук, Е.А. Данилова, М.Г. Стряпан, М.К. Исляйкин // Журн. общей химии, 2008, Т. 78, Вып. 3, С.495 -499.
- Меленчук, Т.В. Способ получения 2-имино-4-тиобиурета / Т.В. Меленчук, Е.А. Данилова, В.А. Таланова, М.К. Исляйкин // Изв. вузов. Химия и химическая технология. 2008. Т.51. Вып. 10. С. 125-127.
- Danilova, Е.А. Three-unit products of condensation of alkylsubstituted thiadiazoles with 1,1-dimethoxy-3-iminoisoindoline / E.A. Danilova, T.V. Melenchuk, E.E. Melekhonova, M.A. Tyutina, M.K. Islyaikin // Macroheterocycles. Macroheterocycles. – 2009. –Vol. 2, No. 3. – P. 246 – 250.
- Melenchuk, Т.V. Synthesis and properties of 1,2,4-thiadiazole containning macroheterocyclic compounds of ABAB-type / Tatiana V. Melenchuk, Elena A. Danilova, Mikhail K. Islyaikin // Journal of Porphyrins and Phthalocyanines. 2008.
V.3-6. N12. P.488. - Меленчук, Т.В. Моделирование одного из возможных механизмов образования 3,5-диамино-1,2,4-тиадиазола методом DFT / Т.В. Меленчук, Е.А. Данилова, М.К. Исляйкин // в кн.: Материалы IV-ой школы-семинара молодых ученых «Квантово-химические расчеты: структура и реакционная способность органических и неорганических молекул», г. Иваново, ИГХТУ, 20-22 мая 2009. ISBN 5-9616-0298-2. С. 142-146. 315 с.
- Данилова, Е.А Синтез и свойства металлокомплексов макрогетероциклических соединений с тиадиазольными фрагментами / Е.А. Данилова, Т.В. Меленчук,
О.Н. Трухина, М.К. Исляйкин, Т.Н. Ломова, Е.Е. Суслова // в сборнике тезисов докладов XXIV Международной Чугаевской конференции по координационной химии. Санкт-Петербург. 15-19 июня 2009 г.- С.57. (652 с.). - Меленчук, Т.В. Комплексы макрогетероциклических соединений на основе N-алкил-1,3,4-тиадиазолинов с Cu(II) и Ni(II) / Т.В. Меленчук, Е.А. Данилова,
М.К. Исляйкин // в сборнике тезисов докладов XXIV Международной Чугаевской конференции по координационной химии. Санкт-Петербург. 15-19 июня 2009 г.- С.114. (652 с.). - Данилова, Е.А. Синтез и свойства тиадиазолсодержащих макрогетероциклических соединений / Е.А Данилова, Т.В. Меленчук, О.Н. Трухина, М.К. Исляйкин / в сборнике тезисов докладов 10-ой Международной конференции по физической и координационной химии порфиринов и их аналогов (ICPC-10). Иваново, ИГХТУ. 1-4 июля 2009 г.- С.60. (209 с.).
- Меленчук, Т.В. Макрогетероциклические соединения на основе алкилзамещенных тиадиазолинов. Синтез. Свойства / Т.В. Меленчук, Е.А. Данилова, М.К. Исляйкин / в сборнике тезисов докладов 10-ой Международной конференции по физической и координационной химии порфиринов и их аналогов (ICPC-10). Иваново, ИГХТУ. 1-4 июля 2009 г.- С.68. (209 с.).
- Мелехонова, Е.Е. Алкилзамещенные тиадиазолины и их свойства / Е.Е. Мелехонова, Т.В. Меленчук / Сборник тезисов докладов научных конференций фестиваля студентов, аспирантов и молодых ученых «Молодая наука в классическом университете». Иваново, ИвГУ. 20-24 апреля 2009 г.- С.53.(128 с.)
- Воронцова, А.Н. Синтез и моделирование образования 3,5-диамино-
-1,2,4-тиадиазола / А.Н. Воронцова, Т.В. Меленчук / Сборник тезисов докладов научных конференций фестиваля студентов, аспирантов и молодых ученых «Молодая наука в классическом университете». Иваново, ИвГУ. 20-24 апреля 2009 г.- С.39. (128 с.) - Данилова, Е.А. Способ получения 3,5-диамино-1,2,4-тиадиазола и моделирование механизма его образования / Е.А Данилова, Т.В. Меленчук, А.А. Воронцова,
М.К. Исляйкин / в кн.: «Новые направления в химии гетероциклических соединений». Материалы Международной конференции, Кисловодск, 3-8 мая 2009. – С.307.(500 с.). - Данилова, Е.А. Новые способы получения аминозамещенных 1,3,4- и
1,2,4-тиадиазолов / Е.А. Данилова, Т.В. Меленчук, Е.Е. Мелехонова, М.К. Исляйкин / в кн.: «Новые направления в химии гетероциклических соединений». Материалы Международной конференции, Кисловодск, 3-8 мая 2009. – С.308. (500 с.). - Danilova E.A., Melenchuk N.V., Islyaikin M.K. New approach to the synthesis of diaminothiadiazoles / 23nd International Symposium on the Organic Chemistry of Sulfur. June 29 – July 4, 2008, Moscow, Russia. P. 81-82 (163 p.).
- Меленчук, Т.В. Способы получения прекурсоров и макрогетероциклических соединений на их основе / Шестьдесят первая научно-техническая конференция студентов, магистрантов и аспирантов, посвященная 1000-летию Ярославля, г. Ярославль Апрель, 2008 г. - С.333. (531с.).
- Судьина, Е.Е. 5-Амино-3-пентил-2-имино-1,3,4-тиадиазолин в реакции образования макрогетероциклических соединений / Е.Е. Судьина, Т.В. Меленчук / Сборник тезисов докладов научных конференций фестиваля студентов, аспирантов и молодых ученых «Молодая наука в классическом университете». Иваново, ИвГУ. 21-25 апреля 2008 г.- 8.ч. С.47 - 48. (124 с.).
- Макрогетероциклические соединения на основе 5-амино-3-алкил-2-имино-1,3,4-тиадиазолинов / Е. Е. Судьина, Т.В. Меленчук, Е.А. Данилова // Сборник тезисов докладов материалы VII Региональной студенческой научной конференции с международным участием «Фундаментальные науки - специалисту нового века» Иваново, ИГХТУ. 22-24 апреля 2008 г.- 8.ч. - С.125. (464 с.)
- Меленчук, Т.В. Синтез и свойства металлокомплексов на основе
1,2,4-тиадиазола / Т.В. Меленчук, Е.А. Данилова, М.К. Исляйкин / в кн.: Седьмая школа – конференция молодых ученых стран СНГ по химии порфиринов и родственных соединений (7-12 сентября 2007 г): Программа и тезисы докладов. – Одесса, 2007. – С. 92. - Меленчук, Т.В. Синтез и свойства макогетероциклических соединений на основе диаминотиадиазолов / Т.В. Меленчук, Е.А. Данилова. М.К. Исляйкин / в кн.: Всероссийская научная конференция «Природные макроциклические соединения и их синтетические аналоги» (2-5 апреля 2007 г., г. Сыктывкар): Тезисы докладов. – Сыктывкар, 2007. – С.88.
- Данилова, Е. А. Азолсодержащие макрогетероциклические соединения. Синтез. Структура. Свойства / Е.А. Данилова, Т.В. Меленчук, М.К. Исляйкин / в кн.: Всероссийская научная конференция «Природные макроциклические соединения и их синтетические аналоги» (2-5 апреля 2007 г., г. Сыктывкар): Тезисы докладов. – Сыктывкар, 2007. – С.52.
- Серова, Т.Л. Синтез и свойства макрогетероциклического соединения на основе 1,2,4-тиадиазола, растворимого в неводных средах / Т.Л. Серова, Т.В. Меленчук / в кн.: Тезисы докладов научных конференций фестиваля студентов, аспирантов и молодых ученых, Иваново, 17 -28 апреля 2007 г.: В 8 ч. – Иваново: Иван. гос. ун-т, 2007. – Ч.5. Актуальные проблемы современного естествознания. II конференция Регионального научно-образовательного центра по наноматериалам «Жидкие кристаллы». С.107.
- Меленчук, Т. В. Диаминотиодиазолы–прекурсоры в синтезе макрогетероциклических соединений / Т. В. Меленчук, Е. А. Данилова, М. К. Исляйкин / Тезисы докладов ХХIХ научной сессии Российского семинара по химии порфиринов и их аналогов (26 декабря 2006 г). Иваново, ИГХТУ. 2006. – С. 76.
- Меленчук, Т.В. 2,5-Диамино-1,3,4-тиадиазол, исходное соединение в синтезе тиадиазолопорфириноидов / Т.В. Меленчук, И.Н. Хохрина / в кн. тез. VI Региональная студенческой научной конференции (с международным участием) «Фундаментальные науки – специалисту нового века». 27-27.04.2006. Тезисы докладов. Иваново, 2006. С. 119.
Подписано в печать 21.09.2009 г. Усл. п. л. 1.00 Уч. изд. л. 1.03
Формат 60Ч84 1/16. Тираж 80 экз. Заказ
Государственное образовательное учреждение высшего профессионального
образование «Ивановский государственный химико-технологический
университет». 153000 г. Иваново, пр-т Ф. Энгельса, 7.
Отпечатано на полиграфическом оборудовании кафедры экономики
и финансов ГОУ ВПО «ИГХТУ»

