Координационные соединения солей металлов viii b группы с протонированным карбамидом
УДК 541.123. 31 : 547.55.42 На правах рукописи
АБДУЛЛИНА ГУЛЬНАРА ГОСМАНОВНА
Координационные соединения солей металлов VIII B группы
с протонированным карбамидом
02.00.01 – Неорганическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
.
Республика Казахстан
Караганда, 2009
Диссертация выполнена на кафедре химии и химических технологий биолого – химического факультета Павлодарского государственного университета им. С.Торайгырова.
| Научные руководители | доктор химических наук, профессор Р.Ш.Еркасов |
| кандидат химических наук, доцент Р.Г. Рыскалиева | |
| Официальные оппоненты: | доктор химических наук, профессор М.Б. Баткибекова |
| доктор химических наук Г.К. Сугурбекова | |
| Ведущая организация | Южно-Казахстанский государственный университет им. М. Ауезова |
Защита состоится «2» декабря 2009 г. в 1100 часов на заседании диссертационного совета ОД 14.07.01. при Карагандинском государственном университете им. Е.А. Букетова по адресу: 100028, г. Караганда, ул. Университетская, 28, химический факультет, актовый зал.
С диссертацией можно ознакомиться в библиотеке КарГУ им. Е.А. Букетова по адресу: г. Караганда, ул. Университетская, 28.
Автореферат разослан «____» октября 2009г.
Ученый секретарь
диссертационного совета ОД 14.07.01
д.х.н.,профессор Ш.К.Амерханова
ВВЕДЕНИЕ
Общая характеристика работы. Диссертационная работа посвящена разработке научных основ образования в растворах координационных соединений солей металлов VIII B группы с протонированным карбамидом, установлению закономерностей взаимодействия в системах соль железа (III) [кобальта (II), никеля (II)] – карбамид – неорганическая кислота – вода, синтезу образуемых в них соединений, определению строения и физико – химических характеристик новых тройных соединений.
Актуальность темы. Одной из важнейших проблем современной химии является исследование условий образования и свойств новых соединений, имеющих научно-практическое значение. Особую актуальность при этом имеют координационные соединения с органическими лигандами, а среди них продукты взаимодействия солей биометаллов с амидам в кислых средах. Они весьма перспективны в качестве органических и аналитических реагентов, исходных продуктов в химической промышленности, кроме того важна их роль в различных биохимических процессах. Помимо биологических и практических аспектов интерес к ним определен и тем, что они являются хорошими объектами для фундаментальных исследований. От соединений амидов с солями биометаллов и неорганическими кислотами следует ожидать комбинирование свойств исходных компонентов с вновь приобретенными. В настоящее время они изучены недостаточно полно.
Степень разработанности темы. В научной литературе имеется небольшое количество работ посвященных описанию способов получения координационных соединений, содержащих одновременно соль металла, амид и неорганическую кислоту. Исследованию синтеза разнолигандных координационных соединений солей биометаллов, карбамида (ацетамида) и неорганических кислот, разработке способов получения солей различных стехиометрических составов, нахождению закономерностей их образования, установлению перспективных областей практического применения некоторых новых соединений посвящены работы сотрудников кафедры неорганической химии КазНУ им. аль-Фараби.
Целью работы являлось изучение процессов взаимодействия в четырехкомпонентных системах соль металла VIII В группы – карбамид – неорганическая кислота – вода методом растворимости при 25 °С и физико-химическое исследование свойств образующихся в них новых соединений.
В задачу исследования входило: изучение растворимости в системах соль ![]() ,
, ![]() ,
, ![]()
![]() – неорганическая кислота –
– неорганическая кислота – ![]() –
– ![]() ; установление составов образующихся соединений; определение концентрационных границ их кристаллизации, установление закономерностей взаимного влияния исходных компонентов; идентификация синтезированных соединений химическими, физическими и физико-химическими методами исследования; установление строения новых синтезированных соединений.
; установление составов образующихся соединений; определение концентрационных границ их кристаллизации, установление закономерностей взаимного влияния исходных компонентов; идентификация синтезированных соединений химическими, физическими и физико-химическими методами исследования; установление строения новых синтезированных соединений.
Объектами исследования являются соединения нитрата железа (III), бромидов (иодидов) кобальта (II) [никеля(II)], перхлората кобальта (II) с протонированным карбамидом.
Предметом исследования являются растворимость в четырехкомпонентных системах соль железа (III) [кобальта (II), никеля (II)] – неорганическая кислота – карбамид – вода при 25 °С, закономерности образования, строение и свойства новых координационных соединений, перспективы их применения.
Методы исследования. В работе использованы следующие физико – химические методы исследования: метод растворимости, пикнометрия, титриметрия, метод Къельдаля, рентгенофазовый анализ, ИК – спектроскопия, квантово – химические расчеты.
Научная новизна исследования. В работе впервые: изучена растворимость в шести четырехкомпонентных системах, содержащих нитрат железа (III), перхлорат кобальта (II), бромид (иодид) кобальта (II) [никеля (II)], их соединения с карбамидом, а также соединения карбамида с азотной, хлорной, бромоводородной и иодоводородной кислотами в растворах соответствующих кислот и солей, содержащих карбамид при 25 °С, установлено образования 20 новых координационных соединений, содержащих в своем составе одновременно соль металла, карбамид, кислоту, определен характер их растворения, разработаны оптимальные условия их синтеза, проведена их идентификация методами химического, рентгенофазового анализов определением физико-химических свойств, предложено строение новых соединений, а для ряда из них найдены геометрические, энергетические и электронные параметры.
Теоретической и практической значимостью является то, что результаты растворимости, а также физико-химические свойства и строение впервые синтезированных соединений относятся к справочному материалу. Найденные закономерности взаимодействия компонентов вносят вклад в развитие теории комплексообразования, теорию и практику физико – химического анализа многокомпонентных систем. Результаты исследования используются в учебном процессе на кафедре химии и химической технологии ПГУ им. С. Торайгырова, ЕНУ им. Л.Н. Гумилева при чтении специальных курсов лекций «Химия координационных соединений» и «Физико-химический анализ многокомпонентных систем». Некоторые полученные новые соединения могут быть применены в сельском хозяйстве в качестве удобрений для повышения урожайности растений.
Достоверность и обоснованность полученных данных подтверждены результатами неоднократного повторения экспериментов. Работа проводилась с использованием классических и современных физических и физико – химических методов анализа. Достоверность результатов подтверждается согласованностью результатов ИК – спектроскопических исследований соединений с квантово – химическим расчетом строения соединений.
Связь темы с планом научно-исследовательских работ. Работа выполнялась в соответствии с планом научно – исследовательских работ, проводимых на кафедре химии и химической технологии ПГУ им. С. Торайгырова по темам: «Разработка основ получения координационных соединений s- и d- металлов с протонированными амидами, обладающими физиологической активностью», которая является продолжением темы, ранее проводимой по программе фундаментальных исследований МОН Республики Казахстан «Исследование физико – химических свойств веществ и материалов из органического и неорганического сырья Казахстана» (номера регистрации 0197 РК 00549 и 0101 РК 010012).
Основные положения, выносимые на защиту:
- растворимость нитрата железа (III), перхлората кобальта (II), бромидов (иодидов) кобальта (II) [никеля (II)], их соединений с карбамидом, а также соединений карбамида с азотной, бромоводородной, иодоводородной, хлорной кислотами в растворах соответствующих кислот и солей, содержащих карбамид при 25 °С;
- закономерности процессов комплексообразования в системах нитрат железа (III), иодид (бромид) никеля (II) [кобальта (II)] и перхлорат кобальта (II) – карбамид – азотная (иодоводородная, бромовородная, хлорная) кислота – вода при 25 °С;
- методики синтеза 20 новых координационных соединений солей железа (III), кобальта (II) и никеля (II) с протонированным карбамидом и результаты идентификации их методами химического, рентгенофазового анализов, физико-химические свойства 20 синтезированных соединений составов:
- предполагаемое строение и геометрические параметры ряда координационных соединений.
Апробация работы. Материалы диссертации докладывались на Международных научно – практических конференциях: «Валихановские чтения – 13» (Кокшетау, 2008), «Научные дни – 2008» (Днепропетровск, София, Белгород - 2008), «Nowoczesnych naukowych osiagniec – 2008» (Przemysl – 2008), «Vda: teorie a praxe – 2008» (Прага – 2008), «VІ Беремжановский съезд по химии и химической технологии» (Караганда – 2008).
Личный вклад автора заключается в планировании и выполнении экспериментальной части диссертационной работы, обобщении результатов проведенных исследований.
Публикации. По материалам диссертации опубликовано 5 статей в научных журналах, рекомендованных Комитетом по контролю в сфере образования и науки МОН РК, и 6 трудов в материалах Международных научных конференций.
Структура и объем работы. Диссертационная работа изложена на 109 страницах машинописного текста, состоит из введения, четырех разделов, заключения, списка использованных источников и приложения. Работа содержит 12 рисунков и 15 таблиц. Список использованных источников составляет 146 наименований.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении показаны актуальность и новизна темы, обозначена цель исследования.
В первой главе обобщены литературные данные по физико-химическим свойствам исходных компонентов: (карбамида, солей железа (III), кобальта (II), никеля (II), неорганических кислот), процессам взаимодействия карбамида с неорганическими кислотами и солями железа, кобальта и никеля.
Во второй главе приведены методика эксперимента, результаты изучения растворимости при 25 °С в системах нитрат железа – карбамид – кислота – вода, соль кобальта – карбамид – кислота – вода, соль никеля – карбамид – кислота – вода, а также обсуждение ряда закономерностей взаимодействия в них.
Растворимость в системах соль железа (кобальта, никеля) – карбамид – вода при 25 С
В качестве основного метода изучения процессов и продуктов взаимодействия солей железа, кобальта и никеля с протонированным карбамидом был использован метод растворимости, который позволил установить области кристаллизации исходных компонентов, двойных и тройных соединений, образующихся в изученных системах, характер растворения их в воде, особенности изменения растворимости амидкислот и соединений солей железа (кобальта, никеля) с протонированным карбамидом. Данная методика заключалась в следующем: в эвтонические составы составляющих трехкомпонентных систем: карбамид – кислота – вода и карбамид – соль – вода, прибавляли определенные всевозрастающие количества четвертого компонента до появления устойчивой твердой фазы. Контроль за твердой фазой проводили как химическим, так и кристаллооптическим анализом.
Полученные результаты по растворимости изображены в виде центральной проекции пространственной изотермы. Точки системы на проекции диаграммы отражают только солевой состав системы. Для учета содержания воды в четырехкомпонентной системе рассчитаны значения водного числа, которое равно количеству моль воды необходимой для растворения 1 моль суммы солей, находящихся в растворе.
В качестве примера на рисунке 1 приведена центральная проекция растворимости системы ![]() . Ветвь изотермы, включающая точки 1 – 6, соответствует выделению из насыщенных растворов смеси
. Ветвь изотермы, включающая точки 1 – 6, соответствует выделению из насыщенных растворов смеси ![]() и
и ![]() . В точке 6 начинается образование нового соединения
. В точке 6 начинается образование нового соединения ![]() . Прибавление в эвтонический раствор системы карбамид – иодоводородная кислота – вода, иодида никеля приводит к кристаллизации смеси
. Прибавление в эвтонический раствор системы карбамид – иодоводородная кислота – вода, иодида никеля приводит к кристаллизации смеси ![]() и
и ![]() , приводящей к образованию нового соединения (точка 10). Ветвь изотермы, соответствующая точкам 10, 15 – 18, отвечает выделению из растворов соединения
, приводящей к образованию нового соединения (точка 10). Ветвь изотермы, соответствующая точкам 10, 15 – 18, отвечает выделению из растворов соединения ![]() . Точки изотермы 18 – 23 отвечает выделению
. Точки изотермы 18 – 23 отвечает выделению ![]() и
и ![]() . Ветвь изотермы, (точки 18, 24 – 28) соответствует образованию соединения
. Ветвь изотермы, (точки 18, 24 – 28) соответствует образованию соединения ![]() . Точки системы 28 – 33 отвечают кристаллизации в равновесную твердую фазу смеси
. Точки системы 28 – 33 отвечают кристаллизации в равновесную твердую фазу смеси ![]() и
и ![]() . В точках системы 28, 34 – 40 происходит кристаллизация
. В точках системы 28, 34 – 40 происходит кристаллизация ![]() . Прибавление в эвтонический раствор системы иодид никеля – карбамид – вода, иодоводородной кислоты (точки изотермы 6, 41 – 45) приводит к кристаллизации
. Прибавление в эвтонический раствор системы иодид никеля – карбамид – вода, иодоводородной кислоты (точки изотермы 6, 41 – 45) приводит к кристаллизации ![]() . Ветвь изотермы, соответствующая точкам 46 – 50, отвечает выделению из растворов декакарбамидиодида никеля и гексакарбамидиодида никеля. Точки системы 18, 45, 51 – 54 отвечают выделению новой тройной соли
. Ветвь изотермы, соответствующая точкам 46 – 50, отвечает выделению из растворов декакарбамидиодида никеля и гексакарбамидиодида никеля. Точки системы 18, 45, 51 – 54 отвечают выделению новой тройной соли ![]() . Точки 45, 55 – 59 отвечает насыщению соединения гексакарбамидиодида никеля. Ветвь изотермы, включающая точки 59 – 65 отвечает кристаллизации из насыщенных растворов эвтонической смеси гексакарбамидиодида никеля и тетракарбамидиодида никеля. Точки системы 28, 59, 66 – 69 отвечают выделению нового тройного соединения
. Точки 45, 55 – 59 отвечает насыщению соединения гексакарбамидиодида никеля. Ветвь изотермы, включающая точки 59 – 65 отвечает кристаллизации из насыщенных растворов эвтонической смеси гексакарбамидиодида никеля и тетракарбамидиодида никеля. Точки системы 28, 59, 66 – 69 отвечают выделению нового тройного соединения ![]() . В точках изотермы 59, 70 – 74 происходит кристаллизация
. В точках изотермы 59, 70 – 74 происходит кристаллизация ![]() . Ветвь изотермы соответствующая точкам 74 – 83 отвечает кристаллизации из насыщенных растворов тетракарбамидиодида никеля и гексагидратиодида никеля. Точки изотермы 74, 84 – 90 соответствуют выделению в твердую фазу
. Ветвь изотермы соответствующая точкам 74 – 83 отвечает кристаллизации из насыщенных растворов тетракарбамидиодида никеля и гексагидратиодида никеля. Точки изотермы 74, 84 – 90 соответствуют выделению в твердую фазу ![]() .
.
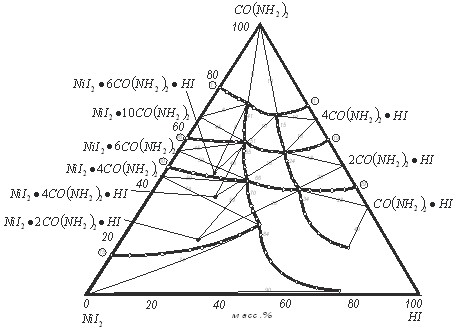
Рисунок 1 – Центральная проекция изотермы растворимости в системе ![]() при 25 °С
при 25 °С
При изучении растворимости в системе ![]() установлены области кристаллизации соединений эвтонических составов составляющих трехкомпонентных системах:
установлены области кристаллизации соединений эвтонических составов составляющих трехкомпонентных системах: ![]() и
и ![]() , концентрационные пределы образования в твердой фазе ранее известных двойных соединений и новых тройных соединений составов:
, концентрационные пределы образования в твердой фазе ранее известных двойных соединений и новых тройных соединений составов: ![]() ,
, ![]() ,
,![]()
В четырехкомпонентной системе ![]() определены области кристаллизации соединений эвтонических составов составляющих трехкомпонентных систем соль кобальта – карбамид – вода и карбамид –кислота – вода и двойных соединений образующихся в них
определены области кристаллизации соединений эвтонических составов составляющих трехкомпонентных систем соль кобальта – карбамид – вода и карбамид –кислота – вода и двойных соединений образующихся в них ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() , а также области выделения в твердую фазу новых соединений составов
, а также области выделения в твердую фазу новых соединений составов ![]() ,
,![]() ,
, ![]() и
и ![]() .
.
В системе ![]() установлены концентрационные границы кристаллизации эвтонических составов трехкомпонентных систем
установлены концентрационные границы кристаллизации эвтонических составов трехкомпонентных систем ![]() ,
, ![]() и двойных соединений образующихся в них
и двойных соединений образующихся в них ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() и
и ![]() . В этой системе определены также области выделения в твердую фазу новых соединений, в составе которых содержатся все три исходных компонента:
. В этой системе определены также области выделения в твердую фазу новых соединений, в составе которых содержатся все три исходных компонента: ![]() ,
, ![]() и
и ![]() .
.
При изучении растворимости в системе ![]() найдены ветви кристаллизации исходных эвтонических составов и двойных соединений
найдены ветви кристаллизации исходных эвтонических составов и двойных соединений ![]() ,
, ![]() ,
, ![]() и
и ![]() образующихся в составляющих трехкомпонентных системах
образующихся в составляющих трехкомпонентных системах ![]() и
и ![]() , а также концентрационные границы кристаллизации новых соединений составов
, а также концентрационные границы кристаллизации новых соединений составов ![]() ,
,![]() и
и ![]() .
.
Изучение растворимости в системе ![]() установило ветви кристаллизации исходных эвтонических составов и двойных соединений:
установило ветви кристаллизации исходных эвтонических составов и двойных соединений: ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() образующихся в составляющих трехкомпонентных системах
образующихся в составляющих трехкомпонентных системах ![]() и
и ![]() . В изученной системе найдены также концентрационные границы образования новых соединений составов
. В изученной системе найдены также концентрационные границы образования новых соединений составов ![]() ,
, ![]() и
и ![]() .
.
Основные закономерности взаимодействия солей железа (кобальта, никеля) с карбамидом в растворах кислот
Кислотно-основное взаимодействие, приводящие к кристаллизации новых координационных соединений, в составе которых присутствуют три исходных компонента, возможно в результате протекания следующих реакций (в качестве примера рассмотрим реакции протекающие в системе ![]() ):
):
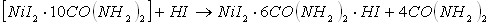
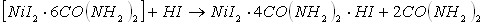

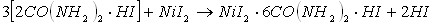
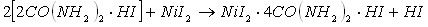
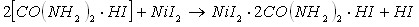
Из приведенных уравнений реакций следует, что образование тройных соединений иодида никеля с протонированным карбамидом, сопровождается вытеснением из состава двойных соединений свободных молекул кислот или карбамида.
При изучении растворимости в системах соль железа (кобальта, никеля) – карбамид – кислота – вода установлено образование ранее известных двойных соединений и 20 новых тройных соединений.
В изученных четырехкомпонентных системах установлены следующие закономерности взаимного влияния на растворимость компонентов и их влияния на растворимость кристализующихся из насыщенных растворов двойных и тройных соединений:
- введение солей металлов в эвтонические растворы приводит к эффекту всаливания солей металлов на растворимость эвтонической смеси, приводящее к образованию тройной соли.
- рост количества кислот оказывает эффект высаливания на растворимость эвтонических смесей и только бромид и перхлорат кобальта оказывают незначительное всаливающее действие, о чем свидетельствуют вычисленные значения водного числа.
- рост содержания неорганических кислот в растворах оказывают всаливающее влияние как на растворимость двойных соединений карбамида с солями металлов, так и на растворимость новых координационных соединений. С ростом концентрации кислот в растворе растворимость исходных солей уменьшается.
- рост количества солей металлов оказывают преимущественно всаливающее действие на растворимость карбамидкислот, исключение составляет действие нитрата железа на растворимость нитрата карбамида. Причиной этого являются очень низкая растворимость нитрата карбамида.
В третьей главе изложены методики синтеза и некоторые физико – химические свойства координационных соединений солей железа, кобальта и никеля с протонированным карбамидом. Идентификация полученных соединений проводилась методами химического, рентгенофазового, ИК – спектроскопического анализов, определением температур плавления, растворимости в органических растворителях, плотности.
Синтез и некоторые физико-химические характеристики координационных соединений солей VІІІ В группы с протонированным карбамидом
Выделенные в кристаллическом состоянии соединения солей железа (кобальта, никеля) с протонированным карбамидом идентифицированы методами химического и рентгенофазового анализа, определением температур плавления (разложения), плотности, растворимости в органических растворителях (таблица 1). Из таблицы видно, что соединения солей железа, кобальта и никеля с протонированным карбамидом в основном разлагаются при температурах значительно ниже температур плавления исходных солей, но выше температуры плавления карбамида. Пикнометрические плотности тройных соединений имеют меньшие значения, чем плотности исходных солей железа, кобальта и никеля, но большие чем плотность карбамида. Плотность синтезированных соединений уменьшается с увеличением массовой доли карбамида в их составе. Полученные координационные соединения нерастворимы в бензоле и толуоле, плохо растворимы в диэтиловом эфире, хорошо растворимы в ацетоне и этаноле.
Таблица 1 – Физико – химические характеристики соединений нитрата железа, перхлората кобальта, бромида и иодида кобальта (никеля) с протонированным карбамидом
| Соединение | d, кг·м-3 | t°пл (разл), °С | Растворимость, г / 100 г растворителя | ||||
| бен-зол | толуол | этанол | ацетон | Диэтило-вый эфир | |||
| 1690 | 185 | 0,02 | н.р.* | 15,10 | 16,41 | 7,25 | |
| 1535 | 178 | н.р. | н.р. | 13,19 | 12,62 | 5,19 | |
| 1420 | (160) | н.р. | н.р. | 18,45 | 14,19 | 4,38 | |
| 2810 | 190 | н.р. | н.р. | 23,72 | 14,00 | 6,22 | |
| 2415 | 173 | н.р. | н.р. | 20,15 | 12,49 | 5,19 | |
| 2105 | (175) | н.р. | н.р. | 14,18 | 13,55 | 8,49 | |
| 1895 | (150) | 0,02 | н.р. | 12,46 | 10,64 | 7,20 | |
| 3210 | 196 | н.р. | н.р. | 14,19 | 9,17 | 5,82 | |
| 2620 | (183) | н.р. | н.р. | 20,02 | 16,46 | 6,19 | |
| 2235 | (170) | 0,02 | н.р. | 25,46 | 18,53 | 7,18 | |
| 2905 | 192 | н.р. | н.р. | 18,19 | 12,92 | 4,93 | |
| 2740 | 175 | н.р. | н.р. | 16,14 | 11,29 | 7,66 | |
| 2265 | (150) | н.р. | н.р. | 21,07 | 13,75 | 4,42 | |
| 3200 | 184 | н.р. | н.р. | 18,10 | 12,67 | 8,33 | |
| 2895 | 163 | н.р. | н.р. | 23,15 | 16,41 | 6,75 | |
| 2450 | (150) | н.р. | н.р. | 15,16 | 10,85 | 7,12 | |
| 2185 | (140) | 0,02 | н.р. | 17,29 | 14,30 | 5,77 | |
| 3010 | (180) | н.р. | н.р. | 10,20 | 11,74 | 3,82 | |
| 2520 | (154) | н.р. | н.р. | 8,94 | 10,15 | 5,14 | |
| 2235 | (130) | н.р. | н.р. | 9,17 | 7,48 | 4,18 | |
н.р.* – нерастворим
Индивидуальность синтезированных соединений установлена химическими методами и подтверждена ренгенофазовым анализом. Закономерностей в смещении наиболее интенсивных пиков у координационных соединений по сравнению с исходными, нет.
Инфракрасные спектры
С целью установления строения и места координации в молекулах карбамида и соли железа (III) [кобальта (II), никеля (II)] были сняты ИК – спектры.
Частоты валентных колебаний карбонильной группы в спектрах соединений смещены в низкочастотную область на 30 – 40 см-1, а частоты валентных колебаний связи С – N в спектрах смещены в высокочастотную область на 20 – 30 см-1, что свидетельствует об образовании связи через карбонильный кислород. Появление в ИК – спектрах соединений полос поглощения в областях 3380 – 3390 см-1 и 1705 – 1715 см-1 указывает на О – протонирование, так как эти частоты поглощения относятся к валентным и деформационным колебаниям ОН – группы.
Частоты валентных антисимметричных колебаний NH-связи соединений солей железа (кобальта, никеля) с протонированным карбамидом на 15 – 20 см-1 смещаются в низкочастотную область. Полосы валентных симметричных колебаний NH - связи в меньшей степени смещены в низкочастотную область на 5 – 15 см-1. Такие изменения указывают на участие аминогруппы карбамида в образовании новых Н – связей NH…Х, где Х – анион кислоты.
Полосы поглощения деформационных колебаний NН2 – группы карбамида при 1610 см-1 практически сохраняют положение, что также может быть результатом участия С = О связи в образовании координационного соединения.
Таким образом, ИК – спектроскопические исследования соединений солей железа (III), кобальта (II) и никеля (II) с протонированным карбамидом показали, что они относятся преимущественно к разнолигандным координационным соединениям, содержащими во внутренней сфере как свободный карбамид, так и протонированный карбамид наряду с анионами соответствующих кислот.
В четвертой главе изложены методика и результаты квантово – химических расчетов комплекса нитрата железа с протонированным карбамидом.
Квантово – химическое исследование структуры комплекса железа с протонированным карбамидом
Особое значение для характеристики новых соединений имеет устойчивость химических соединений, которая определяется величиной энтальпий образования ![]() .
.
Квантово-химическим полуэмпирическим методом РМ3 рассчитаны энтальпии образования комплексных соединений нитрата железа с карбамидом и протонированным карбамидом. Анализ величин ![]() , показывает что, устойчивость исследованных протонированных соединений карбамида и комплексов нитрата железа с карбамидом возрастает в ряду:
, показывает что, устойчивость исследованных протонированных соединений карбамида и комплексов нитрата железа с карбамидом возрастает в ряду:
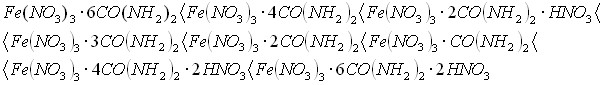
Геометрические параметры молекул карбамида, нитрата карбамида и карбамидных комплексов железа, полученные квантово-химическими расчетами, позволяют найти их пространственноое строения (рисунок 2), что важно для объективной оценки реакционной способности соединений (таблица 3).
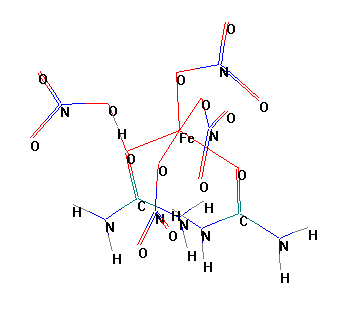
Рисунок 2 – Строение соединений Fe(NO3)3 ·2CO(NH2)2 ·HNO3
Протонирование приводит к увеличению длины связи С=О: она равна в CO(NH2)2 = 0,1227 нм, CO(NH2)2 ·HNO3 =0,1237 нм, Fe(NO3)3 · 2CO(NH2)2 = 0,1285 нм, и Fe(NO3)3 · 2CO(NH2)2 · HNO3 = 0,1360 нм. Таким образом, протонирование азотной кислотой в большей степени влияет на длину связи С=О в карбамидном комплексе железа Fe(NO3)3 · 2CO(NH2)2 · HNO3. Длина связи С–N в молекуле Fe(NO3)3 · 2CO(NH2)2 значительно меньше по сравнению с данным межатомным расстоянием в молекуле карбамида.
Таблица 3 – Геометрические параметры молекул карбамида, нитрата карбамида и карбамидных комплексов железа
| Соединение Параметр | CO(NH2)2 | CO(NH2)2 ·HNO3 | Fe(NO3)3·2CO(NH2)2 | Fe(NO3)3 ·2CO(NH2)2 ·HNO3 |
| r C–O, нм | 0,1227 | 0,1237 | 0,1285 | 0,1360 |
| r C–N, нм | 0,1430 0,1431 | 0,1419 0,1421 | 0,1307 0,1300 0,1405 0,1388 | 0,1418 0,1416 0,1426 0,1309 |
| r N –H, нм | 0,0996 0,0996 0,0996 0,0996 | 0,0996 0,0995 0,0997 0,0995 | 0,0996 0,1011 0,0987 0,0992 | 0,0996 0,0995 0,0996 0,1016 |
| r O–HNO3, нм | - | 0,1754 | - | 0,0994 |
| 120,50 | 112,52 | 107,13 117,52 | 118,82 119,55 136,42 109,91 | |
| - | - | 84,70 105,77 | 115,54 118,30 |
Из сравнения длины связи С–N в молекулах Fe(NO3)3 · 2CO(NH2)2 и Fe(NO3)3 · 2CO(NH2)2 · HNO3 видно, что в результате взаимодействия азотной кислоты с атомом карбонильного кислорода карбамида, данное межатомное расстояние увеличивается. При этом, длина одной связи С–N, а именно в протонированном карбамиде увеличилась незначительно, она равна 0,1309 нм. Это можно объяснить взаимным влиянием пространственного и электронного строения расположенных вокруг центрального атома лигандов. Практически одинаковыми во всех исследуемых соединениях остаются длины связей N–H в аминогруппах амидного фрагмента -CONH2.
Длины связи О…НNO3 в молекулах CO(NH2)2·HNO3 и Fe(NO3)3 · 2CO(NH2)2 · HNO3 равны 0,1754 нм и 0,0994 нм соответственно, что вероятно связано с различной природой образующихся связей в комплексах при протонизации.
В результате происходящего протонирования атома карбонильного кислорода происходит изменение величин валентных углов. Протонирование приводит к уменьшению угла ![]() N–C–O и к увеличению угла
N–C–O и к увеличению угла ![]() Fe–O–C.
Fe–O–C.
Полученные квантово-химические расчеты дополняют ИК-спектроскопические данные и хорошо согласуются с ними, что значительно увеличивает правомерность следующих предполагаемых для синтезированных соединений строений:
| где А* – |
ЗАКЛЮЧЕНИЕ
1. Из данных полученных изотерм растворимости четырехкомпонентных систем: соль ![]() ,
, ![]() ,
, ![]()
![]() – неорганическая кислота –
– неорганическая кислота – ![]() –
– ![]() при 25 °С установлено образование двойных соединений, существование которых было ранее установлено при изучении растворимости составляющих трехкомпонентных систем, а также 20 новых координационных соединений, содержащих в своем составе одновременно три исходных компонента.
при 25 °С установлено образование двойных соединений, существование которых было ранее установлено при изучении растворимости составляющих трехкомпонентных систем, а также 20 новых координационных соединений, содержащих в своем составе одновременно три исходных компонента.
2. Из анализа изотерм растворимости следует, что
а) растворимость тройных соединений увеличивается с ростом содержания кислот в растворе, т.е. проявляется эффект всаливания, о чем свидетельствует уменьшение значений водного числа в этих растворах с ростом концентрации кислот;
б) происходит кристаллизация эвтонических составов и двойных координационных соединений, существование которых было установлено при изучении растворимости в составляющих трехкомпонентных системах соль железа (кобальта, никеля) – карбамид – вода, карбамид – кислота – вода;
в) рост количества кислот оказывают всаливающее действие на растворимость соединений солей металлов с карбамидом;
г) введение солей железа (кобальта, никеля) оказывает всаливающее действие на растворимость амидкислот;
д) растворимость эвтонических составов систем соль металла – карбамид – вода при добавлении кислоты возрастает;
е) растворимость эвтонических составов систем карбамид – кислота – вода в большинстве случаев уменьшается с ростом концентрации исходной соли металла;
ж) рост концентрации кислот в растворах, находящихся в равновесии с исходной солью приводит к снижению их растворимости.
3. На основании изотерм растворимости четырехкомпонентных систем разработаны методика синтеза 20 новых координационных соединений. Их индивидуальность установлена методами химического и рентгенофазового анализов.
4. Идентификация впервые полученных соединений проведена определением температур плавления (разложения), пикнометрической плотности, растворимости в органических растворителях.
5. Испытания ряда синтезированных соединений показали, что они способствуют повышению урожайности растений на 20 – 40% и не оказывают токсического влияния на качество урожая.
6. Результаты ИК – спектроскопического исследования указывают на смещение валентных колебаний С = О связи в низкочастотную область, С – N связи в высокочастотную область, а также на появление полос поглощения ОН – групп, что свидетельствует о О – протонировании карбамида кислотами.
7. Из данных квантово – химических расчетов найдены геометрические, энергетические и электронные параметры соединения состава ![]() хорошо согласующиеся с результатами ИК – спектроскопических исследований.
хорошо согласующиеся с результатами ИК – спектроскопических исследований.
Оценка полноты решений поставленных задач. Задачи, поставленные в диссертационной работе, решены полностью. Изучена растворимость в 6 четырехкомпонентных системах, содержащих соль ![]() ,
, ![]() ,
, ![]()
![]() – неорганическую кислоту – карбамид – воду при 25°С, установлена закономерность взаимного влияния компонентов в системах, найдены концентрационные границы кристаллизации двойных соединений карбамида с исходной солью и неорганической кислотой, а также 20 новых тройных соединений, для которых определен состав и строение, разработана методика их синтеза и определены некоторые физико-химические свойства.
– неорганическую кислоту – карбамид – воду при 25°С, установлена закономерность взаимного влияния компонентов в системах, найдены концентрационные границы кристаллизации двойных соединений карбамида с исходной солью и неорганической кислотой, а также 20 новых тройных соединений, для которых определен состав и строение, разработана методика их синтеза и определены некоторые физико-химические свойства.
Область применения. Установленные закономерности и результаты по растворимости в изученных системах позволяют разработать оптимальные условия синтеза 20 новых координационных соединений, они являются справочным материалом. Геометрические, энергетические и электронные характеристики новых соединений дополняют справочные данные по координационным соединениям.
Список опубликованных работ по теме диссертации
1 Еркасов Р.Ш., Абдуллина Г.Г., Рыскалиева Р.Г. Растворимость в системе Fe(NO3)3-CO(NH2)2 -HNO3-H2O при 25 °С// Вестник ПГУ. Серия Химико-биологическая. – 2008. – № 1. – С. 76 – 85.
2 Абдуллина Г.Г., Ерасов Р.Ш., Рыскалиева Р.Г., Оразбаева Р.С. Растворимость в системе CoBr2 - CO(NH2)2 - HBr - H2O при 25 °С// Вестник ПГУ. Серия Химико-биологическая. – 2008. – № 1. – С. 18 – 27.
3 Абдуллина Г.Г., Ерасов Р.Ш., Рысалиева Р.Г., Кокжалова Б.З. Взаимодействие в системе Сo(ClO4)2 - CO(NH2)2 - HClO4 - H2O при 25 °С// Вестник КарГУ. Серия Химия. – 2008. – Т. 50, № 2. – С. 28 – 34.
4 Абдуллина Г.Г., Ерасов Р.Ш., Рыскалиева Р.Г., Оразбаева Р.С. Взаимодействие в системе NiBr2 - CO(NH2)2 - HBr - H2O при 25 °С// Вестник КазНУ. Серия Химическая. – 2008. – Т. 49, № 1. – С. 216 – 220.
5 Абдуллина Г.Г., Ерасов Р.Ш., Рысалиева Р.Г., Байкенов М.И. Взаимодействие в системе NiI2- CO(NH2)2 - HI - H2O при 25 °С// Вестник КарГУ. Серия Химия. – 2008. – Т. 51, № 3. – С. 57 – 63.
6 Рыскалиева Р.Г., Абдуллина Г.Г., Еркасов Р.Ш. Синтез и физико – химические характеристики координационных соединений нитрата железа с протонированным карбамидом// Мaterialy IV miedzynoroowej naukowi –praktycznej konferencji «Nowoczesnych naukowych osiagniec – 2008». Chemia i chemiczne tehnologie Ekologia. Przemysi Nauka I studia. – 1-14 lutego 2008 roku. – T. 14. – С. 65 – 67.
7 Еркасов Р.Ш., Рыскалиева Р.Г., Масакбаева С.Р., Колпек А., Абдуллина Г.Г. Координационные соединения солей s- и d- металлов с протонированными амидами и перспективы их применения// Труды VІ международного Беремжановского съезда по химии и химической технологии. – Караганда, 2008. – C. 348 – 352.
8 Колпек А., Еркасов Р.Ш., Абдуллина Г.Г., Рыскалиева Р.Г. Синтез координационных соединений бромида никеля и сульфата марганца с протонированным карбамидом// Мaterialy IV mezinarodni vdecko – praktika konference «Vda: teorie a praxe – 2008». – Chemie a chemic tehnologie, Ekologie, Zempis a geologie. Praha Publishing House «Education and Science» s.r.o. 2008. – 16-31 srpna 2008 roku. – D. 10. – С. 56 – 58.
9 Абдуллина Г.Г., Еркасов Р.Ш., Колпек А., Рыскалиева Р.Г. Синтез координационных соединений бромида кобальта и нитрата марганца с протонированным карбамидом// Материали за ІV международна научна практична конференция «Научные дни – 2008». – София, 2008. – Т. 16. – С. 16 – 19.
10 Еркасов Р.Ш., Колпек А., Абдуллина Г.Г., Рыскалиева Р.Г. Масакбаева С.Р. Закономерности взаимодействия некоторых галогенидов биометаллов с протонированными амидами// «Валихановские чтения – 13». Материалы международной научно – практической конференции 24 – 26 апреля. – Кокшетау, 2008. – Т. 7. – С. 11 – 12.
11 Абдуллина Г.Г., Еркасов Р.Ш., Масакбаева С.Р., Рыскалиева Р.Г Синтез координационных соединений хлоридов марганца (кобальта) и иодида никеля с протонированными амидами// Мaterialy IV mezinarodni vdecko – praktika konference «Vda: teorie a praxe – 2008». – Chemie a chemic tehnologie, Ekologie, Zempis a geologie. Praha Publishing House «Education and Science» s.r.o. 2008. – 16-31 srpna 2008 roku. – D. 10. С. 16 – 18.
Абдуллина Гульнара Госманызы
VIII В ТОП МЕТАЛДАРЫ ТЗДАРЫНЫ ПРОТОНДАЛАН КАРБАМИДПЕН КЕШЕНДІ ОСЫЛЫСТАРЫ
«02.00.01 – бейорганикалы химия» мамандыы бойынша химия ылымдарыны кандидаты ылыми дрежесін алу шін дайындалан автореферат
Тйін
Зерттеу таырыбыны зектілігі. Соы кездегі химия ылымдарыны басты мселелеріні бірі ылыми – практикалы маызы бар жаа осылыстарды тзілу жадайлары жне оларды асиеттері. Соны ішінде органикалы лигандалары бар, сіресе биометалл тздарыны амидтермен рекеттесуінен тзілген німдерді зерттеу зекті мселеге айналып отыр. Амидтерді молекуласында екі электрондонорлы орталыты болуы, оларды іргелі зерттеу жобасы шін олдануа ерекше асиетпен амтамасыз етеді. Амидтерді биометалл тздарымен жне бейорганикалы ышылдармен рекеттесуінен тзілген осылыстарды асиеттеріні бастапы осылыстар асиеттеріне сайтынын круге болады. азіргі кезде олар толыымен зерттелген жо.
Жмысты масаты 25 °С температурада ![]() В топ металдар тздары – карбамид – бейорганикалы ышыл – су тртрауышты жйелеріндегі рекеттесу рдістерін жне тзілген жаа осылыстарды зерттеу болып табылады.
В топ металдар тздары – карбамид – бейорганикалы ышыл – су тртрауышты жйелеріндегі рекеттесу рдістерін жне тзілген жаа осылыстарды зерттеу болып табылады.
Зерттеу масатына енгізілді: ![]() ,
, ![]() ,
, ![]() - бейорганикалы ышыл –
- бейорганикалы ышыл – ![]() –
– ![]() жйелеріндегі ерігіштікті зерттеу; тзілген осылыстарды рамдарын анытау; оларды кристалдануыны концентрациялы шегін, бастапы рауыштарды зара серіні задылытарын анытау; синтезделген осылыстарды химиялы, физикалы жне физика – химиялы зерттеу дістері арылы идентификациялау; жаа синтезделген осылыстарды рылымын анытау.
жйелеріндегі ерігіштікті зерттеу; тзілген осылыстарды рамдарын анытау; оларды кристалдануыны концентрациялы шегін, бастапы рауыштарды зара серіні задылытарын анытау; синтезделген осылыстарды химиялы, физикалы жне физика – химиялы зерттеу дістері арылы идентификациялау; жаа синтезделген осылыстарды рылымын анытау.
Зерттеуді ылыми жаалыы. Алаш рет: 25 °С – та темір нитраты, кобальт перхлораты, кобальт (никель) бромидінен (иодиді), оларды карбамидпен, сондай – а ерітінділерде рамында карбамидпен оса сйкес ышылдар жне тздар бар азот, хлор, бромсутек жне иодсутек ышылдарына тратын алты тртрауышты жйелердегі ерігіштік зерттелді, рамында бір мезгілде металл тзы, карбамид, ышыл болатын 20 жаа кешенді осылыс тзілді, оларды ерігіштігі аныталды, оларды синтездеуді отайлы жадайлары сынылды, химиялы, рентгенфазалы дістер, физика – химиялы талдау дістері арылы олар сйкестендірілді, ал кейбір осылыстарды геометриялы, электронды жне энергетикалы параметрлері аныталды
орауа енгізілген негізгі жадайлар:
- 25 °С – та ерітіндіде рамында сйкес ышыл жне тздармен оса карбамиді бар, темір нитраты ![]() , кобальт перхлораты
, кобальт перхлораты ![]() , кобальт
, кобальт ![]() [никель
[никель ![]() ] бромиді (иодиді), оларды карбамидпен, сондай – а карбамидті азот, бромсутек, иодсутек, хлор ышылдарыны ерігіштігі;
] бромиді (иодиді), оларды карбамидпен, сондай – а карбамидті азот, бромсутек, иодсутек, хлор ышылдарыны ерігіштігі;
- 25 °С – та темір нитраты, никель (кобальт) иодиді (бромиді) жне кобальт перхлораты – карбамид – азот (иодсутек, бромсутек, хлор) ышылы – су жйелеріндегі кешенді осылыстар тзілу рдістеріні задылытары;
- темір, кобальт жне никель тздарыны протондалан карбамидпен тзілген 20 жаа кешенді осылыстарын синтездеу дістемесі жне оларды химиялы, рентгенфазалы, физика – химиялы талдау дістері арылы идентификациялау нтижелері, синтезделген осылыстарды физика – химиялы асиеттері:
- кешенді осылыстар атарыны рылымы жне геометриялы параметрлері.
Зерттеу нтижелері:
1. Тртрауышты жйелерді ерігіштік изотермасынан алынан мліметтер: 25 °С – та ![]() ,
, ![]() ,
, ![]() тздары
тздары![]() – бейорганикалы ышыл –
– бейорганикалы ышыл – ![]() –
– ![]() жйелерінен шрауышты жйелерді зерттеген кезде белгілі болан екілік осылыстарды бар болуы, сондай – а бір мезгілде рамында бастапы шрауышта болатын жаа 20 кешенді осылысты тзілуі.
жйелерінен шрауышты жйелерді зерттеген кезде белгілі болан екілік осылыстарды бар болуы, сондай – а бір мезгілде рамында бастапы шрауышта болатын жаа 20 кешенді осылысты тзілуі.
2. Ерігіштік изотермасын талдай отырып
а) ерітіндідегі ышылды млшері скен сайын штік осылыстарды ерігіштігі артады, сонымен атар тзданышты сер байалады, бл былыс осы ерітінділердегі ышыл концентрациясыны артуына байланысты суды саныны азаятынын длелдейді;
б) темір (кобальт, никель) тзы – карбамид – су, карбамид – ышыл – су шрауышты жйелерін зерттеген кезде белгілі болан екілік кешенді осылыстарды жне эвтоникалы рамдарды кристалдануы байалады;
в) ышыл млшеріні артуы металл тздарыны карбамидпен осылыстары ерігіштігіне тзданышты сер етеді;
г) темір (кобальт жне никель) тздарын осан кезде карбамидышыл ерігіштігіне тзданышты сер етеді;
д) металл тзы – карбамид – су жйелеріне ышылды осанда оны ерігіштігі жоарлайды;
е) карбамид – ышыл – су жйелеріндегі эвтоникалы рамдарды ерігіштігі кп жадайларда бастапы металл тзыны артуына байланысты тмендейді;
ж) бастапы тзбен тепе – тедікте тран ерітіндідегі ышыл млшеріні артуы оларды ерігіштігін тмендетеді.
3. Тртрауышты жйелерді ерігіштік изотермасы негізінде жаа 20 кешенді осылысты синтездеу дістемесі сынылды. Оларды жекешелігі химиялы жне рентгенфазалы талдау дістері арылы аныталды.
4. Алаш рет алынан осылыстар оларды балу (айырылу) температураларын, пикнометрлік тыыздыын, органикалы еріткіштерде ерігіштігін анытау арылы идентификацияланды.
5. Синтезделген осылыстарды зерттеу атарлары, оларды сімдіктерді німділігін 20 – 40 %-а арттыратынын жне оларды сапасына зиянды серін тигізбейтінін крсетті.
6. И – спектрлік зерттеу нтижелеріде С = О байланысыны валенттік тербеліс жиіліктеріні тменгі жаына арай ыысуы, С – N байланысыны жоары жаына арай ыысуы, сондай – а ОН – топтарында сііру жолатарыны пайда болуы О – арылы протондалуды длелдейді.
7. Квантхимиялы есептеулері арылы ![]() осылысыны геометриялы, электронды жне энергетикалы параметрлері аныталды, олар И – спектрлік зерттеулеріні мліметтерімен сйкес келеді.
осылысыны геометриялы, электронды жне энергетикалы параметрлері аныталды, олар И – спектрлік зерттеулеріні мліметтерімен сйкес келеді.
ойылан масатты толы шешімін тапандыын баалау. Жмыста ала ойылан масат толыымен шешімін тапты. 25 °С – та ![]() ,
, ![]() ,
, ![]() - бейорганикалы ышыл – карбамид – су 6 тртрауышты жйені ерігіштігі зерттелді, жйелердегі рауыштарды зара серіні задылытары аныталды, бастапы карбамидті тзбен жне бейорганикалы ышылмен екілік осылыстарыны кристалдануыны концентрациялы шегі белгілі болды, сондай – а рамын жне рылымын анытау шін ажетті 20 жаа кешенді осылыс тзілді, оларды синтездеу дістемесі сынылды жне оларды кейбір физика – химиялы параметрлері аныталды.
- бейорганикалы ышыл – карбамид – су 6 тртрауышты жйені ерігіштігі зерттелді, жйелердегі рауыштарды зара серіні задылытары аныталды, бастапы карбамидті тзбен жне бейорганикалы ышылмен екілік осылыстарыны кристалдануыны концентрациялы шегі белгілі болды, сондай – а рамын жне рылымын анытау шін ажетті 20 жаа кешенді осылыс тзілді, оларды синтездеу дістемесі сынылды жне оларды кейбір физика – химиялы параметрлері аныталды.
олданылу саласы. Зерттелген жйелерді ерігіштігі бойынша орнатылан задылытар мен нтижелер 20 жаа координациялы осылыстар синтезіні оптималды шарттарын анытауа ммкіндік береді жне олар анытамалы материал болып табылады. Жаа осылыстарды геометриялы, энергетикалы жне электронды сипатттамалары координациялы осылыстар бойынша анытамалы мліметтерді толытырады.
SUMMARY
On the author’s abstract of the thesis
for a candidate of chemistry degree on specialty 02.00.01 – Inorganic Chemistry
Abdullina Gulnara Gosmanovna
COORDINATION COMPOUNDS OF SALTS OF VIII B GROUP METALS WITH PROTONATED CARBAMIDE
Urgency of the research subject One of the most important problems of modern chemistry is to investigate conditions of formation and properties of new compounds which are of high scientific and practical value. Coordination compounds with organic ligands including products of interaction of biometals salts with amides are of priority interest. The presence of two electron donor groups in amides molecules gives the latter unique properties and makes them particular objects of fundamental research. Products of interaction of amides with biometals salts and inorganic acids are expected to possess combined properties of starting materials with newly acquired ones. At the present moment these compounds are investigated insufficiently.
The purpose of the research The purpose of the research was to investigate processes of interaction in four-component systems, namely salt of ![]() B group metal – carbamide – inorganic acid – water with the help of the solubility method at 25 C with taking into account formation of new compounds.
B group metal – carbamide – inorganic acid – water with the help of the solubility method at 25 C with taking into account formation of new compounds.
The tasks of the research included:
- studying solubility in systems
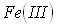 ,
, 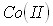 and
and 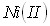 salts – inorganic acid –
salts – inorganic acid – 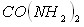 –
– 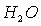 ;
; - establishing composition of the compounds formed;
- determination of concentration interface of their crystallization;
- revealing regularities of mutual interaction of starting materials;
- identification of synthesized compounds by chemical and physico-chemical methods of the research;
- establishing structure of newly synthesized compounds.
Scientific novelty of the research In the work presented for the first time it was studied solubility in 6 four-component systems, containing iron nitrate, cobalt perchlorate, cobalt(nickel) bromide(iodide), their compounds with carbamide as well as carbamide compounds with nitric, hydrobromic, hydriodic, and perchloric acids in solutions of corresponding acids and salts with presence of carbamide at 25 C. It was established 20 new coordination compounds, containing salt of metal, carbamide and acid in their structure simultaneously. It was determined the character of solubility of newly synthesized compounds. Optimal synthesis conditions of the latter were elaborated. Identification of new compounds was carried out with the help of chemical and X-ray рhase analysis as well as determination of physico-chemical properties. There was suggested structure of new compounds.
Main conclusions presented for the thesis defense:
- solubility of iron ![]() nitrate, cobalt
nitrate, cobalt ![]() perchlorate, cobalt
perchlorate, cobalt ![]() [nickel
[nickel ![]() ] bromides (iodides), their compounds with carbamides as well as compounds of carbamide with nitric, hydrobromic, hydriodic, and perchloric acids in solutions of corresponding acids and salts, containing carbamide at 25 C;
] bromides (iodides), their compounds with carbamides as well as compounds of carbamide with nitric, hydrobromic, hydriodic, and perchloric acids in solutions of corresponding acids and salts, containing carbamide at 25 C;
- regularities of complex formation processes in the following systems: iron ![]() nitrate, cobalt
nitrate, cobalt ![]() [nickel
[nickel ![]() ] bromides (iodides), and cobalt
] bromides (iodides), and cobalt ![]() perchlorate – carbamide – nitric (hydrobromic, hydriodic, and perchloric acid – water at 25 C;
perchlorate – carbamide – nitric (hydrobromic, hydriodic, and perchloric acid – water at 25 C;
- methods of synthesis of 20 new coordination compounds of iron, cobalt and nickel salts with protonated carbamide and results of their identification by the methods of chemical and X-ray рhase analysis as well as physico-chemical properties of synthesized compounds with the following composition:
- suggested structure and geometric parameters of the number of coordination compounds.
The results of the research:
1. From the data of solubility isotherms of four-component systems, namely ![]() ,
, ![]() and
and ![]() salts – inorganic acid –
salts – inorganic acid – ![]() –
– ![]() at 25 C it was established formation of double compounds, whose existence had not been earlier determined at studying solubility of constituents of three-component systems. It was also established 20 new coordination compounds, containing three starting components simultaneously.
at 25 C it was established formation of double compounds, whose existence had not been earlier determined at studying solubility of constituents of three-component systems. It was also established 20 new coordination compounds, containing three starting components simultaneously.
2. From the analysis of isotherm the following conclusions have been made:
a) Solubility of triple compounds increases with growth of percentage of acids in solution, i.e. salting effect takes place. This fact is also proved by revealing decreasing values of aqueous number in these solutions with growth of acids concentration.
b) Crystallisation of ephtonical compositions and double coordination compounds takes place. Existence of the latter was revealed at studying solubility in constituents of three-component systems, namely iron (cobalt, nickel) salt – carbamide – water as well as carbamide – acid – water.
c) Growth of acids percentage has a salting effect on solubility of compounds of metals with carbamide.
d) Introduction of iron (cobalt, nickel) salts has a salting effect on solubility of carbamide acids.
e) Solubility of ephotonical compositions of salt of metal – carbamide – water systems increases with addition of acid.
f) Solubility of ephotonical compositions of carbamide – acid – water in most cases decreases with growth of concentration of starting salt of metal.
g) Growth of concentration of acids in solutions, which are in equilibrium with the starting salt, leads to decrease of their solubility.
3. On the basis of solubility isotherms of four-component systems there was elaborated the method of synthesis of 20 new coordination compounds. The structures of the latter were established by methods of chemical and X-ray рhase analysis.
4. Identification of compounds synthesized for the first time was carried out by determination of melting points (destruction), pycnometric density and solubility in organic solvents.
5. Assays of a number of synthesized compounds showed that the latter contributed to the increase of harvest yield on 20-40 %. The compounds do not exhibit toxic effect on harvest.
6. Results of IR-spectroscopic investigation suggested shift of values of valence vibrations of C=O bond to low-frequency field, C–N bond to high-frequency field as well as appearance of a characteristic band of OH-group. The latter fact proves O – protonation of carbamide by acids.
7. From the data of quantum chemical calculations it was found geometric, energetic and electronic parameters of compounds with ![]() composition. Results of quantum chemical calculations are in agreement with IR-spectroscopic data.
composition. Results of quantum chemical calculations are in agreement with IR-spectroscopic data.
Evaluation of fulfillment of the tasks designated Tasks designated in the thesis presented are completely solved. There was studied solubility in 6 four-component systems, containing ![]() ,
, ![]() and
and ![]() salts – inorganic acid – carbamide – water at 25 C. It was established regularity of mutual influence of systems components on solubility. It was found crystallization concentration interface of double compounds of carbamide with the starting and inorganic acid. There were also found 20 new triple compounds. There were determined composition, structure and some physico-chemical properties of the latter. It was elaborated the method of synthesis of 20 triple compounds.
salts – inorganic acid – carbamide – water at 25 C. It was established regularity of mutual influence of systems components on solubility. It was found crystallization concentration interface of double compounds of carbamide with the starting and inorganic acid. There were also found 20 new triple compounds. There were determined composition, structure and some physico-chemical properties of the latter. It was elaborated the method of synthesis of 20 triple compounds.
The fields of application Established regularities and results on solubility in the systems investigated allow elaborating optimal conditions of synthesis of 20 new coordination compounds. The data obtained could be included in a data-base. Geometric, energetic and electronic characteristics of new compounds contribute to data-bases on coordination compounds as well.

