Координационные соединения солей металлов viii b группы с протонированным карбамидом
УДК 541.123. 31 : 547.55.42 На правах рукописи
АБДУЛЛИНА ГУЛЬНАРА ГОСМАНОВНА
Координационные соединения солей металлов VIII B группы
с протонированным карбамидом
02.00.01 – Неорганическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
.
Республика Казахстан
Павлодар, 2009
Диссертация выполнена на кафедре химии и химических технологий биолого – химического факультета Павлодарского государственного университета им. С.Торайгырова.
| Научные руководители | доктор химических наук, профессор Р.Ш.Еркасов |
| кандидат химических наук, доцент Р.Г. Рыскалиева | |
| Официальные оппоненты: | доктор химических наук, профессор М.Б. Баткибекова |
| доктор химических наук Г.К. Сугурбекова | |
| Ведущая организация | Южно-Казахстанский государственный университет им. М. Ауезова |
Защита состоится «29» сентября 2009 г. в 1400 часов на заседании диссертационного совета ОД 14.07.01. при Карагандинском государственном университете им. Е.А. Букетова по адресу: 100028, г. Караганда, ул. Университетская, 28, химический факультет, актовый зал.
С диссертацией можно ознакомиться в библиотеке КарГУ им. Е.А. Букетова по адресу: г. Караганда, ул. Университетская, 28.
Автореферат разослан «____» июня 2009г.
Ученый секретарь
диссертационного совета ОД 14.07.01
д.х.н.,профессор Ш.К.Амерханова
ВВЕДЕНИЕ
Общая характеристика работы. Диссертационная работа посвящена разработке научных основ образования координационных соединений солей металлов VIII B группы с протонированным карбамидом, установлению закономерностей взаимодействия в системах соли железа (кобальта, никеля) – карбамид – неорганическая кислота – вода, синтезу образуемых в них соединений, определению строения и физико – химических характеристик новых тройных соединений.
Актуальность темы. Одной из актуальных задач неорганической химии остается проблема синтеза и изучения строения, свойств координационных соединений с органическими лигандами, представляющих интерес для теории и практики. Особое место имеют координационные соединения, содержащие соли биометаллов, амиды. Наличие в молекулах амидов двух электронодонорных центров – карбонильного кислорода и аминного азота обеспечивает им уникальные свойства, делая их особыми объектами фундаментальных теоретических исследований. Помимо этого, исходные амиды и соли металлов являются потенциальными биологически активными соединениями, а наличие в амидах различных функциональных групп делает их перспективными полупродуктами для органического синтеза.
Систематическое изучение процессов и продуктов взаимодействия солей металлов, неорганических кислот с амидами позволило установить образование большого количества двойных соединений, обладающих широким спектром полезных качеств нашедших применение в промышленности, сельском хозяйстве, органическом синтезе и медицине.
Степень разработанности темы. В мировой практике имеются разрозненные случаи описания способов получения координационных соединений, содержащих в своем составе одновременно соль металла, амид и неорганическую кислоту. Разработкой основ получения разнолигандных координационных солей биометаллов, карбамида (ацетамида) и неорганических кислот занимаются сотрудники кафедры неорганической химии КазНУ им. аль-Фараби. Ими разработаны не только способы получения ряда координационных соединений различных стехиометрических составов, найдены некоторые закономерности их образования, но и установлены перспективные области практического применения некоторых новых соединений.
Целью работы являлось систематическое исследование процессов и продуктов взаимодействия некоторых солей металлов VIII В группы с протонированным карбамидом в водных растворах методом растворимости при 25 °С и определение физико-химических свойств полученных соединений.
В задачу исследования входило:
- изучение растворимости в четырехкомпонентных системах соль железа (кобальта, никеля) – неорганическая кислота – карбамид – вода;
- установление составов образующихся новых соединений, определение оптимальных условий их образования;
- установление закономерностей взаимного влияния компонентов в изученных системах;
- идентификация синтезированных соединений химическими, физическими и физико-химическими методами исследования.
- исследование строения синтезированных соединений.
Объектами исследования являются соединения нитрата железа, бромидов (иодидов) кобальта (никеля), перхлората кобальта с протонированным карбамидом.
Предметом исследования является изучение растворимости в четырехкомпонентных системах соль железа (кобальта, никеля) – неорганическая кислота – карбамид – вода при 25 °С, закономерности образования координационных соединений в этих системах, строение и свойства новых соединений, а также поиск перспективных областей их применения.
Методы исследования. В работе использованы следующие физико – химические методы исследования: метод растворимости, пикнометрия, титриметрия, метод Къельдаля, рентгенофазовый анализ, ИК – спетроскопия, квантово – химический метод расчета.
Научная новизна исследования. В работе впервые:
- изучена растворимость при 25 °С в шести четырехкомпонентных системах, содержащих соль железа (кобальта, никеля) – карбамид – кислоту – воду; в них образуются соединения, существование которых было ранее установлено при изучении растворимости составляющих трехкомпонентных систем, а также 20 новых координационных соединений, содержащих в своем составе одновременно исходные компоненты;
- установлены закономерности взаимного влияния компонентов в изученных системах, характер растворения образующихся координационных соединений; разработаны оптимальные условия синтеза в лабораторных условиях 20 новых соединений;
- проведена идентификация новых координационных соединений методами химического, рентгенофазового анализов, определением температур плавления (разложения), плотности, растворимости в органических растворителях;
- определены геометрические, энергетические и электронные параметры некоторых координационных соединений на основании проведенных квантово – химических расчетов.
Теоретическая и практическая значимость. Установленные закономерности процессов взаимодействия и образования новых соединений в изученных системах вносят существенный вклад в развитие классической теории комплексообразования и строения координационных соединений, в неорганическую химию и физико – химический анализ многокомпонентных систем. Физико-химические свойства и строение впервые синтезированных соединений относятся к справочному материалу.
Отдельные результаты изучения процессов и продуктов взаимодействия в изученных системах используются в учебном процессе на кафедре химии и химической технологии Павлодарского государственного университета им. С. Торайгырова при чтении специальных курсов лекций «Физико-химический анализ многокомпонентных систем» и «Химия координационных соединений».
Полученные в работе геометрические, электронные и термодинамические характеристики могут быть использованы в качестве стандартных величин и для количественной оценки реакционной способности карбамида. Наряду с этим, некоторые синтезированные новые соединения могут быть применены в сельском хозяйстве в качестве удобрений для повышения урожайности растений.
Достоверность и обоснованность полученных данных подтверждены результатами неоднократного повторения экспериментов. Работа проводилась с использованием классических и современных физических и физико – химических методов анализа. Достоверность результатов подтверждается согласованностью результатов ИК – спектроскопических исследований соединений с квантово – химическим расчетом строения соединений.
Связь темы с планом научно-исследовательских работ. Работа выполнялась в соответствии с планом научно – исследовательских работ, проводимых на кафедре химии и химической технологии Павлодарского государственного университета им. С. Торайгырова по темам: «Разработка основ получения координационных соединений s- и d- металлов с протонированными амидами, обладающими физиологической активностью», которая является продолжением темы ранее проводимой по программе фундаментальных исследований МОН Республики Казахстан «Исследование физико – химических свойств веществ и материалов из органического и неорганического сырья Казахстана» (номера регистрации 0197 РК 00549 и 0101 РК 010012).
Основные положения, выносимые на защиту:
- растворимость нитрата железа, перхлората кобальта, бромидов (иодидов) кобальта (никеля), их соединений с карбамидом, а также соединений карбамида с азотной, бромоводородной, иодоводородной, хлорной кислотами в растворах соответствующих кислот и солей, содержащих карбамид при 25 °С;
- закономерности процессов комплексообразования в системах нитрат железа, иодид (бромид) никеля (кобальта) и перхлорат кобальта – карбамид – азотная (иодоводородная, бромовородная, хлорная) кислота – вода при 25 °С;
- методики синтеза 20 новых координационных соединений солей железа, кобальта и никеля с протонированным карбамидом и результаты идентификации их методами химического, рентгенофазового анализов, физико-химические свойства синтезированных соединений;
- предполагаемое строение и геометрические параметры некоторых координационных соединений.
Апробация работы. Материалы диссертации докладывались на Международных научно – практических конференциях: «Валихановские чтения – 13» (Кокшетау, 2008), «Научные дни – 2008» (Днепропетровск, София, Белгород - 2008), «Nowoczesnych naukowych osiagniec – 2008» (Przemysl – 2008), «Vda: teorie a praxe – 2008» (Прага – 2008), «VІ Беремжановский съезд по химии и химической технологии» (Караганда – 2008).
Личный вклад автора заключается в планировании и выполнении экспериментальной части диссертационной работы, обобщении результатов проведенных исследований.
Публикации. По материалам диссертации опубликовано 5 статей в научных журналах, рекомендованных Комитетом по контролю в сфере образования и науки МОН РК, и 6 трудов в материалах Международных научных конференций.
Структура и объем работы. Диссертационная работа изложена на 109 страницах машинописного текста, состоит из введения, четырех разделов, заключения, списка использованных источников и приложения. Работа содержит 12 рисунков и 15 таблиц. Список использованных источников составляет 146 наименований.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обоснованы актуальность и новизна темы, выбор объектов исследования, сформулированы цели, задачи работы и защищаемые положения.
В первой главе, состоящей из двух разделов, рассматриваются физико-химические свойства исходных компонентов: карбамида, солей железа, кобальта, никеля, неорганических кислот и основные моменты процессов взаимодействия карбамида с неорганическими кислотами и солями железа, кобальта и никеля.
Во второй главе содержатся методики изучения взаимодействия протонированного карбамида с солями железа, кобальта и никеля (раздел 2.1), данные по растворимости в системах нитрат железа – карбамид – азотная кислота – вода (раздел 2.2), соль кобальта – карбамид – соответствующая кислота – вода (раздел 2.3) и соль никеля – карбамид – соответствующая кислота – вода при 25 °С (раздел 2.4), а также основные закономерности взаимодействия солей железа (кобальта и никеля) с карбамидом в растворах кислот (раздел 2.5)
В третьей главе описываются методики синтеза соединений солей железа, кобальта, никеля с протонированным карбамидом и определение физико – химических свойств этих соединений. Соединения идентифицированы методами химического и рентгенофазового анализов, определением их температур плавления (разложения), плотности и растворимости в органических растворителях. ИК – спектроскопическими исследованиями установлено предполагаемое строение 20 синтезированных соединений солей железа, кобальта, никеля с протонированным карбамидом.
Приводятся данные по удобрительной активности некоторых синтезированных соединений на рост и развитие пшеницы и лядвенца рогатого.
В четвертой главе изложены методика и результаты квантово – химического исследования комплекса нитрата железа с протонированным карбамидом.
Исследование растворимости в системах соли железа (кобальта, никеля) – карбамид – вода при 25 С проводили исходя из составов эвтонических точек составляющих трехкомпонентных систем: карбамид – кислота – вода и карбамид – соль металла – вода, к которым прибавляли определенные всевозрастающие количества четвертого компонента. Контроль за твердой фазой проводили не только по их химическому составу, но и кристаллооптическим методом с помощью микроскопа МИН – 8.
Полученные экспериментальные данные по растворимости представлены в массовых процентах, в виде центральной проекции изотермы в треугольнике Гиббса-Розебома.
Данные по растворимости в четырехкомпонентной системе иодид никеля – карбамид – иодоводородная кислота – вода изображены на рисунке 1.
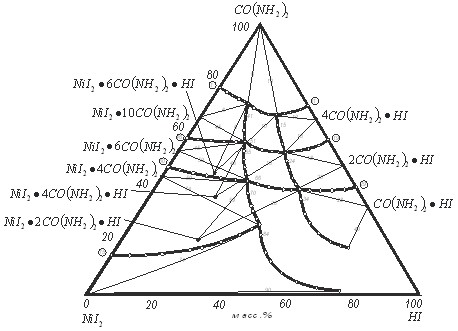 Рисунок 1 – Центральная проекция изотермы растворимости в системе NiI2 - CO(NH2)2 - HI - H2O при 25 °С Рисунок 1 – Центральная проекция изотермы растворимости в системе NiI2 - CO(NH2)2 - HI - H2O при 25 °С | Прибавление в эвтонические растворы системы иодид никеля – карбамид – вода, находящихся в равновесии с твердыми фазами |
Прибавление в эвтонические растворы системы ![]() , находящихся в равновесии с твердыми фазами
, находящихся в равновесии с твердыми фазами ![]() +
+ ![]() (точка 11),
(точка 11), ![]() +
+![]() (точка 19) и
(точка 19) и ![]() +
+ ![]() (точка 29) увеличивающих количеств иодида никеля приводит к их кристаллизации в твердую фазу и к образованию соединений составов 1 : 6 : 1, 1 : 4 : 1 и 1 : 2 : 1 (мольное отношение иодид никеля : карбамид : кислота) соответственно.
(точка 29) увеличивающих количеств иодида никеля приводит к их кристаллизации в твердую фазу и к образованию соединений составов 1 : 6 : 1, 1 : 4 : 1 и 1 : 2 : 1 (мольное отношение иодид никеля : карбамид : кислота) соответственно.
На изотерме растворимости этой системы имеются также ветви кристаллизации двойных соединений, образования которых было установлено при изучении растворимости в составляющих трехкомпонентных системах: ![]() :
: ![]() ,
, ![]() и
и ![]() ,
, ![]() :
: ![]() ,
, ![]() и
и ![]() .
.
При изучении растворимости в системе ![]() установлены области кристаллизации исходных эвтонических составов и двойных соединений, образование которых было установлено при изучении растворимости в составляющих трехкомпонентных системах:
установлены области кристаллизации исходных эвтонических составов и двойных соединений, образование которых было установлено при изучении растворимости в составляющих трехкомпонентных системах: ![]() :
: ![]() и
и ![]() :
: ![]() , а также найдены концентрационные пределы образования новых координационных соединений следующих составов: 1 : 2 : 1, 1 : 4 : 2 и 1:6:2 (мольное отношение нитрат железа : карбамид : азотная кислота).
, а также найдены концентрационные пределы образования новых координационных соединений следующих составов: 1 : 2 : 1, 1 : 4 : 2 и 1:6:2 (мольное отношение нитрат железа : карбамид : азотная кислота).
В системе ![]() установлены области кристаллизации исходных эвтонических составов и двойных соединений бромида кобальта и бромоводородной кислоты с карбамидом составов
установлены области кристаллизации исходных эвтонических составов и двойных соединений бромида кобальта и бромоводородной кислоты с карбамидом составов ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() . В этой системе определены также области выделения в твердую фазу новых соединений, в составе которых содержатся все три исходных компонента:
. В этой системе определены также области выделения в твердую фазу новых соединений, в составе которых содержатся все три исходных компонента: ![]() ,
,![]() ,
, ![]() и
и ![]() .
.
При изучении растворимости в системе ![]() установлены концентрационные границы кристаллизации эвтонических составов трехкомпонентных систем
установлены концентрационные границы кристаллизации эвтонических составов трехкомпонентных систем ![]() и
и ![]() и двойных соединений образующихся в них
и двойных соединений образующихся в них ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() и
и ![]() , а также области выделения в твердую фазу новых соединений составов
, а также области выделения в твердую фазу новых соединений составов ![]() ,
, ![]() и
и ![]() .
.
В системе ![]() найдены ветви кристаллизации исходных эвтонических составов и двойных соединений
найдены ветви кристаллизации исходных эвтонических составов и двойных соединений ![]() ,
, ![]() ,
, ![]() и
и ![]() образующихся в составляющих трехкомпонентных системах
образующихся в составляющих трехкомпонентных системах ![]() и
и ![]() , а также концентрационные границы кристаллизации новых соединений составов
, а также концентрационные границы кристаллизации новых соединений составов ![]() ,
,![]() и
и ![]() .
.
Изучение растворимости в системе ![]() позволило установить ветви кристаллизации исходных эвтонических составов и двойных соединений карбамида с бромидом никеля и бромоводородной кислотой:
позволило установить ветви кристаллизации исходных эвтонических составов и двойных соединений карбамида с бромидом никеля и бромоводородной кислотой: ![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
, ![]() образующихся в составляющих трехкомпонентных системах. В изученной системе найдены также концентрационные границы образования новых соединений составов
образующихся в составляющих трехкомпонентных системах. В изученной системе найдены также концентрационные границы образования новых соединений составов ![]() ,
, ![]() и
и ![]() .
.
Основные закономерности взаимодействия солей железа (кобальта, никеля) с карбамидом в растворах кислот
Анализируя вышеописанные изотермы растворимости, следует отметить, что в четырехкомпонентных системах соль железа (кобальта, никеля) – карбамид –кислота – вода при определенных соотношениях компонентов, происходит кристаллизация практически всех соединений, существование которых было установлено при изучении растворимости в составляющих трехкомпонентных системах, кроме них образуются также новые координационные соединения, содержащие в своем составе одновременно соль железа (кобальта, никеля), карбамид и кислоту.
Кислотно-основное взаимодействие, приводящее к образованию тройных соединений в изученных системах, возможно в результате протекания следующих реакций (в качестве примера рассмотрим реакции протекающие в системе ![]() ):
):
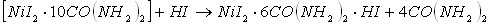
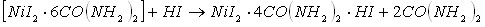
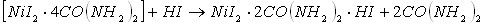
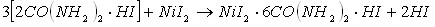
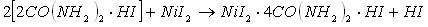
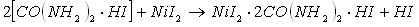
Из приведенных уравнений реакций следует, что образование тройных соединений иодида никеля с протонированным карбамидом, сопровождается вытеснением из состава двойных соединений свободных молекул кислот или карбамида.
В изученных четырехкомпонентных системах установлены следующие закономерности взаимного влияния компонентов и их влияния на растворимость кристализующихся из насыщенных растворов двойных и тройных соединений:
- введение солей металлов в эвтонические растворы систем карбамид – кислота – вода приводит к всаливающему влиянию солей металлов на растворимость эвтонической смеси, приводящее к образованию тройной смеси.
- прибавление возрастающих количеств кислот в эвтонические растворы систем карбамид – соль металла – вода оказывает в основном высаливающее влияние на растворимость эвтонических смесей и только бромид и перхлорат кобальта оказывает незначительное всаливающее действие, о чем свидетельствуют значения водного числа.
- возрастающее содержание неорганических кислот в растворах оказывают всаливающее действие на растворимость образующихся двойных соединений карбамида с солями металлов, а также на растворимость новых координационных соединений. Растворимость исходных солей с ростом концентрации кислот в растворе уменьшается.
- возрастащие количества солей металлов оказывают преимущественно всаливающее влияние на растворимость карбамидкислот, исключение составляет влияние нитрата железа на растворимость нитрата карбамида. Вероятной причиной которого являются очень низкая растворимость нитрата карбамида.
Синтез и некоторые физико-химические характеристики координационных соединений солей железа, кобальта и никеля с протонированным карбамидом
Исходя из полученных изотерм растворимости, разработаны методики их синтеза в лабораторных условиях. Выделенные в кристаллическом состоянии соединения солей железа (кобальта, никеля) с протонированным карбамидом идентифицированы методами химического и рентгенофазового анализа, определением температур плавления (разложения), плотности, растворимости в органических растворителях (таблица 1). Из таблицы видно, что соединения солей железа, кобальта и никеля с протонированным карбамидом в основном разлагаются до плавления при температурах значительно ниже температур плавления исходных солей, но выше температуры плавления карбамида.
Пикнометрические плотности тройных соединений имеют меньшие значения, чем исходные соли железа, кобальта и никеля, но большие по сравнению с карбамидом. Плотность синтезированных соединений уменьшается с увеличением доли карбамида в их составе.
Полученные координационные соединения нерастворимы в бензоле и толуоле, плохо растворимы в диэтиловом эфире, хорошо растворимы в ацетоне и этиловом спирте.
Индивидуальность синтезированных соединений установлена не только химическими методами, но и ренгенофазовым анализом по набору межплоскостных расстояний и интенсивностям соответствующих линий на дифрактограммах. Общих закономерностей в смещении наиболее интенсивных пиков у соединений по сравнению с исходными, нет.
Таблица 1 – Физико – химические характеристики соединений нитрата железа, перхлората кобальта, бромида и иодида кобальта (никеля) с протонированным карбамидом
| Соединение | d, кг·м-3 | t°пл (разл), °С | Растворимость, г / 100 г растворителя | ||||
| бен-зол | толуол | этанол | ацетон | Диэтило-вый эфир | |||
| 1690 | 185 | 0,02 | н.р.* | 15,10 | 16,41 | 7,25 | |
| 1535 | 178 | н.р. | н.р. | 13,19 | 12,62 | 5,19 | |
| 1420 | (160) | н.р. | н.р. | 18,45 | 14,19 | 4,38 | |
| 2810 | 190 | н.р. | н.р. | 23,72 | 14,00 | 6,22 | |
| 2415 | 173 | н.р. | н.р. | 20,15 | 12,49 | 5,19 | |
| 2105 | (175) | н.р. | н.р. | 14,18 | 13,55 | 8,49 | |
| 1895 | (150) | 0,02 | н.р. | 12,46 | 10,64 | 7,20 | |
| 3210 | 196 | н.р. | н.р. | 14,19 | 9,17 | 5,82 | |
| 2620 | (183) | н.р. | н.р. | 20,02 | 16,46 | 6,19 | |
| 2235 | (170) | 0,02 | н.р. | 25,46 | 18,53 | 7,18 | |
| 2905 | 192 | н.р. | н.р. | 18,19 | 12,92 | 4,93 | |
| 2740 | 175 | н.р. | н.р. | 16,14 | 11,29 | 7,66 | |
| 2265 | (150) | н.р. | н.р. | 21,07 | 13,75 | 4,42 | |
| 3200 | 184 | н.р. | н.р. | 18,10 | 12,67 | 8,33 | |
| 2895 | 163 | н.р. | н.р. | 23,15 | 16,41 | 6,75 | |
| 2450 | (150) | н.р. | н.р. | 15,16 | 10,85 | 7,12 | |
| 2185 | (140) | 0,02 | н.р. | 17,29 | 14,30 | 5,77 | |
| 3010 | (180) | н.р. | н.р. | 10,20 | 11,74 | 3,82 | |
| 2520 | (154) | н.р. | н.р. | 8,94 | 10,15 | 5,14 | |
| 2235 | (130) | н.р. | н.р. | 9,17 | 7,48 | 4,18 | |
н.р.* – нерастворим
Инфракрасные спектры
С целью установления строения и места координации в молекулах карбамида и соли железа (кобальта, никеля) были сняты ИК – спектры.
Анализ ИК – спектров соединений осложнен тем, что карбамид соединяется с катионом металла уже в протонированном через атом кислорода состоянии.
Найдено, что частоты валентных колебаний карбонильной связи в спектрах соединений смещены в низкочастотную область на 30 – 40 см-1, а частоты валентных колебаний связи С – N в спектрах смещены в высокочастотную область на 20 – 30 см-1, что свидетельствует об образовании связи через карбонильный кислород. Появление в ИК – спектрах соединений полос поглощения в области 3380 – 3390 см-1 и 1705 – 1715 см-1 указывает на О – протонирование, так как эти частоты поглощения относятся к валентным и деформационным колебаниям ОН – группы.
Частоты валентных антисимметричных колебаний NH-связи соединений солей железа (кобальта, никеля) с протонированным карбамидом на 15 – 20 см-1 смещаются в низкочастотную область. Полосы валентных симметричных колебаний NH - связи в меньшей степени смещены в низкочастотную область (5 – 15 см-1). Такие изменения указывают на участие аминогруппы карбамида в образовании новых Н – связей NH…Х, где Х – анион кислоты.
Полосы поглощения деформационных колебаний NН2 – группы карбамида при 1610 см-1 практически сохраняют неизменное положение, что также может быть результатом участия С = О связи в образовании координационного соединения.
Таким образом, ИК – спектроскопические исследования соединений солей железа, кобальта и никеля с протонированным карбамидом показали, что они относятся преимущественно к разнолигандным координационным соединениям, содержащими во внутренней сфере карбамид и протонированный карбамид наряду с анионами соответствующих кислот.
Для синтезированных соединений предложено следующее строение:
| где А* – |
Квантово – химическое исследование структуры комплекса железа с протонированным карбамидом
Особое значение для характеристики новых соединений имеет устойчивость химических соединений, которая определяется величиной энтальпий образования ![]() .
.
Квантово-химическим полуэмпирическим методом РМЗ рассчитаны энтальпии образования комплексных соединений нитрата железа с карбамидом и протонированным карбамидом. Анализ величин ![]() , показывает что, устойчивость всех исследованных протонированных соединений карбамида и комплексов нитрата железа с карбамидом возрастает в ряду:
, показывает что, устойчивость всех исследованных протонированных соединений карбамида и комплексов нитрата железа с карбамидом возрастает в ряду:
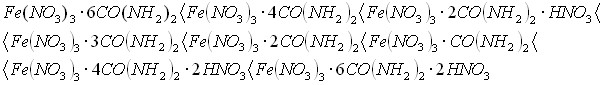
Геометрические параметры молекул карбамида, нитрата карбамида и карбамидных комплексов железа, получаемые квантово-химическими расчетами, позволяют решать вопросы их пространственного строения, что важно для объективной оценки реакционной способности соединений (таблица 3).
Протонирование приводит к увеличению длины связи С=О она равна: в CO(NH2)2 = 0,1227 нм, в CO(NH2)2 ·HNO3 =0,1237 нм, в Fe(NO3)3 · 2CO(NH2)2 = 0,1285 нм, и в Fe(NO3)3 · 2CO(NH2)2 · HNO3 = 0,1360 нм. Таким образом, протонирование азотной кислотой в большей степени влияет на длину связи С=О в карбамидном комплексе железа Fe(NO3)3 · 2CO(NH2)2 · HNO3. Длина связи С–N в молекуле Fe(NO3)3 · 2CO(NH2)2 значительно меньше по сравнению с данным межатомным расстоянием в молекуле карбамида.
Таблица 3 – Геометрические параметры молекул карбамида, нитрата карбамида и карбамидных комплексов железа
| Соединение Параметр | CO(NH2)2 | CO(NH2)2 ·HNO3 | Fe(NO3)3·2CO(NH2)2 | Fe(NO3)3 ·2CO(NH2)2 ·HNO3 |
| r C–O, нм | 0,1227 | 0,1237 | 0,1285 | 0,1360 |
| r C–N, нм | 0,1430 0,1431 | 0,1419 0,1421 | 0,1307 0,1300 0,1405 0,1388 | 0,1418 0,1416 0,1426 0,1309 |
| r N –H, нм | 0,0996 0,0996 0,0996 0,0996 | 0,0996 0,0995 0,0997 0,0995 | 0,0996 0,1011 0,0987 0,0992 | 0,0996 0,0995 0,0996 0,1016 |
| r O–HNO3, нм | - | 0,1754 | - | 0,0994 |
| 120,50 | 112,52 | 107,13 117,52 | 118,82 119,55 136,42 109,91 | |
| - | - | 84,70 105,77 | 115,54 118,30 |
Из сравнения длины связи С–N в молекулах Fe(NO3)3 · 2CO(NH2)2 и Fe(NO3)3 · 2CO(NH2)2 · HNO3 видно, что в результате взаимодействия азотной кислоты с атомом карбонильного кислорода карбамида, данное межатомное расстояние увеличивается. При этом, длина одной связи С–N, а именно в протонированном карбамиде, увеличилась незначительно, она равна 0,1309 нм. Это можно объяснить взаимным влиянием пространственного и электронного строения расположенных вокруг центрального атома комплекса лигандов. Практически одинаковыми во всех исследуемых соединениях остаются длины связей N–H в аминогруппах амидного фрагмента.
Длины связи О…НNO3 в молекулах CO(NH2)2·HNO3 и Fe(NO3)3 · 2CO(NH2)2 · HNO3 равны 0,1754 нм и 0,0994 нм, соответственно, что вероятно связано с различной природой образующихся связей в комплексах при протонизации.
В результате происходящего протонирования атома карбонильного кислорода наблюдается изменение величин валентных углов. Протонизация приводит к уменьшению угла ![]() N–C–O и к увеличению угла
N–C–O и к увеличению угла ![]() Fe–O–C. Анализ геометрических параметров позволил определить строение тройного соединения Fe(NO3)3 ·2CO(NH2)2 ·HNO3, представленное на рисунке 2.
Fe–O–C. Анализ геометрических параметров позволил определить строение тройного соединения Fe(NO3)3 ·2CO(NH2)2 ·HNO3, представленное на рисунке 2.
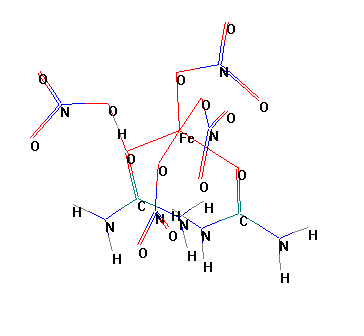
Рисунок 2 – Строение соединений Fe(NO3)3 ·2CO(NH2)2 ·HNO3
Таким образом, анализ рассчитанных квантово – химическим полуэмпирическим методом термодинамических характеристик молекул карбамида, его протонированных форм различного молекулярного состава и комплексных соединений железа с карбамидом, позволяет сделать вывод, что все они в принципе могут быть использованы в качестве индексов при оценке их относительной реакционной способности и в качестве справочных данных.
Сравнительный анализ геометрических параметров показал взаимное влияние различных по электронной и пространственной природе атомов и молекул, входящих в исследуемые комплексы, протонирование атома кислорода карбонильной группы молекулы карбамида оказывает существенное влияние на изменение всех геометрических характеристик исследуемых соединений.
ЗАКЛЮЧЕНИЕ
1. На основании изучения растворимости в 6 четырехкомпонентных системах, содержащих водные растворы нитрата железа, бромида (иодида) кобальта (никеля), перхлората кобальта, азотную (бромоводородную, иодоводородную, хлорную) кислоты при 25 °С, установлено образование в этих системах 20 новых координационных соединений, содержащих одновременно в своем составе соли металлов, карбамид и кислоту,
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ;
;
2. Из анализа полученных изотерм растворимости следует, что,
растворимость тройных соединений увеличивается с ростом содер-жания кислот в растворе, т.е. проявляется всаливающее влияние, о чем свидетельствует уменьшение значений водного числа в этих растворах с ростом концентрации кислот; происходит кристаллизация эвтонических составов и двойных координационных соединений, существование которых было установлено при изучении растворимости в составляющих трехкомпонентных системах соль железа (кобальта и никеля) – карбамид – вода, карбамид – кислота – вода; возрастающие количества кислот оказывают всаливающее действие на растворимость соединений солей металлов с карбамидом; введение солей железа (кобальта и никеля) оказывает всаливающее действие на растворимость карбамидкислот; растворимость эвтонических составов систем соль металла – карбамид – вода при добавлении кислоты возрастает; растворимость эвтонических составов систем карбамид – кислота – вода в большинстве случаев уменьшается с ростом концентрации исходной соли металла; рост концентрации кислот в растворах, находящихся в равновесии с исходной солью приводит к снижению их растворимости.
3. На основании диаграмм растворимости изученных четырехкомпо-нентных систем разработаны методики синтеза в лабораторных условиях 20 новых тройных соединений. Их индивидуальность доказана методами химического и рентгенофазового анализа.
4. Для синтезированных соединений определены температуры плавления (разложения), плотности, растворимости в ряде органических растворителей. Полученные соединения нерастворимы в бензоле и толуоле, плохо растворимы в диэтиловом эфире, хорошо растворимы в ацетоне и этиловом спирте. Плотности солей металлов с протонированным карбамидом имеют промежуточные значения между плотностями карбамида и солей металлов.
5. В результате испытаний некоторых синтезированных соединений выявлено, что они способствуют повышению урожайности растений на 20 – 40% и не оказывают вредного влияния на качество урожая.
6. Смещение в ИК – спектрах полос валентных колебаний С = О связи в низкочастотную область, С – N связи в высокочастотную область, появление в спектрах соединений полос поглощения ОН – групп свидетельствует о протонировании карбамида по атому кислорода карбонильной группы.
7. Квантово – химическими расчетами установлены геометрические, энергетические и электронные параметры соединения состава ![]() , найденные параметры хорошо согласуются с ИК – спектроскопическими исследованиями, протонизация карбамида приводит к росту его устойчивости.
, найденные параметры хорошо согласуются с ИК – спектроскопическими исследованиями, протонизация карбамида приводит к росту его устойчивости.
Оценка полноты решений поставленных задач. Задачи, поставленные в диссертационной работе, решены полностью. В результате проведенных исследований изучены растворимости в четырехкомпонентных системах соль железа (кобальта, никеля) – неорганическая кислота – карбамид – вода, установлены составы 20 новых соединений, определены оптимальные условия их образования, установлены закономерности взаимного влияния компонентов в системах, идентифицированы синтезированные соединения химическими, физическими и физико – химическими методами исследования, выявлены строение и особенности их энергетических характеристик термодинамической стабильности.
Рекомендации по конкретному использованию результатов исследования. Данные по растворимости в изученных системах дают необходимую информацию для выбора оптимальных условий синтеза новых координационных соединений. Физико – химические характеристики новых соединений дополняют справочные данные по координационным соединениям. Полученные данные вносят вклад в неорганическую, координационную химию, химию водородных связей. Результаты квантово – химических расчетов могут быть использованы в качестве индексов при оценке относительной реакционной способности карбамида, нитрата карбамида и карбамидных комплексов железа и они рекомендуются в качестве справочных данных.
Список опубликованных работ по теме диссертации
1 Еркасов Р.Ш., Абдуллина Г.Г., Рыскалиева Р.Г. Растворимость в системе Fe(NO3)3-CO(NH2)2 -HNO3-H2O при 25 °С// Вестник ПГУ. Серия Химико-биологическая. – 2008. – № 1. – С. 76 – 85.
2 Абдуллина Г.Г., Ерасов Р.Ш., Рыскалиева Р.Г., Оразбаева Р.С. Растворимость в системе CoBr2 - CO(NH2)2 - HBr - H2O при 25 °С// Вестник ПГУ. Серия Химико-биологическая. – 2008. – № 1. – С. 18 – 27.
3 Абдуллина Г.Г., Ерасов Р.Ш., Рысалиева Р.Г., Кокжалова Б.З. Взаимодействие в системе Сo(ClO4)2 - CO(NH2)2 - HClO4 - H2O при 25 °С// Вестник КарГУ. Серия Химия. – 2008. – Т. 50, № 2. – С. 28 – 34.
4 Абдуллина Г.Г., Ерасов Р.Ш., Рыскалиева Р.Г., Оразбаева Р.С. Взаимодействие в системе NiBr2 - CO(NH2)2 - HBr - H2O при 25 °С// Вестник КазНУ. Серия Химическая. – 2008. – Т. 49, № 1. – С. 216 – 220.
5 Абдуллина Г.Г., Ерасов Р.Ш., Рысалиева Р.Г., Байкенов М.И. Взаимодействие в системе NiI2- CO(NH2)2 - HI - H2O при 25 °С// Вестник КарГУ. Серия Химия. – 2008. – Т. 51, № 3. – С. 57 – 63.
6 Рыскалиева Р.Г., Абдуллина Г.Г., Еркасов Р.Ш. Синтез и физико – химические характеристики координационных соединений нитрата железа с протонированным карбамидом// Мaterialy IV miedzynoroowej naukowi –praktycznej konferencji «Nowoczesnych naukowych osiagniec – 2008». Chemia i chemiczne tehnologie Ekologia. Przemysi Nauka I studia. – 1-14 lutego 2008 roku. – T. 14. – С. 65 – 67.
7 Еркасов Р.Ш., Рыскалиева Р.Г., Масакбаева С.Р., Колпек А., Абдуллина Г.Г. Координационные соединения солей s- и d- металлов с протонированными амидами и перспективы их применения// Труды VІ международного Беремжановского съезда по химии и химической технологии. – Караганда, 2008. – C. 348 – 352.
8 Колпек А., Еркасов Р.Ш., Абдуллина Г.Г., Рыскалиева Р.Г. Синтез координационных соединений бромида никеля и сульфата марганца с протонированным карбамидом// Мaterialy IV mezinarodni vdecko – praktika konference «Vda: teorie a praxe – 2008». – Chemie a chemic tehnologie, Ekologie, Zempis a geologie. Praha Publishing House «Education and Science» s.r.o. 2008. – 16-31 srpna 2008 roku. – D. 10. – С. 56 – 58.
9 Абдуллина Г.Г., Еркасов Р.Ш., Колпек А., Рыскалиева Р.Г. Синтез координационных соединений бромида кобальта и нитрата марганца с протонированным карбамидом// Материали за ІV международна научна практична конференция «Научные дни – 2008». – София, 2008. – Т. 16. – С. 16 – 19.
10 Еркасов Р.Ш., Колпек А., Абдуллина Г.Г., Рыскалиева Р.Г. Масакбаева С.Р. Закономерности взаимодействия некоторых галогенидов биометаллов с протонированными амидами// «Валихановские чтения – 13». Материалы международной научно – практической конференции 24 – 26 апреля. – Кокшетау, 2008. – Т. 7. – С. 11 – 12.
11 Абдуллина Г.Г., Еркасов Р.Ш., Масакбаева С.Р., Рыскалиева Р.Г Синтез координационных соединений хлоридов марганца (кобальта) и иодида никеля с протонированными амидами// Мaterialy IV mezinarodni vdecko – praktika konference «Vda: teorie a praxe – 2008». – Chemie a chemic tehnologie, Ekologie, Zempis a geologie. Praha Publishing House «Education and Science» s.r.o. 2008. – 16-31 srpna 2008 roku. – D. 10. С. 16 – 18.
Абдуллина Глнара Госманызы
VІІІ В ТОП МЕТАЛЛ ТЗДАРЫНЫ ПРОТОНДАЛАН КАРБАМИДПЕН КЕШЕНДІ ОСЫЛЫСТАРЫ
Химия ылымдарыны кандидаты ылыми дрежесін алу шін дайындалан диссертацияны авторефераты
02.00.01 – бейорганикалы химия
Тйін
Таырыпты зектілігі. Соы кездегі химия ылымдарыны басты масаттарыны бірі ылыми – практикалы маызы зор жаа крделі кешенді осылыстарды алу, сонымен атар оларды отайлы тзілу жолдарын іздеу, рылымын жне асиеттерін зерттеу болып табылады. Бгінгі тада рамында белсенді биометалл тздары, амид жне бейорганикалы ышыл бар кешенді осылыстарды алу зекті мселеге айналып отыр.
Бейорганикалы ышылдарды амидтермен жне биометалдармен рекеттесуі нтижесінде тзілген німдерді жне рдістерді жйелі зерттеуді нтижесінде р трлі масаттара кеінен олданылатын екілік осылыстарды саны артандыы айындалды. Мндай осылыстар химиялы ндірістерде, ауыл шаруашылыында, медицинада жне органикалы синтез шін кптеп олданылады.
Жмысты масаты мен міндеттері. Ерігіштік дісімен 25 °С температурада VІІІ В тобыны кейбір металл тздарыны сулы ерітінділерде протондалан карбамидпен рекеттесу рдісіні задылытарын анытау, алынан осылыстарды физика – химиялы асиеттерін, рылымын зерттеу жне практикалы маызын айындау.
ойылан масаттарды жзеге асыру шін тмендегі баыттарда зерттеу жмыстары жргізілді: темір (кобальт, никель) тздары – карбамид – бейорганикалы ышыл – су тртрауышты жйені 25 °С температурада ерігіштігін зерттеу; зерттеу нтижесінде тзілген жаа осылыстарды рамын анытау жне оларды синтездеуді отайлы дістерін арастыру; зерттелетін жйедегі рауыштарды бір – бірімен зара сері задылытарын, тзілген кешенді осылыстарды ерігіштігін анытау; синтезделген жаа осылыстарды химиялы, физикалы, физика – химиялы дістер арылы идентификациялау (сйкестендіру); синтезделген кешенді осылыстарды рылымын зерттеу.
Жмысты ылыми жаалыы. Алаш рет: 25 °С температурада рамында темір нитраты, кобальт перхлораты, кобальт (никель) бромиді (иодиді) – карбамид – ышыл – су болатын алты тртрауышты жйені ерігіштігі зерттелді; нтижесінде ш рауышты жйелерді ерігіштігін зертеген кезде алынан екілік осылыстар жне бір мезгілде рамында бастапы рауыштармен бірге шінші рауыш болатын 20 жаа штік кешенді осылыс тзілді; зерттелген жйелердегі осылыстарды зара сері задылытары, тзілген кешенді осылыстарды ерігіштік сипаттамалары аныталды; тзілген 20 жаа кешенді осылысты лабораториялы жадайда алуды отайлы дістері арастырылды; жаа кешенді осылыстар химиялы, физикалы жне физика – химиялы дістер арылы, органикалы еріткіштерде ерігіштігін, тыыздыын, балу температураларын анытау арылы сйкестендірілді; кейбір кешенді осылыстара квантхимиялы есептеулер жргізу нтижесінде, оларды геометриялы, энергетикалы электронды параметрлері аныталды.
орауа сынылан негізгі аидалар.
25 °С температурада темір нитраты, кобальт перхлораты, кобальт (никель) бромиді (иодиді) тздарыны карбамид атысында ышылды ортадаы ерігіштігі; темір нитраты, кобальт (никель) бромиді (иодиді) жне кобальт перхлораты – карбамид – азот (бромсутек, йодсутек, хлор) ышылы – су жйелерінде 25 °С температурада кешен тзілу рдістеріні задылытары; темір, кобальт жне никель тздарыны протондалан карбамидпен р трлі лигандты 20 жаа кешенді осылысты алу дістемесі жне оларды химиялы, рентгенфазалы талдау дістері арылы идентификациялау, алынан осылыстар рамыны физика – химиялы асиеттері; кейбір кешенді осылыстарды геометриялы лшемдері жне болжамды рылымы.
Зерттеу нтижелері:
1. 25 °С темепературада 6 тртрауышты жйедегі сулы ерітіндіден тратын темір нитраты, кобальт (никель) бромиді (иодиді) жне кобальт перхлораты, азот (бром, йод, хлор) ышылдарыны ерігіштігін зерттеу негізінде, осы жйелерден бір мезгілде рамында металл тзы, карбамид жне ышыл болатын 20 жаа кешенді осылыс тзілетіндігі аныталды.
2. Ерігіштік изотермасынан алынан талдау нтижесі тмендегідей: штік осылыстарды ерігіштігі ерітіндідегі ышыл млшеріні суіне байланысты артады, сонымен атар тзсыздану сері байалады, бл былыс ышыл концентрациясыны артуына байланысты осы ерітінділердегі су саныны азаятынын длелдейді; темір (кобальт, никель) тзы – карбамид – су, карбамид – ышыл – су шрауышты жйелеріндегі ерігіштікті зерттеген кезде белгілі болан екілік кешенді осылыстарды кристалданатыны аныталды; ышыл млшеріні артуы металл тздарыны карбамидпен осылыстарыны ерігіштігіне тзданышты сер етеді; жйеге темір (кобальт, никель) тздарын осанда карбамид ышыл ерігіштігіне тзсызданышты сер етеді; металл тзы – карбамид – су жйесіні эвтоникалы рамдарыны ерігіштігі ышылды осанда седі; карбамид – ышыл – су жйесіні эвтоникалы рамдарыны ерігіштігі кп жадайларда бастапы тзды концентарциясыны артуына байланысты тмендейді; бастапы тзбен тепе – тедікте тран ерітінділердегі ышыл концентрациясыны артуы оларды ерігіштігіні тмендеуіне келеді.
3. Тртрауышты жйелерді ерігіштік диаграммалары негізінде 20 жаа штік осылысты лаборатория жадайында синтездеуді тиімді дістері сынылды. Оларды жеке асиеттері химиялы жне рентгенфазалы дістер арылы длелденді.
4. Синтезделген осылыстарды балу температуралары, тыыздытары, органикалы еріткіштерде ерігіштігі аныталды. рамында протондалан карбамиді бар металл тздарыны тыыздыы карбамид пен металл тздары арасындаы аралы мндерге ие болады. Алынан осылыстар толуолда, бензолда ерімейді, диэтил эфирінде нашар ериді, ал этил эфирінде жне ацетонда жасы ериді.
5. Синтезделген осылыстарды ауыл шаруашылыындаы маызы зерттелінді. Нтижесінде бл осылыстарды ауыл шаруашылы німдеріні німділігін 20 – 40 пайыза дейін арттыратыны жне німні рамына зиянды серін тигізбейтіні аныталды.
6. Жаа осылыстарды И спектрлеріндегі С = О байланыстарындаы валенттік тербелістер жиілігіні тменгі жиіліктерге арай ыысуы, ал С – N байланысындаы валенттік тербелістер жиілігі жоары жаына арай ыысуы жне ОН – топтары спектрлерінде сііру жолатарыны пайда болуы карбамидті карбонил тобындаы оттек атомы арылы протондалатынын длелдейді.
7. Темірді кешенді осылыстарыны квантхимиялы есептеулері арылы ![]() кешенді осылысыны геометриялы, электронды жне энергетикалы сипаттамалары аныталды, аныталан параметрлер И – спектріні мліметтеріне сйкес келеді. Кешенді карбамидті протондалуы осылысты тратылыыны суіне келеді.
кешенді осылысыны геометриялы, электронды жне энергетикалы сипаттамалары аныталды, аныталан параметрлер И – спектріні мліметтеріне сйкес келеді. Кешенді карбамидті протондалуы осылысты тратылыыны суіне келеді.
ойылан масатты толы шешімін тапандыын баалау. Диссертациялы жмыста ала ойылан масат толыымен шешімін тапты. Жргізілген зерттеу нтижесінде марганец тзы – карбамид – бейорганикалы ышыл – су тртрауышты жйелеріні ерігіштігі аныталды, 20 жаа кешенді осылыс алынды, оларды лабораториялы жадайда алуды отайлы дістері арастырылды, зерттелген жйелердегі рауыштарды зара серіні задалатары аныталды, синтезделіп алынан осылыстар химиялы, физикалы, физика – химиялы зерттеу дістері арылы сйкестендірілді, оларды электронды, энергетикалы сипаттамаларыны ерекшелігі жне рылымы аныталды.
Зерттеу нтижелерін тжірибе жзінде олдану бойынша сыныстар. Зерттелінген жйелердегі ерігіштік бойынша алынан мліметтер жаа кешенді осылысты синтездеуді отайлы дістерін тадауа ммкіндік береді. Жаа осылыстарды физика – химиялы сипаттамалары кешенді осылыстар бойынша анытамалы мліметтерді толытырады. Алынан мліметтер бейорганикалы, координациялы химия салаларына, сутектік байланыстар химиясына з лесін осады. Квантхимиялы есептеулерді нтижелері карбамидті, темірді карбамидті кешендерді реакциялы абілеттілігін анытаан кезде индекстер ретінде олданылуы ммкін, сондай – а оларды анытамалы мліметтері ретінде сынылуы ммкін.
SUMMARY
to the abstract of thesis for a candidate of chemistry degree
on specialty «02.00.01 - Inorganic chemistry»
Abdullina Gulnara Gosmanovna
COORDINATION COMPOUNDS OF SALTS OF METALS VIII B GROUP WITH THE PROTONIZED CARBAMIDE
Urgency of a theme of research. One of actual problems of inorganic chemistry still has a problem of synthesis and studying of a structure and properties of the compounds which are of interest for the theory and practice. The important role thus belongs to chemistry of coordination compounds with organic ligands, being one of actual directions of a modern chemical science and technology. The coordination compounds containing salts of biometals, amides have a special place.
Working out of scientific bases of synthesis of new coordination compounds on the basis of salts of biometals with the protonized amides in acid medium, studying of their structure, physico – chemical properties, laws of formation for last years start to get regular character.
The work purpose was regular research of processes and products of interaction of some salts VIII In groups with the protonized carbamide in water solutions a solubility method at 25 °С and definition physico – chemical properties of the received compounds.
Into the research problem entered: solubility studying in four-componental systems iron salt (cobalt, nickel) – inorganic acid – a carbamide – water; establishment of structures of formed new compounds, definition of optimum conditions of their formation; establishment of laws of mutual influence of components in the studied systems; identification of the synthesised compounds chemical, physical and physico – chemical methods of research; research of a structure of the synthesized compounds.
Scientific novelty of research. In dissertational work for the first time: solubility is studied at 25 °С in six four-componental systems containing salt iron (cobalt, nickel) – a carbamide – acid – water; in them the compounds which existence has been earlier established at studying of solubility of making three-componental systems, and also 20 new coordination compounds containing in the structure simultaneously initial components are formed; laws of mutual influence of components in the studied systems, character of dissolution of formed coordination compounds are established; optimum conditions of synthesis in laboratory conditions of 20 new compounds are developed; identification of new coordination compounds by methods chemical, X-ray analysis, by definition of temperatures of fusion (decomposition), density and solubilities in organic solvents is spent; geometrical, power and electronic parameters of some coordination compounds on the basis of spent quantum – chemical calculations are defined.
The substantive provisions which are taken out on protection: solubility of ferric nitrate, cobaltous perchlorate, bromides (iodides) of cobalt (nickel), their compounds with a carbamide, and also compounds of a carbamide with nitric, hydrogen bromide, hydrogen iodide, chloric acids in solutions of the corresponding acids and salts containing a carbamide at 25 °С; laws of processes complexing in systems iron nitrate, iodide (bromide) of nickel (cobalt) and cobaltous perchlorate – a carbamide – nitric (hydrogen bromide, hydrogen iodide, chloric) acid – water at 25 °С; techniques of synthesis 20 new coordination compounds of salts of iron, cobalt and nickel with the protonized carbamide and results of identification by their methods chemical, X-ray analysis, physical and chemical properties of the synthesised compounds; prospective structure and geometrical parametres of some coordination compounds.
Results of research:
1. On the basis of solubility studying in 6 four-componental systems containing water solutions of ferric nitrate, bromide, iodide of cobalt (nickel) and cobaltous perchlorate, nitric (hydrogen bromide, hydrogen iodide, chloric) acids, at 25 0С formation in these systems of 20 new coordination compounds containing simultaneously in the structure of salt of metals, a carbamide and acid is established.
2. From the analysis of the received isotherms of solubility follows: solubility of threefold compounds increases with growth maintenances of acids in a solution, i.e. it is shown salting influence to what reduction of values of water number in these solutions with growth of concentration of acids testifies; there is a crystallisation of ephtonical structures and the double coordination compounds, which existence has been established at solubility studying in making three-componental systems iron salt (cobalt and nickel) – a carbamide – water, a carbamide – acid – water; increasing quantities of acids render salting action on solubility of compounds of salts of metals with a carbamide; introduction of salts of iron (cobalt and nickel) renders salting action on solubility carbamide acides; solubility ephtonical structures of systems metal salt – a carbamide – water at acid addition increases; solubility ephtonical structures of systems a carbamide – acid – water in most cases decreases with growth of concentration of initial salt of metal; growth of concentration of acids in the solutions which are in balance with initial salt leads to decrease in their solubility.
3. On the basis of diagrammes of solubility of the studied four-componental systems synthesis techniques in laboratory conditions of 20 new threefold compounds are developed. Their individuality is proved by chemical and X-ray analysis methods
4. For the synthesised compounds temperatures of fusion (decomposition), density and solubility in a number of organic solvents are defined. The received compounds are insoluble in benzene and toluene, it is bad solved in ethoxy ethane, it is good solved in acetone and ethanol. Density of salts of metals with the ptotonized carbamide have intermediate values between density of a carbamide and salts of metals.
5. As a result of tests of some synthesized compounds it is revealed, that they promote increase of productivity of plants on 20 – 40 % and do not render harmful influence on quality of a crop.
6. Displacement of strips in infra-red spectrum of valency fluctuations C = O bond in low-frequency area, C – N bonds in high-frequency area, occurrence in spectra of compounds of strips of absorption OH – groups testifies about protonized carbamide on atom of oxygen carbonyl groups.
7. Quantum – chemical calculations establish geometrical, power and electronic parametres of compounds of the structure, ![]() , found parameters will well be agreed with infra-red spectrum researches.
, found parameters will well be agreed with infra-red spectrum researches.
Estimation of completeness of decisions of tasks in view. The problems put in dissertational work, are solved completely. As a result of the spent researches solubilities in four-componental systems iron salt (cobalt, nickel) – inorganic acid – a carbamide are studied – water, structures of compounds are established, optimum conditions of their formation are defined, laws of mutual influence of components in systems are established, the synthesised compounds by chemical, physical and physical and chemical methods of research are identified, structures and features of their power characteristics of thermodynamic stability are revealed.
Recommendations about concrete use of results of research. Data on solubility in the studied systems give the necessary information for a choice of optimum conditions of synthesis of new coordination compounds. Physico – chemical characteristics of new compounds are supplemented with help data on coordination compounds. The obtained data bring the contribution to inorganic, coordination chemistry, chemistry of hydrogen bridges. Results quantum – chemical calculations can be used as indexes at an estimation of relative reactionary ability of a carbamide, nitrate of a carbamide and carbamide complexes of iron and they are recommended as help data.

