Макрокинетика процессов в щелочном аккумуляторе с модифицированным кадмиевым электродом
На правах рукописи
АКСЮТЕНОК МАРИЯ ВЛАДИМИРОВНА
МАКРОКИНЕТИКА ПРОЦЕССОВ В ЩЕЛОЧНОМ АККУМУЛЯТОРЕ С МОДИФИЦИРОВАННЫМ КАДМИЕВЫМ ЭЛЕКТРОДОМ
Специальность 02.00.04 – Физическая химия
(технические науки)
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата технических наук
Нижний Новгород – 2012
Работа выполнена на кафедре «Технология электрохимических производств» Нижегородского государственного технического университета
им. Р.Е. Алексеева.
Научный руководитель: доктор технических наук, доцент
Гунько Юрий Леонидович
Официальные оппоненты: Плохов Сергей Владимирович
доктор технических наук, профессор
Нижегородский государственный технический университет им. Р.Е. Алексеева, кафедра «Биотехнология, физическая и аналитическая химия», профессор
Наумов Юрий Иванович
кандидат технических наук,
ЗАО «Время–Ч», начальник химико-технологического отдела
Ведущая организация: Нижегородский филиал федерального государственного бюджетного учреждения науки Института машиноведения им. А.А. Благонравова РАН
Защита состоится « 28 » декабря 2012 года в 1200 час. на заседании диссертационного совета Д 212.165.06 при Нижегородском государственном техническом университете им Р.Е. Алексеева по адресу: 603950, г. Нижний Новгород, ул. Минина, д.24.
С диссертацией можно ознакомиться в библиотеке Нижегородского государственного технического университета им Р.Е. Алексеева.
Автореферат разослан «27» ноября 2012 г.
Ученый секретарь диссертационного совета Соколова Т.Н
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Никель-кадмиевый аккумулятор (НКА) – один из самых надежных типов источников тока, поэтому рынок промышленных щелочных аккумуляторов большой емкости для тепловозов, вагонов, авиации, систем автономного энергообеспечения и других ответственных областей применений остается практически монопольным для НКА разного конструктивного исполнения.
Среди существующих конструкций электродов, например, таких как ламельная, металлокерамическая, прессованная – наиболее перспективной является прессованная конструкция ввиду её технологичности, экологичности, малой энергозатратности и высоких удельных характеристик получаемого изделия. Однако прессованные электроды применяются преимущественно в малогабаритных аккумуляторах, поэтому разработка технологии изготовления кадмиевого электрода прессованного типа, работоспособного в условиях свободной сборки электродного блока для аккумуляторов большой емкости остаётся актуальной.
При эксплуатации источника тока ухудшение электрических характеристик кадмиевого электрода в конечном итоге приведёт к ограничению срока службы и выходу из строя никель-кадмиевых батарей. Уменьшение ёмкости кадмиевого электрода при длительном циклировании может быть связано с массопереносом активного вещества в теле электрода. Одной из причин возникновения такого массопереноса является как неравномерность распределения тока по поверхности и глубине электрода, так и возникающие градиенты концентраций компонентов электролита. Данные о распределении тока по поверхности электродов в литературе встречаются довольно часто, в тоже время сведения о распределении тока по толщине электродов практически отсутствуют. Сведения о вертикальном и горизонтальном массопереносе активного вещества в литературе отсутствуют, поэтому оценить вклад каждого из видов массопереноса на стабильность емкостных характеристик кадмиевых электродов затруднительно.
Разработка новых типов НК-аккумуляторов весьма длительна и трудоёмка. Значительно упростить и ускорить процесс конструирования можно с помощью создания математических моделей процессов, происходящих в пористом кадмиевом электроде. Однако модели, описывающие связь процессов в межэлектродном пространстве и в пористых электродах, отсутствуют.
Таким образом, разработка технологии изготовления прессованных кадмиевых электродов и исследование факторов, влияющих на срок их службы, а также моделирование разрядных процессов является актуальной научной и практической задачей.
Целью работы является:
- разработка и реализация математических моделей разряда пористого кадмиевого электрода, позволяющих учитывать концентрационные, структурные и фазовые изменения по высоте и толщине электрода, а также прогнозировать влияние различных факторов на удельные емкостные характеристики электрода;
- исследование факторов, влияющих на срок службы кадмиевых электродов;
- разработка технологии изготовления безламельного прессованного высокоёмкого кадмиевого электрода прессованного типа с длительным сроком службы для тяговых никель-кадмиевых аккумуляторов.
Научная новизна работы
- Разработана адекватная математическая модель разряда пористого кадмиевого электрода, позволяющая оценить работоспособность электродов больших габаритов при различных условиях разряда.
- Впервые оценено влияние конвективных потоков электролита в межэлектродном пространстве НК-аккумулятора на электрические характеристики кадмиевого электрода.
- Впервые показано, что для обеспечения механической прочности необходимо создать в объёме активной массы наряду с системой макропор, систему микропор.
- Исследовано влияние улучшающих добавок, вводимых в активную массу кадмиевого электрода, на процесс окисления кадмия в щёлочи и свойства образующихся плёнок продуктов разряда.
Практическая значимость работы
- Разработанная модель разряда пористого кадмиевого электрода позволяет предсказать поведение данного электрода любых габаритов при различных режимах эксплуатации аккумулятора.
- Разработана технология изготовления безламельного кадмиевого электрода для тяговых НК-аккумуляторов, позволяющая обеспечить высокую механическую прочность и повышенные емкостные характеристики в процессе длительной эксплуатации.
Основные положения диссертации, выносимые на защиту:
- математическая модель процесса разряда пористого кадмиевого электрода учитывающая концентрационные изменения в межэлектродном пространстве;
- создание безламельных кадмиевых электродов;
- влияние добавок на процесс окисления кадмия в ограниченном объёме щелочного электролита;
- экспериментальное распределение токов по высоте электрода при заряде и разряде.
- наличие массопереноса как по высоте, так и по толщине кадмиевых электродов.
- влияние геометрических размеров, состава активной массы на емкостные характеристики кадмиевого электрода.
Апробация работы. Основные результаты работы докладывались и обсуждались на научных конференциях: 15-ая Нижегородская сессия молодых ученых. Технические науки (Нижний Новгород, 2010); 15-ая Нижегородская сессия молодых учёных. Естественные науки (Нижний Новгород, 2010); IX Международная молодёжная научно-техническая конференция «Будущее технической науки» (Нижний Новгород, 2010); X Международная молодёжная научно-техническая конференция «Будущее технической науки» (Нижний Новгород, 2011); XI Международная молодёжная научно-техническая конференция «Будущее технической науки» (Нижний Новгород, 2012).
Публикации. По данным диссертационной работы опубликовано 7 работ, из которых 2 статьи входят в перечень рецензируемых научных журналов; 5 тезисов докладов на международных (3) и региональных (2) конференциях.
Структура и объем диссертации. Работа изложена на 140 страницах машинописного текста и состоит из введения, трёх глав, выводов, списка цитируемых источников, включающего 173 наименования и приложений. Диссертация иллюстрирована 17 таблицами и 37 рисунками.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обосновывается актуальность темы, формулируются цели работы и ее практическая значимость.
В первой главе проведен аналитический обзор имеющихся работ по процессам, протекающим на кадмиевом электроде в щелочных растворах. Рассмотрены существующие конструкции и технологии изготовления кадмиевых электродов и проанализированы факторы, влияющие на срок их службы. Рассмотрены существующие подходы к моделированию электрохимических систем.
Методика эксперимента. Приведены схемы установок и конструкции ячеек, описание методики изготовления электродов, техника проведения различных электрохимических измерений и изучения электрических характеристик пористых кадмиевых электродов. Анализ на содержание в электролите тетрагидроксокадмат-ионов производился методом хронопотенциометрии с накоплением на вращающемся дисковом электроде. В работе использовались хронопотенциометрические, хроновольтамперометрические, импедансные методы исследований. Для измерений применялись потенциостат P-30S и Р-30М, импедансметр Z-500P, а также специальные ячейки, позволяющие изучать особенности окисления кадмиевого электрода в условиях ограниченного объема электролита.
Экспериментальная часть состоит из четырёх разделов.
В первом разделе представлено математическое описание многомерной модели разряда пористого кадмиевого электрода.
При составлении модели предполагалось, что процесс окисления кадмия в щелочном растворе протекает через стадию образования пересыщенного раствора тетрагидроксокомплексов кадмия (реакция 1) с дальнейшим их разложением до гидроксида кадмия (реакция 2):
| (1) | |
| (2) |
Эквивалентная схема кадмиевого электрода, учитывающая распределение тока по его высоте, представлена на рисунке 1. Элемент ![]()
![]() соответствует сопротивлению активной массы и токоподводящей основы. Сопротивления
соответствует сопротивлению активной массы и токоподводящей основы. Сопротивления ![]()
![]() могут быть рассчитаны на основе эквивалентной схемы модели единичной цилиндрической поры пористого кадмиевого электрода, разработанной на кафедре ТЭП НГТУ по уравнению (3):
могут быть рассчитаны на основе эквивалентной схемы модели единичной цилиндрической поры пористого кадмиевого электрода, разработанной на кафедре ТЭП НГТУ по уравнению (3):
![]() (3)
(3)
где j – плотность тока, А/см2;
![]()
![]() – поляризация электрода, включающая в себя отклонение электродного потенциала от равновесного значения в отдельных зонах электрода за счёт концентрационных изменений, падения напряжения в электролите и твёрдой фазе и затруднённость протекания электрохимического процесса.
– поляризация электрода, включающая в себя отклонение электродного потенциала от равновесного значения в отдельных зонах электрода за счёт концентрационных изменений, падения напряжения в электролите и твёрдой фазе и затруднённость протекания электрохимического процесса.
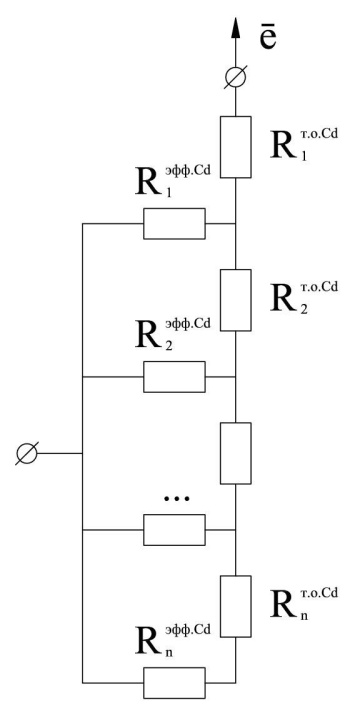 | Рисунок 1 – Модельное представление эквивалентной схемы кадмиевого электрода (разряд): |
Однако схема 1 не отражает в полной мере распределение тока по поверхности кадмиевого электрода, так как не учитывает неравномерность распределения процесса по противоэлектроду. Полная модель будет отражать сопротивления протеканию процессов в поре противоэлектрода, а также сопротивления участков его токопроводящей основы. Кроме того, по высоте электрода необходимо учесть сопротивление электролита и сепаратора, находящегося в межэлектродном пространстве, и тогда схема приобретёт вид (рис. 2)
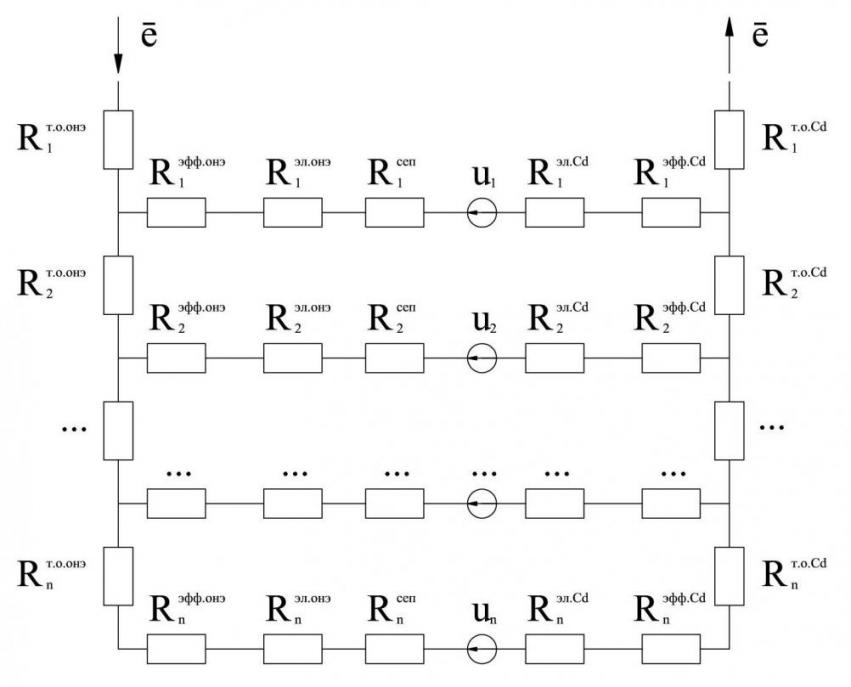
Рисунок 2 – Модель НК-аккумулятора: ![]()
![]() – сопротивление токопроводящей основы кадмиевого электрода,
– сопротивление токопроводящей основы кадмиевого электрода, ![]()
![]() – сопротивление токопроводящей основы оксидноникелевого электрода,
– сопротивление токопроводящей основы оксидноникелевого электрода, ![]()
![]() – сопротивление в поре кадмиевого электрода,
– сопротивление в поре кадмиевого электрода, ![]()
![]() – сопротивление в поре оксидноникелевого электрода,
– сопротивление в поре оксидноникелевого электрода, ![]()
![]() – сопротивление электролита вблизи кадмиевого электрода,
– сопротивление электролита вблизи кадмиевого электрода, ![]()
![]() – сопротивление электролита вблизи оксидноникелевого электрода,
– сопротивление электролита вблизи оксидноникелевого электрода, ![]()
![]() – сопротивление сепарации,
– сопротивление сепарации, ![]()
![]() – источники ЭДС.
– источники ЭДС.
Для упрощения расчётов условно принималось, что эффективные сопротивления противоэлектрода, сопротивления токоподвода и активной массы равны аналогичным величинам для отрицательного электрода. При таком рассмотрении расчёт токов может быть произведён по системе уравнений 4:
 |
Поляризация в уравнении 1 не может быть рассчитана без знания концентрации электролита в порах электрода. Расчёт концентрации в единичной цилиндрической поре нами производился по основному уравнению материального баланса, дополненного выражениями для расчёта изменения концентрации за счёт миграции и протекающих химических и электрохимических реакций. Однако распределение концентрации в единичной цилиндрической поре кадмиевого электрода в значительной мере связано с концентрациями щёлочи в межэлектродном пространстве в зоне кадмиевого электрода.
Концентрация щёлочи в межэлектродном пространстве должна учитывать диффузионный, конвективный перенос и потоки щёлочи через границу электрод/межэлектродное пространство и электролита через сепаратор:
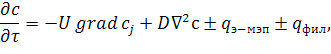 | (5) |
где первое слагаемое в уравнении описывает изменение концентрации за счет возникающих конвективных потоков: u – скорость движения электролита, cj – концентрация гидроксид-ионов;
второе слагаемое – описывает изменение концентрации щёлочи за счет возникающих диффузионных потоков: D – коэффициент диффузии щёлочи;
третье слагаемое – учитывает изменение концентрации за счёт возникающих конвективных потоков на границе электрод/межэлектродное пространство;
четвёртое слагаемое – учитывает изменение концентрации за счёт возникающих фильтрационных потоков электролита через сепаратор.
Расчёт конвективных потоков основан на решении уравнений Навье-Стокса (6):
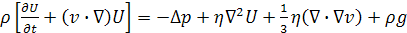 | (6) |
Для полного математического описания движения электролита в межэлектродном пространстве уравнения Навье-Стокса должно быть дополнено уравнением неразрывности потока:
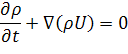 | (7) |
Получить точное решение уравнения Навье-Стокса в условиях свободной конвекции сложно, поэтому нами были введены допущения.
Так как высота электродов значительно больше ширины, то можно не учитывать неравномерность распределения фарадеевских процессов на кадмиевом электроде и противоэлектроде по оси z, а также неравномерность распределения концентрации электролита в этом же направлении. Таким образом, задача из трёхмерной превращается в двухмерную.
Принимается, что сепаратор отстоит от поверхности положительного и отрицательного электродов на одинаковом расстоянии «а» (рис. 3).
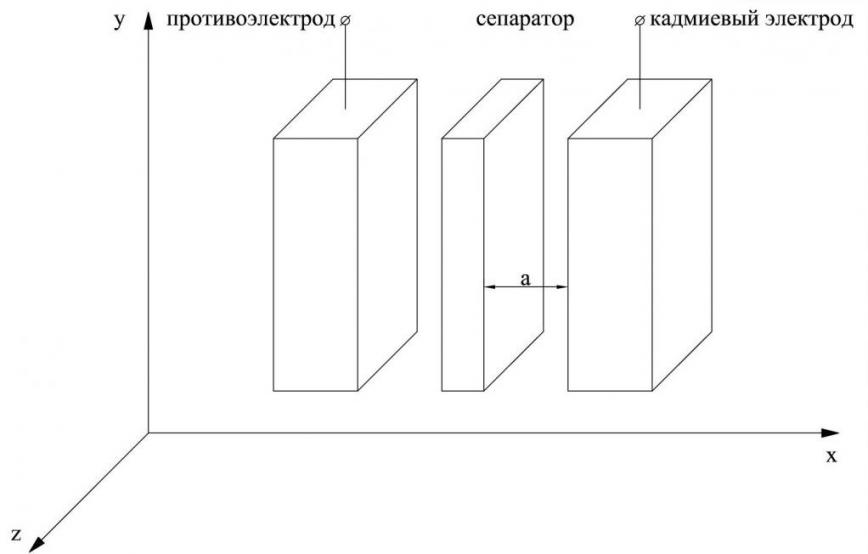 | Рисунок 3 – Блок электродов НК-аккумулятора |
Далее предполагается, что массоперенос в сепараторе затруднён в более значительной степени, чем в межэлектродном пространстве, поэтому градиенты концентраций в межэлектродном пространстве будут значительно меньше, чем в сепараторе и их можно не учитывать. В этом случае, изменение потока в направлении оси х (dux) можно считать равномерным, и при х=а скорость потока по оси х равна скорости фильтрационного потока электролита через сепаратор, которая может быть рассчитана по уравнению 8:
![]() (8)
(8)
где ![]()
![]() – коэффициент фильтрации;
– коэффициент фильтрации; ![]()
![]() – разность давлений по обе стороны сепаратора;
– разность давлений по обе стороны сепаратора; ![]()
![]() – динамическая вязкость;
– динамическая вязкость; ![]()
![]() – толщина сепаратора.
– толщина сепаратора.
В этом случае уравнение неразрывности потока жидкости приобретает вид:
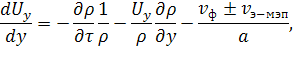 | (9) |
где ![]()
![]() – скорость потока жидкости на границе электрод/межэлектродное пространство, возникающего за счёт изменения пористости электродов и концентрации электролита при разряде;
– скорость потока жидкости на границе электрод/межэлектродное пространство, возникающего за счёт изменения пористости электродов и концентрации электролита при разряде; ![]()
![]() – расстояние от электрода до сепаратора.
– расстояние от электрода до сепаратора.
Таким образом, задача может быть сведена к нахождению конвективного потока только в направлении оси y.
Совместное решение уравнения (6) в направлении оси y и уравнения (9) позволяет рассчитать распределение концентраций щёлочи и возникающие конвективные потоки вдоль положительного и отрицательного электродов. Полученные значения концентраций на разных высотах положительного и отрицательного электродов были использованы для расчётов сопротивлений ![]()
![]() ,
, ![]()
![]() ,
, ![]()
![]() и диффузионных потенциалов, возникающих из-за разности концентраций в зоне положительного и отрицательного электродов. Найденное поле концентраций щёлочи по высоте кадмиевого электрода используется в качестве граничных условий для расчёта концентрации щёлочи и тетрогидроксокадмата по толщине электрода. В дальнейшем производился расчёт поляризации отдельных зон кадмиевого электрода
и диффузионных потенциалов, возникающих из-за разности концентраций в зоне положительного и отрицательного электродов. Найденное поле концентраций щёлочи по высоте кадмиевого электрода используется в качестве граничных условий для расчёта концентрации щёлочи и тетрогидроксокадмата по толщине электрода. В дальнейшем производился расчёт поляризации отдельных зон кадмиевого электрода ![]() по высоте, после чего рассчитывается
по высоте, после чего рассчитывается ![]() по уравнению (3).
по уравнению (3).
Расчёты по разработанной модели показывают, что распределение тока в процессе разряда по высоте электрода значительно меняется (рис. 4).
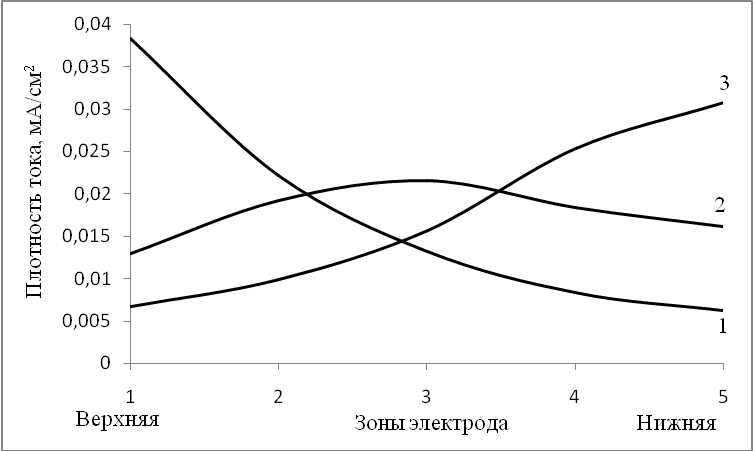 | Рисунок 4 – Расчётное распределение тока по высоте кадмиевого электрода. Время от начала разряда, мин: 1 – 10, 2 – 300, 3 – 456. |
В начальный момент времени основная зона реакции находится в верхней зоне электрода. Постепенно происходит сдвиг зоны сначала в среднюю, а потом в нижнюю зоны электрода.
Это приводит к появлению градиентов концентраций по высоте положительного и отрицательного электродов (рис. 5).
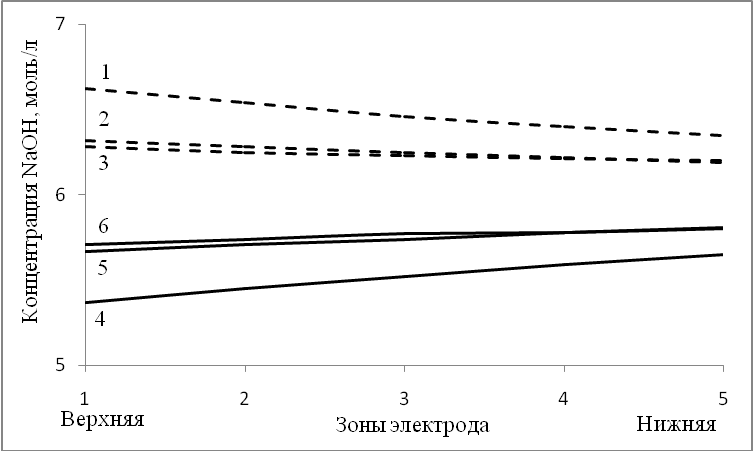 | Рисунок 5 – Расчётное распределение концентрации щёлочи по высоте в зоне положительного (кривые 1,2,3) и отрицательного (кривые 4. 5, 6) электрода. Время от начала разряда, мин: 1, 4 – 10; 2, 5 – 300; 3, 6 – 456. |
В начальный момент времени разряда разница в концентрациях у положительного и отрицательного электрода между верхними и нижними зонами максимальна и достигает соответственно 0,27 и 0,28 моль/л (кривые 1, 4, рис. 5). Однако возникающая разница концентраций в зоне положительного и отрицательного электродов вызывает появление фильтрационных потоков через сепаратор и конвективных потоков вдоль положительного и отрицательного электродов, причём конвективный поток в зоне положительного электрода направлен сверху в низ, а в зоне отрицательного – с низу в вверх. За счёт этих конвективных потоков и смещения зоны реакции разница в концентрациях между верхними и нижними зонами уменьшается и составляет 0,08 моль/л у положительного электрода и 0,09 моль/л у отрицательного электрода.
Такое неравномерное распределение тока и концентрации по высоте кадмиевого электрода приводит к различной работоспособности электродов разных габаритов (рис. 6). Расчёты показывают, что увеличение высоты с 3,5 до 10,5 см приводит к сокращению времени разряда на 30 минут, что качественно согласуется с экспериментально полученными зависимостями (рис. 6). Одновременно увеличение высоты электродов приводит к возрастанию поляризации при его разряде.
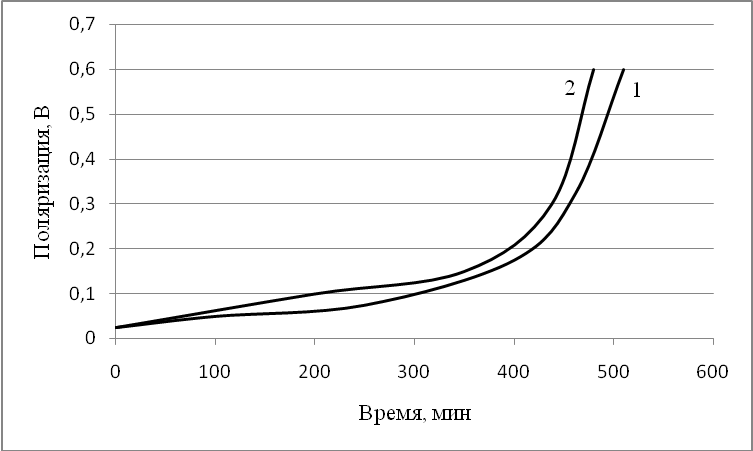 | Рисунок 6 – Расчётная зависимость поляризации от времени разряда. Высота электродов, мм: 1 – 35, 2 – 105. |
Во втором разделе представлена технология изготовления прессованного кадмиевого электрода для тяговых НК-аккумуляторов.
В качестве активного вещества применялся оксид кадмия. Электропроводной добавкой являлся графит, активирующей добавкой – сульфат никеля семиводный. В качестве связующего вещества использовался водно-глицериновый раствор поливинилового спирта. Проводилась оптимизация состава связующего по соотношению воды и глицерина, а также было определено его необходимое содержание в активной массе кадмиевого электрода.
Для создания макропористой структуры вводились порошковые порообразователи на основе борсодержащих соединений – борная кислота и тетраборат натрия. Введение дополнительного количества добавки в активную массу потребовало проведения оптимизации соотношения добавки-порообразователя и связующего вещества. Проведённые исследования не позволили в достаточной степени увеличить механическую прочность и ёмкость электродов.
Анализ экспериментальных данных приводит к выводу о необходимости создания в объёме активной массы наряду с системой макропор и системы микропор. Микропористая структура активной массы создавалась путём её предварительной гидратации.
Дополнительная гидратация активной массы позволила резко снизить набухаемость (~ 1,52 раза) и значительно уменьшить механическое разрушение электродов при циклировании аккумулятора. Повысились емкостные характеристики электродов. Ёмкость гидратированных электродов по сравнению с негидратированными возрасла от 9 до 27% в зависимости от степени гидратации активной массы при разрядной плотности тока 12,5 мА/см2. Электроды сохраняют хорошую работоспособность и при разряде высокими плотностями тока (75,3 мА/см2), ёмкость электродов при этом возрастает на 36% по сравнению с ёмкостью негидратированных электродов.
В ходе дальнейших исследований для предварительно гидратированного активного вещества было рекомендовано использовать в качестве порообразователя – тетраборат натрия или гидроксид лития. С целью создания прочных эластичных плёнок ПВС, удерживающих активную массу на токоподводе и обеспечивающих за счёт этого дополнительную механическую прочность электродов, проводилась их термообработка.
Кадмиевые электроды, изготовленные по предложенной технологии, включающей введение порошкового порообразователя и стадию предварительной гидратации активной массы, имеют высокие коэффициенты использования активного вещества. Для электродов, в состав активной массы которых входит гидроксид лития, коэффициент использования активного вещества составляет ~ 60 70%, для электродов с тетраборатом натрия ~ 55 65%.
Третий раздел посвящён исследованию влияния вводимых добавок на процесс окисления кадмия в ограниченном объёме щелочного электролита.
Для выяснения кинетических параметров процесса окисления кадмия в условиях ограниченного объема электролита, характерных для разряда пористого кадмиевого электрода никель-кадмиевого аккумулятора, были проведены хронопотенциометрические исследования с использованием тонкослойной ячейки.
На основании полученных зависимостей окисления кадмия в электролитах, содержащих добавки гидроксида лития и тетрабората натрия, были рассчитаны значения концентрации и кажущиеся коэффициенты диффузии ионов гидроксокомплекса кадмия (табл. 1).
Таблица 1 Концентрации и кажущиеся коэффициенты диффузии гидроксокомплексов кадмия в 6,25 М растворах NaOH в присутствии добавок гидроксида лития и тетрабората натрия.
| Добавка в электролит | С·102, моль/л | D·105, см2/с |
| Контрольный | 3,17 | 40 |
| Na2B4O7·10Н20 | 2,18 | 26 |
| LiOH· H2O | 1,23 | 13 |
Полученные значения концентраций тетрагидроксокадмат-ионов в приэлектродном слое значительно превышают равновесные концентрации, что может свидетельствовать об образовании пересыщенных тетрагидроксокадматных растворов. Коэффициенты диффузии кадмат-ионов также аномально высоки по сравнению с приводимыми в литературе. Это может указывать на протекание химической реакции разложения образующегося пересыщенного кадматного раствора, в результате чего и происходит быстрая убыль концентрации кадмат-ионов в зоне реакции не только из-за диффузионного переноса кадмат-ионов, но и за счёт протекания реакции (2). На возможность протекания такой химической реакции указывают переменнотоковые исследования.
Свойства образующихся на кадмии твёрдофазных слоёв были также исследованны методом фарадеевского импеданса.
Наиболее точно полученные экспериментальные данные моделируются эквивалентной схемой (рис. 7).
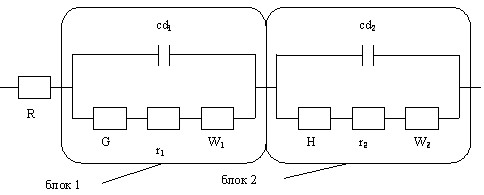
Рисунок 7 – Эквивалентная схема границы электрод-раствор: Rр-ра –сопротивление электролита между рабочим и вспомогательным электродами, cd1и cd2 – емкости двойных электрических слоёв на границах плотная плёнка/электролит и металл/плотная плёнка, r1 и r2 – омические сопротивления слоёв продуктов окисления кадмиевого рабочего электрода, W1 и W2 – сопротивление диффузии (импеданс Варбурга), G –сопротивление гомогенной химической реакции (импеданс Геришера), Н – сопротивление гетерогенной химической реакции (импеданс Хайкина).
Эквивалентная схема состоит из двух последовательно соединённых блоков. Блок 1, по нашему мнению, описывет процессы в рыхлой внешней плёнке![]() , а блок 2 – в плотной внутренней плёнке
, а блок 2 – в плотной внутренней плёнке ![]() .
.
Как видно из схемы, после прохождения стадии ионизации кадмия, образующиеся ионы диффундируют к границе плотная плёнка/электролит (W2) с последующей химической реакции образования тетрагидроксокадмат-ионов (Н). Образовавшиеся тетрагидроксокадмат-ионы диффундируют в порах рыхлой плёнки к границе раздела рыхлая плёнка/электролит (W2) с последующим протеканием химической реакции их разложения (G).
Полученные сопротивления рыхлых и пассивирующих твёрдофазных плёнок, образующихся на кадмии в 6,25 М растворе NaОН представлены в таблице 2.
Таблица 2 Сопротивления плёнок на поверхности кадмиевого электрода. Поляризация 50 мВ
| Электролит без добавок | Электролит с добавкой LiОН· H2О | Электролит с добавкой Na2B4O7·10Н20 | |||
| Сопротивление плёнок, Ом·см2 | Сопротивление плёнок, Ом·см2 | Сопротивление плёнок, Ом·см2 | |||
| r1 | r2 | r1 | r2 | r1 | r2 |
| 4.6 | 2.0 | 1.6 | 5 | 1 | 1.2 |
Сопротивление плотных плёнок в присутствии лития увеличивается, в присутствии тетрабората натрия уменьшается. Сопротивление рыхлых плёнок в присутствии добавок снижается, что может быть связано с образованием плотных плёнок, обладающих повышенным сопротивлением диффузии (табл. 3) и препятствующих нарастанию рыхлого слоя продуктов.
Таблица 3 Значения сопротивления диффузии в плотной плёнке CdO в зависимости от состава электролита
| Электролит | 6 М раствор NaOH | 6 М раствор NaOH c добавкой LiОН· H2О | 6 М раствор NaOH c добавкой Na2B4O7·10Н20 |
| W2, | 119 | 130 | 361 |
Таким образом, процесс окисления кадмия происходит при наличии на поверхности плотной и рыхлой плёнки. Образующиеся плёнки влияют на скорость химических и электрохимических реакций, и могут оказать влияние на характеристики пористых кадмиевых электродов в НК-аккумуляторах.
Четвёртый раздел посвящён выявлению влияния различных факторов на электрические характеристики кадмиевых электродов при циклировании никель-кадмиевых аккумуляторов.
В процессе длительного циклирования происходит самопроизвольное уменьшение ёмкости кадмиевых электродов (рис.8).
На величину отдаваемой ёмкости в процессе эксплуатации аккумулятора оказывает влияние состав активной массы отрицательного электрода и его механическая прочность. Максимальные емкостные характеристики сохранялись на протяжении всего срока испытания у электродов, содержащих в качестве порообразователя гидроксид лития и тетраборат натрия.
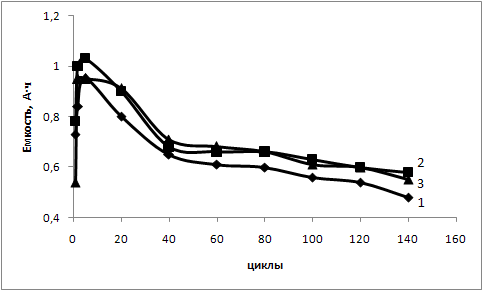 | Рисунок 8 – Разрядная ёмкость электродов при циклировании. Порообразователь в активной массе: 1 – отсутствует; 2 – LiOH·H2O; 3 – Na2B4O7·10H2O. Разрядная плотность тока 12,5 мА/см2. |
Снижение емкости электродов в процессе длительного циклирования может быть связано с укрупнением частиц активного вещества или с его массопереносом. Установлено, что после прохождения 100 циклов заряд-разряда происходит перенос активного вещества от токоотвода в средние зоны электрода (рис. 9). Это может быть связано с образованием тетрагидроксокадматного раствора с максимальной степенью пересыщения в конце разряда в зоне токоотвода, на что указывают расчёты по разряду пористого кадмиевого электрода в рамках одномерной модели.
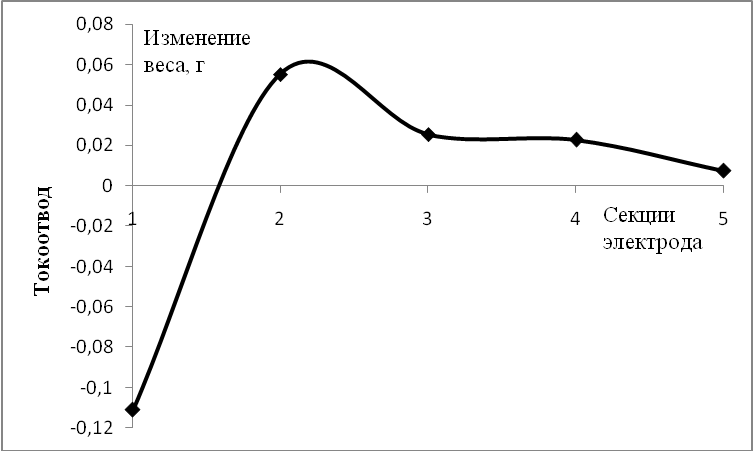 | Рисунок 9 – Изменение веса отдельных секций кадмиевого электрода по толщине после 100 циклов. Разрядная плотность тока 8,4 мА/см2. |
Явление массопереноса наблюдалось также по высоте электрода (рис. 10). Экспериментально было определено, что в верхних зонах электрода происходит убыль активного вещества, при этом в средних наблюдается его максимальное накопление, а в нижней фактически не происходит никаких изменений массы активного вещества (рис. 10).
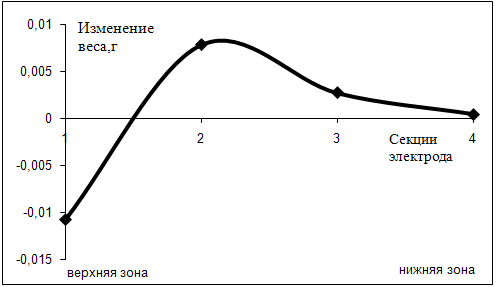 | Рисунок 10 – Изменение веса секций электрода по высоте кадмиевого электрода после 100 циклов. Разрядная плотность тока 8,4 мА/см2. |
Показано, что массоперенос по высоте электрода на порядок меньше, чем по толщине. Это может быть связано с различными расстояниями, на которых происходит массоперенос (толщина исследуемых электродов в данном опыте лежит в пределах 3 – 4 мм, а высота – около 100 мм).
Появляющиеся градиенты концентраций щёлочи и тетрагидроксокадмат-ионов в основном связаны с неравномерностью распределения тока по поверхности (рис. 11).
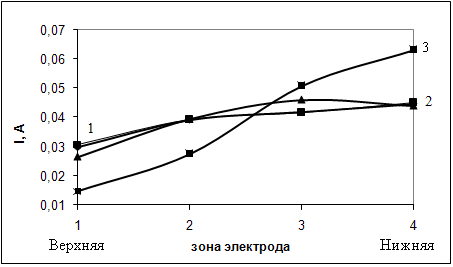 | Рисунок 11 – Экспериментальное распределение тока по высоте кадмиевого электрода. Время с начала разряда, ч: 1 – 1; 2 – 3,5; 3 – 7. Порообразователь – Na2B4O7·10H2O. |
В ходе проведения разряда наблюдается постепенное смещение зоны реакции в нижние зоны электрода (рис. 11). Такой постепенный сдвиг связан с изменением степени окисленности отдельных зон при разряде, а также с уменьшением концентрации щёлочи в верхних зонах электрода.
Аналогичные зависимости характерны и для зарядного процесса (рис. 12). Неравномерное распределение тока у поверхности электрода приводит к возникновению вертикальных градиентов концентрации щёлочи в межэлектродном пространстве. Концентрационные изменения могут быть связаны как со смещением зоны реакции в нижнюю часть электродов, так и с выделением щелочи на кадмиевом электроде и её поглощением на положительном электроде при заряде и обратными процессами при разряде.
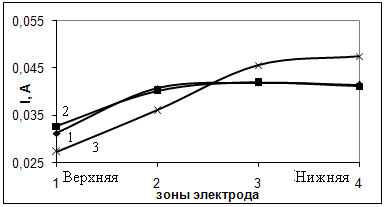 | Рисунок 12 – Экспериментальное распределение тока по высоте кадмиевого электрода. Время с начала заряда, ч: 1 –1; 2 – 3,5; 3 – 7. Порообразователь – Na2B4O7·10H2O. |
В результате описанных явлений могут возникнуть конвективные потоки вдоль поверхности положительного и отрицательного электродов, вносящие свой вклад в кинетику изменения концентрации электролита у поверхности электрода.
Большее различие в распределении тока по высоте электрода при разряде, по сравнению с зарядом, обусловлено, по нашему мнению, значительным влиянием концентрации электролита на разрядный процесс, сопровождающейся уменьшением содержания щёлочи в порах электрода. Меньшие концентрации щёлочи в верхней зоне межэлектродного пространства у поверхности кадмиевого электрода на протяжении всего разряда приводят к снижению диффузионного потока гидрокид-ионов вглубь активной массы и способствуют смещению токов в нижнюю зону отрицательного электрода. Возникающие вертикальные концентрационные градиенты по щёлочи будут зависеть от высоты электрода и разрядной плотности тока (табл. 4).
Таблица 4 – Распределение концентрации электролита по высоте электродов в зависимости от разрядной плотности тока. Время с начала разряда 3,5 часа.
| Высота электродов, мм | Разрядная плотность тока, мА/см2 | Высота отбора проб | |
| 8,2 | 29 | ||
| Концентрация электролита, моль/л | |||
| 35 | 6,2 | 6,8 | Верхняя зона |
| 6,4 | 6,9 | Средняя зона | |
| 6,7 | 7,3 | Нижняя зона | |
| 70 | 6,0 | 6,0 | Верхняя зона |
| 6,3 | 6,8 | Средняя зона | |
| 6,0 | 7,2 | Нижняя зона | |
| 105 | 6,5 | 6,0 | Верхняя зона |
| 7,7 | 7,4 | Средняя зона | |
| 7,6 | 7,4 | Нижняя зона | |
Более значительные концентрационные градиенты щёлочи при увеличении высоты электродов сказались и на их разрядных характеристиках (рис. 13). Даже увеличение высоты с 35 до 70 мм привело к снижению емкостных характеристик на 5%. Дальнейшее увеличение высоты до 105 мм приводит к снижению ёмкости до 9%. При этом наблюдается увеличение электродной поляризации на ~ 50 мВ.
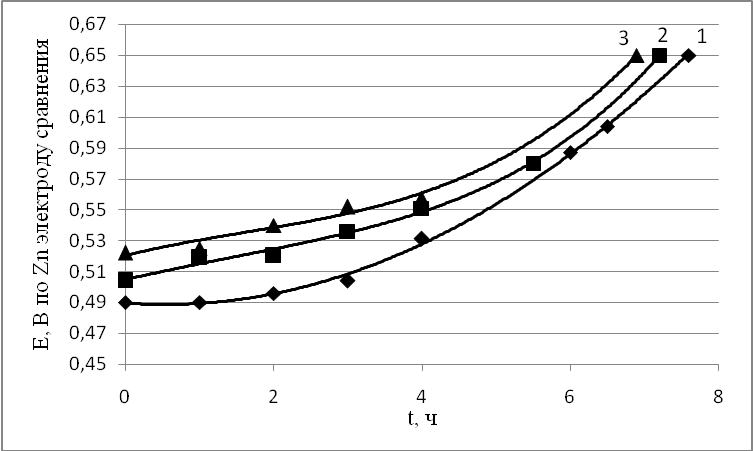 | Рисунок 13 – Влияние высоты электродов на разрядные кривые. Высота электродов, мм: 1 – 35, 2 – 70, 3 – 105. Разрядная плотность тока 8,2 мА/см2. |
Моделирование процесса разряда кадмиевого электрода по его толщине также показало существенное влияние на соответствующие процессы концентрации электролита.
Прямые опыты по разряду кадмиевого электрода в электролитах разных концентраций показали, что с увеличением концентрации NaOH с 4 до 5,5 моль/л происходит возрастание ёмкости кадмиевого электрода на 12%. Дальнейшее повышение до 7 М увеличивает разницу в ёмкостях до 18%.
Выводы
1. Выявлены макрокинетические закономерности процессов в щелочном аккумуляторе на модифицированном кадмиевом электроде, позволяющие рассчитать поляризацию кадмиевого электрода в зависимости от его габаритов и условий разряда.
2. Впервые теоретически установлено и экспериментально подтверждено наличие градиента концентрации щёлочи по высоте в межэлектродном пространстве. Установлена зависимость изменения концентрации щёлочи и разрядной плотностью тока от высоты электрода и принятого режима разряда.
3. Методом фарадеевского импеданса подтверждено двухслойное строение плёнки продуктов реакции окисления кадмия. Определены сопротивления плотного и рыхлого слоёв в присутствии различных добавок. Показано, что кинетика окисления кадмия в щёлочи связана с замедленностью протекания гомогенных и гетерогенных реакций, а также с замедленной диффузией продуктов реакции в плотной и рыхлой плёнках.
4. Разработана технология изготовления прессованного кадмиевого электрода, работоспособного в условиях свободной сборки электродного блока, обладающего высокой механической прочностью и повышенными емкостными характеристиками (0,55 – 0,6 А·ч/см3).
5. Показана необходимость создания системы макро- и микропор за счёт введения порообразователей и гидратации активного вещества.
6. Впервые выявлен массоперенос активного вещества, как по толщине, так и по высоте электрода.
Основное содержание диссертации опубликовано в работах:
1. Аксютенок, М.В. Моделирование зарядно-разрядных процессов на кадмиевом электроде никель-кадмиевого аккумулятора / М.В. Аксютенок, Ю.Л. Гунько, Козина О.Л., М.Г. Михаленко, А.А. Москвичев // Известия высших учебных заведений. Химия и химическая технология. – 2012. – Т. 55. № 4. – С. 96 – 99.
2. Аксютенок, М.В. Особенности окисления кадмия в ограниченном объеме щелочного электролита / М.В. Аксютенок, Ю.Л. Гунько, А.А. Москвичев, О.Л. Козина, М.Г. Михаленко // Вестник Нижегородского университета им. Н.И. Лобачевского. – 2012. – № 4. – С. 154 – 158.
3. Аксютенок, М.В. Влияние добавки гидрокида лития на процесс окисления кадмия в ограниченном объеме щелочного электролита // Труды Нижегородского государственного технического университета им. Р.Е. Алексеева. – Н. Новгород. – 2012. – № 1 (94). – С. 255 – 260.
4. Аксютенок, М.В. Разработка технологии изготовления безламельного кадмиевого электрода НК-аккумулятора (тезисы)/ М.В. Аксютенок, Ю.Л. Гунько // ХV Нижегородская сессия молодых ученых. Технические науки. – Н. Новгород. – 2010. – С. 81 – 82.
5. Аксютенок, М.В. Выбор связующего вещества для кадмиевого электрода прессованного типа / М.В. Аксютенок, Ю.Л. Гунько // ХV Нижегородская сессия молодых ученых. Естественно-научные дисциплины. – Н. Новгород. – 2010. – С. 108.
6. Аксютенок, М.В. Распределение тока по высоте при заряде и разряде кадмиевого электрода никель-кадмиевого аккумулятора (тезисы) / М.В. Аксютенок, Ю.Л. Гунько // Тезисы докладов Х Международной молодежной научно-технической конференции «Будущее технической науки». – Н.Новгород: НГТУ, 2011. – С. 237.
7. Аксютенок, М.В. Массоперенос активного вещества по высоте кадмиевого электрода НК-аккумулятора / М.В. Аксютенок, Ю.Л. Гунько // Тезисы докладов ХI Международной молодежной научно-технической конференции «Будущее технической науки». – Н.Новгород: НГТУ, 2012. – С. 283.
8. Аксютенок, М.В. Создание безламельных кадмиевых электродов с длительным сроком службы в условиях свободной сборки (тезисы) / М.В. Аксютенок, Ю.Л. Гунько // Тезисы докладов IX Международной молодежной научно-технической конференции «Будущее технической науки». – Н.Новгород: НГТУ 2010. – С. 207.

