Физико-химические характеристики электрохимических реакций на границaх раздела молибденовый, вольфрамовый электроды – раствор
УДК 544.653+543.257.2 На правах рукописи
НУРТАЕВА ЖАННА ТУЛЕГЕНОВНА
ФИЗИКО-ХИМИЧЕСКИЕ ХАРАКТЕРИСТИКИ ЭЛЕКТРОХИМИЧЕСКИХ РЕАКЦИЙ НА ГРАНИЦAХ РАЗДЕЛА
МОЛИБДЕНОВЫЙ, ВОЛЬФРАМОВЫЙ ЭЛЕКТРОДЫ – РАСТВОР
02.00.04 – физическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Республика Казахстан
Караганда, 2010
Работа выполнена на кафедре химии и химической технологии
Западно-Казахстанского аграрно-технического университета
имени Жангир хана
Научные руководители: доктор химических наук,
профессор Мендалиева Д.К.
кандидат химических наук,
Кунашева З.Х.
Официальные оппоненты: доктор химических наук,
профессор Амерханова Ш.К.
кандидат химических наук,
Давренбеков С.Ж.
Ведущая организация: АО «Институт химических
наук имени А.Б. Бектурова»
Защита состоится 27 ноября 2010 года в 1100 часов на заседании диссертационного совета ОД 14.07.01 при Карагандинском государственном университете имени академика Е.А. Букетова по адресу: 100028, г. Караганда, ул. Университетская, 28, химический факультет, актовый зал.
С диссертацией можно ознакомиться в библиотеке Карагандинского государственного университета имени академика Е.А. Букетова.
Автореферат разослан « » октября 2010 г.
Ученый секретарь
Диссертационного совета ОД 14.07.01.,
доктор химических наук,
профессор Салькеева Л.К.
ВВЕДЕНИЕ
Общая характеристика работы. Диссертационная работа посвящена исследованию физико-химических характеристик электрохимических реакций на границе раздела молибденовый, вольфрамовый электроды – водные растворы потенциалопределяющих ионов.
Актуальность темы. Современные представления в области электрохимии как науки о механизме электродных процессов дают возможность осуществить целенаправленное проведение электрохимических реакций. Одним из направлений электрохимии, раздела физической химии, является поиск новых металлических электродов, обладающих высокой чувствительностью, коррозионной стойкостью и другими электродными характеристиками, а также совершенствование известных индикаторных электродов. Металлические индикаторные электроды должны удовлетворять не только требованиям высокой электропроводности, химической и термической стабильности, механической прочности, но и должны обладать сравнительной дешевизной, доступностью, удобством в изготовлении, эксплуатации и хранении. Поэтому в настоящее время продолжается поиск новых высокоэффективных электродных материалов. Среди металлов, перспективных для изготовления индикаторных электродов, несомненный интерес представляют молибден и вольфрам, которые устойчивы в агрессивных средах, обладают ценными физико-химическими свойствами, характеризуются относительной дешевизной и доступностью, особенно на территории Казахстана. Изучение проблем, протекающих на границе раздела фаз в различных электрохимических системах из молибдена и вольфрама, представляет теоретический и практический интерес, так как позволяет сделать вывод о возможности применения этих металлов в качестве индикаторных электродов в потенциометрии.
Цель работы заключалась в установлении закономерностей электрохимических реакций, протекающих на границах раздела фаз молибденовый, вольфрамовый электроды - водные растворы потенциалопределяющих ионов и возможности использования их в вариантах потенциометрии.
Для достижения поставленной цели в работе необходимо было решить следующие задачи:
- создание электродов на основе особо чистых металлических молибдена и вольфрама, определение условий проведения исследований, учитывающих природу металлов, выбранных в качестве индикаторных электродов и природу потенциалопределяющих ионов;
- установление электрохимических характеристик молибденового и вольфрамового электродов в растворах ионов металлов меди (II), хрома (III), цинка (II), кадмия (II), никеля (II), кобальта (II), свинца (II), стронция (II) в зависимости от концентрации потенциалопределяющих ионов;
- установление электрохимических характеристик молибденового и вольфрамового электродов в растворах анионов: кислородcодержащих (B4O72-, Cr2O72-, HPO42-) и бескислородных (F-, Cl-, Br-, I-), в зависимости от концентрации потенциалопределяющих ионов;
- определение термодинамических характеристик электрохимических реакций, протекающих на границе раздела молибденовый, вольфрамовый электроды - растворы потенциалопределяющих ионов и установление закономерностей возникновения электродной функции на границе раздела фаз;
- установление возможности использования молибденового и вольфрамового электродов в потенциометрическом титровании ионов меди (II), хрома (III), свинца (II), хрома (VI) и их практического применения в потенциометрическом определении ионов хрома (VI).
Объектами исследования являются индикаторные электроды из металлических молибдена и вольфрама.
Предметом исследования являются электрохимические реакции на границах раздела молибденовый, вольфрамовый электроды – раствор.
Научная новизна результатов заключается в том, что:
- сконструированы электроды из особо чистых металлических молибдена и вольфрама, определены условия функционирования исследуемых электродов: оптимальное значение рН раствора, влияние ионной силы раствора, оптимальная температура;
- определены основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах солей металлов: меди (II), хрома (III), цинка (II), кадмия (II), никеля (II), кобальта (II), свинца (II), стронция (II);
- определены основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах кислородсодержащих (B4O72-, Cr2O72-, H2PO4-) и бескислородных (F-, Сl-, Br-, I-) анионов;
- оценены термодинамические параметры (G#, H#, S#) электрохимических реакций на границе раздела молибденовый, вольфрамовый электроды – растворы потенциалопределяющих ионов; показано, что на межфазной границе Мо(W)-ионы металла наиболее энергетически выгоден процесс с участием ионов Cu (II) и Cr (III); а на межфазной границе Мо(W)-раствор аниона энергетически выгодны электродные реакции кислородсодержащих анионов.
- установлена возможность использования молибденового и вольфрамового электродов в качестве индикаторных в потенциометрическом титровании ионов меди (II), хрома (III), свинца (II), хрома (VI).
Связь темы с планом научно-исследовательских работ. Диссертационная работа выполнена в рамках программы фундаментальных исследований «Разработка научных основ новых технологий и создание перспективных материалов различного функционального назначения» по теме «Исследования электрохимических реакций на d-элементах (титан, молибден, вольфрам), разработка на их основе индикаторных электродов и использование их в эколого-аналитическом контроле» № госрегистрации 0109РК00414, проводимой на кафедре химии и химической технологии Западно-Казахстанского аграрно-технического университета имени Жангир хана (г.Уральск).
Основные положения, выносимые на защиту:
- рабочие условия исследуемых электродов: рН-чувствительность, влияние ионной силы раствора, время установления стабильного потенциала, влияние температуры;
- основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах солей металлов: меди (II), хрома (III), цинка (II), кадмия (II), никеля (II), кобальта (II), свинца (II), стронция (II);
- основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах кислородсодержащих (B4O72-, Cr2O72-, H2PO4-) и бескислородных (F-, Сl-, Br-, I-) анионов;
- термодинамические параметры электрохимических реакций на границе молибденовый, вольфрамовый электроды - растворы потенциалопределяющих ионов;
- возможность потенциометрического титрования модельных растворов меди (II), хрома (III), свинца (II), хрома (VI) с использованием молибденового и вольфрамового электродов в качестве индикаторных;
- результаты определения ионов хрома (VI) в технической воде с индикаторными молибденовым и вольфрамовым электродами.
Практическая ценность работы. Предложены электроды из элементов VI группы молибдена и вольфрама, проявляющие электродную функцию к ряду потенциалопределяющих ионов в широком диапазоне концентраций. Экспериментально обоснована возможность применения металлических молибденового и вольфрамового электродов для потенциометрического титрования ионов хрома (VI) в пробах технической воды.
Результаты работы используются в лекционном и практическом курсах «Физико-химические методы анализа», читаемом в Западно-Казахстанском аграрно-техническом университете для специальностей «Химическая технология органических веществ» и «Химическая технология неорганических веществ».
Апробация работы. Основные результаты работы обсуждались на региональной научно-практической конференции «Реализация стратегии индустриально-инновационного развития республики Казахстан» (Актобе, 2006); X международной научной конференции «Наука и образование – ведущий фактор стратегии «Казахстан-2030» (Караганда, 2007); международной научной конференции молодых ученых «Наука и образование-2007» (Астана, 2007); международной конференции «Экоаналитика Центральной Азии» (Алматы, 2007); международной научно-практической конференции «Экономическое, социальное и культурное развитие Западного Казахстана: история и современность» посвященной 180-летию Оружейной Палаты Бокеевского ханства (Уральск, 2008); 2-ом международном форуме «Аналитика и аналитики» (Воронеж, 2008); на VIII Всероссийской конференции «Аналитика Сибири и Дальнего Востока» (Томск, 2008); на 238-ой конференции Американского химического сообщества (ACS) (Вашингтон, 2009), IV международной конференции «Фундаментальные и прикладные проблемы получения новых материалов: исследования, инновации и технологии» (Астрахань, 2010).
Публикации. По теме диссертации опубликовано 14 работ. Из них 9 статей, 5 тезисов докладов.
Личный вклад автора заключается в непосредственном выполнении экспериментальной части работы, обработке и интерпретации полученных результатов и оформлении их в виде научных публикаций.
Объем и структура работы. Диссертация изложена на 121 страницах машинописного текста, включая 44 рисунка, 55 таблиц. Диссертационная работа состоит из введения, 5 глав, выводов, списка цитируемой литературы, содержащего 110 наименований.
Основное содержание работы
Во введении обоснована актуальность, сформулированы цель и задачи исследования, научная новизна и практическая значимость работы.
1 Характеристики электрохимических процессов протекающих
на границе металл-раствор
Этот раздел посвящен анализу современного состояния электрохимических методов исследования с твердыми, в том числе металлическими, электродами и состоит из 5 пунктов. В разных работах показано практическое применение медного, серебряного, ртутного, платинового и др. металлических электродов в потенциометрии. Работы по подробному изучению электрохимических реакций ионов на молибденовом и вольфрамовом электродах в литературе отсутствуют.
2 Экспериментальная часть
В главе приводится описание материалов и методов, использованных для изготовления электродов, методик экспериментов, оборудования и реактивов.
3 Электрохимические процессы на границах раздела молибденовый, вольфрамовый электроды – потенциалопределяющие ионы
Измерение ЭДС и установление электродной функции исследуемых электродов к различным ионам позволяет сделать вывод о возможности применения их в качестве индикаторных в потенциометрии.
3.1 Выбор условий исследования
Время установления стабильного потенциала свидетельствует о скорости установления обратимого электрохимического процесса на границе раздела фаз поверхность электрода - потенциалопределяющий ион. Для молибденового электрода это время составило в среднем 1-1,5 минуты; в случае вольфрамового электрода – не более 1 минуты. Воспроизводимость результатов измерения ЭДС обоих электродов, полученных в течение всего периода исследований и рассчитанных методом математической статистики составляет ±2 мВ.
Функционирование электрода связано с активностью, а не с концентрацией определяемого вещества. В связи с этим, в качестве фонового электролита был выбран нитрат калия, который позволяет поддерживать ионную силу раствора постоянной.
Учитывая установленную рН-зависимость исследуемых электродов, прямые потенциометрические измерения проводили при постоянном значении рН, равном 6,5, которое поддерживались с помощью 0,1 М растворов HNO3 и KOH.
3.2 Поведение молибденового и вольфрамового электродов в растворах ионов металлов
Для изучения основных характеристик электродов: электродная функция, время установления стабильного потенциала, воспроизводимость в растворах исследуемых ионов металлов, рабочий интервал, выбраны соли меди (II), свинца (II), цинка, никеля, кадмия, кобальта, хрома (III) и стронция различных концентраций, приготовленные в растворе 1,0 М KNO3.
Электродные функции металлических электродов исследовали, измеряя ЭДС электрохимической цепи:
Мо,W Исследуемый раствор КCI (нас.) AgCI/ Ag
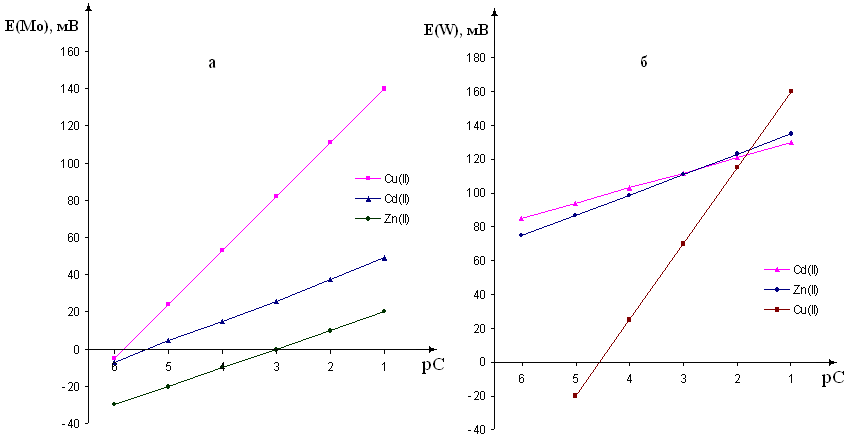
Рисунок 1 – Электродные функции молибденового (a) и вольфрамового (б) электродов в растворах Cu2+, Cd2+ и Zn2+
Как видно из рисунка 1 (а), молибденовый электрод проявляет электродную функцию к ионам меди (II), цинка и кадмия в диапазоне концентраций 1,0·10-6-1,0·10-1 моль/л. Характер функций прямолинеен. Значение тангенса угла наклона различно и составляет для ионов меди (II) 29±2 мВ, для ионов кадмия и цинка 11±2 мВ. Вольфрамовый электрод (рисунок 1 б) функционирует по отношению к ионам меди в интервале концентраций 1,0·10-5-1,0·10-1 моль/л, к ионам кадмия и цинка в области концентраций 1,0·10-6-1,0·10-1 моль/л. Характер функций прямолинеен. Значение тангенса угла наклона составляет для ионов меди (II) 45±2 мВ, для ионов кадмия и цинка – 9±2 мВ.
Молибденовый и вольфрамовый электроды проявляют стабильную электродную функцию к изученным катионам металлов, являющимся по своей природе d-элементами, а также р- и s-элементами в случае Pb2+ и Sr2+. По уменьшению чувствительности к ионам d-элементов для исследуемых металлических электродов можно составить следующие ряды:
Мо: Cu2+>Cr3+>Cd2+=Zn2+>Co2+>Ni2+; W: Cu2+>Cr3+>Cd2+=Zn2+>Co2+>Ni2+
По отношению к ионам Сr (III) электроды показывают одинаковые значения тангенса угла наклона электродных функций; к ионам Cu (II) – W>Мо; к ионам Сd (II) и Zn (II) – Мо>W; к ионам Ni (II) и Co (II) изученные электроды имеют одинаковые значения тангенса угла наклона электродных функций; к ионам Pb (II) и Sr (II) электродная функция уменьшается в ряду Мо>W.
3.3 Поведение молибденового и вольфрамового электродов
в растворах анионов
Для изучения электродных функций Мо и W электродов в растворах анионов были выбраны галогениды калия: фторид-, хлорид-, бромид- и иодид-, а также дихромат и гидрофосфат калия и тетраборат натрия.
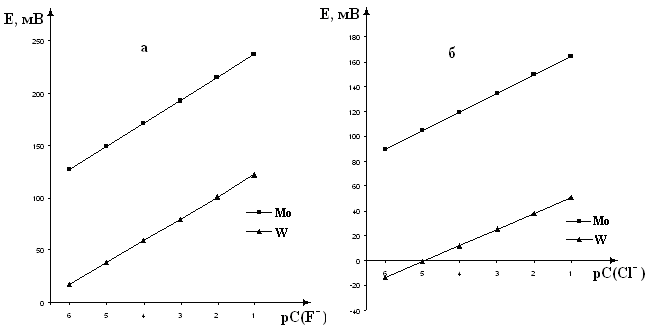
Рисунок 2 – Электродные функции молибденового и вольфрамового
электродов в растворах F- (а) и Сl- (б)
Для молибденового и вольфрамового электродов зависимость потенциала от концентрации F- и Cl- носит линейный характер (рисунок 2). Угловые коэффициенты электродных функций на F- обоих электродов (рисунок 2а) имеют схожие числовые значения: 21±2 мВ (Мо) и 22±2 мВ (W). В случае хлорид-ионов (рисунок 2б) эти значения составляют 13±2 мВ (Мо) и 15±2 мВ (W).
По уменьшению чувствительности к ионам галогенов для исследуемых металлических электродов можно составить следующие ряды:
Мо-электрод: F- > I- > Cl- > Br- W-электрод: F- > I- > Cl- > Br-
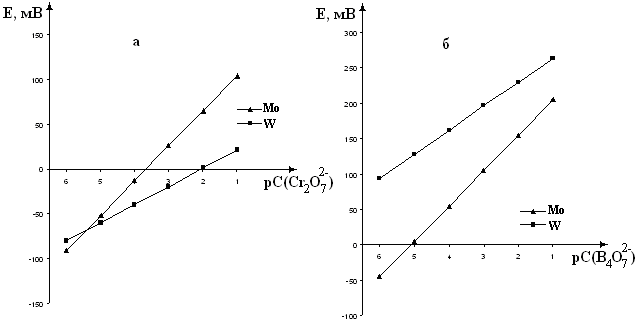
Рисунок 3 – Электродные функции молибденового и вольфрамового
электродов в растворах Сr2O72- (а) и B4O72- (б)
Зависимости Е=f(pC) в растворах Сr2O72- и B4O72- имеют линейный характер для обоих изучаемых электродов (рисунок 3). Наибольшее значение углового коэффициента к обоим ионам имеет электродная функция молибденового электрода (39±2 мВ (Сr2O72-) и 50±2 мВ (B4O72-). Вольфрамовый электрод показывает меньшее значение E/pC (21±2 мВ (Сr2O72-) и 34±2 мВ (B4O72-).
Металлические молибденовый и вольфрамовый электроды показывают наибольшие значения E/pC в растворах кислородсодержащих анионов B4O72-, Cr2O72- и НРО42-.
Мо-электрод: B4O72->Cr2O72->НРО42->F->I->Cl->Br-
W-электрод: B4O72->Cr2O72->F->НРО42->I->Cl->Br-
Высокое значение E/pC молибденовый и вольфрамовый электроды показывают также и в растворах F- и I-. Это, вероятно, связано с тем, что перечисленные потенциалопределяющие ионы обладают наибольшей способностью к специфической адсорбции на границе раздела фаз молибденовый, вольфрамовый электрод-раствор аниона.
4 Термодинамические характеристики электрохимических реакций потенциалопределяющих ионов на молибденовом и вольфрамовом электродах
В данном разделе изучены ЭДС исследуемых электродов при различной температуре (298-328 К) в интервале концентраций ионов 1,0.10-6 – 1,0.10-1 моль/л, что позволило рассчитать термодинамические характеристики электродных реакций катионов (Сu2+, Cr3+, Cd2+, Zn2+, Pb2+) и анионов (Cr2O72-, НРО42-, Cl-) на границе раздела фаз электрод – водный раствор.
4.1 Термодинамические характеристики поведения молибденового и вольфрамового электродов в растворах ионов металлов
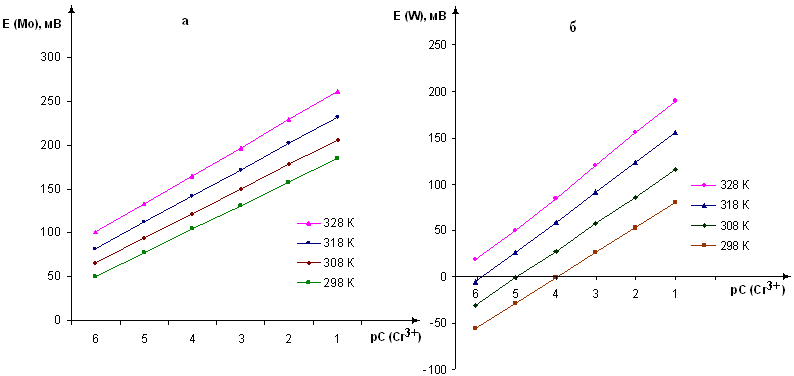
Рисунок 4 – Зависимости ЭДС молибденового (а) и вольфрамового (б) электродов от концентрации Cr3+ при различной температуре
Электродные функции обоих электродов носят прямолинейный характер (рисунок 4) во всем изученном интервале температур (298-328 К) и концентраций (1,0.10-6-1,0.10-1 моль/л). ЭДС электродных процессов возрастают с ростом температуры. Значения температурного коэффициента электродной реакции на обоих электродах имеют положительный знак и возрастают с ростом концентрации потенциалопределяющего иона.
Рассчитаны термодинамические параметры электродной реакции (таблицы 1, 2).
Таблица 1 – Термодинамические функции электродных процессов на Мо электроде в растворах Cr3+ при различной температуре
| рС [Cr3+] Т, К | 1 | 2 | 3 | 4 | 5 | 6 |
| G#, кДж/моль | ||||||
| 298 | -53,6 | -45,1 | -37,9 | -30,1 | -22,3 | -14,5 |
| 328 | -75,6 | -66,3 | -57,0 | -47,8 | -38,5 | -29,3 |
| S#, Дж/моль.К | ||||||
| 298 | 732,3 | 686,1 | 636,8 | 587,6 | 541,3 | 492,1 |
| 328 | 732,3 | 686,4 | 636,8 | 587,6 | 541,3 | 492,1 |
| Н#, кДж/моль | ||||||
| 298 | 164,7 | 158,7 | 151,9 | 144,9 | 139,1 | 132,2 |
| 328 | 164,7 | 158,7 | 151,9 | 144,9 | 139,4 | 132,2 |
Таблица 2 – Термодинамические функции электродных процессов на W электроде в растворах Cr3+ при различной температуре
| рС [Cr3+] Т, К | 1 | 2 | 3 | 4 | 5 | 6 |
| G#, кДж/моль | ||||||
| 298 | -23,2 | -15,3 | -7,5 | 0,3 | 8,1 | 15,9 |
| 328 | -54,9 | -44,9 | -34,7 | -24,6 | -14,7 | -5,2 |
| S#, Дж/моль.К | ||||||
| 298 | 1062,3 | 984,1 | 906,0 | 830,7 | 761,3 | 703,4 |
| 328 | 1062,3 | 984,2 | 905,9 | 830,7 | 761,3 | 703,3 |
| Н#, кДж/моль | ||||||
| 298 | 293,4 | 277,9 | 262,5 | 247,9 | 234,9 | 225,5 |
| 328 | 293,5 | 277,9 | 262,5 | 247,9 | 234,9 | 225,5 |
Анализ данных таблиц 1 и 2 показывает, что положительные значения имеет энтропия (S#) и отрицательные значения имеет энергия Гиббса (G#). Энтропия процесса практически не меняется в изученном интервале температур, но увеличивается с увеличением концентрации потенциалопределяющего иона. Энергия Гиббса уменьшается с ростом температуры и с увеличением концентрации потенциалопределяющего иона. Тепловой эффект электродной реакции (Н#) положителен для процессов как на молибденовом, так и на вольфрамовом электродах, что характерно для эндотермических процессов.
Рассмотрение процессов обратимого разряда ионов кадмия (II), цинка (II) и меди (II) показывает, что энергии Гиббса (G#, кДж) этих процессов изменяется следующим образом (при СМеn+ = const):
Mo > W
Cd (II) -9,8 -25,3
Zn (II) -12,5 -32,4
Cu (II) -28,9 -34,2
Как видно из приведенных данных, наиболее энергетически выгоден процесс разрядки ионов меди (II) на изученных электродах. Сравнение полученных данных со значениями энергий гидратации этих ионов (Gih, кДж/моль): Cd (II) -1778,2 > Zn (II) -2004,1 > Cu (II) -2054,3, показывает, что энергии Гиббса разряда данных катионов находятся в соответствии с их энергиями гидратации. Схожие закономерности наблюдаются и для значений тангенса угла наклона электродных функций (E/рС):
Сравнение данных по энергиям Гиббса и тангенсов угла наклона показывает, что ионы меди (II), имеющие более высокое значение E/рС, обладают меньшей энергией Гиббса разряда на межфазной границе.
Для ионов Сr (III) и Pb (II) наблюдаются следующие закономерности в изменении энергии Гиббса (G#, кДж) процессов, протекающих на изученных электродах:
W > Mo W > Mo
Cr (III) -23,2 -53,6 Pb (II) -9,3 -31,8
Как показывает анализ данных, наиболее энергетически выгодны реакции ионов Cu (II) и Cr (III) на межфазной границе, что согласуется с данными по определению тангенса угла наклона зависимостей Е=f(pC).
Значения термодинамических функций электродных процессов различны на молибденовом и вольфрамовом электродах, что позволяют предполагать, что электродные процессы на различных электродах имеют свои особенности, связанные как с природой аниона, так и с природой электрода.
4.2 Термодинамические характеристики поведения молибденового и вольфрамового электродов в растворах анионов
Рассмотрение электродных реакций анионов Cr2O72-, HPO42- и Сl- показывает, что энергии Гиббса (G#, кДж) этих процессов изменяются следующим образом (при Сиона = сonst):
W > Mo Mo > W
Cr2O72- -19,3 -27,9 Сl- -9,3 -17,6
HPO42- -16,0 -27,9
Сравнение данных по энергиям Гиббса и тангенсов угла наклона показывает, что ионы Cr2O72-, имеющие более высокое значение E/рС, обладают меньшей энергией Гиббса реакции на межфазной границе. Экспериментальные и расчетные данные показывают, что наиболее энергетически выгодны электродные реакции кислородсодержащих анионов на молибденовом и вольфрамовом электродах.
4.3 Обсуждение результатов
В данном пункте проведен анализ полученных экспериментальных данных. Показано, что значения термодинамических функций электродных процессов дополняют экспериментальные данные по изучению электродных функций металлических электродов в растворах катионов и анионов и дают более полную картину процессов, происходящих на границе раздела фаз.
5 Потенциометрическое титрование с молибденовым
и вольфрамовым электродами
В данном разделе приведены результаты по использованию исследуемых металлических электродов в потенциометрическом титровании модельных растворов хрома (III, VI), меди (II), кадмия (II), цинка (II), свинца (II), а также пробы технической воды, содержащей ионы хрома (III, VI).
5.1 Потенциометрическое титрование солей металлов с молибденовым
и вольфрамовым электродами
В качестве титрантов были использованы растворы известных комплексообразующих реагентов. Показано, что исследуемые металлические электроды могут быть использованы для комплексиметрического титрования ионов хрома (ІІІ) и (VI), а также ионов меди (II) и свинца (II). Величина скачков титрования, их четкость, воспроизводимость и малый расход титранта свидетельствуют о принципиальной возможности применения исследуемых электродов в потенциометрических методиках определения этих ионов.
5.2 Потенциометрическое титрование ионов хрома (VI) с молибденовым и вольфрамовым электродами
Определение ионов хрома зачастую связано с чередой трудоемких процессов с использованием большого числа реагентов. Потенциометрия с применением индикаторных электродов позволяет cделать процесс более простым и экспрессным.
Известно, что дифенилкарбазид (ДФК) является наиболее часто применяемым индикатором для определения Cr (VI). ДФК окисляется бихроматом с образованием устойчивого фиолетового катиона.

Учитывая высокую избирательность взаимодействия ДФК с Cr (VI), проводили потенциометрическое титрование модельных растворов Cr (VI) растворами ДФК в кислой среде с применением исследуемых электродов.
Перед титрованием модельных растворов Cr (VI) растворами ДФК электроды отполировывались, выдерживались в 0,1 M растворе дихромата калия в течение 5 минут. Аликвотная порция составляла 10 мл. Результаты титрования проверялись методом введено-найдено (таблица 3).
Представленные на рисунке 5 (а) кривые титрования характеризуются значительными скачками потенциала, лежащими в области (-120) – (-58) мВ для молибденового и (-115) – (-38) мВ для вольфрамового электродов, величина которых зависит от концентрации титранта и реагента, достаточно хорошо воспроизводятся (таблица 3).
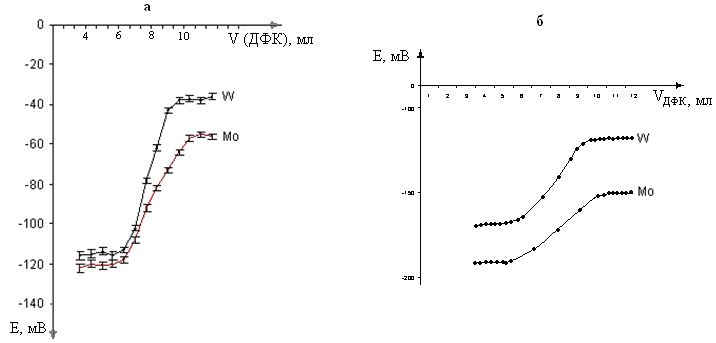
Рисунок 5 – Кривые титрования 10-3 М раствора Cr2O72- (а) и пробы технической воды (б) 10-3 М раствором ДФК
Таблица 3 – Результаты потенциометрического титрования дихромат-ионов металлическими электродами (n=4, P=0,95)
| Электрод | Введено, мг | Найдено, | D,% |
| Mo | 29,42 | 29,19±0.40 | 0,8 |
| W | 29,42 | 29,29±0.34 | 0,4 |
Исходя из положительных результатов потенциометрического титрования, нами была проанализирована проба технической воды с Карачаганакского перерабатывающего комплекса (рисунок 5 б).
Пробу воды пятикратно концентрировали, подкисляли 0,1 мл раствора серной кислоты (1:1), чтобы перевести все ионы хрома (III) в шестивалентное состояние и титровали раствором ДФК концентрации 1,0.10-3 моль/л.
Наилучшие результаты были получены для вольфрамового электрода (рисунок 5 б). Скачок титрования на W-электроде составил в среднем Е=51±2 мВ. Скачок титрования на Mo электроде составил в среднем Е=25±2 мВ.
Расчет по кривым титрования на вольфрамовом электроде дает обнаруженное количество хрома равное в среднем C(Cr)=0,12 мг/л. Результат определения для молибденового электрода составляет в среднем C(Cr)=0,10 мг/л. Анализ этой же пробы на содержание общего хрома фотоэлектроколориметрическим методом дает содержание хрома равное 0,15 мг/л (таблица 4).
Таблица 4 – Результаты потенциометрического титрования пробы технической воды металлическими электродами (n=4, P=0,95)
| Определяемый ион | Титрант | Электрод | Разработанная методика | Известная методика | ||
| Найдено, | Sr | Найдено, | Sr | |||
| Cr (VI) | ДФК | W | 0,12±0,04 | 0,02 | 0,15±0.02 | 0,01 |
| Mo | 0,10±0,04 | 0,02 | ||||
Таким образом, показана возможность применения вольфрамового и молибденового электродов для определения ионов шестивалентного хрома методом комплексиметрического потенциометрического титрования.
Наряду с этим была показана принципиальная возможность использования металлических электродов в потенциометрическом титровании таких ионов металлов как Cu2+, Cr3+, Pb2+ и аниона Cr(VI) с использованием известных комплексообразующих реагентов.
ЗАКЛЮЧЕНИЕ
В результате проведенных исследований:
- созданы электроды из особо чистых металлических молибдена и вольфрама, используемые в качестве индикаторных электродов в вариантах потенциометрии, определены и обоснованы рабочие условия исследуемых электродов: выбор фонового электролита 1,0 М KNO3, рН раствора, ионной силы раствора, температуры;
- определены основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах солей металлов: меди (II), хрома (III), цинка (II), кадмия (II), никеля (II), кобальта (II), свинца (II), стронция (II);
- показано, что по величине тангенсов угла наклона электродных функций молибденового и вольфрамового электродов исследованные ионы d-элементов можно расположить в следующие ряды:
Мо: Cu2+>Cr3+>Cd2+=Zn2+>Co2+>Ni2+ и W: Cu2+>Cr3+>Cd2+=Zn2+>Co2+>Ni2+;
- определены основные электродные характеристики (электродная функция, интервал концентраций потенциалопределяющих ионов, время установления стабильного потенциала, воспроизводимость) в растворах кислородсодержащих (B4O72-, Cr2O72-, H2PO4-) и бескислородных (F-, Сl-, Br-, I-) анионов;
- показано, что по величине тангенсов угла наклона электродных функций молибденового и вольфрамового электродов исследованные анионы можно расположить в следующие ряды:
Мо: B4O72->Cr2O72->НРО42->F->I->Cl->Br- и
W: B4O72->Cr2O72->F->НРО42->I->Cl->Br-;
- оценены термодинамические параметры электрохимических реакций катионов (Cd2+, Zn2+, Сu2+, Cr3+, Pb2+) и анионов (Cr2O72-, HPO42-, Сl- ) на границе раздела молибденовый, вольфрамовый электроды - растворы потенциалопределяющих ионов;
- из расчета термодинамических функций показано, что на межфазной границе Мо(W)-ионы металла наиболее энергетически выгодны реакции ионов Cu (II) и Cr (III); а на межфазной границе Мо(W)-раствор аниона энергетически выгодны электродные реакции кислородсодержащих анионов;
- установлена возможность использования молибденового и вольфрамового электродов в качестве индикаторных в комплексиметрическом потенциометрическом титровании ионов меди (II), хрома (III), свинца (II), хрома (VI) и предложена методика определения ионов шестивалентного хрома в технической воде методом комплексиметрического потенциометрического титрования.
Оценка полноты решений поставленных задач. Задачи, поставленные в диссертационной работе, решены полностью. В результате проведенных исследований изучены электрохимические процессы на границе раздела молибденовый, вольфрамовый электроды - потенциалопределяющие ионы; рассчитаны физико-химические характеристики электрохимических реакций катионов и анионов на границе электрод-раствор; теоретически обоснована и практически установлена возможность использования созданных автором металлических индикаторных молибденового и вольфрамового электродов для определения ЭДС на границе раздела электрод-потенциалопределяющий ион методами потенциометрии.
Рекомендации по конкретному использованию результатов исследования. Предложены электроды из элементов VI В группы молибдена и вольфрама, проявляющие электродную функцию к ряду потенциалопределяющих ионов в широком диапазоне концентраций. Экспериментально обоснована возможность применения металлических молибденового и вольфрамового электродов для потенциометрического титрования ионов хрома (VI) в технических водах. Полученные данные имеют и теоретическую значимость, так как вносят вклад в понимание электрохимических процессов, протекающих на границе металлический индикаторный электрод – водный раствор.
Технико-экономическая эффективность и научный уровень в сравнении с лучшими достижениями в данной области. О научном уровне результатов проведенных исследований свидетельствуют публикации в специализированных журналах, включенных в список изданий, рекомендованных Комитетом по контролю в сфере образования и науки МОН РК, а также обсуждение их в ряде международных конференций.
В целом, научно-методический уровень представленной диссертационной работы отражает комплексность данных исследований.
Список опубликованных работ по теме диссертации.
- Нуртаева Ж.Т., Кунашева З.Х., Мендалиева Д.К. Отклик электродов из молибдена и вольфрама на ионы хрома (III) и (VI) // Научный журнал МОН РК «Поиск». – 2007. – №3. – С. 18-21.
- Нуртаева Ж.Т. Применение молибденового электрода в потенциометрическом титровании // Материалы Х Международной конференции «Наука и образование – ведущий факт стратегии «Казахстан – 2030». – Караганда, 2007. – С. 389-391.
- Нуртаева Ж.Т. Поведение молибденового электрода в растворах солей металлов // Материалы II Международной научной конференции молодых ученых «Наука и образование-2007». – Астана, 2007. – С.133-136.
- Нуртаева Ж.Т., Кунашева З.Х., Мендалиева Д.К. Использование металлического молибдена в качестве электродноактивного вещества в потенциометрии // Вестник КазНУ. Серия химическая (Материалы международной конференции «Экоаналитика Центральной Азии». – 2007. – Т.49, №5. – С. 251-256.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Поведение молибденового и вольфрамового электродов в растворах солей металлов // Вестник КарГУ. Серия химическая. – 2007 – Т. 48, №4. – С. 62-65.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Электроды из вольфрама, молибдена и их сплава для потенциометрического определения галогенидов // Вестник КазНУ. Серия химическая. – 2007 – Т. 48, №4. – С. 202-207.
- Nurtayeva Zh.Т. Кunasheva Z.Kh., Меndaliyeva D.К. Elektrooxidation of molybdenum in hydrophosphate electrolyte in the presence of
superficially-active substances // 18th International Congress of Chemical and Process Engineering. – Prague, 2008. – Р. 227. - Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Применение электродов на основе молибдена, вольфрама и их сплава в потенциометрическом определении ионов хрома (ІІІ) и (VІ) // Рефераты докладов 2-ого международного форума «Аналитика и аналитики». – Воронеж, 2008. – Т.1.-С.184.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Использование металлических молибдена и вольфрама в качестве электродов для комплексометрического титрования ионов хрома (ІІІ) // Материалы VІІІ конференции «Аналитика Сибири и Дальнего Востока- 2008». – Томск, 2008. – С. 187.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Металлические электроды в потенциометрическом титровании // Материалы международной научно-практической конференции «Экономическое, социальное и культурное развитие Западного Казахстана: история и современность» посвященной 180-летию Оружейной Палаты Бокеевского ханства. – Уральск, 2008. – С. 17-20.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Металлические электроды для потенциометрического анализа объектов окружающей среды // Материалы VII Всероссийской конф. По анализу объектов окружающей среды «Экоаналитика-2009». – Йошкар-Ола, 2009. – С. 115.
- Nurtayeva Zh.Т. Кunasheva Z.Kh., Меndaliyeva D.К. Аpplication of molybdenum and tungsten electrodes in the potentiometric titration of the ions of chromium (III) and (VI) // 238th American Chem. Soc. Nation. Meeting & Exposition. – Washington, 2009. – Р.199.
- Кунашева З.Х., Нуртаева Ж.Т., Мендалиева Д.К. Потенциометрическое титрование с применением молибденового электрода // Материалы IV международной конференции «Фундаментальные и прикладные проблемы получения новых материалов: исследования, инновации и технологии». – Астрахань, 2010. – С.240-242.
- Нуртаева Ж.Т. Кунашева З.Х., Мендалиева Д.К. Термодинамические характеристики поведения ионов свинца (II) на вольфрамовом электроде // Известия НАН РК. Серия Химическая. – 2010 – №4. – С. 5-9.
Нртаева Жанна Тлегенызы
Молибден жне вольфрам электродтары - ерітінді бліну шекарасындаы электрохимиялы реакцияларыны физика-химиялы сипаттамалары
Тйін
Жмысты жалпы сипаттамасы. Диссертациялы жмыс молибден жне вольфрам электродтары - потенциаланытаушы иондарыны сулы ерітінділері блу шекарасындаы электрохимиялы реакцияларыны физика-химиялы сипаттамаларын зерттеуге арналан.
Жмысты зектілігі. Физикалы химияны блігі - электрохимияны баыттарыны бірі сезімталдылыы мен коррозияа тратылыы жоары жне таы баса электродты сипаттамалары бар жаа металды электродтарды іздестіру болып табылады. Металды кміс, мыс, кадмий, никель, алайы жне т.б. металдара негізделген атты электродтар тек ана аттас иондарды емес, сонымен атар баса да потенциаланытаушы иондарды анытау шін олданылатыны белгілі. Кп компонентті жйелердегі электрод - ерітінді блу шекарасындаы р-трлі факторлара байланысты тетін процестерді негізгі задылытарын зерттеу, металды молибден жне вольфрамды потенциометрияда индикаторлы электродтар ретінде олдануы туралы болжау жасауа ммкіндік береді. Соы уаытта дебиетте металды электродтарды индикаторлы ретінде олдануы туралы мліметтер те сирек кездеседі. Металды молибден жне вольфрам агрессивті орталарда траты, салыстырмалы арзандылыымен жне олжетерлігімен, сіресе азастан аймаында, сипатталады. Осыан байланысты, металды молибден жне вольфрам негіздерінде индикаторлы электродтарды жасау жне оларды электролиттерді сулы ерітінділеріндегі электрохимиялы жне термодинамикалы сипаттамаларын анытау зекті мселе болып табылады.
Жмысты масаты молибден жне вольфрам электродтары - потенциаланытаушы иондарыны сулы ерітінділері бліну шекарасындаы электрохимиялы реакцияларыны задылытарын жне зерттелген электродтарды потенциометрия варианттарында олдану ммкіндіктерін анытау.
Ж
мысты ылыми жаашылдыы:- жаадан аса таза металды молибден жне вольфрам негізінде электродтар жасалынып, оларды жмысты жадайлары: ерітіндіні рН мні, ерітіндіні ионды кші, температура аныталды;
- мыс (II), хром (III), мырыш (II), кадмий (II), никель (II), кобальт (II), орасын (II), стронций (II) металдарыны тздарында зерттелген электродтарды негізгі электродты сипаттамалары (электродты функция, потенциаланытаушы иондарыны концентрация интервалы, траты потенциал орналасу уаыты, айталаныштыы) аныталды;
- оттекті (B4O72-, Cr2O72-, H2PO4-) жне оттексіз (F-, Сl-, Br-, I-) аниондар ерітінділерінде зерттелген электродтарды негізгі электродты сипаттамалары (электродты функция, потенциаланытаушы иондарды концентрация интервалы, траты потенциал орналасу уаыты, айталанышты) аныталды;
- молибден жне вольфрам электродтары - потенциаланытаушы иондарыны ерітінділері бліну шекарасындаы электрохимиялы реакцияларыны термодинамикалы параметрлері (G#, H#, S#) аныталды; Мо(W)-металл иондары бліну шекарасында Cu (II) и Cr (III) иондары атысында жретін процестер энергетикалы жаынан тиімді екені, ал Мо(W)-аниондар ерітінділері бліну шекарасында оттекті иондарыны реакциялары энергетикалы жаынан тиімді екені крсетілді;
- молибден жне вольфрам электродтарын мыс (II), хром (III), орасын (II), хром (VI) иондарын титрлеуде индикаторлы электродтар ретінде олдану ммкіндігі крсетілді.
Жмысты практикалы ндылыы. Біратар потенциаланытаушы иондара концентрацияларыны ке диапазонында электродты функциялар крсететін VI В тобы элементтері молибден жне вольфрамнан жасалан электродтар сынылды. Молибден жне вольфрам электродтарын техникалы су лгілерінде хром (VI) иондарын потенциометрлік титрлеу шін олдану ммкіндігі тжірибе трінде длелденді.
Жмыс нтижелері Жгір хан атындаы Батыс азастан аграрлы-техникалы университетінде «Органикалы заттарды химиялы технологиясы» жне «Бейорганикалы заттарды химиялы технологиясы» мамандытары шін оылатын «Физика-химиялы талдау дістері» пніні дріс жне практикалы сабатарында олданылады.
Nurtayeva Zhanna Tulegenovna
Physical-chemical characteristics of electrochemical reactions
on the borders molybdenum and tungsten electrodes – solution
Abstract
The general characteristic of the work. The dissertational work has dedicated to the research of the physical-chemical characteristics of electrochemical reactions on the separation border of molybdenum and tungsten electrodes – water solutions of potential-determining ions.
The urgency of the theme. One of the directions of the electrochemistry, the division of the physical chemistry, is the search for the new metal electrodes, which possess high sensitivity, corrosion resistance and other electrode characteristics; and also the improvement of the known indicator electrodes, which are characterized by accessibility, cheapness and prolonged period of a service. The enumeration of the materials, which are used for studying the electrochemical processes on the solid electrodes, is enlarged. It is well known that solid electrodes from silver, copper, cadmium, nickel, tin and others can be used for determining not only same ions, but also other potential-determining ions. However, in the literature sources it is increasingly more rarely mentioned about the use of metal electrodes. The metal molybdenum and tungsten electrodes present undoubted interest among such electrodes. Electrodes made of molybdenum and tungsten are simple in the production, they are convenient in the rotation, they are steady in the aggressive media, and also they differ from some other electrode materials in terms of the duration of the period of operation, in terms of relative cheapness and accessibility, especially on the territory of republic of Kazakhstan. In this connection the study of the problems, which take place on the border of the division of phases in different electrochemical systems made of molybdenum and tungsten is about theoretical and practical interest, since makes it possible to establish the basic regularities, proceeding on the border electrode - solution in the multicomponent systems depending on different factors. The measurement of the electromotive force and the establishment of the electrode function of metal molybdenum and tungsten electrodes to metal ions makes it possible to make a conclusion about the possibility of their application as the indicator electrodes in potentiometry. The method of potentiometry makes it possible to solve both analytical (quantitative determination of ions in the solution) and physical chemistry (determination of the solubility product, stability constant) problems and ensures the determination of the thermodynamic functions of electrode reactions, which makes it possible more deeply understand nature of the appearance of electrode function to the potential-determining ions. In connection with this the establishment of the electrochemical and thermodynamic characteristics of metal electrodes made of molybdenum and tungsten in the solutions of electrolytes is urgent.
The purpose of the research. The establishment of laws governing the electrochemical reactions, which take place on the border of the division of phases the molybdenum, tungsten electrode - solutions of the potential-determining ions and possibility of their use in the versions of potentiometry.
The scientific novelty of the results obtained in the thesis consists in the fact that:
- for the first time created electrodes from the metal molybdenum and tungsten, utilized as the indicator electrodes in the versions potentiometry;
- determined the conditions of the functioning the electrodes being investigated: the optimum value of pH, the influence of the ionic force of solution, the time of the establishment of stable potential, optimum temperature;
- determined fundamental electrode characteristics (electrode function, the interval of the concentrations of the potential-determining ions, the time of the establishment of stable potential) in the solutions of salts of metals and anions (oxygenconteining and without oxygen);
- evaluated the thermodynamic parameters of the electrochemical reaction on the border of division molybdenum, tungsten electrodes - solutions of the potential-determining ions;
- established the possibility of using the molybdenum and tungsten electrodes as the indicator in the potentiometric titration.
Theoretical and practical importance of the work. The indicator electrodes from the elements of VI B group molybdenum and tungsten, which manifest electrode function to a number of the potential-determining ions over a wide range of concentrations were proposed. The possibility of applying the metal molybdenum and tungsten electrodes for the potentiometric titration of the ions of chromium (VI) in the technical water samples was experimentally substantiated.
The results of work are used in the lecture and practical courses “physical- chemical methods of analysis” read at the West Kazakhstan agrarian- technical university after Al-Farabi for the specialties “chemical technology of organic substances” and “the chemical technology of inorganic substances”.

