Количественная спектроскопия ямр поли компонентных систем из приро д ного органического сырья
На правах рукописи
Рохин Александр Валерьевич
количественная Спектроскопия ЯМР
поликомпонентных систем из
природного органического сырья
02.00.03. органическая химия
А в т о р е ф е р а т
диссертации на соискание ученой степени
доктора химических наук
И р к у т с к 2 0 0 7
Работа выполнена в государственном образовательном учреждении высшего профессионального образования «Иркутский государственный университет»
| Научный консультант | доктор химических наук, профессор Кушнарёв Д. Ф. |
| Официальные оппоненты: | доктор химических наук, профессор Гюльмалиев А. М. |
| доктор химических наук, профессор Кривдин Л.Б. | |
| доктор химических наук, профессор Евстафьев С. Н. | |
| Ведущая организация: | Российский университет дружбы народов, г. Москва |
Защита состоится «24» октября 2007 г. в 1000 час. на заседании диссертационного совета Д 212.074.06 при Иркутском государственном университете по адресу: 664033, г. Иркутск, ул. Лермонтова, 126, ауд. 430.
С диссертацией можно ознакомиться в научной библиотеке Иркутского государственного университета и на сайте ВАК РФ.
Отзывы на автореферат высылать по адресу: 664003, г. Иркутск,
ул. К. Маркса, 1, Иркутский государственный университет, химический факультет, Эдельштейн О.А.
Автореферат разослан “02” сентября 2007 г.
Ученый секретарь
диссертационного совета,
кандидат химических наук О. А. Эдельштейн
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Ресурсосбережение включает переработку всех видов природного органического сырья, удовлетворяющую комплексу жёстких и часто противоречащих друг другу требований: экологическая безопасность и высокая эффективность по выходу целевых продуктов, низкая энергоемкость и безотходность. Сдерживающим фактором успешного решения таких задач выступает дефицит знаний о составе, строении и структуре объекта, подвергаемого переработке. Преодоление этого невозможно без расширения арсенала методов количественного анализа, адекватно описывающих состав, молекулярное строение и надмолекулярную структуру природного органического материала, его компонентов и целевых продуктов. Структурно-химические взаимосвязи определяются природой объектов, и как доминанты, положены в основу стратегии поиска методов идентификации и аутентификации целевых продуктов переработки природного органического сырья, оптимизации технологии химических и биохимических процессов.
Разработка методологии исследования состава и строения многокомпонентных систем природного происхождения учитывает их принципиальные особенности такие как высокая молекулярная масса, полидисперсность, фазовая неоднородность, стохастический состав. Эти обстоятельства ограничивают применимость большинства классических химических и физико-химических методов анализа, эффективных для индивидуальных соединений и их компаундов, тогда как для метода спектроскопии ЯМР эти особенности не накладывают никаких ограничений и количественный вариант спектроскопии ЯМР вносит весомый вклад в исследования органических веществ биогенного происхождения. Однако возможности метода для решения теоретических и практических задач химии и переработки природного органического сырья далеко не исчерпаны.
Работа выполнена в рамках государственной научно-технической программы по приоритетному направлению развития науки и техники на 1990-1994гг. 10. «Новые материалы и вещества – основа создания нового поколения техники, технологии и решения специальных задач» по теме 10.1.4.3. «Исследование электрохимических, биохимических и электробиохимических реакций макрокомпонентов древесины» (государственный регистрационный
№ 01860109695) и программы Министерства науки и технической политики РФ «Комплексное использование и воспроизводство древесного сырья». Поддержана грантами РФФИ № 96-03-34297а (1996-1998 гг.) «Разработка комплексной методики анализа структурных групп лигнинов», № 97-04-96151 (1997-1999гг.). «Исследование биокаталитических реакций окисления лигнинов и ароматических соединений – компонентов донных отложений» и «Количественная спектроскопия ядерного магнитного резонанса (ЯМР) гуминовых веществ: методология и методики исследования состава и строения», № 00-03-32965a (2000-2001г.), при поддержке НТП Министерства образования РФ «Научные исследования высшей школы по приоритетным направлениям науки и техники» на 2003-2004 г.г. (гранты № 203.05.07.040 и 204.01.02.014).
Цель работы
Разработка способов оценки влияния различных факторов и их комбинаций на химические, биохимические и технологические процессы переработки многокомпонентных систем природного происхождения, идентификации и аутентификации целевых продуктов на основе информации, полученной методом количественной спектроскопии ЯМР. Формирование концептуальных направлений её использования при решении теоретических и практических задач химии лигнина, угля, гуминовых веществ, многокомпонентных изотопомерных смесей природного происхождения.
Задачи
1. Разработка методических приемов получения достоверной количественной информации из одно- и двумерных спектров ЯМР 1Н и 13С о фрагментном составе, функциональных группах, структурных звеньях и их взаимосвязей, отдельных компонентах, содержащихся в продуктах переработки природного органического сырья:
- для экспертной оценки методов химического анализа природных полимеров, идентификации и количественной оценки содержания различных классов органических соединений и лигнинов в сложных смесях техногенного происхождения;
- для оптимизации условий технологической переработки природных объектов (углей) с целью получения целевых продуктов с заданным составом и свойствами;
- для установления структурно-спектральных взаимосвязей гуминовых веществ, идентификации их сырьевого происхождения и первичного прогнозирования рост-стимулирующей активности промышленных препаратов без проведения полевых испытаний;
2. Разработка методов идентификации и аутентификации многокомпонентных изотопомерных смесей, этанолсодержащих целевых продуктов различного происхождения методом спектроскопии ЯМР на естественном содержании минорных изотопов.
Научная новизна и практическая значимость работы. Обобщены новые наиболее важные результаты по применению одно- и двумерной количественной спектроскопии ЯМР высокого разрешения в исследовании растворов многокомпонентных систем природного происхождения – лигнина, продуктов переработки угля, гуминовых веществ, многокомпонентных изотопомерных смесей различного происхождения.
Методом количественной спектроскопии ЯМР 1Н и 13С изучен фрагментный состав лигнинов, подвергнутых химической модификации различными реагентами, рассмотрены методические аспекты получения достоверной информации о содержании функциональных групп и связей в макромолекулах лигнинов из одномерных и двумерных спектров ЯМР. Спектроскопия ЯМР предложена в качестве метода аттестации и оценки результатов химических способов анализа функциональных групп лигнина и идентификации лигнинов в смесях органических веществ техногенного происхождения.
На основе закономерностей изменения фрагментного состава из спектров ЯМР 1Н, 13С продуктов гидрогенизации каменного угля проведена оптимизация технологических условий процессов каталитического гидрирования угольных смол с высоким содержанием гетероатомных органических соединений с целью получения продуктов заданного состава и свойствами.
Найдены новые статистически надежные взаимосвязи параметров фрагментного состава из спектров ЯМР 13С с рост-стимулирующей активностью гуминовых кислот. Анализ спектров ЯМР 13С более 40 гуминовых кислот показал, что количественная спектроскопия ЯМР 13С при модификации методик анализа спектров – наиболее корректный метод аутентификации промышленных препаратов гуминовых кислот, идентификации их сырьевого происхождения, первичного прогнозирования физиологической активности.
Разработана и аттестована оригинальная методика количественного определения содержания дейтерия в различных фрагментах молекул органических веществ методом спектроскопии ЯМР 2Н на естественном содержании дейтерия. Её применение продемонстрировано при идентификации этанолов различного генезиса и технологий получения в компаундах широкого диапазона его концентраций. С помощью метода спектроскопии ЯМР найдены качественные и количественные критерии дифференциации пищевых и синтетических этанолов, алгоритм идентификации подлинности и географического происхождения вин с использованием компонентного и изотопного анализов.
Объем и структура работы. Диссертационная работа изложена в 5 главах, на 320 страницах, включая таблицы, рисунки и схемы. Библиография насчитывает 600 наименований. В начале глав приводится краткий обзор литературы по решаемой тематике. На защиту выносятся основные положения методологии и алгоритмов количественного изучения ряда поликомпонентных систем природного происхождения – лигнинов, углей, многокомпонентных изотопомерных смесей, гуминовых веществ. В первой главе представлен алгоритм исследования препаратов лигнина на примере лигнина Бъёркмана, выделенного из древесины ели и его модифицированных препаратов с использованием одно- и двумерных экспериментов ЯМР 1Н и 13С. Во второй и третьей главах обсуждаются результаты применения разработанных подходов и методик для исследования продуктов переработки угля (продукты гидрогенизации угля и гуминовые вещества). В четвёртой главе представлены результаты исследования многокомпонентных изотопомерных смесей природного происхождения методом спектроскопии ЯМР на ядрах минорных изотопов. Глава 5 содержит сведения об объектах исследования, методиках пробоподготовки, использованной аппаратуре, элементный состав, условия выделения лигнинов, жидких продуктов переработки угля, гуминовых веществ, многокомпонентных изотопомерных смесей различного происхождения и технике эксперимента ЯМР.
Публикации и апробация. По теме диссертации опубликовано более 70 работ, из них 30 статей и 43 материала конференций различного уровня. Апробация работы осуществлена при защите кандидатской диссертации по теме исследования и широком обсуждении отдельных вопросов на Международном научном конгрессе "Молодежь и наука – третье тысячелетие", YSTM-96 (Москва, 1996), конференции "Идентификация качества и безопасность алкогольной продукции" (Пущино, Моск. область, 1999), Всероссийской конференции "Химический анализ веществ и материалов" (Москва, 2000), III Всероссийской конференции "Новые достижения ЯМР в структурных исследованиях" (Казань, 2000), of EuroConference "Modern analytical methods for food and beverage authentication. (Lednice 29-31.08.02, Czech republic,2002), 1-научно-практической конференции ГТЛ ГТК РФ "Экспертно-исследовательская деятельность в таможенных целях" (Москва, 2001), II научно-практической Международной конференции "Человек-среда-Вселенная" (Иркутск, 2001), Международной конференции "Технология и экологические аспекты переработки минерального сырья" (Иркутск, 2001), 5 Всероссийской научно-практической конференции (Екатеринбург, 2001), 6 международном семинаре по магнитному резонансу (Ростов-на-Дону, 2001), Поволжской конференции по аналитической химии (Казань, 2001), конференции "Химия и химические продукты" (Москва, 2002), "II Международной конференции по новым технологиям и приложениям современных физико-химических методов (ЯМР, хроматография/ масс-спектрометрия, ИК-фурье спектроскопия и их комбинации)" (Ростов-на-Дону, 2003), XVII Менделеевского съезда (Казань, 2003), Всероссийской конференции "Новые достижения ЯМР в структурных исследованиях" с участием зарубежных учёных (Казань, 2005), международной конференции «PIM-2005» (Румыния, 2005), Международной VIII научно-практической конференциии "Химия XXI век: новые технологии, новые продукты" (Кемерово, 2005), III Всероссийской конференции "Гуминовые вещества в биосфере" (Санкт-Петербург, 2005), международного симпозиума "ЯМР в конденсированных средах" (Санкт-Петербург, 2005), Всероссийской конференции "Экспресс-методы количественного анализа: достоинства и недостатки, область применения" (Москва, 2005), Международной IX научно-практической конференциии "Химия XXI век: новые технологии, новые продукты" (Кемерово, 2006), Международной научно-практической конференции (Иркутск, 2006), IV Всероссийской конференции "Химия и технология растительных веществ", (Сыктывкар, 2006), Международной X научно-практической конференциии "Химия XXI век: новые технологии, новые продукты" (Кемерово, 2007).
основные сокращения
| АК | ароматическое кольцо | |
| ГМФТА-D18 | гексаметилфосфортриамид | |
| ДМСО-D6 | диметилсульфоксид дейтерированный | |
| HSQC | 2D гетероядерная корреляционная спектроскопия | |
| ХС | химический сдвиг | |
| ЛМР | лигнин механического размола ели | |
| ЛМР-М | ЛМР ели, метилированный метанолом | |
| ЛМР-ДМС | ЛМР ели, метилированный диметилсульфатом | |
| ЛМР-ДАМ | ЛМР ели, метилированный диазометаном | |
| ЛМР-ДАМ-М | ЛМР ели, последовательно метилированный диазометаном и метанолом | |
| ЛМР-А | ЛМР ели, ацетилированный | |
| S, S | сирингильные звенья лигнина: | |
| G, G | гваяцильные звенья лигнина: | |
| Н, Н | п-оксифенильные звенья лигнина: | |
| ГК | гуминовая кислота | |
| СЭ | синтетический этанол | |
| ПЭ | пищевой этанол | |
| ТС | тяжёлая смола полукоксования | |
| ОЛМ | обесфеноленное лёгкое масло | |
| КО | кубовый остаток | |
| ВП | вакуумный погон | |
| ЛВ | лигнинное вещество сточных вод БЦБК | |
| смола КАУ | смола термодеструкции угля Канско-Ачинского бассейна | |
| ГВ | гуминовые вещества | |
| РА | рост-стимулирующая активность гуминовых веществ |
С О Д Е Р Ж А Н И Е Р А Б ОТ Ы
Во введении обоснована актуальность научного направления: разработка методологии использования количественной спектроскопии ЯМР на различных ядрах для исследования многокомпонентных систем природного происхождения; фундаментальная научная новизна и практическая значимость работы.
Количественная спектроскопия ЯМР делает возможным не только идентифицировать сигналы отдельных ядер 1Н и 13С в зависимости от их окружения, но и строго оценивать их абсолютное или относительное содержание. Это позволяет с высокой избирательностью выявлять особенности химической структуры, количественно оценивать соотношения фрагментов в многокомпонентных системах природного и синтетического происхождения.
Предмет и объекты исследования методом количественной спектроскопии ЯМР 1Н и 13С представлены на схеме (рис. 1), в диссертационной работе материал рассматривается в той же последовательности.
Глава I. Количественная спектроскопия ЯМР как экспертный метод оценки химических способов анализа лигнинов и способ идентификации природных полимеров в сложных смесях техногенного происхождения
Лигнин полифункциональный, гетероцепной, хаотически построенный природный полимер ароматической природы, не гидролизующийся до мономеров. Нерегулярная структура этого наиболее распространенного в природе полимера, его полифункциональность, многообразие типов связей приводит к снижению избирательности многих аналитических реагентов, успешно используемых для анализа органических соединений и их смесей. Это затрудняет исследование его химического строения большинством химических и физических методов.

Рис. 1. Предмет и объекты исследования методом количественной спектроскопии ЯМР на ядрах 1Н, 2Н, 13С, 17О, 31Р.
При изучении химической структуры лигнина наиболее информативным признан метод спектроскопии ЯМР. В основном, в ЯМР-исследованиях используются химически модифицированные препараты лигнина, вследствие их хорошей растворимости и информативности спектров. Для ацетилированных препаратов оценивают содержание фенольных и спиртовых групп ОН, что является одной из основных задач при исследовании структуры лигнинов. К настоящему времени разработаны и интенсивно используется ~ 30 различных способов оценки функциональных групп, которые основаны на методах модификации препаратов лигнина химическими реагентами (силилирование, фторирование, фосфорилирование и т.д.) с последующей оценкой содержания функциональных групп по спектрам ЯМР 19F, 29Si, 31P, 199Hg. Однако ни в одном из вышеперечисленных методов не установлены степень конверсии различных типов ОН-групп в реакциях, возможная трансформация химического строения макромолекулы лигнина при данных видах химического воздействия. В связи с этим нами предпринята попытка разработки новых приемов в исследовании химической структуры лигнина методом количественной спектроскопии ЯМР в одно- и двумерном представлении.
Основные методические приёмы отработаны при исследовании препаратов лигнина низших растений (папоротник), травянистых (пшеница, хлопчатник) и высших растений (ель, лиственница, береза, осина), выделенных различными способами из древесной матрицы.
Цель данного этапа работы состояла в разработке независимого метода контроля изменения химической структуры макромолекулы лигнина, модифицированного в различных химических процессах. Алгоритм анализа макромолекул лигнинов методом количественной спектроскопии ЯМР представлен на рис. 2:
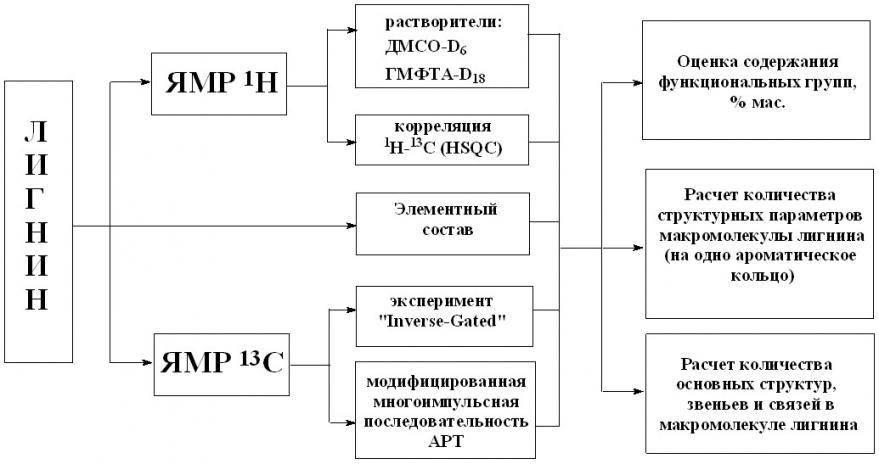
Рис. 2. Алгоритм исследования химической структуры препаратов лигнина методом количественной спектроскопии ЯМР в сочетании с 2D-экспериментами.
Характеристика исходного ЛМР ели. Наиболее сложным в анализе лигнинов является дифференцированное определение содержания функциональных групп (фенольных, карбоксильных и спиртовых групп ОН, альдегидных, кетонных, сложноэфирных), различных типов связей (арил-арильных и арил-алкильных простых эфирных связей, двойных связей) и фрагментов S, G, Н. В работе основное внимание уделено разработке специальных методов и приёмов для решения этой задачи. В табл. 1, 2 приведены результаты анализа химической структуры исходного ЛМР ели.
Спектры ЯМР препаратов лигнина обычно регистрируют в растворе ДМСО-D6, в котором сигналы 1Н ОН-групп фенолов и карбоксильных групп перекрываются с сигналами атомов водорода ароматических колец и двойных связей. В растворителе ГМФТА-D18, более основном, чем ДМСО-D6, сигналы атомов водорода карбоксильных и фенольных групп ОН смещаются в более слабое поле (912 м.д.). Это позволило произвести дифференцированную оценку указанных атомов водорода.
Таблица 1. Количество структурных фрагментов (Nx) в препарате ЛМРЕ, приходящееся на 100 АК
| Фрагменты и основные структурные звенья | Литературные данные | Nx | Погрешность r, % | |
| Спектроскопия ЯМР | Химический анализ | |||
| S | — | 12 | 12 | 8,5 |
| G | 95 | 94 | 9192 | 9,5 |
| H | 2 | 35 | 3 | 6,7 |
| 405/4ОМе | — | — | 5 | 9,5 |
| Cар-О | 208 (+>С=С<) | — | 212 | 6,7 |
| Сар-С | 155 | — | 150 | 6,7 |
| СНар | 250 | — | 238 | 6,7 |
| >С=С< | 12 | — | 13 | 6,7 |
| СНОалк | 212 | — | 214 | 6,7 |
| Сбок. цепей | — | — | 303 | 12,7 |
| Сбок. цепей (без С(О)ОR и Салк) | 279282 | 300 | 288 | 12,7 |
| ОНар+алк | 138 | 131132 | 134 | 7,3 |
| СарОН | 31 | 20 34 | 34 | 7,3 |
| -СалкОН | 68 | 75 78 | 57 | 8,5 |
| -СалкОН | 39 | 25 | 43 | 8,5 |
| ОСН3 | — | — | 10 | 6,7 |
| ОСН3 | 95 | 96 | 4,2 | |
| СО | 21 | 15 46 | 30 | 6,7 |
| СОН | 9 | 3 9 | 8 | 6,7 |
| -СО | 10 | 6 8 | 6 | 10,0 |
| С(О)ОН | — | 5 | 5 | 7,3 |
| С(О)ОR | 5 | 2 23 | 6 | 7,9 |
| Cтепень замещенности АК | 0,5 | 0,4 0,6 | 0,6 | 6,7 |
Расчёт степени ароматичности лигнина (fa) и количества основных структурообразующих элементов его макромолекулы произведён с учётом количества атомов углерода фрагментов >СН=СН< и >СН=СН2. Идентификация и оценка двойных связей представляет собой особенно трудную задачу: их невозможно определить не только химическими, но и физико-химическими методами, в том числе и методом спектроскопии ЯМР, если анализировать спектры 1Н и 13С, зарегистрированные традиционными способами со стандартными растворителями. Для решения этой задачи предложено использовать гетероядерные корреляционные спектры в двумерном представлении (рис. 3 а, б) в растворе ГМФТА-D18 и спектры ЯМР 13С модифицированного варианта многоимпульсной последовательности спинового эха (рис. 4 б, в). Область спектра ЯМР 13С 160102 м.д. включает: сигналы атомов углерода СарО (164140 м.д.), Сатомов двойных связей (161140 м.д.) в структурах типа ArC=CC(O)OH; СарС (140125 м.д.) Сатомов двойных связей (138115 м.д.) и групп СНар (135102 м.д.), т.е. наблюдается существенное перекрывание сигналов, препятствующее их идентификации. По спектру HSQC, зарегистрированному в растворе ГМФТА-D18 (рис. 3б), и подспектрам ЯМР 13С ЛМРЕ, произведено отнесение сигналов С-Н атомов двойных связей и их количественная оценка.
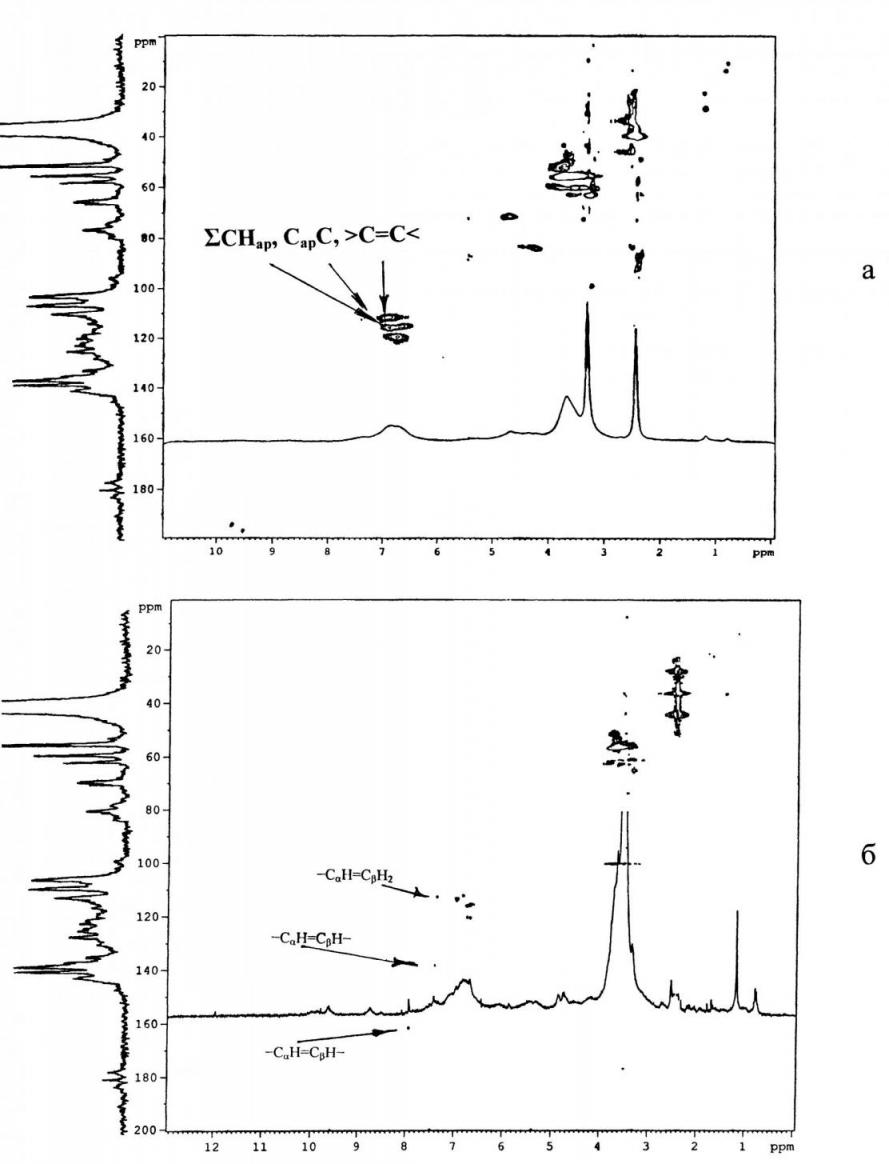
Рис. 3. 2D HSQC-спектры ЛМРЕ в ДМСО-D6 (а) и ГМФТА-D18 (б)
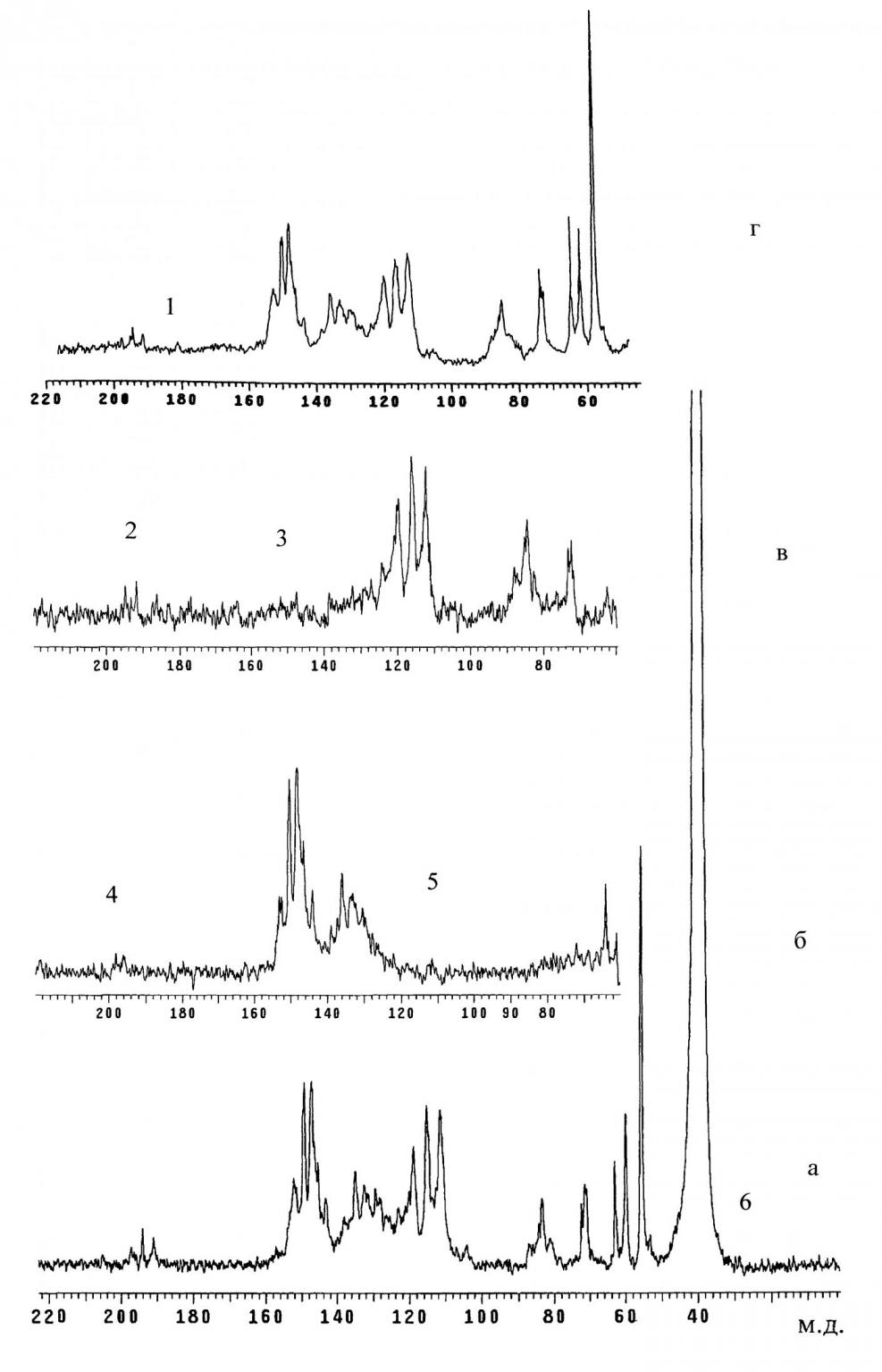
Рис. 4. Спектры (а, г) и подспектры (б, в) ЯМР 13С растворов очищенного (а) и неочищенного (г) ЛМРЕ в растворе ДМСО-D6 c добавкой 0,02М релаксанта Cr(AcAc)3: 1 – атомы углерода >С=О групп спиродиенона; 2 – атомы углерода >С=О групп кетонов; 3 – атомы углерода С-групп связей >С=С<; 4 – атомы углерода >С=О групп альдегидов; 5 – атомы углерода С-групп связей >С=С<; 6 – атомы углерода СН2-групп боковых цепей.
Сравнительный анализ спектров ЯМР 13С препаратов ЛМР ели, полученных по методу Бъёркмана до и после очистки, позволил установить отсутствие в спектре очищенного ЛМРЕ соединений с ХС 181,4 м.д. (рис. 4 г), фрагмента >С=О спиродиенона. Следовательно, структура спиродиенона не связана ковалентными связями с трехмерной полимерной матрицей лигнина, как другие структуры (пинорезинольные, фенилкумарановые и т.д.), поскольку трудно предположить, что метод очистки лигнина от низкомолекулярных примесей может столь избирательно воздействовать на макромолекулу с деструкцией связей макромолекулы лигнина со спиродиеноном.
Таким образом, благодаря модифицированной нами программе спинового эха, спектров ЯМР в двумерном представлении и специфических комплексообразователей возможно прямое определение содержания описанных выше фрагментов, детализирующих структуру макромолекулы лигнина. Разработанный подход позволил определить содержание всех основных структурных фрагментов макромолекулы лигнина, функциональных групп, связей и звеньев в расчете на 100 ароматических колец (табл. 1) и в % мас. (табл. 2).
Таблица 2. Содержание функциональных групп в препарате ЛМР ели, определенное из спектров ЯМР и химическими методами анализа, мас.%.
| Функциональные группы | Содержание функциональных групп, мас.%. | ||
| ЯМР | Химический анализ | Литературные данные | |
| СН3О | 15,8 | 15,86 | 14,39 15,75 |
| ОНфен | 3,0 | 2,72 | 2.51 2,91 |
| ОНалк | 8,0 | 8,82 | 7,60 9,16 |
| -ОНалк | 1,4 | — | — |
| - ОНалк | 5,6 | — | — |
| С=О | 4,3 | — | 2,71 3,60 |
| С=О | 1,6 | — | — |
| С(О)Н | 2,7 | — | — |
| С(О)ОR | 4,4 | — | — |
| С(О)ОН | 1,2 | 1,52 | 1,13 |
Другая отличительная черта предложенного подхода в исследовании химической структуры лигнина – методика определения длины боковых цепей, которая рассчитывается с учётом интегральных дескрипторов фрагментного состава из спектров ЯМР 13С: атомов углерода двойных связей (С=С), карбонильных (С=О), альдегидных (С(О)Н), карбоксильных (С(О)О) групп, окисленных алифатических (СалкО), пинорезинольных, фенилкумарановых (СН), алифатических атомов углерода (Салк):
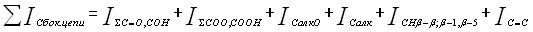 (2).
(2).
Атомы углерода в области 4010 м.д. обычно игнорируют при расчетах Сбоковой цепи, хотя сигналы в диапазоне 3628 м.д. соответствуют СН2-группам структур, типа секойзиларицирезинола, кониферилового спирта, эвгенола; в расчет не принимаются также атомы углерода сложноэфирных групп:
Количественная спектроскопия ЯМР 1Н, 13С как экспертный метод оценки химических способов определения функциональных групп лигнина. Традиционные химические методы определения содержания функциональных групп в препаратах лигнина (метилирование, ацетилирование) используются на протяжении более 100 лет и считаются наиболее точными и надёжными. В табл. 3 приведены результаты исследований структуры лигнинов ели методом количественной спектроскопии ЯМР, подвергнутых химической модификации различными реагентами (метанолом, диметилсульфатом, диазометаном, ангидридом уксусной кислоты) с целью определения содержания гидроксильных групп (фенольных, карбоксильных спиртовых), при этом спектроскопия ЯМР выступает в качестве независимого метода аттестации химических способов анализа (табл. 3, 4).
Таблица 3. Количество структурных фрагментов и связей (Nx) в модифицированных и исходном препаратах ЛМР ели, приходящееся на 100 АК
| Фрагменты и структурные звенья | Лигнины ели | |||||
| ЛМР | ЛМР-М | ЛМР-ДМС | ЛМР-ДАМ | ЛМР-ДАМ-М | ЛМР-А | |
| S | 4 5 | 5 6 | 9 | 40 | 31 | 5 |
| G | 88 | 85 | 54 | 4 5 | 2 3 | 89 |
| G (С-4 ОСН3) | — | — | 25 | 45 | 60 | 6 |
| H | 3 | 3 | 11 | 4 | 1 2 | — |
| Cар-О | 211,8 | 215,3 | 212,5 | 205,6 | 206,5 | 208.0 |
| Сар-С | 118,3 | 108,0 | 136,7 | 130,5 | 120,8 | 134.3 |
| СНар | 270,0 | 276,7 | 250,8 | 263,8 | 270,3 | 257.7 |
| Сбок. цепей | 315,3 | 232,0 | 304,9 | 361,5 | 328,3 | 535.7 |
| Сар-ОН | 35,6 | 46,1 | 9,0 | 24,7 | 2,6 | 2,50 |
| Салк-ОН | 100,0 | 52,2 | 27,8 | 44,6 | 37,4 | 68.0 |
| ОСН3 | 105,4 | 142,6 | 147,2 | 151,8 | 137,9 | 115.7 |
| ОСН3 | — | 37,2 | 41,9 | 46,4 | 32,5 | — |
При химическом анализе концентрацию реагирующих ОН-групп рассчитывают по приросту (в % мас.) содержания метоксильных или ацетильных групп в лигнине после реакции. По разработанной методике содержание ОН-групп оценивается как по приросту метоксильных групп, так и по уменьшению содержания СООН и ОН-групп, установленное из спектров ЯМР 1Н, 13С. Изменения фрагментного состава позволяют установить соотношения основных и побочных реакций, протекающих в условиях метилирования или ацетилирования (табл. 4).
Таблица 4. Содержание функциональных групп в модифицированных и исходных препаратах ЛМР ели, определенное из спектров ЯМР, % мас.
| Элементный состав, функциональные группы | Лигнины ели | |||||
| ЛМР | ЛМР-М | ЛМР-ДМС | ЛМР-ДАМ | ЛМР-ДАМ-М | ЛМР-А | |
| Выход, % | 75,7 | 78,3 | 94,1 | 71,1 | 96,4 | |
| СН3О | 16,0 | 18,8 | 23,3 | 20,2 | 22,0 | 15,1 |
| СН3О | 6,8 | 7,3 | 4,2 | 5,9 | ||
| ОНфен | 3,0 | 4,0 | 0,8 | 1,8 | 0,2 | 0,01 |
| ОНалк | 7,2 | 5,2 | 2,1 | 3,3 | 3,3 | 3,0 |
| -ОНалк | 1,4 | 1,2 | 1,4 | 0,1 | 0,5 | |
| - ОНалк | 5,6 | 4,0 | 1,0 | 3,2 | 2,8 | |
| С=О | 5,1 | 2,2 | 2,2 | 1,6 | 4,6 | 1,6 |
| С(О)Н | 1,2 | 1,6 | 2,8 | 2,2 | 1,8 | 0,8 |
| С(О)ОR | 4,4 | 1,4 | 2,2 | 2,5 | 5,3 | 25,6 |
| С(О)ОН | 1,2 | 1,6 | 0,02 | 0,3 | 0,3 | 0,02 |
Метилирование метанолом (ЛМРМ). Модифицирование ЛМР ели метанолом приводит к метилированию -бензилспиртовых и карбоксильных групп. Метилирование модельных соединений показало, что наряду с основными реакциями одновременно протекает процесс переалкилирования -бензилэфирных групп лигнина с образованием новых фенольных групп ОН:
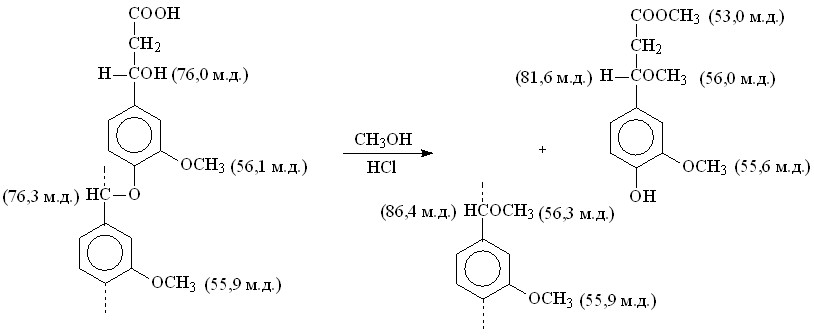
Анализ фрагментного состава из спектров ЯМР 1Н в растворе ГМФТА-D18 обнаружил отсутствие взаимодействия карбоксильных групп с метанолом. Их концентрация в пределах погрешности эксперимента совпадает с содержанием в исходном ЛМРЕ (табл. 4).
По спектрам ЯМР 1Н определено количество (в расчете на 100 АК) образовавшихся в результате реакции переалкилирования -бензилэфирных и фенольных ОН-групп, количество гидролизовавшихся связей -О-4. В модифицированном образце их содержание составило 10,5/100АК, в ЛМР ели – 20/100, что соответствует гидролизу 50% -бензилэфирных связей лигнина. Расчет спектра ЯМР 13С показал уменьшение в 3,2 раза содержания фрагментов
СНОалк, относящихся к атомам С, при связях -О-4 и атомам С-ОН. Это свидетельствует и о процессе гидролиза связей -О-4, что не предполагалось методикой метилирования лигнина метанолом.
В модифицированном лигнине уменьшилось количество алифатических атомов углерода, приходящееся на одно ароматическое кольцо (без учета ОСН3-групп) и соответственно длины боковой цепи (табл. 3). В исходном препарате лигнина содержится 1,4% мас. -ОН и 0,5% мас. ОН-карбоксильных групп. В метилированном препарате прирост ОН-групп составил 3,7% мас., если учесть, что не прореагировали карбоксильные ОН-группы, то – 4,2% мас., что в 2 раза превышает их содержание в исходном ЛМР ели.
Таким образом относительная погрешность определения содержания ОН карбоксильных групп и -ОН спиртовых групп составляет не менее 50%, исключительно за счёт реакции переалкилирования.
В реакции метилирования лигнина метанолом обнаружена интенсивная деструкция макромолекулы лигнина, что подтверждается не только уменьшением количества связей -О-4 и -О-4, но и уменьшением в 1,4 раза пинорезинольных, фенилкумарановых связей, в 2,9 раза олефиновых фрагментов. Это неизбежно приводит к завышенному значению концентрации метоксильных групп в модифицированном препарате, если оценку производить по приросту содержания метоксильных групп, выраженному в % мас. и существенной погрешности в оценке содержания -ОН спиртовых и ОН-карбоксильных групп при стандартных химических методах анализа лигнинов.
Метилирование диметилсульфатом (ЛМРДМС). Модифицирование ЛМР ели диметилсульфатом должно приводить к метилированию первичных, вторичных спиртовых и фенольных групп, как показано на примере соединений, моделирующих фрагменты макромолекулы лигнина:
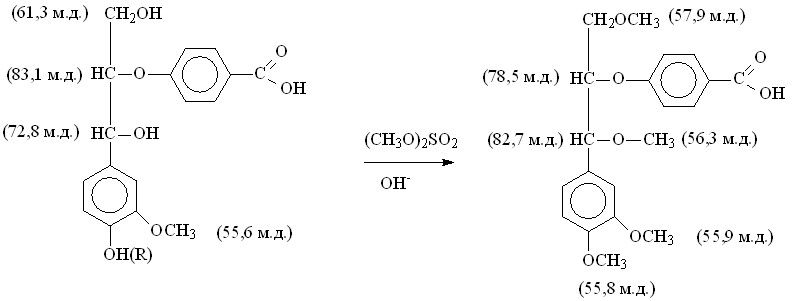
Относительное содержание атомов водорода фенольных ОН-групп в спектрах ЯМР 1Н уменьшилось в 4,3 раза, т.е. остались непрореагировавшими ~25% от количества их в исходном лигнине (табл. 4).
Анализ спектров ЯМР 1Н и 13С препарата ЛМРЕ-ДМС показывает, что в макромолекуле лигнина практически не осталось карбоксильных ОН-групп, при этом на такое же количество увеличилось содержание сложноэфирных групп (табл.4). Это свидетельствует о протекании побочной реакции метилирования карбоксильных ОН-групп, что не учитывается данной методикой.
Обнаружены >СН2ОSO3 фрагменты, на протекание данной побочной реакции указывают резонансные сигналы в области 70-80 м.д. в спектре СН2+С. Поскольку в результате реакции не образуется структурный фрагмент >СН2-О-СН3, как предполагалось по вышеприведенной схеме реакции, то невозможно произвести оценку содержания спиртовых -ОН-групп химическим способом по приросту групп -ОСН3.
Метод спектроскопии ЯМР 13С позволяет провести такую оценку по убыванию интегральной интенсивности сигналов -СН2ОН групп в области 58-65 м.д. и одновременно по приросту интегральной интенсивности сигналов в области 70-80 м.д. (по спектрам СН2+С). Из 56,5 -СН2ОН групп (в расчете на
100 АК) в ЛМРЕ прореагировало 47 групп.
Метилирование диметилсульфатом приводит к разрыву -О-4 и -О-4 связей, но в отличии от реакции метилирования метанолом, в этой реакции не происходит деструкции боковых цепей. Средняя длина боковой цепи остается практически такой же, как и в исходном лигнине.
Суммарное содержание групп ОНфен и ОНалк в исходном ЛМРЕ составляет 10,2% мас. Расчет концентрации этих групп, осуществленный только по приросту метоксильных групп, дает всего 7,3% мас. С учётом реакции сульфирования -СН2ОН групп расчет показал, что содержание ОНалк составляет 5,3% масс. Если учесть содержание непрореагировавших фенольных и карбоксильных групп, то получим значение, близкое к их содержанию в исходном ЛМР.
Метилирование диазометаном (ЛМРДАМ). Известно, что диазометан чрезвычайно легко и количественно реагирует с гидроксильными группами и как следует из схемы реакции, должен метилировать ОН-группы фенолов и карбоновых кислот:

Известно, что кроме метилилирования диазометаном ОН-групп, могут протекать реакции с участием структурных единиц лигнина, содержащих - или -карбонильную группу со смежной ОН- или ароксильной группой с образованием 1,1-дизамещенного этиленоксида:
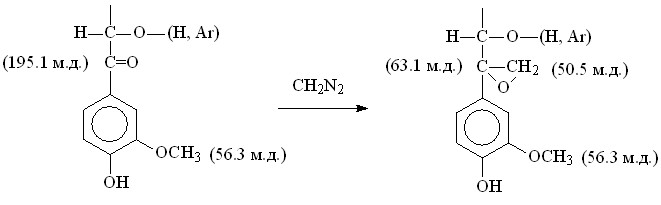
Анализ спектра ЯМР 1Н препарата ЛМРЕ-ДАМ, зарегистрированного в растворе ГМФТА-D18, показывает, что только часть фенольных групп ОН прореагировали с диазометаном. Количество непрореагировавших фенольных ОН- групп составляет 24,7/100АК или 1,8% мас.
Прирост метоксильных групп в лигнине, метилированном диазометаном, составил 4,2% мас., что соответствует наличию в лигнине 2,3% ОН-групп. В исходном ЛМР ели их суммарное количество равняется 4,2% мас. Следовательно, результаты, полученные с помощью метилирования диазометаном (2,1% мас.), занижены в 1,5 раза.
Конверсия карбоксильных ОН-групп прошла практически на 100%, т.е. в реакцию вступило 5,3/100АК. В 2 раза уменьшилось содержание двойных связей, это свидетельствует о присоединении диазометана к боковой цепи, что приводит к увеличению её средней длины до 3,6 атомов углерода, приходящихся на ароматическое кольцо. Таким образом, если оценивать содержание ОН-групп по приросту ОСН3-групп, то результат будет занижен на 28% отн.
Последовательное метилирование: диазометаном и метанолом (ЛМРДАММ). Метилирование двумя метилирующими агентами диазометаном и метанолом применяется для определения суммарного содержания фенольных, кислотных и спиртовых ОН-групп, находящихся в -положении к ароматическому кольцу.
Их сумма в ЛМРЕ составляет 4,9% мас., определенная по приросту содержания метоксильных групп 3,3% мас. (табл. 4). Причины недооценки аналогичны описанным выше: непрореагировавшие ОHфен, изменение структуры модифицированного лигнина за счет побочных реакций и потери массы. При последовательном воздействии двух химических реагентов происходит существенная деструкция макромолекулы лигнина: исчезают карбоксильные ОН-группы, увеличивается содержание фрагментов С(О)ОR, уменьшается количество олефиновых фрагментов, в 2,5 раза снижается количество атомов С и С, участвующих в образовании алкил-арильных простых эфирных связей, содержание спиртовых групп -СН2ОН уменьшается в 2 раза.
Результат последовательного воздействия двух реагентов приводит к модифицированному препарату лигнина ели, средняя структурная формула которого не соответствует исходному ЛМРЕ и полученные данные о содержании гидроксильных групп нельзя напрямую переносить на исходный лигнин.
Ацетилирование (ЛМРА). Метод ацетилирования наиболее универсальный, надежный и часто применяемый метод для количественного определения гидроксильных групп, как в индивидуальных, так и в многокомпонентных системах природного происхождения. Предполагается, что ацетилируются только спиртовые и фенольные ОН-группы.
В отличие от других методов потеря массы лигнина в процессе реакции составляет всего 4%.
В спектре ЯМР 1Н ацетилированного лигнина практически отсутствуют сигналы атомов водорода карбоксильных групп С(О)ОН. Это указывает на реакцию ацилирования карбоксильных групп, что не учитывает методика. Доля атомов водорода фенольных гидроксильных групп уменьшилась в 30 раз по сравнению с исходным ЛМРЕ. Однако и в ацетилированном препарате, несмотря на высокий процент превращения кислых ОН-групп, не прореагировало 3% мас. алифатических групп ОН.
Концентрация всех кислых групп ОН (в том числе карбоксильных), рассчитанная по спектру ЯМР 13С ацетилированного лигнина, составляет 9,9% мас.; по спектру ЯМР 1Н ацетилированного лигнина – 10,1%, тогда как в исходном лигнине – 10,7% мас. В этом случае результаты по суммарному содержанию кислых групп ОН удовлетворительно согласуются с полученными для исходного ЛМР ели.
Установлено, что в процессе химических реакций и последующего выделения модифицированных препаратов лигнина происходит деструкция макромолекулы, что приводит к значительным потерям массы лигнина, при этом отщепляются низкомолекулярные соединения, химическая структура которых не соответствуют усредненной структуре макромолекулы лигнина; протекают побочные химические реакции, в том числе и не обнаруженные для модельных соединений; из-за пространственных затруднений конверсия функциональных групп ни в одном из методов не достигает 100%. В совокупности это приводит к непредсказуемой модификации химической структуры исследуемого природного полимера и, как следствие, к большим погрешностям в оценке содержания функциональных групп.
Разработанный метод контроля трансформации химической структуры макромолекулы лигнина в результате химических реакций может быть рекомендован в качестве аттестационного для всех методик оценки функциональных групп в лигнинах, использующих химическую модификацию.
Идентификация лигнинов в сложных смесях органических соединений техногенного происхождения. Анализ смесей органических соединений техногенного происхождения, в частности компонентов сточных вод целлюлозно-бумажных комбинатов (ЦБК) – сложная и трудоёмкая задача. Она представляет интерес в плане расширения информационной базы о составе и свойствах этих смесей, поскольку поступление экстрактивных веществ древесины и лигнина в водоемы приводит к их накоплению вследствие медленной трансформации и длительному токсичному влиянию на гидробионтов, к нарушению экологического баланса.
Идентификацию лигнинов в сточных водах сульфатно-целлюлозного производства (смесь полифункциональных и полидисперсных по молекулярной массе веществ) обычно проводят традиционными химическими методами, а также методами ИК- и УФ-спектроскопии по наличию в спектрах полос поглощения хиноидных групп.
Метод идентификации и количественной оценки лигнинов в сточных водах ЦБК продемонстрирован нами на примере исследования так называемых «лигнинных веществ» (ЛВ), выделенных из биологически очищенных сточных вод Байкальского ЦБК.
ЛВ выделены из сточных вод сорбционным методом и разделены по растворимости в воде на две фракции. Первая из них с Мw до 28000 (фракция I) практически полностью осаждается из водной среды при рН < 3 и вносит основной вклад в цветность сточных вод. Вторая фракция с Мw до 7000 – составляет около 14% от всех ЛВ, выделена упариванием из нейтрализованного фильтрата после отделения ЛВ фракции I, с последующим растворением в бутаноле (фракция III). ЛВ, не растворившиеся в бутаноле (~20%), с Mw 3200 представляют фракцию II. Фрагментный состав фракций приведён в табл. 5.
Таблица 5. Распределение атомов углерода (qx) по структурным фрагментам фракций I, II, III, % отн.
| Фрагмент | qх фракций | Диапазон ХС 13С, м.д., отнесение сигналов | |||
| I | II | III | |||
| С=О, С(О)Н | 1,5 | 0,1 | 2,6 | 220-186 | С=О кетонов, альдегидов |
| >С=Охин. | 1,8 | 1,3 | 3,0 | 186-180 | С=О хиноидных структур |
| С(О)О(Н, R) | 5,9 | 7,7 | 10,7 | 185-164 | С(О)ОН, С(О)ОR |
| Сар-О, Сар-Cl | 2,8 | 8,2 | 9,8 | 164-140 | Сар-О, Сар-Cl, С-3, С-5 S,S |
| Сар.-С, Сар-Н. | 22,0 | 24,7 | 29,2 | 140-103 | С-4 в S,S; C-1, C-2, C-5, C-6 в G,G и H,H; С-2,С-6 в S,S; -CH=CH- |
| С-1 угл. | 0,3 | 0,2 | 0,3 | 103-96 | С-1 аномерные атомы углеводов |
| >СН-О- (1) | 2,9 | 0,3 | 0,4 | 96-80 | С в -О-4, -, НС-ОН; С в -О-4 |
| >СН-О- (2) | 7,1 | 1,0 | 2,0 | 80-65 | С в -О-4 |
| -СН2-О- | 5,0 | 1,4 | 1,3 | 65-59 | Н2С-ОН |
| ОСН3 | 3,7 | 3,2 | 2,4 | 59-55 | ОСН3 в Ar-OCH3 |
| Салк | 37,7 | 51,4 | 38,3 | 55-20 | С, СН, СН2, СН3 алифатические |
| fa | 34,7 | 32,0 | 39,0 | 164-103 | cтепень ароматичности |
Анализ спектров ЯМР 13С фракций I-III позволил идентифицировать лигнины, углеводы и насыщенные карбоновые кислоты.
Содержание лигнина, оценили по характеристичным сигналам атомов углерода в области 93-65 м.д., которые принадлежат атомам С и С в связях -O-4, -O-4 (в экстрактивных веществах древесины подобных структурных фрагментов нет). Иным способом провести идентификацию лигнина практически невозможно. Поскольку БЦБК использует древесину хвойных пород, а способ делигнификации – сульфатная варка, за основу расчета содержания лигнина в I-III (табл. 6) приняли количество атомов углерода в расчете на АК, принадлежащих связям -O-4, -O-4 и группам ОСН3, характерное для макромолекул лигнинов щелочных способов делигнификации древесины хвойных пород.
Установлено, что количество хиноидных групп никак не коррелирует с содержанием лигнина в составе фракций I-III (см. табл. 5 и 6), следовательно, оценить содержание лигнина в смесях органических веществ техногенного происхождения по концентрации этих групп не представляется возможным.
Таблица 6. Содержание функциональных групп, углеводов, лигнина и карбоновых кислот во фракциях I, II, III
| Функциональная группа | Содержание,% мас. | ||
| I | II | III | |
| >С=Окет, альд. | 1,9 | 0,4 | 2,4 |
| >С=Охин | 2,2 | 0,5 | 2,8 |
| С(О)ОН, С(О)ОR | 11,5 | 5,0 | 16,1 |
| ОСН3 | 5,0 | 1,4 | 2,5 |
| Углеводы | 2,0 | 0,6 | 1,7 |
| Лигнин | 39,2 | 7,2 | 13,5 |
| Карбоновые кислоты | 58,8 | 92,2 | 84,8 |
Идентификацию и количественную оценку углеводов проводили по сигналам анамерных атомов углерода в области 93103 м.д. Карбоновые кислоты (до 92 %, табл. 6), представлены преимущественно соединениями с длинными алифатическими цепями, являющимися продуктами жизнедеятельности бактерий и микроорганизмов, используемых при биохимической очистке сточных вод БЦБК.
Разработанный подход идентификации лигнинов универсален и может быть применен при анализе любых смесей растворимых органических соединений, техногенного происхождения, содержащих продукты переработки древесины.
Глава II. Количественная спектроскопия ЯМР 1Н и 13С как метод оценки оптимальных условий каталитического гидрирования тяжёлых угольных смол
Основными процессами химической переработки угля являются коксование и полукоксование, т.е. термодеструкция угольной матрицы (рис. 5). Выделяющиеся каменноугольные смолы содержат ценные химические компоненты, которым до настоящего времени не находят квалифицированного применения. Основными препятствиями их переработки является поликомпонентность, высокая концентрация кислород-, азот- и серосодержащих органических соединений, полидисперсность, нестабильность состава, что существенно затрудняет идентификацию индивидуальных компонентов угольных смол и проведение анализа их структурно-группового состава.
В настоящей главе рассматривается применение количественной спектроскопии ЯМР 1Н и 13С с целью оптимизации технологических процессов получения продуктов с заданным составом и свойствами при переработке угольных смол. Достижение поставленных целей контролировали с помощью разработанных в настоящей работе подходов к характеристике многокомпонентных систем природного и техногенного происхождения на основе фрагментного состава, полученного методом количественной спектроскопии ЯМР 1Н и 13С. Закономерности изменения фрагментного состава позволяют выявить наиболее эффективные способы переработки углеводородного сырья, оценивать вклад отдельных реакций, что имеет важное теоретическое и практическое значение. Включение в схему анализа спектроскопии ЯМР в количественном варианте, позволяет увеличить экспрессность и точность анализа, избежать ряда трудоёмких операций, которые могут изменить состав анализируемого объекта.
Определение состава исходного сырья. Каталитической термодеструкции угля различных месторождений Восточной Сибири подвергали жидкофазные продукты переработки угля – тяжелую смолу (ТС), кубовый остаток среднего масла (КО), образующихся при переработке смолы среднетемпературного коксования угля, вакуумный погон (ВП), выделенный ректификацией под вакуумом до 450 0С из тяжелой смолы; в качестве растворителя использовали обесфеноленное легкое масло (ОЛМ), являющееся отходом этого производства (рис.5).
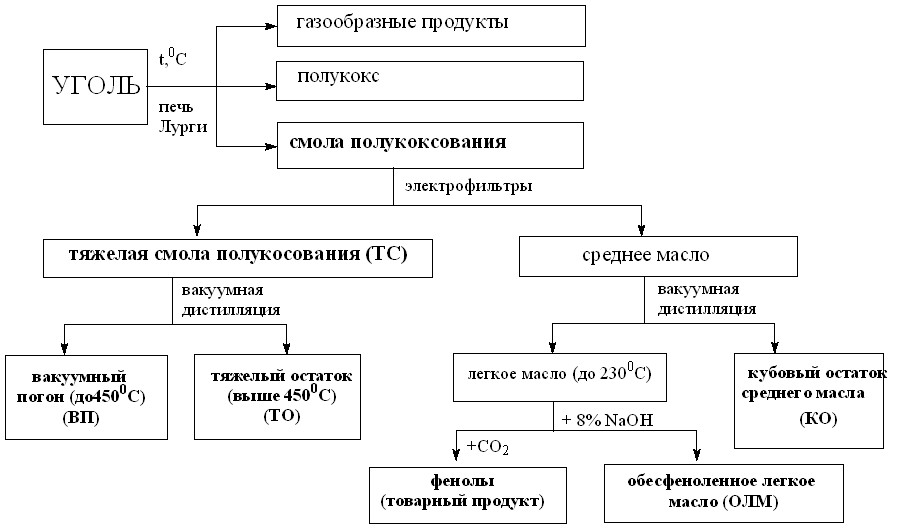
Рис.5. Схема переработки угля и объекты исследования
Наиболее эффективным процессом переработки угольных смол является каталитическая деструктивная гидрогенизация. Известно, что доминирующими реакциями каталитического гидрирования угольных смол являются реакции гидрирования, крекинга, изомеризации, диспропорционирования и деалкилирования.
Установление группового состава получаемых гидрогенизатов химическими методами – трудоёмкий и длительный процесс, сопровождающийся значительными потерями и погрешностями количественной оценки их содержания в многокомпонентных смесях. Качество структурно-спектральных взаимосвязей технологического процесса оценивали по фрагментному составу, полученному из спектров ЯМР 1Н и 13С (результаты ЯМР-исследований сопоставляли с результатами химических методов анализа угольных смол и продуктов их гидрогенизации, табл. 7).
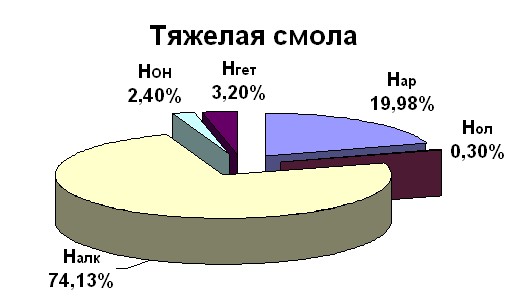
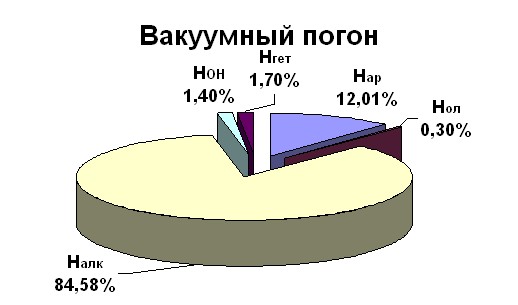
ТС, КО, ВП – вязкие системы, представляющие собой неравновесные смеси кислых (карбоновые кислоты и фенолы), основных (азотсодержащие соединения) и нейтральных компонентов (альдегиды, эфиры, алканы, арены, сероорганические соединения и т.д.). Фрагментный состав исходного сырья представлен на рис. 6: НОН – атомы водорода карбоновых кислот, фенолов, карбазолов, Нар – атомы водорода ароматического кольца, Нгет – алифатические и ароматические атомы водорода в гетероциклических углеводородах, Нол – атомы водорода двойных связей, Налк – алифатические атомы водорода нейтральных соединений.
Таблица 7. Относительное содержание водорода фенольных гидроксильных групп фенолов из спектров ЯМР 1Н (ЯМР) и химических методов (Х.М.)
| Объект исследования | [H], % мас. | qOH фен, %отн. | Фенолы, % мас. | |||
| Нон | Нон | ЯМР | Х.М. | |||
| 9,5 -12,8 м.д. | 9,5-10,0 м.д. Диорто-замещенные фенолы | Суммарное содержание | Диорто-замещенные фенолы | Суммарное содержание фенолов | ||
| Исходные смолы | ||||||
| ОЛМ | 10.7 | 0,35 | 0,07 | 4,7±0,6 | 1,0 | 3,0 |
| КО | 8.7 | 2,81 | 0,22 | 30,6±4,2 | 2,5 | 30,1 |
| ВП | 9.1 | 1,80 | 0,22 | 20,5±2,8 | 2,6 | 19,6 |
| ТС | 6.6 | 2,26 | 0,39 | 18,7±2,6 | 3,3 | 18,2 |
| Смеси смол | ||||||
| ТС : ОЛМ = 2:1 | 8.0 | 1,39 | 0,19 | 13,9±1,9 | 2,0 | 13,1 |
| ТС : ОЛМ = 1:1 | 8.7 | 1,44 | 0,19 | 15,7±2,2 | 2,1 | 10,6 |
| ВП : ОЛМ = 2:1 | 9.6 | 1,01 | 0,05 | 12,1±1,6 | 0,6 | 12,0 |
| КО : ОЛМ = 2:1 | 9.4 | 1,91 | 0,18 | 22,4±3,1 | 2,2 | 21,1 |
| ВП:КО:ОЛМ = 1:1:1 | 9.5 | 1,92 | 0,16 | 22,8±3,1 | 2,0 | 17,6 |
 |  |
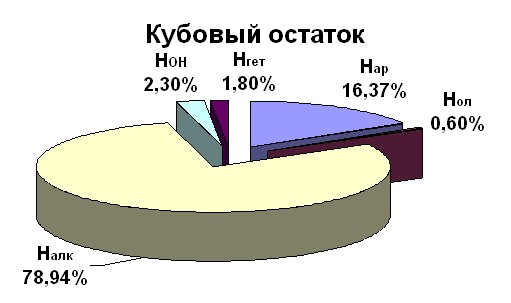 | 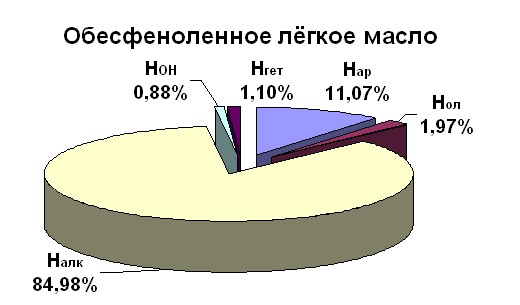 |
Рис. 6. Фрагментный состав исходного сырья из спектров ЯМР 1Н в растворе ГМФТА-D18
Разработан надёжный и экспрессный метод определения содержания фенолов (в % мас.) в многокомпонентных смесях с использованием количественной спектроскопии ЯМР 1Н.
Наблюдаемые значения ХС атомов водорода ОН-групп фенолов в ГМФТА-D18 отражают комбинацию тонких внутримолекулярных эффектов заместителей, так электроноакцепторные, в основном, дезэкранируют атомы водорода ОН-групп. Отнесение отдельных сигналов к конкретному соединению по спектрам ЯМР проведено для модельных смесей фенолов методом добавок. В спектрах ЯМР 1H в ГМФТА-D18 выделены четыре группы сигналов ОН-групп фенолов и проведена количественная оценка содержания основных структурных фрагментов (рис. 6, табл. 7).
Пространственно затрудненные полиалкилфенолы в наименьшей степени способны к образованию комплекса (1:1) с ГМФТА-D18. Сигналы ОН-групп моно- и диалкил- ортозамещённых фенолов обнаруживаются в области 9,5-10,5 м.д. (Нон I).
Для триалкилзамещённых фенолов важную роль играет симметрия расположения заместителей и пространственное строение молекул. В стерически затруднённых (2,3,6-замещённые алкилфенолы) сигналы ОН-групп наблюдаются в области 9,0-9,3 м.д., при меньшем экранировании (3,4,5-алкилзаме-щённые, 2,3,4,5-замещенные фенолы) в области 10,0-10,5 м.д. (Нон, II).
Сигналы ОН-групп нафтолов, пара-алкилзамещённых фенолов находятся в области 10,5-11,6 м.д. (НонIII). Фенолы с электроноакцепторными заместителями в мета- и пара-положениях, альдегидными группами сдвигают сигналы атомов водорода ОН-групп в область 11,6-12,8 м.д. (Нон IV). В области 12,8 -14 м.д. расположены атомы водорода С(О)ОН групп карбоновых кислот.
На рис. 7 представлены результаты определения содержания фенолов в исходном сырье традиционными химическими методами и из спектров ЯМР 1Н, зарегистрированных в растворе ГМФТА-D18, рассчитанные по соотношению: ![]() , где qOH фен. – доля атомов водорода фенольных групп ОН, [H] – содержание водорода, %, ММфен – средняя молекулярная масса фенолов из расчёта на среднюю структурную формулу С8Н9,5О1,5, вариация концентраций фенолов приведена в табл. 7.
, где qOH фен. – доля атомов водорода фенольных групп ОН, [H] – содержание водорода, %, ММфен – средняя молекулярная масса фенолов из расчёта на среднюю структурную формулу С8Н9,5О1,5, вариация концентраций фенолов приведена в табл. 7.
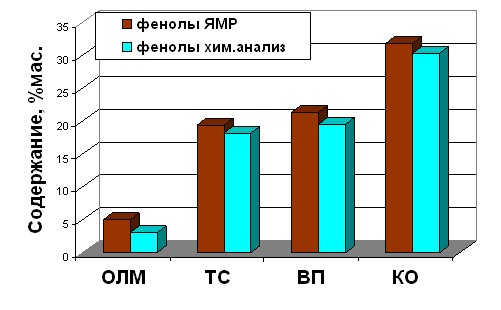
Рис. 7. Результаты оценки содержания фенолов химическим методом и количественной спектроскопией ЯМР 1Н
Результаты (табл. 7) объясняют причину отличия в оценке содержания фенолов различными способами: при химическом выделении фракции фенолов диорто-замещенные фенолы, как правило, не полностью извлекаются из сложных смесей.
Оптимизация каталитического процесса получения низкомолекулярных фенолов из угольных смол в статических условиях. Серия автоклавных экспериментов с использованием в качестве компаундов сырья фракций термической переработки углей Черемховского и Канско-Ачинского бассейнов преследовала три цели: получение низших одноатомных фенолов, уменьшение доли гетероатомных соединений в гидрогенизатах, увеличение выхода насыщенных углеводородов. При этом варьировали следующие параметры процесса гидрогенизации состав и количество катализатора, температуру реакции, давление водорода, состав исходной реакционной смеси. Проведено >100 экспериментов, испытано >10 катализаторов, содержащих молибден, вольфрам, алюминий и другие металлы в сульфидной или оксидной формах.
В табл. 8 приведены результаты исследования суммарных фенолов, выделенных из тяжелой смолы полукоксования угля Черемховского местрождения; фенолов, выделенных из гидрогенизатов суммарных фенолов по методике селективной экстракции (методика Стадникова).
Таблица 8. Относительное содержание атомов водорода фенольных смесей в структурных фрагментах из спектров ЯМР 1Н в ГМФТА-D18, %
| Структурные фрагменты | Диапазоны ХС, м.д. | Объект исследования | ||
| Суммарные фенолы из исходной смолы | Фенолы из гидрогенизата (катализатор НВС) | Фенолы из гидрогенизата (катализатор НВСА) | ||
| НCOOH | 12,8 14,0 | 0,4 | 0,2 | 0,4 |
| НOH IV | 11,6 12,8 | 0,6 | 0,4 | |
| НOH III | 10,5 11,6 | 3,1 | 3,4 | |
| НOH II | 10,0 10,5 | 4,6 | 2,0 | 2,4 |
| НOH I | 9,5 10,5 | 0,8 | 0,7 | 0,9 |
| Нар | 6,0 9,3 | 28,0 | 24,8 | 24,4 |
| H | 2,0 4,5 | 40,2 | 36,6 | 32,1 |
| H | 1,0 2,0 | 19,2 | 23,1 | 26,7 |
| Н | 0,5 1,0 | 6,9 | 8,9 | 9,4 |
| НОН фенолов, % мас. | 6,5 | 10,3 | 11,5 | |
| Фенолы, % мас. | 93,8 | 79,0 | 87,7 | |
| Средняя длина цепи | 1,6 | 1,9 | 2,1 | |
В спектрах ЯМР 1Н исследуемых смесей наблюдаются сигналы С(О)ОН атомов оксикарбоновых кислот и ОН-групп фенолов. В исходной смоле доминируют 3,4,5- или 2,3,4,5-алкилзамещенные фенолы в присутствии небольшого количества диорто-замещенных фенолов в диапазоне 9,410,5 м.д. (Нон, II) и 9,510,5 м.д. (НOH, I). Каталитическое гидрирование исходной смолы приводит к образованию нафтолов, 4-(3,4)-алкилзамещённых фенолов (10,511,6 м.д.) и фенолов с электроноакцепторными заместителями в мета- и пара-положениях (11,612,8 м.д.).
Анализ состава фенолов исходных смол и гидрогенизатов (табл. 8) позволяют предложить один из возможных путей деструкции молекул полизамещенных алкилфенолов с образованием низкомолекулярных алкилзамещённых одноатомных фенолов в процессе каталитической гидрогенизации:
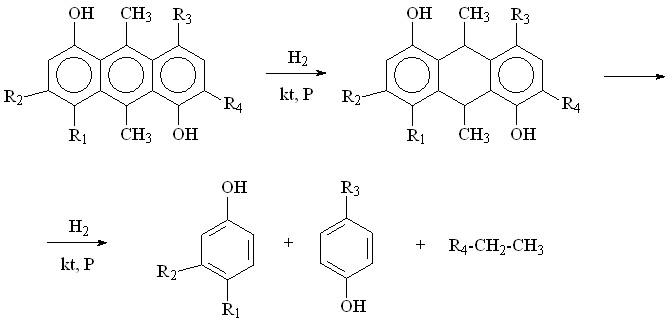
Детализацией изменений параметров фрагментного состава фенольных фракций и суммарных продуктов гидрогенизации угольных смол (рис. 8) выявлены оптимальные условия их гидрирования – на первой ступени для достижения максимального выхода низкомолекулярных одноатомных фенолов реакцию рекомендовано проводить при температуре 350°С, давлении 4 МПа на никельвольфрамсульфидном катализаторе (НВС).
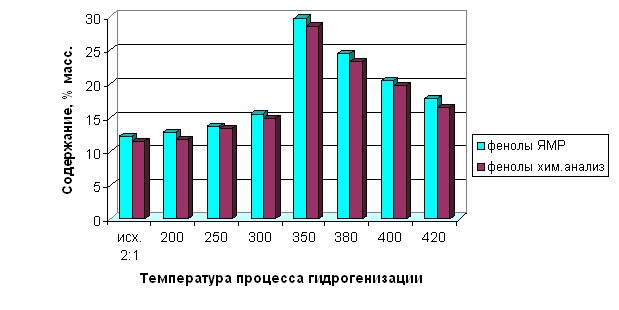
Рис. 8. Содержание фенолов в гидрогенизатах смолы КАУ (смесь КАУ :ОЛМ = 2:1) химическим методом и количественной спектроскопией ЯМР 1Н
Оптимизация условий процесса каталитического гидрирования угольных смол в проточных установках. Последовательное изучение процессов каталитического гидрирования угольных смол в автоклаве завершено серией экспериментов в проточных установках полупромышленного типа. Доминирующими реакциями гидрогенизации угольных смол являются гидрирование и крекинг при участии реакций изомеризации, диспропорционирования, деалкилирования. Прогнозировать состав, обуславливающий образование надмолекулярных структур и наличия стабильных радикалов в гидрогенизатах, крайне трудно из-за поликомпонентности, поэтому эффективность выбранных параметров технологического процесса оценивали по содержанию отдельных функциональных групп и фрагментов (табл. 9).
По разработанной методике, характеризующей распределение спектральной плотности в ароматическом и алифатическом диапазоне спектров ЯМР 1Н и 13С, получен фрагментный состав жидкофазных продуктов термодеструкции углей Черемховского и Канско-Ачинского месторождений: вакуумного погона (ВП, t 450 0С), обесфеноленного лёгкого масла (ОЛМ). В настоящем разделе работы разрабатываемый подход к оценке оптимальных условий технологических процессов продемонстрирован на примере исследования суммарных продуктов каталитической гидрогенизации тяжелых угольных смол Черемховского месторождения, полученных в проточной установке.
Таблица 9. Фрагментный состав исходной смолы и продуктов гидрогенизации из спектров ЯМР 1Н, 13С, %
| Фрагмент | Фрагментный состав, % | |||||
| ВП : ОЛМ 2 : 1 | I ступень | II ступень | III ступень | |||
| опыт 1 (Ni-Mo) | опыт 2 (Al-Ni-Mo) | 1 опыт (Ni-WS2) | 2 опыт (Ni-WS2) | |||
| Нap | 14,3 | 11,2 | 5,4 | 7,8 | 1,5 | 1,8 |
| НС=С | 0,5 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| H | 27,3 | 27,2 | 14,7 | 17,0 | 10,6 | 8,7 |
| Н | 42,3 | 45,2 | 59,8 | 52,5 | 57,7 | 62,2 |
| Н | 14,7 | 14,5 | 20,1 | 22,6 | 30,2 | 27,3 |
| НСООН | 0,1 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| НОНфен | 0,9 | 1,5 | 0,0 | 0,0 | 0,0 | 0,0 |
| С=О+ С(О)О | 4,8 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| СН2 | 24,7 | 31,8 | 37,5 | 46,5 | 56,5 | 55,3 |
| СН | 3,8 | 7,6 | 22,6 | 12,2 | 23,4 | 21,7 |
| CH3 | 14,0 | 14,5 | 15,3 | 15,2 | 13,6 | 14,4 |
| СНар | 22,3 | 19,6 | 9,9 | 14,0 | 2,4 | 4,1 |
| Сар-О | 7,6 | 5,5 | 0,0 | 0,0 | 0,0 | 0,0 |
| Сар | 23,0 | 10,8 | 9,1 | 11,1 | 3,6 | 4,5 |
| fa | 52,9 | 44,1 | 19,6 | 26,0 | 6,0 | 8,5 |
| Ак = Н/Н | 1,4 | 38,6 | 55,9 | 50,2 | 20,8 | |
| Аг= Нар/Нар | 21,7 | 51,8 | 30,4 | 72,2 | 76,9 | |
| = Ак/Аг | 0,1 | 0,8 | 1,8 | 0,7 | 0,3 | |
Гидрогенизацию угольных смол проводили в две или три ступени. Гидрогенизаты второй ступени подвергали гидроочистке (III ступень гидрогенизации).
I ступень легкий гидрокрекинг тяжелой смолы или выделенного из нее вакуумного погона (ВП) в смеси с обесфеноленным легким маслом (ОЛМ). На этой стадии происходит гидрооблагораживание исходного продукта: уменьшение содержания асфальтенов, частичный гидрогенолиз азот- и серосодержащих соединений, увеличение выхода низкокипящих одноатомных фенолов за счет деалкилирования высших фенолов.
II ступень — гидрокрекинг обесфеноленного гидрогенизата I ступени под давлением водорода и при повышенной температуре. На этой стадии наблюдаются резкие изменения в составе полученного продукта: уменьшение или полное отсутствие асфальтенов, кислых компонентов, азот- и серосодержащих соединений и увеличение до 80-90% углеводородов различного строения, преимущественно алканов.
III ступень — гидроочистка гидрогенизатов II ступени для получения углеводородов определенного строения.
При гидрогенизации смол реакции гидрирования и крекинга конкурируют как между собой, так и с другими реакциями (изомеризации, конденсации, диспропорционирования). Вклад каждой из основных реакций оценивается из спектров ЯМР 1Н, в результате расчета показателей гидрирующей Аг и крекирующей Ак активности катализатора, мерой которых может служить отношение разности доли атомов водорода конденсированных ароматических колец и метильных групп в гидрогенизате к их доле исходном продукте:
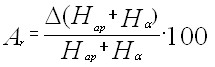
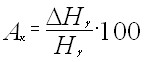
Отношение величин (Ак/Аг=) – мера эффективности процесса.
Анализ суммарного продукта гидрокрекинга (ступень I, табл. 9) обнаружил существенное увеличение выхода низкокипящих одноатомных фенолов за счет деалкилирования высших фенолов (доля НОНфен увеличивается в 1,8 раза) и восстановление соединений с С=О группами, протекание реакции гидрирования ненасыщенных структур. На II ступени доминируют реакции гидрирования ароматических колец: в 1,4 – 2,0 раза снижается степень ароматичности продуктов (fa); крекинг углеводородов наблюдается с образованием разветвленных алканов, увеличение степени разветвлённости фрагментов. На III ступени усиливается роль реакции гидрирования ненасыщенных соединений, заметно, что в опыте 1 образуются более разветвленные алканы с короткими цепями, чем в опыте 2 (табл.8). Следовательно, меняя условия процесса можно получать смесь алканов заданного строения.
Сложность изучаемых объектов, многообразие химических реакций, затрудняют выделение основных по значимости параметров, которые необходимо использовать для оценки структурных изменений в исследуемых объектах.
С целью установления иерархии процессов, протекающих при каталитическом гидрировании угольных смол был применен метод главных компонент факторного анализа. Процедура поиска наиболее значимых аналитических параметров включала следующие этапы: регистрация количественных спектров ЯМР 1Н и 13С, формирование на их основе матрицы наблюдений, факторный анализ, идентификация факторов.
Факторный анализ, объективно вскрывая внутренние связи главной части массива экспериментальных результатов, не постулирует их зависимость от априорно выбранной комбинации параметров. В отличие от регрессионного анализа, в котором произвольно задается число переменных, описывающих эксперимент, число анализируемых факторов в факторном анализе воспроизводит экспериментальную матрицу параметров.
Факторный анализ проводили с тремя массивами данных (табл. 10):
I. Полная матрица, т. е. продукты гидрогенизации охарактеризованы всеми структурными параметрами. II. Матрица, содержащая параметры спектров ЯМР 1Н и fа. III. Матрица, содержащая параметры только спектров ЯМР 13С.
Таблица 10. Факторные нагрузки на структурные параметры продуктов гидрогенизации смол углей Канско-Ачинского и Черемховского бассейнов
| Ва- риант | Фак- тор | Общ- ность | Переменные | |||||||||
| Нар | Н | Н | Н | fa | Cap | CHap | СН | СН2 | СН3 | |||
| I | 1 | 65 | 0,73 | 0,71 | -0,86 | -0,28 | 0,84 | 0,89 | 0,43 | -0,32 | -0,87 | -0,04 |
| 2 | 15 | -0,03 | 0,01 | -0,02 | 0,01 | 0,08 | -0,01 | 0,02 | -0,36 | 0,05 | -0,98 | |
| 3 | 9 | -0,32 | -0,50 | 0,05 | 0,95 | -0,23 | -0,28 | -0,01 | -0,04 | 0,26 | -0,01 | |
| 4 | 5 | 0,48 | 0,15 | -0,36 | -0,08 | 0,37 | 0,04 | 0,84 | -0,34 | -0,39 | -0,05 | |
| II | 1 | 75 | 0,90 | 0,38 | -0,77 | -0,19 | 0,67 | — | — | — | — | — |
| 2 | 18 | -0,33 | -0,48 | 0,05 | 0,95 | -0,22 | — | — | — | — | — | |
| III | 1 | 57 | — | — | — | — | — | 0,91 | 0,37 | -0,20 | -0,88 | -0,10 |
| 2 | 22 | — | — | — | — | — | -0,26 | 0,02 | 0,03 | -0,06 | 0,99 | |
| 3 | 14 | — | — | — | — | — | -0,27 | -0,35 | 0,94 | 0,09 | 0,02 | |
Установлено, что экспериментальная матрица первого варианта описывается четырьмя факторами с суммарной дисперсией 94%. Дисперсии факторов, а также их проекции на переменные (структурные параметры) приведены в табл. 10. Первый фактор имеет наиболее высокие отрицательные нагрузки на переменные Н и СН2 и положительные — на переменные Нар, Н, fа, Сар. Соотношение факторных нагрузок для переменных, определяющих первый фактор, зависит от условий проведения гидрогенизации. Поскольку знаки факторных нагрузок для переменных Н, Н, СН2 и Нар, fа, Сар противоположны друг другу, характер их группирования отражает доминирующий процесс, т. е. гидрогенизацию ароматических колец и повышение содержания насыщенных фрагментов. Второй и третий факторы, вклад которых в суммарную дисперсию составляет 24%, указывают на изменения содержания атомов углерода СН3-групп и Н-протонов, что связано с соответствующим процессом крекингом алифатических цепей. Четвёртый фактор, отражает процессы, вклад которых невелик (5%) и связан с изменением содержания третичных атомов углерода ароматических колец.
Обработка совокупности экспериментальных параметров показывает, что наиболее ярко выражены нагрузки на переменные, учитывающие процессы гидрирования ароматических колец и деструкции алкильных цепей. Для выяснения степени информативности спектров ЯМР 1Н обработана матрица, состоящая из структурных параметров, получаемых только из спектров ЯМР 1Н и параметра fа (вариант II). Совокупность экспериментальных результатов описывается на 93% двумя факторами. Первый фактор (75% общей дисперсии) характеризуется сильной связью с параметрами Нар и Н, причем, как в варианте I, знаки факторных нагрузок противоположны. Второй фактор вновь характеризует перераспределение протонов алифатического фрагмента, что тоже согласуется с вариантом I.
Результат обработки структурных параметров, полученных только из спектров ЯМР 13С (вариант III), показывает, что распределение факторных нагрузок для этих структурных параметров совпадает с таковым для вариантов, рассмотренных выше. Таким образом, для выявления основных структурных особенностей продуктов гидрогенизации смол, заметно отличающихся по структурно-групповому составу, можно оперировать значениями структурных параметров, полученных исключительно из спектров ЯМР 1Н. Это дает возможность отказаться от привлечения сложной процедуры получения количественных подспектров ЯМР 13С и существенно повысить экспрессность методики, понизить трудоёмкость при сохранении информативности.
Таким образом, показано, что с помощью метода количественной спектроскопии ЯМР можно производить достоверную и надежную оценку оптимальных условий каталитической гидрогенизации тяжелых угольных смол, а также количественно характеризовать вклад различных реакций в процессы гидрогенизации.
Глава III. Количественная спектроскопия ЯМР в исследовании гуминовых веществ
Гуминовые вещества (ГВ) и угли – объекты, генетически связанные химической модификацией растительного сырья. Молекулярное строение представлено стохастическими структурами нерегулярного строения, отличающиеся гетерогенностью структурных элементов и полидисперсностью. К таким объектам неприменимы способы численного описания строения, характеризующего количество атомов в основном структурообразующем звене, типов связей между ними. Отсутствие методологических подходов к анализу последовательного превращения органического вещества лигнина определило актуальность проведения систематических исследований их строения, результаты которых служат основой для их классификации.
Гуминовые вещества (ГВ) бурых углей. Результаты количественной спектроскопии ЯМР 13С ГВ окисленных углей, частично обобщенные в монографии[1], позволили предложить набор дескрипторов, количественно характеризующих углеродсодержащие фрагменты, которые могут быть использованы для оценки их рост-стимулирующей активности. Подход перспективен для предварительного отбора по параметрам спектров ЯМР 13С окисленных углей, пригодных для создания физиологически активных препаратов ГВ без проведения трудоёмких лабораторных и полевых испытаний.
Изучена активность гуминовых веществ, окисленных в пластах бурых углей месторождений Монголии: свободных гуминовых кислот, осаждённых НС1 (рН=2) из щелочного экстракта бурого угля (СГК) и его остатка после обработки разбавленной азотной кислотой (СГК 1), а также отдельных групп соединений входящих в них – гиматомелановых кислот (ГМК, ГМК 1), гумусовых кислот (ГК, ГК 1), фульвокислот – (ФК, ФК 1), соответственно (рис. 9, табл. 11).
Проведенное исследование гуминовых препаратов из окисленных углей Восточной Сибири (Хандинское, Щеткинское и Березовское месторождения) показало значимый рост-стимулирующий эффект.
Результаты настоящего раздела с учётом информации по фрагментному составу изученных ГВ и данных по их биотестированию позволяют предполагать, что незначительная рост-стимулирующая активность практически у всех изученных препаратов ГВ углей Монголии может быть обусловлена высоким содержанием полициклических ароматических структур.
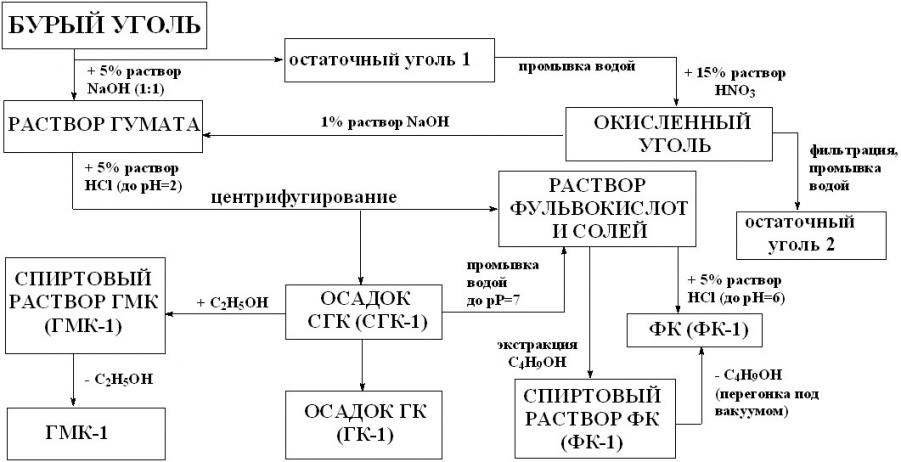
Рис.9. Выделение ГВ из бурого угля, окисленного азотной кислотой.
Таблица 11. Параметры фрагментного состава и относительная рост-стимулирующая активность (РА) некоторых ГВ
| Образец | >C=O | СООН | СарО | СарС,Н | СалкO | Cалк | РА* расчет |
| СГК | 5,3 | 13,0 | 10,8 | 51,4 | 3,0 | 16,5 | 0,40 |
| СГК-1 | 5,1 | 11,4 | 8,1 | 57,6 | 2,8 | 14,0 | 0,31 |
| ГК | 5,0 | 13,5 | 7,6 | 57,6 | 3,3 | 13,0 | 0,35 |
| ГК-1 | 4,9 | 12,6 | 9,6 | 51,1 | 6,8 | 15,0 | 0,42 |
| ГМК | 4,0 | 11,4 | 6,1 | 37,9 | 9,1 | 31,5 | 0,38 |
| ГМК-1 | 2,9 | 12,3 | 6,2 | 39,6 | 4,9 | 34,3 | 0,32 |
| ФК | 4,4 | 13,0 | 6,5 | 57,9 | 4,0 | 14,2 | 0,33 |
| ФК-1 | 1,0 | 13,4 | 6,2 | 63,5 | 1,8 | 14,1 | 0,28 |
*Рассчитано по соотношению: РА= 34,1 – 104,4х (r=0,85, r=16,3), где 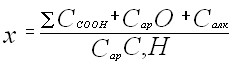
Это проявляется в дополнительном воздействии на растительные культуры (пшеница, кукуруза, картофель), схожим с таковым для нефтепродуктов, содержащих конденсированные ароматические структуры. Справедливость такого предположения в отношении обсуждаемых ГВ углей Монголии подтверждена совокупностью результатов их развернутого элементного анализа, ИК-спектроскопии, количественной спектроскопии ЯМР 1Н и 13С с редактированием спектров и оценкой величины эффекта Оверхаузера, позволяющим количественно определить содержание конденсированных ароматических структур, оценить доминирующий структурный фрагмент ГВ.
Основываясь на результатах элементного и фрагментного состава ГВ, значениях эффектов Оверхаузера в многоимпульсном эксперименте 1Н-1Н
NOESY, можно предложить «усредненный» фрагмент ГВ. Так, исходя из модели ГВ угля Мистерски-Логинова и низких положительных значений эффектов Оверхаузера, может быть предложен структурный единичный фрагмент ГВ следующего вида:
Такая усреднённая структура (40С, 37Н, 150, 1N, т.е. ММ=771) содержит 2С=О, 4СОО, 5СарО, 17СарС,Н (из них только 21 СарН), 5СалкО и 7Салк. Распределение водорода следующее: 2Нар, 3ОН, 2СООН, 18 атомов водорода в алкильных группах и 12 - у Сsp3 рядом с атомом кислорода. Измеренное среднее значение ММ (29,3 кДа) соответствует химически несвязанной слоисто-пачечной структуре из 5-6 слоев.
Результаты, полученные методом количественной спектроскопии ЯМР 13С и биотестированием ряда окисленных углей Сибирской платформы и Монголии, позволяют сделать предположение, что особенности молекулярного строения ГВ углей и их биологическая активность определяются геоклиматическими условиями процесса углеобразования и характером исходного сырья. В первую очередь, это касается содержания в растительном сырье лигнина – основы моноциклических ароматических фенилпропановых структур. Для выявления его значимости целесообразен детальный анализ фрагментного состава ГВ окисленных углей других сопредельных территорий.
Исходя из результатов проведенного нами исследования ГВ, для прогнозирования РА, предлагается следующий алгоритм тестирования угля и ГВ:
1. Анализ исходного бурого угля (ГОСТ 9517-94) (определение влажности, зольности на сухое вещество, выхода свободных гуминовых веществ на сухое и сухое беззольное состояние, зольности гуминовых веществ);
2. Установление молекулярного строения ГВ (элементный состав, молекулярно-массовое распределение, содержание функциональных групп и фрагментов методами ЯМР 13С и потенциометрического титрования) и прогнозирование на их основе РА.
Количественная спектроскопия ЯМР 13С в идентификации, аутентификации и выявлении сырьевого происхождения промышленных гуминовых веществ. ГВ выполняют ряд важных функций – регулируют процессы роста растений, улучшают физико-химические свойства почвы, стимулируют процессы дыхания, синтез белков и углеводов. Несмотря на широкое многообразие физико-химических методов исследования ГВ, полного понимания их строения, механизма действия, роли, функций в биосфере пока нет. Однако рынок предложений ГВ из разных видов сырья – бурых углей, торфов, сапропеля, лигнина неуклонно растёт. Предлагаемые препараты значительно различаются по своему составу, биологической активности, стоимости. Основная проблема, ограничивающая их широкое применение – отсутствие методов выявления источников их происхождения, установления строения и активности. Необходимо создание банка данных по строению ГВ и его связи со свойствами, характером и степенью воздействия на растения, живые организмы и т.д.
Методом количественной спектроскопии ЯМР 13С нами изучен состав ряда товарных ГВ с целью оценки возможных перспектив их использования (табл. 12).
Параметры фрагментного состава ГВ из спектров ЯМР являются строгим количественным отражением распределения атомов 1Н и 13С по функциональным группам и фрагментам этого сложного объекта (табл. 12). Если для задач аутентификации препаратов ГВ возможности методов ЯМР-, ИК-спектроскопии, гель-хроматографии в режиме «отпечатка пальцев» вполне сопоставимы, то выявление сырьевого происхождения более целесообразно осуществлять по спектрам ЯМР 13С с идентификацией и количественной оценкой различных функциональных групп, определяющих практические свойства препаратов.
Общей особенностью спектров ЯМР 13С ГВ из углей, является наличие в них трех четко выраженных спектральных максимумов с положением 30 м.д., 130 м.д. и 178 м.д., содержание в них фрагментов СалкО (12% и менее), значительное – C(O)O и CарО – (20% и более), ответственных по полученным выше результатам, за их рост-стимулирующую активность (РА).
Что касается других фрагментов в препаратах, они варьируются весьма широко, по-видимому, в зависимости от степени их зрелости и характера исходного сырья. Анализ фрагментного состава ГВ позволяет выявить ряд препаратов (3, 8, 15, табл. 12), которые либо не соответствуют заявленному источнику происхождения, либо претерпели дополнительную химическую обработку, или компаундирование.
Таблица 12. Фрагментный состав гуминовых веществ (%), переосажденных из коммерческих гуминовых препаратов по данным спектроскопии ЯМР 13С и их относительная рост-стимулирующая активность (РА)
[2]
| № | Наименование | C=O | C(O)O | CарO | CарC,H | CалкO | Cалк | РА |
| ГК Химреактив | 0.4 | 6.6 | 7.4 | 38.3 | 25.8 | 21.4 | 0.65 | |
| ГК Плодородие (торф+сапропель) | 1.8 | 12.0 | 9.0 | 51.4 | 3.8 | 21.7 | 0.86 | |
| Оксигумат (бурый уголь) | 3.7 | 6.3 | 9.9 | 54.6 | 13.2 | 12.3 | 0.82 | |
| Лигногумат (лигнин) | 1.4 | 6.3 | 21.5 | 38.4 | 21.9 | 8.4 | 1.66 | |
| Гумистар (вермикомпост) | 1.2 | 8.3 | 5.6 | 32.9 | 17.3 | 33.9 | 0.55 | |
| Гумат-80 Урожай (бурый уголь) | 2.4 | 8.5 | 11.8 | 51.6 | 2.0 | 23.9 | 1.00 | |
| Pow-Humus (леонардит) | 1.4 | 8.9 | 8.4 | 49.6 | 4.2 | 27.4 | 0.76 | |
| Энергум (бурый уголь) | 0.8 | 9.2 | 8.8 | 50.2 | 10.8 | 20.1 | 0.80 | |
| Гель (торф) | 1.1 | 9.7 | 5.5 | 31.9 | 21.3 | 30.5 | 0.57 | |
| IHSS St (леонардит) | 4.1 | 9.9 | 10.0 | 48.5 | 5.7 | 21.9 | 0.89 | |
| Энерген (бурый уголь) | 2.0 | 10.0 | 8.8 | 55.7 | 1.7 | 18.4 | 0.81 | |
| Агрокор | 10 | 11 | 2 | 11 | 12 | 54 | 0.34 | |
| Теравита (леонардит) | 3.0 | 7.7 | 7.7 | 60.7 | 2.4 | 18.1 | 0.69 | |
| Лигногумат-2 (лигнин) | 1.7 | 0.5 | 11.0 | 49.6 | 27.6 | 9.7 | 0.80 | |
| Энерген-2 (бурый уголь) | 3.1 | 8.7 | 9.0 | 43.2 | 14.4 | 21.2 | 0.80 | |
| Орггум (торф) | 13.8 | 7.7 | 10.8 | 29.0 | 13.8 | 21.5 | 0.91 |
Глава IV. Количественные аспекты спектроскопии ЯМР 2Н в анализе изотопного состава органических веществ и водно-органических растворов
Любое органическое вещество за счёт вхождения в его состав минорных изотопов водорода, углерода, кислорода, азота является сложной смесью изотопомеров. Например, этиловый спирт, являясь индивидуальным соединением, можно рассматривать как многокомпонентную систему, так как фрагменты молекулы содержат минорные изотопы и представляют собой смесь из изотопомеров: метильная группа (СН3, CH2D, CHD2, CD3), метиленовая группа (СН2, CHD, CD2), гидроксильная группа (ОН, ОD).
Разработана методика количественного определения содержания дейтерия в водородсодержащих структурных фрагментах молекул жидких или растворенных индивидуальных веществ и их смесей методом спектроскопии ЯМР 2Н в сильных магнитных полях (> 6Т) без использования стабилизации резонансного условия (отношение частота/поле).
Область применения методики – измерение природного фракционирования водорода в органических молекулах, изучение механизмов химических реакций, доказательство или опровержение аутентичности веществ по дифференциальному и интегральному содержанию в них изотопов водорода, мониторинг технологических процессов переработки природного сырья, определение сырьевого и географического происхождения индивидуальных веществ. Методика аттестована Госстандартом РФ (№ 105-05-99), код МВИ ФР.1.31.1999.00073 и переаттестована ФГУП «УНИИМ» № 224.01.17.011/2006.
Содержание изотопа 2Н, как маркер сырьевой природы этанола. Осуществлён изотопный анализ этанолов различного генезиса (спектрометр ЯМР VXR 500S с рабочей частотой для ядер 2Н 76.7 МГц и термостатированным датчиком для ампул диаметром 10 мм).
Установлено, что в процессе перегонки виноматериалов происходит значительное изменение изотопного состава водорода этильного фрагмента отогнанного спирта. Диапазон вариаций дейтерия во фракциях достигает 12ррm для СН3 и 6 ррm для СН2 групп, что в несколько раз превышает погрешность измерений, т.е. неполная дистилляция этанола может вносить основную ошибку в результаты анализа. Реализована возможность регистрации спектров ЯМР 2Н водно-спиртовых смесей (> 30% об. этанола) без предварительной дистилляции этанола в отсутствии стабилизации резонансного условия частота / поле.
Проведен анализ представительной серии (более 200 образцов) пищевых, синтетических и гидролизных этанолов (ПЭ, СЭ и ГЭ) и установлен диапазон вариаций природного содержания дейтерия в метильной и метиленовой группах (рис. 10, 11). С учетом граничных значений областей зерновых ПЭ и СЭ возможно решение обратной задачи – установление сырьевого происхождения этанола по изотопным параметрам образца:
- Этанол, изотопный состав которого соответствует «нейтральной зоне» (110 120 ppm для СН3 и 135 140 ppm для СН2 групп), является продуктом компаундирования ПЭ и СЭ. Зная фрагментное распределение 2Н для одного из компонентов, можно оценить соотношение ПЭ и СЭ в смеси.
- Этанол с минимальными значениями (D/Н) по обеим, или хотя бы по одной из координат (<130 ppm для СН2 и/или <105 ppm для СН3 группы) практически всегда является ПЭ, с максимальными (>145 ppm для СН2 и/или >125 ppm для СН3 группы) – СЭ.
Этанол с изотопными параметрами выделенных областей соответствует ПЭ (СЭ), но не исключает примесь СЭ (ПЭ) в количестве, определяемом изотопным составом последней.
| Рис. 10. Фрагментное распределение дейтерия в ПЭ, СЭ, ГЭ | Рис. 11. Фрагментное распределе-ние 2Н в ПЭ из зерна и СЭ |
Показано, что в силу особенностей изотопного состава ГЭ проблему его идентификации целесообразно решать как независимую, используя совокупность методов ЯМР 1Н, 2Н, 13С, масс-спектрометрию изотопных отношений и ХМС (рис. 12).
Рис. 12. Экспресс-алгоритм анализа подлинности вин
На основе сочетания количественных методов спектроскопии ЯМР для компонентного и изотопного анализа разработан эффективный алгоритм идентификации водно-органических растворов, возможности которого проиллюстрированы на примере натуральных виноградных вин (рис. 12).
ЗАКЛЮЧЕНИЕ
Разработаны способы оценки влияния различных факторов на химические, биохимические и технологические процессы переработки многокомпонентных систем природного происхождения, идентификации и аутентификации целевых продуктов на основе информации, полученной методом количественной спектроскопии ЯМР. Определены концептуальные направления использования структурно-спектральной информации при решении теоретических и практических задач химии лигнина, угля, многокомпонентных изотопомерных смесей различного происхождения, гуминовых веществ.
Выводы
1. Создан оригинальный алгоритм исследования химической структуры природных стереонерегулярных полимеров – лигнинов, на основе совокупности данных количественной спектроскопии ЯМР 1Н и 13С и 2D ЯМР спектроскопии. Показано, что фрагментный состав адекватно описывает химическое строение макромолекул лигнинов.
2. Разработанный метод исследования лигнинов предложено использовать для контроля и аттестации существующих и вновь разрабатываемых методов функционального анализа природных полимеров, использующих предварительную химическую модификацию препаратов. Продемонстрированы возможности экспертной оценки различных методов анализа. Показано, что практически все химические реакции, используемые в традиционном функциональном анализе макромолекул лигнинов, не приводят к 100% конверсии функциональных групп, при этом вызывают существенную трансформацию структуры макромолекулы из-за непредсказуемых побочных процессов, что в совокупности приводит к заниженным значениям концентрации определяемых функциональных групп.
3. Предложен метод идентификации и определения содержания макромолекул лигнинов в сложных смесях техногенного происхождения на основе количественной спектроскопии ЯМР 13С.
4. Методом количественной спектроскопии ЯМР 1Н и 13С осуществлен мониторинг процессов каталитического гидрирования тяжелых угольных смол с высокой концентрацией гетероатомных органических соединений (угли Канско-Ачинского и Черемховского бассейнов). Разработана методика определения содержания фенолов в угольных смолах, их смесях и гидрогенизатах. На базе фрагментного и компонентного анализа смол и их гидрогенизатов найдены оптимальные условия каталитического гидрирования угольных смол с целью получения продуктов определенного состава.
5. Показано, что фрагментный состав продуктов гидрогенизации смол позволяет детально охарактеризовать изменения в строении и составе, происходящие в химических технологических превращениях и выявить их доминирующие типы. Основные химические процессы, состоят в гидрировании ароматических циклов и деструкции алкильных заместителей. Параметры спектров ЯМР 1Н и 13С, отражающие изменения структуры на молекулярном уровне, наиболее полно характеризуют механизм процессов гидрогенизации. Привлечение метода главных компонент факторного анализа показало, что доминирующие процессы могут быть идентифицированы на основе данных только спектров ЯМР 1Н, что значительно повышает экспрессность анализа продуктов гидрогенизации.
6. Оптимизированы условия регистрации спектров ЯМР 13С гуминовых кислот, выявлена взаимосвязь параметров их фрагментного состава с их химическим строением и свойствами. Анализ спектров более 40 различных гуминовых кислот показал, что количественная спектроскопия ЯМР 13С – наиболее корректный метод идентификации их сырьевого происхождения, первичного прогнозирования рост-стимулирующей активности, аутентификации гуминовых кислот промышленных препаратов,.
7. Проведена оценка возможностей количественной спектроскопии ЯМР 2Н по идентификации и аутентификации некоторых целевых продуктов. Разработана и аттестована оригинальная методика количественного определения естественного содержания дейтерия во фрагментах молекул органических веществ. Её применение позволяет проводить идентификацию многокомпонентных изотопомерных смесей на примере этанолов из различного сырья и технологий получения в компаундах широкого диапазона концентраций. С помощью метода спектроскопии ЯМР на ядрах 2Н, 17О, 31Р найдены качественные и количественные критерии дифференциации пищевых и синтетических этанолов, алгоритм идентификации подлинности и географического происхождения вин с использованием компонентного и изотопного анализов.
Основное содержание диссертации изложено в публикациях:
- Рохин А.В., Каницкая Л.В., Калихман И.Д., Кушнарев Д.Ф., Бабкин В.А., Калабин Г.А. Дифференцированное определение содержания спиртовых, фенольных и кислотных гидроксильных групп в лигнинах методом спектроскопии ЯМР 1Н. // Химия древесины. 1992. № 1. C. 76-79.
- Рохин А.В., Каницкая Л.В., Заказов А.Н., Гоготов А.Ф., Кушнарев Д.Ф., Бабкин В.А., Калабин Г.А. Количественная спектроскопия ЯМР 1Н и 13С лигнинов водно-этанольной варки древесины осины // Химия природных соединений. 1993. № 2. С. 277-280.
- Каницкая Л.В., Заказов А.Н., Россинский О.А., Рохин А.В., Бабкин В.А. Исследование структурных изменений диоксанлигнина ели при действии пероксида водорода и боргидрида натрия // Лесной журнал. 1993. № 2-3. С. 147-154.
- Рохин А.В., Каницкая Л.В., Кушнарев Д.Ф., Калабин Г.А., Абдуазимов Х.А., Смирнова Л.С., Пулатов Б.Х. Количественная спектроскопия ЯМР 1Н и 13С диоксанлигнинов хлопчатника (Gossipium) // Химия природных соединений. 1994. № 6. C. 798-808.
- Шевченко Г.Г., Рохина Е.Ф., Белик Н.А., Рохин А.В., Латышев В.П. Применение метода ЯМР 1Н для изучения состава фенолов исходных и гидрированных смол / "Природные ресурсы, экология и социальная среда Прибайкалья" // сб. научных трудов ИГУ, программа "Университеты России", Иркутск: ИГУ, 1995. – С.90-95.
- Рохина Е.Ф., Шевченко Г.Г., Белик Н.А., Рохин А.В., Латышев В.П. ЯМР спектроскопия угольных смол и продуктов их превращений / "Природные ресурсы, экология и социальная среда Прибайкалья" // сб. научных трудов ИГУ, программа "Университеты России", Иркутск: ИГУ, 1995. – С.85-89
- Rokhin A.V., Kanitskaya L.V., Kushnarev D.F.,Gogotov A.F.,Babkin., V.A.,Kalabin G.A.Study of lignin structure of water-ethanol pulping of aspen wood // Int. Conf. Ecologically pure technological processes enwironment protection problems. Russia, june 18-22, 1996, Irkutsk. – 1996. – P.24-25.
- Рохин А.В. Комплексная методика анализа структурных групп препаратов лигнина различного происхождения методом ядерного магнитного резонанса на ядрах водорода-1 и углерода-13 // Сборник научных докладов областного конкурса на лучшую научную работу по естественным, техническим и гуманитарным наукам. Иркутск: ИГУ. 1996. 120с.
- Rokhin A.V., Kanitskaya L.V., Kushnarev D.F., Gogotov A.F., Babkin V. A. On chemical structure of lignin preparation of alkaline methods of delignification of aspen wood // Int. Conf. Ecologically pure technological processes enwironment protection problems, Russia, june 18-22, 1996. –Irkutsk. – 1996. – P. 25-27.
- Каницкая Л.В.., Рохин А.В., Гоготов А.Ф., Кушнарёв Д.Ф., Калабин Г.А Количественная спектроскопия ядерного магнитного резонанса 1Н и 13С препаратов лигнина щелочных способов делигнификации // Химия в интересах устойчивого развития. – 1996. – Т. 4, № 4-5. – С. 281-288.
- Каницкая Л.В., Рохин А.В., Кушнарев Д.Ф., Калабин Г.А. Исследование структуры лигнинов методом спектроскопии ЯМР 1Н и ЯМР 13С // Высокомолекулярные соедин. – 1997. – Т.39, № 6. – С.965-971.
- Каницкая Л.В., Рохин А.В., Кушнарев Д.Ф., Калабин Г.А. Химическая структура макромолекулы диоксанлигнина пшеницы: исследование методом спектроскопии ЯМР на ядрах 1Н и 13С // Высокомолекулярные соедин. Сер.А – 1998. Т.40, № 5. – С. 800-805.
- Калабин Г.А., Рохин А.В., Кушнарев Д.Ф. Идентификация сырья производства этилового спирта методом спектроскопии ЯМР 2Н // Материалы конференции "Идентификация качества и безопасность алкогольной продукции", Пущино, Моск. область, 1-4 марта 1999г. – 1999. – С.62.
- Калабин Г.А., Рохин А.В., Кушнарев Д.Ф. Анализ и оптимизация состава алкогольных напитков методами количественной спектроскопии ЯМР на естественном содержании изотопов 1Н, 2Н, 13С и 17О // Материалы конференции "Идентификация качества и безопасность алкогольной продукции", Пущино, Моск. область, 1-4 марта 1999. – 1999. – С.63.
- Каницкая Л.В., Рохин А.В., Кушнарев Д.Ф., Абдуазимов Х.А., Калабин Г.А. Химическая структурная неоднородность диоксанлигнина хлопчатника // Высокомолекулярные соедин. Сер.А – 1999. – Т. 41,
№ 3. – С. 503-510. - Каницкая Л.В., Медведева С.А., Рохин А.В., Волчатова И.В., Гаврилова Г.А., Турчанинов В.К. Дегидрогенизационная полимеризация о-метокси-фенола при ферментативном катализе: исследование химической структуры полимеров // Высокомолекулярные соедин. Сер.А – 1999. – Т. 41, № 8. – С.1237-1245.
- Медведева С.А., Каницкая Л.В., Рохин А.В., Кушнарев Д.Ф., Калабин Г.А. К вопросу о наличии лигнина в низкоорганизованных растениях: сфагновом мхе, хвоще топяном, папоротнике орляке // Химия в интересах устойчивого развития. – 1999. – Т. 7. – С. 331-337.
- Каницкая Л.В., Рохин А.В., Чеченина Т.Е., Кушнарёв Д.Ф. Количественная спектроскопия ЯМР 1H и 13C лигнинов // Материалы Всеросс. конф. "Химический анализ веществ и материалов", Москва, 16-21 апреля, 2000г. – 2000. – С.23-24.
- Калабин Г.А., Каницкая Л.В., Рохин А.В., Кушнарёв Д.Ф. ЯМР в химии лигнина // Материалы III Всеросс. конф. "Новые достижения ЯМР в структурных исследованиях", Казань, 4-7 апреля, 2000. – 2000. – С.28.
- Каницкая Л.В., Рохин А.В., Костыро Я. А., Кушнарёв Д.Ф. Химическое строение диоксанлигнинов травянистых растений. Количественная спектроскопия ЯМР 1H и 13C // Материалы III Всеросс. конф. "Новые достижения ЯМР в структурных исследованиях", Казань, 4-7 апреля, 2000. – 2000. – С.89.
- Каницкая Л.В., Рохин А.В., Кушнарёв Д.Ф, Калабин Г.А., Абдуазимов Х.А. Неоднородность химического строения макромолекул лигнина различных растительных тканей. Исследование методом спектроскопии ЯМР на ядрах 1Н и 13С // Высокомолекулярные соединения. Сер. А. – 2000. – Т. 42, № 6. – С.1042-1047.
- Kalabin G.A., Belovezhets K.I., Rokhin A.V., Kozlov J.P., Rykov Y.P., Kushnarev D.F., Kulagina N.V., Apostolova I.Y. Some aspects of applying quantitative spectroscopy NMR 2Н for Russian customs laboratory issues // Abstracts of EuroConference "Modern analytical methods for food and beverage authentication, Lednice 29-31.08.02, Czech rebublic. – 2002. – P. 24.
- Рохин А.В., Сапожников Ю.М., Кулагина Н.В., Кушнарёв Д.Ф., Калабин Г.А. Обзор. Определение содержания минорных изотопов методом спектроскопии ЯМР в молекулах спиртосодержащих жидкостей методом спектроскопии ЯМР // Сборник трудов Госстандарта России. – М.: Госстандарт РФ, 2001. – С.58-91.
- Кушнарев Д.Ф., Рохин А.В., Пройдаков А.Г., Яковлева Ю.Н., Островская Р.М., Новикова Л.Н., Калабин Г.А. Предсказание физиологической активности гуминовых кислот на основе фрагментного состава из спектров ЯМР 13С / Сб. трудов РУДН "Актуальные проблемы экологии и природопользования. – Вып. 2. – 2001. – С.16-21.
- Рохин А.В., Кушнарев Д.Ф., Кулагина Н.В., Трунов С.В., Сапожников Ю.М., Калабин Г.А. Определение содержания минорных изотопов методом спектроскопии ЯМР в молекулах спиртосодержащих жидкостей // Материалы 1-научно-практической конференции ГТЛ ГТК РФ "Экспертно-исследовательская деятельность в таможенных целях", Москва, апрель 2001. – 2001. – С.33-34.
- Шевченко Г.Г., Рохина Е.Ф., Белик Н.А., Рохин А.В., Латышев В.П. К вопросу о технологии утилизации отходов угольных производств // Сборник "Материалы II научно-практической Международной конференции «Человек-среда-Вселенная»", Иркутск, декабрь-2001. – 2001. – С.122-128.
- Шевченко Г.Г., Рохина Е.Ф., Белик Н.А., Рохин А.В., Латышев В.П. Отработка технологии утилизации отходов угольных производств // Материалы Международной конференции "Технология и экологические аспекты переработки минерального сырья", Иркутск, 2001. – 2001. – С.129-130.
- Шевченко Г.Г., Рохин А.В., Белик Н.А., Рохина Е.Ф., Латышев В.П. Разработка способа переработки угольных смол // Материалы Международной конференции "Технология и экологические аспекты переработки минерального сырья", Иркутск, 2001. – 2001. – С.131-132.
- Рохин А.В., Хилько Е.Г., Кушнарев Д.Ф., Калабин Г.А. Применение спектроскопии ЯМР 1Н и 13С для таможенного контроля нефтепродуктов различного происхождения // Материалы 1-научно-практической конференции ГТЛ ГТК РФ "Экспертно-исследовательская деятельность в таможенных целях". – Москва, 2001. – С. 34-35.
- Окроян Г.Р., Рохин А.В., Кушнарев Д.Ф. Изучение времени релаксации водных растворов методом спектроскопии ЯМР 17О // Материалы 1-научно-практической конференции ГТЛ ГТК РФ "Экспертно-исследовательская деятельность в таможенных целях". – Москва, 2001. – С. 35-36.
- Калабин Г.А., Дроздовская Е.В., Рохин А.В., Козлов Ю.П., Кушнарёв Д.Ф., Кулагина Н.В. Спектроскопия ЯМР в сертификации пищевой продукции // Материалы 5 Всероссийской научно-практической конференции, 03-07.12.01, Екатеринбург. 2001. С.26-29.
- Калабин Г.А., Рыков Р.С., Дроздовская Е.В., Рохин А.В., Козлов Ю.П., Кушнарёв Д.Ф., Кулагина Н.В. Количественная мультиядерная спектроскопия ЯМР в идентификации сырьевой, региональной и технологической природы технической и пищевой продукции // Материалы 6 международного семинара по магнитному резонансу, 08-11.10.02, Ростов-на-Дону. 2001. С.274-275.
- Калабин Г.А., Беловежец К.И., Рохин А.В., Козлов Ю.П., Кушнарёв Д.Ф., Окроян Г.Р. Разработка прецезионных методик спектроскопии ЯМР 1Н, 2Н и 13С для анализа изотопного, изомерного, фрагментного и компонентного состава органических веществ // Поволжская конференция по аналитической химии: Материалы конференции, Казань, 20-22.11.01. С.10-13.
- Калабин Г.А., Козлов Ю.П., Кулагина Н.В., Рохин А.В., Рыков Р.С. Идентификация и контроль качества продуктов биотехнологических процессов методами спектроскопии ЯМР // Материалы конференции "Химия и химические продукты", Москва. – 2002. – С.166-167.
- Дашицыренова А.Д., Рохин А.В., Кушнарёв Д.Ф., Калабин Г.А., Пройдаков А.Г. Гумусовые кислоты окисленных бурых углей Бурятии: предсказание физиологической активности ни основе фрагментного состава из спектров ЯМР 13С // Актуальные проблемы экологии и природопользования. (Сб. научн. трудов). М.: изд-во РУДН. 2003. С.246-248.
- Алексеева Е.В., Рохин А.В., Кушнарев Д.Ф., Рзаева Л.Э., Калабин Г.А. Спектроскопия ЯМР 17О водных растворов электролитов // Материалы II Международной конференции по новым технологиям и приложениям современных физико-химических методов (ядерный магнитный резонанс, хроматография/масс-спектрометрия. ИК-Фурье спектроскопия и их комбинации) для изучения окружающей среды, 15-21 сентября 2003г., Ростов-на-Дону. – 2003. – С.107.
- Калабин Г.А., Рохин А.В., Апрелкова Н.Ф., Пройдаков А.Г., Кушнарёв Д.Ф. Дашицыренова А.Д. Количественная спектроскопия ЯМР 13С гуминовых веществ бурых углей различного происхождения. // Материалы II Международной конференции по новым технологиям и приложениям современных физико-химических методов (ядерный магнитный резонанс, хроматография/масс-спектрометрия. ИК-Фурье спектроскопия и их комбинации) для изучения окружающей среды, 15-21 сентября 2003г., Ростов-на-Дону. – 2003. – С.109-110.
- Калабин Г.А., Апрелкова Н.Ф., Пройдаков А.Г., Рохин А.В., Кушнарев Д.Ф., Дашицыренова А.Д. Механизм природного распределения дейтерия в синтетическом этиловом спирте // Материалы XVII Менделеевского съезда, Казань. – 2003 – С. 86.
- Фёдорова Т.Е., Дудкин Д.В., Першина Л.А., Рохин А.В., Бабкин В.А. Анализ химического состава гуминоподобных веществ лузги подсолнечника, подвергнутой окислительному аммонолизу при механическом воздействии методом количественной спектроскопии ЯМР 1Н и 13С // Химия растительного сырья. – 2003. – № 4. – С.25-29.
- Калабин Г.А., Кулагина Н. В., Рохин А.В., Рыков Р.С., Козлов Ю.П., Кушнарев Д.Ф. Идентификация сырьевой природы этанола методом спектроскопии ЯМР 2Н // Вестник РУДН. Сер. "Экология и безопасность жизнедеятельности" – 2003. – № 7. – С.87-98.
- Дашицыренова А.Д., Куликова Н.А., Калабин Г.А., Кушнарёв Д.Ф., Рохин А.В. Предсказание физиологической активности гуминовых кислот бурых углей юга Сибирской платформы на основе данных ЯМР 17O // Материалы VII Международного семинара по магнитному резонансу (спектроскопия, томография и экология), Ростов-на-Дону. 2004. С. 114-115.
- Кулагина Н.В., Сахабутдинов А.Г., Кушнарев Д.Ф., Рохин А.В., Пройдаков А.Г., Калабин Г.А. Об участии воды в формировании молекулы спирта при биоконверсии глюкозы // Вестник ИрГТУ. – 2004. – № 4. – С.150.
- Танцырев А.П., Каницкая Л.В., Рохин А.В., Левковская Г.Г. Диметилгидразоны моносахаридов // ЖОрХ. – 2004. – Т.40, вып.11. – С.1735-1736.
- Оленников Д.Н., Танхаева Л.М., Николаева Г.Г., Рохин А.В., Кушнарёв Д.Ф. Биологически активные вещества сухого экстракта какалии копьевидной // Химия растительного сырья. – 2004. – № 3. – С.59-62.
- Olennikov D.N., Tankhaeva L.M., Nikolaeva G.G., Nikolaev S.M., Rokhin A.V., Kushnarev D.F. Biologically active compounds from Cacalia hastata leaves. 3. Organic acids // Chemistry of natural compounds. – 2004. – Vol. 40, № 3 – С.289.
- Калабин Г. А., Дашицыренова А.Д., Рохин А.В., Кушнарёв Д.Ф., Пройдаков А.Г. Количественная спектроскопия ЯМР в идентификации гуминовых веществ и прогнозировании их свойств // Материалы IV Всероссийской конференции "Новые достижения ЯМР в структурных исследованиях" с участием зарубежных учёных, 4-7 апреля 2005г., Казань. – 2005. – С.36.
- Kalabin G.A., Rzaeva L.E., Erofeeva V.S., Rokhin A.V., Kuschnarev D.F. 17O NMR investigation of water clusters in a water. Elerctrolyte system // Материалы конференции «PIM-2005», 21-25 сентября 2005г., Румыния. – 2005. – С.107-114.
- Климова Н.С., Рохин А.В., Калабин Г.А. Возможности спектроскопии ЯМР в идентификации растительных масел с повышенным лечебно-диагностическими свойствами // Вестник РУДН. – 2005 г. – С.360-365.
- Монхжаргал Ш., Новикова Л.Н., Медведева С.А., Кушнарёв Д.Ф., Дашицыренова А.Д., Калабин Г.А Состав гуминовых веществ, выделенных из Монгольского бурого угля // Химия твёрдого топлива. – 2005. – № 4 – С.14-21.
- Монхжаргал Ш., Новикова Л.Н., Медведева С.А., Кушнарёв Д.Ф., Дашицыренова А.Д., Рохин А.В., Калабин Г.А Состав гуминовых веществ, выделенных из бурого угля и окисленного азотной кислотой остатка // Химия твёрдого топлива. – 2005. – № 3 – С.63-70.
- Dashitsyrenova A.D., Kalabin G.A., Kuschnarev D.F., Proydakov A.G., Rokhin A.V. NMR spectroscopy in identification of humic substances and prediction its properties // Studia Universitatis Babes-Bolyai. Phisica.4b. 2005. P.591-594.
- Рохина Е.Ф., Латышев В.П., Рохин А.В., Шевченко Г.Г. Глубокая переработка угольных смол с целью получения сырья для химической промышленности// Труды Международной VIII научно-практ. Конф. "Химия XXI век: новые технологии, новые продукты", 10-14 мая 2005г., Кемерово. – 2005. – С. 313-315.
- Калабин Г.А., Дашицыренова А. Д., Кушнарев Д.Ф., Рохин А.В., Пройдаков А.Г. Количественная спектроскопия ЯМР в идентификации гуминовых веществ и прогнозировании их свойств // Материалы III Всероссийской конференции "Гуминовые вещества в биосфере", 1-3 марта 2005г., Санкт-Петербург. – 2005. – С.62-63.
- Калабин Г.А., Дашицыренова А. Д., Кушнарев Д.Ф., Рохин А.В., Пройдаков А.Г. Количественная спектроскопия ЯМР 13С гуминовых веществ бурых углей различного происхождения // Материалы международного симпозиума «ЯМР в конденсированных средах»– С-Петербург, 11-15 июля 2005г. – С.42.
- Калабин Г.А., Рохин А.В., Кушнарев Д.Ф. Идентификация и предсказание технических характеристик нефтепродуктов методом количественной спектроскопии ЯМР // Материалы Всероссийской конференции "Экспресс-методы количественного анализа: достоинства и недостатки, область применения", 19 апреля 2005г.,Москва. – 2005. – С. 48.
- Рзаева Л.Э., Калабин Г. А., Кушнарёв Д.Ф., Ерофеева В.С., Рохин А.В. Структурные особенности воды в системе «вода-электролит» // Материалы международного симпозиума NMRCM-2005 «ЯМР в конденсированных средах», 11-15 июля 2005г., С-Петербург. – 2005. – С.41.
- Dashitsyrenova A.D., Kalabin G.A., Kuschnarev D.F., Proydakov A.G., Rokhin A.V. NMR spectroscopy in identification of humic substances and prediction its properties// Proceedings of the Fourth Conference "Isotopic and molecular processes", Cluj-Napoca. 2005. P.151.
- Дашицыренова А.Д., Калабин Г.А., Кушнарёв Д.Ф., Пройдаков А.Г., Рохин А.В., Кулагина Н.В., Сахабутдинов А.Г. Влияние гуматов окисленных бурых углей на процесс спиртового брожения // Вестник РУДН. Сер. "Экология и безопасность жизнедеятельности". 2005. №1 (11). С.167-172.
- Дашицыренова А.Д., Пройдаков А.Г., Кушнарёв Д.Ф., Рохин А.В., Калабин Г.А. Окисленные угли Гусиноозерского месторождения – эффективное сырье для производства безбалластных гуматов // Химия твёрдого топлива. – 2006. – № 1. – С.22-28.
- Рохин А.В., Каницкая Л.В., Кушнарёв Д.Ф., Калабин Г.А. Химическая структура макромолекулы лигнина ели по результатам исследования методами количественной спектроскопии ЯМР 1Н, 13С и 2D ЯМР-экспериментов // Научное обозрение. – 2006. – № 1. – С. 97-112.
- Рохина Е.Ф., Латышев В.П., Рохин А.В., Шевченко Г.Г. Перспективы получения одноатомных фенолов деструктивной гидрогенизацией угольных смол // Труды Международной IX научно-практической конференции "Химия XXI век: новые технологии, новые продукты", 16-18 мая 2006г., Кемерово. – 2006. – С. 115-120.
- Рохин А.В., Щетский С.Б. Исследование структуры лигнина методом спектроскопии ЯМР // Материалы студенческой научно-практической конференции, г. Екатеринбург. – 2006. – С. 120.
- Апрелкова Н.Ф., Матвиевская Н.С., Кушнарев Д.Ф., Рохин А.В. Оценка физиологической активности гуминовых веществ методом полярографии и спектроскопии ЯМР // Сб. Международной научной конференции «Химия, химическая технология и биотехнология на рубеже тысячелетий», 11-16 сентября 2006, г. Томск. – 2006. – С. 127-128.
- Шаулина Л.П., Кушнарев Д.Ф., Рохин А.В.Определение фосфора в пищевых продуктах. // Сб. VI Всеросийской конференции по анализу объектов окружающей среды «Экоаналитика» г.Самара, 26-30 сентября, 2006г. –С.56-57.
- Рохин А.В., Рохина Е.Ф., Латышев В.П., Шевченко Г.Г. Исследование фенолов угольных смол методом спектроскопии ЯМР // Труды Международной научно-практической конференции "Перспективы развития химической переработки горючих ископаемых", 10-15 сентября 2006г., Санкт-Петербург. – 2006. – С. 120-125.
- Медведева Е.Н., Федорова Т.Е., Ванина А.С., Рохин А.В., Бабкин В.А. Зависимость строения арабиногалактана из древесины лиственницы сибирской от способа его выделения и очистки// Материалы IV Всероссийской конференции "Химия и технология растительных веществ", Сыктывкар, июнь 2006. – 2006. – С. 268.
- Куприянович Ю.Н., Медведева С.А., Рохин А.В. Синтез и строение полимерных моделей лигнина на основе фенилпропановых структур // Материалы IV Всероссийской конференции "Химия и технология растительных веществ", Сыктывкар, июнь 2006. – 2006. – С.269.
- Рохин А.В., Рохина Е.Ф., Шевченко Г.Г. Перспективы исследование фенолов угольных смол методом спектроскопии ЯМР // Труды Международной научно-практической конференции, 12-15 октября 2006г., Иркутск. – 2006. – С. 50-52.
- Носкова Л.П., Рохин А.В., Сорокин А.П. Получение восков и гуминовых кислот из бурого угля Сергеевского месторождения // Химия твёрдого топлива. – 2007. – № 3. – С. 9-15.
- Рохина Е.Ф., Шевченко Г.Г., Рохин А.В. Химические продукты на основе гидрогенизатов смол термодеструкции углей Сибири // Труды Международной X научно-практической конференции "Химия XXI век: новые технологии, новые продукты", 15-18 мая 2007 г., Кемерово. – 2007. – С. 143-145.
- Рохин А.В., Новикова Л.Н., Каницкая Л.В., Кушнарёв Д.Ф. Количественная спектроскопия ЯМР в анализе сточных вод Байкальского целлюлозно-бумажного комбината // Труды Международной X научно-практической конференции "Химия XXI век: новые технологии, новые продукты", 15-18 мая 2007 г., Кемерово. – 2007. – С. 141-143.
- Рохин А.В., Каницкая Л.В., Кулагина Н.В., Рохина Е.Ф., Кушнарёв Д.Ф. Количественная спектроскопия ЯМР 1Н и 13С в процессах переработки угольных смол // Труды Международной X научно-практической конференции "Химия XXI век: новые технологии, новые продукты", 15-18 мая 2007 г., Кемерово. – 2007. – С. 145-147.
- Семёнова З.В., Кушнарёв Д.Ф., Литвинцева М.А., Рохин А.В. Гуминовые кислоты сапропеля озера Очауль // Химия твёрдого топлива. – 2007. – № 3. – С. 3-8.
[1] Калабин Г.А., Каницкая Л.В., Кушнарев Д.Ф. Количественная спектроскопия ЯМР природного органического сырья и продуктов его переработки. – М.:Химия, 2000. – 408 с.
Автор благодарит О.С. Якименко (факультет почвоведения МГУ им. М.В. Ломоносова) за предоставленные образцы.

