Оптимизация процессов кристаллизации биоматериалов
На правах рукописи
УДК 548.5:532.5
БЕЗБАХ Илья Жанович
ОПТИМИЗАЦИЯ ПРОЦЕССОВ КРИСТАЛЛИЗАЦИИ БИОМАТЕРИАЛОВ
Специальность 01.04.07 – Физика конденсированного состояния
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата физико-математических наук
Москва – 2007
Работа выполнена в государственном образовательном учреждении высшего профессионального образования "Московский государственный технический университет им. Н.Э. Баумана" и в Научно-исследовательском центре "Космическое материаловедение" Института кристаллографии им. А.В. Шубникова Российской академии наук
Научный доктор физико-математических наук
руководитель: Стрелов Владимир Иванович
Официальные доктор технических наук, профессор
оппоненты: Андреев Владимир Викторович
кандидат физико-математических наук
Плотников Федор Алексеевич
Ведущая организация: Филиал ФГУП "Научно-исследовательский
физико-химический институт им. Л.Я. Карпова"
Защита состоится « 31 » октября 2007 г. в 16:00 часов на заседании
диссертационного совета Д 212.141.17 при ГОУ ВПО "Московский
государственный технический университет им. Н.Э. Баумана" по адресу: 248600, г. Калуга, ул. Баженова, д. 2, МГТУ им. Н.Э. Баумана, Калужский филиал.
Ваши отзывы в двух экземплярах, заверенные печатью,
просьба высылать по указанному адресу.
С диссертацией можно ознакомиться в библиотеке
ГОУ ВПО МГТУ им. Н.Э. Баумана, Калужский филиал
(г. Калуга, ул. Баженова, д. 2)
Автореферат разослан « 27 » сентября 2007 г.
Ученый секретарь
диссертационного совета
канд. техн. наук, доцент Лоскутов С.А.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Кристаллизация биоматериалов в настоящее время используется для удовлетворения растущей потребности структурной биологии для определения кристаллографических параметров органических молекул, что в дальнейшем позволяет проводить как синтез новых веществ с требуемыми свойствами, так и решать некоторые фундаментальные вопросы функционирования живых систем в целом. Важнейшим фактором, ограничивающим эти исследования, являются процессы роста биокристаллов, оптимизация условий которых в настоящее время проводится, в основном, эмпирическими методами.
В связи с этим, изучение закономерностей роста биокристаллов и разработка новых методов их получения являются актуальной научной задачей, что подтверждается и ростом числа публикаций в этой области исследований.
Кристаллы белков выращиваются из растворов путем доведения раствора до определенных значений пересыщения. Пересыщение ![]() определяется как отношение текущей концентрации белка к его растворимости
определяется как отношение текущей концентрации белка к его растворимости ![]() . В общем случае пересыщение может достигаться путем изменения концентрации осадителя, белка и нейтральных добавок, pH, температуры и других параметров.
. В общем случае пересыщение может достигаться путем изменения концентрации осадителя, белка и нейтральных добавок, pH, температуры и других параметров.
Как и в случае неорганических соединений, при достижении пересыщения система, содержащая белок, движется к состоянию равновесия, при котором вещество распределяется между раствором и твердой фазой.
Рост кристаллов белков можно разделить на три существенных этапа: зародышеобразование, рост, достижение равновесия и прекращение роста. Кристаллы белков зарождаются при высоком уровне пересыщения, от 3 до 10, растут же при ![]() , а при
, а при ![]() происходит растворение твердой фазы. Кристаллы белков растут очень медленно – их скорость роста на 2–3 порядка меньше, чем у неорганических кристаллов.
происходит растворение твердой фазы. Кристаллы белков растут очень медленно – их скорость роста на 2–3 порядка меньше, чем у неорганических кристаллов.
В настоящее время для получения биокристаллов используются такие методы, как объемная кристаллизация, микродиализ, свободная диффузия через поверхность раздела белка и осадителя, метод диффузии паров. Одним из важных факторов, объединяющих эти процессы, является тепломассоперенос (ТМП), определяющий качество получаемых кристаллов. Изучение особенностей и оптимизация процессов ТМП при кристаллизации белковых молекул позволяет определить лимитирующие условия процессов получения совершенных кристаллов, разработать методы управления процессом кристаллизации. В связи с этим, целью работы являлась оптимизация процесса выращивания в земных и космических условиях высокосовершенных кристаллов белков размером не менее 100 мкм на основе математического моделирования и экспериментального исследования процессов ТМП в растворе белка, а также разработка метода и аппаратуры для температурного управления ростом кристаллов на примере модельного белка лизоцима.
Объекты и методы исследования. Объектом исследований были выбраны кристаллы белка (фермента) лизоцима – широко известного представителя биоматериалов, структура и свойства которого достаточно исследованы, что позволяло проводить сравнительный анализ результатов разработанного метода кристаллизации. В качестве методов исследования использовались математическое моделирование и экспериментальные исследования особенностей кристаллизации биоматериалов (в т.ч. для определения граничных условий), разработка экспериментальной аппаратуры для получения высокосовершенных кристаллов белков, а также методы рентгеноструктурного анализа для изучения совершенства структуры полученных кристаллов.
Задачи исследования:
1. Определить основные факторы, влияющие на процесс кристаллизации белков.
2. Установить закономерности процессов кристаллизации биоматериалов на примере кристаллизации белка лизоцима для земных и космических условий, в зависимости от интенсивности конвективных течений (в т.ч. конвекции Марангони) и внешних энергетических воздействий на раствор белка. Определить условия преобладания диффузионного ТМП.
3. Определить оптимальные условия и разработать метод выращивания высокосовершенных кристаллов белков, пригодных для рентгеноструктурного анализа (размером не менее 100 мкм).
4. Разработать методику и алгоритм (программу) управления процессом зародышеобразования и роста биокристаллов.
Научная новизна. В ходе выполнения диссертационной работы впервые получены следующие результаты:
1. Установлены закономерности роста кристаллов биоматериалов при задании и прецизионном управлении температурой всего раствора белка и в локальной точке капилляра для обеспечения образования единичных центров кристаллизации.
2. Разработана математическая модель управления процессом кристаллизации, позволяющая определить зависимость количества и размеров образующихся кристаллов от величины пересыщения в растворе, величины критического пересыщения раствора и скорости кристаллизации.
3. Разработан алгоритм и оригинальная методика управления температурой как всего объема раствора белка, так и в локальной точке при кристаллизации биоматериалов.
4. На основе теоретических расчетов процессов ТМП в растворах белков разработан метод и экспериментальная установка для получения высокосовершенных кристаллов биоматериалов, в которой осуществляется не только управление температурой с точностью регулирования не хуже ±0,1°C, но и реализована возможность создания пересыщения раствора в заданном месте капилляра за счет точечного подвода или отвода тепла (т.е. путем создания локального градиента температуры).
Практическая значимость работы состоит в разработке метода управляемой кристаллизации биоматериалов, обеспечивающего раздельное управление процессом как на этапе зародышеобразования, так и в процессе роста образовавшихся кристаллов. Этот способ температурного управления процессом кристаллизации биоматериалов является технологичным и эффективным для выращивания высокосовершенных кристаллов, при этом конвекция в растворе практически исключается, а влияние вибраций на процесс кристаллизации минимизируется и, таким образом, обеспечиваются преимущественно диффузионные условия массопереноса белка, т.е. условия стабильности для самоорганизации молекул белка и встраивания их в кристалл.
На защиту выносятся:
1. Результаты математического моделирования процесса взаимной диффузии молекул белка и осадителя для реальных условий кристаллизации модельного белка лизоцима.
2. Результаты исследования влияния диффузионных и конвективных процессов на кристаллизацию белков в земных и космических условиях с учетом термогравитационной и термокапиллярной (Марангони) конвекции.
3. Математическая модель процессов ТМП в растворе белка для управления процессом кристаллизации при создании в растворе локального градиента температуры.
4. Разработанный метод выращивания высокосовершенных кристаллов белков в градиенте температуры в ячейках капиллярного типа.
Апробация работы. Основные результаты, представленные в диссертации, были доложены и обсуждены на следующих конференциях:
1. Всероссийская научно-техническая конференция "Прогрессивные технологии, конструкции и системы в приборо- и машиностроении " (Калуга, 2004 г.).
2. ХIV Международная конференция по росту кристаллов "Fourteenth International Conference on Crystal Growth" (ICCG-14) (Гренобль, Франция, 2004 г.)
3. VI Международная конференция "Рост монокристаллов и тепломассоперенос" (ICSC-2005) (Обнинск, 2005 г.).
4. ХI и ХII Национальные конференции по росту кристаллов (Москва, 2004, 2006 гг.).
5. Российский симпозиум "Космическое материаловедение" (КМ-2007) (Калуга, 2007 г.).
Результаты работы использованы в НИЦ "Космическое материаловедение" ИК РАН (г. Калуга) для экспериментальной кристаллизации модельного белка лизоцима с высоким совершенством структуры при прецизионном управлении градиентом температуры в ячейках капиллярного типа.
Публикации. По теме диссертации опубликовано 12 печатных работ.
Объем работы. Диссертационная работа включает шесть глав, выводы, список литературы и три приложения. Она изложена на 126 страницах текста, содержит 23 рисунка, 2 таблицы, 71 библиографических названий.
Благодарности. Автор выражает искреннюю благодарность доктору технических наук, профессору В.Г. Косушкину (КФ МГТУ им. Н.Э. Баумана, г. Калуга) за неоценимую поддержку при подготовке диссертации, ценные советы и замечания; также благодарит коллектив Лаборатории белковой кристаллографии и лично И.П. Куранову (ИК РАН, г. Москва) за предоставление кристаллизационных растворов и проведение рентгеноструктурных исследований.
СОДЕРЖАНИЕ РАБОТЫ
Во введении обосновывается актуальность задачи, указываются основные цели исследования и положения, выдвигаемые на защиту.
Первая глава посвящена анализу литературных данных по теме работы. В ней иллюстрируются особенности структуры биоматериалов, указывается проблема сложности кристаллизации, приводится обзор применяемых методов выращивания биокристаллов в наземных и космических условиях. На примере изучения особенностей оборудования, применявшегося для выращивания биокристаллов в космосе, иллюстрируется низкая стабильность тепловых условий и невозможность динамического управления процессом кристаллизации в большинстве из описываемой кристаллизационной аппаратуры. Анализируются существующие методы математического моделирования процессов роста биокристаллов, указываются особенности различных подходов к моделированию: моделирование диффузионного массопереноса в кристаллизационных растворах и средах с поверхностью раздела газ-жидкость, моделирование диффузионно-конвективного тепломассопереноса, моделирование зародышеобразования, моделирование кинетики роста биокристаллов, моделирование температурно-зависимых процессов кристаллизации биоматериалов. Обращается внимание на отсутствие общепринятой модели, описывающей рост биокристаллов. На основе анализа литературных данных формулируются задачи исследования.
Во второй главе диссертации проводится исследование процесса взаимной диффузии для молекул белка и осадителя в условиях реальных экспериментов по выращиванию кристаллов белков на примере модельного протеина лизоцима. Моделировались изменения во времени концентраций соли, белка и пересыщения, результаты сравнивались с данными практических экспериментов, выполненных по двум методикам: 1) диализа – камеры с растворами соли и белка разделены мембраной, проницаемой для молекул соли и непроницаемой для молекул белка; 2) свободной диффузии – мембрана между камерами с растворами соли и белка отсутствует. Нестационарный перенос массы, количества движения и плотности в растворе описывался системой уравнений Навье-Стокса в безразмерной форме и приближении Буссинеска при постоянной температуре.
Приводятся результаты одномерного расчета динамики распределения пересыщения раствора белка в кристаллизационной камере, демонстрирующие хорошее согласие полученных результатов с результатами практических экспериментов. Максимальное различие в количественных значениях относительных пересыщений составляет ~4%.
Отмечается, что описанная модель позволяет в первом приближении решать основные задачи моделирования процесса диффузионного массопереноса при росте биокристаллов в земных и космических условиях. Однако исследовать особенности процессов тепло- и массопереноса для кристаллизационных растворов в земных и космических условиях требуется с учетом влияния на них конвективных и вибрационных воздействий.
Третья глава диссертации посвящена исследованию влияния конвективных процессов на процесс кристаллизации для случая нестационарного режима ТМП. Решается задача определения характера (структуры и скоростей) конвективных потоков в зависимости от интенсивностей термогравитационной и термокапиллярной (Марангони) конвекций при выращивании кристаллов биоматериалов в земных и космических условиях на примере модельного белка лизоцима.
Учитывалось, что конвекция Марангони является отрицательным фактором при кристаллизации методом диффузии паров, поскольку в этом методе присутствует свободная поверхность (жидкость-газ). Также и в методе жидкостной диффузии возможно присутствие открытой поверхности раствора.
Одним из основных факторов, влияющих на процесс кристаллизации, является стабильность поддержания температуры кристаллизационного процесса, которая на практике, как правило, не превышает ±1°C.
Для описания процессов, происходящих в растворах при выращивании кристаллов биоматериалов, использовалась математическая модель на основе системы уравнений Навье-Стокса в приближении Буссинеска. Расчетная область имела цилиндрическую форму с осью симметрии на левой ее границе. Расчет проводился для экспериментально используемой концентрации белка лизоцима в водном растворе – 50 мг/мл. Перепад температур задавался на верхней границе расчетной области.
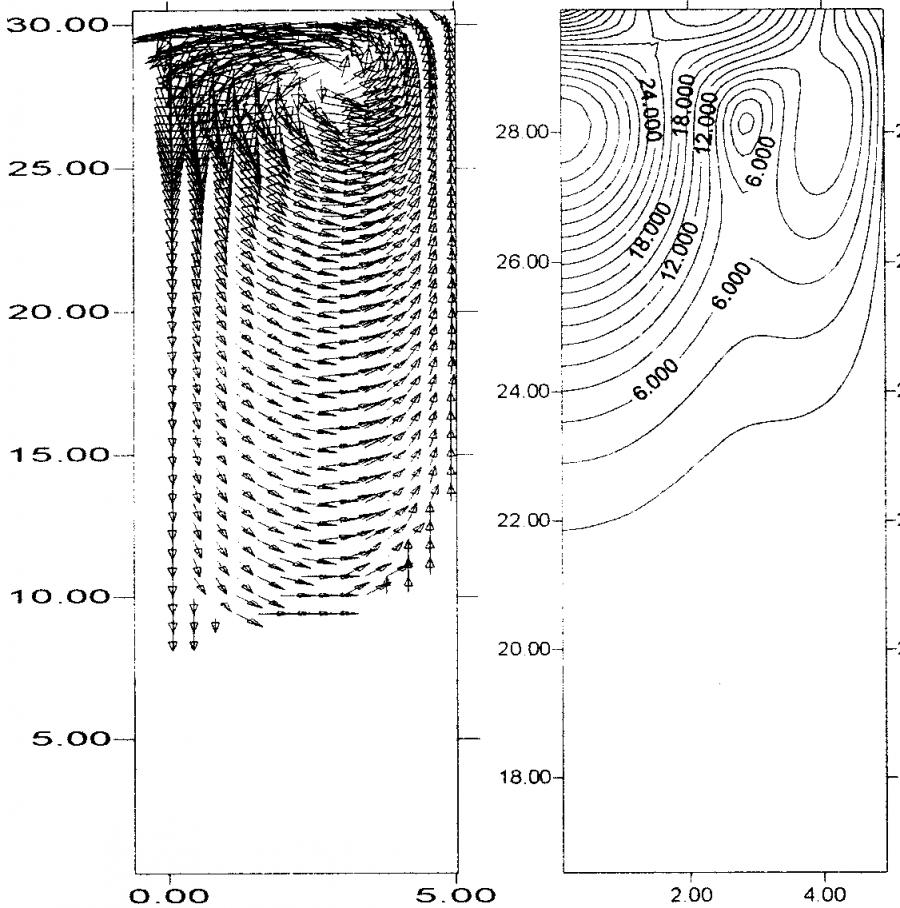
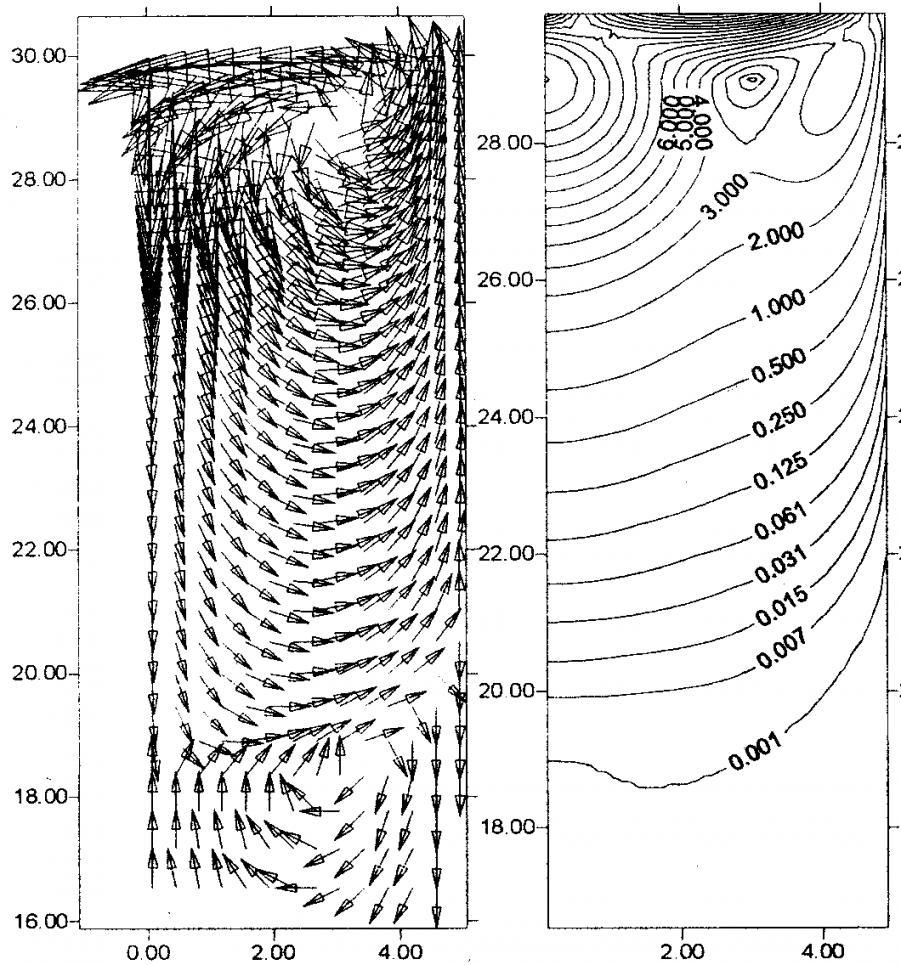
Проведенные расчеты показали, что при отсутствии конвекции Марангони в земных условиях реализуется режим термогравитационной конвекции, конкурирующей с диффузионным массопереносом (рис. 1). При этом конвективные потоки развиваются до половины кристаллизационного объема по высоте. Скорость конвективных потоков в верхней части составляет
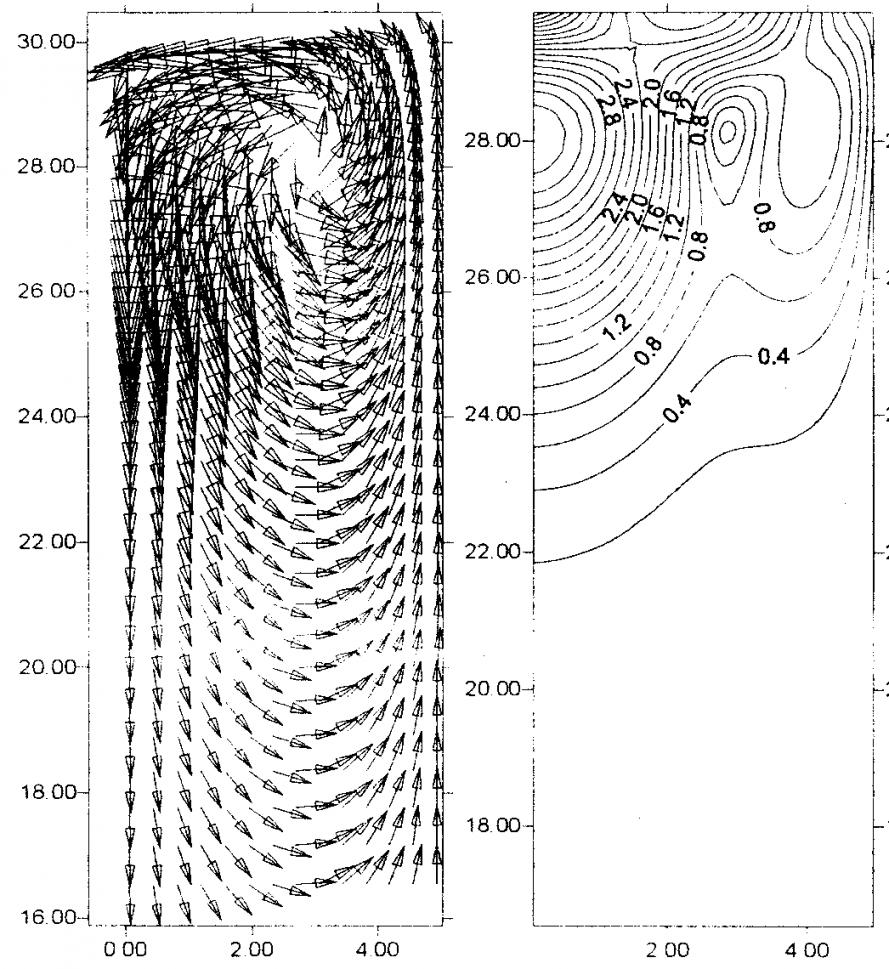
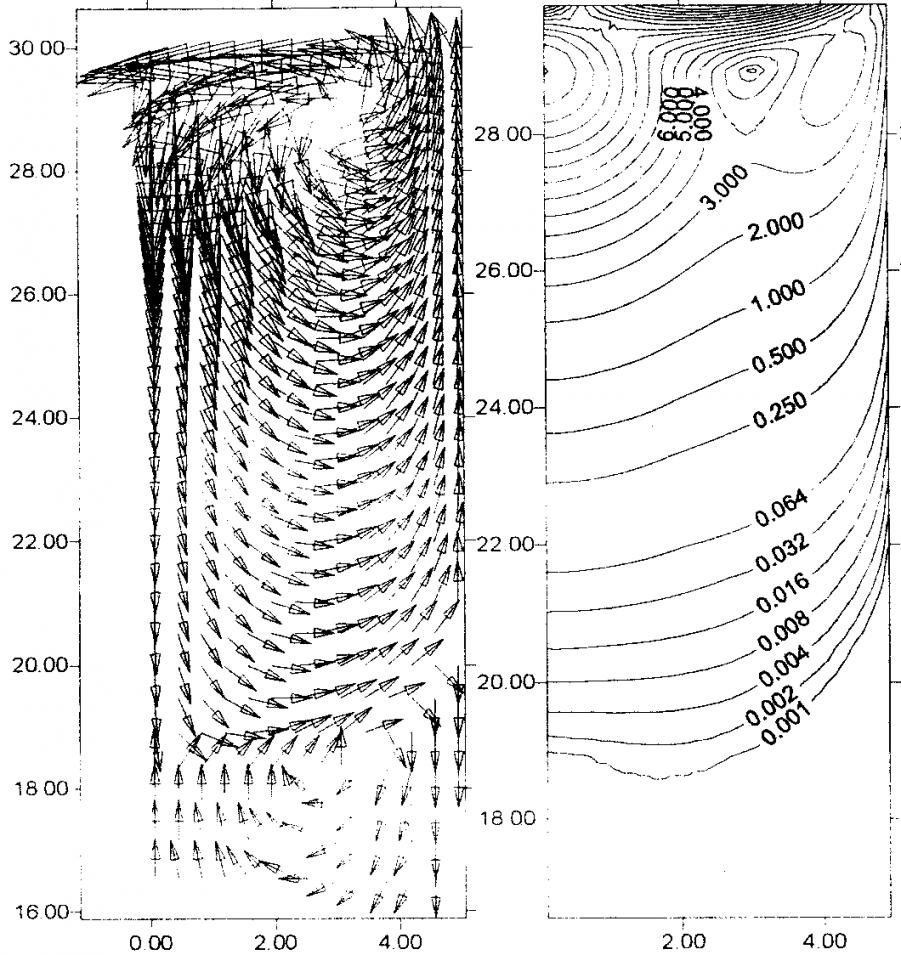
~10–5 мм/с. Эти расчеты подтверждают общепринятое представление о доминировании конвекционного переноса над диффузионным при единичной гравитации. В космических же условиях, как показывают расчеты, термогравитационная конвекция значительно ослабляется – скорость конвективных потоков уменьшается до ~10–9 мм/с (рис. 2). Диффузионный массоперенос в таких условиях является преобладающим.
(а) (б) (а) (б)
I. Mn = 0; ![]() , мм/с II. Mn 0;
, мм/с II. Mn 0;![]() , мм/с
, мм/с
Рис. 1. Структура (а) и изолинии (б) скорости ![]() конвективных потоков в растворе белка при наличии (II) и отсутствии (I) конвекции Марангони в земных условиях, T = 1°C
конвективных потоков в растворе белка при наличии (II) и отсутствии (I) конвекции Марангони в земных условиях, T = 1°C
(а) (б) (а) (б)
I. Mn = 0; ![]() , мм/с II. Mn 0;
, мм/с II. Mn 0; ![]() , мм/с
, мм/с
Рис. 2. Структура (а) и изолинии (б) скорости ![]() конвективных потоков в растворе белка при наличии (II) и отсутствии (I) конвекции Марангони в космических условиях, T = 1°C
конвективных потоков в растворе белка при наличии (II) и отсутствии (I) конвекции Марангони в космических условиях, T = 1°C
Совсем другая картина наблюдается при наличии конвекции Марангони. В этом случае даже при небольшом перепаде температур на открытой поверхности раствора существенным образом меняются структура и интенсивность конвективных течений: для значения T = 1°C скорость конвективных потоков существенно возрастает и составляет ~1 мм/с как для земных, так и для космических условий, однако снижаясь до ~10–1 мм/с лишь при понижении перепада температуры до T = 0,1°C. В этих случаях вблизи свободной поверхности раствора наблюдается преобладание конвективного массопереноса.
Для широко применяемого метода лежачей капли проведенные расчеты показали, что при наличии перепада температур (который всегда возможен в этом методе, что вызывает конвекцию Марангони) как для земных, так и для космических условий реализуется режим доминирования конвекции Марангони. Конвективные потоки развиваются по высоте всей капли, придавая кристаллизационному раствору вращательное движение и приводя тем самым к нарушению диффузионного режима массопереноса. Для обычных значений T = 1°C их скорость имеет порядок ~1 мм/с и не зависит от размера капли. При понижении перепада температуры до T = 0,1°C скорость снижается до ~10–1 мм/с, т.е. имеет пропорциональную зависимость от градиента температур, как и для случая объемного раствора. Проведенные расчеты показывают, что для метода лежачей капли конвективный массоперенос в объеме раствора всегда будет преобладать над диффузионным.
Проведенные теоретические расчеты показали существенное влияние нестабильностей температуры и возникающей конвекции Марангони на процессы ТМП при выращивании биоматериалов как в земных, так и в космических условиях. При этом показано, что причиной их возникновения является наличие температурного градиента на свободной поверхности раствора. Полученные результаты доказывают необходимость достижения высокой стабильности тепловых условий при выращивании кристаллов биоматериалов.
Четвертая глава диссертации посвящена исследованиям влияния вибраций на процесс кристаллизации белков, так как энергетические воздействия существенно влияют на стабильность процесса кристаллизации. При этом исследования влияния вибрационных воздействий на процесс кристаллизации биоматериалов основаны на предварительных расчетно-экспериментальных исследованиях влияния вибрационных воздействий на рост неорганических кристаллов. Установлено, что при выращивании кристаллов полупроводников (на примере Ge, легированного Ga) поступательные колебания, осуществляемые вдоль градиента температуры (по нормали к фронту кристаллизации), в широком диапазоне частот (0,5 200 Гц) и амплитуд микроускорений (до 2·10–1 g0) не оказывают влияния на процессы тепломассопереноса в расплаве и, соответственно, на однородность распределения легирующей примеси в кристалле, что согласуется с проведенными теоретическими расчётами. Однако к существенным нарушениям в распределении примеси приводят торсионные колебания (осуществляемые вокруг оси выращиваемого кристалла) при наличии свободной поверхности расплава.
При открытой поверхности расплава (присутствие конвекции Марангони) к образованию в кристаллах микронеоднородности (полосчатости) приводят в области частот (0,5 200 Гц) колебания с уровнем амплитуд
> 10–2g0. При амплитудах < 5·10–3g0 в выращенных кристаллах полосы роста отсутствуют. Очевидно, что возникновение полос роста связано с тем, что при достижении критического уровня вибраций в непосредственной близи от фронта кристаллизации возникают сдвиговые смещения расплава, которые изменяют стационарный характер конвективных течений.
Влияние вибраций на процесс кристаллизации биоматериалов исследован для двух случаев вибрационных воздействий, характерных для условий роста белков в космосе на Международной космической станции (МКС) (g/g0 > 10–6): вибрационные возмущения, перпендикулярные градиентам концентрации белка и соли, и параллельные к градиентам концентрации.
Расчеты для земных условий показали, что если эксперимент проводить в гелевой среде, то вибрации не оказывают влияния на характер массопереноса в растворе, и процесс идет в режиме диффузионного массопереноса.
В условиях же микрогравитации действуют периодические, высокочастотные возмущения (10–6 < g/g0 < 10–2; 0,1 – 300 Гц по данным цитируемой работы), практически определенные при реализации экспериментов по кристаллизации модельного белка лизоцима на МКС.
Расчеты для первого случая показали, что при кристаллизации из-за образования градиентов концентрации соли и белка в белковой камере при вибрационных возмущениях, перпендикулярных градиентам концентрации, возникают конвекционные участки. Для второго случая установлено, что при вибрационных возмущениях, параллельных градиентам концентрации, возникновение таких участков строго ограничено зонами, в которых происходит зародышеобразование или осаждение образовавшихся кристаллов. Область, подверженная конвекции при наличии таких вибрационных возмущений, перемещается с фронтом зародышеобразования, тогда как в оставшейся части белковой камеры конвекции нет, поэтому в ней следует ожидать улучшения качества кристаллов.
В обоих случаях (при росте неорганических и органических кристаллов) установлено существенное влияние вибрационных воздействий на процессы массопереноса и, соответственно, совершенство получаемых кристаллов в определенном диапазоне частот и амплитуд микроускорений. Однако при этом влияние вибрационных воздействий на процесс кристаллизации биоматериалов носит более сложный характер.
В пятой главе диссертации исследована возможность и показано преимущество использования температуры как средства управления кристаллизацией белков и представлен разработанный метод управления процессом кристаллизации. Показано, что в качестве регулирующих параметров могут использоваться концентрация и разные типы осадителей, внесение или изначальное присутствие нейтральных добавок (буферы, гели, масла), затравливание (в т.ч. материалами с особыми свойствами), наложение электрических и магнитных полей. Однако для практической реализации управляемого выращивания биокристаллов необходимо было выбрать пригодный для физического моделирования параметр. Исследована возможность раздельного управления кристаллизацией белка в капилляре с помощью температуры: отвод тепла в одной точке раствора (![]() ) с термостатированием всего объема (
) с термостатированием всего объема (![]() ) (рис. 3).
) (рис. 3).
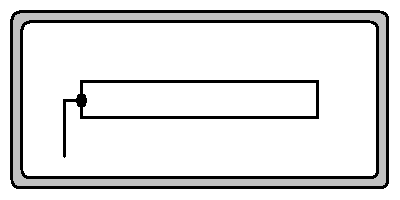
Рис. 3. Схематическое изображение кристаллизационной ячейки с капилляром
В этом методе становится возможным разделить зародышеобразование и непосредственно рост путем повышения пересыщения ![]() (
(![]() –концентрация белка) в конкретном месте капилляра для стимулирования зародышеобразования (
–концентрация белка) в конкретном месте капилляра для стимулирования зародышеобразования (![]() ) и, после образования единичных центров кристаллизации, понижения пересыщения в этом месте до оптимального для роста (
) и, после образования единичных центров кристаллизации, понижения пересыщения в этом месте до оптимального для роста (![]() ).
).
Для описания температурно-управляемого процесса кристаллизации белка была разработана математическая модель, включающая в себя уравнения неразрывности, количества движения и переноса концентрации белка, решаемые в естественных переменных. Для описания встраивания белковых молекул в кристалл потребовалась специфическая постановка граничных условий – сток массы белка, вызываемый только изменением ![]() . Отметим, что влияние
. Отметим, что влияние ![]() осуществляется через зависимость кривой растворимости на левой границе, зародышеобразование на которой наиболее вероятно.
осуществляется через зависимость кривой растворимости на левой границе, зародышеобразование на которой наиболее вероятно.
Система уравнений имеет следующий вид:
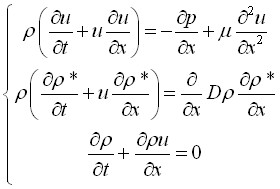 , (1)
, (1)
где ![]() – плотность раствора,
– плотность раствора, ![]() – скорость,
– скорость, ![]() – время,
– время, ![]() – координата,
– координата, ![]() – давление,
– давление, ![]() – динамическая вязкость белка,
– динамическая вязкость белка, ![]() – концентрация белка,
– концентрация белка, ![]() – плотность белка,
– плотность белка, ![]() – коэффициент диффузии белка.
– коэффициент диффузии белка.
Граничные условия. При ![]() ставятся следующие условия:
ставятся следующие условия:
для скорости 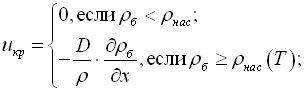 (2)
(2)
если ![]() , то
, то ![]() , иначе
, иначе ![]() ; (3)
; (3)
![]() ; (4)
; (4)
где ![]() – скорость вывода массы белка в кристалл,
– скорость вывода массы белка в кристалл, ![]() – плотность воды;
– плотность воды; ![]() – плотность белка, соответствующая насыщению при данной температуре;
– плотность белка, соответствующая насыщению при данной температуре; ![]() – температура на левом конце, значение может поддерживаться или меняться по линейному закону. При
– температура на левом конце, значение может поддерживаться или меняться по линейному закону. При ![]()
![]() и
и ![]() ;
; ![]() .
.
В расчетах использовались реальные размеры капилляра: ![]() 30 мм,
30 мм, ![]() 1,5 мм (в таких капиллярах проводился процесс кристаллизации). В связи с наличием преобладающего размера (
1,5 мм (в таких капиллярах проводился процесс кристаллизации). В связи с наличием преобладающего размера (![]() ) была рассмотрена одномерная модель гидродинамики.
) была рассмотрена одномерная модель гидродинамики.
Начальные условия. При ![]() концентрация белка в растворе
концентрация белка в растворе ![]() 50 мг/мл,
50 мг/мл, ![]() . Используемая для вычислений зависимость растворимости модельного белка лизоцима от
. Используемая для вычислений зависимость растворимости модельного белка лизоцима от ![]() показана на рис. 4.
показана на рис. 4.
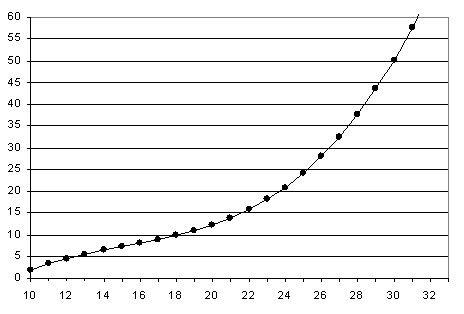
Рис. 4. График аппроксимированной зависимости растворимости лизоцима, использованный для вычислений
Проводились расчеты процессов ТМП при кристаллизации белка лизоцима с наложением градиента температуры на ячейку капиллярного типа (рис. 3). Предварительно методом математического моделирования процессов ТМП было установлено, что при таких температурных условиях тепловая конвекция в капилляре отсутствует.
а
б
в
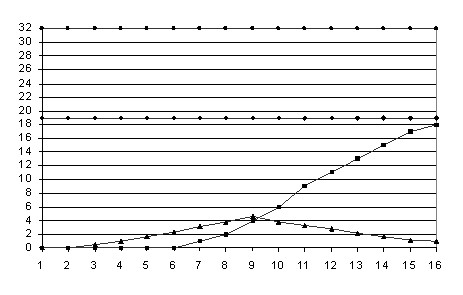
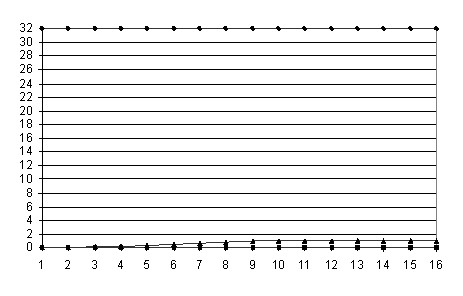
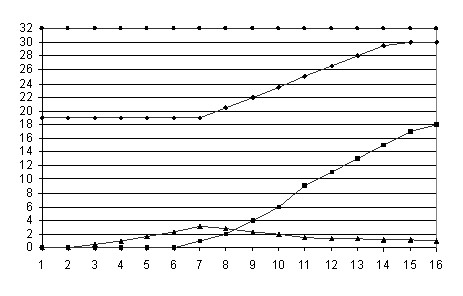
Рис. 5. Временные зависимости выведенной в кристалл массы белка (![]() , мг,
, мг, ![]() ) и создаваемого при этом в растворе пересыщения (
) и создаваемого при этом в растворе пересыщения (![]() ,
, ![]() ) от значений температуры в точке отвода тепла (
) от значений температуры в точке отвода тепла (![]() , °С,
, °С, ![]() ) и в объеме (
) и в объеме (![]() , °С,
, °С, ![]() )
)
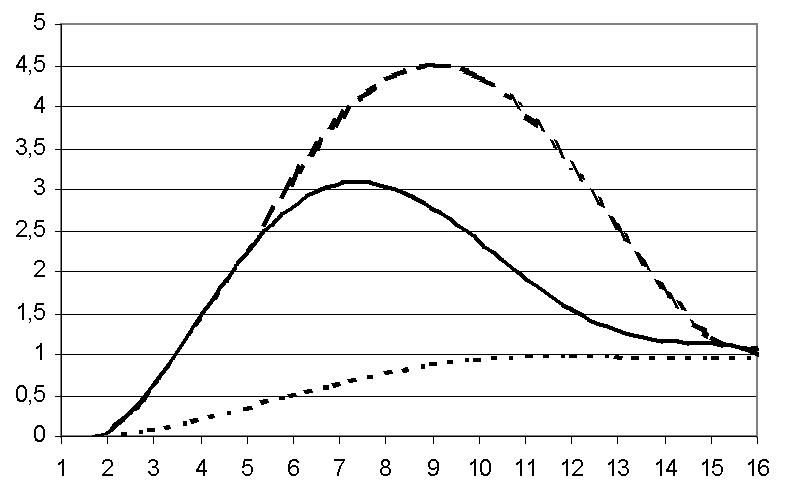
Рис. 6. Временные зависимости создаваемого в растворе пересыщения ![]() :
:
пунктирная линия (а) – неуправляемый эксперимент с разностью температур;
точечная линия (б) – эксперимент без разности температур;
сплошная линия (в) – эксперимент с управлением температурой
Расчетная область описывает только жидкую фазу, процесс кристаллизации характеризуется значением пересыщения на границе и количеством выведенной в кристалл массы белка. Сетка из 60 точек, равномерная. Шаг по времени 1 с.
В результате проведенных расчетов были получены временные зависимости выведенной в кристалл массы белка и создаваемого при этом в растворе пересыщения (для характеризации процесса кристаллизации). Меняющимся параметром в расчетах являлась температура в точке отвода тепла ![]() при стабилизации температуры объема раствора
при стабилизации температуры объема раствора ![]() . В первом случае она поддерживалась постоянной и достаточной для зародышеобразования и кристаллизации, вызываемой разностью температур (
. В первом случае она поддерживалась постоянной и достаточной для зародышеобразования и кристаллизации, вызываемой разностью температур (![]() 19°С), во втором – равной температуре объема раствора, что недостаточно для зародышеобразования и кристаллизации (
19°С), во втором – равной температуре объема раствора, что недостаточно для зародышеобразования и кристаллизации (![]() 32°С), в третьем же – менялась по линейному закону со скоростью 1,5°С/час (0,025°С/мин), начиная с расчетного момента зародышеобразования (
32°С), в третьем же – менялась по линейному закону со скоростью 1,5°С/час (0,025°С/мин), начиная с расчетного момента зародышеобразования (![]() ). Отметим, что т.к. требуется снижение пересыщения до
). Отметим, что т.к. требуется снижение пересыщения до ![]() , необходимо повышение растворимости, и, соответственно, температуры.
, необходимо повышение растворимости, и, соответственно, температуры.
На рис. 5 представлены результаты расчетов для трех различных типов экспериментов, а рис. 6 резюмирует расчетные значения пересыщения для этих случаев. Проведенные расчеты показывают, что в первом случае (рис. 5а), (рис. 6а) кристаллизация имеет место, но пересыщение возрастает до ![]() , что является избыточным и будет приводить к массовому зародышеобразованию. Во втором случае (рис. 5б), (рис. 6б) пересыщение не достигает значения
, что является избыточным и будет приводить к массовому зародышеобразованию. Во втором случае (рис. 5б), (рис. 6б) пересыщение не достигает значения ![]() , и зародышеобразования не происходит. В третьем же случае (рис. 5в), (рис. 6в) управление температурой по заданному закону на определенном этапе, после образования единичных зародышей, позволяет предотвратить дальнейшее возрастание пересыщения и плавно понизить его до значения
, и зародышеобразования не происходит. В третьем же случае (рис. 5в), (рис. 6в) управление температурой по заданному закону на определенном этапе, после образования единичных зародышей, позволяет предотвратить дальнейшее возрастание пересыщения и плавно понизить его до значения ![]() , необходимого для роста образовавшихся зародышей. При этом показано, что расчетное значение выведенной в кристалл массы белка
, необходимого для роста образовавшихся зародышей. При этом показано, что расчетное значение выведенной в кристалл массы белка ![]() 0,18 мг соответствовало размерам (0,8 мм
0,18 мг соответствовало размерам (0,8 мм ![]() 0,9 мм
0,9 мм ![]() 0,5 мм) образовавшегося в реальных экспериментах кристалла лизоцима. При таком варианте проведения эксперимента (с введением теплового управления) следует ожидать улучшения совершенства образующегося кристалла.
0,5 мм) образовавшегося в реальных экспериментах кристалла лизоцима. При таком варианте проведения эксперимента (с введением теплового управления) следует ожидать улучшения совершенства образующегося кристалла.
Полученные результаты теоретически доказали возможность управления с помощью температуры процессом кристаллизации биоматериалов в земных и, соответственно, в космических условиях при создании локального градиента температуры в растворе. На их основе была поставлена и реализована задача создания кристаллизационной ячейки для выращивания в капиллярах кристаллов биоматериалов с помощью управления температурой.
В шестой главе диссертации представлены результаты разработки метода и кристаллизационной аппаратуры для выращивания высокосовершенных кристаллов биоматериалов. Рассматривается методика получения биокристаллов с управляемым процессом кристаллизации. Приводятся результаты экспериментов по кристаллизации модельного белка лизоцима.
Описывается конструкция экспериментальной аппаратуры, которая применяется для температурного управления процессом кристаллизации. Она способна поддерживать и управлять температурой в пределах 440°C с точностью ±0,1°C. Запечатанный капилляр, содержащий кристаллизационный раствор, находится в одной части термостатированного корпуса, а в другой части располагается управляющая электроника. Капилляр в определенном месте контактирует с термоуправляемым конусом, создающим перепад температуры в заданной точке. Управляющими параметрами в процессе кристаллизации являются две температуры: всего корпуса-термостата и конуса, которые могут быть установлены в заданных пределах с шагом 0,1°C. При практических экспериментах корпус работает как термостат, поддерживая температуру в капилляре с общим объемом раствора 1020 мкл с точностью ±0,1°C, а конус исполняет роль источника или стока тепла в зависимости от режима работы. Процесс зародышеобразования и кристаллизации наблюдается через микроскоп, для чего объем раствора подсвечивается светодиодом. Это позволяет на определенном этапе обнаружить появление единичных зародышей вблизи точки контакта и своевременно начать изменение температуры конуса (и, соответственно, пересыщения в растворе), предотвращая дальнейшее массовое зародышеобразование.
Лизоцим из белка куриных яиц (производитель Sigma) кристаллизовался из водного раствора (концентрация 50 мг/мл) с использованием в качестве осадителя соли NaCl (концентрация 8%, pH = 4,6). Для оптимизации экспериментов по кристаллизации использовалась известная зависимость растворимости белка от температуры.
На рис. 7 показаны кристаллы лизоцима, выращенные в капилляре без управления температурой, т.е. обычным методом свободной диффузии. Исходные водные растворы содержали 50 мг/мл белка и 8 % соли NaCl при pH = 4,6 соответственно. Продолжительность процесса кристаллизации – 1 сутки; в результате эксперимента было получено большое число кристаллов малого размера (0,1–0,2 мм) и низкого качества, при этом температура корпуса была постоянной и равной 20°C, с точностью поддержания ±0,1°C.
На рис. 8 показаны кристаллы лизоцима, выращенные в разработанной экспериментальной аппаратуре с применением теплового управления. Капилляр с кристаллами белка сфотографирован через микроскоп. Состав исходного раствора и капилляр те же. Продолжительность процесса до появления кристаллических зародышей – 1 сутки; роста образовавшихся кристаллов – 5 суток. Получено три кристалла большого размера
(0,6–0,8 мм). Температура корпуса устанавливалась равной 32°C, с точностью поддержания ±0,1°C, температура конуса в начале эксперимента составляла 7°C и увеличивалась до 19°C после обнаружения зародышей.

Рис. 7. Фотография кристаллов лизоцима, выращенных без управления
температурой методом свободной диффузии

Рис. 8. Фотография кристаллов лизоцима, выращенных в капилляре с применением метода управления температурой
Приводятся результаты рентгеновского исследования выращенных кристаллов. Снятые 75 рентгенограмм позволили собрать набор с полнотой 97,8% в интервале углов дифракции, позволяющих получение разрешения до 1,5 . Исследованный кристалл лизоцима принадлежал к пространственной группе P4 с параметрами элементарной ячейки: ![]() 79,131 ,
79,131 , ![]() 79,131 ,
79,131 , ![]() 37,992 ; мозаичность кристалла 0,204; средний R-фактор по эквивалентным отражениям – 5,63% в зоне разрешения до 1,6 .
37,992 ; мозаичность кристалла 0,204; средний R-фактор по эквивалентным отражениям – 5,63% в зоне разрешения до 1,6 .
Полученные характеристики набора интенсивностей указали на высокое, с современных позиций, качество выращенного кристалла, которое превосходит качество кристаллов, обычно выращиваемых в наземных изотермических экспериментах.
Полученные результаты позволяют сделать вывод, что управление температурой дает возможность не только управлять процессом на этапах зародышеобразования и дальнейшей кристаллизации, но и создать оптимальные условия для выращивания высококачественных кристаллов белков.
В 3-х приложениях приводятся материалы, иллюстрирующие программную реализацию основных аспектов диссертационной работы (алгоритм расчета взаимной диффузии белка и осадителя в практических кристаллизационных экспериментах; алгоритм расчета процесса кристаллизации лизоцима с управлением температурой, реализованный в математическом пакете Matlab на встроенном языке программирования; алгоритм обмена данными и командами между управляющим персональным компьютером и разработанной кристаллизационной аппаратурой, реализованный в среде разработки Delphi).
ОСНОВНЫЕ РЕЗУЛЬТАТЫ И ВЫВОДЫ
1. Установлены закономерности процессов тепломассопереноса при росте в капиллярах кристаллов биоматериалов, в том числе при действии возмущающих воздействий (конвективных и вибрационных), определяющие условия преобладания диффузионного массопереноса.
2. Разработана и программно реализована математическая модель, описывающая процесс зарождения и роста кристаллов белка из раствора. Математическая модель описывает образование зародышей кристаллов и их рост в зависимости от локального значения перенасыщения.
3. С помощью предложенной модели определены оптимальные условия (на примере выращивания кристаллов лизоцима из водного раствора) кристаллизации белков размером не менее 100 мкм: стабильность поддержания температуры должна быть не хуже ±0,1°C; локальный градиент температуры – не более 1°C/см. Созданная модель вполне адекватна моделируемому явлению и может быть использована для параметрических исследований и прогнозных расчетов процесса кристаллизации белков при переменных температурных полях.
4. На основе проведенных теоретических расчетов исследована и показана возможность кристаллизации в капиллярах белков с высоким совершенством их структуры, недостижимом при использовании традиционно используемых в настоящее время методов кристаллизации, заключающаяся в реализации метода управляемой кристаллизации белков, обеспечивающего раздельное управление процессом роста кристаллов как на этапе их зародышеобразования, так и в процессе кристаллизации.
5. Показано, что управление процессом зарождения и роста может осуществляться путем: а) задания и прецизионного поддержания требуемой температуры всего раствора белка в капилляре; б) поддержания в локальной точке капилляра с раствором соответствующей температуры для обеспечения необходимого пересыщения для зарождения единичных (1–2) центров кристаллизации; в) изменения температуры в локальной точке капилляра и, соответственно, пересыщения в процессе разращивания кристалла.
6. Разработан опытный лабораторный образец экспериментального блока-кристаллизатора биокристаллов. В этой системе осуществляется не только управление температурой раствора с точностью регулирования ±0,1°C, но и реализована возможность создания пересыщения белка в соответствующем месте капилляра за счет точечного подвода или отвода в этом месте тепла (т.е. создания в этом месте локального температурного градиента), что исключает возможность образования множества зародышей по всему объему раствора, находящегося в контролируемых изотермических условиях, что исключает и многоцентровую спонтанную кристаллизацию.
ОСНОВНОЕ СОДЕРЖАНИЕ ДИССЕРТАЦИИ ОТРАЖЕНО В СЛЕДУЮЩИХ РАБОТАХ
1. Математическое моделирование и оптимизация роста биокристаллов / И.Ж. Безбах, В.Г. Косушкин, В.И. Стрелов и др. // Прогрессивные технологии, конструкции и системы в приборо- и машиностроении: Материалы Всероссийской научно-технической конференции. – М., 2004. – Т.1. – С.277–278.
2. Numerical models for biocrystal growing / V.P. Ginkin, B.G. Zakharov, I.Zh. Bezbakh et al. // Abstracts of the 14th International Conference on Crystal Growth. – Grenoble (France), 2004. – P.335.
3. Управление процессами кристаллизации биоматериалов в земных и космических условиях / И.Ж. Безбах, Б.Г. Захаров, В.И. Стрелов и др. // Тезисы докладов XI Национальной конференции по росту кристаллов. – М., 2004. – С.355.
4. Математическое моделирование и экспериментальные исследования влияния вибраций и конвекции Марангони на микрооднородность кристаллов полупроводников / В.И. Стрелов, Б.Г. Захаров, И.Ж. Безбах и др. // Поверхность. – 2005. – №10. – С.80–87.
5. Моделирование процесса управления ростом кристаллов белков в земных и космических условиях / И.Ж. Безбах, В.И. Стрелов, В.Г. Косушкин и др. // Рост монокристаллов и тепломассоперенос: Труды
6-й международной конференции. – Обнинск, 2005. – Т.3. – С.545–551.
6. Математическое моделирование и экспериментальные исследования влияния температурных градиентов на процессы кристаллизации для земных и космических условий / В.И. Стрелов, Б.Г. Захаров, И.Ж. Безбах и др. // Кристаллография. – 2005. – Т.50, №3. – С.536–544.
7. Mathematical modeling and experimental investigation of the effect of temperature gradients on crystallization processes under terrestrial and space conditions / V.I. Strelov, B.G. Zakharov, I.Zh. Bezbakh et al. // Crystallography Reports. – 2005. – V.50, No.3. – P.490–498.
8. Прецизионное температурное управление процессом кристаллизации биоматериалов / И.Ж. Безбах, В.И. Стрелов, Н.И. Сосфенов и др. // Тезисы докладов XII Национальной конференции по росту кристаллов. – М., 2006. – С.330.
9. Оптимизация роста кристаллов белков с применением метода теплового управления / И.Ж. Безбах, В.Г. Косушкин, В.И. Стрелов и др. // Методы исследования и проектирования сложных технических систем: Сборник статей (Труды МГТУ №592). – М., 2006. – С.18–26.
10. Кристаллизация белка лизоцима в прецизионно-управляемом градиенте температуры / В.И. Стрелов, Б.Г. Захаров, И.Ж. Безбах и др. // Кристаллография. – 2007. – Т.52, №6. – С.1134–1139.
11. Безбах И.Ж., Стрелов В.И., Захаров Б.Г. Управление процессом зародышеобразования и роста биокристаллов // Тезисы докладов Российского симпозиума "Космическое материаловедение". – Калуга, 2007. – С.38.
12. Моделирование роста биокристаллов под воздействием управляющего теплового поля / В.П. Гинкин, И.Ж. Безбах, В.И. Стрелов и др. // Тезисы докладов Российского симпозиума "Космическое материаловедение". – Калуга, 2007. – С.43.
Безбах Илья Жанович
Оптимизация процессов кристаллизации биоматериалов
Автореферат диссертации на соискание ученой степени
кандидата физико-математических наук
Подписано в печать 25.09.2007.
Бумага офсетная 80 г/м2. Формат 60x84 1/16.
Усл. печ. л. 1. Уч.-изд. л. 1. Тираж 100 экз. Заказ № 176.
Отпечатано в Редакционно-издательском отделе
КФ МГТУ им. Н.Э. Баумана
248000, г. Калуга, ул. Баженова, 2, тел. 57-31-87

