Возможности клинического применения персонифицированной симбионтной терапии при синдроме раздраженной толстой кишки
На правах рукописи
СУНДУКОВА
Зарина Руслановна
ВОЗМОЖНОСТИ КЛИНИЧЕСКОГО ПРИМЕНЕНИЯ ПЕРСОНИФИЦИРОВАННОЙ СИМБИОНТНОЙ ТЕРАПИИ ПРИ СИНДРОМЕ РАЗДРАЖЕННОЙ ТОЛСТОЙ КИШКИ
14.01.04 – внутренние болезни
03.02.03 – микробиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2010
Работа выполнена на кафедре терапии и клинической фармакологии Государственного образовательного учреждения дополнительного профессионального образования «Санкт-Петербургская медицинская академия последипломного образования Министерства здравоохранения Российской Федерации».
Научные руководители:
доктор медицинских наук профессор Симаненков Владимир Ильич
доктор медицинских наук профессор Суворов Александр Николаевич
Официальные оппоненты:
доктор медицинских наук профессор Барановский Андрей Юрьевич
доктор медицинских наук профессор Бойцов Алексей Геннадьевич
Ведущая организация: Государственное образовательное учреждение высшего профессионального образования «Санкт-Петербургский государственный медицинский университет им. акад. И.П.Павлова Министерства здравоохранения Российской Федерации».
Защита диссертации состоится «___» ____________2010 г. в «___» часов на заседании диссертационного совета Д 208.089.01 при Санкт-Петербургской медицинской академии последипломного образования (191015, Санкт-Петербург, ул. Кирочная, д. 41).
С диссертацией можно ознакомиться в фундаментальной библиотеке академии (195196, Санкт-Петербург, Заневский пр., д. 1/82).
Автореферат разослан «___» ____________________2010 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук профессор А.М.Лила
Актуальность проблемы. Актуальность работы связана с высокой частотой встречаемости дисбиоза с тенденцией к неуклонному росту заболеваемости. Учитывая широкое и неконтролируемое применение антибиотических лекарственных средств, нет оснований предполагать, что в ближайшие годы ситуация изменится к лучшему (Лобзин Ю.В., 2006, Барановский А.Ю., 2007).
В клинической практике для коррекции микробиоценоза используется несколько классов препаратов. Наибольшее распространение приобрели пробиотики, включающие непатогенные штаммы лакто-, бифидобактерий, реже энтерококки. К сожалению, терапия пробиотиками не всегда дает положительный результат (Шендеров Б.А.,2003).
Недостаточная эффективность пробиотической терапии может быть связана с индивидуальностью микробиоценоза каждого человека. Состав микрофлоры образует сообщества и специфичен на штаммовом уровне для каждого индивидуума. (Ткаченко Е.И., 2007). Промышленные штаммы пробиотиков чужеродны для макроорганизма, они не имеют «пароля» для входа микробов внутрь биопленки кишечника, и, поэтому, пребывают в нем транзиторно (Осипов Г.А., 2005). Таким образом, создание нового аутопробиотика представляется весьма актуальным
Цель работы: разработка методики персонифицированной симбиотной терапии, а также оценка ее влияния на течение СРК.
Для достижения поставленной цели были определены следующие задачи:
- Сопоставить характер полостной и пристеночной микрофлоры кишечника в илеоцекальной зоне.
- Разработать методику выделения «чистой» культуры индивидуальной симбионтной микрофлоры.
- Оценить в эксперименте на животных безопасность и переносимость аутопробиотика.
- Провести клиническое исследование безопасности и переносимости аутопробиотической терапии на здоровых добровольцах.
- Сравнить влияние применения пробиотика, содержащего Enterococcus fecium L3 и выделенных аутоштаммов на микробиологические характеристики и клиническое течение заболевания у пациентов с СРК.
Научная новизна. Впервые был создан и изучен аутопробиотик на основе энтерококков.
Практическая значимость работы. В результате исследования разработана технология получения аутопробиотика и создан новый метод лечения персонифицированной симбионтной терапии (ПЕРСТ).
Основные положения диссертации, выносимые на защиту.
- Данные экспериментального и клинического исследований аутопробиотика, содержащего Enterococcus fecium, свидетельствуют о его безопасности и позитивном влиянии на синдром дисбиоза при СРК.
- Аутопробиотическая терапия способствует редукции основных клинических проявлений СРК.
- Сравнительный анализ влияния пробиотика, содержащего запатентованный штамм Enterococcus fecium L3, и аутопробиотика, содержащего Enterococcus fecium, свидетельствует о сопоставимой безопасности и большем позитивном влиянии аутопробиотика.
Личный вклад автора в проведенное исследование. Вклад автора в исследование заключался в определении основной цели работы, личном участии в клиническом, молекулярно-генетическом исследовании пациентов, а также проведении лечебных мероприятиях, выполнении статистической обработки и анализа полученных данных.
Реализация результатов исследования. Полученные результаты внедрены в педагогический и научно-исследовательский процесс на кафедре терапии и клинической фармакологии СПб МАПО, а также научно-исследовательскую работу НИИ Экспериментальной медицины и лечебно-диагностический процесс гастроэнтерологического отделения больницы №26.
Апробация работы. Результаты исследования доложены на 2-м Международном конгрессе по пробиотикам Санкт Петербург - Пробиотики 2009; на конференции молодых ученых в СПб МАПО в 2010 г.
По теме диссертации опубликовано 10 печатных работ, в том числе две статьи в изданиях, рекомендованном ВАК.
Объем и структура диссертации. Диссертация изложена на 145 страницах, состоит из введения, обзора литературы, материалов и методов исследования, собственных наблюдений, заключения, выводов, практических рекомендаций и библиографического указателя, включающего 95 отечественных и 187 иностранных источника литературы, иллюстрирована 38 таблицами и 46 рисунками.
Материалы и методы исследования.
Общая характеристика животных. Клинической фазе исследования предшествовала экспериментальная, проведенная на животных. Изучение безопасности и эффективности пробиотической терапии проводилось на 20 здоровых крысах-самцах линии Wistar с дисбиозом, индуцированным антибиотиками. Все крысы содержались при сходных условиях температуры, влажности и освещения, получали однотипное питание. Длительность эксперимента 8 - дней.
Общая характеристика больных. Чтобы сопоставить видовые и количественные характеристики пристеночной микрофлоры илеоцекальной зоны и полостной микрофлоры, обследовано 20 человек. В качестве модели, для изучения пристеночной микрофлоры толстой кишки, были выбраны- колонобиоптат больных с диагнозом синдрома раздраженной толстой кишки, у которых колоноскопия и биопсия проводилась в целях исключения опухолевого процесса, воспалительных заболеваний кишечника и др.
После доклинической фазы, было проведено исследование на переносимость и безопасность аутопробиотика на основе собственных E. faecium на 7 здоровых добровольцах с обязательной процедурой подписания информированного согласия. Аутопробиотик приготовлялся из чистой, генетически охарактеризованной чистой культуры энтерококка, выделенного из собственных фекалий каждого добровольца. Средний возраст добровольцев составлял 28±0,5 лет, участвовали 5 женщин и 2 мужчин. Длительность приема
исследуемого препарата 10 дней. Доза препарата - 100 мл 2 раза в день молочно
кислой закваски, содержащей собственных энтерококков.
На последнем этапе исследования, на основе клинико-лабораторных показателей 102 пациентов, было выделено 60 человек, страдающих синдромом раздраженной толстой кишки. Методом случайной выборки пациенты были разделены на 3 группы. В 1 и 2 группах по 25 человек, в 3 группе 10 человек. Средний возраст в 1 группе составил 43,8±2,3 года, соотношение мужчин и женщин – 9 (36%) и 16 (64%) человек соответственно, средняя продолжительность заболевания - 6,12±1,6 года. Во 2 группе количество мужчин составило 7 (28%) человек, женщин – 18 (72%), средний возраст - 50,1±2,9 лет и средняя продолжительность заболевания - 5,5±1,2 года. В третьей группе было 3 (30%) мужчин и 7 (70%) женщин, средний возраст составил 45,6±3,2 лет и средняя продолжительность заболевания - 8,3±1,6 года. Достоверных различий между группами по полу, возрасту и средней длительности заболевания не выявлено.
В соответствии с поставленными задачами пациенты в группах получали различные схемы терапии. Пациентам 1 группы проводилась терапия аутопробиотиком на основе E. faecium, в дозе 100 мл/сут.. Во второй группе пациенты получали E. faecium L3 (промышленный штамм), в дозе 100 мл/сут. В 3 группе пациенты получали базовую среду (автоклавированное молоко). Обследование на этапе наблюдения проводилось дважды: до лечения и после окончания терапии.
Методы исследования. Программа обследования животных включала следующие разделы:
- Лабораторный.
- Морфологический.
- Микробиологический и молекулярно-генетический.
- Иммунологический.
- Статистическая обработка полученных данных.
Программа обследования всех больных включала следующие разделы:
- Клинико-лабораторный.
- Эндоскопический с прицельной биопсией.
- Морфологический.
- Микробиологический и молекулярно-генетический.
- Иммунологический.
- Исследование показателей качества жизни.
- Статистическая обработка полученных данных.
Все исследования, исключая эндоскопию с прицельной биопсией, выполнялись на каждом этапе наблюдения: до лечения и после лечения через 10-14 дней.
Статистическую обработку результатов проводили при помощи пакета STATISTICA 8.0. В случаях нормального распределения величин использовали параметрические методы исследования (t-критерий Стьюдента, корреляционный анализ). В других случаях применялись непараметрические методы исследования – U критерий Манна-Уитни, двухвыборочный критерий Колмогорова-Смирнова, T-критерий Вилкоксона, ранговый коэффициент Спирмена. Достоверными считались различия, при которых коэффициент доверительной вероятности (p) был ниже 0,05. Для установления связей между показателями проводили корреляционный анализ.
Результаты исследования.
Сопоставление видовых и количественных характеристик полостной микрофлоры и пристеночной микрофлоры илеоцекальной зоны у пациентов с СРК.
С целью сопоставления видовых и количественных характеристик пристеночной и полостной микрофлоры илеоцекальной зоны, было обследовано 20 человек. Для изучения пристеночной микрофлоры толстой кишки, были взяты образцы колонобиоптата больных с диагнозом синдрома раздраженной кишки, у которых колоноскопия и биопсия проводилась в целях исключения опухолевого процесса, воспалительных заболеваний кишечника. 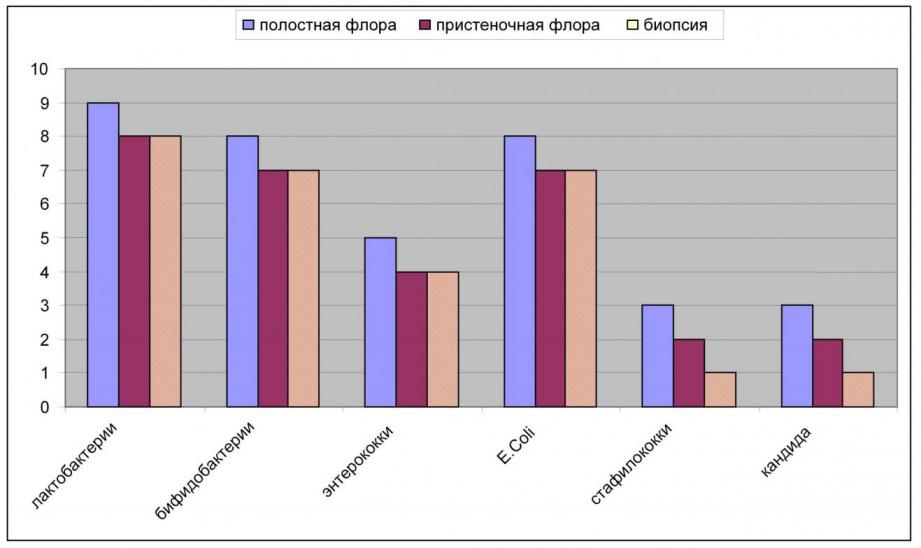
Рисунок 1. Сравнительный анализ пристеночной и полостной
микрофлоры в илиоцекальной зоне.
Достоверных различий в видовом и количественном составе пристеночной и полостной микрофлоры не выявлено. При оценке микрофлоры кишечника можно ориентироваться на данные посева кала, не прибегая к инвазивным методам исследования.
Экспериментальный раздел
Изучение эффективности и безопасности пробиотической терапии проводили на половозрелых белых лабораторных крысах. Перед проведением экспериментов животные были разделены на три группы: А, Б и К (по 4 крысы в каждой группе). Животным групп А и Б ежедневно в одно и то же время (первая половина дня) per os в течение трех дней вводили антибактериальные препараты в количестве 15 и 10 мг чистого вещества, растворенного в дистиллированной воде, соответственно, ампициллин (ОАО «Органика», Россия) и метронидазол (ОАО «Ирбитский Химико-фармацевтический завод», Россия). Затем крысам группы А с третьего дня (через 6 часов после введения антибиотиков) в течение 6 дней вводили 500 мкл молочнокислой закваски, содержащей 5,5х108 КОЕ /мл Enterococcus faecium L5. Данный штамм, как и исходный штамм E. faecium L3, обладает способностью ферментировать сахара, в частности мальтозу и лактозу и отличается от исходного штамма L3 лишь введенным в данный штамм геном устойчивости к эритромицину. Данная маркировка позволяла отслеживать судьбу штамма в организме животных. Крысам группы Б с третьего по девятый день ежедневно вводили молоко в объеме 500 мкл. Животные группы К ежедневно в течение первых трех дней получали дистиллированную воду в объеме 500 мкл, а затем в течение 6 дней – молоко в том же объеме. Микробиологическое исследование проводили в соответствии с Отраслевым стандартом 2003 и рекомендациям.
В ходе эксперимента осуществлялось наблюдение за аппетитом, весом, характером стула и поведением лабораторных животных, проводилось 3-х кратное микробиологическое исследование фекалий на 1,3 и 8-й дни. Перед использованием собственных штаммов энтерококков проводилось их генетическая идентификация и исследование на наличие факторов патогенности методом полимеразной цепной реакции (ПЦР).
Предварительно была исследована пристеночная и просветная флора толстой кишки и показано, что в фекалиях можно обнаружить практически тот же спектр и количество бактерий, которые удается выделить при анализе биопсийного материала. В наших экспериментах при бактериологическом исследовании фекалий животных, выявлены существенные изменения в составе микробиоты кишечника. После воздействия антибактериальными препаратами, в фекалиях крыс увеличивалось количество бактерий родов Klebsiella., Proteus и Candida Clostridium spp. Escherichia coli c низкой ферментативной активностью.
После введения штамма L5, аутопробиотических энтерококков была отмечена элиминация появившихся после воздействия антибиотиками условно-патогенных бактерий. В то же время, у животных группы Б существенных изменений в количестве Klebsiella spp. и Proteus spp. не наблюдались, в ряде случаев в конце экспериментов происходило восстановление флоры без воздействия пробиотиков. Эта тенденции просматривалась более отчетливо при введении не молока, а фосфатного буфера. По-видимому, молоко являлось дополнительной нагрузкой для процесса пищеварения и могло угнетать полезную микрофлору, препятствовать быстрому восстановлению микробиоты. Ранее в экспериментах на здоровых животных уже было показано, то энтерококки в этих условиях, как правило, исчезают быстрее из кишечника.
По данным микробиологического исследования после воздействия антибиотиков к 3-му дню отмечалось снижение количества лактобацилл, бифидобактерий, эшерихий, энтерококков увеличивалось количество или появлялись в титрах до 5 lg КОЕ/ мл условнопатогенные микроорганизмы: Klebsiella spp., Proteus spp., Candida spp. Подобные изменения микробитоты желудочно-кишечного тракта после введения ампициллина уже были описаны ранее при исследовании влияния различных групп антибиотиков крысам [Шендеров Б.А., 2004]. Та же тенденция отмечалась в группе, получавшей молочнокислую закваску на основе L. fermentum Z. Однако в группах контроля увеличение лактобацил, бифидобактерий и энтерококков проявлялось в меньшей степени. Не элиминировали или лишь незначительно изменяли свои количества рассматриваемые условно-патогенные бактерии (УПБ). Обращало на себя внимание то, что пробиотические энтерококки проявляли большую антибактериальную активность и снижали количество эшерихий в 1000 раз, подавляли рапространение протея и клебсиелл. На клебсиеллы недостаточно эффективно действовали ауопробиотики, а молоко даже увеличивало их число. Количество бифидобактерий и лактобацилл к 8 дню эксперимента увеличивалось во всех группах и имело тенденцию к увеличению в группе аутопробиотиков на 8 день по сравнению с 3-м днем (с 4,00±0,89 до 6,00±0,26). В группе контроля тоже есть некоторое увеличение количества бифидобактерий с 5,00±0,71 до 6,00±0,30, но достоверная динамика не отмечалась. В отличие от двух вышеперечисленных групп у крыс, получавших молоко и L.5 отмечается снижение количества бифидобактерий. Количество лактобацилл достоверно увеличилось в группе аутопробиотиков с 5,17±0,70 до 7,00±0,27.
По данным микробиологического исследования после воздействия антибиотиков к 3-му дню отмечалось снижение количества всех групп микроорганизмов во всех группах. Количество энтерококков на 8 день имеет четкую тенденцию к увеличению по сравнению с 3-м днем в группах аутопробиотика (с 2,34±0,80 до 4,00±0,26 и E. faecium L5 с 2,00±0,00 до 4,33±0,34). Количество бифидобактерий имеет тенденцию к увеличению в группе аутопробиотиков на 8 день по сравнению с 3-м днем (с 4,00±0,89 до 6,00±0,26). В группе контроля тоже есть некоторое увеличение количества бифидобактерий с 5,00±0,71 до 6,00±0,3,00, но достоверная динамика не отмечалась. В отличие от двух вышеперечисленных групп у крыс, получавших молоко и L.5 отмечается снижение количества бифидобактерий, но p > 0,05. Количество лактобацилл достоверно увеличилось в группе аутопробиотиков с 5 до 7 lg КОЕ/ мл.
После доклинической фазы, было проведено исследование на переносимость и безопасность аутопробиотика на основе собственных E. faecium на 7 практически здоровых добровольцах с обязательной процедурой подписания информированного согласия. Средний возраст добровольцев составлял 28±0,53 лет, участвовали 5 женщин и 2 мужчин. Длительность приема исследуемого препарата 10 дней. Доза препарата - 100 мл 2 раза в день молочно-кислой закваски, содержащей 108 собственных энтерококков.
Перед началом и в конце исследования проводился клинический осмотр испытуемых, выполнялось биохимическое исследование крови на основные показатели и электролиты, изучалась липидограмма, определялись уровни иммуноглобулинов, IL-1 и IL-8 сыворотки крови.
Достоверных изменений лабораторных показателей не отмечено. При оценке уровней интерлейкинов IL-1 и IL-8 достоверных изменений не выявлено. Значимо не изменился уровень холестерина и других показателей липидограммы, хотя в литературе есть данные о позитивном влиянии пробиотических штаммов на его уровень. Возможно, это влияние проявляется у пациентов, более старшего возраста, при наличии исходных нарушений липопротеидного обмена.
Ни один из добровольцев не отметил появления нежелательных явлений, симптомов диспептических расстройств. Испытуемые оценили приятные органолептические свойства закваски, что увеличило приверженность. Во всех случаях, кроме двух, отмечалось тенденция к изменению формы стула по Бристольской шкале в сторону размягчения (с типа 1 и 2 на тип 4), улучшение аппетита и увеличение массы тела.
При оценке динамики основных показателей кишечной микрофлоры у здоровых добровольцев достоверно значимых изменений не наблюдалось, что может быть связано с исходным отсутствием дисбиотических нарушений у них.
По результатам испытания на добровольцах можно сделать вывод о безопасности аутопробиотика и возможности продолжения изучения эффективности аутопробиотической терапии в клинике.
Клиническое изучение персонифицированной симбионтной терапии
Скрининг был осуществлен у 102 пациентов с синдромом раздраженного кишечника. По критериям включения, для динамического проспективного наблюдения, выделена группа из 60 больных с СРК.
Пациенты с синдромом раздраженного кишечника методом случайной выборки были поделены на 3 группы.
1. Группа (25 человек) – получала персонифицированную симбионтную терапию (в виде молочно-кислой закваски, содержащей 108 КОЕ /мл собственных энтерококков в 1 мл закваски, в дозе 100 мл/сутки- по 50 мл 2 раза в день в течение 10 дней).
- Группа (25 человек) – получала терапию синбиотиком Ламинолакт (в виде молочно – кислой закваски Авена, содержащей Enterococcus faecium L-3 в дозе 100 мл/сутки по 50 мл 2 раза в день в течение 10 дней).
- Группа (10 человек) – контрольная – получала базовую среду (стерильное топленое молоко - после автоклавирования) - без добавок в суточной дозе 100 мл.
Таблица 1
Сравнительная характеристика групп пациентов до лечения
| Показатель | I группа (Аутопробиотик), n=25 | II группа (L3), n=25 | III группа (контрольная), n=10 |
| Мужчины | 10 (31%) | 11(41%) | 3 (30%) |
| Женщины | 15 (69%) | 14(59%) | 7 (70%) |
| Возраст (M±m, min-max) | 43,8±2,3 22-63 | 50,1±2,9 22-70 | 45,6±3,2 22-67 |
| Возрастной состав: - до 30 лет - от30 до 50 лет - старше 50 лет | 3 (12%) 16 (64%) 6 (24%) | 2(8,3%) 14(58,3%) 8(33,4%) | 3 (13,1%) 12 (52,1%) 8 (34,8%) |
| Диагноз: - СРК | 25 (75%) | 25(80%) | 9 (90%) |
| Средняя длительность заболевания (M±m, min-max), годы | 6,12±1,6 1-25 | 5,5±1,2 1-24 | 8,3±1,6 1-25 |
По всем показателям группы сравнимы, достоверных различий между ними не выявлено.
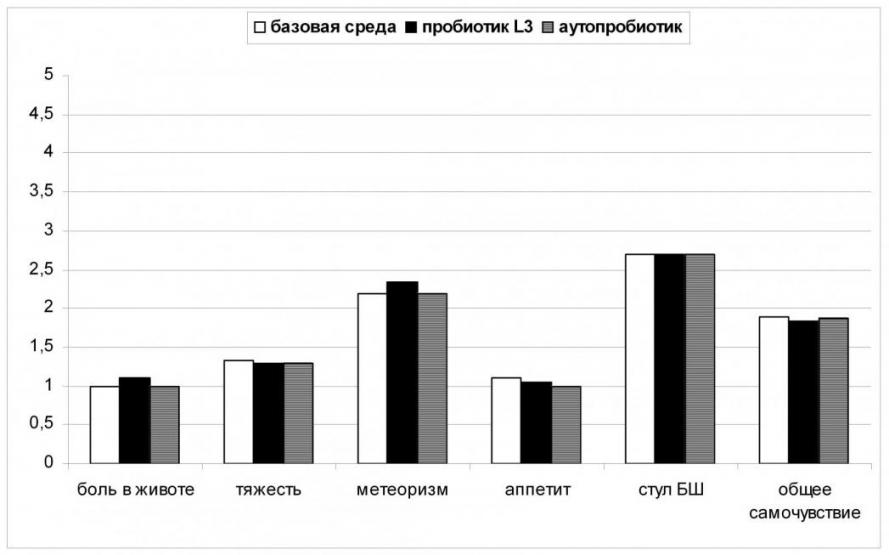
Рисунок 2. Сравнение клинических данных в группах «базовая среда», «пробиотик L3», «аутопробиотик» до лечения
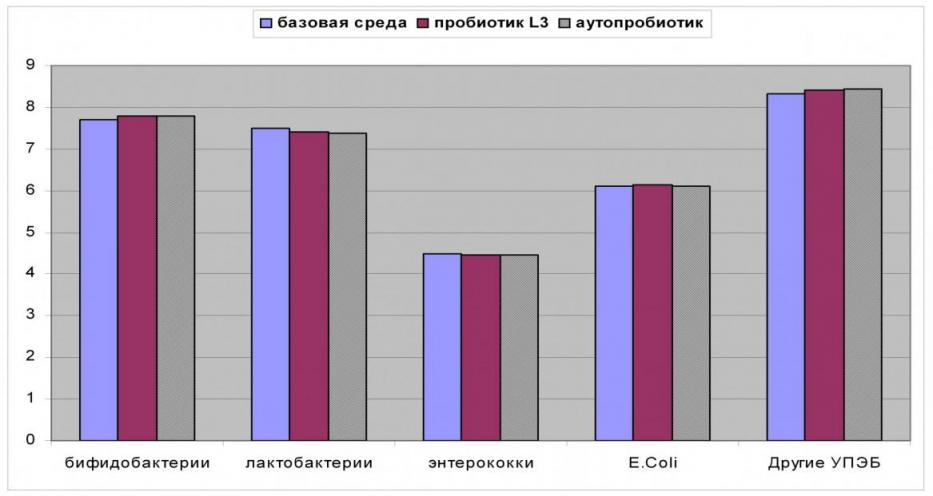
Рисунок 3. Характеристика кишечной микрофлоры у пациентов с СРК в группах «аутопробиотик», «базисная среда», «пробиотик L3» до лечения (lgКОЕ)
После лечения в группах, получавших пробиотическую терапию, наблюдалось достоверное уменьшение выраженности клинической симтоматики по сравнению с группой получавшей базовую среду, при этом в группе аутопробиотической терапии, по сравнению с группой получавшей промышленный штамм Enterococcus faecium L-3, наблюдалось достоверное уменьшение выраженности метеоризма и улучшение общего самочувствия.
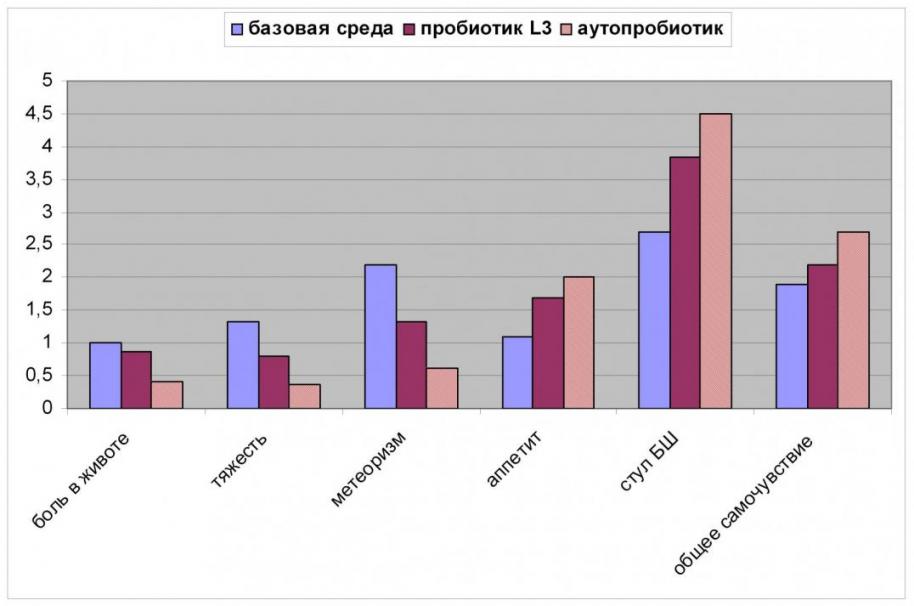
Рисунок 4. Сравнение клинических данных в группах «аутопробиотик», «базовая среда», «пробиотик L3» после лечения
При исследовании микрофлоры кишечника у пациентов, после лечения, выявлено достоверное увеличение представителей нормальной микрофлоры кишечника и достоверное снижение представителей условно-патогенной микрофлоры в группах получавшик аутопробиотик и промышленный штамм Enterococcus faecium L-3, по сравнению с группой, получавшей базовую среду. В то же время, при сравнении между группами, получавшими пробиотические штаммы, выявлено достоверно большее количество бифидобактерий и лактобацилл и снижение условно-патогенной микрофлоры в группе получавших аутопробиотик.
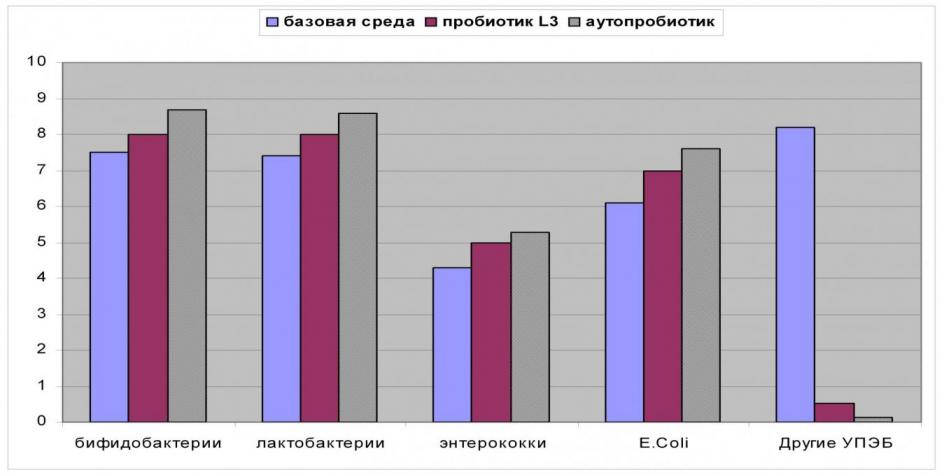
Рисунок 5. Динамика кишечной микрофлоры у пациентов с СРК в группах «аутопробиотик», «базовая среда», «пробиотик L3» после лечения (lgКОЕ)
Динамика показателей качества жизни у пациентов с СРК в условия различных схем терапии.
Качество жизни у пациентов с СРК в данном исследовании проводилось с использованием опросника SF-36.
Было выявлено, что у пациентов с СРК имеются значительные снижения показателей по шкалам ролевого физического и эмоционального функционирования, жизнеспособности, общего здоровья и физической боли. При анализе полученных данных видно, что в первых двух группах, после курса терапии, наблюдается достоверное улучшение показателей качества жизни практически по всем шкалам. Лишь в группе пациентов, получавших аутопробиотик, показатели качества жизни по некоторым шкалам (ролевое физическое, ролевое эмоциональное функционирование, общее здоровье) к концу наблюдения несколько более улучшились по сравнению с группой получавшей пробиотиком L3. В контрольной группе динамики не наблюдается.
Выводы
- Достоверных различий между просветной и пристеночной микрофлорой в илеоцекальной зоне кишечника у пациентов, страдающих СРК, не выявлено.
- Для создания аутопробиотика может быть использована просветная микрофлора, выделенная из фекалий пациентов.
- Аутоштаммы Enterococcus faecium могут применяться в качестве пробиотического продукта при СРК.
- Терапия аутопробиотиком достоверно или существенно снижает выраженность клинических проявлений и улучшает состояние кишечного биоценоза при СРК.
- Редукция клинической симтоматики и нормализация кишечной микрофлоры при СРК более выражены при применении аутопробиотика, чем на фоне лечения пробиотиком L3 (промышленный пробиотик на основе Enterococcus faecium).
Практические рекомендации
- Стандартное микробиологическое исследование просветной микрофлоры у больных с СРК отражает наиболее существенные характеристики кишечного микробиоценоза, что позволяет использовать посев кала на дисбиоз в целях контроля эффективности пробиотической терапии.
- Для коррекции состояния кишечного микробиоценоза у больных с СРК может использоваться разработанный аутопробиотик, содержащий Enterococcus fecium.
- Применение аутопробиотика, содержащего Enterococcus fecium 108 КОЕ в 1 мл, в дозе по 50 мл два раза в сутки, в комплексной терапии СРК способствует уменьшению выраженности клинических проявлений.
Список работ, опубликованных по теме диссертации
- Симаненков В.И. Современные подходы к методам диагностики и коррекции дисбиоза / В.И. Симаненков, З.Р. Сундукова // Актуальные проблемы клинической медицины: Материалы конференции, посвященной 100-летию Колпинской Городской больницы №33. - СПб, 2008. – С. 59.
- Симаненков В.И. Постинфекционный синдром раздраженного кишечника: есть ли место в терапии пробиотикам? / В.И Симаненков, А.Н. Суворов, С.М. Захаренко, А.Н. Бочкарева, З.Р. Сундукова // Инфекционные болезни. – 2009. – Т. 7, №3. – С. 68 - 75.
- Сундукова З.Р. Опыт доклинического изучения аутопробиотиков / З.Р. Сундукова, В.Н. Донец // Актуальные вопросы клинической и экспериментальной медицины: Сборник тезисов к научно-практической конференции молодых ученых. - СПб, 2009. – С. 62.
- Донец В.Н. Воздействие аутопробиотиков на крыс в экспериментах при дисбиозе / В.Н. Донец, З.Р. Сундукова // Актуальные вопросы клинической и экспериментальной медицины: Сборник тезисов к научно-практической конференции молодых ученых. - СПб, 2009. – С. 28.
- Симаненков В.И. Сопоставление видовых и количественных характеристик полостной микрофлоры и пристеночной микрофлоры илеоцекальной зоны / В.И. Симаненков, А.Н. Суворов, З.Р. Сундукова, В.Н. Донец // Гастроэнтерология Юга России.– Рост, 2009. – С. 87.
- Тарасова Е.И. Влияние пробиотических энтерококков на иммунную систему крыс с экспериментальным дисбиозом кишечника / Е.И. Тарасова, Е.И. Ермоленко, В.В. Донец, З.Р. Сундукова, А.Н. Суворов // 2-ой Международный конгресс по пробиотикам Санкт Петербург- Пробиотики 2009, Р. 140, М. 39.
- Сундукова З.Р. Опыт клинического изучения аутопробиотиков / З.Р. Сундукова, В.Н. Донец // 2-ой Международный конгресс по пробиотикам Санкт Петербург - Пробиотики 2009, Р. 137, М. 38.
- Донец В.Н. Безопасность использования аутопробиотиков у добровольцев / В.Н. Донец, З.Р. Сундукова // 2-ой Международный конгресс по пробиотикам Санкт Петербург - Пробиотики 2009, Р. 46, М. 13.
- Симаненков В.И. Опыт экспериментального и доклинического изучения аутопробиотиков / В.И. Симаненков, А.Н. Суворов, В.Н. Донец, Е.И. Ермоленко, З.Р. Сундукова // Гастроэнтерология Юга России. – Рост, 2009. – С. 83.
- Симаненков В.И. Персонифицированная симбионтная терапия и качество жизни больных с синдромом раздраженного кишечника / В.И. Симаненков, А.Н. Суворов, О.И.Соловьева З.Р.Сундукова // Ученые записки СПбГМУ им. академика И.П.Павлова. - 2010. – Т. XVII, №2. – С. 126.

