Синтез, свойства и биологическая активность 3-ароил-3,4-дигидро-2 н -1,4-бензоксазин-2-онов
На правах рукописи
Рассудихина Наталья Анатольевна
СИНТЕЗ, СВОЙСТВА И БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ 3-АРОИЛ-3,4-ДИГИДРО-2Н-1,4-БЕНЗОКСАЗИН-2-ОНОВ
15.00.02 - фармацевтическая химия, фармакогнозия
Автореферат диссертации
на соискание ученой степени
кандидата фармацевтических наук
Пермь-2008
Диссертационная работа выполнена в ГОУ ВПО «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель: доктор химических наук,
профессор Гейн Владимир Леонидович
Официальные оппоненты: доктор фармацевтических наук,
профессор Коркодинова Л.М.,
доктор химических наук,
профессор Абашев Г.Г.
Ведущая организация: ГОУ ВПО «Пятигорская государственная Фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию»
Защита диссертационной работы состоится 18 марта 2008 г в ч на заседании диссертационного совета Д 208.068.01 при ГОУ ВПО «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию», по адресу: 614990, г. Пермь, ГСП-277, ул. Ленина, 48, e-mail: [email protected] факс: 2-12-94-76
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию», по адресу: 614070, г. Пермь, ул. Крупской, 46
Автореферат разослан « » февраля 2008 г
Ученый секретарь
диссертационного совета Д 208.068.01, к.ф.н., доцент Метелева Е.В.
Актуальность темы. В настоящее время внимание исследователей привлекают азотсодержащие гетероциклические системы, особенно содержащие несколько различных гетероатомов, которые могут рассматриваться, как исходные вещества для построения новых биологически активных соединений. В этом плане, представляют интерес 1,4-бензоксазиноны, которые находят применение в органическом синтезе, как удобные для модификации синтоны с кольчато-цепным енаминокарбонильным звеном. Данные соединения можно так же использовать для построения разнообразных аннелированных гетероциклических систем на основе оксалильных производных. Анализ литературных данных по химии и биологической активности бензоксазинонов показывает, что как химические свойства, так и биологическая активность соединений этого ряда в данный момент привлекает возрастающее внимание ученых, о чем свидетельствует большое количество статей на эту тему.
Продолжая синтез потенциально биологически активных соединений, представляло интерес на основании реакции эфиров ароилпировиноградных кислот с различными замещенными о-аминофенолами осуществить синтез 3-ацилметилен-1,4-бензоксазин-2-онов, изучить их строение, исследовать их свойства и установить, каким образом заместители в положении 6 и 7 гетероциклической системы и в ароилиденовом остатке влияют на химические свойства и биологическую активность полученных веществ.
Цель работы. Целью исследования является синтез новых 6(7)-замещенных 3-ацилметилен-1,4-бензоксазин-2-онов и их производных, обладающих противомикробной, противовоспалительной и анальгетической активностью, а так же соединений, оказывающих влияние на свертывающую систему крови.
Задачи исследования. Для достижения намеченной цели необходимо было решить следующие задачи:
1. Осуществить синтез 6(7)-замещенных 3-ацилметилен-1,4-бензоксазин-2-онов реакцией 4-метил-, 4-хлор-, 4-этилсульфонил-, 5-метил-, 5-нитро-о-аминофенолов с эфирами ацилпировиноградных кислот.
2. На основе реакций оксазинонов с нуклеофильными и электрофильными реагентами разработать методы синтеза ряда их производных.
3. Выявить среди полученных веществ соединения с противомикробной, противовоспалительной и анальгетической активностью, а так же соединения, оказывающие влияние на свертывающую систему крови.
Научная новизна работы. Изучена реакция эфиров ацилпировиноградных кислот с замещенными о- и м- аминофенолами. В случае взаимодействия метиловых эфиров ацилпировиноградных кислот с замещенными o-аминофенолами образуются 6(7)-замещенные 3-ацилметилен-1,4-бензоксазин-2-оны. При взаимодействии метиловых эфиров ароилпировиноградных кислот с м-аминофенолом образуются 2-ароилметилен-6-гидрокси-2,3-дигидроиндол-3-оны. При использовании в качестве субстрата -кетоглутаровой кислоты, в реакции ее с о-аминофенолами образуются 6-замещенные-3-(2-карбоксиэтил)-1,4-бензоксазин-2-оны, которые имеют структуру с эндо-азометиновой двойной связью.
С целью изучения свойств полученных соединений, а так же синтеза новых биологически активных соединений, нами было изучено взаимодействие бензоксазинонов с гидразином, с фенилизоцианатом, бутиламином, п-толуидином и оксалилхлоридом. В случае с гидразин гидратом и п-толуидином образуются соответствующие хиноксалин-2-оны. В случае с оксалилхлоридом - образуются 3-бензоил-8-этилсульфонил-2,4-дигидро-1Н-пирроло[2,1-c][1,4]бензоксазин-1,2,4-трионы, которые легко присоединяют воду с образованием 3-бензоил-8-этилсульфонил-2,3а-дигидрокси-3а,4-дигидро-1Н-пирроло[2,1-с][1,4]бензоксазин-1,4-дионов. Реакция метиловых эфиров ацилпировиноградных кислот с 2-амино-3-гидроксипиридином приводит к конденсированной гетероциклической системе 3-ацилметилен-пиридино[2,3-b]-1,4-оксазин-2-она. Установлено, что при взаимодействии 6-замещенных 1,4-бензоксазин-2-онов с фенилизоцианатом образуются 3-ароил-7-метил-3,4-дигидро-4-фениламинокарбонил-1,4-бензоксазин-2-оны. Найдено, что при взаимодействии 7-метил-3-ацилметилен-1,4-бензоксазин-2-она с бутиламином образуется 3-(2-бутилиминопропилен)-7-метил-1,4-бензоксазин-2-он. На основании данных ЯМР 1Н, ИК-спектроскопии, и масс–спектрометрии установлена структура и выявлены особенности строения полученных соединений. Среди испытанных соединений обнаружены вещества, обладающие антимикробной, противовоспалительной активностью, так же влияющие на свертывающую систему крови.
Практическая ценность. Разработаны методы препаративного синтеза 7-замещенных-3-ароил-1,4-бензоксазин-2-онов, 6-замещенных-3-ароил-1,4-бензоксазин-2-онов, 2-ароилметилен-6-гидрокси-2,3-дигидроиндол-3-онов, 6-замещенных-3-(2-карбоксиэтил)-1,4-бензоксазин-2-онов, 3-бензоил-8-этилсульфонил-2,4-дигидро-1Н-пирроло-[2,1-с]-1,4-бензоксазин-1,2,4-трионов, 6(7)-замещенных-3-(2-фенил-2-п-толилимино-этилиден)-3,4-дигидро-бензо-1,4-оксазин-2-онов, 6(7)-бензо-1,4-оксазин-2-онов, 3-(2-(п-бромфенил)-2-оксоэтилиден)-3,4-дигидро-4-фениламинокарбонил-бензо-1,4-оксазин-2-онов, 7-замещенных-3-(2-бутиламин-2-м-нитрофенил)-3,4-дигидро-1,4-бензоксазин-2-онов.
Публикации. По материалам диссертации опубликовано две работы в центральной печати, две статьи в сборниках и 6 тезисов докладов на конференциях различного уровня.
Апробация. Результаты работы доложены на 70-ой юбилейной итоговой Республиканской научной конференции студентов и молодых ученых с международным участием «Вопросы теоретической и практической медицины» (Уфа, 2005), на Всероссийской конференции «Техническая химия. Достижения и перспективы» (Пермь, 2006), на 5-ой научной школе-конференции по органической химии (Казань, 2005) и др.
Структура и объем диссертации. Диссертационная работа общим числом 132 страницы машинописного текста состоит из введения, обзора литературы, обсуждения результатов собственных исследований, экспериментальной части, биологической части, приложения и выводов, содержит 30 таблиц. Список литературы включает 88 наименований работ отечественных и зарубежных авторов.
Основные положения, выносимые на защиту.
- Результаты исследования взаимодействия эфиров ацилпировиноградных кислот с замещенными о- и м- аминофенолами.
- Установление структуры полученных соединений на основании данных ИК, ЯМР 1Н-спектроскопии и масс-спектрометрии.
- Изучение химических свойств полученных соединений.
- Биологическая активность полученных соединений.
Основное содержание диссертации
1. Взаимодействие эфиров ацилпировиноградных кислот с о- и м- аминофенолами
B результате реакции метиловых эфиров ацилпировиноградных кислот с o-аминофенолом при кратковременном кипячении эквимолярных количеств исходных реагентов в уксусной кислоте независимо от характера заместителя в эфире образуются 3-ацилметилен-1,4-бензоксазин-2-оны (Iа-п). Были получены как известные I(д-м, п), так и ранее неизученные I(а-г, н, о) соединения:
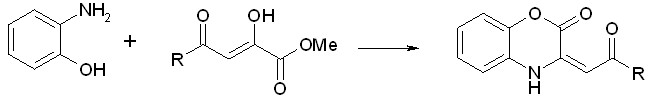
I(а-п)
R= 3-метил-5-фенил-2-тиенил(а); 2,4-диметил-5-оксазолин(б); 2,4-диметил-5-тиазолин(в); 3-BrC6H4(г); PhCH=CH2(д); 2,4,6-(CH3)3C6H3(е); C6H5(ж); 4-CH3OC6H4(з); 4-CIC6H4(и); 4-BrC6H4(к); 4-FC6H4(л); 2-тиенил(м); C6H5CH2CH2(н); 5-метил-2-фурил(о); CH3(п);
Полученные соединения (Iа-п) представляют собой желтые кристаллические вещества, растворимые в диметилформамиде и диметилсульфоксиде и не растворимые в воде.
В ИК-спектрах бензоксазинонов (Iа-п) присутствует полоса поглощения карбонильной группы в положении 2 (лактонная) при 1740-1790 см-1, полоса поглощения кетонной карбонильной группы, сопряженной с двойной С=С связью при 1620-1645 см-1, полоса поглощения NH- связи при 3200-3400 см-1.
В ЯМР 1Н-спектрах соединений (Iа-п) наблюдается сигнал CH= протона при 6,30-6,99 м.д., группа линий ароматических протонов в области 7,00 - 8,20 м.д., сигнал NH-протона при 12,00-12,95 м.д.
В масс-спектрах полученных соединений (Iа-п) присутствует пик молекулярного иона и пики фрагментных ионов, подтверждающие данную структуру.
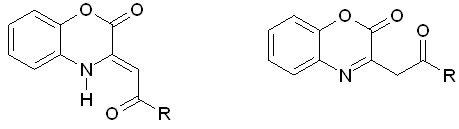
(А) (В)
Данные ЯМР 1Н-спектров свидетельствуют о том, что соединения существуют приимущественно в форме 3-ацилметиленбензоксазинонов (А). Кроме того, по положению сигнала NH-протона в ЯМР 1Н-спектре, можно сделать вывод о существовании полученных соединений (Iа-п в растворе) с внутримолекулярной водородной связью, которая образуется между атомом водорода гетероцикла и атомом кислорода карбонильной группы боковой цепи.
С целью оценки влияния взаимного расположения гидрокси и аминогрупп в молекуле аминофенола на направление реакции последних с эфирами ацилпировиноградных кислот, нами было изучено взаимодействие их с м-аминофенолом.
Нами было обнаружено, что взаимодействие метиловых эфиров ароилпировиноградных кислот с м-аминофенолом приводит к образованию 2-ароилметилен-6-гидрокси-2,3-дигидроиндол-3-онов (IIа-в). Такое протекание реакции, по-видимому, объясняется тем, что на первой стадии образуется промежуточный анил, который в условиях проведения реакции циклизуется в гетероциклическую систему 2,3-дигидроиндол-3-она:
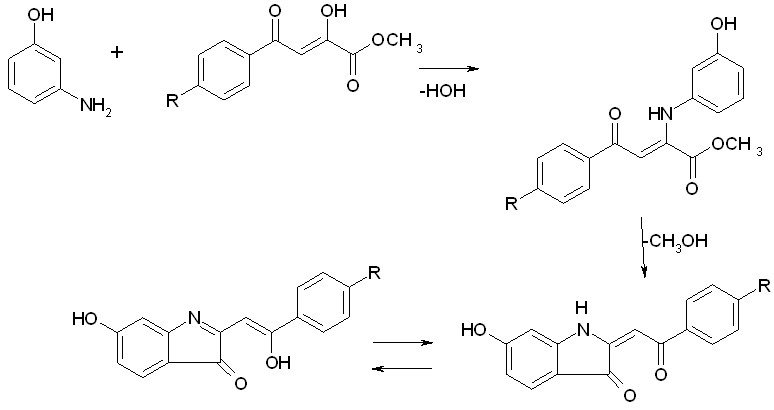
А IIа-в
R=H(а), CH3(б), CH3O(в)
В ЯМР 1Н-спектрах соединений (IIа-в) наблюдается сигнал CH= протона при 7,33-7,40 м.д., группа линий ароматических протонов в области 7,0 – 8,3 м.д., сигнал ОH-протона при 10,20-10,30 м.д., а так же сильно уширенный сигнал протона при 13,80 м.д., что свидетельствует о возможном существовании соединений в енольной форме А.
В масс-спектре полученного соединения (IIа) присутствует пик молекулярного иона с m/z 265[M]+, пики фрагментных ионов с m/z 77 [Ph]+, 105 [PhCO]+, подтверждающие данную структуру. Следует отметить, что полученные соединения (IIа-в) являются структурными изомерами соединений (Iа-п).
2. Взаимодействие эфиров ацилпировиноградных кислот с 4-замещенными 2-аминофенолами
С целью изучения влияния различных заместителей в положении 4 о-аминофенола на протекание реакции с эфирами ацилпировиноградных кислот, нами было изучено взаимодействие метиловых эфиров ароилпировиноградных кислот с 2-амино-4-этилсульфонил-, 2-амино-4-хлор-, 2-амино-4-метилфенолами и 2,4-диаминофенолом.
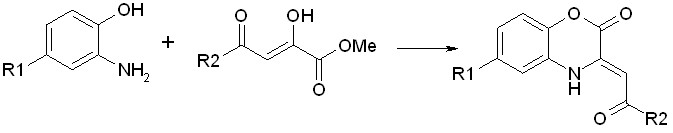
- IIIа-х, IVа-х, Vа-х, VIа, г, ж;
R1(IIIа-х) = С2Н5SO2;
R2(IIIа-х) = C6H5(а); 4-CIC6H4(б); 4-CH3C6H4(в); 4-CH3OC6H4(г); 4-FC6H4(д); 4-Br-C6H4(е); 4-NO2C6H4(ж); 3,4-(CH3O)2C6H3(з); 2,4-диметил-5-тиазолин(и); 2-фурил(к); 2-тиенил(л); 3-CH3OC6H4(м); 4-C2H5OC6H4(н); 2,4-(CI)2C6H3(о); 3-NO2C6H4(п); 4-OHC6H4(р); CH3(с); 3-Br-C6H4(т); 4-C2H2C6H4(у); 3-метил-5-фенил-2-тиенил(ф); (CH3)3C(х);
R1(IVа-х) = Cl;
R2(IVа-х) = C6H5(а); 4-CIC6H4(б); 4-CH3OC6H4(в); 3,4-(CH3O)2C6H3(г); 4-Br-C6H4(д); 4-NO2C6H4(е); 3-NO2C6H4(ж); 4-FC6H4(з); 3-CH3OC6H4(и); 2,4-диметил-5-оксазолин(к); 4-CH3C6H4(л); 4-C2H5O-C6H4(м); 3-Br-C6H4(н); 2,4-диметил-5-тиазолин(о); 2-фурил(п); 2-тиенил(р); CH3(с); 3-метил-5-фенил-2-тиенил(т); C2H2C6H4(у); C(C3H9)3(ф); CH2CH-(CH3)2(х);
R1(Vа-х) = CH3;
R2(Vа-х) = C6H5(а); 4-FC6H4(б) 3-метил-5-фенил-2-тиенил(в); 2,4-диметил-5-оксазолин(г); 4-CH3OC6H4(д); 3-CH3OC6H4(е); 4-CIC6H4(ж); 4-CH3C6H4(з); C2H4C6H4(и); 4-Br-C6H4(к); 4-NO2C6H4(л); 3-NO2C6H4(м); C2H2C6H4(н); 2,4-диметил-5-тиазолин(о); 2-фурил(п); 2-тиенил(р); CH3(с); 3,4-(CH3O)2C6H3(т); CH2CH-(CH3)2(у); 4-C2H5O-C6H4(ф); 3-Br-C6H4(х);
R1(VIа, г, ж) = NH2;
R2(VIа, г, ж) =C6H5(а); 4-CH3OC6H4(г); 4-NO2C6H4(ж);
Проведенные исследования показали, что при кратковременном кипячении эквимолярных количеств исходных реагентов в уксусной кислоте в качестве единственного продукта образуются 6-замещенные-3-ацилметилен-1,4-бензоксазин-2-оны (IIIа-х, IVа-х, Vа-х, VIа, г, ж).
По положению сигнала NH-протона в ЯМР 1Н-спектре, можно сделать вывод о существовании полученных соединений (в растворе) с внутримолекулярной водородной связью, которая образуется между атомом водорода гетероцикла и атомом кислорода карбонильной группы боковой цепи.
Следует отметить, что замена этилсульфонильной группы или атома хлора на метильный заместитель в молекуле о-аминофенола несколько облегчает протекание реакции, что, по-видимому, связано с электронодонорным характером метильной группы и некоторым повышением электронной плотности на атомах азота и кислорода в о-аминофеноле.
В реакции с 2,4-диаминофенолом повышение электронной плотности за счет присутствия второй аминогруппы приводит к понижению выходов соединений, а так же существенному осмолению реакционной смеси. Такое протекание реакции, по-видимому, объясняется присутствием в молекуле о-аминофенола третьего нуклеофильного центра, что может приводить к неоднозначному протеканию реакции, а так же расщеплению исходного эфира ацилпировиноградной кислоты.
3. Взаимодействие 3-амино-4-гидроксибензолсульфокислоты с эфирами ацилпировиноградных кислот
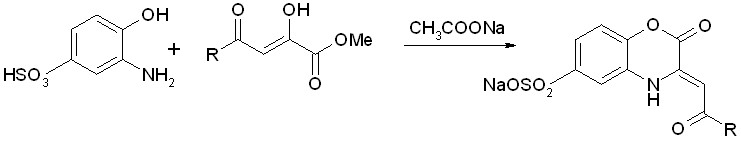
С целью получения водорастворимых бензоксазин-2-онов в воде нами было изучено взаимодействие 3-амино-4-гидроксибензолсульфокислоты с метиловыми эфирами ацилпировиноградных кислот. Проведенные исследования показали, что при кратковременном кипячении эквимолярных количеств исходных реагентов в уксусной кислоте в присутствии ацетата натрия в качестве единственного продукта образуются натриевые соли 3-ацилметилен-2-оксо-1,4-бензоксазин-6-сульфокислоты (VIIа-к):
VIIа-к
R= CH3(а); 4-CH3OC6H4(б); 4-CIC6H4(в); 2,4-(CI)2C6H3(г); 4-BrC6H4(д); 4-FC6H4(е); C2H2C6H4(ж); 3,4-(CH3O)2C6H3(з); 3-CH3OC6H4(и); 2-тиенил (к);
Полученные соединения (VIIа-к) представляют собой желтые и оранжево-красные кристаллические вещества, высокоплавкие, растворимые в воде, уксусной кислоте, диметилформамиде и диметилсульфоксиде.
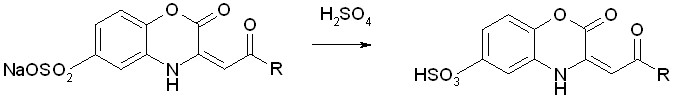
При обработке натриевых солей 3-ацилметилен-2-оксо-1,4-бензоксазин-6-сульфокислот (VIIа-з) серной кислотой образуются 3-ацилметилен-2-оксо-1,4-бензоксазин-6-сульфокислоты (VIIIа-з):
VIIа-з VIIIа-з
R= CH3(а); 4-CH3OC6H4(б); 4-CIC6H4(в); 2,4-(CI)2C6H3(г); 4-BrC6H4(д); 4-FC6H4(е); C2H2C6H4(ж); 3,4-(CH3O)2C6H3(з);
Полученные соединения (VIIIа-з) представляют собой желтые и оранжево-красные кристаллические вещества, высокоплавкие растворимые в воде, уксусной кислоте, диметилформамиде и диметилсульфоксиде. Структура полученных соединений подтверждена ИК- и ЯМР 1Н-спектрами.
4. Взаимодействие эфиров ацилпировиноградной кислоты с 5-замещенными 2-аминофенолами
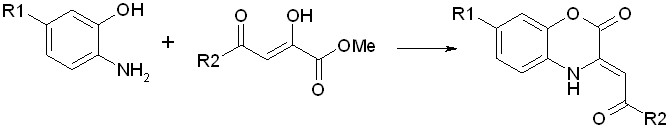
С целью оценки влияния положения заместителя в о-аминофеноле на протекание реакции с метиловыми эфирами ацилпировиноградных кислот, а так же на оценку биологической активности полученных соединений, было изучено взаимодействие эфиров ацилпировиноградных кислот с 2-амино-5-метил- и 2-амино-5-нитрофенолом:
 IXа-к, Xа-у
IXа-к, Xа-у
R1(IXа-к) = CH3;
R2(IXа-к) = 4-C6H4OH (а); CH3(б); 3,4-(CH3O)2C6H3(в); 4-CH3OC6H4(г); 2-фурил(д); 2-тиенил (е); 4-CH3C6H4 (ж); 4-C6H5 (з); 3-NO2C6H4(и); 4-NO2C6H4(к);
R1(Xа-у) = NO2;
R2(Xа-у) = OC2H5(а); 3-метил-5-фенил-2-тиенил(б); 2,4-диметил-5-оксазолин(в); 2,4-диметил-5-тиазолин(г); 4-CH3OC6H4(д); 3-CH3OC6H4(е); 4-CH3C6H4(ж); C6H5(з); 4-CIC6H4(и); 4-BrC6H4(к); 4-NO2C6H4(л); 3,4-(CH3O)2C6H3(м); 4-BrC6H4(н); C2H4C6H4(о); C2H2C6H4(п); 2-фурил(р); 2-тиенил(с); CH3(т); 5-метил-2-фурил(у);
Проведенные исследования показали, что при кратковременном кипячении эквимолярных количеств исходных реагентов в уксусной кислоте в качестве единственного продукта с хорошим выходом образуются 7-замещенные-3-ацилметилен-1,4-бензоксазин-2-оны (IXа-к, Xа-у). Структура полученных соединений подтверждена ИК- и ЯМР 1Н-спектроскопией.
Следует отметить, что присутствие метильной группы в положении 5 2-аминофенола не оказывает существенного влияния на протекание реакции по сравнению с таковыми в случае 4-метил-2-аминофенола. Присутствие заместителя в положении 7 1,4-бензоксазинового цикла так же не влияет на таутомерное равновесие соединений IX. Так же, в целом, нитро-группа в положении 5 2-аминофенола не оказывает существенного влияния на протекание реакции.
5. Взаимодействие замещенных о-аминофенолов с -кетоглутаровой кислотой
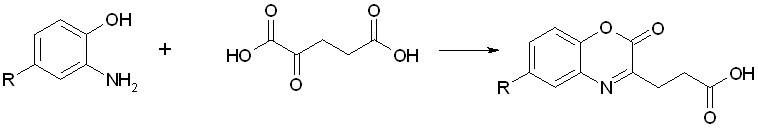
С целью изучения взаимодействия 4-замещенных о-аминофенолов с соединениями, содержащими - и,-дикарбонильную систему, нами была изучена реакция 2-амино-, 2-амино-4-метил-, 2-амино-4-хлор- и 2-амино-4-этилсульфонилфенола с таким естественным метаболитом как -кетоглутаровая кислота. Эквимолярные количества исходных реагентов растворяли в уксусной кислоте при нагревании, затем сливали и выдерживали при комнатной температуре в течение суток. Исследования показали, что в качестве единственного продукта образуются 6-замещенные 3-(2-карбоксиэтил)-1,4-бензоксазин-2-оны(XIа-г):
(XIа-г)
R= Н(в); CH3(а); CI(б); C2H5SO2(г);
Полученные соединения (XIа-г) представляют собой бесцветные кристаллические вещества, растворимые в этаноле, уксусной кислоте, диметилформамиде и диметилсульфоксиде и не растворимые в воде.
Данные ЯМР 1Н-спектров свидетельствуют о том, что соединения (XIа-г), в отличие от (I-X), имеют структуру с эндоазометиновой двойной связью (форма А), что по-видимому, объясняется наличием карбонильной группы в положении боковой цепи и невозможности вследствие этого образования внутримолекулярной водородной связи и реализации формы В:
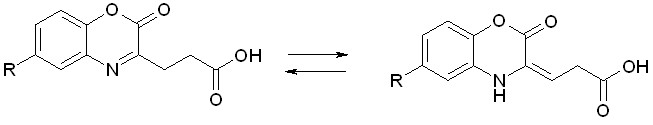
А В
Cледует отметить, что выходы об
разующихся бензоксазинонов несколько ниже, чем соединений (I-X), что по-видимому, объясняется меньшей реакционной способностью -кетоглутаровой кислоты в реакциях с о-аминофенолами.
6. Взаимодействие ароилпировиноградных кислот и их эфиров с 2-амино-3-гидроксипиридином
Продолжая синтезы потенциально биологически активных соединений, а так же с целью формирования конденсированной гетероциклической системы, содержащей в своем составе фрагмент 1,4-оксазина, нами было изучено взаимодействие 2-амино-3-гидроксипиридина с эфирами пировиноградных кислот. Исследования показали, что при кипячении исходных реагентов в уксусной кислоте происходит осмоление реакционной смеси без образования каких-либо идентифицируемых продуктов. Однако, при проведении реакции с ароилпировиноградными кислотами в тех же условиях нами были выделены 3-ацилметиленпиридино[2,3-b]-1,4-оксазин-2-оны(XIIа,б):
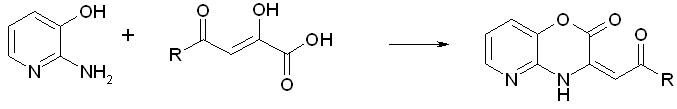
XII(а,б);
R=CH3(а), C6H5(б);
Данные спектров свидетельствуют о том, что полученные пиридино[2,3-b]-1,4-оксазин-2-оны, как и описанные ранее 3-ацилметилен-1,4-бензоксазин-2-оны, существуют в форме А (см. стр. 6) с экзометиленовой двойной связью.
7. Химические свойства 6(7)-замещенных-1,4-бензоксазин-2-онов
С целью синтеза биологически активных соединений и изучения свойств 3-ацилметилен-1,4-бензоксазин-2-онов нами было изучено взаимодействие полученных бензоксазинонов с электрофильными и нуклеофильными реагентами.
7.1. Взаимодействие с электрофильными реагентами
7.1.1. Реакция с оксалилхлоридом
С целью изучения свойств полученных соединений нами было изучено взаимодействие 6-этилсульфонилбензоксазинонов III(а,е,в,ж,г,р,о) с оксалилхлоридом. При кипячении эквимолярных количеств реагентов в абсолютном толуоле в течение двух часов в качестве единственного продукта образуются 3-ароил-8-этилсульфонил-2,4-дигидро-1Н-пирроло[2,1-c][1,4]бензоксазин-1,2,4-трионы(XIIIа-ж):
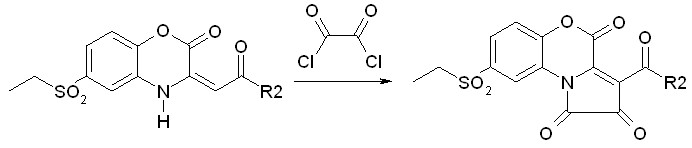
III(а,е,в,ж,г,р,о) XIII(а-ж)
R2=C6H5(а); 4-Br-C6H4(б); 4-CH3C6H4(в); 4-NO2C6H4(г); 3-CH3OC6H4(д); 4-HOC6H4(е); 2,4-(CI)2C6H3(ж);
Так как соединения, аналогичные соединениям (XIIIа-ж), судя по литературным данным, легко присоединяют ОН-нуклеофилы, нами было изучено их взаимодействие с водой:
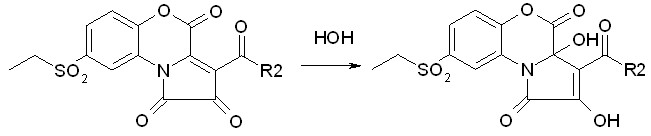 XIII(а-ж) XIV(а-ж)
XIII(а-ж) XIV(а-ж)
R2=C6H5(а); 4-Br-C6H4(б); 4-CH3C6H4(в); 4-NO2C6H4(г); 3-CH3OC6H4(д); 4-HOC6H4(е); 2,4-(CI)2C6H3(ж);
Было установлено, что соединения XIII(а-ж) реагируют с водой, в соотношении 1:1, при нагревании и осторожном сливании растворов реагентов практически мгновенно, образуя с высоким выходом продукты присоединения воды по активированной кратной связи в положении 3 3-бензоил-8-этилсульфонил-2,3а-дигидрокси-3а,4-дигидро-1Н-пирроло[2,1-с][1,4]бензоксазин-1,4-дионы (XIVа-ж).
Полученные соединения (XIVа-ж) представляют собой желтые высокоплавкие кристаллические вещества, плавящиеся с разложением, легкорастворимые в ДМФА и ДМСО, труднорастворимые в обычных апротонных органических растворителях.
7.1.2. Реакция с фенилизоцианатом
Проведенные исследования показали, что при кипячении эквивалентных количеств исходных реагентов в 10мл диоксана образуются 3-ароилметилен-7-метил-3,4-дигидро-4-фениламинокарбонил-1,4-бензоксазин-2-оны XVа-б:
. 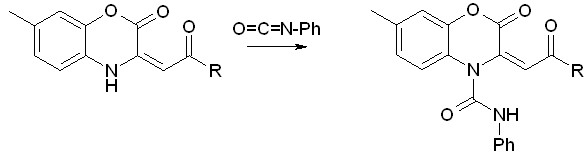
XVа-б
R = 4-OHC6H4 (а); 4-Br-C6H4(б);
Структура полученных соединений подтверждена ИК- и ЯМР 1Н-спектрами.
7.2. Взаимодействие 3-ацилметилен-1,4-бензоксазин-2-онов с мононуклеофильными реагентами
7.2.1. Реакция с пара-толуидином
Исследования показали, что для проведения реакции может быть использовано два метода:
1) сплавление эквимолярных количеств исходных реагентов в течение 15-20 мин до окончания газовыделения при температуре 190-200°С (метод А);
2) кипячение эквимолярных количеств исходных реагентов в уксусной кислоте в течение 5 часов (метод Б).
Независимо от используемого метода качестве единственного продукта образуются 1-N-п-толил-6-этилсульфонил-3-ацилметилен-3,4-дигидрохиноксалин-2-оны (XVIа,б):
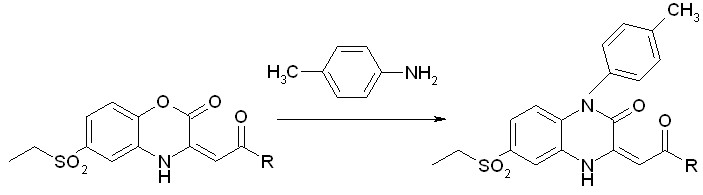
IIIс, IIIн XVIа-б
R= CH3(а); 4-C2H5OC6H4(б)
Данные спектров свидетельствуют, что полученные хиноксалины существуют в енаминной форме с экзоэтиленовой двойной связью, которая как и в случае бензоксазинонов стабилизируется внутримолекулярной водородной связью.
7.2.2. Реакция с бутиламином
Нами была изучена реакция 7-метил-3-ацетилметилен-1,4-бензоксазин-2-она с бутиламином. Найдено, что при выдерживании эквимолярных количеств исходных реагентов при температуре 150-160°С в течение 30 мин. до окончания газовыделения образуется 3-(2-бутилиминопропилен)-7-метил-1,4-бензоксазин-2-он XVII:
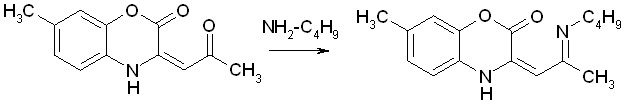
XVII
Перенос реакционного центра на карбонильную группу боковой цепи объясняется, по-видимому, тем, что ацетильная карбонильная группа является более реакционноспособной по сравнению с лактонным карбонилом и карбонильной группой ароильного заместителя, так как она является более стерически доступной и не сопряженной с ароматическим или гетероциклическим заместителем.
7.3. Взаимодействие с бинуклеофильными реагентами
Реакция с гидразин гидратом
Нами было изучено взаимодействие 6(7)-замещенных 1,4-бензоксазин-2-онов с гидразином с целью изучения влияния на ход реакции заместителей в ароматическом кольце и боковой цепи. Исследования показали, что для проведения реакции может быть использовано два метода:
1) при выдерживании исходных бензоксазин-2-онов (IIIа, IIIз, Xи, IVо) с двойным избытком гидразина в течение получаса при температуре 190-200°С до окончания газообразования (метод А);
2) при кипячении исходных бензоксазин-2-онов с двойным избытком гидразина в среде уксусной кислоты в течение 3-5 часов (метод Б).
Независимо от используемого метода в качестве единственного продукта образуются 6(7)-замещенные-1-амино-3-ароилметилен-1,4-хиноксалин-2-оны.
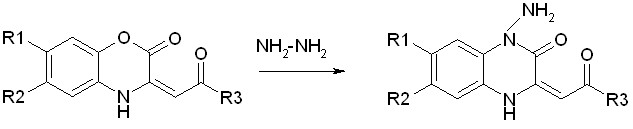
XVIIIа-г
R1(а)= Н; R2= SO2C2H5; R3= C6H5;
R1(б)= Н; R2= SO2C2H5; R3= 3,4-(CH3O)2C6H3;
R1(в)= NO2 ;R2= Н; R3= 4-CIC6H4(в);
R1(г)= Н; R2= CI; R3= 5-фенил-3-тиазолин;
По-видимому, такое протекание реакции объясняется тем, что гидразин атакует лактонную карбонильную группу в положении 2 гетероцикла с последующей рециклизацией в гетероциклическую систему 1-амино-3-ароилметилен-1,4-хиноксалина.
8. Биологическая активность полученных соединений
Известно, что замещенные 1,4-бензоксазиноны широко используются в синтетической органической химии, а ряд этих соединений и их производных обладает различными видами биологической активности.
В связи с этим представляло интерес исследовать противомикробную, анальгетическую, противовоспалительную активность полученных соединений и изучить их влияние на свертывающую систему крови. Всего фармакологическому скринингу было подвергнуто 90 полученных соединений.
8.1. Противомикробная активность
Антимикробная активность изучена на кафедре микробиологии Пермской государственной фармацевтической академии доцентом Ворониной Э.В., под руководством зав. каф. д.ф.н. Одеговой Т.Ф.
Противомикробную активность определяли методом последовательных разведений раствора исследуемого соединения в мясопептонном бульоне (МПБ) и изучали активность по отношению к St. aureus и E. сoli..
Антимикробная активность была исследована у 90 соединений. Исследования показали, что в ряду 6-замещенных 3-ароилиден-1,4-бензоксазин-2-онов наблюдается противомикробное действие, минимальная ингибирующая концентрация (МИК) варьирует от 125 до 1000 (мкг/мл). Характерно, что при введении атома фтора в фенацилиденовый остаток, наблюдается значительное повышение активности, как в отношении золотистого стафилококка, так и в отношении кишечной палочки (МИК 125мкг/мл в отношении золотистого стафилококка и 250мкг/мл в отношении кишечной палочки). В целом, активность изученных соединений сравнима с противомикробным действием дихлорида ртути, этакридина лактата и хлорамина (минимальная ингибирующая концентрация 500 мкг/мл в отношении золотистого стафилококка и 250 мкг/мл в отношении кишечной палочки).
Найдено соединение IIIд с выраженным антимикробным действием, которое можно рекомендовать для углубленных исследований.
8.2. Противовоспалительная активность
Противовоспалительная активность изучена на кафедре патологии и физиологии Пермской государственной фармацевтической академии под руководством проф. Сыропятова Б.Я.
Были проведены исследования на противовоспалительную активность 10 соединений ряда замещенных 3-ацилметилен-1,4-бензоксазин-2-онов. Опыты выполнены на белых беспородных крысах обоего пола массой 180-220г. Исследуемые соединения вводили в дозе 50 мг/кг внутрибрюшинно за 1 час до моделирования каррагенинового воспаления. Каррагениновый отек вызывали субплантарным введением 0,1 мл 1% раствора каррагенина. Воспалительный отек регистрировали онкометрически через 1, 3 и 5 часов после введения каррагенина. Контрольным животным вводили эквиобъемное количество растворителя. Полученные данные приведены в таблице 1.
Проведенные исследования показали, что соединения Vа, IVа, IVб, IIIж, IIIг, Xб оказали высокую противовоспалительную активность, поэтому представляют интерес для дальнейших исследований.
8.3. Анальгетическая активность
Изучение анальгетической активности проведено на кафедре физиологии и патологии Пермской государственной фармацевтической академии под руководством проф. Сыропятова Б.Я. Исследовано 13 соединений. Анальгетическая активность изучалась на беспородных белых мышах весом от 16-22г методом термического раздражения («горячая пластинка»). Исследуемые соединения вводили в дозе 50 мг/кг внутрибрюшинно в виде взвеси в 2% крахмальной слизи за 30 минут до помещения животного на металлическую пластинку, нагретую до 54°С. Показателем болевой чувствительности служила длительность пребывания животного на горячей пластинке до наступления оборонительного рефлекса (облизывание лапок, подскакивание), измеряемого в секундах. Препарат сравнения анальгин в дозе 50 мг/кг при внутрибрюшинном введении. Наблюдения проводили через 30 мин, 1, 2 и 3 часа. Как видно из таблицы 2, соединения IVа и Xз проявили анальгетическое действие, сравнимое с действием эталона сравнения.
8.4.Исследования влияния соединений на свертывающую систему крови
Исследования влияния соединений на свертывающую систему крови проведены на кафедре физиологии и патологии Пермской государственной фармацевтической академии под руководством проф. Сыропятова Б.Я.
Исследования проведены с помощью коагулометра «Минилаб 701». Для исследования использовали цитратную (3,8%) кровь (9:1). Влияние соединений на свертывание крови изучали в одинаковой концентрации (1 мг/мл). В качестве эталона сравнения гемостатической активности использовали этамзилат, который испытывали в той же концентрации – 1 мг/мл крови. Исследовано 18 соединений, полученные данные приведены в таблице 3. Как видно из таблицы, большинство исследованных соединений проявляют гемостатическое действие, поэтому можно рекомендовать данный ряд для поиска соединений с гемостатической активностью. Наиболее высокую активность проявили соединения VIIб, VIIе, VIIж, VIIз, VIIк, VIIIе, VIIIз. Эталон сравнения этамзилат ускоряет свертывание крови в той же концентрации только на 15,2%.
Таблица 1. Исследование соединений на противовоспалительную активность
| Соединение | % прироста стопы | % торможения | ||||
| 1ч | 3ч | 5ч | 1ч | 3ч | 5ч | |
| Vа IVа IIIа IVб IIIг Контроль IIIж Xб Xв IVг Vж Контроль Натриевая соль мефенамовой кислоты Диклофенак | 16,1± 3,08 P>0,05 13,7 ± 3,16 P>0,05 17,0 ± 2,97 P>0,05 16,1 ± 3,90 P>0,05 18,9 ± 1,71 P>0,05 18,3± 4,41 14,3 ± 3,04 P>0,05 17,0 ± 0,60 P>0,05 19,4 ± 6,27 P>0,05 24,4 ± 3,42 P>0,05 28,2 ± 5,33 P>0,05 20,1 ± 1,16 14,7 ± 2,64 P<0,01 15,4 ± 2,80 P>0,05 | 25,8± 2,99 P<0,001 21,1± 6,75 P<0,001 75,9± 3,03 P<0,01 25,6 ± 4,43 P<0,001 28,5 ± 2,47 P<0,001 52,8 ± 2,77 P>0,05 28,5 ± 2,47 P<0,001 39,6 ± 9,49 P<0,05 50,6 ± 5,29 P>0,05 48,8 ± 6,48 P>0,05 46,9 ± 1,53 P<0,02 60,4 ±3,53 P<0,05 23,6 ± 2,93 P<0,05 17,8 ± 4,30 P<0,001 | 29,1 ± 0,90 P<0,001 24,1 ± 3,03 P<0,001 75,6 ± 4,43 P>0,05 18,9 ± 1,10 P<0,001 35,3 ± 5,63 P<0,001 59,4 ± 0,57 P<0,001 37,1 ± 2,45 P<0,001 42,7 ± 7,87 P<0,002 62,8 ± 3,65 P<0,01 57,9 ± 7,10 P<0,05 56,0 ± 4,00 P<0,001 76,8 ± 2,16 P<0,05 31,6 ± 4,77 P<0,001 31,9 ± 4,70 P<0,001 | 12,0 25,1 7,1 12,0 0 - 28,8 15,4 3,5 0 0 - 14,9 40,1 | 51,1 60,0 0 51,5 46,0 - 52,8 34,4 16,2 19,2 22,3 - 42,3 62,1 | 51,0 59,4 0 68,2 40,6 - 51,7 44,4 18,2 24,6 27,1 - 38,8 68,8 |
Таблица 2. Исследование соединений на анальгетическую активность
| Соединение | Контроль | Рефлекс ч/з 30 мин | Рефлекс ч/з 1 час | Рефлекс ч/з 2 часа | Рефлекс ч/з 3 часа |
| Vа | 7,1 ± 0,59 | 8,7 ± 0,56 Р > 0,05 22,5% | 10,6 ± 0,98 Р < 0,05 49,3% | 10,6 ± 0,76 Р < 0,002 49,3% | 9,9 ± 0,80 Р < 0,02 39,4% |
| IVа | 7,4 ± 0,62 | 7,6 ± 0,44 Р > 0,05 2,7% | 11,5 ± 1,18 Р < 0,01 55,4% | 11,5 ± 0,82 Р < 0,001 55,4% | 11,9 ± 0,66 Р < 0,002 60,8% |
| IVб | 11,2 ± 0,66 | 12,5 ± 0,45 Р > 0,05 11,6% | 14,6 ± 1,04 Р < 0,02 30,4% | 15,6 ± 0,78 Р < 0,001 39,3% | 13,1 ± 0,81 Р > 0,05 17,0% |
| Xз | 9,0 ± 0,52 | 14,6 ± 2,42 Р > 0,05 62,2% | 10,9 ± 0,82 Р > 0,05 21,1% | 14,9 ± 1,42 Р < 0,002 65,6% | 13,1 ± 1,39 Р < 0,02 45,6% |
| IIIж | 9,2 ± 0,56 | 12,6 ± 1,09 Р > 0,02 37,0% | 11,7 ± 0,79 Р < 0,02 27,2% | 13,3 ± 1,42 Р < 0,02 44,6% | 10,7 ± 0,35 Р < 0,05 16,3% |
| Анальгин | 10,6 ± 1,51 | 12,6 ± 1,19 Р< 0,05 | 20,8 ± 2,24 Р< 0,05 | 25,8±2,88 Р< 0,05 | 30,3 ± 4,01 Р < 0,05 |
Таблица 3. Исследования соединений на свертывающую систему крови
| № | Время свертывания,сек; контроль | Время свертывания,сек; опыт | % изменения свертываемости | Р |
| VIIа VIIб VIIв VIIг VIIд VIIе VIIж VIIз VIIи VIIк VIIIа VIIIб VIIIв VIIIг VIIIд VIIIе VIIIж VIIIз | 38,9±2,35 45,1±2,10 45,6±2,11 48,6±3,26 54,7±4,55 51,1±3,26 44,7±1,22 48±2,03 57,5±4,47 61,0±3,23 92,3±2,04 95,1±3,82 80,2±6,50 86,9±3,91 36,4±1,44 35,2±2,34 36,1±1,83 33,0±0,76 | 36,4±2,12 40,5±3,06 47,5±3,38 56,5±4,25 55,1±5,56 46,3±3,34 39,8±1,47 42,3±1,16 55,2±5,91 53,2±2,55 83,7±4,75 88,4±3,49 76,9±5,66 77,7±4,48 38,2±2,19 31,5±1,19 38,0±1,27 24,9±0,51 | +6,4 +10,2 -4,2 -16,3 -0,7 +10,4 +11,0 +12,4 +4,0 +14,7 +9,3 +7,0 +4,1 +10,6 -4,9 +10,5 -5,3 +24,5 | >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 <0,05 <0,05 >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 >0,05 <0,01 |
| Этамзилат | 28,9± | 24,5±0,94 | +15,2 | <0,01 |
ВЫВОДЫ
1. Установлено, что при взаимодействии метиловых эфиров ацилпировиноградных кислот с замещенными аминофенолами образуются 6-(7)-замещенные 3-ацилметилен-1,4-бензоксазин-2-оны, существующие в форме с экзоэтиленовой двойной связью.
2. Реакция метиловых эфиров ацилпировиноградных кислот с м-аминофенолом приводит к образованию 2-ароилметилен-6-гидрокси-2,3-дигидроиндол-3-онов, являющихся структурными изомерами бензоксазинонов.
3. Установлено, что при взаимодействии 2-аминофенола, 2-амино-4-метилфенола, 2-амино-4-хлорфенола и 2-амино-4-этилсульфонилфенола с -кетоглутаровой кислотой образуются 6-замещенные 3-(2-карбоксиэтил)-1,4-бензоксазин-2-оны, существующие в форме с эндометиленовой двойной связью.
4. Реакция метиловых эфиров ацилпировиноградных кислот с 2-амино-3-гидроксипиридином приводит к конденсированной гетероциклической системе 3-ацилметиленпиридино[2,3-b]-1,4-оксазин-2-она.
5. Взаимодействие 3-ацилметилен-1,4-бензоксазин-2-онов с оксалил хлоридом, протекает с образованием 3-ароил-8-этилсульфонил-2,4-дигидро-1Н-пирроло[2,1-c][1,4]бензоксазин-1,2,4-трионов, которые легко присоединяют воду, превращаясь в 3-бензоил-8-этилсульфонил-2,3а-дигидрокси-3а,4-дигидро-1Н-пирроло[2,1-с][1,4]бензоксазин-1,4-дионы.
6. Установлено, что при взаимодействии 6-замещенных 1,4-бензоксазин-2-онов с фенилизоцианатом образуются 3-ароил-7-метил-3,4-дигидро-4-фениламинокарбонил-1,4-бензоксазин-2-оны.
7. Обнаружено, что при взаимодействии 6(7)-замещенных 1,4-бензоксазин-2-онов с гидразином приводит к 1-амино-3-ароилметилен-6(7)-замещенным 1,4-хиноксалин-2-онам, а при взаимодействии с п-толуидином образуются соответствующие 1-N-толил-3-ацилметилен-3,4-дигидро-хиноксалин-2-оны.
8. Установлено, что при взаимодействии 7-метил-3-ацилметилен-1,4-бензоксазин-2-она с бутиламином образуется 3-(2-бутилиминопропилен)-7-метил-1,4-бензоксазин-2-он.
9. Получено 90 новых соединений, строение которых подтверждено данными ЯМР 1Н, ИК и масс-спектроскопии, из которых 90 исследовано на антимикробную, 10 на противовоспалительную, 13 на анальгетическую активность, так же изучено влияние 18-и полученных соединений на свертывающую систему крови.
10. На основании проведенных исследований и анализа данных структура - активность выделены соединения для дальнейшего углубленного исследования.
Основные результаты исследований отражены в работах:
- Гейн, В.Л. Синтез и биологическая активность 6-замещенных 3-ароил-1,4-бензоксазин-2-онов / В.Л. Гейн, Н.А. Рассудихина, Э.В. Воронина // Хим. – фармац. журн. - 2006. – Т. 40, № 10. – С. 77.
- Гейн, В.Л. Взаимодействие замещенных о-аминофенолов с эфирами ацилпировиноградных кислот и -кетоглутаровой кислотой. Протовомикробная активность полученных соединений / В.Л. Гейн, Н.А. Рассудихина, Н.В. Шепелина, М.И. Вахрин, Е.Б.Бабушкина, Э.В. Воронина // Унивнрситетская наука: взгляд в будущее. Сборник трудов юбилейной научной конференции КГМУ и сессии Центр.- Чернозем. Науч. Центра РАМН, посвященная 70-летию КГМУ. Том II. – Курск. - 2005. – С.260.
- Рассудихина Н.А. Синтез 6-замещенных 3-ароилиден-1,4-бензоксазин-2-онов / Н.А. Рассудихина, В.Л. Гейн // Тезисы докладов 70-й юбилейной итоговой Республиканской научной конференции студентов и молодых ученых с международным участием «Вопросы теоретической и практической медицины». – Уфа, 2005. - С.57
- Гейн, В.Л. Синтез и биологическая активность 6(7)-замещенных 3-ацилметилен-1,4-бензоксазин-2-онов / В.Л. Гейн, Н.А. Рассудихина, Н.В. Данилова, Б.Я. Сыропятов, Л.Н. Маркова, М.И. Вахрин, Е.Б.Бабушкина // Вестник ПГФА. – 2007. - №2. – С.31-33.
- Гейн, В.Л. Синтез 2-ароилметилен-6-гидрокси-2,3-дигидроиндол-3-онов / В.Л. Гейн, А.В. Деменева, Н.А. Рассудихина, М.И. Вахрин // Журн. орг. химии. - 2006. – Т. 42, №4. – С.634-635.
- Гейн, В.Л. Взаимодействие замещенных о-аминофенолов с эфирами ацилпировиноградных кислот и -кетоглутаровой кислотой / В.Л. Гейн, Н.А. Рассудихина, Н.В. Шепелина, М.И. Вахрин, Е.Б.Бабушкина, Э.В. Воронина // Тезисы докладов научной конференции. – Саратов. – 2007. – С.80-81.
- Рассудихина Н.А. Взаимодействие эфиров ацилпировиноградных кислот с аминофенолами / Н.А. Рассудихина, А.В. Деменева, Л.И. Варкентин, М.И. Вахрин, В.Л. Гейн // Тезисы докладов всероссийской конференции «Техническая химия. Достижения и перспективы». – Пермь. – 2006. – Том 1. – С.175-177.
- Рассудихина Н.А. Синтез и биологическая активность 7-замещенных 3-ароилиден-1,4-бензоксазин-2-онов / Н.А. Рассудихина, В.Л. Гейн // Разработка, исследование и маркетинг новой фармацевтической продукции. Сборник научных трудов. – Пятигорск, 2005. – С.404-405.
- Шепелина Н.В. Синтез и свойства 7-замещенных 3-ароилиден-1,4-бензоксазин-2-онов / Н.В. Шепелина, Н.А. Рассудихина, Э.В. Воронина, В.Л. Гейн // Вестник ПГФА. – 2006. - №1. – С.52.
- Рассудихина Н.А. Синтез и биологическая активность 6(7)-замещенных 3-ацилметилен-1,4-бензоксазин-2-онов / Н.А. Рассудихина, В.Л. Гейн, Н.В. Данилова, Б.Я. Сыропятов, Л.Н. Маркова, М.И. Вахрин, Е.Б.Бабушкина // Материалы Российской научно-практической конференции, посвященной 70-летию ПГФА. – Пермь. - 2007. – С.98-100.

