Исследования по стандартизации измельченного лекарственного растительного сырья и его водных извлечений
На правах рукописи
БЕСЕДИНА НАДЕЖДА АЛЕКСАНДРОВНА
ИССЛЕДОВАНИЯ ПО СТАНДАРТИЗАЦИИ ИЗМЕЛЬЧЕННОГО ЛЕКАРСТВЕННОГО РАСТИТЕЛЬНОГО СЫРЬЯ И ЕГО ВОДНЫХ ИЗВЛЕЧЕНИЙ
15.00.02- ФАРМАЦЕВТИЧЕСКАЯ ХИМИЯ, ФАРМАКОГНОЗИЯ
Автореферат диссертации на соискание ученой степени
кандидата фармацевтических наук
Москва-2007
Диссертационная работа выполнена в ГОУ ВПО Московская медицинская академия им. И.М. Сеченова Росздрава
Научный руководитель: доктор фармацевтических наук
Алла Анатольевна Сорокина
Официальные оппоненты:
- доктор фармацевтических наук,
заслуженный деятель науки РФ профессор
ГОУ ВПО «Пятигорская государственная фармацевтическая академия»
Дарья Алексеевна Муравьева
- доктор фармацевтических наук, профессор
Всероссийского научно-исследовательского института лекарственных
и ароматических растений РАСХН
Тамара Дарижаповна Даргаева
Ведущая организация:
ГОУ ВПО «Ярославская государственная медицинская академия»
Защита состоится «12» ноября 2007г. в 14 часов на заседании диссертационного совета Д.208.040.09 при ГОУ ВПО Московская медицинская академия им. И.М. Сеченова Росздрава по адресу:
121998, г. Москва, Никитский бульвар, д.13.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО
ММА им. И.И. Сеченова по адресу:117418 Москва, Нахимовский пр-т, 49.
Автореферат разослан «02» октября 2007г
| Ученый секретарь диссертационного совета Д.208.040.09 | ||
| доктор фармацевтических наук, профессор |  | Наталья Петровна Садчикова |
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Для изготовления водных извлечений используют все морфологические группы сырья: цветки, листья, травы, почки, коры, плоды, семена и подземные органы. Большая часть из них выпускается в фильтр-пакетах (ФП), в которых размеры частиц сырья не превышают 2 мм. Дисперсность сырья в фильтр-пакетах находится в широких пределах от 2 мм до 0,16 мм и менее. Сырье с такой степенью дисперсности еще недостаточно хорошо изучено относительно выхода биологически активных веществ, их концентраций в водных извлечениях. Переход БАВ из сырья в водные извлечения определятся наряду с размером частиц так же морфологическими особенностями сырья и химическим составом. В нормативной документации, регламентирующей изготовление водных извлечений (ГФ XI) отсутствуют какие-либо указания на использование лекарственного растительного сырья в ФП для получения настоев и отваров. Поэтому представляет интерес изучение порошкованного лекарственного растительного сырья из различных морфологических групп и различных по химическому составу и водных извлечений, получаемых из него.
Цель и задачи исследования. Целью настоящего исследования является фармакогностическое изучение порошкованного лекарственного растительного сырья, используемого для изготовления фильтр-пакетов и обоснование системы стандартизации сырья и водных извлечений получаемых из фильтр-пакетов.
Задачи исследования:
- Провести анализ современного состояния нормативной документации, методик получения, стандартизации настоев и отваров из порошкованного ЛРС.
- Разработать характеристики подлинности и показатели качества настоев и отваров, получаемых из фильр-пакетов.
- Изучить влияние размера частиц, условий настаивания порошкованного сырья, выпускаемого в фильтр-пакетах на качество настоев и отваров.
- С использованием современных физико-химических методов анализа провести углубленное изучение химического состава порошкованого ЛРС и водных извлечений.
- Разработать требования к качеству водных извлечений из порошкованного ЛРС, фасованного в фильтр-пакеты.
Научная новизна. Научная новизна исследования заключается в комплексном изучении водных извлечений, из сырья, фасованного в фильтр-пакеты, во взаимосвязи с измельченностью и условиями настаивания.
Изучено влияние измельченности на качество получаемых водных извлечений для 30 видов ЛРС, различных морфологических групп и фасованного в ФП. Установлены оптимальные для каждого вида размеры частиц сырья, позволяющие получать настои и отвары с более высоким содержанием действующих веществ. Выявлены закономерности влияния размера частиц сырья и химического состава на качество водных извлечений. Для характеристики сырья, используемого при изготовлении водных извлечений предложен показатель «Экстрактивные вещества при настаивании», регламентирующий содержание в сырье гидрофильной группы биологически активных веществ.
Практическая значимость.
- Научно обоснована возможность использования методики получения водных извлечений, приводимой в инструкции по применению в фильтр-пакетах.
- Разработан проект общей фармакопейной статьи «Определение содержания экстрактивных веществ в лекарственном растительном сырье», в котором для характеристики сырья, используемого для изготовления водных извлечений, включен показатель: Экстрактивные вещества при настаивании.
- Показана целесообразность введения регламентации в порошкованном лекарственном растительном сырье фракций, обеспечивающих максимальное содержание действующих веществ.
- Показана необходимость использования для изготовления фильтр-пакетов только обмолоченной травы.
Апробация работы. Основные результаты работы доложены на 2-ой Всероссийской научно-методической конференции «Пути и формы совершенствования фармацевтического образования», Воронеж – 20-22 апреля 2005г, на научно-практической конференции «Современные методы стандартизации и контроля качества лекарственных средств», Москва- 30-31 мая 2006г, на 3-й Всероссийской научно-методической конференции «Пути и формы совершенствования фармацевтического образования. Создание новых физиологически активных веществ», Воронеж – 22-24 марта 2007.
Связь темы диссертационной работы с планом научных работ учреждения. Диссертационная работа выполнена в соответствии с планом НИР кафедры фармакогнозии ГОУ ВПО ММА им. И.М. Сеченова по теме: «Фармакогностическое изучение лекарственного растительного сырья, лекарственных сборов, лекарственных форм из сырья и разработка методов их стандартизации с учетом антропогенных факторов, оценки качества и сертификации» (код темы 04.07.093, проблема № 1006 АМН РФ, Государственный регистрационный номер: 01200110546).
Публикации. По диссертации опубликовано 15 печатных работ в научных журналах, сборниках международных конференций и научных трудах.
Положения, выносимые на защиту по итогам исследований ЛРС, фасованного в фильтр-пакеты:
- Характеристики подлинности и показатели качества порошкованного ЛРС.
- Результаты исследования измельченности ЛРС, технологии изготовления настоев и отваров и влияния бумаги на качество получаемых извлечений.
- Данные по антиокислительной активности ЛРС.
- Изучение микробиологического состояния сырья и водных извлечений из ЛРС.
Объем и структура диссертации. Диссертационная работа изложена на 174 страницах машинописного текста, состоит из 8 глав, введения, обзора литературы, экспериментальной части, выводов, списка литературы, включающего 159 источника, из них 12 на иностранных языках и приложения. Диссертация содержит 45 таблиц, 29 рисунков и 18 фотографических снимков. Полученные результаты обработаны статистически, обобщены в таблицах, выражены в соответствующих формулах, которые приведены в работе.
Объекты и методы исследования.
Объектами исследования служили: промышленные образцы 30 видов сырья в фильтр-пакетах (подземные органы: корневища аира, корневища с корнями валерианы, корни алтея, корневища и корни девясила; трава: зверобоя, душицы, тысячелистника, пустырника, мелиссы, хвоща, чабреца, фиалки, череды, чистотела; листья: брусники, толокнянки, подорожника, мяты, шалфея, сены, почечного чая; цветки: ромашки, календулы, гибискуса, липы; плоды: шиповника, боярышника, соплодия ольхи; кора крушины), поступающие в аптечную сеть г. Москвы от ОАО «Красногорсклексредства», ЗАО фирмы «Здоровье», ООО фирмы «Техмедсервис» и других производителей и водные извлечения, изготовленные из них.
Определение размера частиц лекарственного растительного сырья проводили в соответствии с общей статьей ГФ XI «Определение измельченности порошков и сита», вып.2, стр.19.
Исследование внешних признаков порошкованого сырья проводили на бинокуляре МБС-2 и стереомикроскопе МБИ-6 с окулярами х7 и х15, объективами х8 и х40.
Водные извлечения из лекарственного растительного сырья готовили в соответствии с: 1) методикой ГФ XI, вып.1, стр.147; 2) согласно инструкциям по применению для каждого вида сырья.
Оптическое вращение водных извлечений определяли по методике ГФ XI, вып.1, стр.30.
Присутствие основных групп биологически активных веществ в изучаемых объектах устанавливали с помощью общепринятых качественных реакций с водными извлечениями из сырья. Реактивы, используемые при проведении качественного и количественного химического анализа, готовились по методикам, указанным в ГФ XI, вып.2.
Числовые показатели (влажность, экстрактивные вещества, окисляемые вещества) определяли согласно методикам ГФ XI, т.1, стр.285-295
Хроматографическое изучение флавоноидов, фенолкарбоновых кислот, фенологликозидов, сеннозидов проводили методами тонкослойной и высокоэффективной жидкостной хроматографии (ТСХ и ВЭЖХ).
Определение арбутина и гидрохинона проводили методом обратно- фазовой ВЭЖХ с флуориметрическим детектированием. Определение сеннозидов А и В в листьях кассии проводится методом обратно-фазовой ВЭЖХ с фотометрическим детектированием. Определение гиперозида в цветках и плодах боярышника проводится методом обратно-фазовой ВЭЖХ с фотометрическим детектированием.
Изучение микробиологической чистоты лекарственного растительного сырья и водных извлечений проводили в соответствии со статьей ГФ XI, вып.2, стр.193 (испытание на микробиологическую чистоту) и Изменением № 3 от 19.06.03, категория 4А– «лекарственное растительное сырье «ангро», применяемое в виде настоев и отваров, приготовленные с использованием термической обработки».
Оценку антиокислительной активности водных извлечений проводили титрометрическим методом (Максимова Т.В., Никулина И.Н., Пахомов В.П, Шкарина Е.И., Чумакова З.В., Арзамасцев А.П. Способ определения антиокислительной активности. Патент № 2170930 на изобретение; зарегистрирован в Государственном реестре изобретений РФ 20 июля 2001г.)
Статистическую обработку экспериментальных данных проводили общепринятым методом с определением среднего арифметического и ошибки среднего. Достоверность результатов оценивали параметрически по t- критерию Стьюдента.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ.
В статье ГФ XI «Настои и отвары» и в приказах МЗ нет упоминания о фильтр-пакетах и методике изготовления извлечений из них. Методика, приведенная в инструкциях к применению сильно отличается от фармакопейной по ряду технологический параметров. Настои и отвары из фильтр-пакетов вошли в медицинскую практику в 90-х годах 20-го столетия.
Изучение дисперсности лекарственного растительного сырья в фильтр-пакетах.
Изучена дисперсность более 30 видов лекарственного растительного сырья, выпускаемого в фильтр-пакетах, различных морфологических групп сырья: листья, травы, цветки, плоды, коры, подземные органы.
Проведенные исследования показали, что соотношение стеблей, листьев и цветков в изучаемых фракциях трав для различных растений неодинаково. Это связано, в первую очередь, с морфолого-анатомической характеристикой самих растений (опушенность, размеры листовой пластинки, характером соцветий и строением цветка и т.п.). В изучаемых объектах соотношение стеблей, листьев и цветков прямо пропорционально размеру частиц: с увеличением дисперсности сырья в нем уменьшается содержание стеблей (они труднее измельчаются) и увеличивается – листьев и цветков, в которых в основном и содержатся биологически активные вещества. Но существуют виды лекарственных растений, которые не подчиняются этой закономерности. Так, трава тысячелистника во всех фракциях представлена в основном стеблями, что связано с наличием у данного растения толстого, разветвленного стебля и небольших по размеру ланцетовидных, дваждыперисторассеченных листьев, а так же мелких (не более 5 мм), многочисленных корзинок собранных на верхушке стеблей в сложный щиток. При увеличении дисперсности листьев и цветков выход БАВ из них увеличивается, что, в свою очередь, влияет на качество водных извлечений, приготавливаемых из данного вида сырья.
Установлено, что для морфологической группы травы характерно с увеличением измельченности повышение во фракциях процентного содержания цветков и листьев и снижение – стеблей. Установлено, что в фильтр-пакетах преобладающими фракциями являются для трав частицы сырья с размером 2,0-0,5 мм (рис. 1); для коры – 2,0-1,0 мм; для плодов – 2,0-0,5мм; корневищ с корнями валерьяны – 2,0-0,25мм, а корневищ аира –2,0- 1,0 мм.
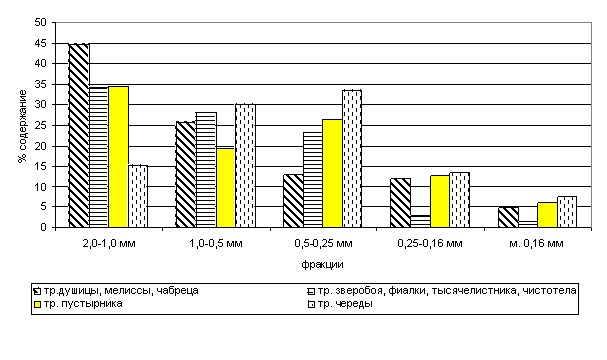
Рис. 1. Фракционный состав растительного сырья в фильтр-пакетах (травы).
Установлено, что преобладающими фракциями сырья в фильтр-пакетах являются для цветков календулы – 2,0-0,5 мм, а ромашки – 0,5-0,16 мм.
Изучение влияния некоторых факторов на качество водных извлечений из лекарственного растительного сырья в фильтр-пакетах.
Для оценки характеристик подлинности настоев и отваров из ЛРС, в ФП были использованы водные извлечения, приготовленные по методике, приведенной в инструкциях по применению: 1 ФП (1,5 г) заливали 100 мл кипящей дистиллированной воды, что соответствует концентрации 1:66, и настаивали 15 мин (30 мин для кожистых листьев, подземных органов и плодов), далее фильтровали и доводили извлечение до 100 мл дистиллированной водой.
Принимая во внимание, что в нормативной документации на жидкие лекарственные формы указывается цвет и прозрачность, а для лекарственного растительного сырья – запах и вкус, эти характеристики устанавливали и для водных извлечений из фильтр-пакетов. Подавляющие большинство представляло собой прозрачные жидкости. Присутствие опалесценции в водных извлечениях из цельных фильтр-пакетов связанно с попаданием мелких частиц сырья через поры бумаги в раствор. Извлечения из сырья с дисперсностью менее 0,16 мм и 0,25-0,16 мм были в основном мутными. Интенсивность окрашивания и запах извлечений увеличивались с уменьшением размера частиц сырья, используемого для приготовления водных извлечений. Для сырья, содержащего эфирные масла с уменьшением размера частиц до 0,5-0,25 мм усиливался аромат, а далее - уменьшался. Окраска извлечений, варьировала от желтовато-зеленой (листья, травы), красновато-желтой, розовой, малиновой, фиолетовой (цветки, плоды, коры) до желто-коричневой (подземный органы).
В ходе изучения качественного состава водных извлечений из ФП были выбраны методики тонкослойной хроматографии, которые могут быть использованы и при анализе как цельного, так и измельченного сырья. На примере водных извлечений травы тысячелистника, показано, что основное содержание действующих веществ сосредоточено в цветках и листьях и фракции сырья, в которых они преобладают, будут характеризоваться наибольшим количеством действующих веществ (рис.2).
Критериями качества водных извлечений были выбраны следующие показатели: экстрактивные вещества при настаивании (сухой остаток), который показывает сумму всех веществ, в том числе и действующих, переходящих в извлечение при данном режиме настаивания, содержание окисляемых веществ, позволяющее оценить количество всех фенольных соединений, переходящих в воду.
Сухой остаток в настоях из фильтр-пакетов варьирует в пределах от 0,2 до 1,0 % и зависит от химического состава БАВ лекарственного растительного сырья.
__________________________________________________________________________
К
Л
Г
Р
1 2 3 4 5 6 7 8 9 10 11 12
стандарты ФП 2,0 1,0 0,5 0,25 0,16 стеб. Лист цвет. Л+цв
К,Р,Г,Л
Система: этилацетат-уксусная кислота-вода (ЭУВ)
Сорбент: пластинка «Kiezelgel 60 F254» фирмы «Merk»
Детектор: 5 % спиртовой раствор хлорида алюминия, УФ- свет
1,2: К- раствор ГСО кверцетина в 95 % спирте, Р- раствор ГСО рутина в 95 % спирте, Г- раствор ГСО гиперозида 95 % спирте, Л - раствор ГСО лютеолина в 95 % спирте
3- настой фильтр-пакета травы тысячелистника, 4- настой фракции 2,0-1,0 мм тысячелистника, 5- настой фракции 1,0-0,5 мм тысячелистника, 6- настой фракции 0,5-0,25 мм тысячелистника, 7- настой фракции 0,25-0,16 мм тысячелистника, 8- настой фракции менее 0,16 мм тысячелистника
9- водное извлечение из стеблей тысячелистника, 10-водное извлечение из листьев тысячелистника, 11-водное извлечение из цветков тысячелистника, 12-водное извлечение из листьев и цветков (1:1) тысячелистника.
Рис.2. Схема сравнительной хроматограммы водных извлечений из фильтр-пакета и фракций травы тысячелистника (флавоноиды).
Установлено, что сухой остаток увеличивается для ЛРС, содержащего полисахариды и значительно снижается в сырье, содержащем витамины, органические кислоты (рис.3.). При изучении сухого остатка настоев, полученных из отдельных фракций ЛРС из фильтр-пакетов, показано, что с ростом дисперсности сырья возрастает величина сухого остатка.
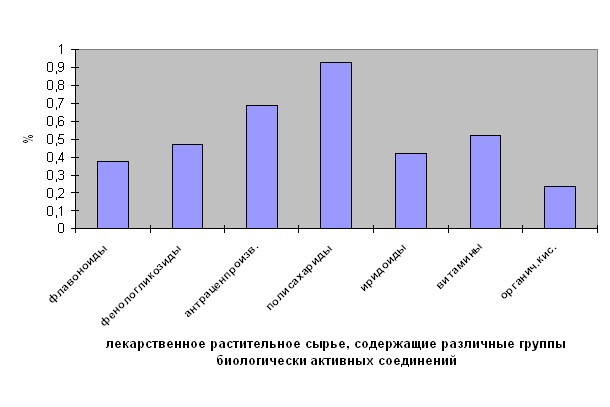 Рис. 3. Значение сухого остатка в водных извлечениях из сырья, различного химического состава.
Рис. 3. Значение сухого остатка в водных извлечениях из сырья, различного химического состава.
Содержание окисляемых веществ в порошкованном ЛРС варьирует в пределах от 0,03 до 0,3% (рис.4).
Изучение влияния дисперсности сырья и условий настаивания на содержание биологически активных веществ в настоях из фильтр-пакетов
Содержание действующих веществ в настоях, полученных из фильтр-пакетов, определяли: СМФ, ФЭК, гравиметрически, титрометрически, с помощь ВЭЖХ анализа. Данные представлены в таблице 1.
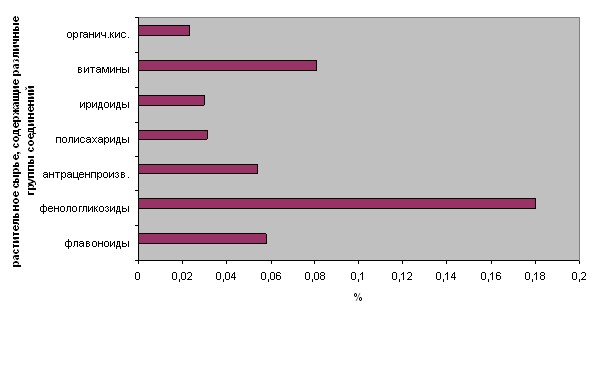 Рис. 4. Значение окисляемых веществ из водных извлечений сырья, фасованного в фильтр-пакеты.
Рис. 4. Значение окисляемых веществ из водных извлечений сырья, фасованного в фильтр-пакеты.
Таблица 1
Содержание биологически активных веществ в настоях из фильтр-пакетов
| БАВ | Водные извлечения из ЛРС | Содержание, % (среднее значение) |
| Антраценпроизводные | Листья сены Кора крушины | 0,13-0,16 |
| Органические кислоты | Корневища с корнями валерианы, корневища аира | 0,044-0,330 |
| Аскорбиновая кислота | Плоды шиповника | 0,01-0,04 |
| Сумма флавоноидов в пересчете на рутин | Листья мяты, шалфея, трава душицы, тысячелистника, зверобоя и др. | 0,012-0,050 |
| Полисахариды | Цветки ромашки, календулы, корни алтея | 0,05-0,40 |
| Сумма антоцианов в пересчете на цианидин-3,5-дигликозид | Цветки гибискуса | 0,05-0,1 |
ВЭЖХ - анализ травы зверобоя, фасованного в ФП, и полученных настоев (рис. 5) показал присутствие в сырье флавоноидов - рутина, гиперозида, витексина, астрагалина, синенсетина и антраценпроизводных – гиперицина (время удерживания 36,3 мин) и псевдогиперицина (время удерживания 25,4 мин).
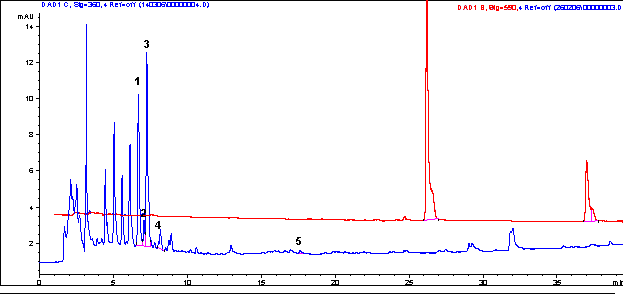
Рис. 5. А – Хроматограмма основных флавоноидов настоя из травы зверобоя (1 – рутин, 2 – витексин, 3 – гиперозид, 4 – астрагалин, 5 - синенсетин); Б – Хроматограмма псевдогиперицина и гиперицина.
Установлено, что в водные извлечения переходят лучше гликозидированные формы флавоноидов (рутин, гиперозид), а конденсированные антраценпроизводные (гиперицин и псевдогиперицин) в них практически отсутствуют. Наибольшее содержание рутина и гиперозида наблюдается во фракциях с размером частиц 0,5-0,16 мм. Максимальный выход гиперицина и псевдогиперицина приходится на фракции с размером частиц 0,25-0,16 мм и менее 0,16 мм. Это связано с содержанием в данных фракциях до 70 % цветков, богатых указанными соединениями (табл. 2).
Таблица 2
Влияние дисперсности травы зверобоя на выход БАВ
| Размер частиц сырья | Содержание в настое, мг/г | |||
| гиперицин | псевдогиперицин | рутин | гиперозид | |
| 2,0-1,0 мм | 0,009± 0,001 | 0,034±0,002 | 6,601±0,330 | 2,801± 0,140 |
| 1,0-0,5 мм | 0,039± 0,002 | 0,121± 0,006 | 15,019±0,750 | 6,338± 0,316 |
| 0,5-0,25 мм | 0,094± 0,004 | 0,289± 0,014 | 19,827± 0,991 | 8,339± 0,417 |
| 0,25-0,16 мм | 0,226± 0,011 | 0,671± 0,033 | 20,064± 1,003 | 9,927± 0,496 |
| Менее 0,16 мм | 0,116±0,006 | 0,698± 0,035 | 14,849± 0,742 | 8,903± 0,445 |
Спиртовые извлечения из травы зверобоя характеризуются более высоким содержанием псевдогиперицина и гиперицина.
При изучении влияния дисперсности ЛРС и условий настаивания на выход БАВ использовали следующие методики приготовления водных извлечений. Соотношение сырья и экстрагента во всех методиках было одинаково 1:133 (1,5 г сырья на 200 мл воды):
- фармакопейную методику для настоев – сырье заливали водой, комнатной температуры и в течение 15 мин настаивали на кипящей водяной бане, далее 45 мин охлаждали, процеживали, отжимали сырье и доводили объем полученного извлечения до 200 мл;
- по инструкции на упаковке сырья - сырье заливали 200 мл кипящей воды и настаивали 15 мин, процеживали, отжимали сырье и доводили объем полученного извлечения до 200 мл;
- водная длительная исчерпывающая экстракция - сырье заливали 50 мл воды и кипятили с обратным холодильником 15 мин на водяной бане (4 раза), объем доводили до 200 мл;
- спиртовая экстракция - сырье заливали 50 мл 95 % спиртом и кипятили с обратным холодильником 30 мин на водяной бане (4 раза), объем доводили до 200 мл (табл.3).
Таблица 3
Влияние режима настаивания на выход БАВ травы зверобоя
| Режим настаивания сырья | Содержание, мг/мл | |||
| Гиперицин | Псевдо- гиперицин | Рутин | Гиперозид | |
| Методика ГФ XI | 0,056±0,002 | 0,236±0,011 | 13,704±0,681 | 6,158±0,307 |
| инструкция на упаковке | 0,067±0,003 | 0,265±0,013 | 14,616±0,730 | 6,915±0,345 |
| Водная экстракция (исчерпывающая) | 0,070±0,003 | 0,283±0,014 | 13,941±0,697 | 6,290±0,314 |
| Спиртовая экстракция (исчерпывающая) | 0,381±0,019 | 0,437±0,021 | 7,460±0,373 | 4,932±0,246 |
При использовании фармакопейной методики по сравнению с методикой, описанной в инструкции по применению, наблюдается незначительное снижение выхода БАВ, что возможно обусловлено температурным фактором. Водная длительная экстракция показала, что обе методики дают переход БАВ около 90 % при данной измельченности сырья (менее 2 мм). Особенно это актуально для морфологической группы – плоды, где измельченность сырья до размера частиц проходящих сквозь сито с диаметром отверстий 2 мм позволяет увеличить выход БАВ с 20 % (цельное или слабо измельченное сырье – 3-5 мм) до 80 % (сырье, фасованное в ФП с размером частиц 2 мм и менее).
Определение антиокислительной активности водных извлечений из растительного сырья, фасованного в фильтр-пакеты.
Многие биологически активные вещества (БАВ) растений, например, лигнаны, флавоноиды, органические кислоты, витамины, сапонины, фосфолипиды, аминокислоты и др. обладают антиокислительной активностью, которая позволяет использовать лекарственное растительное сырье в качестве антиоксидантов. Антиокислительная активность (АОА) сырья и его водных извлечений зависит от концентрации в них БАВ и измельченности объекта (рис. 6). Проведенный сравнительный анализ показал, что водные извлечения из листьев брусники и толокнянки обладают более выраженной антиокислительной активностью, чем настои из растительного сырья, содержащего флавоноиды (травы душицы, зверобоя, листьев мяты и шалфея, плодов боярышника, цветков календулы). Настои из ЛРС, содержащего витамины и органические кислоты (плоды шиповника и цветки гибискуса) по своей активности уступают настоям из сырья, содержащего фенологликозиды. Горечи, иридоиды и антраценпроизводные (настои травы тысячелистника, пустырника, коры крушины) имеют среднюю степень выраженности антиокислительной активности, и практически таковая отсутствует у сырья, содержащего полисахариды, валепотриаты, горькие гликозиды и др. (корневища с корнями валерианы, корневища аира, трава череды, листья подорожника большого).
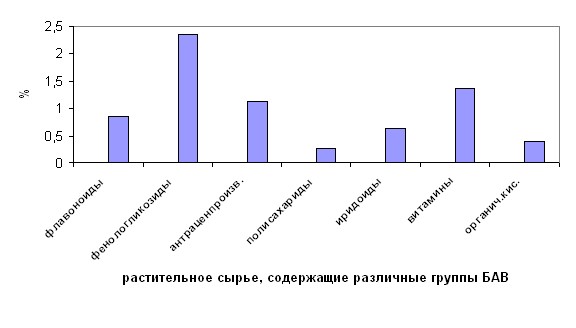
Рис.6. Антиокислительная активность водных извлечений.
Изучение влияние бумаги, используемой для производства фильтр-пакетов, на выход биологически активных веществ
Для изготовления фильтр-пакетов промышленностью используют два типа бумаги: термосвариваемую и нетермосвариваемую, которые различаются показателями качества (плотность, толщина, разрываемость, пропуск воздуха, прочность, влажность, запах).
Химический анализ бумаги, используемой для производства фильтр-пакетов из ЛРС, показал, что она в своем составе содержит следы различных органических растворителей, микроэлементов и др. соединений, которые используются при производстве бумаги в целлюлозно-бумажной промышленности и не превышают норм предельно допустимых количеств химических веществ, выделяющихся из материалов, контактирующих с пищевыми продуктами.
Вместе с тем в ходе выполнения работы было отмечено, что значения окисляемых веществ и сухого остатка в водных извлечениях из ФП различных видов ЛРС выше этих показателей в извлечениях, полученных непосредственно из сырья, использовавшегося для изготовления ФП (табл.5).
Таблица 4
Влияние бумаги фильтр-пакетов на содержание БАВ в настое.
| ЛРС | Содержание действующих веществ | ФП | |
| ФПц (с бумагой) | РФП (без бумаги) | ||
| 1 | 2 | 3 | 4 |
| Листья Сены | Сенозида А, мг/г | 15,600 ± 0,780 | 16,620 ± 0,831 |
| Сенозида В, мг/г | 13,000± 0,650 | 13,940 ± 0,697 | |
| Плоды боярышника | Гиперозида, мг/г | 0,080± 0,004 | 0,080±0,007 |
| Рутина, мг/г | 0,020± 0,001 | 0,030± 0,001 | |
| Органических кислот % | 0,052±0,002 | 0,044± 0,002 | |
| Листья брусники | Арбутина, мг/г | 54,230± 2,711 | 52,000± 2,600 |
| Гидрохинона, мг/г | 2,150 ± 0,107 | 0,85 ± 0,042 | |
| Органических кислот % | 0,133±0,006 | 0,122± 0,006 | |
| Трава душицы | Флавоноиды % | 0,010±0,001 | 0,009± 0,0001 |
| Органических кислот % | 0,056±0,003 | 0,054± 0,002 | |
| Трава тысячелистника | Флавоноиды % | 0,037±0,002 | 0,041± 0,002 |
| Органических кислот % | 0,045±0,002 | 0,044±0,002 | |
| Кора Крушины | Антраценпроизводные, % | 0,142±0,007 | 0,151±0,007 |
| Органических кислот % | 0,318± 0,015 | 0,335± 0,016 | |
| Корневища аира | Органических кислот % | 0,143±0,010 | 0,132±0,006 |
| Плоды шиповника | Аскорбиновой кислоты % | 0,012±0,007 | 0,011±0,001 |
| Органических кислот % | 0,066±0,003 | 0,061±0,003 | |
| Трава пустырника | Флавоноиды % | 0,033±0,002 | 0,045± 0,002 |
| Органических кислот % | 0,046±0,023 | 0,048±0,002 | |
| Листья шалфея | Флавоноиды % | 0,013±0,001 | 0,014± 0,001 |
| Органических кислот % | 0,027±0,001 | 0,025±0,001 | |
| Листья подорожника | Полисахаридов, % | 0,376±0,018 | 0,423±0,021 |
| Трава череды | Полисахаридов, % | 0,120±0,006 | 0,123±0,006 |
Предположительно, это связано с выделением бумагой в водную среду под действием температуры при изготовлении настоев различных соединений.
Было изучено влияние бумаги на выход БАВ из сырья для 20 видов сырья (табл. 4). Проведенные исследования показали, что бумага, используемая для производства фильтр-пакетов, задерживает выход таких групп биологически активных соединений как антраценпроизводные,
Таблица 5
Влияние бумаги фильтр-пакетов на содержание показатели качества настоев для некоторых видов сырья
| ЛРС | ФП | Содержание, % | |
| Окисляемых веществ (ОВ) | Сухого остатка (СО) | ||
| Трава душицы | ФПц (с бумагой) | 0,104±0,005 | 0,252±0,013 |
| РФП (без бумаги) | 0,106±0,005 | 0,371±0,018 | |
| Трава тысячелистника | ФПц (с бумагой) | 0,029±0,001 | 0,228±0,011 |
| РФП (без бумаги) | 0,046±0,002 | 0,333±0,016 | |
| Листья толокнянки | ФПц (с бумагой) | 0,227±0,011 | 0,472±0,023 |
| РФП (без бумаги) | 0,268±0,013 | 0,529±0,026 | |
| Цветки ромашки | ФПц (с бумагой) | 0,024±0,002 | 0,374±0,018 |
| РФП (без бумаги) | 0,031±0,001 | 0,392±0,019 | |
| Плоды боярышника | ФПц (с бумагой) | 0,032±0,002 | 1,786±0,053 |
| РФП (без бумаги) | 0,022±0,009 | 1,599±0,034 | |
| Корневища с корнями валерианы | ФПц (с бумагой) | 0,028±0,002 | 0,274±0,026 |
| РФП (без бумаги) | 0,025±0,001 | 0,252±0,029 | |
| Бумага для приготовления ФП без ЛРС | 0,004±0,002 | 0,054±0,004 | |
| Вода, используемая для изготовления водных извлечений | 0,002±0,001 | 0,003±0,002 | |
Примечание: ФПц- цельный фильтр-пакет (с бумагой); РФП- сырье из фильтр-пакета (без бумаги).
фенолгликозидов, полисахаридов и практически не влияет на выход флавоноидов, органических кислот, аскорбиновой кислоты (табл. 4).
Изучение микробиологической чистоты лекарственного растительного сырья и его водных извлечений
Были проведены микробиологические исследования ЛРС в ФП и водных извлечений из них. Испытание на микробиологическую чистоту включали количественное определение жизнеспособных бактерий и грибов по методикам ГФ XI и дополнениям, а также выявление микроорганизмов, наличие которых недопустимо в нестерильных лекарственных средствах.
Микробиологическая обсемененность свеже приготовленных настоев, полученных согласно методикам инструкций по применению (с использованием воды с температурой 90-950С) отсутствует, извлечения могут считаться условно стерильными. Стерильность сохраняется до момента полного остывания извлечения (от 1ч до 1,5ч).
В дальнейшем происходит увеличение общего количества микроорганизмов при отсутствии патогенной микрофлоры. Видовой состав микроорганизмов в исследуемых водных извлечений был достаточно однородным. В значительном количестве выделялись бактерии рода Bacillus. Большинство выделенных грибов по характеру колоний и структуре мицелия относились к плесневым грибам родов Aspergillus, Mucor и Penicillium. Частота обнаружения дрожжевых грибов была незначительна.
Таблица 6
Обсемение аэробными микроорганизмами водных извлечений из растительного сырья
| Лекарственное растительное сырье | Содержание микроорганизмов в настоях, КОЕ/г | ||||
| Время хранения водных извлечений, час | |||||
| 1 | 2 | 3 | 6 | 24 | |
| Листья мяты перечной | 1,6 х 104 | 1,7 х 104 | 2,1 х 104 | 8 х 105 | 9 х 105 |
| Листья подорожника большого | 2,5 х 104 | 4,1 х 104 | 7,3 х 106 | 3,4 х 107 | 1,0 х 109 |
| Плоды шиповника | 2,3 х 102 | 5,6 х 102 | 6,0 х 102 | 8,5 х 102 | 3,6 х 106 |
| Листья толокнянки | 102 | 21 | 12 | 4 | 10 |
Рост обсемененности аэробными микроорганизмами водных извлечений из лекарственного растительного сырья в фильтр-пакетах во времени зависел от вида сырья и состава БАВ. (табл. 6).
Выводы
- Проведен информационный анализ состояния нормативной документации, методик получения, стандартизации настоев и отваров из порошкованного лекарственного растительного сырья.
- Исследованы и отобраны характеристики и показатели, которые можно использовать в анализе водных извлечений из растительного сырья, выпускаемого в фильтр-пакетах: прозрачность, цветность, запах, вкус, качественные реакции и сухой остаток.
- Изучено влияния измельченности и условий настаивания порошкованного сырья, выпускаемого в фильтр-пакетах, на качество настоев и отваров. Установлена для каждой морфологической группы сырья оптимальная измельченность, при которой достигается наибольший выход биологически активных веществ.
- Изучена дисперсность 30 видов лекарственного растительного сырья, выпускаемого в фильтр-пакетах, различных морфологических групп: листья, травы, цветки, плоды, коры, подземные органы. Установлено, что для морфологической группы «травы» во фракциях с увеличением измельченности повышается процентное содержание цветков и листьев и понижается – стеблей.
- С использованием современных физико-химических методов анализа проведено углубленное изучение химического состава порошкованого сырья и водных извлечений. Полученные результаты хроматографического анализа сырья, фасованного в фильтр-пакеты, и водных извлечений показывают возможность и целесообразность включения использованных ТСХ - методик в раздел «качественные реакции» соответствующих нормативных документов.
- На примере травы тысячелистника показано, что для получения качественных настоев из трав, фасованных в фильтр-пакеты, необходимо использовать обмолоченное сырье, из которого удалены стебли.
- Используя ВЭЖХ анализ, показано, что качество настоев из фильтр-пакетов, изготовленных согласно инструкции по применению, по содержанию действующих веществ незначительно уступает настоям, изготовленным по ГФ XI.
- Проведено санитарно-химическое исследование бумаги, используемой для производства фильтр-пакетов. Установлено, что в процессе изготовления водных извлечений под действием температуры бумага выделяет в водную среду вещества окислительно-восстановительного характера.
- Статистически достоверно показано, что бумага, используемая для производства фильтр-пакетов, задерживает такие группы соединений, как антраценопроизводные, фенологликозиды и полисахариды и практически не влияет на выход флавоноидов, органических кислот и аскорбиновой кислоты.
- Для характеристики лекарственного растительного сырья, используемого для изготовления настоев и отваров, предложен числовой показатель «Экстрактивные вещества при настаивании». Разработан и передан в фармакопейный комитет проект общей фармакопейной статьи «Определение содержания экстрактивных веществ в лекарственном растительном сырье».
- Определена антиокислительная активность водных извлечений из лекарственного растительного сырья, фасованного в фильтр-пакеты. Наибольшая активность отмечена для настоя из листьев брусники, наименьшая - в настоях из сырья валерианы и аира.
- Проведенные микробиологические исследования показали, что использование методики изготовления водных извлечений, приведенной в «инструкции по применению» позволяет получать условно стерильные настои.
Основное содержание диссертационной работы изложено в следующих публикациях:
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Исследование травы душицы, зверобоя, тысячелистника, фасованных в фильтр-пакеты// Актуальные проблемы фармации: Сб. научных работ.- Барнаул, 2005. – вып.2 – с. 23-27.
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Изучение флавоноидного состава фракций порошков травы душицы, тысячелистника, зверобоя и пустырника методом планарной хроматографии// XII Российский национальный конгресс «Человек и лекарство»: тезисы докладов.- М., 2005.- 18-22 апреля 2005 – с. 739.
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Дисперсность сырья в фильтр-пакетах и качество настоев// Пути и формы совершенствования фармацевтического образования: материалы 2-й всероссийской конференции «Фармобразование-2005».- Воронеж, 2005.- 20-22 апреля 2005- с. 296-299.
- А.А. Сорокина, И.А. Самылина, Н.А. Беседина. Оценка показателей антиокислительной активности водных извлечений из растительного сырья, фасованного в фильтр-пакеты// IX Международный съезд «Актуальные проблемы создания новых лекарственных препаратов природного происхождения»: Фитофарм 2005.- Санкт-Петербург, 2005.- 22-25 июня 2005- с. 134-137.
- Н.А. Беседина, Н.В. Кочергина, А.А. Сорокина. Характеристика водных извлечений из порошкованного сырья брусники и толокнянки// Юбилейный сборник научных трудов.- Барнаул, 2005.-с.25-29.
- Н.А. Беседина, А.А. Сорокина. Фильтр-пакеты: дисперсность сырья и качество водных извлечений// Фармация. 2005. № 6. с.27-31.
- Н.А. Беседина, А.А. Сорокина. Исследование водных извлечений из цветков ромашки аптечной и календулы лекарственной, фасованных в фильтр-пакеты// Актуальные проблемы фармации: Сб. научных работ.- Барнаул, 2006. – вып.3 – с. 29-34.
- Н.А. Беседина, П.А Апухтин, А.С. Осипов, А.А. Сорокина. Изучение водных извлечений из Hibiscus sabdariffa// Актуальные проблемы фармации: Сб. научных работ.- Барнаул, 2006. – вып.3 – с. 34-39.
- А.М. Власов, К.И. Эллер, Е.В. Чукарина, Н.А. Беседина. «Определение индикаторных компонентов в водных извлечениях травы зверобоя с помощью ВЭЖХ» // Фармация. 2006. № 4. с.15-18.
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Влияние бумаги на качество водных извлечений// XIII Российский национальный конгресс «Человек и лекарство»: тезисы докладов.- М., 2006.- 3-7апреля 2006 – с. 692.
- А.А. Сорокина, И.А. Самылина, Н.А. Беседина. Некоторые аспекты изготовления водных извлечений из сырья, фасованного в фильтр-пакеты // X Международный съезд «Актуальные проблемы создания новых лекарственных препаратов природного происхождения»: Фитофарм 2006.- Санкт-Петербург, 2006.- 22-25 июня 2006- с. 134-137.
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Изучение водных извлечений плодов шиповника // Приоритеты фармацевтической науки и практики: Материалы заочной международной конференции.-М., 2006- с.179.
- Н.А. Беседина, А.А. Сорокина. Исследование водных извлечений порошкованного лекарственного растительного сырья // Пути и формы совершенствования фармацевтического образования: материалы 3-й Всероссийской конференции «Фармобразование-2007».- Воронеж, 2007.- 22-24 марта 2007, ч.1 - с. 71-74.
- Н.А. Беседина, А.А. Сорокина, И.А. Самылина. Изучение водных извлечений листьев подорожника большого // Сборник научных трудов конгресса «Традиционная медицина -2007». –М., 2007.- 1-3 марта 2007- с.35.
- Н.А. Беседина, А.А. Сорокина. Биотехнологические аспекты получения водных извлечений // Сборник научных трудов конгресса «Традиционная медицина -2007». –М., 2007.- 1-3 марта 2007- с.36-37.

