Эхокардиографические критерии гипертонического сердца
На правах рукописи
Демидова Наталья Юрьевна
Эхокардиографические критерии
«гипертонического сердца»
14.00.19 - лучевая диагностика, лучевая терапия
Автореферат диссертации на соискание
ученой степени доктора медицинских наук
Нижний Новгород - 2008
Работа выполнена на кафедре лучевой диагностики ЦПК и ППС
ГОУ ВПО «Нижегородской государственной медицинской академии Федерального агентства по здравоохранению и социальному развитию» РФ и в ФГУЗ Клинической Больнице №50 ФМБА России
г. Саров.
Научный консультант:
доктор медицинских наук, профессор Белоусов Юрий Васильевич
Официальные оппоненты:
доктор медицинских наук, профессор Королева Любовь Юрьевна
ГОУ ВПО Нижегородская государственная медицинская академия
г. Н.Новгород
доктор медицинских наук, профессор Дроздецкий Сергей Ильич
ВМИ ФСБ РФ г. Н.Новгород
доктор медицинских наук Казакова Лариса Васильевна
ГУ Нижегородская областная детская клиническая больница
г. Н.Новгород
Ведущая организация:
ФГУ институт хирургии им. А.В. Вишневского Росмедтехнологий
Защита диссертации состоится «_____» _____________ 2008 года
в _____ часов на заседании диссертационного совета Д 208.061.02 при
Нижегородской государственной медицинской академии
(603005, г. Н. Новгород, пл. Минина, 10/1)
С диссертацией можно ознакомиться в библиотеке Нижегородской государственной медицинской академии по адресу: г. Н.Новгород, ул. Медицинская, 3А.
Автореферат разослан «_____» ______________ 2008 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук,
профессор Лукушкина Елена Федоровна
общая характеристика работы
Актуальность проблемы. Эпидемиологические исследования показывают, что одним из основных направлений в решении проблемы снижения сердечно-сосудистой заболеваемости и смертности является эффективный контроль за АГ – самой распространенной в популяции сердечно-сосудистой патологией. Причем эффективный контроль за АГ предусматривает не столько снижение артериального давления как такового, сколько уменьшение риска повреждения органов-мишеней и риска смерти, тесно ассоциированных с высокими цифрами АД (Ф.Т. Агеев, Т.В. Фофанова, 2004). Контроль за АД – важный, но не единственный фактор, который следует учитывать у пациента с АГ (Кириченко Л.Л. и соавт., 2004). Эхокардиография позволяет более точно определить степень поражения сердца при АГ, что имеет значение при определении прогноза заболевания, выборе активности лечения и для анализа эффективности гипотензивной терапии.
Артериальная гипертония остается одной из ведущих причин развития сердечной недостаточности. Существует множество причин, объясняющих взаимосвязь между АГ и СН. Основные акценты делаются на нарушении сократительной и диастолической функции ЛЖ. При АГ развиваются структурно-функциональные изменения ЛЖ, которые характеризуются развитием гипертрофии, диастолической и систолической дисфункции миокарда с последующим формированием ХСН (Васюк Ю.А. и соавт., 2005). При этом симптомы ХСН чаще обусловлены не снижением систолической функции ЛЖ, а изменением диастолической жесткости миокарда вследствие гипертрофии с нарушением функционального взаимодействия желудочков сердца (Васюк Ю.А. и соавт., 2005). Частота развития диастолической дисфункции ЛЖ у больных АГ достигает 60% и в значительной степени определяет прогноз заболевания (Вебер В.Р. и соавт., 2005). При АГ ремоделирование развивается не только в левом, но и в правом желудочке. В основе вовлечения в патологический процесс правого желудочка лежит механизм выравнивания нагрузки на межжелудочковую перегородку, которая зависит от эластических свойств МЖП и механических характеристик свободной стенки правого и левого желудочков (Cittadini А. et al, 1995). От степени вовлеченности правых отделов в ремоделирование сердца, от структурных и функциональных изменений ПЖ во многом зависят темпы развития и прогрессирования СН у больных АГ и, в конечном счете, прогноз исхода заболевания. Предотвращение ремоделирования сердца может быть ключом к прерыванию порочного круга в формировании ХСН. Таким образом, «гипертоническое сердце» требует комплексного изучения структурно-функциональных характеристик как левого, так и правого отделов сердца.
Наличие у больного гипертрофии ЛЖ указывает на необходимость раннего начала эффективной антигипертензивной терапии. При этом снижение массы миокарда ЛЖ является одной из целей проводимого лечения. По реакциям гипертрофированного ЛЖ на снижение АД можно судить об адекватности гипотензивной терапии, решать важные прогностические вопросы. Определение полного спектра структурных и функциональных изменений сердца у больных с АГ необходимо для определения риска сердечных осложнений, выбора агрессивности гипотензивного лечения и контроля эффективности медикаментозной терапии.
Изменения в сердце, развивающиеся при АГ, претерпевают тот или иной процесс ремоделирования. По определению M. Pfeffer (1985): «Ремоделирование – это структурно-геометрические изменения левого желудочка, включающие в себя процессы гипертрофии миокарда и дилатации сердца, приводящие к изменению его геометрии и нарушению систолической и диастолической функции». В настоящее время процесс ремоделирования ЛЖ рассматривается как собирательное понятие, объединяющее патологические изменения, происходящие как на уровне отдельных клеток и интерстициального пространства миокарда, так и всей камеры ЛЖ в целом. Доказано, что развитию гипертрофии ЛЖ предшествует изменение его геометрической формы, которое также является предиктором возникновения у пациента ХСН и увеличения риска смерти. Общей чертой всех видов ГЛЖ является увеличение массы ткани ЛЖ, хотя она существует во многих формах и подтипах, которые различаются по прогнозу и лечению. В настоящее время выделяют следующие геометрические модели ЛЖ: 1) нормальная геометрическая форма, 2) концентрическое ремоделирование (относительная толщина стенок ЛЖ более 0,45 при нормальной ММЛЖ), 3) концентрическая гипертрофия (увеличение ММЛЖ при ОТС ЛЖ > 0,45), 4) эксцентрическая гипертрофия (увеличение массы миокарда при ОТС ЛЖ < 0,45), где ОТС ЛЖ = (МЖП + ЗСЛЖ)/КДР.
Таким образом, понятие ремоделирования в широком смысле включает изменение геометрии ЛЖ при нормальном индексе ММЛЖ и гипертрофию ЛЖ различных видов и типов. В узком же смысле под ремоделированием понимают изменение структуры ЛЖ при отсутствии гипертрофии ЛЖ. Структурные и функциональные изменения, возникающие в сердце при АГ, являются не столько компенсаторной реакцией, сколько самостоятельной причиной дальнейшего прогрессирования заболевания и независимым негативным прогностическим фактором (Kannel W. et al., 1989; Devereux R. et al., 2000). Негативное прогностическое значение гипертрофии левого желудочка показано в многочисленных эпидемиологических исследованиях, однако вопрос о прогностической значимости различных вариантов ремоделирования миокарда остается сегодня открытым (Конради А.О., 2003).
Цель исследования – Оценить методом эхокардиографии характер ремоделирования сердца при артериальной гипертензии, его прогностическое значение для определения индивидуального кардиоваскулярного риска и оптимизации тактики лечения пациента.
Задачи исследования. В соответствии с целью исследования решались следующие задачи:
1. Изучить основные ЭхоКГ-параметры, характеризующие структурно-функциональное состояние сердца при различных геометрических типах ремоделирования левого желудочка
2. Изучить выраженность признаков ХСН при различных типах ремоделирования ЛЖ у пациентов с АГ и оценить прогностическую значимость геометрических типов ремоделирования левого желудочка как предикторов неблагоприятных исходов и хронической сердечной недостаточности
3. Изучить геометрию ЛЖ при различных типах диастолической дисфункции и исследовать связь признаков гипертрофического ремоделирования и параметров диастолической функции
4. Изучить закономерности развития синдрома легочной гипертензии при различных вариантах диастолической дисфунцкии левого желудочка и соотношения диастолической дисфункции левого и правого желудочков у пациентов с АГ
5. Определить наиболее характерные эхокардиографические признаки и степень тяжести «гипертонического сердца»
6. В условиях длительного проспективного наблюдения с помощью современного неинвазивного метода ЭхоКГ оценить динамику структурных и функциональных показателей сердца у больных АГ в зависимости от регулярности и адекватности гипотензивного лечения
Научная новизна. Впервые проведена сравнительная оценка прогностической значимости различных вариантов ремоделирования левого желудочка у больных АГ.
Определено, что в контрольной группе здоровых лиц относительная толщина стенки ЛЖ была 0,39±0,04. Предложено выделить вариант гипертрофии, диагностическими признаками которого считать гипертрофию ЛЖ без дилатации его полости с ОТС 0,35 – 0,43. Доказано, что этот тип гипертрофии характеризуется относительно благоприятным прогнозом.
Выявлено, что дилатация полости ЛЖ является неблагоприятным фактором даже при концентрической гипертрофии ЛЖ и часто сопровождается снижением его сократительной функции. Эксцентрическая ГЛЖ с ОТС менее 0,34 и дилатацией полости ЛЖ является прогностически наиболее неблагоприятным вариантом ремоделирования для развития ХСН.
В работе получены новые данные о распространенности различных типов ремоделирования ЛЖ, изолированной гипертрофии папиллярных мышц и асимметричной гипертрофии ЛЖ среди больных АГ. Доказано, что использование при оценке процессов ремоделирования ЛЖ не только индекса массы миокарда ЛЖ и относительной толщины его стенок, но и индекса конечно-диастолического размера ЛЖ, выявление локальной гипертрофии стенок ЛЖ и/или папиллярных мышц, позволяет более точно определить степень кардиоваскулярного риска у конкретного пациента с АГ. Это позволяет подобрать оптимальное гипотензивное лечение.
Изучена зависимость частоты диастолической дисфункции ЛЖ от варианта ремоделирования ЛЖ, а также коррелятивная зависимость показателей диастолической дисфункции ЛЖ от его морфологических параметров и типа диастолической дисфункции. Впервые показано, что в отличие от гипертрофического типа ДД, коррелятивная взаимосвязь между показателями морфологии ЛЖ и параметрами его диастолической дисфункции, возрастом пациентов при псевдонормальном и рестриктивном типе ДД очень слабая. При этих типах диастолической дисфункции ЛЖ выявлена умеренная корреляционная зависимость между соотношением Е/А и КСР ЛЖ, средним давлением в легочной артерии. Впервые изучено соответствие диастолической дисфункции ЛЖ и диастолической дисфункции ПЖ у пациентов с АГ, выявлена умеренная корреляционная зависимость диастолической дисфункции левого и правого желудочков, а также ДД ПЖ и морфологией как правого так и левого желудочков. Показано, что прогрессирование процессов ремоделирования и диастолической дисфункции левого желудочка отрицательно влияет на морфо-функциональное состояние правого желудочка. При нарушении диастолической функции правого желудочка по псевдонормальному типу выявлена умеренная корреляционная зависимость соотношения Е/А правого желудочка и КДР левого желудочка. Таким образом, дилатация и сферизация полости ЛЖ, повышение конечно-диастолического объема ЛЖ, а, следовательно, и конечно-диастолического напряжения стенки ЛЖ отрицательно сказывается на морфо-функциональном состоянии правого желудочка. Изучение состояния правого желудочка позволяет уточнить стадию ХСН.
Учитывая разнообразие геометрических типов ремоделирования ЛЖ и сочетание их с различными типами диастолической дисфункции, затрудняющими оценку тяжести поражения сердца при АГ для клинических врачей, предложена эхокардиографическая классификация «гипертонического сердца». Таким образом, проведена комплексная оценка анатомического и гемодинамического состояния сердца при АГ, выявлены совокупные эхокардиографические параметры, имеющие прогностическое значение для определения индивидуального риска сердечно-сосудистых осложнений у пациента с АГ и выбора оптимальной индивидуальной программы медикаментозного и немедикаментозного воздействия.
Подтверждено, что обратное развитие сердечно-сосудистого ремоделирования при антигипертензивной терапии наблюдается при условии достижения целевого уровня АД и стабилизации его в течение нескольких лет. Для более эффективного контроля гипотензивной терапии предложено учитывать не только динамику индекса ММЛЖ, но и типа ремоделирования ЛЖ, типа диастолической дисфункции обоих желудочков, класса «гипертонического сердца», как показателей, качественно отражающих динамику процесса, позволяющих достоверно оценить эффективность лечения у конкретного пациента. Выявлено при проспективном наблюдении, что отсутствие эффективного лечения приводит к усугублению процессов ремоделирования сердца и прогрессированию сердечно-сосудистого континуума.
Показано, что эхокардиографический контроль необходим даже при эффективном гипотензивном лечении, поскольку у ряда больных, несмотря на достижение целевого уровня АД, ухудшаются структурные характеристики ЛЖ и его диастолическая функция.
Предложенная нами комплексная оценка характера ремоделирования сердца при АГ в каждом конкретном случае позволит избежать необоснованных терапевтических вмешательств и оптимизировать подход к лечению артериальной гипертензии.
Практическая значимость работы. Эхокардиографическое исследование при АГ является высокочувствительным методом оценки состояния сердца, позволяющим выявить ранние структурно-функциональные изменения миокарда и изучить динамику этих изменений в процессе наблюдения и лечения больных.
Предложены номограммы для определения эхокардиографического типа ремоделирования ЛЖ, которые позволяют быстро определить геометрическую модель левого желудочка, не прибегая к сложным расчетам. Посредством этого можно оценить риск сердечно-сосудистых осложнений у конкретного пациента с АГ, что имеет огромное значение в ежедневной клинической практике.
Эхокардиографическое исследование с определением типа ремоделирования левого желудочка, степени нарушения его диастолической функции, стадии развития «гипертоничческого сердца» позволяет выделить группу больных с более высоким сердечно-сосудистым риском и подобрать этой группе пациентов адекватное гипотензивное лечение, контролируя его эффективность не только уровнем снижения АД, но и динамикой структурно-функциональных показателей сердца.
Внедрение динамического эхокардиографического наблюдения за больными с артериальной гипертензией повышает мотивацию больных к лечению и помогает врачу-кардиологу разработать идеальную индивидуальную программу медикаментозного и немедикаментозного лечения благодаря более полной информации об ответе гипертрофированного ЛЖ на проводимое лечение. Достижение эффективного контроля АД в течение длительного периода времени сопровождается существенным обратным развитием структурных изменений в сердце вплоть до «нормализации» его геометрии. При этом регулярная антигипертензивная терапия, не обеспечивающая целевого уровня АД, не приводит к коррекции ремоделирования. Улучшение структурно-функциональных показателей сердца чаще достигается при первой степени АГ.
Реализация результатов исследования.
Научные выводы и результаты исследования внедрены в практическую работу стационара, лечебный и диагностический процесс поликлиники № 1 и 2 ФГУЗ КБ №50 ФМБА России г.Саров.
Апробация результатов работы. Материалы выполненного исследования представлены в виде докладов и тезисов на IV Всероссийской научно-практической конференции “Современные методы диагностики заболеваний сердечно-сосудистой системы” (Новосибирск, 28-29 мая 2001); II Российском национальном конгрессе кардиологов (Москва, 9-11 октября 2001); II съезде врачей ультразвуковой диагностики Поволжья и Южного округа (Волгоград, 12-13 сентября 2001); международной конференции, посвященной 10-летию отделения ультразвуковой диагностики института хирургии им. Вишневского (Москва, 4-6 октября 2004); на научно-практической конференции в рамках «Недели здорового сердца» (Н. Новгород, 2005); на V, VI и VIII ежегодных конференциях общества специалистов по сердечной недостаточности (Москва, декабрь 2004, 2005, 2007); V съезде специалистов ультразвуковой диагностики Поволжья 2006; на V Съезде Российской Ассоциации специалистов ультразвуковой диагностики в медицине 2007.
Публикации.
По результатам диссертации опубликовано 45 печатных работ, из них 29 в изданиях, рекомендованных ВАК.
Структура и объем работы. Диссертация изложена на 204 страницах машинописного текста, состоит из введения, 8 глав, включающих обзор литературы, материалы и методы исследования, результаты собственных исследований, заключения с обсуждением результатов, выводов и практических рекомендаций. Работа содержит 31 рисунок, 19 таблиц, 54 диаграммы. Указатель литературы содержит 292 источника (140 отечественной и 152 иностранной литературы).
содержание работы
Материал и методы исследования. В исследование было включено 737 пациентов с артериальной гипертензией от 23 до 73 лет (средний возраст больных АГ составил 52,5 ± 2,4 года). Всем больным проводилось полное общеклиническое обследование. В исследование не включались больные с пороками сердца, нарушениями ритма, вторичными формами АГ, инсулинзависимым СД и другими эндокринными заболеваниями, с неудовлетворительным качеством изображения при эхокардиографическом обследовании.
Характеристика пациентов представлена в таблице 1.
Таблица 1.
Характеристика пациентов изучаемой группы
| Показатели | Абсолютное количество | Относительное количество |
| Всего пациентов | 737 | 100% |
| Мужчины | 350 | 47,5% |
| Женщины | 387 | 52,5% |
| Из них женщины в постмено- паузальном периоде | 117 | |
| Узловой зоб | 10 | 1,6% |
| Ожирение | 219 | 29,7% |
| ИБС | 125 | 17% |
| ИМ | 35 | 4,7% |
Ультразвуковые исследования проводились автором работы на аппарате Aloca 2000 (Япония), Siemens Sonolini G 60 S (Германия), Sonoice 8000 электронными секторными датчиками 2-4 Мгц в М -, В - и D - режимах, а также в режиме цветового картирования.
При оценке геометрического строения ЛЖ в В-режиме измерялась толщина передней, перегородочной, задней и боковой стенок ЛЖ в диастолу из парастернального доступа по короткой оси на уровне створок МК и папиллярных мышц. Передне-задний размер папиллярных мышц определялся из позиции короткой оси ЛЖ в парастернальной проекции. В М-режиме проводилось измерение толщины МЖП и задней стенки ЛЖ в диастолу, КДР и КСР ЛЖ, передне-заднего размера ЛП. Расчет объемов ЛЖ проводился по формуле L. Teicholtz (1976): V= (7/(2.4+D))·D3, а так же по модифицированному алгоритму Симпсона. Масса миокарда ЛЖ (ММЛЖ) рассчитывалась по формуле R. Devereux и N. Reichek (1977): ММЛЖ=1,04[(МЖП+ЗС+КДР)3–КДР3]–13,6. В каждом случае ММЛЖ индексировалась к площади поверхности тела. Рассчитывались показатели насосной функции ЛЖ: фракция выброса (ФВ%), фракционное укорочение диаметра ЛЖ, скорость укорочения волокон миокарда (mvcf).
Диастолическая функция ЛЖ оценивалась по данным допплерэхокардиографии, проведенной в импульсном и цветовом режимах. Трансмитральный кровоток получали из апикальной четырехкамерной позиции, стробируемый объем располагался на уровне кончиков створок МК. Рассчитывались следующие показатели трансмитрального кровотока: максимальная скорость раннего диастолического наполнения (Е пик м/с), максимальная скорость наполнения ЛЖ во время систолы предсердий (А пик м/с), соотношение этих скоростей (Е/А), время ускорения (АТ) и время замедления раннего диастолического наполнения ЛЖ (ДТ мс), а также период изоволюмического расслабления (IVRT мс). Аналогично изучалась диастолическая функция ПЖ. Определялось время ускорения (ВУ) и время изгнания (ВИ) в выходном тракте ПЖ. Среднее легочное артериальное давление (ЛАД) рассчитывали по методу, предложенному Kitabatake et al. (1983): log 10 = -2.8(AT/ET) + 2.4. Исследовали кровоток в легочных венах.
В результате проведенных исследований предложено внести изменения в существующую классификацию геометрических типов левого желудочка, разработаны дополнительные критерии различных типов ремоделирования ЛЖ при АГ (Демидова Н.Ю., Белоусов Ю.В., 2004). Признаками гипертрофического ремоделирования (ГР) ЛЖ мы считали локальное увеличение толщины стенок ЛЖ более 11 мм, выявленные в В-режиме, и/или ОТС ЛЖ 0,44, при неувеличенном ИММЛЖ (менее 110г/м2 у женщин и 134 г/м2 у мужчин), нерасширенной полости ЛЖ (КДР/S менее 3,1 см/м2 у мужчин и менее 3,2 см/м2 у женщин).
Критерием гипертрофии папиллярных мышц мы считали увеличение передне-заднего размера хотя бы одной из двух папиллярных мышц более 11 мм, что согласуется с данными Кobashi A. и соавт. (1998). Гипертрофию папиллярных мышц также считали признаком гипертрофического ремоделирования.
Мы использовали следующие критерии различных типов гипертрофии ЛЖ:
1. Нормоцентрическая ГЛЖ (НЦГ) – увеличение ИММЛЖ при ОТС ЛЖ 0,35-0,43 без дилатации полости ЛЖ.
2. Концентрическая ГЛЖ (КЦГ) – увеличение ИММЛЖ при ОТС ЛЖ 0,44 и более без дилатации полости ЛЖ.
3. Концентрическая ГЛЖ с дилатацией полости ЛЖ (КЦГ+дилат) – увеличение ИММЛЖ при ОТС ЛЖ 0,44 и дилатации полости ЛЖ.
4. Псевдонормоцентрическая ГЛЖ (ПНЦГ) – гипертрофия ЛЖ при ОТС ЛЖ 0,35-0,43 в сочетании с дилатацией полости ЛЖ.
5. Эксцентрическая гипертрофия ЛЖ (ЭЦГ) – увеличение ИММЛЖ при ОТС ЛЖ 0,34 и дилатации полости ЛЖ.
Критериями нормальной диастолической функции ЛЖ служили следующие показатели: соотношение Е/А более 1, но менее 2,0, длительность DT более 150 мс, но менее 220 мс, продолжительность IVRT более 64 мс, но менее или равно 86 мс. Гипертрофический тип нарушения диастолической функции ЛЖ характеризовался уменьшением соотношения Е/А менее 1, удлинением периода DT более 220 мс и периода IVRT более 94 мс. Рестриктивный тип ДД характеризовался соотношением Е/А более 2,0, длительностью периода DT менее 150 мс и периода IVRT менее 64 мс. Диагностическими критериями псевдонормального типа диастолической дисфункции мы считали: соотношение Е/А более 1, но менее 2,0; увеличение переднезаднего размера ЛП (37 мм – 43 мм); наличие признаков гипертрофического ремоделирования ЛЖ; нарушение замыкательной функции МК (функциональная регургитация 1-2 ст.); изменение кровотока в легочных венах, что согласуется с канадской классификацией ДД (Farias C., 1999) и с классификацией Nishimura R.A., Tajik A.J. (1997), а также сисследованиями Shaikh M.A., Lavine S.G. (1988), Фейгенбаума Х. (1999), В.Х. Ваизова, Н.Н. Федосовой (2001). Статистический анализ полученных данных проводился с использованием стандартных методов статистики, включая расчет средних величин (M±2m) и вычисление критерия t Стьюдента. Различия между группами считали статистически достоверными при р<0,05. Взаимосвязь параметров оценивался путем расчета коэффициента корреляции r.
результаты исследования и их обсуждение
Результаты изучения ремоделирования сердца и прогностической значимости различных вариантов ремоделирования. Были изучены особенности ремоделирования ЛЖ у 215 пациентов АГ, среди них 118 женщин и 97 мужчин. Средний возраст больных АГ составил 51,5 ± 1,4 года. В соответствии с классификацией АГ, рекомендованной ВОЗ и Международным обществом по изучению гипертонии (1999) первая степень АГ выявлена у 102 пациентов, вторая - у 51, третья - у 62 пациентов. Длительность артериальной гипертензии колебалась от 1 до 43 лет, в среднем составив 9,75 ± 1,3 года, в группе больных с первой степенью АГ - 7,7 ± 2,1 лет, со второй степенью АГ - 11,8 ± 3,0, с третьей - 13,2 ± 2,6 года.
Не увеличенный индекс массы миокарда ЛЖ определялся у 40 пациентов, из них у 18 выявлены признаки ремоделирования: локальная гипертрофия одного или двух сегментов ЛЖ и/или гипертрофия папиллярных мышц, ОТС ЛЖ более 0,44. У 22 пациентов с АГ не выявлено признаков поражения сердца.
Для выявления признаков ремоделирования левого желудочка необходимо обязательно проводить исследование в В-режиме, поскольку ультразвуковой луч в М-режиме не всегда проходит через наиболее гипертрофированный участок.
Локальная гипертрофия ЛЖ в одном или двух сегментах встретилась в 22,5% случаев среди пациентов с нормальным индексом массы миокарда ЛЖ, причем в 12,5% она не была выявлена в М-режиме.
Гипертрофия папиллярных мышц обнаружена у 18 (45%) пациентов с АГ и нормальным индексом ММЛЖ, причем у 11 из них гипертрофия папиллярных мышц сочеталась с гипертрофией стенок ЛЖ, обнаруженной в В-режиме. У 7 (17,5%) пациентов гипертрофия папиллярных мышц была изолированная.
На этом основано наше предложение считать изолированную гипертрофию папиллярных мышц признаком гипертрофического ремоделирования.
Абсолютные размеры переднелатеральной мышцы по результатам проведенного исследования превышают размеры заднемедиальной во всех группах пациентов с АГ, в том числе и в контрольной группе здоровых лиц. Среднее значение передне-заднего размера переднелатеральной папиллярной мышцы (ALPM) в контрольной группе (по данным исследования 29 здоровых лиц) составило 9,3±0,4 мм, заднемедиальной папиллярной мышцы (PMPM) – 8,4±0,6 мм.
Корреляционная связь между ММЛЖ и размером передней и задней папиллярных мышц была умеренной (0,42 и 0,52 соответственно), а между ММЛЖ и относительной величиной ALPM/PMPM ее не наблюдалось. Это позволяет утверждать, что с увеличением ММЛЖ папиллярные мышцы гипертрофируются относительно равномерно.
Гипертрофия ЛЖ может существовать во многих видах и подтипах, так пациенты с артериальной гипертензией могут иметь гипертрофию левого желудочка, которая моделирует гипертрофическую кардиомиопатию (Х. Фейгенбаум, 1999) и провести дифференциальный диагноз между этими состояниями в таком случае очень сложно.
По данным нашего исследования асимметричная гипертрофия (с коэффициентом асимметрии 1,3) встретилась в 42 случаях, что составило 19,5%, и в 14 (6,5%) случаях коэффициент асимметрии составил 1,5 и более. В настоящем исследовании подтвердились данные предыдущего исследования (Белоусов Ю.В, Демидова Н.Ю., 2001) о преимущественной гипертрофии МЖП с увеличением ММЛЖ у больных с АГ, что отражено на рисунке 1.
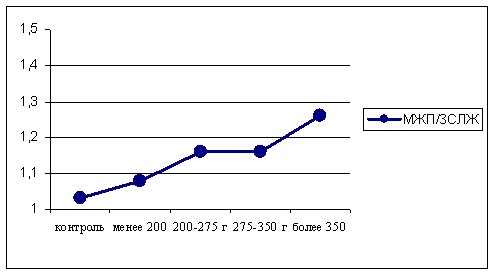
Рисунок 1. Соотношение толщины МЖП и задней стенки ЛЖ в зависимости от ММЛЖ
Однако, корреляционная связь между толщиной МЖП и ММЛЖ, толщиной задней стенки ЛЖ и ММЛЖ была сильнее во втором случае (0,67 и 0,72 соответственно). Утолщение МЖП встретилась в 76,6% случаев среди больных АГ с гипертрофией ЛЖ, а утолщение задней стенки ЛЖ – в 44,6% случаев в той же группе. Корреляционная связь между ММЛЖ и коэффициентом асимметрии была слабая (0,28). Это позволяет сделать вывод, что для АГ характерна преимущественно симметричная гипертрофия ЛЖ, с равномерным утолщением стенок ЛЖ и папиллярных мышц.
Известно, что концентрическая гипертрофия ЛЖ (ГЛЖ) более опасна в риске развития внезапной смерти, а эксцентрическая – в вероятности развития ХСН. Поэтому для определения риска заболевания необходимо точно определять геометрическую модель гипертрофированного ЛЖ. В связи с появлением теории сердечно-сосудистого континуума изменился подход к классификации эхокардиографических геометрических типов ЛЖ.
В результате проведенных нами исследований 285 больных с АГ (Демидова Н.Ю., Белоусов Ю.В. 2004) было показано, что ГЛЖ при относительной толщине стенки ЛЖ 0,35-0,43 и нерасширенной полости левого желудочка имеет наиболее благоприятные показатели морфологии, диастолической функции ЛЖ и клинического течения заболевания среди пациентов с ГЛЖ. Было предложено называть этот тип геометрии ЛЖ – нормоцентрическая гипертрофия ЛЖ. Дальнейшее изучение прогностической значимости геометрического типа ЛЖ в плане определения риска развития ХСН показало, что дилатация полости ЛЖ даже при концентрической гипертрофии, когда относительная толщина стенки ЛЖ более 0,44, является прогностически неблагоприятным фактором (снижается систолическая функция, увеличивается частота симптомов хронической сердечной недостаточности, утяжеляется степень диастолической дисфункции ЛЖ) (рисунок 2,3,4). Эти изменения прогрессируют с увеличением полости ЛЖ и уменьшением относительной толщины его стенки. Наиболее плохие результаты получены при ГЛЖ с ОТС менее 0,35 и КДР ЛЖ более 56 мм.
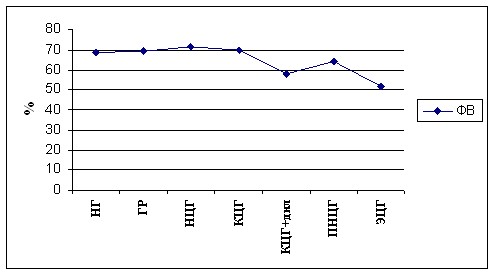
Рисунок 2. Фракция выброса левого желудочка в зависимости от типа ремоделирования
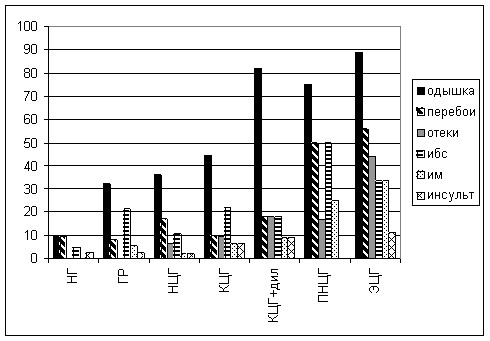
Рисунок 3. Частота встречаемости симптомов ХСН и ассоциированных заболеваний в зависимости от типа ремоделирования ЛЖ
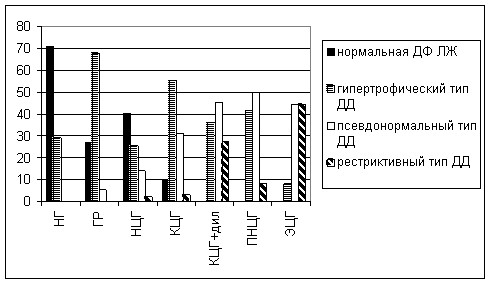
Рисунок 4. Внутригрупповое распределение типов диастолической дисфункции при различных типах ремоделирования ЛЖ
В результате проведенных нами исследований предложено использовать следующие диагностические критерии геометрических типов ремоделирования ЛЖ:
1. Нормальная геометрическая форма (НГ) – ИММЛЖ не увеличен, толщина стенок ЛЖ и папиллярных мышц не превышает 11 мм, полость ЛЖ не расширена (КДР/S менее 3,1 см/м2 у мужчин и менее 3,2 см/м2 у женщин) ОТС ЛЖ<0,45;
2. Гипертрофическое ремоделирование (ГР) – ИММЛЖ не увеличен, полость ЛЖ не расширена, определяется локальная гипертрофия стенок ЛЖ, папиллярных мышц, выявленные в В-режиме, и/или ОТС ЛЖ0,44;
3. Нормоцентрическая ГЛЖ (НЦГ) – увеличение ИММЛЖ при ОТС ЛЖ 0,35-0,43 без дилатации полости ЛЖ (КДР/S менее 3,1 см/м2 у мужчин и менее 3,2 см/м2 у женщин).
4. Концентрическая ГЛЖ (КЦГ) – увеличение ИММЛЖ при ОТС ЛЖ0,44 без дилатации его полости.
5. Концентрическая ГЛЖ с дилатацией полости ЛЖ (КЦГ+дилат) – увеличение ИММЛЖ при ОТС ЛЖ 0,44 и дилатации его полости.
6. Псевдонормоцентрическая ГЛЖ (ПНЦГ) – гипертрофия ЛЖ при ОТС ЛЖ 0,35-0,43 в сочетании с дилатацией его полости.
7. Эксцентрическая гипертрофия ЛЖ (ЭЦГ) – увеличение ИММЛЖ при ОТС ЛЖ0,34 и дилатации полости ЛЖ.
Целесообразным считаем выделять подтипы:
А) Асимметричную гипертрофию ЛЖ, для которой характерна диспропорциональная гипертрофия межжелудочковой перегородки с коэффициентом асимметрии 1,3;
Б) Симметричную гипертрофию ЛЖ – с коэффициентом асимметрии меньше 1,3.
По данным нашего исследования асимметричная гипертрофия МЖП чаще встречалась в группе с гипертрофическим ремоделированием ЛЖ при нормальной массе миокарда и при концентрической гипертрофии ЛЖ. Единичные случаи встречались при нормоцентрической гипертрофии и концентрической гипертрофии с дилатацией полости ЛЖ. Асимметричную гипертрофию ЛЖ тем не менее необходимо выделять, так как она является предиктором внезапной смерти, требует наблюдения и, возможно, медикаментозного воздействия.
На рисунке 5 демонстрируется частота обнаружения функциональной митральной регургитации (1,2 степени) при различных геометрических типах ЛЖ.
Рисунок 5. Относительное количество пациентов с функциональной митральной недостаточностью 1-2 степени в группах
Нарушение замыкательной функции митрального клапана функционального характера достоверно чаще встречается при геометрических типах, характеризующихся дилатацией полости ЛЖ. Гипертрофическое ремоделирование ЛЖ приводит к изменению формы ЛЖ, приводя к изменению расположения папиллярных мышц, в результате чего нарушается замыкательная функция митрального клапана и формируется функциональная (относительная) митральная регургитация (Демидова Н.Ю., Белоусов Ю.В., 2002). Митральная регургитация имеет огромное клиническое значение, поскольку не только снижает величину ударного объема, но и способствует дальнейшей дилатации полости ЛЖ и его гемодинамической перегрузке (Беленков Ю.Н., Мареев В.Ю., 2002). Объемная перегрузка, развивающаяся в результате нарушения замыкательной функции митрального клапана и повышения конечного диастолического давления в ЛЖ играет огромное значение в поворотном моменте сердечно-сосудистого континуума, в переходе от концентрической гипертрофии ЛЖ к эксцентрической (Беленков Ю.Н., Мареев В.Ю., 2002).
Одним из ключевых следствий дилатации и сферизации полости ЛЖ является повышение конечно-диастолического объема ЛЖ, дилатация полости ЛЖ непосредственно увеличивает работу ЛЖ и его потребность в кислороде. Повышение конечно-диастолического стресса на стенку ЛЖ приводит к гипоперфузии субэндокардиальных слоев миокарда и, тем самым, ухудшает функцию ЛЖ (Беленков Ю.Н., Мареев В.Ю., 2002).
Таким образом, при определении типа геометрии ЛЖ предложено учитывать не только ОТС ЛЖ, но, дополнительно, индекс конечно-диастолического размера ЛЖ, выявлять локальную гипертрофию одного или двух сегментов стенки ЛЖ и папиллярных мышц в В-режиме.
Для облегчения определения варианта ремоделирования ЛЖ в клинической практике мы предложили использовать номограммы, построенные по методу Wilfred F. и соавт. (1998). В основе построения графиков лежит формула определения ММЛЖ, которая зависит от двух измерений: КДР ЛЖ и суммы толщины межжелудочковой перегородки и задней стенки ЛЖ. Эти же измерения лежат в основе определения относительной толщины стенки ЛЖ. Мы использовали наиболее распространенную формулу определения ММЛЖ - формулу «Пенн-куб»: ММЛЖ = 1,04ґ[(КДР+МЖП+ЗСЛЖ)3 – КДР3)] – 13,6.
Номограммы построены в зависимости от пола и площади поверхности тела (рисунок 6,7).

Рисунок 6. Номограммы для определения варианта ремоделирования ЛЖ у мужчин с площадью тела 1,8м2
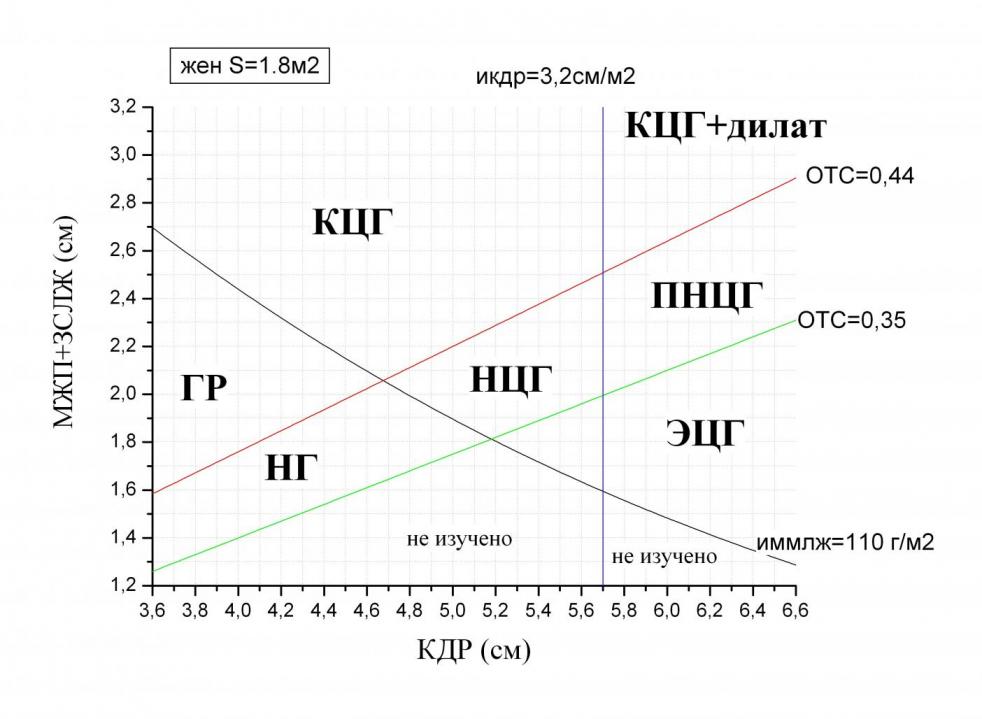
Рисунок 7. Номограммы для определения варианта ремоделирования ЛЖ у женщин с площадью тела 1,8м2
Результаты исследования признаков гипертрофического ремоделирования и параметров диастолической функции ЛЖ. Для больных с АГ чрезвычайно характерны нарушения диастолической функции ЛЖ, которые обусловлены в основном развитием его гипертрофии, а также увеличением содержания коллагена в миокарде, что приводит к повышению его ригидности (Шляхто Е.В., 2003). Была исследована корреляционная зависимость признаков гипертрофического ремоделирования и параметров диастолической функции ЛЖ при различных ее типах.
В исследование вошли 194 больных с АГ, среди них 88 мужчин и 106 женщин. Возраст пациентов всей серии колебался от 23 до 73 лет (средний возраст 52,4 ± 1,6 лет). Пациенты распределены на две группы: А – 144 пациента с нормальной ДФ и нарушением ДФ ЛЖ по гипертрофическому типу; В – 50 пациентов с псевдонормальным и рестриктивным типом диастолической дисфункции. Результаты исследования показывают, что при гипертрофическом типе ДД имеется умеренная корреляционная зависимость между признаками гипертрофического ремоделирования ЛЖ и параметрами его диастолической дисфункции, что соответствует многочисленным исследованиям (рисунок 8,9,10).
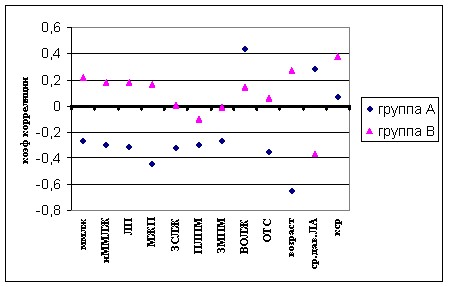
Рисунок 8. Взаимосвязь отношения Е/А и показателей морфологии ЛЖ

Рисунок 9. Взаимосвязь времени замедления раннего диастолического потока и показателей морфологии ЛЖ
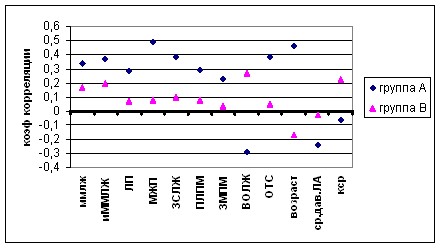
Рисунок 10. Взаимосвязь времени изоволюмического расслабления и показателей морфологии ЛЖ
Однако при псевдонормальном и рестриктивном типе ДД эта связь была очень слабая. Очевидно, при этих типах диастолической дисфункции ведущую роль играют другие факторы.
Корреляционная связь между соотношением Е/А и КСР, средним давлением в легочной артерии, увеличение размера ЛП и КДР ЛЖ при псевдонормальном типе ДД, косвенно подтверждает, что определенную роль в нарушении диастолической функции при данном типе играет митральная регургитация. Частота встречаемости митральной регургитации по данным исследования Ф.Т. Агеева (1997) при умеренных диастолических расстройствах (гипертрофический тип трансмитрального диастолического спектра) составляет 50%, при выраженных нарушениях диастолы (псевдонормальный тип спектра) – 59%, а при тяжелых (рестриктивный тип спектра) уже 93% (Ф.Т. Агеев, 1997). По данным нашего исследования митральная регургитация встретилась в группе с гипертрофическим типом ДД в 17,2% случаев, в группе с псевдонормальным типом ДД – в 71,7% случаев. Однако необходимо продолжить исследование, чтобы изучить зависимость параметров диастолической функции ЛЖ и объема митральной регургитации.
Результаты изучения гемодинамики малого круга кровообращения и диастолической функции правого желудочка. В достаточно большом числе научных исследований показано, что при артериальной гипертензии (АГ) наблюдается повышение давления в системе легочной артерии (ЛА), причины и патофизиологические механизмы которого активно изучаются. [53, 57, 68, 69, 74]. Дж. Х. Ньюман указывает, что легочной гипертензией считается повышение среднего давления в ЛА до значения, превышающего 20 мм рт. ст. в покое или 30 мм рт. ст. при умеренной нагрузке [96]. Учитывая полученные выше результаты об умеренной корреляционной связи между параметрами диастолической дисфункции ЛЖ и средним давлением в легочной артерии при псевдонормальном и рестриктивном типе ДД, мы провели исследование характеристик кровотока на уровне клапана легочной артерии с целью выявления зависимости развития синдрома легочной гипертензии (ЛГ) и диастолической дисфункции ЛЖ у больных АГ.
По результатам проведенного нами исследования (107 пациентов с АГ) у больных АГ с нормальной диастолической функцией (ДФ) и с гипертрофическим типом диастолической дисфункции (ДД) среднее значение времени изгнания в ЛА не превышало 333 мс, а при псевдонормальном типе ДД оно составило 353±10,2 мс. При этом соотношение времени ускорения ко времени изгнания (ВУ/ВИ) потока в легочной артерии в контрольной группе здоровых лиц было равно 0,45; в группе с нормальной ДФ при АГ - 0,44; а при гипертрофическом типе ДД этот коэффициент уменьшался до 0,39. При псевдонормальном типе ДД спектр кровотока в выходном тракте ПЖ приближался к нормальному (ВУ/ВИ-0,41), однако значительно увеличивалось время изгнания. Л.И. Ольбинская и А.И. Синопальников (1983) считают, что повышение диастолического давления ЛА при нормальных размерах ЛП наблюдается на фоне гиперфункции миокарда ЛЖ и не является признаком левожелудочковой недостаточности. По данным проведенного нами исследования, при гипертрофическом типе ДД средний размер ЛП и время изгнания в выходном тракте ПЖ не превышают нормальных значений, систолическая функция ЛЖ не нарушена (ФВ-69,2±2,06). Однако среднее легочное артериальное давление, рассчитанное по формуле Kitabatake et al. (1983), колебалось от 13 до 57 мм рт. ст. и у 47,6% процентов больных превышало 20 мм рт. ст. Это отражает нарушение процессов релаксации миокарда ЛЖ. При псевдонормальном типе диастолической дисфункции истощаются компенсаторные возможности сердца и полноценная систола ПЖ обеспечивается за счет удлинения времени изгнания. Только у 7 (25%) больных с псевдонормальным типом ДД время выброса не превышало 333 мс, у 5 из них сохранялась асимметрия потока в выходном тракте ПЖ и лишь у 2 (7,1%) пациентов спектр кровотока в выходном тракте ПЖ не изменился. У 52% больных этой группы среднее легочное артериальное давление, рассчитанное по формуле Kitabatake, превышало 20 мм.рт.ст.. Следует отметить, что переднезадний размер ПЖ (на фоне проводимого лечения) в группе больных с псевдонормальным типом ДД не превышал 31 мм и составил в среднем 23,8 ± 2,4 мм, трикуспидальная регургитация не превышала первую степень, у 3 больных отмечалась пастозность ног. Таким образом, при псевдонормальном типе ДД появляются первые признаки дисфункции правого желудочка – нормальная систола ПЖ обеспечивается за счет ее удлинения. При этом типе ДД чаще, чем при гипертрофическом типе встречается синдром легочной гипертензии.
В нормальных условиях диастолическое межжелудочковое взаимодействие незначительно, но при перегрузке камер сердца объемом или сопротивлением становится важным (S. Chakko, 1990). При артериальной гипертензии (В.А. Сандриков, Т.Г. Никитюк и соавт., 2004) происходит нарушение диастолической функции ПЖ, которое проявляется в длительном расслаблении ПЖ и перераспределении транстрикуспидального кровотока в поздней диастоле. Однако изучение диастолической функции сердца в основном касается левых отделов, изменения диастолической функции правого желудочка при АГ практически не изучены (В.Р. Вебер, М.П. Рубанова, 2005).
По данным проведенного нами исследования 147 пациентов, тип диастолической дисфункции ПЖ соответствовал типу диастолической дисфункции ЛЖ в 60,2% случаев. В 33% случаев диастолическая дисфункция ПЖ была легче, чем левого. В 6,8% случаев диастолическая дисфункция ПЖ была более выражена, чем ДД левого желудочка. В изучаемой группе определена умеренная корреляционная зависимость между типом диастолической функции правого желудочка и типом диастолической функции левого желудочка (коэффициент корреляции r=0,64), максимальной скоростью пика Е правого желудочка и пика Е левого желудочка (коэффициент корреляции r=0,39), соотношением Е/А транстрикуспидального кровотока и Е/А трансмитрального кровотока (r=0,44). Выявлена умеренная корреляционная зависимость между типом диастолической функции правого желудочка и
1) типом ремоделирования левого желудочка (r = 0,41),
2) толщиной передней стенки правого желудочка (r = 0,43),
3) толщиной МЖП (r = 0,38),
4) КДР ПЖ (r = 0,3).
В группе с нарушением диастолической функции правого желудочка по псевдонормальному типу (21 человек) выявлена умеренная корреляционная зависимость соотношения Е/А правого желудочка и КДР левого желудочка (коэффициент корреляции r = -0,41). Таким образом, дилатация и сферизация полости ЛЖ, повышение конечно-диастолического объема ЛЖ отрицательно сказывается и на морфо-функциональном состоянии правого желудочка. Полученные данные заставляют пересмотреть позицию, когда результаты изучения функциональных особенностей левых отделов сердца механически переносятся на правые. Диастолическая функция правого желудочка заслуживает самостоятельного изучения. Гемодинамическое и анатомическое состояние левого желудочка оказывает влияние на состояние правого желудочка, изучение состояния правого желудочка позволяет оценить вовлеченность в сердечно-сосудистый континуум большого круга кровообращения, точнее определить тяжесть ХСН.
Таким образом, поражение сердца при АГ многогранно, в патологический процесс вовлекается не только ЛЖ, но и все остальные камеры сердца. Однако современная классификация АГ содержит лишь один фактор, имеющий значение в определении поражения сердца: гипертрофию левого желудочка. Но для эффективного предупреждения хронической сердечной недостаточности необходимо четко представлять механизмы развития декомпенсации.
Результаты исследования характерных эхокардиографических критериев «гипертонического сердца». На наш взгляд, поражение сердца при АГ может быть классифицировано по степени тяжести. Ю.М. Губачев и В.В. Макиенко (2000) также считают оправданным определение стадий развития “гипертонического сердца”. Мы провели исследование, имеющее целью выявить наиболее характерные эхокардиографические критерии “гипертонического сердца” на этапе поражения органов-мишеней, а также при наличии ассоциированных клинических состояний: стенокардии, ИМ, хронической сердечной недостаточности, операции на коронарных сосудах. Однако чтобы выявить наиболее характерные признаки именно “гипертонического сердца”, из исследования были исключены пациенты с АГ при наличии зон гипокинезии, локализующихся более чем в одном сегменте.
В исследование вошли 281 пациентов АГ, среди них 130 мужчин и 151 женщина. Возраст пациентов колебался от 23 до 74 лет, средний возраст составил 52,9 ± 1,4 года. В соответствии с классификацией АГ, рекомендованной ВОЗ и Международным обществом по изучению гипертонии (1999) первая степень АГ выявлена у 125 пациентов, вторая - у 57, третья - у 99 пациентов.
Мы изучили распределение больных с различными типами геометрии ЛЖ и его диастолической функции в зависимости от степени АГ. Результаты представлены на рисунках 11,12, 13.

Рисунок 11. Распределение больных по типам геометрии ЛЖ и его диастолической дисфункции при 1 степени АГ

Рисунок 12. Распределение больных по типам геометрии ЛЖ и его диастолической дисфункции при 2 степени АГ
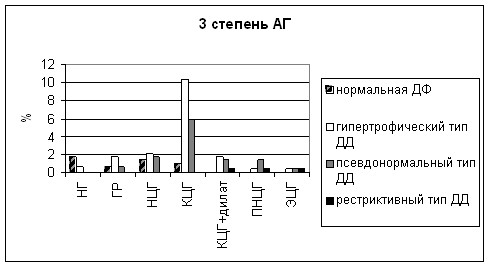
Рисунок 13. Распределение больных по типам геометрии ЛЖ и его диастолической дисфункции при 3 степени АГ
Диаграммы демонстрируют, что при первой степени АГ чаще встречаются пациенты без признаков поражения сердца, достаточно большую группу составляют больные АГ с гипертрофическим ремоделированием, НЦГ и КЦГ с сохраненной диастолической функцией ЛЖ. При второй и третьей степени АГ резко увеличивается доля пациентов с диастолической дисфункцией и увеличивается количество пациентов, у которых гипертрофия ЛЖ сочетается с дилатацией полости ЛЖ.
Преимущественным поражением сердца при АГ является концентрическая гипертрофия ЛЖ, которая в нашем исследовании встретилась в 44,6% случаев, чаще она сочеталась с гипертрофическим типом ДД ЛЖ (25,4 %).
Геометрический тип ЛЖ отражает тяжесть поражения сердца, но при этом диастолическая дисфункция в той или иной степени ухудшает прогноз заболевания. Многообразие сочетаний различных типов геометрии ЛЖ и его диастолической дисфункции затрудняет оценку тяжести поражения сердца. Поэтому предлагается сгруппировать их и выделить эхокардиографический (морфофункциональный) класс “гипертонического сердца”. Первый класс – начальная стадия поражения сердца, второй класс – умеренно выраженное поражение сердца, третий класс – тяжелое поражение сердца и четвертый – конечная стадия, необратимое поражение сердца.
К начальной стадии поражения сердца мы предлагаем относить нормальный тип геометрии ЛЖ с гипертрофическим типом ДД ЛЖ, ремоделирование ЛЖ с сохраненной ДФ и с нарушением диастолической функции ЛЖ по гипертрофическому типу, однако диастолическая функция ПЖ должна быть сохранена. Умеренно выраженное поражение сердца включает – гипертрофию ЛЖ без дилатации его полости с нормальной ДФ ЛЖ или с гипертрофическим типом ДД ЛЖ, а также ремоделирование ЛЖ с нарушением его диастолической функции по псевдонормальному типу; диастолическая функция правого желудочка сохранена или нарушена по гипертрофическому типу. Гипертрофия ЛЖ при отсутствии расширения его полости, но в сочетании с псевдонормальным типом ДД ЛЖ, гипертрофическим или псевдонормальным типом ДД ПЖ, концентрическая ГЛЖ с дилатацией полости ЛЖ, псевдонормоцентрическая ГЛЖ – характерны для тяжелого поражения сердца. Конечная стадия, необратимое поражение сердца, – характеризуются обнаружением эксцентрической ГЛЖ и, как правило, сопровождается тяжелыми нарушениями ДФ обоих желудочков. В эхокардиографическом заключении необходимо указывать состояние систолической функции ЛЖ у пациента с эхокардиографическими признаками гипертонического сердца. Известно, что систолическая дисфункция может быть манифестированной и бессимптомной. Однако клинические признаки ХСН будут отражаться в диагнозе функциональным классом НК, что также как и обнаружение зон гипокинезии, переводит заболевание из класса поражения органов мишеней в класс наличия ассоциированных заболеваний.
Распределение пациентов с различными эхокардиографическими классами ГС в зависимости от степени АГ представлено на рисунке 14.
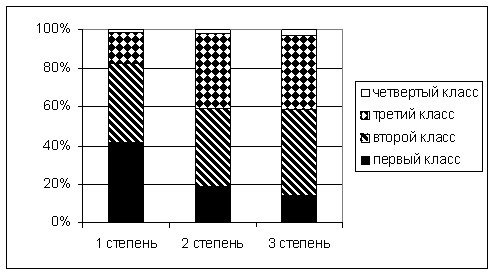
Рисунок 14. Распределение эхокардиографических классов гипертонического сердца в зависимости от степени артериальной гипертензии
Таким образом, врач ультразвуковой диагностики, делая свое заключение, указывает эхокардиографический класс гипертонического сердца с расшифровкой геометрического типа ЛЖ и его диастолической и систолической дисфункции, отмечает, насколько вовлечен в процесс малый круг кровообращения и правый желудочек. Это поможет врачу-клиницисту оценить тяжесть поражения сердца у конкретного пациента на основании данных ЭХОКГ и других методов исследования, выбрать план медикаментозного воздействия, контролировать его эффективность.
Результаты динамического наблюдения за больными АГ с ремоделированием сердца на фоне гипотензивной терапии. Имеющиеся данные доказательной кардиологии свидетельствуют о том, что эффективное снижение АД является необходимым, но недостаточным условием эффективности антигипертензивных препаратов. Не вызывает сомнений, что при лечении АГ у больных с ГЛЖ необходимо применять препараты, не только оказывающие гипотензивное действие, но имеющие также доказанную способность к снижению риска развития тяжелых ССЗ (Гиляревский С.Р., 2005).
В соответствии с основной целью нашего исследования мы изучили возможности эхокардиографического контроля эффективности гипотензивного лечения. Проведено длительное (в течение 7 лет) исследование 132 больных АГ. Мужчин было – 59, женщин – 73, их средний возраст составил 51,9±1,6 лет. Закончили исследование в установленные сроки – 111 (84,1%) человек, за период наблюдения умерло 6 (4,5%) пациентов. В 2 случаях причиной смерти был инсульт, в 2 – острая сердечная недостаточность. Один больной умер от онкозаболевания, один – в результате суицида. К концу исследования по различным причинам не осмотрено 15 (13,5%) человек.
Протокол проспективного исследования включал общеклиническое обследование, ЭКГ, общепринятые лабораторные исследования. ЭхоКГ проводилось при включении в исследование, через 4 месяца, через год и через 3-6 лет после начала исследования. Средний срок наблюдения составил – 4±0,24 года, количество осмотров одного больного от 3-х до 9-ти, в среднем – 4.
На конец осмотра 12 (10,8%) пациентов не принимали лекарств длительное время (более 1 года), что соответствует показателю не лечившихся пациентов на начало наблюдения, однако количество пациентов получающих несовременные гипотензивные средства резко сократилось за период наблюдения – от 18 до 2-х человек. Таким образом, количество пациентов, сознательно отказывающихся от приема гипотензивных средств, на протяжении наблюдения составило около 10%.
В начале исследования (1998-99) нерегулярно принимали лекарства или не лечились вообще 75 (56,8%) человек, регулярно лечились 57 (43,2%) человек. К концу исследования 90 (81,1%) человек стали принимать лекарства регулярно, однако только тридцать девять (35,1%) пациентов лечились эффективно и достигли целевого уровня АД. Таким образом, за период с 1998 г. по 2005 г. улучшилась приверженность пациентов к лечению, но, несмотря на это, только треть пациентов достигает целевого уровня АД.
По данным литературы (Бойцов С.А., 2005) в последние годы замедлился рост показателей эффективности контроля уровня АД, что может быть расценено, как свидетельство исчерпания резервов существующей системы лечения АГ. Действительно, основной скачок показателей контроля за уровнем АД состоялся в период между 1976-80 гг. и 1988-1991 гг. – с 10% до 29% (в 3 раза!), когда собственно и создавалась действовавшая до сих пор система. В дальнейшем наступила практически стагнация в динамике этих показателей – с 1991 г. по 2000г. количество больных АГ, достигающих целевого уровня АД, возросло только на 5% (с 29% до 34%) (Бойцов С.А., 2005). Данные нашего исследования соответствуют этим показателям.
Пациенты были распределены на 3 группы. В первую группу вошли 39 пациентов, достигнувших целевого уровня АД. Все пациенты этой группы закончили исследование. Во вторую группу вошли 60 пациентов, которые принимали лекарства регулярно, но не достигли целевого уровня АД. 51 пациент закончили исследование, трое умерло (один – от острой сердечной недостаточности на фоне тяжелого нарушения ритма, у двоих причиной смерти были не сердечно-сосудистые заболевания). В третью группу вошли 33 пациента, которые принимали лечение не регулярно и не достигли целевого уровня АД. 21 пациент этой группы закончили исследование, трое умерло: 2 – от инсульта, 1 – от острой сердечной недостаточности. Эффективность лечения оценивалась по частоте развития конечной композитной (комбинированной) точки, включавшей случаи смерти, нефатального инфаркта миокарда, нефатального инсульта, транзиторной ишемической атаки, дисциркуляторной энцефалопатии, нестабильной стенокардии, появления или прогрессирования признаков хронической сердечной недостаточности, проведение реваскуляризации, формирование порока аортального клапана в результате кальциноза клапанных структур. Определялось отношение абсолютного количества этих случаев в группе к количеству пациентов.
Основным эхокардиографическим критерием был класс гипертонического сердца, который оценивался через год и через 3-7 лет. Положительной динамикой считали переход в класс с менее тяжелым поражением сердца, отрицательной - переход в класс с более тяжелым поражением сердца относительно первоначального исследования.
Дополнительным эхокардиографическим критерием была динамика геометрического типа и диастолической дисфункции ЛЖ, индекса ММЛЖ.
Определялась однонаправленная положительная, однонаправленная отрицательная динамика геометрических типов и диастолической дисфункции, отсутствие динамики и разнонаправленная динамика через 1 год наблюдения и в конце исследования.
Положительной однонаправленной динамикой считали:
1) переход геометрического типа ЛЖ в менее тяжелый (ПНЦГ, КЦГ+дилат КЦГ НЦГ ремоделирование норма) и типа диастолической дисфункции в менее тяжелый (рестриктивный псевдонормальный гипертрофический нормальный) через год и в конце наблюдения, сравнивая результат с предыдущим исследованием, а так же стабилизацию ранее достигнутого положительного результата.
2) улучшение одного параметра (геометрического типа ЛЖ или диастолической функции ЛЖ) при стабильности второго.
Отрицательной динамикой считали переход геометричекого типа и/или типа диастолической дисфункции в более тяжелый через год и в конце наблюдения, сравнивая результат с предыдущим исследованием, а также стабилизацию ранее достигнутого отрицательного результата; ухудшение одного параметра при стабильности второго.
Разнонаправленной динамикой считали улучшение одного параметра при ухудшении второго. Распределение больных по степени АГ в группах представлено на рисунке 15.

Рисунок 15. Распределение больных по степени АГ в группах
Результаты исследования демонстрируют, что только при достижении целевого уровня АД достоверно улучшаются структурно-функциональные показатели сердца, при сравнении результатов первой и третьей групп (р=0,001). Причем, в первой группе достоверно (р=0,05) увеличивается количество пациентов с однонаправленной положительной динамикой геометрического типа и диастолической функции ЛЖ к концу исследования (рисунок 16).
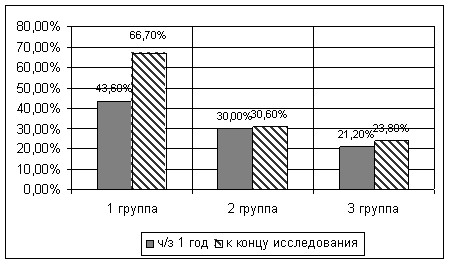
Рисунок 16. Относительное количество пациентов с однонаправленной положительной динамикой геометрического типа и диастолической дисфункции сердца в зависимости от характера лечения
Эти результаты подтверждаются и результатами наблюдения за динамикой индекса ММЛЖ (таблица 2).
Таблица 2.
Динамика индекса массы миокарда ЛЖ (г/м2) на этапах длительного наблюдения (М± 2m)
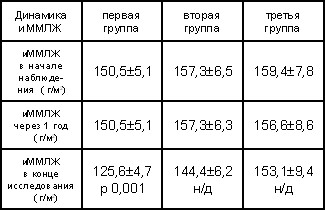
Однако, относительное количество пациентов с улучшением диастолической функции ЛЖ (при изучении этого признака независимо от геометрического типа) за период наблюдения увеличилось недостоверно. По данным Арутюнова Г.П. и соавт. (2000), даже через 12 месяцев стабильно нормального АД на фоне терапии у 20% больных АГ сохраняются явления диастолической дисфункции ЛЖ. В нашем исследовании у 16 (41%) пациентов со стабилизацией АД на целевом уровне на протяжении всего периода наблюдения (3-7 лет) диастолическая функция ЛЖ не улучшалась, а у 9 (23%) больных она ухудшилась. Известно, что не все препараты, достоверно снижающие АД, улучшают диастолическую функцию сердца, и эти пациенты нуждаются в коррекции лечения.
В доступной литературе нет данных об изменении типов ремоделирования ЛЖ и воспроизводимости этого показателя при длительном наблюдении. По данным нашего исследования тип геометрии ЛЖ является достаточно устойчивым параметром, однако в процессе продолжительного наблюдения всей группы пациентов с АГ на фоне гипотензивной терапии наблюдались следующие варианты перехода типов ремоделирования ЛЖ (рисунок 17):
НЦГ КЦГ+дилат
ГР КЦГ ПНЦГ
НГ ЭЦГ
Рисунок 17. Варианты взаимопереходов геометрических типов ЛЖ при длительном наблюдении
При анализе изменения характера геометрии ЛЖ в группе с эффективным лечением было выявлено, что тип ремоделирования изменился в положительную сторону в 59% случаев. При этом наблюдались взаимные переходы: КЦГГР (3чел), КЦГНЦГГР (4 чел), КЦГНЦГ (6 чел), КЦГГРНГ (1 чел), КЦГНЦГНГ (1чел), НЦГГР (3 чел), НЦГНГ (2 чел), ГРНГ (3 чел). В 28,2% случаев тип геометрии левого желудочка в этой группе не изменился, в 12,8 % – ухудшился.
Таким образом, основной целью лечения пациентов с АГ должно быть снижение повышенного АД и поддержание его на целевом уровне, улучшение структурно-функциональных показателей сердца. Результаты нашего исследования подтверждают данные многочисленных исследований, завершившихся в последние годы, что только «жесткий» контроль АД может достоверно снизить частоту сердечно-сосудистых осложнений (рисунок 18).

Рисунок 18. Эффективность различных вариантов лечения
Среди пациентов, достигнувших целевого снижения АД, с помощью одного антигипертензивного препарата лечились 16 (41%), 21 (54%) применяли комбинации двух препаратов и более.
Однако эхокардиографический контроль необходим и в группе эффективного гипотензивного лечения. Так у пяти (12,8%) пациентов этой группы, несмотря на стабилизацию целевого уровня АД, отмечалась отрицательная динамика структурно-функциональных показателей и прогрессирование симптомов сердечной недостаточности, что требовало коррекции лечения.
Учитывая достаточно большой размер ошибки измерения индекса ММЛЖ, при динамическом наблюдении за ГЛЖ на фоне лечения у конкретного пациента изучать только этот показатель недостаточно. Индекс ММЛЖ хорошо отражает эффективность лечения в достаточно большой группе, когда нивелируется ошибка измерения. Однако в каждом конкретном случае, эта величина очень изменчива и не объективна. Мы предлагаем при динамическом наблюдении учитывать геометрический тип ЛЖ, тип диастолической дисфункции ЛЖ, класс гипертонического сердца, так как эти показатели более постоянные и качественно отражают динамику структурно-функциональных изменений сердца. Отсутствие адекватного контроля за АД в популяции больных с АГ является одной из наиболее острых социальных и медицинских проблем российской кардиологии. По данным нашего исследования эффективное снижение АД до целевого уровня и стабилизация его на этом уровне длительное время (более 1 года) осуществилась у 35,1% пациентов, находившихся под наблюдением от 3-х до 7 лет. Причем, среди пациентов с первой степенью АГ 44,6% больных лечились адекватно, а среди пациентов со второй и третьей степенью АГ лишь 18,6% достигли целевого АД.
Выводы
1. Наиболее характерным поражением сердца при АГ является концентрическая гипертрофия ЛЖ, преимущественно симметричная, с равномерным утолщением стенок и папиллярных мышц и нарушением его диастолической функции по гипертрофическому типу. Эхокардиографическая классификация поражения сердца при АГ по степени тяжести должна учитывать структурное и функциональное состояние левого и правого желудочков.
2. Основными эхокардиографическими параметрами типов геометрии ЛЖ являются не только относительная толщина его стенок и индекс массы миокарда, но также индекс конечно-диастолического размера полости ЛЖ, локальная гипертрофия его стенок и папиллярных мышц, выявленные в В-режиме. Гипертрофия левого желудочка с нерасширенной полостью и относительной толщиной стенки 0,35-0,44 является относительно благоприятным вариантом гипертрофии.
3. Геометрический тип ЛЖ является предиктором прогноза ХСН. Дилатация полости ЛЖ является неблагоприятным прогностическим признаком. В группе больных с дилатацией полости ЛЖ отмечается достоверное (p<0,001) снижение фракции выброса и усиление симптомов ХСН. Митральная регургитация играет существенную роль в переходе от концентрической гипертрофии к эксцентрической, способствуя дилатации полости ЛЖ.
4. Подтверждено наличие умеренной корреляционной связи между показателями гипертрофического ремоделирования ЛЖ и параметрами его диастолической дисфункции при гипертрофическом типе (r от 0,3 до 0,47). При псевдонормальном и рестриктивном типе ДД эта связь очень слабая. В последнем случае выявлена умеренная корреляционная связь между параметрами диастолической дисфункции ЛЖ и средним давлением в легочной артерии (r =0,37), конечно-систолическим размером ЛЖ (r =0,38).
5. Тяжесть диастолической дисфункции ЛЖ определяет частоту появления синдрома легочной гипертензии при АГ. Выявлена умеренная корреляционная зависимость между нарушением диастолической функции левого и правого желудочков, между типом диастолической функции правого желудочка и морфологией как правого, так и левого желудочков.
6. Эхокардиографический контроль позволяет оценить эффективность гипотензивной терапии у конкретного больного, учитывая динамику геометрического типа ЛЖ и его диастолической функции, класса “гипертонического сердца”. При условии длительной адекватной терапии у больных с АГ возможно обратное развитие ремоделирования сердца.
Практические рекомендации
Для стратификации риска больных АГ целесообразно определять геометрический тип ремоделирования левого желудочка, тип диастолической дисфункции левого и правого желудочка, эхокардиографический класс «гипертонического сердца». Использование предложенных нами номограмм для определения эхокардиографической геометрии левого желудочка и классификации «гипертонического сердца» поможет врачу-клиницисту быстро оценить тяжесть поражения сердца у конкретного пациента с АГ, наметить план медикаментозного воздействия, контролировать его эффективность. Для установления ремоделирования сердца при нормальном индексе ММЛЖ обязательно исследование в В-режиме с целью выявления локальной гипертрофии стенок ЛЖ и папиллярных мышц.
При лечении больных с гипертрофией ЛЖ обратное развитие его ремоделирования наиболее вероятно у пациентов, добившихся стойкой стабилизации АД на целевом уровне и имеющих 1 степень АГ. Эффект от лечения следует ожидать в течение первых 6-12 месяцев терапии.
Эхокардиографический контроль гипотензивного лечения следует проводить не реже 1 раза в 4-6 месяцев в период подбора адекватной терапии и 1-2 раз в год при стабилизации АД на целевом уровне для изучения структурно-функционального состояния сердца и коррекции лечения, предупреждения сердечно-сосудистых осложнений.
Список работ, опубликованных по теме диссертации
1. Белоусов Ю.В., Демидова Н.Ю. Влияние патологической ориентации ПСМК на диастолическую функцию гипертрофированного ЛЖ //Сборник статей V Межрегионального кардиологического форума “Профилактика и своевременное лечение – залог успеха в кардиологии”. Н.Новгород. 15-18 мая 2201 г. С.32-34.
2. Белоусов Ю.В., Демидова Н.Ю. Характерные морфологические признаки гипертрофированного ЛЖ при АГ и ГКМП в зависимости от степени развития гипертрофии. //Сборник статей V Межрегионального кардиологического форума “Профилактика и своевременное лечение – залог успеха в кардиологии”. Н.Новгород. 15-18 мая 2201 г. С.34-36.
3. Белоусов Ю.В., Демидова Н.Ю. Зависимость диастолической функции ЛЖ от выраженности гипертрофии и других его морфологических особенностей. //Патология кровообращения и кардиохирургия. Новосибирск. 2001. № 2. С.38-45.
4. Белоусов Ю.В., Демидова Н.Ю. Морфологические особенности гипертрофированного левого желудочка при АГ и ГКМП. //Патология кровообращения и кардиохирургия. Новосибирск. 2001. № 3. С.56-63.
5. Демидова Н.Ю. Изучение динамики ГЛЖ и диастолической функции ЛЖ на этапах лечения. //Патология кровообращения и кардиохирургия. Новосибирск. 2001. № 4. С.70-74.
6. Белоусов Ю.В., Демидова Н.Ю. Морфологические особенности гипертрофированного левого желудочка при АГ и ГКМП //Сборник тезисов IV Всероссийской научно-практической конференции. Новосибирск. 2001. С. 157-158.
7. Белоусов Ю.В., Демидова Н.Ю. Зависимость диастолической функции ЛЖ от выраженности гипертрофии и других его морфологических особенностей. //Сборник тезисов IV Всероссийской научно-практической конференции. Новосибирск. 2001. С. 82-83.
8. Демидова Н.Ю. Результаты комбинированного лечения ингибиторами АПФ и b-блокаторами больных с гипертрофией левого желудочка. //Эхография. 2001. №4. С.357-359.
9. Белоусов Ю.В., Демидова Н.Ю. Морфологические особенности гипертрофированного ЛЖ при АГ и ГКМП и их влияние на диастолическую функцию ЛЖ. //Сборник тезисов II Российского национального конгресса кардиологов. Москва. 9-11 октября. 2001. С.42.
10. Белоусов Ю.В., Демидова Н.Ю. Зависимость диастолической функции ЛЖ от выраженности гипертрофии и других его морфологических особенностей. //Нижегородский медицинский журнал. 2001. № 4. С. 29-38.
11. Демидова Н.Ю. Сравнительный результат длительного неконтролируемого гипотензивного лечения при гипертрофии левого желудочка. //Эхография. 2001. Том 2. №4. С.434.
12. Демидова Н.Ю. Влияние комбинированного лечения ингибиторами АПФ и b-блокаторами на гипертрофию левого желудочка. //Эхогрфия. 2001. Том 2. №4. С. 434.
13. Демидова Н.Ю. Зависимость нарушения диастолической функции левого желудочка от выраженности его гипертрофического ремоделирования. //Эхография. 2001. Том 2. №4. С. 434.
14. Демидова Н.Ю. Зависимость нарушения диастолической функции левого желудочка от выраженности его гипертрофического ремоделирования при артериальной гипертонии и гипертрофической кардиомиопатии. //Патология кровообращения и кардиохирургия. Новосибирск. 2002. № 2. С.51-56.
15. Демидова Н.Ю. Случай семейной гипертрофической кардиомиопатии с преимущественной гипертрофией папиллярных мышц. //Патология кровообращения и кардиохирургия. Новосибирск. 2002. № 2. С.72-76.
16. Демидова Н.Ю., Белоусов Ю.В. Анатомо-функциональная характеристика гипертрофированного миокарда при артериальной гипертензии и гипертрофической кардиомиопатии. //Ультразвуковая и функциональная диагностика. Москва. 2002. № 2. С. 176.
17. Белоусов Ю.В., Демидова Н.Ю. Оценка эффективности комбинации ингибиторов АПФ и b-блокаторов при лечении больных с гипертрофией левого желудочка. // Ультразвуковая и функциональная диагностика. Москва. 2002. № 2. С. 170.
18. Белоусов Ю.В., Демидова Н.Ю. Морфологические особенности гипертрофированного левого желудочка при артериальной гипертензии и гипертрофической кардиомиопатии //Нижегородский медицинский журнал. 2002. №3. С. 11-19.
19. Демидова Н.Ю. Гипертрофическое ремоделирование и диастолическая дисфункция левого желудочка: ранние признаки декомпенсации. //Патология кровообращения и кардиохирургия. Новосибирск. 2003. № 2. С.59-62.
20. Демидова Н.Ю. Анатомо-функциональная характеристика гипертрофированного миокарда при артериальной гипертензии
//Материалы научно-практической конференции Федерального управления “Медбиоэкстрем”. Саров, 2-4 апреля 2003. С.75-78.
21. Демидова Н.Ю. Соответствует ли классификация геометрических типов ремоделирования левого желудочка теории сердечно-сосудистого континуума? //Эхография. 2004. Т. 5. № 1. С. 83-87.
22. Демидова Н.Ю. Диастолическая дисфункция левого желудочка и синдром легочной гипертензии у лиц с гипертонической болезнью. //Эхография. 2004. Т.5. № 3. С. 222-225.
23. Белоусов Ю.В., Демидова Н.Ю. Современные взгляды на ремоделирование левого желудочка у пациентов с артериальной гипертензией. //Материалы конференции, посвященной 10-летию отделения ультразвуковой диагностики. Москва, 4-6 октября 2004. С. 58.
24. Белоусов Ю.В., Демидова Н.Ю. Современный взгляд на классификацию геометрических типов ремоделирования левого желудочка. //Материалы конференции, посвященной 10-летию отделения ультразвуковой диагностики. Москва, 4-6 октября 2004. С. 59.
25. Демидова Н.Ю. Синдром легочной гипертензии у лиц с гипертонической болезнью. //Материалы конференции, посвященной 10-летию отделения ультразвуковой диагностики. Москва, 4-6 октября 2004. С. 65.
26. Демидова Н.Ю., Белоусов Ю.В. Диастолическая функция левого желудочка при его гипертрофии // Эхография. 2004. Т.5. № 4. С. 362-366.
27. Демидова Н.Ю., Белоусов Ю.В. Классификация геометрических типов ремоделирования левого желудочка и теория сердечно-сосудистого континуума. //Материалы I общероссийского съезда, V ежегодной конференции общества специалистов по сердечной недостаточности. Москва, 7-9 декабря 2004. С. 114.
28. Демидова Н.Ю. Диастолическая функция левого желудочка и легочная гипертензия у лиц с гипертонической болезнью.
//Сборник трудов Центральной медсанчасти №50. Выпуск 1. 2004. С. 62-65.
29. Демидова Н.Ю., Белоусов Ю.В. Ремоделирование левого желудочка как отражение теории сердечно-сосудистого континуума. //Ремедиум. Специальный выпуск для врачей. Атеросклероз. Июнь 2005. С. 57-59.
30. Демидова Н.Ю., Белоусов Ю.В. Современный взгляд на классификацию геометрических типов ремоделирования левого желудочка. //Ремедиум. Специальный выпуск для врачей. Атеросклероз. Июнь 2005. С. 59-62.
31. Демидова Н.Ю., Белоусов Ю.В. Эхокардиографические признаки “гипертонического сердца”. //Ремедиум. Специальный выпуск для врачей. Атеросклероз. Июнь 2005. С. 62-65.
32. Демидова Н.Ю. Эхокардиографические геометрические типы левого желудочка как отражение теории сердечно-сосудистого континуума. //Патология кровообращения и кардиохирургия. Новосибирск. 2005. № 3. С.70-74.
33. Демидова Н.Ю., Белоусов Ю.В. Прогностическое значение геометрических типов левого желудочка в риске развития ХСН у больных с артериальной гипертензией. //Тезисы VI ежегодной конференции общества специалистов по сердечной недостаточности. Москва, 7-9 декабря 2005. С. 65-66.
34. Демидова Н.Ю. Эхокардиография в диагностике “гипертонического сердца”. //Сборник трудов Центральной медсанчасти №50. Выпуск 2. 2005. С. 19-25.
35. Демидова Н.Ю. Результаты длительного эхокардиографического контроля за эффективностью гипотензивного лечения. //Патология кровообращения и кардиохирургия. Новосибирск. 2006. № 3. С.75-81.
36. Демидова Н.Ю., Белоусов Ю.В. Эхокардиографические признаки «гипертонического сердца» //Патология кровообращения и кардиохирургия. Новосибирск. 2006. № 4. С.75-78.
37. Демидова Н.Ю. Возможности эхокардиографической оценки эффективности гипотензивного лечения при длительном проспективном наблюдении //Тезисы V съезда специалистов ультразвуковой диагностики Поволжья. Пренатальная диагностика. 2007. №1. Том 6. С. 61.
38. Демидова Н.Ю. Прогностическое значение вариантов ремоделирования левого желудочка у больных с артериальной гипертензией //Тезисы V съезда специалистов ультразвуковой диагностики Поволжья. Пренатальная диагностика. 2007. №1. Том 6. С. 61-62.
39. Демидова Н.Ю. Изучение состояния малого круга кровообращения и функции ПЖ у лиц с гипертонической болезнью //Тезисы V съезда специалистов ультразвуковой диагностики Поволжья. Пренатальная диагностика. 2007. №1. Том 6. С. 62.
40. Демидова Н.Ю. Диастолическая функция правого желудочка при различных типах диастолической дисфункции левого желудочка у больных артериальной гипертензией. //Патология кровообращения и кардиохирургия. Новосибирск. 2007. № 3. С.55-58.
41. Демидова Н.Ю. Результаты исследования диастолической функции правого желудочка у больных артериальной гипертензией. //Сборник работ сотрудников Клинической больницы №50. Выпуск 4. 2007. С. 81-84.
42. Демидова Н.Ю. Результаты изучения диастолической функции правого желудочка у пациентов с артериальной гипертензией. //Ультразвуковая и функциональная диагностика. Москва. 2007. № 3. C.88.
43. Демидова Н.Ю., Белоусов Ю.В. Возможности эхокардиографии в определении тяжести поражения сердца при артериальной гипертонии (АГ). //Ультразвуковая и функциональная диагностика. Москва. 2007. № 3.C.89.
44. Демидова Н.Ю., Белоусов Ю.В. Результаты эхокардиографической оценки эффективности гипотензивного лечения. //Ультразвуковая и функциональная диагностика. Москва. 2007. № 3. C.89.
45. Демидова Н.Ю. Варианты ремоделирования левого желудочка как предикторы развития ХСН. //Тезисы II конгресса (VIII ежегодной конференции) общества специалистов по сердечной недостаточности. Москва, 5-7 декабря 2007.
Сокращения
АГ – артериальная гипертензия
АГЛЖ – асимметричная гиперторфия левого желудочка
АД – артериальное давление
АК – аортальный клапан
АО – аорта
БЛНПГ – блокада левой ножки пучка Гиса
ВОЛЖ – выходной отдел ЛЖ
ГБ – гипертоническая болезнь
ГЛЖ – гипертрофия левого желудочка
ГКМП – гипертрофическая кардиомиопатия
ГР – гипертрофическое ремоделирование
ДКМП – дилатационная кардиомиопатия
ДД – диастолическая дисфункция
ДФ – диастолическая функция
ЗСЛЖ – задняя стенка ЛЖ
ИАПФ – ингибиторы ангиотензинпревращающего фермента
ИБС – ишемическая болезнь сердца
ИММЛЖ – индекс массы миокарда ЛЖ
ИКДР – индекс конечно-диастолического размера ЛЖ
КА – коэффициент асимметрии
КДО – конечно-диастолический объем ЛЖ
КДР – конечно-диастолический размер ЛЖ
КСО – конечно-систолический объем ЛЖ
КСР – конечно-систолический размер ЛЖ
КЦГ – концентрическая гипертрофия ЛЖ
КЦГ+дилат. – концентрическая гипертрофия ЛЖ с дилатацией его полости
ЛГ – легочная гипертензия
ЛЖ (LV) – левый желудочек
ЛП (LA) – левое предсердие
МЖП – межжелудочковая перегородка
МК – митральный клапан
ММЛЖ (LVMass) – масса миокарда левого желудочка
МР (MReg) – митральная регургитация
НГ – нормальная геометрия ЛЖ
НЦГ – нормоцентрическая гипертрофия ЛЖ
ОТС – относительная толщина стенки ЛЖ
ПЖ (RV) – правый желудочек
ПП (RA) – правое предсердие
ПСМК (AML) – передняя створка митрального клапана
ПНЦГ – псевдонормоцентрическая гипертрофия ЛЖ
СН – сердечная недостаточность
ТМДП – трансмитральный диастолический поток
УЗД – ультразвуковая диагностика
ФВ – фракция выброса
ЭЦГ – эксцентрическая гипертрофия ЛЖ
ALPM – переднелатеральная папиллярная мышца
АТ – время ускорения раннего диастолического наполнения ЛЖ
DT – время замедления раннего диастолического наполнения ЛЖ
IVRT – период изоволюмического расслабления
LVOT – выходной отдел ЛЖ
РМРМ – заднемедиальная папиллярная мышца

