Атрофические и метаболические изменения в головном мозге и их связь с неврологическими нарушениями при рассеянном склерозе.
На правах рукописи
Ильвес
Александр Геннадьевич
Атрофические и метаболические изменения в головном мозге и их связь с неврологическими нарушениями при рассеянном склерозе.
14.00.16 – патологическая физиология
14.00.13 – нервные болезни
Автореферат
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2008
Диссертация выполнена в Институте мозга человека Российской академии наук
Научные руководители:
доктор медицинских наук
профессор Столяров Игорь Дмитриевич
академик РАМН
профессор Скоромец Александр Анисимович
Официальные оппоненты:
доктор медицинских наук
профессор Тюкавин Александр Иванович
доктор медицинских наук
профессор Помников Виктор Григорьевич
Ведущая организация: Военно-медицинская академия имени С.М. Кирова
Защита диссертации состоится «___»_________2008 года в ___часов на заседании диссертационного совета Д 208.089.02 при ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию» (191015, г. Санкт-Петербург, ул. Кирочная, д. 41).
С диссертацией можно ознакомиться в фундаментальной библиотеке ГОУ ДПО «Санкт-Петербургская медицинская академия последипломного образования Федерального агентства по здравоохранению и социальному развитию» (195196, г. Санкт-Петербург, Заневский пр., д.1/82).
Автореферат разослан «___»_________2008 года
Ученый секретарь диссертационного совета
доктор медицинских наук доцент Г.Н. Горбунов
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ.
Актуальность темы. Успехи в изучении патогенеза рассеянного склероза (РС) предопределили появление терапии, замедляющей развитие заболевания. Однако остаются неясными механизмы развития и прогрессирования неврологических симптомов у больных РС, что препятствует разработке методов восстановления утраченных функций.
РС – заболевание с аутоиммунными механизмами, характеризующееся появлением ограниченных зон воспаления, демиелинизации и аксонального повреждения в центральной нервной системе, которые могут быть выявлены морфологически и с помощью магнитно-резонансной томографии (МРТ). Множественные очаги демиелинизации являются наиболее ранней и частой находкой при МРТ исследовании, однако большинство очагов остаются «клинически немыми».
Общепризнанным является диффузное поражение белого и серого вещества ЦНС, приводящее к развитию атрофии головного и спинного мозга. Атрофия, вероятно, связана с Валлеровской дегенерацией, ретро- и антеградной нейродегенерацией (Coleman M.P., Perry V.H., 2002). В ряде МРТ исследований показано вовлечение в атрофический процесс при РС серого вещества коры и подкорковых ядер уже на самых ранних стадиях заболевания (Chard D.T. et al., 2004; Davies G.R. et al., 2005).
Неуклонно нарастающая инвалидизация пациентов чаще всего связана с нарушениями движения. Выраженность неврологических симптомов при РС в большой степени связана с общей атрофией головного мозга, проявляющейся уменьшением объема мозговой паренхимы, увеличением желудочков и субарахноидальных пространств. Однако степень и последовательность вовлечения двигательной коры, мозжечка и базальных ганглиев в патологический процесс и влияние локальной атрофии на развитие клинической картины РС остаются неясными (Simon J.H., 2006). Измерение тотальной атрофии широко используется в оценке эффективности новых методов патогенетической терапии РС. Однако до настоящего времени недостаточно сведений о механизмах, лежащих в основе атрофии, факторах и причинах вариабельности проявлений атрофического процесса у различных пациентов и при различных типах течения РС (Miller D.H. et al., 2002; Simon J.H., 2006).
Наряду с атрофическими процессами при РС описана функциональная реорганизация серого вещества головного мозга, наличие которой показано в работах с использованием функциональной МРТ и позитронно-эмиссионной томографии (ПЭТ). По мнению ряда авторов, реорганизация носит компенсаторный характер и развивается по мере прогрессирования заболевания (Filippi M. et al., 2003).
Изучение соотношения процессов атрофии и функциональной реорганизации серого вещества у пациентов с РС может способствовать выявлению механизмов, лежащих в основе прогрессирования заболевания и развития тяжелой нетрудоспособности.
Цель исследования: определение взаимосвязи атрофии и скорости метаболизма глюкозы в головном мозге с выраженностью неврологических расстройств у больных рассеянным склерозом с различной инвалидизацией.
В задачи работы входило:
1. Выполнить неврологическое обследование больных рассеянным склерозом, оценить выраженность неврологических нарушений по шкале функциональных систем и расширенной шкале инвалидизации.
2. Определить с помощью позитронно-эмиссионной томографии изменения скорости метаболизма глюкозы в головном мозге больных рассеянным склерозом по сравнению со здоровыми добровольцами.
3. Оценить с помощью магнитно-резонансной томографии изменения объема мозговых структур у больных рассеянным склерозом по сравнению со здоровыми добровольцами.
4. Сопоставить изменения скорости метаболизма глюкозы в головном мозге и объема мозговых структур с выраженностью неврологических нарушений у пациентов с различной степенью инвалидизации.
Научная новизна работы. В результате комплексного сравнительного анализа клинических проявлений, изменений объема структур головного мозга и скорости метаболизма глюкозы в сером веществе головного мозга показано, что у больных рассеянным склерозом наряду с общей атрофией головного мозга наблюдается локальная атрофия структур, содержащих серое вещество (таламус, базальные ганглии, мозжечок). Установлено, что процессы тотальной и локальной атрофии могут развиваться независимо друг от друга.
Выявлена последовательность вовлечения структур головного мозга в атрофические процессы, коррелирующая с этапами развития инвалидизации при рассеянном склерозе. Установлено, что атрофия чечевицеобразных ядер и мозжечка имеет место уже у пациентов с минимальными неврологическими нарушениями. При умеренной инвалидизации у больных выявлено уменьшение объема мозговой паренхимы, увеличение субарахноидальных пространств, желудочков и локальная атрофия хвостатых ядер. Показано, что параллельно атрофическим процессам в головном мозге развивается функциональная реорганизация серого вещества, направленная на компенсацию неврологического дефицита. Продемонстрирована важная роль атрофии таламуса и базальных ганглиев в развитии выраженной инвалидизации больных.
Теоретическая и практическая значимость работы. Полученные данные расширяют представления о роли поражения серого вещества головного мозга в патогенезе рассеянного склероза и углубляют знания о механизмах развития клинических проявлений данного заболевания. Дальнейшие исследования в этом направлении позволят понять роль повреждения подкорковых структур в генезе двигательных нарушений не только при рассеянном склерозе, но и при других демиелинизирующих и нейродегенеративных заболеваниях.
Измерение локальной атрофии и скорости метаболизма глюкозы в различных структурах головного мозга является информативным способом диагностики стадии и прогноза течения заболевания. Определение степени структурно-метаболических нарушений в головном мозге целесообразно использовать для выбора тактики лечения и оценки эффективности новых методов терапии рассеянного склероза.
Основные положения, выносимые на защиту
1. У больных рассеянным склерозом по мере нарастания инвалидизации развивается общая атрофия головного мозга и локальная атрофия мозговых структур, содержащих серое вещество. Отсутствуют корреляции между выраженностью тотальной атрофии и уменьшением объема таламуса и подкорковых ядер.
2. Последовательность развития локальной атрофии структур мозга, содержащих серое вещество, и этапы развития инвалидизации при рассеянном склерозе совпадают. Параллельно прогрессированию атрофии, в головном мозге больных наблюдается функциональная реорганизация серого вещества, направленная на компенсацию неврологического дефицита.
3. Развитие тяжелых двигательных нарушений у больных сопровождается уменьшением объема таламуса и базальных ганглиев. Выявляются корреляции между скоростью метаболизма глюкозы в областях мозга, не связанных с моторными функциями, и выраженностью пирамидных и координаторных симптомов.
Личный вклад автора в проведенное исследование
Автор участвовал в определении цели и задач исследования. Диссертантом собраны и обобщены данные специальной литературы, проведен подбор пациентов, оценка неврологического статуса и тяжести инвалидизации, обработка электронных изображений МРТ, анализ результатов ПЭТ. Выполнена статистическая обработка полученных данных и анализ взаимосвязи клинических, МРТ и ПЭТ данных.
Апробация работы
Основные положения диссертации доложены и обсуждены на ежегодных Всероссийских конференциях «Нейроиммунология» (Санкт-Петербург, 2000 – 2007), на II Российском Конгрессе по патофизиологии «Патофизиология органов и систем» (Москва, 2000), на IX Всероссийском съезде неврологов (Ярославль, 2006), на Конгрессе Европейского неврологического общества (Париж, 2001), на конференциях Европейского Комитета по изучению и лечению рассеянного склероза (Милан, 2003; Мадрид, 2006; Прага, 2007).
Внедрение результатов исследования
Результаты диссертации используются в учебном процессе факультета пост-дипломного образования кафедры неврологии и мануальной медицины ГОУ СПб ГМУ им. академика И.П. Павлова. Материалы исследования используются в научно-практической работе отдела лучевой диагностики ФГУ «Российский научный центр радиологии и хирургических технологий» Федерального агентства по высокотехнологичной медицинской помощи. Разработанные методики внедрены в лечебно-диагностическую работу клиники Института мозга человека РАН.
По материалам диссертации опубликовано 23 печатные работы в отечественных и зарубежных изданиях, из них 5 статей в журналах рекомендованных ВАК.
Структура и объем диссертации
Диссертация изложена на 121 страницах машинописного текста, содержит 11 таблиц и 13 рисунков. Работа состоит из введения, обзора литературы, характеристики материалов и методов исследования, результатов собственных исследований и их обсуждения, выводов, практических рекомендаций, списка литературы, включающего 10 отечественных и 221 зарубежных источников.
СОДЕРЖАНИЕ РАБОТЫ.
Общая характеристика материала и методики исследования. В Институте мозга человека РАН обследовано 144 больных с диагнозом рассеянный склероз, определенный согласно критериям Мак-Дональда. Возраст больных: от 18 до 60 лет, длительность заболевания: от 1 до 30 лет. Группа контроля: 25 здоровых добровольцев в возрасте от 18 до 52 лет. Все обследованные пациенты и здоровые добровольцы были праворукими.
Программа обследования: сбор анамнеза, неврологический осмотр, МРТ и ПЭТ обследование.
Для балльной оценки выраженности неврологических нарушений и степени инвалидизации использовались шкалы состояния функциональных систем и расширенная шкала инвалидизации (EDSS). Средний балл обследованной группы больных по шкале EDSS составил 3,5 балла (от 1,0 до 8,0). На основании степени инвалидизации больные были разделены на три группы. 1: EDSS 3,0 баллов – легкая инвалидизация; 2: EDSS от 3,5 до 6,0 баллов – больные способны самостоятельно ходить - умеренная инвалидизация; 3: EDSS > 6,0 баллов - больные нуждаются в посторонней помощи при ходьбе - выраженная инвалидизация.
ПЭТ-обследование выполнено 105 пациентам, проводилось на позитронно-эмиссионном томографе PC2048-15B. Использовалась относительная (выраженная в процентах от среднего значения активности, накопленной во всем головном мозге) оценка скорости метаболизма глюкозы (СМГ). Значения СМГ рассчитывались в областях интереса, соответствующих анатомо-функциональному строению мозга согласно стереотаксическому атласу Taleirach and Tournoux (Talairach J., Tournoux P., 1988).
МРТ обследование с целью верификации диагноза выполнено всем 144 пациентам, обработка и анализ электронных МРТ изображений выполнены у 55 пациентов. МРТ исследования проводились по общепринятой методике в трех проекциях в режимах Т1, Т2 и протонной плотности на аппарате «Magnetom Vision» фирмы «Siemens» c напряжением поля 1,5 Тл. Индекс атрофии (ИА) рассчитывался как отношение объема интересующей исследователя мозговой структуры к объему супратенториального внутричерепного пространства при помощи специализированной программы обработки МРТ-изображений «Java Image», позволяющей вычислять объем областей интереса неправильной формы, обрисованных автоматически (эквиденсный контур) или в ручном режиме по анатомическим ориентирам.
Статистический анализ: исходными данными для статистического анализа служили клинико-анамнестические данные, балльная оценка по шкалам функциональных систем и EDSS, индекс атрофии структур головного мозга и значения относительной скорости метаболизма глюкозы в 64-х областях интереса.
Для статистического анализа использовались корреляционный и дисперсионный анализ (с коррекцией на множественность сравнений по Бонферрони). Оценка статистической значимости различий между отдельными группами проводилась методом Тьюки.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Изменения и взаимосвязь объемов мозговых структур у больных РС с различной степенью инвалидизации (см. таб. 1). Отмечается значимое увеличение объема субарахноидальных пространств и желудочков, уменьшение объема мозговой паренхимы в группе пациентов с умеренной инвалидизацией по сравнению с контрольной группой. При выраженной инвалидизации тотальная атрофия нарастает.
Уменьшение объема мозжечка наблюдается уже в группе больных с легкой инвалидизацией и нарастает по мере развития инвалидизации. Имеет место прямая корреляция между снижением объема мозжечка и выраженностью тотальной атрофии (p<0,01).
Уменьшение объема чечевицеобразных ядер наблюдается в группе больных с легкой инвалидизацией и прогрессирует при нарастании степени инвалидизации.
В группе больных с легкой инвалидизацией отмечена тенденция к уменьшению объема хвостатых ядер, однако статистически значимо только отличие между группами легкой и средней тяжести. Уменьшение объема хвостатых ядер прямо коррелирует с объемом чечевицеобразных ядер (p<0,01), в то время как отсутствует взаимосвязь между изменением объемов хвостатых ядер и выраженностью тотальной атрофии.
Значимое уменьшение объема таламуса наблюдается только в группе больных с выраженной инвалидизацией. Имеет место прямая корреляция между объемом таламуса и хвостатых ядер (p<0,01). При этом взаимосвязи между объемом таламуса, с одной стороны, и показателями тотальной атрофии, объемом мозжечка и чечевицеобразных ядер, с другой, не выявлено.
Отсутствует корреляция выраженности тотальной и локальной атрофии головного мозга с длительностью заболевания и возрастом больных.
Таблица 1
Объем (индекс атрофии в %) мозговых структур в группах больных рассеянным склерозом с различной степенью инвалидизации.
| исследуемые анатомические структуры мозга | 1 группа контроль (n=25) | 2 группа EDSS3 (n=19) | 3 группа 3<EDSS6 (n=25) | 4 группа EDSS>6 (n=11) |
| субарахноид. пространство | 5,97±1,23 | 5,14 ± 0,92 | 9,96 ± 0,55* | 12,16±0,83 |
| желудочки | 1,43 ± 0,65 | 1,72 ± 0,48 | 3,40 ± 0,29** | 4,57±0,44 |
| мозговая паренхима | 92,60 ± 1,42 | 93,15 ± 1,06 | 86,64 ± 0,63* | 83,27±0,95** |
| мозжечок | 9,19±0,47 | 8,56±0,37** | 8,04±0,21** | 7,42±0,32** |
| левое чечевицеобраз-ное ядро | 0,52 ± 0,04 | 0,36 ± 0,03* | 0,32 ± 0,02 | 0,29±0,03 |
| правое чечевицеобраз-ное ядро | 0,52 ± 0,04 | 0,36±0,03* | 0,33 ± 0,02 | 0,29±0,03 |
| левое хвостатое ядро | 0,31 ± 0,03 | 0,29 ± 0,02 | 0,24±0,01** | 0,23±0,02 |
| правое хвостатое ядро | 0,30 ± 0,03 | 0,29 ± 0,02 | 0,25±0,01** | 0,22±0,02 |
| левый таламус | 0,91 ± 0,09 | 0,90 ± 0,07 | 0,84 ± 0,04 | 0,69±0,06* |
| правый таламус | 0,88 ± 0,08 | 0,91 ± 0,06 | 0,87±0,04 | 0,67±0,05* |
Примечание: * - р<0.01 при сравнении с предыдущей группой
** - р<0.05 при сравнении с предыдущей группой
жирным шрифтом выделены отличия от группы контроля с р<0.01
Взаимосвязь объемов мозговых структур с неврологическими симптомами в группе больных рассеянным склерозом. При корреляционном анализе изменений объема мозговых структур и выраженности неврологических нарушений выявлено, что развитие тотальной атрофии (увеличение объема субарахноидальных пространств, желудочков и уменьшение объема мозговой паренхимы) коррелирует с развитием пирамидных, мозжечковых, чувствительных и зрительных нарушений. Стволовые нарушения взаимосвязаны только с объемом желудочков. Выраженность тазовых нарушений коррелирует с уменьшением объема мозговой паренхимы (p<0,01).
Степень выраженности пирамидных и координаторных расстройств, играющих основную роль в развитии инвалидизации больных рассеянным склерозом, коррелирует со снижением объемов мозжечка и чечевицеобразных ядер (p<0,01), а также хвостатых ядер обоих полушарий (p<0,05).
Не выявлено взаимосвязи между объемом таламуса и выраженностью неврологических симптомов.
Общий балл по шкале EDSS (интегративный показатель степени нетрудоспособности больных) коррелирует как с показателями общей атрофии, так и с объемами мозжечка и подкорковых ядер (р<0,01), но не коррелирует с объемом таламуса.
Изменения регионарной скорости метаболизма глюкозы у больных РС с различной степенью инвалидизации, взаимосвязь выявленных изменений с выраженностью локальной атрофии (см. таб. 2, рис. 1 – 4).
Таблица 2
Скорость метаболизма глюкозы (в %) в различных мозговых структурах в группах больных РС с различной степенью инвалидизации.
| исследуемая область интереса | 1 группа Контроль (n=25) | 2 группа EDSS3 (n=36) | 3 группа 3<EDSS6 (n=58) | 4 группа EDSS>6 (n=11) |
| правое полушарие мозжечка | 100,99±1,54 | 101,17±1,18 | 95,36±1,50* | 91,74±2,33 |
| левое полушарие мозжечка | 98,89±1,29 | 99,83±0,98 | 96,42±1,25* | 92,26±2,02 |
| Поле Бродмана (ПБ) 4 слева | 110,98±0,96 | 109,52±0,72 | 112,09±0,94** | 115,06±1,38 |
| ПБ 4 справа | 110,09±0,95 | 108,85±0,71 | 110,37±0,92** | 111,73±1,39 |
| левое чечевицеобраз-ное ядро | 101,24±1,01 | 104,17±0,75 | 106,25±0,96 | 108,23±1,47 |
| правое чечевицеобраз-ное ядро | 101,12±1,03 | 104,09±0,77 | 105,31±0,98 | 105,88±1,50 |
| левое хвостатое ядро | 90,86±1,55 | 92,07±1,16 | 87,68±1,50 | 87,26±2,26 |
| правое хвостатое ядро | 92,61±1,31 | 93,91±0,98 | 92,10±1,27 | 91,82±1,91 |
| таламус слева | 92,78±1,7 | 90,12±1,28 | 86,24±1,63** | 84,58±2,49 |
| таламус справа | 92,93±1,62 | 90,35±1,21 | 86,42±1,57** | 85,73±2,36 |
Примечание: * - р<0.01 при сравнении с предыдущей группой
** - р<0.05 при сравнении с предыдущей группой
жирным шрифтом выделены отличия от группы контроля с р<0.01
Анализ изменений СМГ в коре и подкорковых структурах головного мозга показал, что СМГ в мозжечке при легкой инвалидизации существенно не изменяется, снижается при умеренной и при выраженной инвалидизации. В то же время, уменьшение объема мозжечка выявляется уже у пациентов с легкой инвалидизацией.


Рис. 1 Скорость метаболизма глюкозы в мозжечке (верхний график) и объем мозжечка (нижний график) в группах больных РС с различной степенью инвалидизации.
Примечание: по оси ординат: относительная СМГ (верхний график), индекс атрофии (нижний график);
по оси абсцисс: группа контроля -1; группы пациентов: 2 – с легкой, 3 – с умеренной, 4 – с выраженной инвалидизацией
Скорость метаболизма глюкозы в первичной моторной коре значимо увеличивается у пациентов с выраженной инвалидизацией. Отмечается положительная корреляция между выраженностью мозжечковых нарушений и регионарной СМГ в области поля Бродмана 4 доминантного полушария.

Рис. 2 Скорость метаболизма глюкозы в поле Бродмана 4 левого полушария в группах больных РС с различной степенью инвалидизации.
Примечание: по оси ординат: относительная СМГ;
по оси абсцисс: группа контроля – 1;
группы пациентов: 2 – с легкой, 3 – с умеренной, 4 – с выраженной инвалидизацией
Уменьшение объема чечевицеобразных ядер сопровождается повышением в них скорости метаболизма глюкозы.


Рис. 3 Скорость метаболизма глюкозы в левом чечевицеобразном ядре (верхний график) и объем левого чечевицеобразного ядра (нижний график) в группах больных РС с различной степенью инвалидизации
Примечание: по оси ординат: относительная СМГ (верхний график), индекс атрофии (нижний график);
по оси абсцисс: группа контроля -1; группы пациентов: 2 – с легкой, 3 – с умеренной, 4 – с выраженной инвалидизацией;
С самого начала заболевания снижается скорость метаболизма глюкозы в таламусе, однако его объем значимо уменьшается только в группе пациентов с выраженной инвалидизацией.
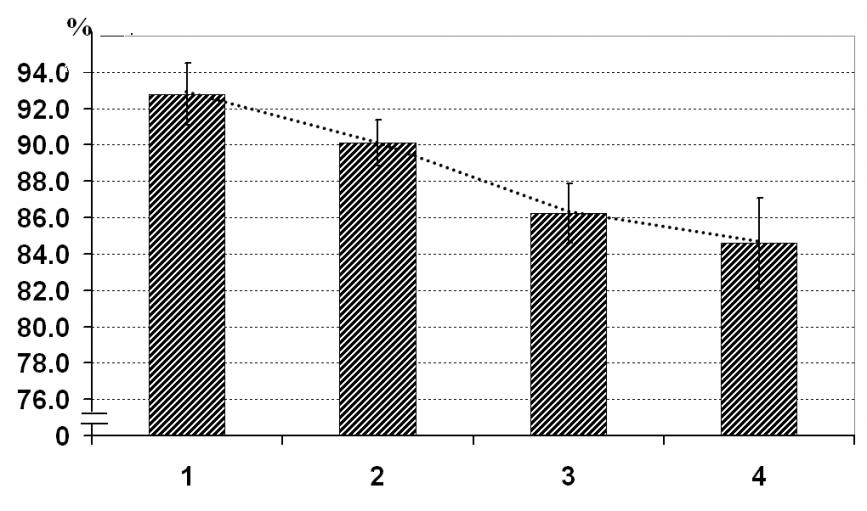

Рис. 4 Скорость метаболизма глюкозы в таламусе слева (верхний график) и объем таламуса (нижний график) слева в группах больных РС с различной степенью инвалидизации
Примечание: по оси ординат: относительная СМГ (верхний график), индекс атрофии (нижний график);
по оси абсцисс: группа контроля -1; группы пациентов: 2 – с легкой, 3 – с умеренной, 4 – с выраженной инвалидизацией
Результаты корреляционного анализа скорости метаболизма глюкозы с выраженностью неврологических симптомов в группах больных РС с различной степенью инвалидизации. При корреляционном анализе изменений СМГ и выраженности неврологических симптомов в группе пациентов с легкой инвалидизацией значимых корреляций не выявлено.
В группе пациентов с умеренной инвалидизацией выявлены значимые корреляции (p<0.01):
а) отрицательные: между мозжечковыми нарушениями и СМГ в сером веществе мозжечка; между степенью пирамидных нарушений и СМГ в области полей Бродмана 20, 37;
б) положительные: между степенью мозжечковых нарушений и СМГ в области поля Бродмана 4 слева; между степенью пирамидных нарушений и СМГ в области гиппокампа, обоих хвостатых ядер, чечевицеобразного ядра слева, таламуса.
Таким образом, у пациентов с легкой инвалидизацией неврологические нарушения в первую очередь связаны с уменьшением объема подкорковых мозговых структур. При умеренной инвалидизации, наряду с развитием тотальной и локальной атрофии, имеют место изменения скорости метаболизма глюкозы в головном мозге. СМГ снижается в зонах, непосредственно отвечающих за выполнение движений, и повышается в зонах, функционально связанных со структурами, отвечающими за выполнение нарушенных функций. Это может свидетельствовать о развитии функциональной реорганизации серого вещества головного мозга, которая, вероятно, играет компенсаторную роль.
При корреляционном анализе выраженности неврологических симптомов и СМГ с объемами мозговых структур в группе больных с выраженной инвалидизацией показано отсутствие взаимосвязи между регионарной СМГ, объемом мозжечка и выраженностью неврологических нарушений (в том числе координаторных). Пирамидные и чувствительные нарушения также не коррелируют с регионарной СМГ в структурах головного мозга.
Снижение СМГ в мозжечке коррелирует с уменьшением объема таламуса. В то же время уменьшение объема таламуса и чечевицеобразных ядер коррелирует с нарастанием СМГ в первичной моторной коре (полях Бродмана 4) правого и левого полушария. Кроме того, уменьшение объема таламуса коррелирует с повышением СМГ в первичной соматосенсорной коре (поля Бродмана 1,2,3) в левом полушарии.
Таким образом, развитие тяжелых обездвиживающих неврологических нарушений у больных РС сопровождается значимым снижением объема таламуса и дальнейшей атрофией базальных ганглиев и мозжечка, на фоне которых изменения СМГ в сером веществе головного мозга претерпевают разнонаправленные изменения, захватывают зоны, функционально не связанные с областями, ответственными за утраченные функции и перестают играть компенсаторную роль.
ВЫВОДЫ
1. По мере прогрессирования заболевания у больных рассеянным склерозом развивается общая атрофия головного мозга и локальная атрофия мозжечка, подкорковых ядер и таламуса.
2. Тотальная атрофия головного мозга развивается у пациентов с умеренной инвалидизацией и нарастает у тяжелых больных. Выраженность тотальной атрофии коррелирует со степенью пирамидных, мозжечковых, чувствительных, зрительных нарушений и с тяжестью инвалидизации.
3. Объем мозжечка уменьшается, начиная с группы больных с легкой инвалидизацией. У больных с легкой и умеренной инвалидизацией уменьшение объема мозжечка сопровождается снижением скорости метаболизма глюкозы в обоих полушариях мозжечка и нарастанием координаторных и пирамидных расстройств.
4. Локальная атрофия подкорковых структур на ранних этапах заболевания проявляется уменьшением объема чечевицеобразных ядер. По мере развития заболевания в атрофический процесс вовлекаются хвостатые ядра, а на поздних этапах - таламус. Выраженность пирамидных, координаторных расстройств и степень инвалидизации коррелируют со снижением объемов чечевицеобразных и хвостатых ядер.
5. У пациентов с умеренной инвалидизацией имеет место функциональная реорганизация серого вещества головного мозга. Выраженность координаторных нарушений коррелирует со снижением скорости метаболизма глюкозы в мозжечке и ее повышением в первичной моторной коре доминантного полушария. Пирамидные нарушения прямо коррелируют со скоростью метаболизма глюкозы в гиппокампе, хвостатых ядрах и чечевицеобразном ядре слева, таламусе и обратно коррелируют со скоростью метаболизма глюкозы в области полей Бродмана 20 и 37.
6. Для больных с выраженной инвалидизацией характерно отсутствие корреляции между регионарной скоростью метаболизма глюкозы и очаговыми неврологическими нарушениями. Это свидетельствует о срыве функциональной реорганизации серого вещества головного мозга, связанном с прогрессированием общей и локальной атрофии подкорковых структур, в первую очередь, таламуса.
Практические рекомендации
1. Для прогноза развития инвалидизации, выбора тактики лечения больных рассеянным склерозом, а также оценки эффективности новых методов терапии целесообразно измерение тотальной и локальной атрофии при МРТ исследовании, а также оценка скорости метаболизма глюкозы в головном мозге с помощью позитронно-эмиссионной томографии.
2. Анализ взаимосвязей метаболических и структурных нарушений в головном мозге целесообразно использовать для изучения патогенеза демиелинизирующих и нейродегенеративных заболеваний, в частности выяснения роли повреждения подкорковых структур в развитии двигательных расстройств.
3. Результаты изучения изменений объемов структур и скорости метаболизма глюкозы в головном мозге целесообразно включить в программу обучения студентов, аспирантов и ординаторов высших учебных заведений.
Список работ, опубликованных по теме исследования
1. Столяров И.Д. Neuropsychological battery and positron-emission tomography in multiple sclerosis patients. / И.Д.Столяров, А.Г.Ильвес, Л.Н.Прахова и др. // Multiple Sclerosis. – 1999. - Vol. 5, Suppl. 1. – Р.36.
2. Столяров И.Д. Инструментальные и нейроиммунологические характеристики демиелинизирующего процесса при рассеянном склерозе. Современные подходы к диагностике и лечению нервных и психических заболеваний. / И.Д.Столяров, Р.П.Огурцов, Г.Н.Бисага, Л.Н.Прахова, М.С.Рудас, А.Г.Ильвес и др. // Материалы конференции «Нейроиммунология».- СПб., 2000.– С. 382.
3. Прахова Л.Н. Cortical patterns of psychological disturbances measured with positron emission tomography (PET). / М.С.Рудас, Л.Н.Прахова, А.Г.Ильвес и др. // Revue Neurologique. – 2000. - Suppl.3. – P. 98.
4. Столяров И.Д. Positron emission tomography, magnetic resonance imaging and immunological findings in multiple sclerosis patients. / И.Д.Столяров, М.С.Рудас, А.Г.Ильвес и др. // European J. of Neurology. – 2000. - Vol.7, Suppl.3. – P. 128.
5. Столяров И.Д. Нейроимидж и нейроиммунологические характеристики при рассеянном склерозе. / И.Д.Столяров, Р.П. Огурцов, М.С. Рудас, А.Г.Ильвес и др. // Тезисы докладов II Российского Конгресса по патофизиологии «Патофизиология органов и систем».– М., 2000. – С. 38-39.
6. Прахова Л.Н. Neuropsychological, clinical, MRI and PET correlates in multiple sclerosis patients. / Л.Н.Прахова, М.С.Рудас, А.Г.Ильвес и др. // Journal of Neurology. - 2001. - Vol.248, Suppl.2. – P. 531.
7. Прахова Л.Н. Новые возможности изучения патогенеза клинико-психологических нарушений у больных рассеянным склерозом. / Л.Н.Прахова, Г.Н.Бисага, А.М.Петров, Г.В.Катаева, А.Г.Ильвес и др. // Материалы конференции «Нейроиммунология».- СПб., 2001. - С. 224-226.
8. Петров А.М. Grey matter involvement in multiple sclerosis pathogenesis. / А.М.Петров, Л.Н.Прахова, М.С.Рудас, А.Г.Ильвес и др. // Multiple Sclerosis. – 2001. - Vol.7, Suppl.1. – P. 026.
9. Прахова Л.Н. The cortex metabolic alterations in multiple sclerosis (MS) patients - the role in pathophysiology of disease. / Л.Н.Прахова, А.Г.Ильвес, Г.В.Катаева и др. // Journal of Neurology. - 2002. - Vol. 1, Suppl. 2. – P. 309.
10. Никифорова И.Г. Correlations of clinical and immunological data with magnetic resonance imaging parameters in patients with multiple sclerosis. / И.Г.Никифорова, А.Г.Ильвес, И.Д.Столяров и др. // Abstracts 6th EFNS Congress of Neurology. – Vienna. - 2002. – P. 2095.
11. Абдурахманов М.А. Рассеянный склероз. Практическое руководство / М.А.Абдурахманов, Н.И.Артемюк, Я.В.Власов, М.В.Вотинцева, Е.В.Ивашкова, А.Г.Ильвес, И.Г.Никифорова, Н.В.Николаева, Р.П.Огурцов, Л.А.Пестова, А.М.Петров, Л.Н.Прахова / под ред. И.Д. Столярова, Б.А. Осетрова.- СПб.: Элби-СПб., 2002. – 176 с.
12. Столяров И.Д. Некоторые современные методы диагностики и патогенетической терапии рассеянного склероза. / И.Д.Столяров, Г.Н.Бисага, М.В.Вотинцева, А.Г.Ильвес и др. // Неврологический вестник (журнал им. В.М.Бехтерева).– 2002.- Т.34, № 1-2. - С. 65-72.
13. Прахова Л.Н. Метаболические нарушения в сером веществе головного мозга при аутоиммунном демиелинизирующем заболевании нервной системы человека и их роль в формировании клинической картины заболевания. / Л.Н.Прахова, А.Г.Ильвес, Г.В.Катаева и др. // Доклады Академии наук.– 2002. - Т.386, № 5. - С. 1-3.
14. Ильвес А.Г. Effect of Glatiromer acetate (GA) therapy on regional cerebral metabolic abnormalities in MS patients (pilot study). / А.Г.Ильвес, Л.Н.Прахова, Г.В.Катаева и др. // Multiple Sclerosis. - 2002. - Vol.7, Suppl.1. – P.233.
15. Ильвес А.Г. Изменения метаболизма глюкозы головного мозга у больных рассеянным склерозом и их роль в формировании клинической картины и в развитии прогрессирования заболевания. / А.Г.Ильвес, Л.Н.Прахова, Г.В.Катаева и др. // Журнал неврологии и психиатрии им. С.С.Корсакова.– 2003.- Спецвыпуск. Рассеянный склероз, №2. - С. 53-60.
16. Никифорова И.Г. Relapsing-remitting and secondary progressive multiple sclerosis: relationship between clinical, immunological and MRI data. / И.Г.Никифорова, А.Г.Ильвес, А.М.Петров и др. // Multiple Sclerosis.- 2003. - Vol.9, Suppl.1, - P. S107.
17. Прахова Л.Н. Использование позитронно-эмиссионной томографии для оценки состояния серого вещества головного мозга у больных рассеянным склерозом. / Л.Н.Прахова, А.Г.Ильвес, Г.В.Катаева и др. // Организация специализированной медицинской помощи больным рассеянным склерозом (Материалы рабочего совещания). – Томск, 2003. - С. 58-64.
18 Резникова Т.Н. ПЭТ-исследование головного мозга человека и психологические защитные механизмы личности больных рассеянным склерозом. / Т.Н.Резникова, И.Ю.Терентьева, Г.В.Катаева, А.Г.Ильвес // Физиология человека. – 2004. – Т.30, № 4. – С. 25-31.
19. Прахова Л.Н. Клинико-радиологические корреляции при различной тяжести течения рассеянного склероза. / Л.Н.Прахова, А.Г.Ильвес, Г.В.Катаева и др. // Материалы IX Всероссийского съезда неврологов. – Ярославль, 2006. - С. 339.
20. Ильвес А.Г. Клинико-радиологические (ПЭТ и МРТ) корреляции у больных рассеянным склерозом разной тяжести. / А.Г.Ильвес, Л.Н.Прахова, Г.В.Катаева и др. // Журнал неврологии и психиатрии им. С.С.Корсакова.- 2006.- Спецвыпуск. Рассеянный склероз, № 3. - С.81-86.
21. Ильвес А.Г. Development and disruption of functional cerebral grey matter reorganization depending on disease progression in MS patients (according PET and MRI data). / А.Г.Ильвес, Л.Н.Прахова, Г.В.Катаева и др. // Multiple Sclerosis. - 2006. - Vol.12, Suppl.1. – S44.
22. Минеев К.К. Взаимосвязь объема и активности очагов поражения в головном мозге (по данным магнитно-резонансной томографии (МРТ)) и когнитивных нарушений у больных рассеянным склерозом. / К.К.Минеев, А.Г.Ильвес, Г.В.Катаева и др. // Нейроиммунология. – 2006. - Т. IV, № 3-4. - С.57-62.
23. Минеев К.К. Особенности неврологического и когнитивного статуса больных рассеянным склерозом в зависимости от локализации, объема очагов демиелинизации и выраженности атрофии головного мозга. / К.К.Минеев, Л.Н.Прахова, А.Г.Ильвес и др. // Журнал неврологии и психиатрии им. С.С.Корсакова.- 2007.- Спецвыпуск. Рассеянный склероз, № 4. - С.46-49.

