Резервуарно-пластические операции в лечении рака средне- и нижнеампулярного отделов прямой кишки
На правах рукописи
ЛИТВИНОВ Олег Александрович
РЕЗЕРВУАРНО-ПЛАСТИЧЕСКИЕ ОПЕРАЦИИ
В ЛЕЧЕНИИ РАКА СРЕДНЕ- И НИЖНЕАМПУЛЯРНОГО
ОТДЕЛОВ ПРЯМОЙ КИШКИ
14.00.27 – хирургия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Санкт-Петербург
2007
Работа выполнена в Военно-медицинской академии имени С.М. Кирова
Научный консультант-
доктор медицинских наук профессор ЗУБАРЕВ Петр Николаевич
Официальные оппоненты:
член-корреспондент РАМН доктор медицинских наук
профессор МАЙСТРЕНКО Николай Анатольевич
доктор медицинских наук профессор
ВАСИЛЬЕВ Сергей Васильевич
доктор медицинских наук профессор
ТОПУЗОВ Эскендер Гафурович
Ведущая организация – ГУ «Санкт-Петербургский научно-исследовательский институт скорой помощи им. И.И. Джанелидзе»
Защита состоится 15 октября 2007 г. в 14 часов на заседании диссертационного совета Д 215.002.10 при Военно-медицинской академии им. С.М. Кирова (194044, Санкт-Петербург, ул. Лебедева, д.6).
С диссертацией можно ознакомиться в фундаментальной библиотеке Военно-медицинской академии им. С.М. Кирова.
Автореферат разослан «____» _______________2007 года.
УЧЕНЫЙ СЕКРЕТАРЬ ДИССЕРТАЦИОННОГО СОВЕТА
доктор медицинских наук профессор
ДУЛАЕВ Александр Кайсинович
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования
Проблема хирургического лечения рака прямой кишки приобретает все большее социальное значение. В последние десятилетия отмечается рост показателей заболеваемости больных злокачественными новообразованиями прямой кишки [Кныш В.И. и соавт., 1996; Аксель Е.М., Бармина Н.М., 1999; Ривкин В.Л. и соавт., 2001; Becker H., 1995; Yasutomi M., 1997; Hojo K., 1998; Guillem J.G., Cohen A.M., 1999]. Ежегодно в мире выявляется 600 тыс. случаев злокачественного поражения дистальных отделов толстой кишки и половина из них умирает [Абелев Г.И. и соавт., 2004]. В России каждый год регистрируется более 40 тыс. случаев рака прямой кишки [Аксель Е.М., Горбачева И.А., 2004]. В настоящее время основным методом лечения рака прямой кишки остается хирургический. Лучевая и химиотерапия применяются в комплексном лечении, дополняя оперативное вмешательство.
Современные тенденции в хирургии рака прямой кишки определяются расширением показаний к функционально сберегательным операциям. В настоящее время в специализированных лечебных учреждениях до 70,0% - 80,0% всех радикальных вмешательств при раке прямой кишки составляют сфинктеросохраняющие операции [Бондарь Г.В. и соавт., 1989; Кныш В.И. и соавт., 1996; Лазарев Г.В. и соавт., 1997; Покровский Г.А. и соавт., 1998; Konn M. et al., 1993; Hg A.K. et al.,1997]. Многие авторы в последние годы обсуждают возможность более широкого применения сфинктеросохраняющих методик при лечении рака нижнеампулярного отдела прямой кишки [Блинов Н.Н. и соавт., 1996; Васильев С.В. и соавт., 1999; Марголин Л.М. и соавт., 2000; Баширов С.Р., Жерлов Г.К., 2003; Бондарь Г.В. и соавт., 2003; Yeatmen T.J., Bland K.I., 1989; Leo E. et al., 1993; Parc R.F., Sales J.P., 1993; Breen E., Bleday R., 1997].
Необходимость дальнейшего совершенствования методов хирургического лечения рака прямой кишки, в значительной мере, диктуется негативными функциональными результатами некоторых сфинктеросохраняющих операций и обусловлены утратой резервуарной функции прямой кишки [Одарюк Т.С. и соавт., 2001; Schibli M., Rittmann W.W., 1991; Lewis W.G. et al., 1992; Ortiz H. et al., 1995; Dehni N. et al., 1998; Barrier A. et al., 1999; Gamagami R. et al., 2000]. Эти нарушения, описанные в литературе, как "синдром низкой передней резекции", могут наблюдаться у 25,0% - 46,0% больных, перенесших различные варианты брюшно-анальной резекции прямой кишки и низкой передней резекции [Покровский Г.А. и соавт., 1998; Воробьев Г.И. и соавт., 2000; Cugnenc P.H. et al., 1981; Karanjia N.D. et al., 1992; Lewis W.G. et al., 1992]. Улучшение функциональных результатов в таких случаях возможно при формировании толстокишечных резервуаров [Васильев С.В. и соавт., 1999; Одарюк Т.С. и соавт., 2001; Жерлов Г.К. и соавт., 2003; Lazorthes F. et al., 1986; Parc R. et al., 1986; Nicholls R.J. et al., 1988; Berger A. et al., 1992]. Поэтому эта методика рассматривается как наиболее очевидная альтернатива традиционным резекциям прямой кишки с наложением колоанальных анастомозов, позволяющая добиться лучшего качества жизни оперированных пациентов [Майстренко Н.А. и соавт., 1998; Яицкий Н.А. и соавт., 2002; Parc R.F. et al., 1993; Araki Y. et al., 1999]. Вместе с тем, в хирургическом лечении рака прямой кишки резервуарная техника в нашей стране широкого применения все еще не нашла и ее используют лишь некоторые авторы [Бондарь Г.В. и соавт., 1990; Васильев С.В. и соавт., 1999; Воробьев Г.В. и соавт., 2000].
Несмотря на увеличение роли органосохраняющих вмешательств в лечении рака прямой кишки, от 10% до 30% больных нуждаются в выполнении брюшно-промежностной экстирпации прямой кишки. Экстирпация считается операцией выбора при низко расположенных опухолях с поражением анального канала и сфинктера, при опухолях низкой степени дифференцировки. Несмотря на удовлетворительные непосредственные и отдаленные исходы этого вмешательства, функциональные результаты не удовлетворяют ни хирурга, ни больного.
В связи с трудностями адаптации стомированных больных к изменившимся условиям жизни, в последние годы в лечении рака нижнеампулярного отдела прямой кишки все чаще применяются сфинктеросохраняющие и резервуарно-пластические операции (имитирующие резервуарную и запирательную функцию прямой кишки). Но эти виды оперативных вмешательств в настоящее время имеют ограниченное применение: они являются технически более сложными, выполняются в начальных стадиях заболевания и в основном у пациентов трудоспособного возраста.
Таким образом, поиск оптимальных методов хирургического лечения рака средне- и нижнеампулярного отделов прямой кишки остается актуальной и не до конца решенной проблемой.
Цель исследования – улучшение функциональных результатов хирургического лечения больных раком средне- и нижнеампулярного отделов прямой кишки.
Задачи исследования:
- Изучить особенности патоморфологии рака средне- и нижнеампулярного отделов прямой кишки.
- Изучить непосредственные результаты различных видов оперативных вмешательств при раке средне- и нижнеампулярного отделов прямой кишки.
- Провести сравнительный анализ функциональных результатов различных видов операций по поводу рака средне- и нижнеампулярного отделов прямой кишки.
- Изучить качество жизни пациентов со злокачественными новообразованиями средне- и нижнеампулярного отделов прямой кишки в послеоперационном периоде.
- Оценить отдаленные результаты оперативных вмешательств при раке средне- и нижнеампулярного отделов прямой кишки.
- Разработать и усовершенствовать технику выполнения резервуарно-пластических операций при раке средне- и нижнеампулярного отделов прямой кишки.
- Усовершенствовать тактику хирургического лечения рака средне- и нижнеампулярного отделов прямой кишки.
Научная новизна
Новизна исследования заключается в изучении и комплексном анализе функциональных результатов различных вариантов оперативного лечения рака средне- и нижнеампулярного отдела прямой кишки с учетом характера операций и осложнений. Для определения изменений функционального состояния прямой кишки после различных видов хирургического лечения применен метод импедансометрии, показавший свою эффективность в оценке запирательной функции прямой кишки. Изучено качество жизни больных раком прямой кишки и проанализирована его динамика в послеоперационном периоде. Разработаны и внедрены в клиническую практику новые методы хирургического лечения рака прямой кишки с формированием Э-образных толстокишечных резервуаров и глютеопластика при локализации опухоли в средне- и нижнеампулярном отделах прямой кишки.
Практическая ценность
Внедрен в клиническую практику метод импедансометрии, позволяющий объективно оценивать запирательную функцию прямой кишки.
Оптимизированы показания для наиболее часто применяемых в хирургической практике оперативных вмешательств в лечении рака среднеампулярного отдела прямой кишки.
С целью улучшения функциональных результатов брюшно-анальной резекции прямой кишки в клиническую практику внедрены хирургические вмешательства с формированием Э-образных толстокишечных резервуаров.
С целью улучшения функциональных результатов брюшно-промежностной экстирпации прямой кишки в клиническую практику внедрены хирургические вмешательства с формированием Э-образных толстокишечных резервуаров и глютеопластикой в области промежностной сигмостомы.
Положения, выносимые на защиту:
1. Применение сфинктеросохраняющих и резервуарно-пластических операций в лечении рака средне- и нижнеампулярного отделов прямой кишки не приводит к увеличению частоты послеоперационных осложнений, местных рецидивов и госпитальной летальности. Отдаленные результаты этих операций определяются в основном стадией опухолевого процесса.
2. Брюшно-анальная резекция прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара по своим отдаленным функциональным результатам является, наряду с передней аппаратной резекцией, оптимальным хирургическим вмешательством при раке среднеампулярного отдела прямой кишки.
3. Выполнение брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы позволяет улучшить функциональные результаты хирургического лечения рака нижнеампулярного отдела прямой кишки.
Реализация и апробация работы
Основные положения диссертации доложены и обсуждены на научно-практической конференции, посвященной 40-летию Санкт-Петербургской клинической больницы РАН (Санкт-Петербург, 2002), на научной конференции, посвященной 80-летнему юбилею профессора Петрова В.П. (Красногорск, 2004), на научной конференции, посвященной 85-летнему юбилею профессора Лыткина М.И. (Санкт-Петербург, 2004), на Всероссийской конференции с международным участием «Гастро-2004» (Санкт-Петербург, 2004), на международном хирургическом конгрессе «Новые технологии в хирургии» (Ростов-на-Дону, 2005), на IX, X Российских онкологиических конгрессах (Москва, 2005, 2006), на Всероссийской конференции «Невский радиологический форум (Санкт-Петербург, 2007), на Всероссийской конференции «Актуальные вопросы клиники, диагностики и лечения в многопрофильном лечебном учреждении» (Санкт-Петербург, 2007).
Результаты исследования нашли применение в практической работе хирургических клиник ВМедА, колопроктологического отделения ЛОКБ, в онкохирургическом отделении МСЧ №70, в педагогической работе кафедры общей хирургии ВМедА им С.М. Кирова.
Объем работы
Диссертация состоит из введения, 5 глав, заключения, выводов и практических рекомендаций. Работа изложена на 183 страницах, содержит 63 рисунка и 44 таблицы. Библиографический указатель включает в себя 314 источников, из которых 141 отечественных и 173 иностранных.
Материалы и методы исследования
Работа основана на анализе результатов хирургического лечения 112 больных раком прямой кишки. Из них 49 (44%) женщин и 63 (56%) мужчины в возрасте от 25 до 81 года (58,9±11,1 года). Все больные были разделены на две группы, в зависимости от локализации опухоли. Первую группу составили 43 пациента с локализацией опухоли в нижнеампулярном отделе прямой кишки (расстояние до нижнего края опухоли от анокутанной складки менее 6 см). Во вторую группу вошли 67 больных раком среднеампулярного отдела прямой кишки (расстояние до нижнего края опухоли от анокутанной складки от 6 до 12 см).
В работе использованы общепринятые клинико-лабораторные и инструментальные методы обследования больных, а также следующие специальные методы: эндоректальная сонография (n=46); компьютерная томография органов малого таза (n= 37); селективная нижняя мезентерикография (n=8); фиброколоноскопия (n=96); ректороманоскопия (n=112); ирригоскопия (n=54); гистологическое исследование операционных препаратов (n=112) и биопсийного материала (n=96); импедансометрия (n=76); изучение выживаемости больных (n=112); оценка функциональных результатов сфинктеросохраняющих вмешательств (n= 64); оценка качества жизни пациентов (n=60).
Эндоскопическая диагностика опухолевого поражения прямой кишки базировалась на данных ректороманоскопии и фиброколоноскопии, полученных при использовании ректоскопа РВ-1 (Россия) и колоноскопа "Olympus CF-P30L" (Япония). Эндоскопия завершалась взятием биопсийного материала для гистологической верификации диагноза.
Эндоректальная сонография проводилась на ультразвуковом аппарате «Siemens Sonoline Elegra» (Германия) с применением цифрового конвексного эндоректального датчика частотой 6,5 МГц (6,5EC10). Показанием к исследованию являлся верифицированный рак прямой кишки. При этом оценивали следующие ультразвуковые признаки: размеры и расположение опухоли, наружный контур кишки, дифференциацию слоев кишечной стенки и степень инвазии в нее опухоли, размеры и количество выявляемых в параректальной клетчатке лимфатических узлов, поражение рядом расположенных органов. По данным эндоректальной сонографии у 33 больных (71,7%) наблюдали прорастание опухолью всех слоев стенки прямой кишки, сопровождающееся в том числе экстраорганным ростом и неровностью наружного контура кишки. У 4 больных (8,7%) выявили инвазию рака до мышечного слоя, при этом наблюдался преимущественно экзофитный рост опухоли. Чувствительность и специфичность метода в оценке местного роста опухоли по нашим данным приведена в таблице 1. Лимфаденопатию параректальной клетчатки наблюдали у 29 (63%) из 46 обследованных пациентов. Специфичность сонографической диагностики регионарных лимфогенных метастазов достигает 65,5% и зависит от количества и размеров идентифицированных лимфатических узлов. Так, частота метастатического поражения лимфатических узлов до 1,0 см в диаметре составила 18,4%, более 1,0 см в диаметре – 87,9%.
Таблица 1
Чувствительность и специфичность эндоректальной сонографии
в оценке степени местного распространения рака прямой кишки
| T1 | T2 | T3 | T4 | N1 | N2 | |
| Чувствительность | 97% | 100% | 100% | 100% | 100% | 100% |
| Специфичность | 75% | 70% | 77% | 45% | 85% | 46% |
Полученные результаты позволяют рекомендовать применение эндоректальной сонографии для уточнения степени местного распространения опухолевого процесса у больных с первично выявленным раком прямой кишки, особенно при стадиях Т1-3.
Компьютерная томография (КТ) органов малого таза выполнена 37 больным с использованием томографа "Somatom" (Siemens, Германия). Оценивали распространение опухоли по окружности кишечной стенки, глубину раковой инвазии, состояние регионарных лимфатических узлов, окружающей клетчатки и близлежащих анатомических образований малого таза. Данные томографического исследования также использовали для предоперационного стадирования опухоли.
Результаты КТ сопоставляли с данными эндоскопических и морфологических исследований. Компьютерную томографию малого таза обязательно выполняли пациентам с подозрением на экстраорганный рост опухоли и врастание в соседние органы, а также больным (12 пациентов) перед проведением предоперационной лучевой терапии (для разметки).
В исследовании использованы результаты обследования и лечения 8 пациентов раком нижне- и среднеампулярного отделов прямой кишки, которым с целью профилактики местного рецидива опухоли выполнена эндоваскулярная масляная химиоэмболизация верхней прямокишечной артерии в неоадъювантном режиме (приоритетная справка №2005137428 от 01.12.05г.). Процедуру выполняли в условиях рентгеноперационной с использованием для дигитальной субтракционной ангиографии ANGIOSTAR и POLISTAR фирмы “Siemens” (Германия). После пункции и катетеризации правой бедренной артерии по Сельдингеру, висцеральный сосудистый катетер 5F устанавливали в нижней брыжеечной артерии с последующей суперселективной катетеризацией верхней прямокишечной артерии. В просвет катетера вводили химиопрепарат (оксалиплатин 50 мг), смешанный с контрастным препаратом (4-5 мл) и сверхжидким липиодолом (6-8мл). Эмболизацию осуществляли до тех пор, пока в артерии не прекращался кровоток. Осложнений во время выполнения эндоваскулярной масляной химиоэмболизации верхней прямокишечной артерии (ЭМХЭВПА) выявлено не было. В одном случае выполнение ЭМХЭВПА не представилось возможным в связи с тем, что у пациента был диагностирован выраженный атеросклероз аорты и ее ветвей. При оперативных вмешательствах каких-либо характерных макроскопических изменений в кишке и параректальной клетчатке выявлено не было. При микроскопическом исследовании удаленных препаратов было выявлено наличие частиц липиодола в артериолах регионарных (параректальных) лимфатических узлов, а также в сосудах опухоли и параректальной клетчатки.
Для стадирования опухолевого процесса применяли клиническую классификацию рака прямой кишки по системе TNM (2003 год, шестое издание) и в модификации Dukes. Определение стадии опухолевого процесса до операции основывалось на данных эндоректальной сонографии, УЗИ органов брюшной полости, рентгенографии органов грудной полости, компьютерной томографии. Окончательное стадирование осуществлялось по результатам гистологического исследования.
Для проведения морфологического исследования удаленные операционные препараты фиксировали в 10-кратном объёме 10% раствора нейтрального формалина. Гистологические срезы окрашивали гематоксилин-эозином, по Ван-Гизону и муцин-кармином на слизь. Микроскопическую структуру опухоли оценивали в соответствии с Международной гистологической классификацией опухолей кишечника. В обязательном порядке изучали глубину прорастания опухоли в стенку прямой кишки, определяли наличие метастазов рака в параректальных лимфатических узлах и их количество. С целью выявления лимфогенного метастазирования гистологическому исследованию подвергали не менее 8-12 параректальных лимфатических узлов.
Выживаемость больных изучали актуариальным методом построения таблиц дожития [Двойрин В.В., Клименков А.А., 1985]. Всего в разные сроки отдаленные результаты изучены у 77,2% оперированных больных.
Функциональные результаты сфинктеросохраняющих операций (64 наблюдения) оценивали через 3, 6 и 12 месяцев после вмешательства. Оценивали следующие показатели: частота стула; консистенция стула; наличие инконтиненции и ее степени; характер дефекации; наличие предвестников дефекации.
Для оценки состояния запирательной функций прямой кишки после операции был использован метод импедансометрии [Рябчук Ф.Н. и соавт., 2001]. Исследование проводили с помощью компьютерного медицинского комплекса «Гастролог» (ОАО «Завод «Радиоприбор» г. Санкт-Петербург). В ходе исследования оценивали состояние запирательной функций прямой кишки – базальный тонус и амплитуду максимальных произвольных сокращений.
Для исследования качества жизни применялась российская тест версия (после валидизации) опросника MOS SF-36 (Medical Outcomes Study 36-Item Short-Form Health Survey). Анкетирование осуществлялось как до операции, так и в качестве мониторинга после операции (через 3 и 6 месяцев).
Статистическая обработка материала выполнена при помощи программ "Statistika" для "Windows" с использованием методов вариационной статистики и t-критерия Стьюдента.
Характеристика оперативных вмешательств
Все операции выполняли, соблюдая онкологические принципы: абластику и антибластику. Выбор метода хирургического вмешательства был основан на всестороннем анализе данных предоперационного обследования больных. Окончательное решение о выполнении того или иного вида операции принимали после сопоставления результатов предоперационного обследования пациента с данными интраоперационной ревизии органов брюшной полости и малого таза.
Основные виды оперативных вмешательств по поводу рака средне- и нижнеампулярного отделов представлены в таблице 2.
Таблица 2
Виды оперативных вмешательств у больных раком прямой кишки (n=112)
| Виды операций | Количество больных | |
| абс. | % | |
| Брюшно-промежностная экстирпация прямой кишки (БПЭ) | 24 | 21,4 |
| Брюшно-промежностная экстирпация прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы (БПЭ + Э) | 21 | 18,8 |
| Брюшно-анальная резекция прямой кишки с низведением сигмовидной (БАР) | 18 | 16 |
| Брюшно-анальная резекция прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара (БАР + Э) | 11 | 9,8 |
| Передняя резекция прямой кишки (ПРПК) | 38 | 34,0 |
Брюшно-промежностную экстирпацию прямой кишки выполняли при раке нижнеампулярного отдела, при наличии инструментальных и клинических признаков инвазии опухоли в окружающие органы и ткани, при наличии признаков метастатического поражения параректальных лимфатических узлов и наличии отдаленных метастазов, низкой степени дифференцировки опухоли – T3-4N0-2M0-1.
При раке нижнеампулярного отдела прямой кишки T2N0M0, достаточной длине толстой кишки и удовлетворительном общесоматическом состоянии пациента выполняли брюшно-промежностную экстирпацию прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы (приоритетная справка № 2004121540 от 13.07.2004г.). Оригинальность методики заключалась в следующем. После выполнения брюшно-промежностной экстирпации прямой кишки левые отделы ободочной кишки мобилизовали до селезеночного изгиба. Мобилизованный отдел толстой кишки низводили в малый таз. Следующим этапом дистальный отрезок сигмовидной кишки складывали в форме буквы Э. Формировали межпетлевой анастомоз бок в бок длиной 9-10 см двухрядными узловыми швами. Ниже резервуара оставляли дистальный отрезок сигмовидной кишки длиной 8-10 см. (рис. 1).




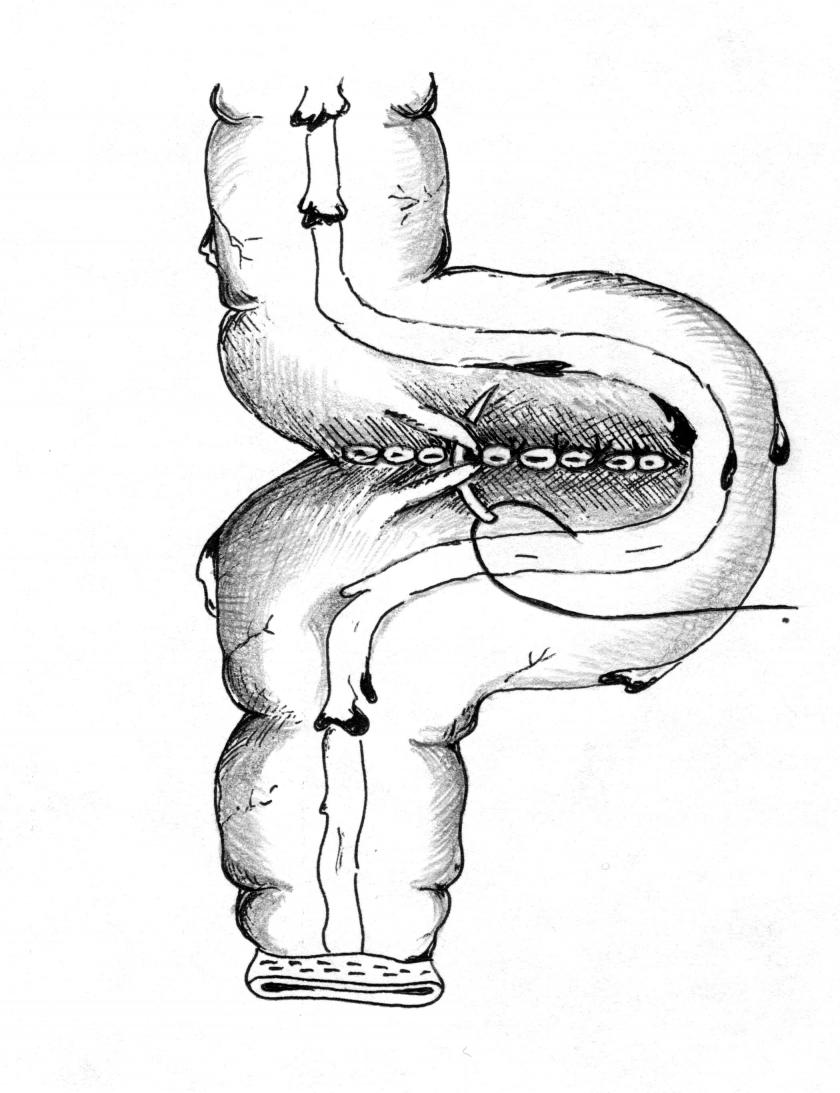
Рисунок 1. Формирование Э-образного толстокишечного резервуара двухрядными узловыми капроновыми швами.
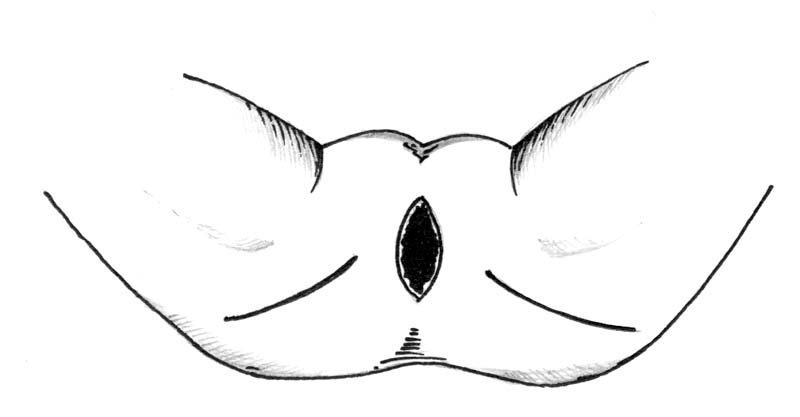
Из линейных разрезов в промежности длиной 15 см обнажали поверхности больших ягодичных мышц. С каждой стороны формировали лоскут ягодичной мышцы на ножке шириной 4 см и длиной 12-14 см. Лоскуты проводили через туннели в подкожной жировой клетчатке в промежностную рану, куда предварительно низводили дистальный отрезок сигмовидной кишки. Свободные концы мышечных лоскутов разделяли в виде ножниц. Ножки мышечных лоскутов размерами 1,5 на 3-4 см сшивали под кожей над и под дистальным отрезком сигмовидной кишки, формируя мышечное кольцо. Сигмовидную кишку подшивали к коже промежности в виде плоской колостомы. Разгрузочную колостому не накладывали (рис. 2).
 а
а  б
б
 в
в г
г
 д
д
Рисунок 2. Глютеопластика в области промежностной сигмостомы: а – линии разрезов; б – выделение лоскута ягодичной мышцы на сосудистой ножке; в – формирование ножек мышечного лоскута в виде ножниц; г – создание мышечного кольца в области промежностной сигмостомы; д – окончательный вид операции.
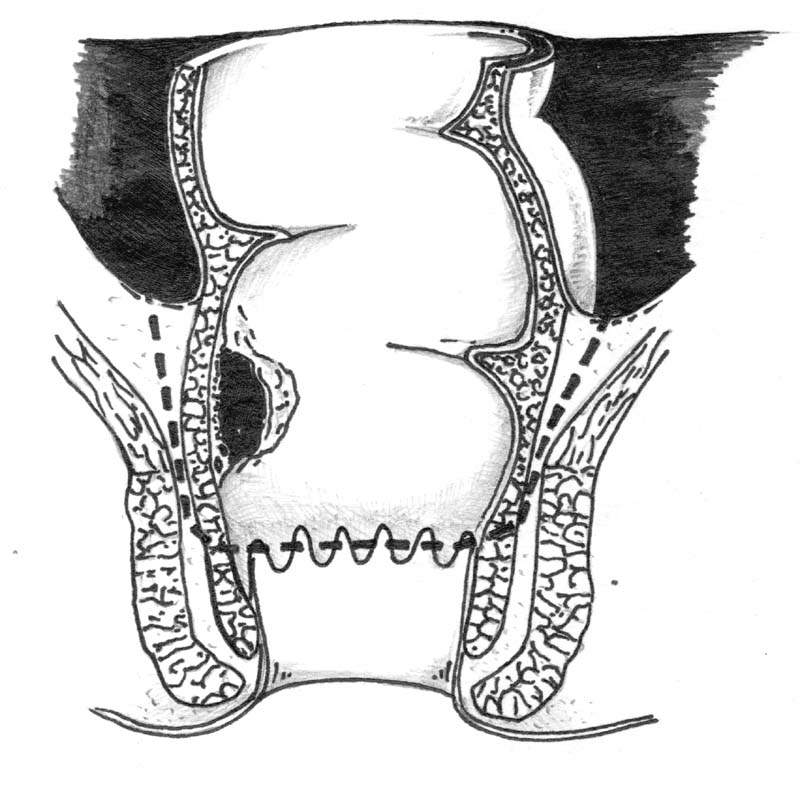
Типичную брюшно-анальную резекцию прямой кишки с низведением сигмовидной и БАР с низведением и формированем Э-образного (5 см) толстокишечного резервуара (приоритетная справка № 2004121539 от 13.07.2004г.), выполняли при раке среднеампулярного отдела прямой кишки – расстояние от анокутанной складки до нижнего края опухоли 6-8 см при отсутствии признаков прорастания опухоли в окружающие органы и ткани –T1-3N0-2M0-1. Превентивную колостому не накладывали (рис. 3).
 а
а  б
б
Рисунок 3. Брюшно-анальная резекция прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара: а – уровень резекции; б – окончательный вид операции.
Переднюю аппаратную резекцию прямой кишки выполняли при раке среднеампулярного отдела при локализации опухоли на расстоянии 8-12 см от анокутанной складки при отсутствии признаков прорастания новообразования в окружающие органы и ткани – T1-3N0-2M0-1. Для наложения межкишечного анастомоза использовали сшивающие аппараты ILS 29 ("Ethicon").
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Для выяснения особенностей морфологического строения рака прямой кишки в рамках наших проспективных клинических наблюдений изучены все 112 операционных препаратов. Распределение опухолей прямой кишки по их гистологическому виду приведено в таблице 3.
Таблица 3
Частота рака прямой кишки разного гистологического строения (n=112)
| Гистологическое строение | Количество больных | |
| абс. | % | |
| аденокарцинома | 98 | 87,5 |
| аденокарцинома со слизеобразованием | 7 | 6,2 |
| перстневидноклеточный рак | 3 | 2,7 |
| плоскоклеточный рак | 4 | 3,6 |
В наших наблюдениях аденокарциномы всех видов выявлены в 93,7% случаев. При этом, умереннодифференцированные аденокарциномы составили 72,4% от общего их числа, высокодифференцированные опухоли отмечены в 3 раза реже (23,5%). Низкодифференцированные аденокарциномы обнаружены в 4,1% случаев (табл. 4).
Таблица 4
Морфологическая дифференцировка аденокарцином прямой кишки (n=98)
| Степень дифференцировки | Количество больных | |
| абс. | % | |
| высокодифференцировая | 23 | 23,5 |
| умереннодифференцированная | 71 | 72,4 |
| низкодифференцированная | 4 | 4,1 |
В 57,7 % случаев высокодифференцированные аденокарциномы прорастали все слои кишечной стенки, при этом в 3,8% случаев опухоль переходила на окружающие органы и ткани (табл. 5). Для умереннодифференцированных аденокарцином эти показатели составили 62,0% и 6,6% соответственно. В группе больных с низкодифференцированными аденокарциномами прорастание всех слоев кишечной стенки отмечено в 75% случаев, а инвазия опухоли в окружающие органы и ткани составила 50%.
Таблица 5
Зависимость глубины инвазии опухоли от гистологического строения (n=112)
| Глубина инвазии | Гистологическое строение опухоли | ||||
| аденокарцинома | перстне-видно-клеточ-ный рак | плоско-клеточ-ный рак | |||
| высокодиф-ференци-рованная | умеренно-дифферен-цированная | низкодиф-ференци-рованная | |||
| pT1 | 3 | 5 | - | - | 1 |
| pT2 | 8 | 23 | 1 | 1 | 1 |
| pT3 | 14 | 42 | 1 | 2 | 2 |
| рТ4 | 1 | 5 | 2 | - | - |
Таблица 6
Частота лимфогенного метастазирования рака прямой кишки
в зависимости от степени местного распространения опухоли (n=112)
| Глубина инвазиии | Количество больных | ||
| общее | с метастазами в лимфоузлы | % больных | |
| рТ2 | 34 | 7 | 20,6 |
| рТ3 | 62 | 27 | 43,5 |
| рТ4 | 8 | 5 | 62,5 |
По данным гистологических исследований метастазы в регионарные лимфатические узлы выявлены у 39 больных (34,8%), при этом у 4 из них обнаружены отдаленные метастазы. У 7 из 39 больных (17,9%) глубина инвазии опухоли ограничивалась мышечным слоем. В 34 наблюдениях из 39 гистологическое строение опухоли соответствовало аденокарциноме высокой (9 пациентов), умеренной (23 больных) и низкой (2 больных) степени морфологической дифференцировки. Чаще всего регионарное лимфогенное метастазирование было обнаружено при местном распространении опухоли, соответствующем рТ3 (табл. 6).
В целом, по данным морфологических исследований основу нашего клинического материала составили пациенты с блюдцеобразной формой (64,3%) рака прямой кишки. По гистологическому строению опухоль чаще всего была верифицирована в качестве умереннодифференцированной аденокарциномы (63,4%) с инвазией всех слоев кишечной стенки в 61,9% случаев, частотой лимфогенного метастазирования соответственно у 34,8% больных. При этом, глубина инвазии опухоли в стенку прямой кишки зависит от степени ее дифференцировки, а частота регионарного метастазирования определяется глубиной опухолевой инвазии.
Общая послеоперационная летальность после хирургического лечения рака прямой кишки составила 4,5%.
В ближайшем послеоперационном периоде различные осложнения развились у 33 больных (29,5%) (табл. 7). Следует также отметить, что среди больных с осложнениями превалировали пациенты (76,9%) с глубоким (рТ3-4) внутристеночным распространением опухоли.
Таблица 7
Частота послеоперационных осложнений
в зависимости от вида оперативного вмешательства (n =112)
| Вид вмешательства | Количество больных с осложнениями | |
| абс. | % | |
| БПЭ (n=24) | 7 | 29,7 |
| БПЭ + Э (n=21) | 9 | 42,9 |
| БАР (n=18) | 9 | 50 |
| БАР + Э (n=11) | 2 | 18,2 |
| ПРПК (n=38) | 5 | 13,2 |
Все случаи послеоперационных осложнений были разделены нами на две группы: общехирургического характера и обусловленные техническими особенностями оперативных вмешательств на дистальном отделе толстой кишки. Осложнения общехирургического характера диагностированы в 15 случаях (13,4%) (табл. 8).
Таблица 8
Характер общехирургических осложнений (n=15)
| Вид вмешательства | Число осложнений | |||||
| Нагное-ние п/о раны | Тромбоз бедренной артерии | Пресак-ральный абсцесс | Пневмония | ТЭЛА | Кровотечение из зоны анастомоза | |
| БПЭ | 4 | 1 | — | 1 | — | — |
| БПЭ + Э | 1 | — | — | — | — | |
| БАР | 2 | — | — | — | 1 | — |
| БАР + Э | 1 | — | — | — | ||
| ПРПК | 1 | — | 1 | 1 | — | 1 |
| Всего | 9 | 1 | 1 | 2 | 1 | 1 |
Основную массу общехирургических осложнений (9 из 15) составили различной степени выраженности нагноения срединной или промежностной послеоперационных ран. Кровотечение из зоны сигморектоанастомоза на 9-е сутки после передней аппаратной резекции прямой кишки диагностировано в одном наблюдении.
Послеоперационные осложнения, связанные с техническими особенностями вмешательств на прямой кишке (необходимость низведения дистальных отделов толстой кишки), отмечены у 18 больных (16,4%) (табл. 9). Следует отметить, что осложнения, связанные со спецификой колоректальной хирургии, встречались несколько чаще, чем осложнения общехирургического характера. У трех пациентов осложнения были тяжелыми и потребовали повторных сложных оперативных вмешательств.
Таблица 9
Частота специфических осложнений (n =18)
| Вид вмешательства | Количество больных с осложнениями | |
| абс. | % | |
| БПЭ | 2 | 9,1 |
| БПЭ + Э | 8 | 38,1 |
| БАР | 6 | 33,3 |
| БАР + Э | 1 | 9,1 |
| ПРПК | 1 | 2,6 |
У больных, которым была выполнена брюшно-анальная резекция прямой кишки, наиболее тяжелым специфическим осложнением была несостоятельность в области сигмоанального анастомоза, за счет тракции дистального участка низведенной сигмовидной кишки вверх. Клинические признаки этих осложнений проявлялись на 4-5-е сутки после операции и манифестировали клиникой местного отграниченного перитонита малого таза. Пациентам была выполнена релапаротомия, санация и дренирование полости малого таза, сформирована двухствольная колостома. Противоестественный задний проход был закрыт через 2 месяца после операции.
В группе больных с брюшно-промежностной экстирпацией с формированием Э-образного резервуара и глютеопластикой наиболее частым специфическим осложнением была стриктура промежностной сигмостомы (5 случаев). В двух наблюдениях ее причиной явился непротяженный некроз (I ст.) низведенной сигмовидной кишки, который был обусловлен избыточным сдавлением кишечной стенки и ее ишемией вновь сформированным сфинктером из больших ягодичных мышц. Следует отметить, что данные осложнения встречались на раннем этапе освоения методики. Стриктуры развивались в сроки от 3 до 12 месяцев и устранялись оперативным путем. У одной больной диагностировано протяженное продуктивное воспаление (11 см) низведенной сигмовидной кишки, что привело к нагноению послеоперационных ран промежности в области глютеопластики. Гнойно-воспалительные осложнения в области промежности купированы наложением двухствольной трансверзостомы.
Анализ результатов оперативного лечения рака средне- и нижнеампулярного отделов прямой кишки основывался на комплексной оценке состояния пациентов в послеоперационном периоде. Основу изучения функциональных результатов операций составили данные анкетирования больных, включавшие оценку характера стула (частота, консистенция и др.), функции континенции, наличии предвестников дефекации и качества жизни. Объективная оценка функциональных результатов осуществлялась по данным импедансометрии.
Полученные нами результаты импедансометрии свидетельствуют, что запирательная функция сфинктера прямой кишки после выполнения сфинктеросохраняющих операций практически не страдает. В группах после брюшно-анальной резекции прямой кишки с низведением сигмовидной (независимо от наличия или отсутствия резервуара) и передней резекции прямой кишки наблюдается незначительное снижение базального тонуса (табл. 10).
Таблица 10
Данные импедансометрии
| Виды оперативных вмешательств | Число обследований | Базальный тонус (Ом) | Амплитуда максимальных произвольных сокращений (Ом) |
| Контрольная (без операции) | 20 | 135,5±14,3 | 35,4±15,2 |
| Брюшно-анальная резекция прямой кишки с низведением | 14 | 95,3±30,1 | 20±5,3 |
| Передняя резекция прямой кишки | 16 | 104,5±20,4 | 27,5±6,2 |
Амплитуда максимальных произвольных сокращений после брюшно-анальной резекции и передней резекции прямой кишки варьирует в пределах нижней границы нормы. Однако при изучении данных анкетирования у пациентов после операций по поводу рака среднеампулярного отдела прямой кишки функциональные результаты достоверно зависели от вида оперативного вмешательства. Наилучшие показатели отмечены после передней аппаратной резекции. Средняя частота стула после этой операции составляла 2-3 раза в сутки в течение первого месяца и через 3-6 месяцев полностью нормализовывалась. Консистенция стула – от кашицеобразного в течение 1-3 месяцев после операции до оформленного. Синдром «низкой передней резекции» встречался в 23,6 % случаев. Инконтиненция I степени диагностирована у 9 пациентов. Через 3-6 месяцев после операции больные чувствуют себя удовлетворительного и жалоб со стороны желудочно-кишечного тракта практически не предьявляют. Все больные непенсионного возраста сохранили работоспособность.
После брюшно-анальной резекции прямой кишки с низведением сигмовидной частота стула в течение первого месяца составляла в среднем 7-8 раз в день, жидким или кашицеобразным содержимым. Через полгода после вмешательства частота стула урежается только до 5-7 раз в день. В течение 1 месяца после операции нарушения континенции определялись у 47,6% больных: у 19% - I степени, еще у 19% – II, у 9,6% – III степени. Континенция восстанавливалась через 12 и более месяцев после операции, однако у одного пациента отмечена инконтиненция I степени даже через 5 лет после операции. У 30% больных через год и более после операции имеют место преходящие нарушения континенции, которые носят сезонный характер (лето) и связаны с расширением диеты. Введение в рацион большего количества продуктов, содержащих клетчатку, меняет консистенцию стула на кашицеобразный и приводит к инконтиненции I-II степени. Трудоспособность у таких больных восстанавливается позднее, чем в группе пациентов после передней резекции прямой кишки.
После брюшно-анальной резекции прямой кишки с формированием Э-образного толстокишечного резервуара функциональные результаты у больных были значительно лучше, чем у пациентов после типичной брюшно-анальной резекции. Так, частота стула в течение первого месяца в среднем составляла 4-5 раз в день, преимущественно кашицеобразным содержимым. Однако уже через 3 месяца после операции частота стула урежалась до 2-3 раз в день, а через полгода – стул становился оформленным с частотой 1-2 раза в сутки. К концу первого года после операции стул в среднем 1 раз в сутки, отмечаются периодические запоры – стул 1 раз в два дня, консистенция оформленная. Двое больных через 4 года после операции для облегчения опорожнения резервуара используют слабительные. Никто из пациентов не страдает императивными позывами, дефекация у всех одномоментная и никто из них не придерживается какой-либо специальной диеты. В данной группе больных нарушения континенции сведено к минимуму, только у одного больного отмечена инконтиненция II степени. Континенция восстанавливается полностью через 6 месяцев после операции. За исключением одного больного, все пациенты непенсионного возраста сохранили работоспособность.
Оценка профиля качества жизни выполнялась у 31 пациента с локализацией опухоли в среднеампулярном отделе прямой кишки. На дооперационном этапе определялось достоверное снижение всех параметров качества жизни относительно общепопуляционного профиля. Суммарные показатели физического и психического здоровья составили 45±6,7 и 58,2±7,3, соответственно. Изучение качества жизни у пациентов с диагностированным раком среднеампулярного отдела прямой кишки через три месяца после оперативного вмешательства показало, что лучшие параметры по большинству шкал опросника имеют место после выполнения передней аппаратной резекции прямой кишки. Сопоставление суммарных показателей качества жизни убедительно подтвердило превосходство результатов аппаратной резекции прямой кишки над другими видами оперативного лечения (рис. 4). 
Рисунок 4. Суммарные показатели качества жизни больных раком среднеампулярного отдела прямой кишки через 3 месяца после операции. (СФК – суммарный физический компонент здоровья, СПК – суммарный психический компонент здоровья).
Кроме того, оказалось, что интегральные показатели физического и психического здоровья лучше при выполнении брюшно-анальной резекции, дополненной формированием Э-образного резервуара, чем у больных с типичной брюшно-анальной резекцией прямой кишки. Суммарный физический компонент при передней резекции прямой кишки, брюшно-анальной резекции с формированием резервуара и типичной брюшно-анальной резекции составил 53,3±5,4, 48,6±6,2, 39,7±6,8 (р0,05), соответственно. Суммарный психический компонент при тех же видах операций был 61,2±6,4, 51,3±5,4, 42,7±6,9 (р0,05), соответственно. Изучение данных анкетирования через 6 месяцев после операции у больных раком среднеампулярного отдела прямой кишки показал улучшение качества жизни у всех оперированных. При сравнении трех видов оперативных вмешательств по суммарным показателям качества жизни было установлено, что через полгода после операции результаты брюшно-анальной резекции с и без формирования Э-образного резервуара близки к результатам передней аппаратной резекции прямой кишки.
Частота развития местных рецидивов после операций по поводу рака среднеампулярного отдела прямой кишки составила 14,5%. Хотя при брюшно-анальной резекции прямой кишки с формированием Э-образного толстокишечного резервуара рецидивы рака встречались относительно чаще, чем при других сфинктеросохраняющих вмешательствах, эти отличия были статистически недостоверны. При оценке выживаемости пациентов со злокачественным поражением среднеампулярного отдела прямой кишки по методу E. Kaplan – P. Meier трех- и пятилетняя выживаемость составили 73,1±7,5% и 68,2±8,5% соответственно (рис. 5).

Рисунок 5. Кумулятивная выживаемость пациентов раком среднеампулярного отдела прямой кишки.
При сравнительном анализе актуариальной выживаемости в зависимости от вида выполненного оперативного пособия пятилетние показатели были: после передней аппаратной резекции прямой кишки – 70±12,2%, после брюшно-анальной резекции дополненной формированием Э-образного резервуара – 66,7±19,2%, после типичной брюшно-анальной резекции – 55,3±14,2%.
Таким образом, сравнительный анализ вариантов оперативного лечения рака среднеампулярного отдела прямой кишки с учетом функциональных результатов, послеоперационных осложнений и кумулятивной выживаемости показал, что операцией выбора при расположении опухоли от 7 до 12 см от анокутанной складки является передняя аппаратная резекция. При технической невозможности выполнения аппаратной резекции (дистальный клиренс резекции менее 2-3 см) показана брюшно-анальная резекция с формированием Э-образного (5 см) толстокишечного резервуара, поскольку данный вид операции по своим функциональным показателям близок к передней резекции прямой кишки.
Комплексный сравнительный анализ результатов оперативного лечения рака нижнеампулярного отдела прямой кишки показал, что при импедансометрии значения базального тонуса в колостоме на передней брюшной стенке (после выполнения брюшно-промежностной экстирпации прямой кишки) был почти в два раза ниже, чем после экстирпации с формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы (27,2±5,1Ом и 40,1±4,7Ом (р0,05), соответственно) (табл. 11).
Таблица 11
Данные импедансометрии после оперативного лечения рака нижнеампулярного отдела прямой кишки
| Виды оперативных вмешательств | Число обследований | Базальный тонус (Ом) | Амплитуда максимальных произвольных сокращений (Ом) |
| Контрольная группа (без операции) | 20 | 135,5±14,3 | 35,4±15,2 |
| Противоестественный задний проход | 7 | 27,2±5,4 | 6,5±1,3 |
| БПЭ + Э | 16 | 40,1±7,3 | 14,8±4,2 |
Значение глубины перистальтических волн у больных после брюшно-промежностной экстирпации прямой кишки с глютеопластикой указывали на более эффективную запирательную функцию, в сравнении с лишенной сфинктера колостомой (14,8±4 Ом и 6,5±1 Ом (р0,05), соответственно).
Опрос пациентов о характере стула выявил, что после брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы частота стула в течение первого месяца составляла в среднем 4-5 раз в день, преимущественно кашицеобразным содержимым. Через 3 месяца после операции она урежалась до 3-4 раз в день, а через 6 месяцев имел место оформленный стул 1-2 раза в сутки. В отдаленном периоде - стул в среднем 1 раз в сутки, отмечаются периодические запоры, дефекация многомоментная. Большинство больных для облегчения опорожнения резервуара используют слабительные препараты, очистительные клизмы. Нарушения континенции имеются у всех больных данной группы. Однако с течением времени степень инконтиненции уменьшается. В среднем через год после вмешательства появляются предвестники дефекации в виде вздутия, тяжести и распирания в нижних отделах живота у трети больных. Появляется чувство наполнения сформированной ампулы с позывом к дефекации. Половина пациентов способна удерживать газы за счет произвольного сокращения ягодичных мышц в области промежностной сигмостомы.
Качество жизни больных раком нижнеампулярного отделов прямой кишки до лечения было значительно снижено. Суммарные физический и психический компонент здоровья составили 45,6±6,1 и 55±5,4, соответственно. Спустя 3 месяца после операции значимо лучшие показатели качества жизни имели место у больных после брюшно-промежностной экстирпацией с формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы. Противоположные результаты отмечены у больных с формированием anus prаeternaturalis на передней брюшной стенке. Практически по всем шкалам опросника наблюдалось снижение параметров качества жизни. Пациенты этой группы характеризовались резким ограничением в выполнении физической нагрузки, испытывали периодический болевой синдром, сохранялось ощущение выраженной усталости. Резкое снижение показателей опросника по шкалам, отражающим психическое здоровье свидетельствует о преобладании у больных данной категории плохого настроения, отрицательных эмоций и постоянной депрессии. Данные изменения следует расценивать как следствие наложенного противоестественного заднего прохода на передней брюшной стенке. Сравнение двух видов оперативного вмешательства по суммарным показателям физического и психического здоровья также показало превосходство качества жизни после выполнения брюшно-промежностной экстирпации, дополненной формированием Э-образного резервуара и глютеопластикой (45,5±7,3 и 60,5±6,9 против 30±5,2 и 49±5,7 (р0,05), соответственно) (рис. 6). Через 6 месяцев после операции профиль качества жизни у пациентов с локализацией опухоли в нижнеампулярном отделе прямой кишки значимо не отличался от такового в ближайшем послеоперационном периоде. Однако у больных после брюшно-промежностной экстирпацией прямой кишки с формированием Э-образного толстокишечного резервуара и глютеопластикой наблюдалось дальнейшее улучшение показателей, характеризующих эмоциональное состояние человека и его влияние на профессиональную или повседневную деятельность.

Рисунок 6. Суммарные показатели качества жизни больных раком нижнеампулярного отдела прямой кишки через 3 месяца после операции. (СФК – суммарный физический компонент здоровья, СПК – суммарный психический компонент здоровья).
Пациенты отмечали прибавление сил и энергии, снижение усталости, утомляемости. Показатели качества жизни больных с противоестественным задним проходом оставались неизменными.
Местный рецидив развился у одного пациента после резервуарно-пластической операции по поводу рака нижнеампулярного отдела Т3N2M0 и носил экстраорганный характер. Двое больных после типичной брюшно-промежностной экстирпации прямой кишки умерли в раннем послеоперационном периоде от развившихся осложнений.
Актуариальная выживаемость после операций у пациентов с поражением нижнеампулярного отдела прямой кишки была в период наблюдения до года 91±4,3%, от 1 до 2 лет – 75±6,9% (рис. 7).
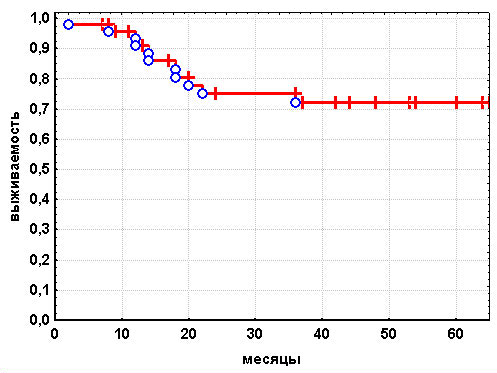
Рисунок 7. Кумулятивная выживаемость больных раком нижнеампулярного отдела прямой кишки.
Пятилетний рубеж пережили 72±7,2% оперированных. При сравнительном анализе кумулятивной выживаемости лучшие результаты отмечены у больных после брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы. В этой группе пациентов пятилетняя выживаемость составила 83,5±8,8%, тогда как в группе после типичной брюшно-промежностной экстирпации данный показатель равнялся 71,4±17%, соответственно. Данное наблюдение объясняется наличием в последней группе пациентов с более запущенными стадиями рака прямой кишки.
Полученные результаты свидетельствуют, что разработанная и внедренная в клиническую практику оригинальная методика брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы позволяет улучшить функциональные результаты хирургического лечения рака нижнеампулярного отдела прямой кишки. Данный способ оперативного пособия позволяет избежать главного фактора инвалидизации пациентов – противоестественного заднего прохода на передней брюшной стенке. Кроме того, разработанная методика не требует наложения превентивной колостомы. Сочетание значительного по размерам толстокишечного резервуара (10 см) и вновь созданного из ягодичных мышц сфинктера создает приемлемую в повседневной жизни промежностную сигмостому, что значительно улучшает социально-психологическую адаптацию и трудовую реабилитацию этой тяжелой категории больных.
Таким образом, наиболее важными направлениями улучшения хирургического лечения рака средне- и нижнеампулярного отделов прямой кишки являются дифференцированный подход к выбору адекватного объема и вида оперативного вмешательства, с учетом предоперационного стадирования опухоли и стремление к выполнению сфинктеросохраняющих и резервуарно-пластических операций.
Выводы
1. В большинстве случаев рака средне- и нижнеампулярного отделов прямой кишки имеет место умереннодифференцированная аденокарцинома (63,4%). Степень дифференцировки опухоли определяет глубину поражения стенки прямой кишки, что в свою очередь влияет на увеличение частоты регионарного метастазирования.
2. В ближайшем послеоперационном периоде различные осложнения и их сочетания отмечены в 29,5% случаях. Из них осложнения общехирургического характера составили 13,4% наблюдений, а связанные с техническими особенностями вмешательств на прямой кишке – 16,4% случаев. Внедрение в хирургическую практику резервуарно-пластических операций не приводит к увеличению частоты послеоперационных осложнений и летальности.
3. При раке среднеампулярного отдела прямой кишки наилучшие функциональные результаты получены после выполнения передней аппаратной резекции прямой кишки. Формирование Э-образного толстокишечного резервуара улучшает функциональные результаты брюшно-анальной резекции прямой кишки с низведением сигмовидной. Брюшно-промежностная экстирпация прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы улучшает функциональные результаты хирургического лечения рака нижнеампулярного отдела прямой кишки.
4. Лучшие параметры качества жизни имеют место после выполнения передней аппаратной резекции прямой кишки. Интегральные показатели физического и психического здоровья лучше при выполнении брюшно-анальной резекции прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара, чем у больных с традиционной брюшно-анальной резекцией прямой кишки с низведением. Качество жизни больных нижнеампулярным раком прямой кишки значимо лучше после брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы, чем у пациентов, которым выполнена экстирпация прямой кишки с формированием anus prаeternaturalis.
5. Пятилетняя выживаемость у больных, оперированных по поводу рака среднеампулярного отдела прямой кишки составила 68,2±8,5%. Актуариальная выживаемость после операций у пациентов с поражением нижнеампулярного отдела прямой кишки через пять лет составила 72±7,2%. Выживаемость больных в обеих группах не зависела от метода хирургического лечения, а определялась стадией опухолевого процесса.
6. У больных раком среднеампулярного отдела прямой кишки операцией выбора является передняя аппаратная резекция прямой кишки, а при технической невозможности ее выполнения – брюшно-анальная резекция прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара.
7. При хирургическом лечении больных раком нижнеампулярного отдела прямой кишки с целью улучшения функциональных результатов и качества жизни оперированных пациентов целесообразно выполнять брюшно-промежностную экстирпацию прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы.
Практические рекомендации:
1. Для улучшения результатов хирургического лечения рака средне- и нижнеампулярного отделов прямой кишки необходим дифференцированный подход к выбору метода операции, который основывается на дооперационном стадировании рака прямой кишки и интраоперационной ревизии органов брюшной полости и малого таза.
2. Обязательными методами предоперационной диагностики являются: ректороманоскопия, фиброколоноскопия, эндоректальная сонография, компьютерная томография органов малого таза, рентгенография легких и УЗИ органов брюшной полости. При выявлении на этапе дооперационного стадирования рака T3NX-X+M0 – больным показано проведение неоадъювантной лучевой терапии в течение 5 дней (СОД=25Гр).
3. Для уменьшения частоты местного рецидивирования и интраоперационного метастазирования больным раком средне- и нижнеампулярного отделов прямой кишки показано проведение неоадъювантной регионарной химиотерапии – суперселективной масляной химиоэмболизации верхней прямокишечной аретрии.
4. При расположении опухоли в среднеампулярном отделе прямой кишки (8-12 см от анокутанной складки) показано выполнение передней аппаратной резекции прямой кишки. В случае локализации опухоли на 6-8 см от анокутанной складки и технической невозможности выполнения передней аппаратной резекции целесообразно выполнять брюшно-анальную резекцию прямой кишки с низведением сигмовидной и формированием Э-образного толстокишечного резервуара. Наличие отдаленных метастазов у больных данной категории не является противопоказанием к выполнению передней резекции и брюшно-анальной резекции прямой кишки с формированием Э-образного резервуара.
5. У больных раком нижнеампулярного отдела прямой кишки, радикальном удалении опухоли, удовлетворительном состоянии и отсутствии тяжелой сопутствующей соматической патологии, достаточной длине левых отделов ободочной кишки для низведения показано выполнение брюшно-промежностной экстирпации прямой кишки с низведением сигмовидной в рану промежности, формированием Э-образного толстокишечного резервуара и глютеопластикой в области промежностной сигмостомы.
Список работ, опубликованных по теме диссертации:
- Зубарев П.Н. Методы лечения больных с колоректальным раком IV стадии / П.Н. Зубарев, Г.И. Синенченко, И.Г. Игнатович, О.А. Литвинов, С.Н. Петров, А.И. Хватов, С.М. Алешкина, Д.Г. Прохоров // Анналы хирург. гепатологии. – 1999. – Т. 4, №2. – С. 190-191.
- Прохоров Г.Г. Ближайшие результаты криодеструкции метастазов рака в печени / Г.Г. Прохоров, В.Б. Муравьев, Д.Г. Прохоров, О.А. Литвинов // Диагностика и лечение опухолей печени. – СПб., 1999. – С. 95.
- Прохоров Г.Г. Возможности современной криохирургии в лечении онкологических больных / Г.Г. Прохоров, В.Б. Муравьев, Д.Г. Прохоров, О.А. Литвинов // 3-я ежегодная Российская онкологическая конференция. – СПб., 1999. – С. 164.
- Прохоров Г.Г. Опыт применения криодеструкции метастазов печени / Г.Г. Прохоров, С.И. Морозова, О.А. Литвинов, В.Б. Муравьев, Д.Г. Прохоров // Анналы хирург. гепатологии. – 1999. – Т. 4, №2. – С. 197.
- Прохоров Г.Г. Показания к криохирургическому лечению метастазов рака в печени / Г.Г. Прохоров, В.Б. Муравьев, Д.Г. Прохоров, О.А. Литвинов // Диагностика и лечение опухолей печени. – СПб., 1999. – С. 126.
- Шишляков С.В. Особенности анестезиологического обеспечения криохирургических операций на печени / С.В. Шишляков, Ю.Ю. Щербаков, О.А. Литвинов // Диагностика и лечение опухолей печени. – СПб., 1999. – С.151.
- Прохоров Г.Г. Криодеструкция метастазов печени / Г.Г. Прохоров, О.А. Литвинов, Д.Г. Прохоров, В.Б. Муравьев // Вестн. хирургии. – 2000. – Т. 159, №3. – С. 177.
- Прохоров Г.Г. Криохирургия в лечении метастатических опухолей печени / Г.Г. Прохоров, О.А. Литвинов // Тр. / Воен. – мед. акад. – СПб., 2000. – Т. 251. – С. 174-181.
- [Прохоров Г.Г.] Prochorov G.G. Thermophysical border of cryosurgical treatment of the large metastasis in a liver / [Г.Г. Прохоров, С.И. Морозова, Д.Г. Прохоров, А.П. Андреев, А.В. Власова, О.А. Литвинов]. G.G. Prochorov, S.I. Morosova, D.G. Prochorov, A.P. Andreev, A.V. Vlasova, O.A. Litvinov // Cryosurgery. – 2000. – Vol. 4. – Р. 11-12.
- Зубарев П.Н. Первый опыт выполнения резервуарно-пластических операций при лечении рака нижнеампулярного отдела прямой кишки / П.Н. Зубарев, О.А. Литвинов, А.Г. Арустамов // Актуальные вопросы грудной, сердечно-сосудистой и абдоминальной хирургии. – СПб., 2001. – С. 100-101.
- Прохоров Г.Г. Острая гипотермия при криохирургических операциях / Г.Г. Прохоров, Д.А. Гранов, С.И. Морозова, Д.Г. Прохоров, А.П. Андреев, А.В. Власова, А.Ю. Чудаков, О.А. Литвинов // Достижения криомедицины. – СПб., 2001. – С. 52-55.
- [Прохоров Д.Г.] Prochorov D.G. Acute Total Body Hypothermia in Cryosurgery / [Д.Г. Прохоров, А.П. Андреев, А.В. Власова, О.А. Литвинов]. D.G. Prochorov, A.P. Andreev, A.V. Vlasova, O.A. Litvinov // Basics of сryosurgery. – Wien; New York, – 2001. – Р. 307-314.
- [Прохоров Г.Г.] Prochorov G.G. Lesions / [Г.Г. Прохоров, Д.Г. Прохоров, О.А. Литвинов]. G.G. Prochorov, D.G. Prochorov, O.A. Litvinov // Basics of сryosurgery. – Wien; New York, – 2001. – Р. 130-133.
- Арустамов А.Г. Профилактика тромбоэмболических осложнений при выполнении резервуарно-пластических операций на толстой кишке / А.Г. Арустамов, О.А. Литвинов, Н.С. Солопов // Материалы науч. -практ. конф., посвящ. 40-летию Санкт-Петербургской клинической больницы РАН. – СПб., 2002. – С. 37-38.
- Кочетков А.В. Оценка функциональных результатов радикальных операций по поводу рака прямой кишки / А.В. Кочетков, О.А. Литвинов, И.А. Соловьев, Н.С. Солопов // Гастроэнтерология Санкт-Петербурга. – 2004, №2-3. – С. 81.
- Литвинов О.А. Брюшно-анальная резекция прямой кишки с низведением, формированием Э-образного толстокишечного резервуара в лечении рака среднеампулярного отдела прямой кишки / О.А. Литвинов, А.Г. Арустамов, И.А. Соловьев // Совершенствование специализированной медицинской помощи в многопрофильном стационаре. – Красногорск, 2004. – С. 244-246.
- Литвинов О.А. Применение Э-образных резервуаров в хирургическом лечении рака прямой кишки / О.А. Литвинов, И.Г. Игнатович, И.А. Соловьев // Актуальные вопросы клинической хирургии. – СПб., 2004. – С. 96-98.
- Литвинов О.А. Резервуарно-пластические операции в лечение рака нижнеампулярного отдела прямой кишки / О.А. Литвинов, А.Г. Арустамов, И.А. Соловьев // Совершенствование специализированной медицинской помощи в многопрофильном стационаре. – Красногорск, 2004. – С. 246-247.
- Соловьев И.А. Эндоскопическое удаление крупных ворсинчатых опухолей толстой кишки с обработкой их основания лучевой аргоновой коагуляцией / И.А. Соловьев, Д.К. Джачвадзе, И.Г. Игнатович, О.А. Литвинов // Актуальные вопросы клинической хирургии. – СПб., 2004. – С.117-118.
- Алентьев С.А. Новый способ неоадьювантной химиотерапии в комплексном лечении рака прямой кишки / С.А. Алентьев, О.А. Литвинов, И.Г. Игнатович, М.Л. Гринев, И.И. Дзидзава, С.М. Рыбаков, И.А. Соловьев // Сб. науч. статей, посвящ. 100-летию железнодорожной медицины на станции Волховстрой. – СПб., 2005. – С. 81-82.
- Зубарев П.Н. Масляная химиоэмболизация сигмовидных и верхних прямокишечных артерий у больных раком сигмовидной и прямой кишки / П.Н. Зубарев, Б.Н. Котив, С.А. Алентьев, О.А. Литвинов, И.Г. Игнатович, М.В. Лазуткин, И.А. Соловьев // Материалы 9-го Российского онкологического конгресса. – М., 2005. – С. 188.
- Игнатович И.Г. Использование аргон-плазменной коагуляции при удалении крупных ворсинчатых опухолей толстой кишки / И.Г. Игнатович, О.А. Литвинов, И.А. Соловьев // Новые технологии в хирургии. – Ростов н/Д., 2005. – С. 368
- Литвинов О.А. Хирургическое лечение рака прямой кишки / О.А. Литвинов, И.Г. Игнатович, И.А. Соловьев // Новые технологии в хирургии. – Ростов н/Д., 2005. – С. 354-355.
- Алентьев С.А. Значение эндоректальной сонографии в оценке степени местного распространения рака прямой кишки / С.А. Алентьев, И.Г. Игнатович, И.А. Соловьев, О.А. Литвинов // Материалы 10-го Российского онкологического конгресса. – М., 2006. – С. 214.
- Алентьев С.А. Масляная химиоэмболизация печеночной артерии с использованием оксалиплатина при метастазах колоректального рака в печень / С.А. Алентьев, Б.Н. Котив, И.И. Дзидзава, О.А. Литвинов, И.А. Соловьев // Анналы хирург. гепатологии. – 2006. – Т. 11, №3. – С. 178.
- Зубарев П.Н. Способ комбинированного лечения рака левой половины толстой кишки и верхнеампулярного отдела прямой кишки / П.Н. Зубарев, С.А. Алентьев, Б.Н. Котив, О.А. Литвинов, И.А. Соловьев, И.И. Дзидзава, М.В. Лазуткин, И.Г. Игнатович // Усовершенствование способов и аппаратуры, применяемых в учебном процессе, медико-биологических исследованиях и клинической практике. – СПб., 2006. – Вып. 37. – С. 36.
- Литвинов О.А. Возможности эндоректаальной сонографии в оценке степени местного распространения опухолевого процесса у больных раком прямой кишки / О.А. Литвинов, С.А. Алентьев, А.Г. Арустамов, И.Г. Игнатович, И.А. Соловьев // Вестн. Санкт-Петербург. мед. акад. – 2006. – Т.7, №4. – С. 61-66.
- Алентьев С.А. Предоперационная масляная химиоэмболизация верхней прямокишечной артерии при раке прямой кишки / С.А. Алентьев, Б.Н. Котив, М.В. Лазуткин, О.А. Литвинов, И.А. Соловьев // Невский радиологический форум «Новые горизонты». – СПб., 2007. – С. 506-507.
- Зубарев П.Н. Резервуарная техника в хирургическом лечении рака среднеампулярного отдела прямой кишки / П.Н. Зубарев, О.А. Литвинов, И.Г. Игнатович, И.А. Соловьев // Вестн. Рос. Воен. – мед. акад. – 2007. – №1, прилож. – С. 563.
- Зубарев П.Н. Формирование толстокишечного резервуара в хирургическом лечении рака среднеампулярного отдела прямой кишки / П.Н. Зубарев, О.А. Литвинов, И.Г. Игнатович, И.А. Соловьев // Вестн. Рос. Воен. – мед. акад. – 2007. – №2. – С. 5-10.
- Зубарев П.Н. Первый опыт предоперационной масляной химиоэмболизации верхней прямокишечной артерии при раке прямой кишки / П.Н. Зубарев, Б.Н. Котив, С.А. Алентьев, О.А. Литвинов, И.Г. Игнатович, М.В. Лазуткин, И.А. Соловьев // Вестн. Национального мед. – хир. центра им. Н.И. Пирогова. – 2007. – Т. 2, №1. – С.45-47.
- Литвинов О.А. Резервуарно-пластическая техника в хирургическом лечении рака нижнеампулярного отдела прямой кишки / О.А. Литвинов // Вестн. Рос. Воен. – мед. акад. – 2007. – №1, прилож. – С. 562.
- Литвинов О.А. Резервуарно-пластические операции в лечении рака нижнеампулярного отдела прямой кишки / О.А. Литвинов, И.А. Соловьев // Вестн. Рос. Воен. – мед. акад. – 2007. – №2. – С. 10-15.
- Соловьев И.А. Возможности эндоректальной сонографии в дооперационном стадировании рака прямой кишки / И.А. Соловьев, С.А. Алентьев, О.А. Литвинов, И.Г. Игнатович // Вестн. Рос. Воен. – мед. акад. – 2007. – №1, прилож. – С. 564.
- Соловьев И.А. Значение эндоректальной сонографии в выборе способа комбинированного лечения рака прямой кишки / И.А. Соловьев, С.А. Алентьев, Н.А. Олейник, И.Г. Игнатович, О.А. Литвинов // Невский радиологический форум «Новые горизонты». – СПб., 2007. – С. 235-237.

