Кинетика процесса окисления глюкозы с помощью микроорганизма escherichia coli в присутствии экзогенных медиаторов
На правах рукописи
КУЗЬМИЧЕВА ЕЛЕНА ВАЛЕРЬЕВНА
КИНЕТИКА ПРОЦЕССА ОКИСЛЕНИЯ ГЛЮКОЗЫ С ПОМОЩЬЮ МИКРООРГАНИЗМА ESCHERICHIA COLI В ПРИСУТСТВИИ ЭКЗОГЕННЫХ МЕДИАТОРОВ
Специальность 02.00.05 – электрохимия
АВТОРЕФЕРАТ
диссертации на соискание учёной степени
кандидата химических наук
Саратов – 2009
Работа выполнена на кафедре физической химии
ГОУ ВПО «Саратовский государственный университет
им. Н.Г. Чернышевского»
Научный руководитель: доктор химических наук, профессор
Казаринов Иван Алексеевич
Официальные оппоненты: доктор химических наук
Камнев Александр Анатольевич
доктор технических наук, профессор
Шпак Игорь Евгеньевич
Ведущая организация: Воронежский государственный
университет, г. Воронеж
Защита состоится 26 июня 2009 г. в 1400 часов на заседании Диссертационного совета Д 212.243.07 по химическим наукам при ГОУ ВПО «Саратовский государственный университет им. Н.Г. Чернышевского» по адресу: 410012, г. Саратов, ул. Астраханская, д. 83, I корпус.
С диссертацией можно ознакомиться в Зональной научной библиотеке им. В.А. Артисевич Саратовского государственного университета им. Н.Г. Чернышевского.
Автореферат разослан 25 мая 2009 г.
Ученый секретарь
диссертационного совета,
доктор химических наук В.В. Сорокин
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. На протяжении XX века мировой расход энергии существенно возрос, что привело энергетику в неуравновешенное состояние. Интерес к разработке альтернативных источников энергии, в том числе и химических источников тока, не ослабевает в связи с грядущим глобальным истощением на Земле источников полезных ископаемых, используемых для нужд энергетики. В настоящее время новым витком в развитии электрохимической энергетики является создание биологических топливных элементов (БТЭ), представляющих собой устройства, которые используют биологические компоненты как катализаторы для генерации электричества.
В отличие от химических топливных элементов, биологические работают при более мягких условиях, а именно при комнатных температуре и давлении. Они также используют нейтральный электролит и недорогие катализаторы. В БТЭ в качестве катализаторов применяют либо целые микроорганизмы, либо ферментные препараты. В связи с этим БТЭ подразделяют на ферментные топливные элементы (ФТЭ) и микробные топливные элементы (МТЭ). Кроме того, в отличие от химических топливных элементов, использующих водород, этанол и метанол как топливо, БТЭ в качестве топлива могут использовать энергетически ёмкие, но электрохимически пассивные вещества (углеводы, органические кислоты и спирты), а также многие органические отходы. Это открывает возможность одновременного решения энергетической и экологической проблем.
Перспективным направлением является подход, основанный на использовании в качестве биокатализаторов целых микроорганизмов. По мощности и кулоновской эффективности МТЭ, использующие экзогенные редокс-медиаторы для переноса электронов от бактериальной клетки к электроду, пока уступают МТЭ с прямым переносом электронов. Эффективность их работы зависит от многих параметров. К ним в первую очередь следует отнести природу экзогенного медиатора и микроорганизма и их совместимость друг с другом. Каталитическая активность микроорганизмов в присутствии экзогенных редокс-медиаторов, а также кинетика процессов, протекающих на микробных медиаторных электродах, на сегодняшний день мало изучены. Существует только несколько попыток их исследования c применением современных методов экспериментальной электрохимии. Между тем, исследование кинетических закономерностей процессов, протекающих на биоанодах, представляется действительно актуальной задачей, поскольку они могут служить фундаментальной основой при создании МТЭ медиаторного типа.
Цель работы. Установление кинетических закономерностей процесса окисления глюкозы с помощью микроорганизма Escherichia coli в присутствии экзогенных медиаторов.
Для достижения поставленной цели необходимо решить следующие основные задачи:
- изучить электрохимическое поведение экзогенных редокс-медиаторов, выбранных из различных классов веществ (тиазины, азины и оксазины), в рабочем электролите и оценить их коэффициенты диффузии;
- определить эффективность работы исследуемых медиаторов в биоэлектрохимической системе;
- изучить электрохимическими методами кинетику процесса биоэлектрокаталитического окисления глюкозы клетками Escherichia coli и определить кинетические параметры этого процесса;
- создать макет микробного топливного элемента и изучить кинетику процесса окисления глюкозы на микробном медиаторном аноде в условиях его работы.
Научная новизна. Впервые электрохимическими методами проведено изучение каталитической активности микроорганизма Escherichia сoli при окислении глюкозы в присутствии экзогенных медиаторов – метиленового синего, нейтрального красного и галлоцианина. Обосновано и доказано, что метиленовый синий и галлоцианин являются эффективными медиаторами при реализации микробного медиаторного анода на основе клеток Escherichia сoli. Установлено, что процесс окисления метиленового синего на биоаноде протекает в режиме смешанного диффузионно-кинетического контроля, а процесс окисления галлоцианина – в режиме диффузионной кинетики. Определены кинетические характеристики реакции окисления метиленового синего на биоаноде – порядок реакции и гетерогенная константа скорости.
На основе уравнения Михаэлиса-Ментен проведен кинетический анализ процессов диффузии метиленового синего и галлоцианина между клеткой (катализатором) и контактирующим с ней раствором. Показано, что метиленовый синий является более эффективным медиатором по сравнению с галлоцианином в реакции окисления глюкозы с помощью микроорганизма Escherichia coli.
Изучена кинетика процесса окисления глюкозы бактериальными клетками в условиях работы макета микробного топливного элемента. Показано, что лимитирующей стадией в работе микробного медиаторного анода является процесс окисления медиатора – метиленового синего.
Практическая значимость. Разработан микробный медиаторный анод на основе клеток Escherichia coli для процесса окисления глюкозы и оптимизированы условия его работы. Проведенные испытания на макете микробного топливного элемента показали, что предложенный микробный медиаторный анод на основе глюкозы и микроорганизма Escherichia coli работает удовлетворительно и может быть в дальнейшем использован для практических целей при создании медиаторного микробного топливного элемента. Данные по электрохимическим характеристикам микробного медиаторного анода могут быть использованы при создании микробных биосенсоров.
На защиту выносятся следующие положения:
- возможность использования метиленового синего и галлоцианина в качестве медиаторов, осуществляющих эффективный перенос электронов от микроорганизма Escherichia coli на электрод;
- результаты исследования кинетических закономерностей процесса окисления глюкозы с помощью бактериальных клеток Escherichia coli, протекающего в присутствии экзогенных редокс-медиаторов, во внешнедиффузионной и внутридиффузионной цепи;
- результаты испытания работы микробного медиаторного анода в макете микробного топливного элемента.
Апробация работы. Основные результаты работы были представлены на III Всероссийском семинаре с международным участием «Топливные элементы и энергоустановки на их основе» (Екатеринбург, 2006), на III Всероссийской конференции «Физико-химические процессы в конденсированном состоянии и на межфазных границах» «ФАГРАН-2006» (Воронеж, 2006), на VI Всероссийской конференции молодых ученых «Современные проблемы теоретической и экспериментальной химии» (Саратов, 2007), на XVIII Менделеевском съезде по общей и прикладной химии (Москва, 2007), на III Всероссийской конференции «Актуальные проблемы электрохимической технологии» (Энгельс, 2008), на VII Международной конференции «Фундаментальные проблемы электрохимической энергетики» (Саратов, 2008), а также на IV Всероссийской конференции «Физико-химические процессы в конденсированном состоянии и на межфазных границах» «ФАГРАН-2008» (Воронеж, 2008).
Личный вклад соискателя заключается в анализе литературных источников и написании литературного обзора, постановке и проведении эксперимента, обсуждении результатов исследования, подготовке статей, материалов конференций, рукописей диссертации и автореферата.
Публикации. По материалам диссертации опубликовано 12 печатных работ, в том числе 3 статьи, 2 из которых в журнале, входящем в перечень ведущих рецензируемых журналов, рекомендуемых ВАК, 6 статей в сборниках научных трудов, 3 тезисов докладов.
Объём и структура работы. Диссертация состоит из введения, пяти глав, включая литературный обзор, выводов и списка цитируемой литературы (121 наименование). Работа изложена на 109 страницах машинописного текста, иллюстрирована 49 рисунками и содержит 13 таблиц.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Во введении обосновывается актуальность исследования, сформулирована цель работы, отражены научная новизна и практическая значимость, перечислены положения, выносимые на защиту.
Первая глава является литературным обзором, посвященным проблематике биологических топливных элементов. Рассмотрены особенности работы БТЭ ферментного и микробного типов. Показано, что МТЭ (медиаторные и безмедиаторные) являются перспективными альтернативными источниками электрической энергии. Подробно описаны механизмы электронного переноса в МТЭ, а также представлены сведения о видах микроорганизмов и медиаторов, которые могут быть использованы при их создании. Указаны основные проблемы МТЭ и области их применения.
Вторая глава содержит подробное описание методики эксперимента. Для исследований была выбрана следующая модельная система: моногидрат глюкозы С6Н12О6·H2O (х.ч.) в качестве субстрата, клетки Escherichia coli штамма К-12 в качестве биологического катализатора и окислительно-восстановительные индикаторы - метиленовый синий (ч.д.а.) из класса тиазинов, нейтральный красный (ч.д.а.) из класса азинов и галлоцианин (ч.д.а.) из класса оксазинов в качестве медиаторов. Для проведения электрохимических измерений использовали стеклянную трёхэлектродную герметичную ячейку с разделенными анодным и катодным пространствами. Эксперименты проводили в термостатируемых условиях при температуре 37°С в атмосфере аргона. Вращающиеся дисковые электроды были выбраны в качестве рабочих электродов, которые представляли собой диски из стеклоуглерода и платины площадью 0.071 см2 и 0.39 cм2, соответственно. Вспомогательный электрод был выполнен из платиновой проволоки, скрученной в спираль. Потенциометрические измерения проводились относительно насыщенного хлоридносеребряного электрода сравнения, потенциал которого составлял +0.201 В относительно нормального водородного электрода. Рабочим электролитом служил фосфатный буферный раствор (pH 7.0) с добавкой хлорида натрия в качестве фонового электролита. Снятие поляризационных кривых проводилось с помощью потенциостата IPC-соmpact, соединенного с персональным компьютером. Амперометрические измерения были сделаны с помощью потенциостата П-5848. В этом случае электрический отклик рабочего электрода регистрировался самопишущим потенциометром КСП 4.
Третья глава посвящена установлению кинетических закономерностей процесса окисления глюкозы клетками Escherichia coli, протекающего в присутствии экзогенных редокс-медиаторов во внешнедиффузионной цепи.
Возможность использования метиленового синего, нейтрального красного и галлоцианина в качестве медиаторов, осуществляющих перенос электронов от микроорганизма на электрод, была изучена с помощью метода циклической вольтамперометрии. Циклические вольтамперные кривые были сняты при различных скоростях вращения на стеклографитовом дисковом электроде для различных концентраций исследуемых медиаторов (рис. 1-3).
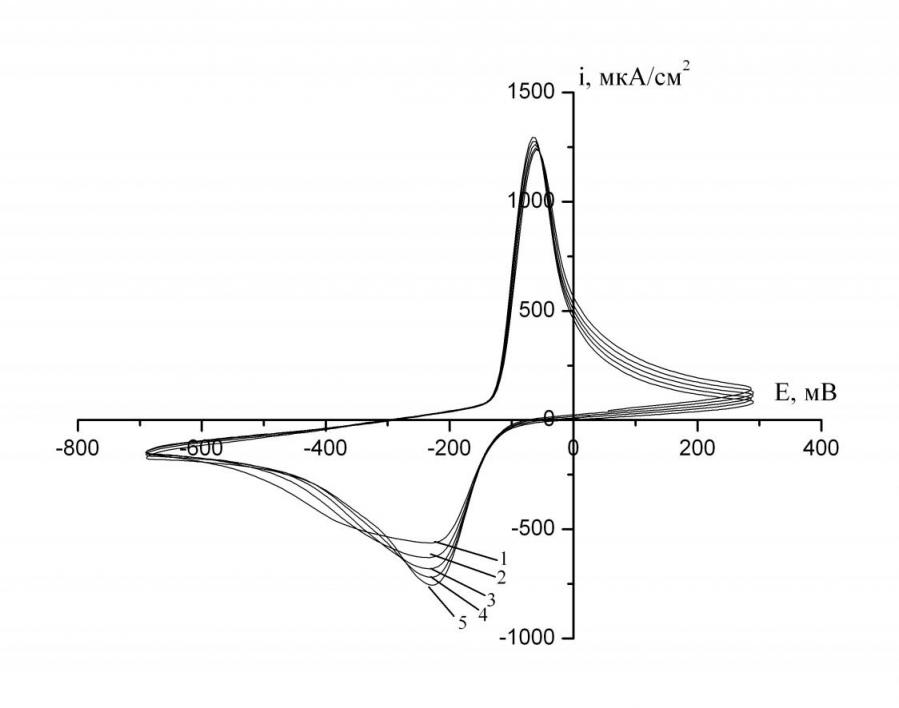
Рис. 1. Циклические вольтамперные кривые стеклографитового вращающегося дискового электрода, снятые в рабочем электролите (pH 7.0), содержащем 1.25·10-3 моль/л метиленового синего и 2·10-3 моль/л глюкозы при различных скоростях вращения (рад/с): 1-178.0; 2-240.6; 3-293.1; 4-345.2; 5-397.6. Скорость развертки потенциала 10 мВ/с.
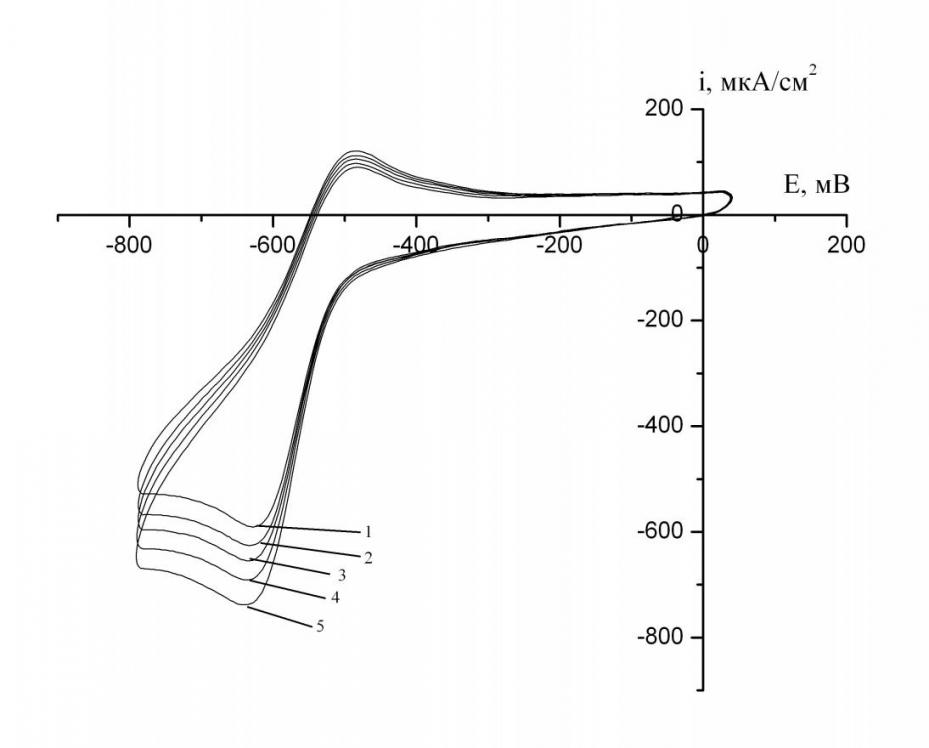
Рис. 2. Циклические вольтамперные кривые стеклографитового вращающегося дискового электрода, снятые в рабочем электролите (pH 7.0), содержащем 1.25·10-3 моль/л нейтрального красного и 2·10-3 моль/л глюкозы при различных скоростях вращения (рад/с): 1-178.0; 2-240.6; 3-293.1; 4-345.2; 5-397.6. Скорость развертки потенциала 10 мВ/с.

Рис. 3. Циклические вольтамперные кривые стеклографитового вращающегося дискового электрода, снятые в рабочем электролите (pH 7.0), содержащем 5·10-4 моль/л галлоцианина и 2·10-3 моль/л глюкозы при различных скоростях вращения (рад/с): 1-178.0; 2-240.6; 3-293.1; 4-345.2; 5-397.6. Скорость развертки потенциала 10 мВ/с.
Установлено, что электрохимические реакции восстановления метиленового синего, нейтрального красного и галлоцианина на электроде протекают в режиме диффузионной кинетики. По уравнению Левича определены коэффициенты диффузии исследуемых медиаторов, которые близки между собой и составляют (1.3±0.1)·10-6 см2/с, (1.1±0.2)·10-6см2/с и (1.5±0.1)·10-6 см2/с для метиленового синего, нейтрального красного и галлоцианина, соответственно. Из циклических вольтамперных кривых определены значения анодных и катодных электрохимических ёмкостей и установлено, что метиленовый синий и галлоцианин на стеклографитовом электроде работают обратимо, а нейтральный красный является необратимо работающим редокс-медиатором.
Для определения эффективности работы метиленового синего, нейтрального красного и галлоцианина в биоэлектрохимической системе глюкоза - клетки Escherichia coli проведены амперометрические измерения процесса окисления глюкозы бактериальными клетками на вращающемся дисковом электроде при различных концентрациях субстрата и исследуемых медиаторов в рабочем электролите (рис. 4-6). Из рис. 4 видно, что при добавлении бактериальных клеток в рабочий электролит, содержащий в качестве медиатора метиленовый синий, начинается резкое возрастание плотности анодного тока, поскольку происходит увеличение концентрации восстановленной формы метиленового синего в объёме раствора, о чем свидетельствует постепенное обесцвечивание электролита. Кривые проходят через максимум, после чего наблюдается постепенное снижение плотности тока во времени с выходом на постоянное значение. Величина плотности тока максимума возрастает при увеличении скорости вращения дискового электрода. Общая скорость процесса зависит от объёмной концентрации медиатора и субстрата в растворе. Показано, что процесс окисления метиленового синего на биоаноде протекает в режиме смешанного диффузионно-кинетического контроля. Установлено, что порядок реакции по медиатору и глюкозе приблизительно равен единице, а среднее значение гетерогенной константы скорости процесса анодного окисления метиленового синего при его различной объемной концентрации составляет 1.74·10-3 см/с.
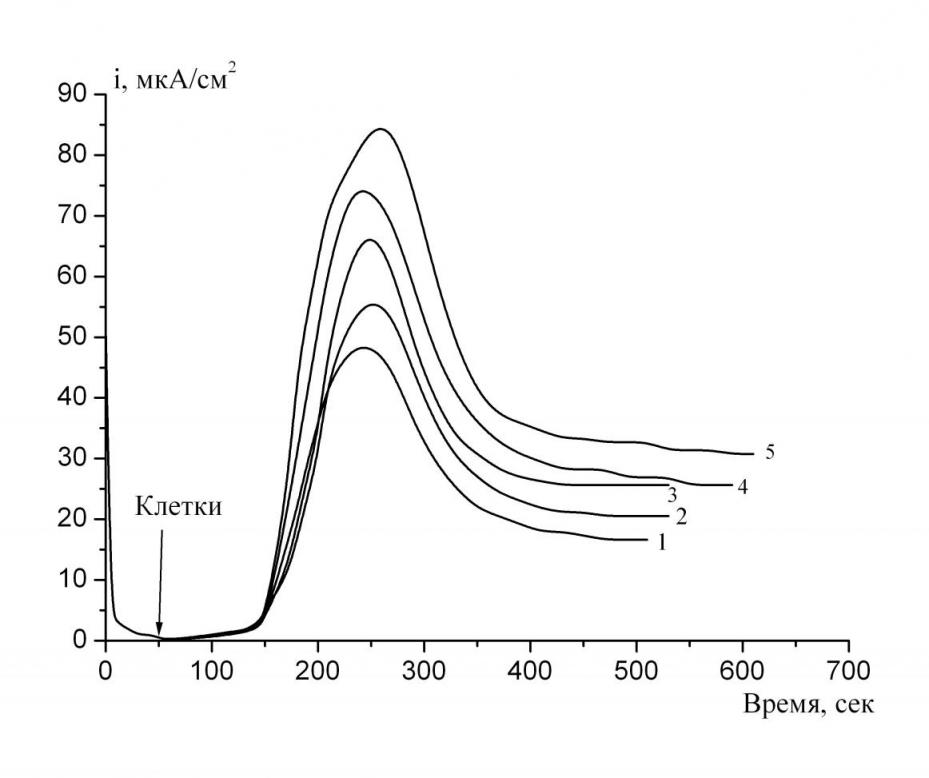
Рис. 4. Потенциостатические кривые анодного окисления метиленового синего на вращающемся дисковом электроде в рабочем электролите, содержащем 7.510-4 моль/л медиатора, 4.6·10-3 моль/л глюкозы и 2 мг вл.веса/мл клеток при различных скоростях вращения (рад/с): 1- 36.6; 2-54.5; 3- 80.6; 4- 104.6; 5- 151.8 при потенциале +0.250 В.
Из рис. 5 видно, что при добавлении бактериальных клеток в рабочий электролит, содержащий в качестве медиатора галлоцианин, наблюдается медленное возрастание плотности анодного тока, поскольку происходит увеличение концентрации восстановленной формы галлоцианина в объёме раствора, о чем свидетельствует постепенное обесцвечивание электролита. Плотность тока достигает предельного значения за время 2500-3000 с, что примерно в 10 раз продолжительнее, чем для метиленового синего. Установлено, что электрохимическая реакция окисления галлоцианина на биоаноде протекает в режиме диффузионной кинетики.
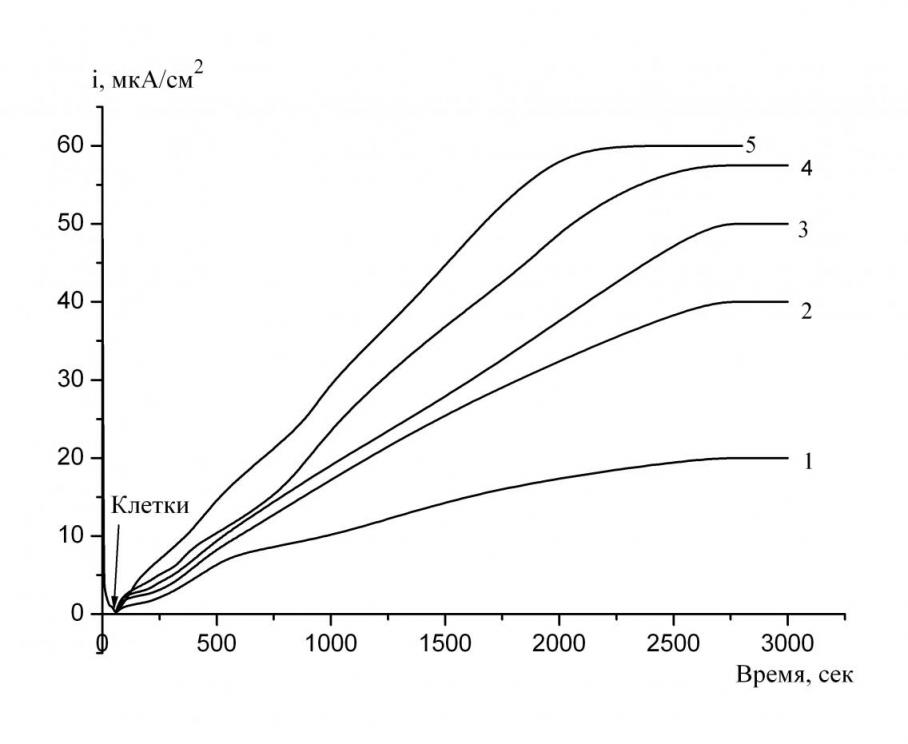
Рис. 5. Потенциостатические кривые анодного окисления галлоцианина на стеклографитовом вращающемся дисковом электроде в рабочем электролите, содержащем 1·10-3 моль/л глюкозы и 2 мг вл.веса/мл клеток при различных концентрациях галлоцианина (моль/л): 1-1.25·10-4; 2-2.5·10-4; 3-5·10-4; 4-7.5·10-4; 5-1·10-3. Скорость вращения 36.6 рад/с, при потенциале +0.250 В.
Из рис. 6 видно, что при введении бактериальных клеток в рабочий электролит, не происходит возрастания плотности анодного тока. Это связано, по всей видимости, с неудовлетворительной работой нейтрального красного как медиатора, осуществляющего перенос электронов от микроорганизма на электрод.
Таким образом, изучение поведения экзогенных медиаторов в биоэлектрохимической системе показало, что метиленовый синий и галлоцианин являются эффективными окислительно-восстановительными системами в условиях работы микробного медиаторного анода на основе бактериальных клеток Escherichia coli, а нейтральный красный не может быть использован в качестве медиатора, осуществляющего перенос электронов от микроорганизма на электрод.
В связи с этим в четвёртой главе проведено изучение каталитической активности микроорганизма Escherichia coli при окислении глюкозы в присутствии экзогенных медиаторов – метиленового синего и галлоцианина. При этом особую важность представляло построение кинетических моделей и описание механизмов протекания ферментативных реакций. Одним из фундаментальных представлений о механизме ферментативной реакции является представление о фермент-субстратном комплексе, образующемся при превращении субстрата в продукт под действием фермента.
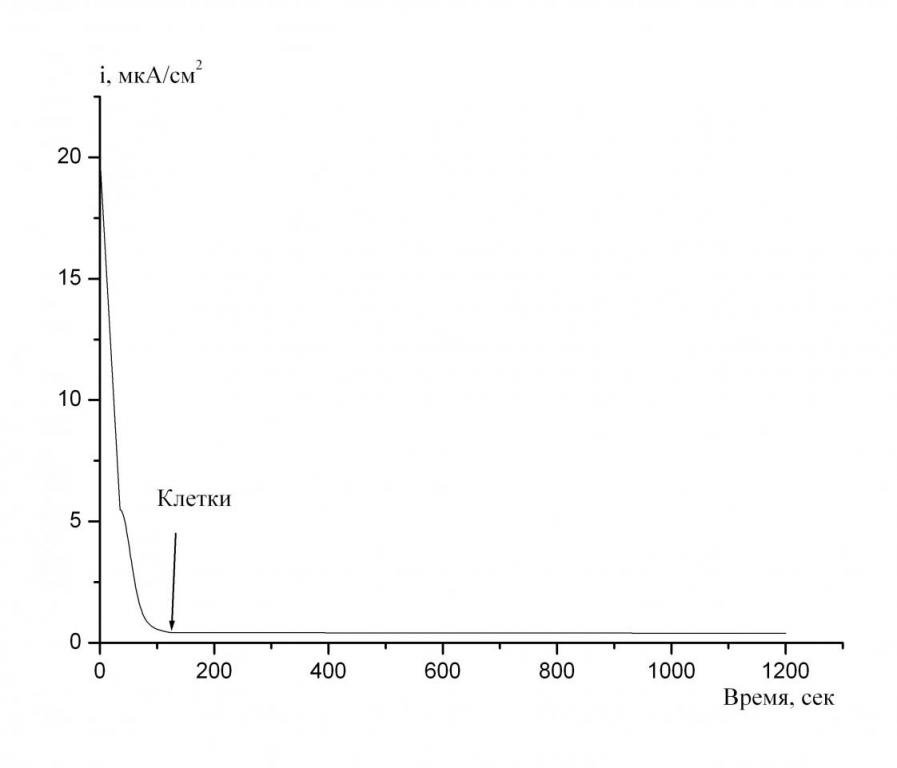
Рис. 6. Потенциостатическая кривая анодного окисления нейтрального красного на стеклографитовом вращающемся дисковом электроде в рабочем электролите, содержащем 5·10-4 моль/л нейтрального красного, 1·10-3 моль/л глюкозы и 2 мг вл.веса/мл клеток. Скорость вращения дискового электрода 36.6 рад/с, потенциал +0.250 В.
Считается, что механизм ферментативной реакции заключается в следующем: субстрат образует комплекс с активным центром фермента, в комплексе происходят фермент-субстратные изменения, образуются продукты реакции, которые уходят из активного центра, освобождая его для взаимодействия с новой молекулой субстрата. Медиатор должен быть специфическим субстратом фермента и, кроме того, электрохимически активным на электроде. С учётом вышеизложенного, схема процесса переноса электронов в системе субстрат-микроорганизм-медиатор-электрод была представлена в виде:
![]() (1),
(1),
![]() (2),
(2),
МВ![]() МОк + ne- (3),
МОк + ne- (3),
где Sклет и Pклет – субстрат и продукт внутри бактериальной клетки, соответственно;
Mок,клет и Mв,клет – окисленная и восстановленная формы медиатора внутри бактериальной клетки, соответственно;
Mок и Mв – окисленная и восстановленная формы медиатора вне бактериальной клетки, соответственно;
Eок,клет и Ев,клет - фермент, локализованный в цитоплазматической мембране бактериальной клетки, в окисленном и восстановленном состояниях, соответственно.
В работе проведён анализ процессов диффузии метиленового синего, галлоцианина и субстрата между клеткой (катализатором) и контактирующим с ней раствором, то есть в условиях, когда скорость реакции определяется внутридиффузионными эффектами, а именно, массопереносом внутри частицы катализатора (реакции (1) и (2)). Для этого были выполнены амперометрические измерения процесса окисления глюкозы бактериальными клетками Escherichia coli на стеклографитовом электроде при различных концентрациях субстрата и медиаторов. Показано, что с увеличением концентрации субстрата и медиаторов величина силы тока (скорость реакции) возрастает (рис. 7).
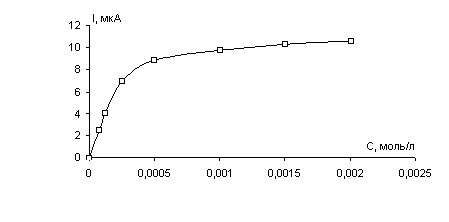 Рис. 7. Зависимость величины тока максимума процесса анодного окисления метиленового синего от концентрации медиатора при избыточной концентрации субстрата, равной 1·10-3 моль/л. В рабочем электролите содержится 2 мг вл.веса/мл клеток.
Рис. 7. Зависимость величины тока максимума процесса анодного окисления метиленового синего от концентрации медиатора при избыточной концентрации субстрата, равной 1·10-3 моль/л. В рабочем электролите содержится 2 мг вл.веса/мл клеток.
Установлено, что в заданных экспериментальных условиях при концентрациях метиленового синего и субстрата, равных 2·10-3 моль/л и 1·10-3 моль/л, соответственно, наблюдается эффект насыщения, то есть скорость процесса перестает зависеть от концентрации. Для галлоцианина эффект насыщения наблюдается при концентрациях медиатора и субстрата, равных 1·10-3 моль/л. Для анализа экспериментальных данных была применена математическая модель, основанная на уравнении Михаэлиса-Ментен (уравнение 4) и учитывающая константы распределения субстрата и медиаторов между внутренней средой клетки и анализируемым раствором:
(4),
![]() (5),
(5),
![]() (6),
(6),
где KS,p и KM,p - константы распределения субстрата и медиатора между внутренней средой клетки и внешним раствором, соответственно;
КS,клет и КМ,клет – константы Михаэлиса для субстрата и окисленной формы электронных медиаторов, соответственно;
Sклет и S – субстрат внутри и вне бактериальной клетки, соответственно;
Mок, клет и Mок – окисленная форма медиатора внутри и вне бактериальной клетки, соответственно;
Imax – максимальная скорость реакции.
Учитывая, что измерения ведутся при избытке субстрата и медиаторов можно использовать следующие упрощенные уравнения:
![]() (при
(при ![]() << 1 – избыток субстрата) (7),
<< 1 – избыток субстрата) (7),
![]() (при
(при ![]() << 1 – избыток медиатора) (8).
<< 1 – избыток медиатора) (8).
Каталитическая активность клеток в присутствии метиленового синего и галлоцианина была охарактеризована тремя параметрами: максимальной скоростью реакции (Imax) и отношениями константы Михаэлиса к константе распределения для субстрата (KS,клет/KS,p) и для исследуемых медиаторов (KМ,клет/KМ,p), которые были определены из экспериментальных данных (рис. 8). Как правило, из данных по стационарной кинетике эти параметры определяют на основе линеаризации уравнения Михаэлиса:
![]() (9),
(9),
![]() (10).
(10).
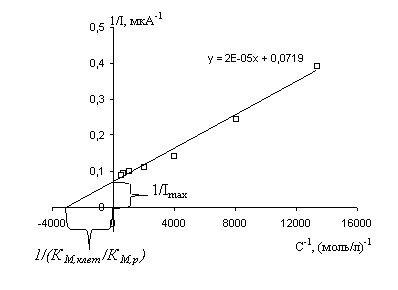
Рис. 8. Зависимость величины обратного тока максимума процесса анодного окисления метиленового синего от обратной величины концентрации медиатора. В рабочем электролите содержится 2 мг вл.веса/мл клеток и 1·10-3 моль/л глюкозы.
Показано, что отношение Imax/(КM,клет/КМ,р), которое характеризует эффективность медиаторов, для метиленового синего составляет 4.4·10-2 с-1, а для галлоцианина 2.8·10-2 с-1 (таблица 1). Следовательно, скорость диффузии метиленового синего между клеткой и контактирующим с ней раствором больше, чем у галлоцианина. Таким образом, метиленовый синий является более эффективным медиатором по сравнению с галлоцианином в реакции окисления глюкозы с помощью микроорганизма Escherichia сoli.
В пятой главе проведена апробация работы микробного медиаторного анода в макете топливного элемента. Анодом служил пористый графитовый электрод, легированный металлической платиной, а катодом - диоксидносвинцовый электрод. В качестве медиатора для создания микробного медиаторного анода был использован метиленовый синий. Рабочее напряжение такого макета микробного топливного элемента составляло от 1.0 В до 1.4 В, что определялось степенью заряженности диоксидносвинцового электрода. Получены разрядные кривые исследуемого макета микробного топливного элемента при различных разрядных токах.
Таблица 1. Значения параметров процесса окисления глюкозы бактериальными клетками Escherichia coli в присутствии медиаторов – метиленового синего и галлоцианина.
| Медиатор | Imax, мкА | КМ,клет/КМ,р ·104, моль/л | Imax/(КM,клет/КМ,р) ·102, с-1 | |
| Метиленовый синий | 13.7 | 3.1 | 4.4 | |
| Галлоцианин | 12.0 | 4.3 | 2.8 | |
В качестве примера на рис. 9 приведена разрядная кривая исследуемого макета микробного топливного элемента при токе разряда 10 мА.
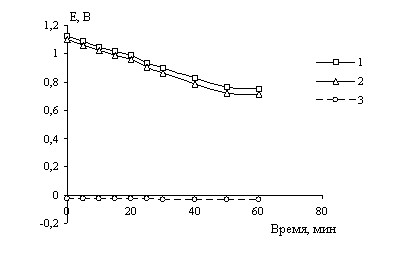 Рис. 9. Разрядные кривые исследуемого макета микробного топливного элемента при токе разряда 10мА: 1 – напряжение макета микробного топливного элемента, 2 - потенциал диоксидносвинцового катода, 3 - потенциал микробного медиаторного анода.
Рис. 9. Разрядные кривые исследуемого макета микробного топливного элемента при токе разряда 10мА: 1 – напряжение макета микробного топливного элемента, 2 - потенциал диоксидносвинцового катода, 3 - потенциал микробного медиаторного анода.
Показано, что работа макета микробного топливного элемента ограничена диоксидносвинцовым электродом, а предложенный микробный медиаторный анод на основе глюкозы и микроорганизма Escherichia coli работает удовлетварительно и может быть в дальнейшем использован для практических целей при создании медиаторного микробного топливного элемента.
Для изучения кинетики процесса анодного окисления исследуемого микробного медиаторного электрода были сняты в прямом и в обратном направлениях поляризационные кривые пористого графитового электрода в условиях работы макета микробного топливного элемента. Анализ полученных кривых показал, что лимитирующей стадией в работе микробного медиаторного анода является процесс окисления медиатора – метиленового синего.
ОСНОВНЫЕ ВЫВОДЫ И РЕЗУЛЬТАТЫ РАБОТЫ
1. Изучено электрохимическое поведение некоторых окислительно-восстановительных систем: метиленового синего, нейтрального красного и галлоцианина на стеклографитовом электроде в фосфатном буферном растворе (pH 7.0). Показано, что метиленовый синий и галлоцианин являются обратимыми окислительно-восстановительными системами и могут быть использованы в качестве медиаторов при реализации микробного анода на основе клеток Escherichia coli. Установлено, что электрохимические реакции восстановления исследуемых медиаторов на рабочем электроде протекают в режиме диффузионной кинетики. Определены их коэффициенты диффузии, которые близки между собой и составляют (1.3±0.1)·10-6 см2/с, (1.1±0.2)·10-6 см2/с и (1.5±0.1)·10-6 см2/с для метиленового синего, нейтрального красного и галлоцианина, соответственно.
2. Изучено поведение исследуемых медиаторов в биоэлектрохимической системе глюкоза – медиатор – клетки Escherichia coli. Показано, что метиленовый синий и галлоцианин являются эффективными окислительно-восстановительными медиаторами при реализации условий работы микробного медиаторного анода, а нейтральный красный работает не эффективно.
3. Изучена кинетика процесса биоэлектрохимического окисления глюкозы бактериальными клетками Escherichia coli с использованием метиленового синего и галлоцианина в качестве медиаторов. Показано, что общая скорость электрохимической реакции зависит от концентрации медиаторов и субстрата в объеме раствора. Из зависимости общей скорости биоэлектрохимического процесса от скорости вращения дискового электрода установлено, что процесс окисления метиленового синего на биоаноде протекает в режиме смешанного диффузионно-кинетического контроля, а процесс окисления галлоцианина – в режиме диффузионной кинетики.
4. Определены кинетические характеристики реакции окисления метиленового синего на биоаноде – порядок реакции и гетерогенная константа скорости. Показано, что порядок реакции по медиатору и глюкозе приблизительно равен единице, а среднее значение гетерогенной константы скорости процесса анодного окисления метиленового синего при его различной объемной концентрации составляет 1.74·10-3 см/с.
5. Изучена каталитическая активность микроорганизма Escherichia coli в условиях работы микробного медиаторного анода. Показано, что с увеличением концентрации медиаторов и субстрата скорость процесса возрастает. В заданных экспериментальных условиях при концентрациях метиленового синего и субстрата, равных 2·10-3 моль/л и 1·10-3 моль/л, соответственно, наблюдается эффект насыщения, то есть скорость процесса перестает зависеть от концентрации. Для галлоцианина эффект насыщения наблюдается при его концентрации, равной 1·10-3 моль/л.
6. На основании уравнения Михаэлиса-Ментен был проведен анализ кинетики процессов диффузии метиленового синего и галлоцианина между катализатором и контактирующим с ним раствором. Отношение максимального тока процесса к эффективной константе обмена Imax/(КM,клет/КМ,р) для метиленового синего составляет 4.4·10-2 с-1, а для галлоцианина составляет 2.8·10-2с-1. Это указывает на то, что скорость обмена метиленового синего между клеткой (катализатором) и контактирующим с ней раствором быстрее, чем у галлоцианина.
7. Проведено испытание микробного медиаторного анода на основе клеток Escherichia coli для процесса окисления глюкозы в разработанном макете топливного элемента, в котором катодом являлся диоксидносвинцовый электрод. Показано, что работа макета топливного элемента в данных условиях ограничена диоксидносвинцовым электродом, а процесс окисления микробного медиаторного анода лимитируется скоростью окисления медиатора – метиленового синего.
Основное содержание работы изложено в следующих публикациях:
1. Казаринов И.А., Власова Е.Л., Кузьмичева Е.В. Биотопливные элементы: современное состояние и перспективы // Топливные элементы и энергоустановки на их основе: Тезисы докладов III Всероссийского семинара с международным участием.- Екатеринбург: Изд-во Урал. ун-та, 2006.- С. 17-20
2. Казаринов И.А., Кузьмичева Е.В. Биотопливные элементы – новое направление в развитии электрохимической энергетики // Физико-химические процессы в конденсированном состоянии и на межфазных границах (ФАГРАН-2006): Материалы III Всероссийской конференции.- Воронеж: Научная книга, 2006.- Т. 1.- С. 113-116
3. Казаринов И.А., Кузьмичева Е.В, Игнатов О.В. Микробный топливный элемент на основе микроорганизма Escherichia coli // Физико-химические процессы в конденсированном состоянии и на межфазных границах (ФАГРАН-2006): Материалы III Всероссийской конференции.- Воронеж: Научная книга, 2006.- Т. 1.- С. 116-117
4. Казаринов И.А., Кузьмичева Е.В., Степанов А.Н. Анализ современного состояния и перспективы развития биотопливных элементов // Тезисы докладов XVIII Менделеевского съезда по общей и прикладной химии.- М.: Граница, 2007.- Т. 3.- С.139
5. Казаринов И.А., Кузьмичева Е.В., Степанов А.Н., Игнатов О.В. Кинетика электрокаталитического окисления глюкозы бактериальными клетками Escherichia coli в присутствии электронного акцептора // Тезисы докладов XVIII Менделеевского съезда по общей и прикладной химии.- М.: Граница, 2007.- Т. 3.- С.179
6. Кузьмичева Е.В., Казаринов И.А., Степанов А.Н., Фокина Т.Э., Пройдакова А.С. Изучение кинетики электрокаталитического окисления глюкозы бактериальными клетками Escherichia coli в присутствии медиатора // Современные проблемы теоретической и экспериментальной химии: Межвуз. сборник науч. трудов VI Всерос. конф. молодых ученых с международ. участием.- Саратов: Изд-во «Научная книга», 2007.- С. 311-312
7. Кузьмичева Е.В., Решетов В.А., Казаринов И.А., Игнатов О.В. Разрядные характеристики микробного топливного элемента на основе микроорганизма Escherichia coli // Электрохимическая энергетика.- 2007.- Т. 7, №1.- С. 33-37
8. Кузьмичева Е.В., Степанов А.Н., Казаринов И.А., Игнатов О.В. Изучение кинетики окисления глюкозы бактериальными клетками Escherichia coli с помощью метода вращающегося дискового электрода // Электрохимическая энергетика.- 2007.- Т. 7, №4.- С. 200-204
9. Кузьмичева Е.В., Казаринов И.А. Изучение кинетики процесса окисления микробного медиаторного анода // Материалы III Всероссийской конференции «Актуальные проблемы электрохимической технологии».- Саратов: Изд-во Саратовского государственного технического университета, 2008.- С. 329-331
10. Кузьмичева Е.В., Казаринов И.А., Игнатов О.В. Кинетика биоэлектрохимического окисления глюкозы с помощью микроорганизмов Escherichia coli // Фундаментальные проблемы электрохимической энергетики: Материалы VII Междунар. конф./ Под ред. проф. И.А. Казаринова.- Саратов: Изд-во Сарат. ун-та, 2008.- С. 138
11. Кузьмичева Е.В., Казаринов И.А., Игнатов О.В. Изучение кинетики процесса окисления микробного медиаторного анода методом вращающегося дискового электрода // Материалы IV Всероссийской конференции «Физико-химические процессы в конденсированных средах и на межфазных границах (ФАГРАН-2008)».- Воронеж: Научная книга, 2008.- С. 161-164
12. Кузьмичева Е.В., Казаринов И.А. Современное состояние, проблемы и перспективы развития микробных топливных элементов // Все материалы. Энциклопедический справочник.- 2008, №7.- С. 28-36
БЛАГОДАРНОСТИ
В заключение автор выражает благодарность своему научному руководителю профессору, д.х.н. И.А. Казаринову за постановку задач и помощь в их решении, сотрудникам Учреждения Российской академии наук Института биохимии и физиологии растений и микроорганизмов РАН (г. Саратов), профессору, д.б.н. О.В. Игнатову за постоянное внимание к работе и методологическую помощь в проведении биохимических экспериментов и м.н.с. Л.Н. Маркиной за помощь, оказанную при выращивании клеток Escherichia coli.
КУЗЬМИЧЕВА ЕЛЕНА ВАЛЕРЬЕВНА
КИНЕТИКА ПРОЦЕССА ОКИСЛЕНИЯ ГЛЮКОЗЫ С ПОМОЩЬЮ МИКРООРГАНИЗМА ESCHERICHIA COLI
В ПРИСУТСТВИИ ЭКЗОГЕННЫХ МЕДИАТОРОВ
Специальность 02.00.05 – электрохимия
Автореферат
диссертации на соискание учёной степени
кандидата химических наук
Подписано в печать 22 мая 2009 г.
Формат 6084 1/16. Объем 1,25 п.л. Тираж 100 экз. Заказ №
Отпечатано в типографии Саратовского государственного университета.
410012, г. Саратов, ул. Астраханская, 83.

