Молекулярные комплексы гетероароматических n-оксидов и ацетиленовых аминов с v-акцепторами, как модель исследования нуклеофильности и основности соединений с пространственно доступными реакционными це
На правах рукописи
АНДРЕЕВ ВЛАДИМИР ПЕТРОВИЧ
МОЛЕКУЛЯРНЫЕ КОМПЛЕКСЫ ГЕТЕРОАРОМАТИЧЕСКИХ N-ОКСИДОВ И АЦЕТИЛЕНОВЫХ АМИНОВ С
v-АКЦЕПТОРАМИ, КАК МОДЕЛЬ ИССЛЕДОВАНИЯ НУКЛЕОФИЛЬНОСТИ И ОСНОВНОСТИ СОЕДИНЕНИЙ С ПРОСТРАНСТВЕННО ДОСТУПНЫМИ РЕАКЦИОННЫМИ ЦЕНТРАМИ
02.00.03 – органическая химия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора химических наук
Москва
2007
Работа выполнена на кафедре молекулярной биологии, биологической и органической химии Петрозаводского государственного университета.
Научный консультант:
доктор химических наук, профессор Вапиров Владимир Васильевич
Официальные оппоненты:
доктор химических наук, профессор Борисова Елена Яковлевна
доктор химических наук, профессор Травень Валерий Федорович
доктор химических наук, профессор Тришин Юрий Георгиевич
Ведущая организация: Санкт-Петербургский государственный технологический институт (технический университет)
Защита состоится …….. 2007 года в часов на заседании диссертационного совета Д 212.120.01 в Московской государственной академии тонкой химической технологии им. М.В. Ломоносова по адресу: 117571, г. Москва, просп. Вернадского, 86.
С диссертацией можно ознакомиться в библиотеке МИТХТ им. М.В. Ломоносова.
С авторефератом диссертации можно ознакомиться на сайте ВАК РФ http://vak.ed.gov.ru
Автореферат разослан « » ___________ 2007 г.
Ученый секретарь
Диссертационного совета Д 212.120.01
кандидат химических наук,
старший научный сотрудник Лютик Алла Игоревна
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы. Исследованию молекулярных комплексов различных классов лигандов с участием v-акцепторов посвящено множество обзоров. Актуальность данного научного направления обусловлена теоретической ценностью исследования процессов комплексообразования и широчайшим применением таких комплексов в различных отраслях промышленности, физической электроники, медицине и других областях. Особую роль молекулярные комплексы играют в биологических системах, среди которых достаточно упомянуть сложные молекулы гемоглобина, хлорофилла, цианкобаламина.
В этой связи очень актуальным представляется направление исследований молекулярных комплексов с гетероароматическими N-оксидами. С одной стороны, на их основе синтезировано большое количество биологически активных веществ, что обуславливает их практическое применение. Немаловажным является и тот факт, что in vivo в процессе метаболизма аминов (в частности азотсодержащих гетероциклов) образуются их N-оксидированные производные. С другой стороны они обладают целым рядом уникальных свойств, что принципиально отличает этот класс соединений от неокисленных аналогов. Доступность реакционного центра N-оксидов при его низкой основности и в настоящее время остается почти единственным обьяснением их высокой нуклеофильной реакционной способности, принятой называть супернуклеофильностью. Исследование данного феномена наиболее удобно на модельных реакциях комплексообразования с участием различных типов v-акцепторов, включая соединения p- и d- элементов, а также сложные органические структуры подобные металлопорфиринам.
Не менее перспективными лигандами являются и ацетиленовые амины и их ЧАС, донорно-акцепторные комплексы которых в литературе практически не описаны. В этой связи закономерным является не только восполнение пробела научных знаний в области комплексообразования с участием этих лигандов, но и сравнительный анализ с другими классами соединений с целью получения информации о перспективах их использования.
Исходя из актуальности выбранного научного направления диссертационная работа была направлена на систематическое исследование процессов комплексообразования с участием гетероароматических N-оксидов, ацетиленовых аминов и ЧАС с различными типами v-акцепторов, что позволило разработать и усовершенствовать целый ряд синтетических методов и оригинальных теоретических представлений.
Диссертация выполнена в соответствии с планом НИР ПетрГУ по проблеме “Молекулярные комплексы гетероароматических N-оксидов в органической и биологической химии”, а также в рамках Грантов Международного научного фонда NFX 000 и NFX 300.
Целью настоящей работы является комплексное систематическое исследование процессов координации гетероароматических N-оксидов, ацетиленовых аминов и ЧАС с v-акцепторами.
В связи с этим в задачу исследования входили:
- разработка новых и усовершенствование известных методов синтеза вторичных и третичных ацетиленовых аминов, ацетиленовых четвертичных аммониевых солей (ЧАС), а также гетероароматических N–оксидов.
- синтез и исследование состава, структуры и устойчивости молекулярных комплексов гетероароматических N-оксидов c различными типами v-акцепторов: кислотами Бренстеда-Лоури (H+) и Льюиса (BF3, AlCl3, ZnCl2, CuCl2 и металлопорфирины).
- исследование количественных закономерностей процессов комплексообразования с участием v-акцепторов.
- теоретическое обоснование основности, нуклеофильности и электрофильности с точки зрения свойств изучаемых лигандов и их поведения в процессах комплексообразования
- поиск новых областей практического применения (экстракционные и антикоррозионные свойства, биологическая активность) исследуемых соединений.
Научная новизна. Впервые синтезированы молекулярные комплексы гетероароматических N-оксидов с различными типами v-акцепторов и с использованием физико-химических (ИК, электронная, ЯМР 1Н и ЯМР 13С спектроскопия, рентгеноструктурный анализ) методов доказана их структура.
На основании впервые полученных экспериментальных данных дано теоретическое обоснование супернуклеофильности N–оксидов пиридинов в реакциях переноса ацильных групп. В отличие от пиридинов переходное состояние реакции с их участием стабилизируется образованием системы с прямым резонансным сопряжением между нуклеофильным и электрофильным компонентами. Предложена новая шкала основности и нуклеофильности, основанная на параметрах, характеризующих образование аксиальных комплексов Zn-ТФП с лигандами (основаниями/нуклеофилами).
Впервые показана возможность активации реакций нуклеофильного замещения в ряду гетероароматических N-оксидов v-акцепторами различного типа (кислоты Бренстеда-Лоури и Льюиса); установлено, что этот подход может быть использован и в неокисленных гетероциклах. Разработаны новые условия и усовершенствованы методы синтеза галогенопроизводных хинолинов, хинолонов, гетероароматических N-оксидов и стирильных производных N-оксидов хинолинового ряда.
Впервые исследованы кинетические закономерности кватернизации -, -, -ацетиленовых аминов галогенидными соединениями и прототропная изомеризация под действием 3-аминопропиламида натрия. Разработаны новые методы синтеза ацетиленовых аминов и ЧАС. Получены 2 авторских свидетельства на синтез вторичных -ацетиленовых аминов и использование ацетиленовых аминов в качестве ингибиторов кислотной коррозии стали.
Впервые исследована экстракция соединений d-элементов и лантаноидов гетероароматическим N-оксидами, моно- и диацетиленовыми ЧАС и предложены новые перспективные экстрагенты.
Обнаружены новые пути регуляции Na,K-АТФазной активности нервных клеток нейромедиаторами и гетероароматическими N-оксидами. Впервые показано, что гетероциклические N-оксиды обладают апоптогенной и дифференцирующей активностью на клетки опухолевой линии К 562.
Практическая значимость работы. Разработаны новые условия и усовершенствованы методы синтеза галогенопроизводных хинолинов, хинолонов, гетероароматических N-оксидов и стирильных производных N-оксидов хинолинового ряда.
Предложенный принцип активации нуклеофильного замещения кислотами Бренстеда-Лоури и Льюиса может быть распространен на другие типы реакций, в которых за счет образования донорно-акцепторных комплексов n,v-типа возможно изменение заряда в реакционных центрах реагентов.
Разработаны новые методы синтеза ацетиленовых аминов и ЧАС. Практическая ценность данной части работы подтверждена получением 2 авторских свидетельств - на синтез вторичных -ацетиленовых аминов и использование ацетиленовых аминов в качестве ингибиторов кислотной коррозии стали.
Установленные в диссертационной работе закономерности комплексообразования Zn-ТФП и гемина позволяют на основании данных электронной спектроскопии () при наличии корреляционных уравнений достаточно просто рассчитывать константы устойчивости комплексов металлопорфиринов (МП) с v-акцепторами, -константы Гаммета, а при отсутствии стерических факторов и pKa лигандов в растворителях, значительно различающихся по полярности. Константы устойчивости аксиальных донорно-акцепторных комплексов Zn-ТФП с лигандами в хлороформе предложены в качестве параметров, характеризующих нуклеофильность (в реакциях SN) и основность реагентов.
Предложены новые перспективные экстрагенты (стирильные производные N-оксидов пиридинов и ацетиленовые ЧАС) d- и f-элементов периодической таблицы Д.И. Менделеева.
N-Оксиды пиридинового, хинолинового и акридинового рядов, являющиеся высокоспецифичными ингибиторами/активаторами мембранной Na,K-АТФазы, могут быть рекомендованы для разработки на их основе фармакологически активных препаратов.
Данные полученные относительно биологической активности (применительно к дифференцировке и апоптозу опухолевых клеток К 562) N-оксидов пиридинового и хинолинового ряда могут быть полезны для специалистов в области химиотерапии опухолей человека и использованы для преодоления фенотипа множественной лекарственной устойчивости.
Апробация работы. Результаты работы доложены и обсуждены на российских и международных конференциях, из которых наиболее значимыми являются: 11th International Conference of Organic Synthesis (Amsterdam, The Netherlands, 1996), Third Workshop “Russian Technologies for Industrial Applications “ (Russia, Saint-Petersburg, 1999), European Conference on calorimetry and thermal analysis for environment (Zakopane, Poland, 2005), International Conference on Organic Chemistry “Organic chemistry since Butlerov and Belstein until present (Russia, Saint-Petersburg, 2006), IV Всероссийская конференция по химии ацетилена и его производных (Баку, 1979), Всесоюзная конференция по развитию органического синтеза (Ленинград, 1980), вторая Международная конференция “Актуальные тенденции в органическом синтезе на пороге новой эры” (Санкт-Петербург, 1999), первая Всероссийская конференция по химии гетероциклов памяти А.Н. Коста (Суздаль, 2000), Российский семинар по химии порфиринов и их аналогов (Иваново, 2004).
Публикации. По теме диссертации опубликованы: 35 статей, в том числе 2 обзорных, 36 тезисов докладов на конференциях, получено два авторских свидетельства.
На защиту выносятся:
- Методы синтеза ацетиленовых аминов и ЧАС, гетероароматических N-оксидов и донорно-акцепторных комплексов этих соединений с v-акцепторами
- Особенности строения синтезированных соединений и их комплексов с v-акцепторами
- Общие закономерности и особенности химического поведения, а также специфические свойства молекулярных комплексов гетероароматических N-оксидов, ацетиленовых аминов и ЧАС и их донорно-акцепторных компонентов
Структура и объем работы. Диссертация изложена на 427 страницах, содержит 100 таблиц и 76 рисунков. Она включает введение, обзор литературных данных, обсуждение результатов, экспериментальную часть, выводы, список цитируемой литературы (645 наименований).
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
1. Гетероароматические N-оксиды
1.1. Объекты исследования
Выбор в качестве объектов исследований N-оксидов обусловлен тем, что производные пиридина, хинолина и акридина широко используются в качестве лекарственных соединений, а в организме в результате их метаболизма могут образовываться продукты окисления по атому азота. Кроме того, N-оксиды ряда пиридина в виде молекулярных комплексов с некоторыми v-акцепторами нашли широкое применение как экологически безопасные регуляторы роста растений. Таким образом, на примерах гетероароматических N-оксидов можно было бы моделировать процессы, близкие к природным.
С другой стороны, возможность широкой вариации заместителей в гетероароматическом ядре N-оксидов позволило бы рассмотреть влияние электронных эффектов на их реакционную способность.
N-Оксиды пиридинов, хинолинов и акридинов (I-V) получали по известным в литературе методам. Для расширения спектра лигандов при исследовании процессов комплексообразования нами были также использованы производные пиридинов (VI а–ж) и получены некоторые стирильные производные N-оксидов пиридинов и хинолинов кипячением N-оксидов 2- и 4–метилпиридинов и хинолинов с ароматическими альдегидами в присутствии метилата калия в абсолютном метаноле в атмосфере азота. Нами было показано, что реакцию можно проводить в гораздо более мягких условиях: в этанольном растворе KOH на воздухе при 20-60°С. Например, конденсация N-оксидов 2- и 4-метилхинолинов осуществляется с выходом 70-90%. Следует отметить, что в этой системе с пара-нитробензальдегидом реакция заканчивается при комнатной температуре за 15 мин, тогда как при использовании метилата калия продукт конденсации не удается получить. Строение полученных впервые соединений подтверждено элементным анализом и спектральными методами.

Х = а) H, б) CH3, в) OCH3, г) NO2, д) Cl, е) Br, ж) N3, з) NHNH2, и) CH=CHC6H5, к) CH=CHC6H4(4-OCH3), л) CH=CHC6H4(4-N(CH3)2, м) CH=CHC6H4(4-NO2), н) CH=CHC6H4(2,4-OCH3), о) OC6H5
Y = а) H, б) 4-CH3, в) 4-CN, г) 3-COOC2H5, д) 4-CONHNH2, е) 3-NH2, ж) 3-CONH2, з) CH=CHC6H4(4-OCH3)
Необходимые для исследования реакции нуклеофильного замещения 2,4-дибромхинолин и 4-нитрохинолин получали взаимодействием N-оксида 4-нитрохинолина с PBr3 в CHCl3 и этилацетате.
Индивидуальность синтезированных веществ проверяли по данным элементного анализа, температурам плавления, ИК спектрам и с помощью методов ТСХ и ВЭЖХ. Методом порошкового РСА были определены структуры дигидрата N-оксида хинолина и N-оксида 4-(4-диметиламиностирил)пиридина.
1.2. Молекулярные комплексы N-оксидов с v-акцепторами
1.2.1. Комплексы N-оксидов пиридинов, хинолинов и акридина с HCl и BF3
В литературе отсутствуют данные о выделении в индивидуальном состоянии гидрогалогенидов нитропроизводных N-оксидов пиридинового, хинолинового и акридинового рядов.
Предпринятые нами попытки получить продукты взаимодействия N-оксида 4-нитрохинолина (4-NQO) с соляной или бромистоводородной кислотами или с газообразными HCl и HBr показали, что нитрогруппа чрезвычайно легко замещается на атом хлора или брома. Даже в осадке, образующемся при пропускании в течение 15 секунд газообразного HCl через N-оксида 4-нитрохинолина в смеси гексан - хлороформ (1:1), идет реакция замещения нитрогруппы на атом хлора с образованием N-оксида 4-хлорхинолина (за 1 сутки на 20%). При пропускании же хлороводорода через хлороформные растворы N-оксидов пиридинов (VIг,о-р) выделяются стабильные гидрохлориды состава 1:1.
В ИК спектрах гидрохлоридов (в KBr) появляются широкие полосы (OH) в области 2330-1800 см-1. Полоса (NO) (1264-1288 см-1) сохраняется неизменной (в спектрах (Iп·HCl) и (Iр ·HCl) уменьшает интенсивность), а в случае (Iг·HCl) и (Iр·HCl) появляются новые полосы при 1196 см-1 для первого и 1228 см-1 и 1186 см-1 для второго соединения, что указывает на протонирование N-оксидной группы.
Ранее отмечалось, что с BF3 N-оксид (Iг) не образует комплексов, вероятно, из-за его низкой основности. Однако нам удалось получить аддукты с этим v-акцептором состава 1:1 взаимодействием BF3Et2O с N-оксидами (Iг,п-с) в CHCl3.
В электронных спектрах этих комплексов, как и в случае гидрохлоридов, длинноволновая полоса поглощения претерпевает гипсохромный сдвиг на 50-65 нм и уменьшает свою интенсивность.
В ИК спектрах комплексов с BF3 (в KBr) исходная полоса (NO) (1264-1288 см-1) сохраняется, но уменьшает свою интенсивность. При этом появляются новые полосы (NO) 1150-1120 см-1. В случае комплекса Iп·BF3 полоса (NO) 1264 см-1 смещается до 1256 см-1.
Аналогичные изменения в ИК и электронных спектрах наблюдаются и при взаимодействии других комплексов нитро-, хлор-, метил-, метоксипроизводных и незамещенных пиридинов, хинолинов и акридинов с галогенводородами и BF3, свидетельствуя о том, что комплексообразование во всех случаях осуществляется по атому кислорода N-оксидной группы.
Ввиду того, что согласно литературным данным первое протонирование N-оксида (Iл) идет по аминогруппе мы исследовали взаимодействие стирильных производных N-оксидов пиридинов и хинолинов с HCl и BF3 в различных растворителях. Методами ПМР, ИК и электронной спектроскопии было показано, что образование донорно-акцепторной связи в хлороформе, ДМСО и 96% этаноле идет с участием группы NO (двойная связь стирильного фрагмента устойчива к электрофильному присоединению HCl), и только в случае соединений (Iл), (IIл) и (IIIл) вторая молекула акцептора присоединяется к диметиламиногруппе. Все аддукты были выделены в индивидуальном состоянии и их структура подтверждена элементным анализом и спектроскопическими методами.
Нами показано, что электронная спектроскопия является очень удобным и информативным методом исследования процессов внутримолекулярного переноса заряда в этих соединениях. В ЭСП N-оксидов положение длинноволновой полосы поглощения симбатно электронным эффектам заместителей (NO2 < H < OCH3 < N(CH3)2), а при комплексообразовании претерпевает значительный гипсохромный сдвиг в случае нитропроизводных, слабое коротко- (N-оксиды (Iа), (IIа)) или длинноволновое (N-оксид (IIIа) смещение в незамещенных соединениях и увеличивающийся в соответствии со степенью прямого резонансного сопряжения (4-OCH3 < 2,4-OCH3 < < 4-N(CH3)2)) батохромный сдвиг в других соединениях.
Нами обнаружено, что замена в четвертом положении N-оксида-4-метилпиридина (4-MePyO) метильной ( -0.17) на метоксигруппу ( -0.268) приводит к очень сильным изменениям в ПМР спектрах аддуктов с трифторидом бора: в 4-MePyO·BF3 все протоны пиридинового кольца имеют различные химические сдвиги (смещены в слабое поле по сравнению с N-оксидами), а в 4-MeOPyO·BF3 пары протонов H2 и H6, H3 и H5 равноценны. Этот эффект может быть объяснен разной геометрией комплексов обусловленной различной гибридизацией атома кислорода, так как при наличии в четвертом положении пиридинового кольца электроноакцепторных заместителей (например, в N-оксиде (Iг)) должны увеличиваться вклады резонансных структур, где атом кислорода находится в состоянии sp2 гибридизации, а в случае электронодонорных (например, в N-оксиде (Iв)) - с отрицательным зарядом на атоме кислорода (sp3 – гибридизация, рис. 1). В соответствии с этим в первом случае комплексообразование должно приводить к аддукту, в ПМР спектре которого все протоны в пиридиновом кольце будут иметь различные значения химических сдвигов (структура А). При образовании же одинарной связи (структура Б) между атомом азота пиридинового кольца и атомом кислорода в состоянии sp3-гибридизации быстрые (во временных рамках ПМР спектроскопии) конформационные изменения молекулы приведут к усреднению химических сдвигов протонов H2,6 и H3,5. Однако нельзя исключать и возможность существования некоторых комплексов гетероароматических N-оксидов (например, при наличии заместителей в положениях 2,6) в виде одной устойчивой конформации, в которой sp3-гибридная орбиталь кислорода, образующая связь с атомом бора, может находиться в плоскости, перпендикулярной пиридиновому кольцу и проходящей через атомы N и С4.
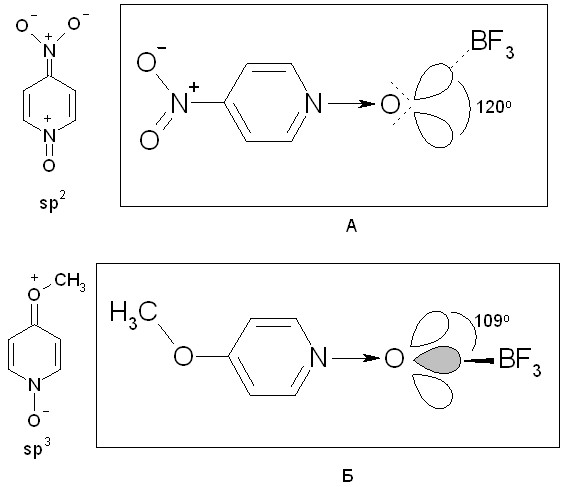
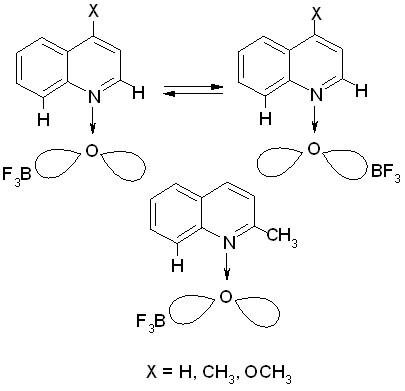
Рис.1. Вероятная геометрия взаимодействия атома кислорода группы NO с молекулой трифторида бора в N-оксидах пиридинов и хинолинов.
Нами обнаружено, что в случае менее основных, чем 4-MeOPyO (pKa 2.05) N-оксидов 4-хлорпиридина (pKa 0.36), пиридина (pKa 0.79), 2-метилпиридина (pKa 0.97), 4-метилпиридина ( pKa 1.29), а также 4-стирилпиридина (pKa 1.10) и 4-(4-метоксистирил)пиридина (pKa 1.25) ПМР спектры молекулярных комплексов c BF3 соответствуют реализации структуры А (все протоны пиридинового кольца имеют различные химические сдвиги). Для аддукта же N-оксида 4-(4-диметиламиностирил)пиридина ( pKa 1.43), содержащего N(CH3)2 группу, которая находится в прямом резонансном сопряжении с атомом кислорода N- оксидной группы и при участии его в комплексообразовании должна значительно увеличивать свои электронодонорные свойства, характерна структура Б.
Тем не менее, однозначный вывод о возможности перегибридизации атома кислорода (sp2 sp3) при взаимодействии гетероароматических N-оксидов с трифторидом бора можно сделать только на основании данных рентгеноструктурного анализа. С этой целью нами была исследована методом РСА пространственная структура комплексов 4-MePyO·BF3 и 4-MeOPyO·BF3, полагая, что в соответствии с данными протонного магнитного резонанса в первом случае атом бора будет находиться в плоскости пиридинового кольца, а во втором нет. Однако оказалось, что в кристаллах аддуктов N-оксидов 4-метил- и 4-метоксипиридина с BF3 углы N – O – B равны 113.93 o и 113.27 o, а торсионные углы между плоскостью проходящей через атомы N – O – B и
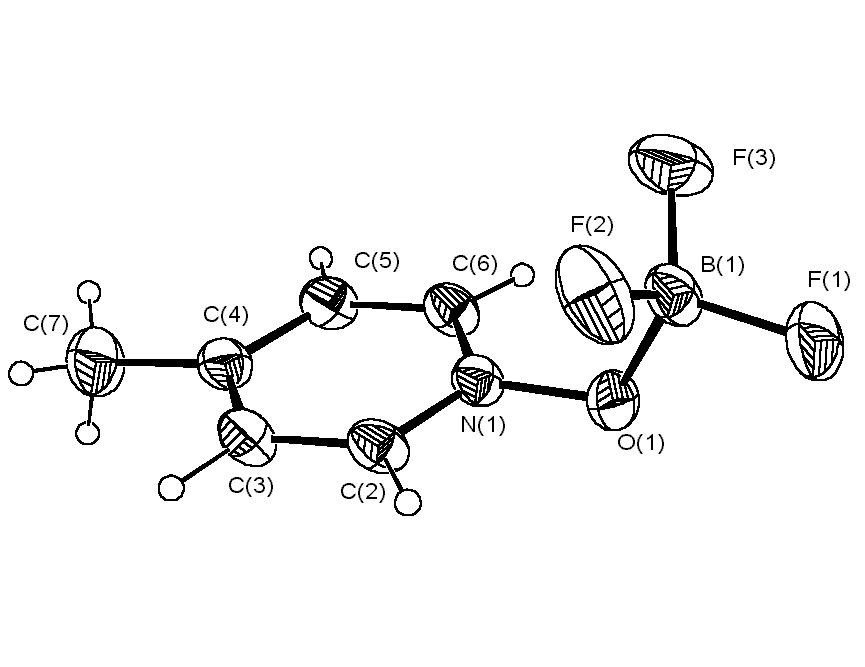
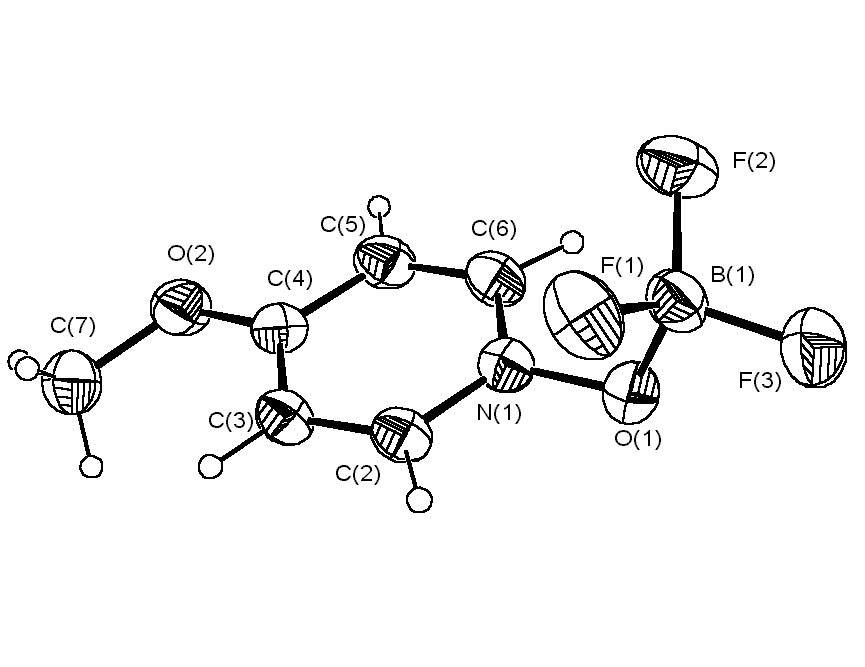
Рис. 2. Структура комплексов N-оксидов 4-метилпиридина и 4-метоксипиридина с BF3
плоскостью пиридинового кольца составляют 87.81o и 87.63o, соответственно (рис. 2). Таким образом, атом кислорода в этих соединениях находится в состоянии sp3-гибридизации, что согласуется с данными ПМР спектроскопии для комплекса 4-MeOPyO·BF3 (равноценность протонов H2,6 и H3,5), но не с наличием четырех типов протонов в пиридиновом кольце 4-MePyO·BF3.
Это кажущееся противоречие, по-видимому, объясняется тем, что в растворе и в твердом состоянии устойчивость и пространственная структура аддукта N-оксида 4-метилпиридина с BF3 определяется совершенно разными факторами. Если в жидкой фазе (sp2-гибридизация атома кислорода) его конформация определяется свойствами растворителя, то в твердой фазе ( sp3-гибридизация) - взаимодействием с атомами соседних молекул. Тот факт, что даже в процессе кристаллизации 4-MePyO·BF3 также возможна перегибридизация атома кислорода свидетельствует о низком энергетическом барьере данного конформационного перехода.
Таким образом нами обнаружено, что при образовании кристаллов молекулярных комплексов гетероароматических N-оксидов пиридинов с BF3 происходит sp2 – sp3 перегибридизация атома кислорода. Однако в растворах вероятность этого процесса зависит от основности лиганда, пространственной доступности реакционного центра и природы растворителя. В отсутствии стерических факторов образованию связи O-B за счет sp2-гибридной орбитали атома кислорода должны благоприятствовать растворители малоспособные к ее поляризации и заместители с –М эффектом находящиеся в прямом резонансном сопряжении с группой NO.
Согласно данным ПМР спектроскопии 2-MeQO·BF3, QO· BF3, 4-MeQO· BF3 и 4-MeOQO· BF3 существуют в ДМСО в виде двух компонентов в пропорциях 95:5, 7:1, 3:2 и 1:1, соответственно, с преобладанием аддуктов с сигналами протонов в более сильном поле. A priori для всех этих комплексов можно предположить по три пространственные формы, в одной из которых атом кислорода находится в sp3- (структура типа Б), а в двух других в sp2-гибридизации (структуры типа А) с BF3 пространственно сближенным в плоскости со вторым или восьмым атомом углерода хинолинового кольца (рис.1). К сожалению, данные ПМР спектроскопии не позволяют сделать однозначный выбор в пользу двух структур. Однако принимая во внимание тот факт, что в исследованных нами методом РСА комплексах с BF3 (а также с ZnCl2 и CuCl2, рис.3,4) акцепторы находятся в плоскостях перпендикулярных к плоскостям гетероциклов, по-видимому, в растворе 2-MeQO·BF3 в ДМСО присутствуют стерически более выгодная структура Б с sp3-гибридизованным атомом кислорода (95%) и форма с максимальным расстоянием между BF3 и CH3 (рис.1).
Относительная устойчивость пространственных изомеров комплексов QO·BF3, 4-MeQO·BF3, и 4-MeOQO·BF3 c одинаковым стерическим окружением N-оксидной группы должна определяться прежде всего электронными факторами заместителей, и поэтому с увеличением электронодонорных свойств в ряду H < CH3 < OCH3 должно увеличиваться содержание структуры Б. При этом, если даже в случае 4-MeOQO·BF3 (самое сильное из трех основание) согласно данным ПМР спектроскопии стереоизомеры с sp3- и sp2-гибридизованным атомом кислорода находятся в соотношении 1:1, то QO и 4-MeQO тем более преимущественно должны существовать в виде наименее напряженных структур типа А (рис.1, справа вверху).
Интересно, что в ПМР спектре комплекса N-оксида (IIIл·BF3), в котором присутствует электронодонорная группа N(CH3)2 (как и в случае (Iл·BF3)) и имеется заместитель во втором положении (как в случае 2-MeQO·BF3) проявляется только один компонент. По-видимому, и в данном случае атом кислорода группы NO находится в состоянии sp3 –гибридизации.
Таким образом, методом ПМР нами впервые показано, что молекулярные комплексы гетероароматических N-оксидов с трифторидом бора в растворах являются либо индивидуальными изомерами (N-оксиды пиридинов, 2-DQO), или существуют в виде двух стереоизомеров (QO, 2-MeQO, 4-MeQO, и 4-MeOQO), пространственная структура и соотношение которых зависят от совокупности электронных и стерических факторов заместителей в гетероцикле.
1.2.2. Комплексы гетероароматических N-оксидов с ZnCl2 и CuCl2
В предыдущем разделе автореферата обсуждались молекулярные комплексы N-оксидов пиридинов, хинолинов и акридина с жёсткими (BF3 и H+ ) кислотами Льюиса (согласно принципу ЖМКО). Нам представлялось обоснованным продолжить изучение особенностей комплексообразования также с несколько более мягкими кислотами - v-акцепторами Zn2+ и Cu2+ и, в частности, выяснить состояние гибридизации атома кислорода в аддуктах, т.к. соли этих металлов нередко используются в органическом синтезе как катализаторы, а комплексы солей цинка с производными N-оксида пиридина являются эффективными и экологически безопасными активаторами роста растений.
Нами в качестве объектов исследования были выбраны, с одной стороны, хлориды цинка и меди, образующие с N-оксидами пиридина соединения более простого состава, чем соли с анионами меньшей основности, и, с другой, N-оксиды без электроноакцепторных заместителей, снижающих основность лиганда, но с различным стерическим окружением около группы NO, обычно принимающей участие в комплексообразовании.
При смешивании насыщенных растворов N-оксидов (Iк,л), (IIа), (IIIб,и,л) с хлоридами меди и цинка в этаноле образуются аддукты с ZnCl2 2:1 (донор:акцептор), а с CuCl2 2:1 и 1:1. Исключение составляют N-оксиды (IIIи) и (IIIл), содержащие стирильный заместитель во втором положении и образующие комплексы состава только 2:1. Мы зарегистрировали также существование и других типов аддуктов. Так, после смешения растворов (IIa) и CuCl2 выпадает осадок желтого цвета, который быстро в зависимости от соотношения исходных веществ превращается в красный или чёрный комплексы состава 2:1 или 1:1. Кроме того, при медленном добавлении к раствору CuCl22H2O в этаноле раствора N-оксида (IIIб) нам удалось получить аддукт состава 2:3.
В ИК спектрах комплексов с ZnCl2 и CuCl2 полосы (NO) имеют меньшую интенсивность или исчезают совсем, и появляются новые полосы в области 1210-1150 см-1 за счет образования донорно-акцепторной связи, что находится в согласии с литературными данными для аддуктов N-оксида пиридина. Кроме того, в области 350-300 см-1 возникают полосы поглощения, обусловленные наличием связей металл-хлор и кислород-металл.
Методом РСА нами была установлена структура комплексов N-оксида (IIIб) ZnCl2 и CuCl2 и (IIа) с CuCl2. Комплекс N-оксида 2-метилхинолина с CuCl2 состава 2:1 (рис. 3) может быть представлен как транс-изомер, в котором планарные ароматические циклы в первом приближении почти параллельны друг другу (торсионный угол 9.54o), а координационные центры вокруг катиона меди не лежат в одной плоскости, причем торсионный угол между плоскостью ароматического ядра и плоскостью проходящей через атомы N-O-Cu составляет 74.19°. Это полностью исключает возможность сопряжения атома кислорода с ароматическим ядром и перекрывания негибридной орбитали кислорода с комплексообразователем. В данном случае наиболее вероятным типом гибридизации кислорода является sp3.

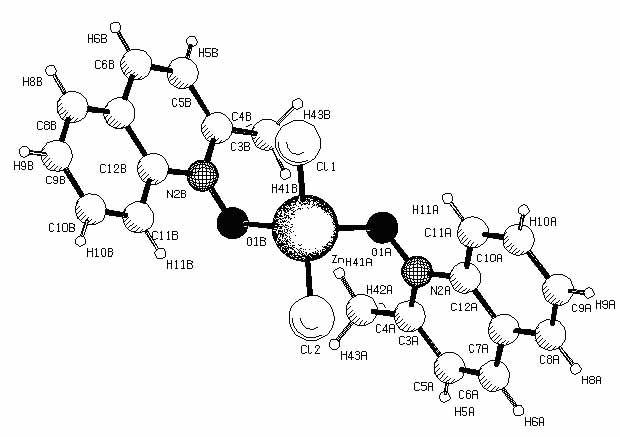
Рис. 3. Структура комплексов N-оксида 2-метилхинолина с CuCl2 и. ZnCl2 состава 2:1.
Из полученных нами данных РСА биядерного комплекса CuCl2 с N-оксидом хинолина состава 1:1 (рис.4) видно, что он не является планарным, чего можно было бы ожидать при сохранении sp2-гибридного состояния кислорода (как в исходном N-оксиде). Следует подчеркнуть, что в данном комплексе два атома кислорода и два атома меди находятся в одной плоскости, по отношению к которой плоскость ароматического ядра повернута примерно на 90°. В этом случае исключается возможность сопряжения N-оксидной группы с ароматическим ядром, а все указанные валентные углы могут быть интерпретированы в рамках sp3-гибридизации атома кислорода или sp2-гибридного состояния с дополнительным перекрыванием его негибридной орбитали с орбиталью комплексообразователя.
Анализ длин связей в четырехчленном цикле Cu(1)–O(1)–Cu(1b)–O(1b) показывает, что связи Cu-О являются неравноценными: связи Cu(1)–O(1) и Cu(1b)–O(1b) имеют длину 2.106, а Cu(1)-O(1b) и Cu(1b)–O(1) - 2.002. Укорочение связи Cu-О при одном из координационных центров, по-видимому, свидетельствует о дополнительном перекрывании орбиталей кислорода и комплексообразователя. Таким образом, на основании данных РСА можно предположить, что атом кислорода в комплексе N-оксида хинолина состава 1:1 находится в состоянии sp2-гибридизации, в котором орбиталь с неподелённой электронной парой, выведенная из сопряжения с ароматическим кольцом, перекрывается с вакантной орбиталью меди.
Нами было обнаружено, что при смешении насыщенных растворов N-оксида (IIк) и CuCl2·H2O в 96% этаноле в зависимости от условий выделения можно получить два типа аддуктов: мелкокристаллического осадка состава (Iк)2· (CuCl2)2 (при немедленном выделении) и кристаллов, образующихся при испарении растворителя в течение месяца. В последнем случае согласно данным РСА молекулярный комплекс имеет состав (Iк)2·(CuCl2)2·(C2H5OH)·(H2O) (рис.4).
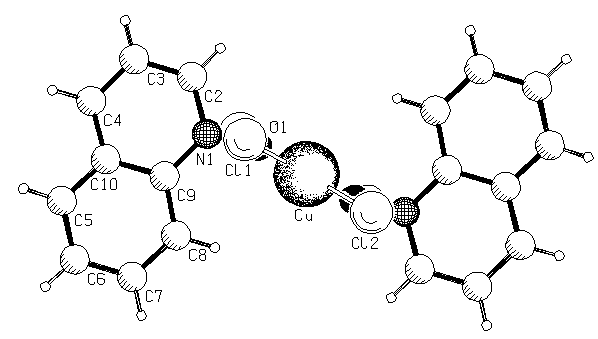
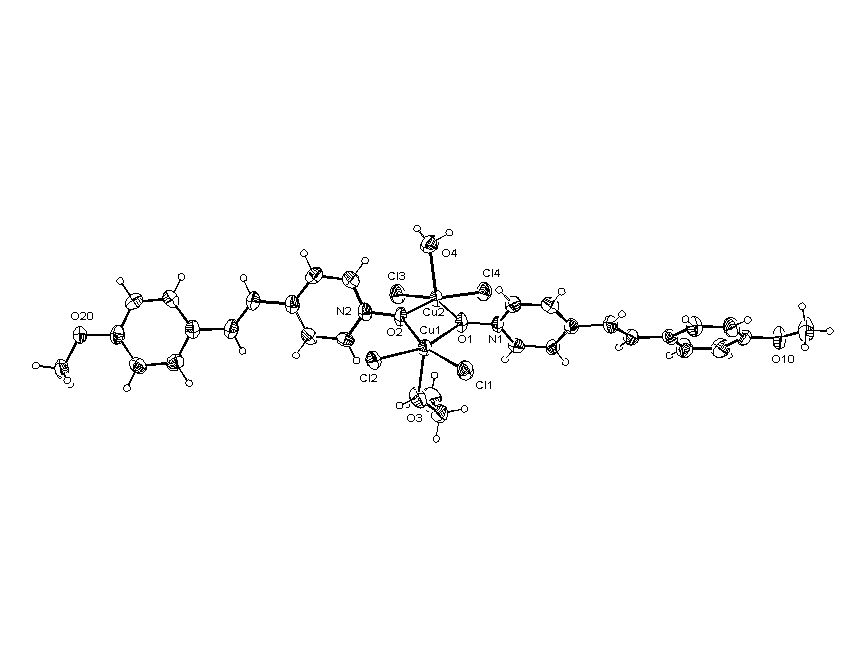
Рис. 4. Структура комплексов N-оксида хинолина с CuCl2 состава 1:1 и (Iк)2·(CuCl2)2·(C2H5OH)·(H2O).
В этом случае комплексообразователь увеличивает свое координационное число от 4 (для ранее рассмотренных комплексов) до 5. Согласно данным РСА донорно-аакцепторные связи с атомами меди образуются за счет групп NO (а не OCH3) N-оксида 4-MPyO При этом дополнительно один атом меди в комплексе координирует молекулу спирта, а второй молекулу воды. Два атома меди и два кислорода N-оксидных групп практически лежат в одной плоскости. Гетероароматические ядра в комплексе находятся в плоскостях, которые по отношению к плоскости четырехчленного цикла Cu-OCu-O образуют торсионные углы 73-75°, что исключает сопряжение атомомв кислорода N-оксидных групп с ароматической системой. Плоскости ароматических колец стирильных заместителей в комплексе расположены под углом 21-24° по отношению к плоскости гетероциклов, что должно приводить к некоторому ослаблению сопряжения. Валентные углы, образованные с участием кислорода, по-видимому, свидетельствуют о его sp2-гибридном состоянии, при котором перпендикулярная негибридная орбиталь связана с одной из вакантных d-орбиталей меди, образуя дополнительную –связь.
Таким образом, данные ПМР спектроскопии и РСА свидетельствуют о возможности перегибридизации атома кислорода группы NO при взаимодействии гетероароматических N-оксидов не только с такой жесткой кислотой Льюиса как BF3, но и с более мягкими ZnCl2 и CuCl2. При этом тип гибридизации в растворе и кристалле зависит от природы лиганда, и акцептора, их соотношения и пространственных напряжений возникающих в процессе комплексообразования. Во всех рассмотренных выше случаях показано отсутствие сопряжения атома кислорода с -системой гетероцикла, что указывает на переход атома кислорода от sp2- к sp3-гибридному состоянию, за исключением биядерных комплексов N-оксидов с хлоридом меди, в которых sp2-гибридное состояние атома кислорода может сохраняться благодаря с дополнительному перекрыванию его негибридной орбитали с орбиталями атомов меди.
1.2.3. Комплексообразование металлопорфиринов с N-оксидами
1.2.3.1. Комплексы пиридинов, хинолинов, N-оксидов пиридинов, хинолинов и акридинов с металлопорфиринами
Исходя из химической значимости процесса аксиальной координации металлопорфиринов и возможности её осуществления при проявлении N-оксидами биологического действия, нам представляется обоснованным исследование молекулярных комплексов металлопорфиринов с гетероароматическими N-оксидами. Для этого мы выбрали (5,10,15,20-тетрафенилпорфинато-4N)цинк(II) (Zn-ТФП), являющийся одним из наиболее доступных металлопорфиринов.
Нами обнаружено, что зависимость lgK аксиальных комплексов Zn-ТФП как с N-оксидами пиридинов, так и с пиридинами с заместителями в 4-положении от PyO- и -констант Гаммета, а также от pKa лигандов в H2O, CH3CN, CH3NO2, ацетоне и CH3OH является линейной (рис. 5). Таким образом, для предсказания устойчивости аксиальных комплексов можно использовать данные по основности лигандов в полярных растворителях, значительно отличающихся по природе взаимодействия с растворенным веществом.
Нами также показано, что в отсутствие стерических эффектов степень батохромного сдвига полос поглощения (I, II, III и Соре) в электронных спектрах Zn-ТФП в хлороформе при добавлении гетероароматических N-оксидов ряда пиридина, хинолина и акридина (или пиридинов) линейно зависит от -констант Гаммета и основности лигандов (рис.6). Гемин (хлороферрипротопорфирин-IX) в ацетоне проявляет необычные свойства при комплексообразовании с N-оксидами: электроноакцепторные заместители в молекуле N-оксида способствуют батохромному сдвигу длинноволновых полос поглощения, а электронодонорные гипсохромному. При этом наблюдается линейная зависимость между сдвигами длинноволновых полос поглощения с -константами Гаммета и PyO-константами. В отличие от Zn-ТФП сдвиг полосы Соре при образовании комплексов с гемином не зависит от характера заместителя в молекуле N-оксида.
Рис. 5. Зависимость lgК комплек- Рис.6. Зависимость смещения
сов Zn-ТФП с N-оксидами пири- полос поглощения Соре (1), III (2),
динов в хлороформе при 298 К II (3) и I (4) в электронных спект-
от pKa лигандов в воде (1), в ме- рах Zn-ТФП в хлороформе от -
таноле (2), в ацетоне (3), в нитро- констант Гаммета при координации
метане (4) и в ацетонитриле (5); с N-оксидами пиридинов и полосы
(6) – зависимость lgK – pKa(H2O) поглощения II с пиридинами (5).
для пиридинов.
Для подтверждения структуры аксиальных комплексов, регистрируемых методом ЭСП, нами были получены смешением насыщенных растворов Zn-ТФП с N-оксидами (VI, VII, VIII, IX, X) и хинолином в водном ацетоне 22 аддукта (выпадение осадков наблюдается в течение нескольких минут), которые представляют собой фиолетовые (с оттенками от синего до красного) вещества состава 1:1. В ИК спектрах этих соединений положение полос поглощения самого Zn-ТФП почти не изменяется. Однако нужно отметить уменьшение интенсивности очень сильной полосы при 1003 см-1. В ИК спектрах комплексов с Zn-ТФП полосы (NO) уменьшают интенсивность или исчезают совсем, а вместо них появляются новые полосы в области 1210 - 1175 см-1, которые накладываются на полосы поглощения МП (1209 и 1177 см-1). Такие изменения в ИК спектрах гетероароматических N-оксидов вызваны координацией Zn-ТФП по атому кислорода N-оксидной группы.
Все выделенные нами молекулярные комплексы Zn-ТФП с гетероароматическим N-оксидами являются мелкокристаллическими соединениями. Однако нам удалось вырастить кристалл аддукта Zn-ТФП с N-оксидом изохинолина, который имел достаточные размеры для исследования методом рентгеноструктурного анализа. Данные РСА подтверждают, что он является аксиальным молекулярным комплексом состава 1:1. В комплексе Zn-ТФП с N-оксидом изохинолина (рис.7) атом цинка с остаточным положительным зарядом отстоит от плоскости порфиринового ядра (находящейся под углом 115.5° к плоскости изохинолинового кольца) на расстоянии 0.323 и 2.100 от атома кислорода N-оксида изохинолина. Геометрия комплекса Zn-ТФП·iQO наиболее вероятно соответствует sp3-гибридному состоянию кислорода, так как торсионный угол между плоскостью гетероцикла и плоскостью включающей фрагмент N-O-Zn составляет 77.70°, что исключает сопряжение атома кислорода как с гетероароматическим кольцом, так и с комплексообразователем.
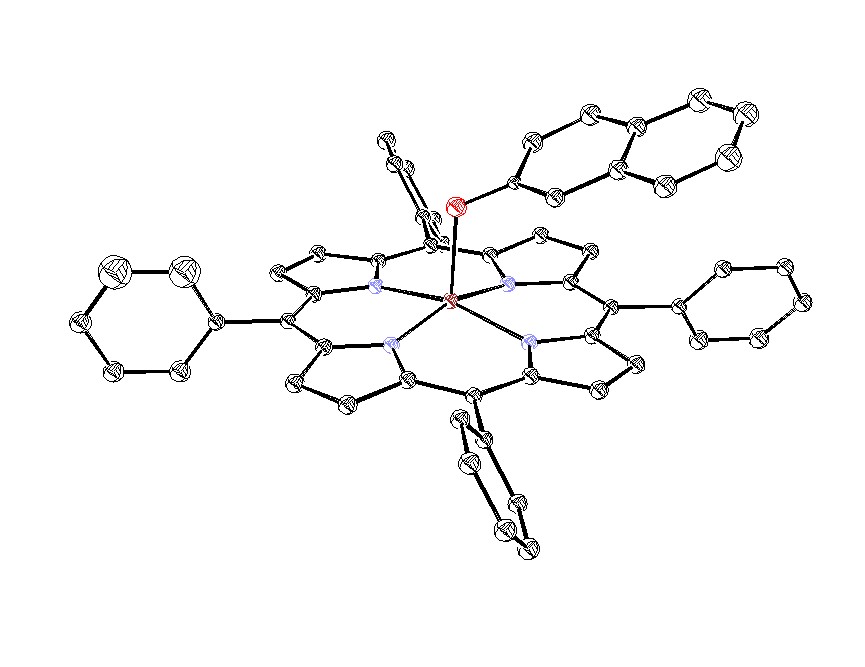
Рис. 6. Структура молекулы комплекса Zn-ТФП· iQO состава 1:1.
Таким образом, на основании данных элементного анализа, электронной и ИК спектроскопии можно сделать вывод, что при взаимодействии Zn-ТФП с исследованными лигандами образуются молекулярные комплексы n,v-типа состава 1:1 с донорно-акцепторной связью между атомом кислорода NO группы и атомом цинка металлопорфирина.. Однако мы не исключаем возможность образования в определённых условиях комплексов иного типа, которые могут не регистрироваться в используемых нами условиях эксперимента.
1.2.3.2. Новая шкала основности/нуклеофильности
Комплексообразование Zn-ТФП с лигандом (L) имеет много 
общего с реакциями нуклеофильного замещения. Реакция замещения при Csp3 может осуществляться как диссоциативный (SN1) или как синхронный процесс (SN2) как в прямом, так и в обратном направлении.
![]()
Y- + R-X [ Y- ··· R ··· X - ] Y-R + X-
Следовательно, с одной стороны, реакции нуклеофильного замещения можно рассматривать как равновесные процессы конкурентного взаимодействия комплексообразователя (карбокатион, реакции SN1) с двумя разными лигандами или распада комплекса, содержащего два разных лиганда (активированный комплекс, реакции SN2). С другой стороны, комплексообразование подобно реакциям замещения (обмена) с участием комплексов состава 1:1 (Zn-ТФП·L) или 1:2 (Zn-ТФП·2L), в которых нуклеофил и уходящая группа могут отличаться друг от друга или быть идентичными.
Литературные и полученные нами экспериментальные данные (калориметрическое титрование, электронная, флуоресцентная и ПМР спектроскопия, РСА) показывают, что величины констант устойчивости (К), смещений максимумов полос поглощения () МП и химических сдвигов () МП и лиганда, а также расстояния между Zn, ТФП и L могут быть использованы в качестве параметров относительной основности/нуклеофильности реагентов. При этом комплексообразование Zn-ТФП с лигандами должно описываться уравнениями подобными уравнениям Гаммета и Тафта, константа устойчивости комплекса K должна (как и константа скорости k) характеризовать нуклеофильность (основность, pKa) лиганда, причем соотношение между K и k определяться электронными и стерическими факторами. Однако, очевидно, что если одни и те же значения * и ES входят в уравнения для расчета lgK и lgk, то можно получить два других, где будет содержаться только одна из этих переменных (lgK/k = a1 + b1·ES и lgK/k = a2 + b2 ·* ).
Нами показано, что подобные соотношения для аминов и N-оксидов пиридинов описываются хорошими коэффициентами корреляции. Поэтому мы предлагаем в качестве модельного процесса при исследовании нуклеофильности реагентов использовать реакцию их комплексообразования с Zn-ТФП в хлороформе, а в качестве параметра нуклеофильности, зависящего от основности лиганда, поляризуемости нуклеофильного центра и молекулы в целом, электронных и пространственных факторов действующих в реагенте – константу устойчивости молекулярного комплекса Zn-ТФП·L состава 1:1 (а при использовании спектрофотометров и ЯМР спектрометров высокого разрешения также и ). Однако следует подчеркнуть, что константы устойчивости в качестве меры нуклеофильности следует использовать только в тех случаях, когда существует уверенность, что образующийся комплекс состава 1:1 является аксиальным (n,v-типа), так как в противном случае их величины будут определяться иной совокупностью взаимодействий участников комплексообразования и описываться иными (возможно гораздо более сложными) корреляционными уравнениями.
1.2.3.3. Относительная нуклеофильная реакционная способность пиридинов и N-оксидов пиридинов
Более высокая чувствительность нуклеофильности N-оксидов пиридинов по сравнению с пиридинами к основности в реакциях с электрофильными субстратами неизбежно должна приводить к пересечению прямых (lgk = lgk0 + pKa ) при некотором значении pKa, при котором их реакционная способность станет одинаковой (своего рода изопараметрическая точка ), а затем произойдет ее обращение. В случае реакций ацилирования это явление экспериментально недостижимо, но при алкилировании фенацилбромидом и метилиодидом происходит реальное обращение реакционной способности данных серий нуклеофилов (рис.7), т.е. “супернуклеофильность” пиридин-N-оксидов зависит от природы электрофильного партнера.
Рис.7 Зависимость lgk реакции N-оксидов пиридинов (1) и пиридинов (2) с бензоилхлоридом (а) и метилиодидом (б) в ацетонитриле при 25°С от pKa нуклеофилов в ацетонитриле
На основании данных по комплексообразованию с BF3, ZnCl2, CuCl2 и Zn-ТФП мы полагаем, что электрофильный агент на начальном этапе реакции с гетероароматическими N-оксидами может приводить к поляризации связи NO, в ходе которой (по аналогии с механизмами реакций с участием двойной связи) не исключено образование соответствующего -комплекса, а затем и химической связи с атомом кислорода как за счет пары электронов, занимающих негибридную, находящуюся в сопряжении с гетероциклом, орбитали, так и одной из двух sp2-гибридных орбиталей атома кислорода). С нашей точки зрения “супернуклеофильность” N-оксидов пиридинов в реакциях переноса ацильных групп (например, взаимодействия с PhCOCl) можно обьяснить стабилизацией переходного состояния благодаря образованию системы с прямым резонансным сопряжением между нуклеофильным и электрофильным компонентами, что невозможно для реакций с участием пиридинов и алкилгалогенидов.
Иодистый метил является очень слабой кислотой Льюиса, и поэтому N-оксиды пиридинов с этим субстратом, по-видимому, образуют связь с участием sp2- гибридной орбитали атома кислорода. Однако увеличение основности N-оксидов, стерических затруднений реакции (заместители в положениях 2,6 пиридинового кольца и большой обьем алкильной группы иодида) должны, как и в случае комплексов с трифторидом бора, благоприятствовать sp2-sp3 перегибридизации атома кислорода группы NO.
Согласно литературным данным происходят “странные” изменения устойчивости в ряду продуктов алкилирования N-оксидов PyO – 2-Me-PyO – 2,6-Me2-PyO: уменьшение - при введении первой метильной группы во второе положение пиридинового кольца и увеличение, противоречащее телескопичности (усилению роли) стерических эффектов, при введении второго заместителя в шестое положение. Скорость распада солей, содержащих при атоме кислорода метильную и этильную группы, становится даже меньше, чем в случае производных N-оксида пиридина и только при наличии изопропильной группы она возрастает и становится такой же, как в случае этокси-2,6-диметилпиридиний иодида, как будто бы в этом случае стерический фактор становится не столь существенным, как электронное влияние.
Такое изменение устойчивости продуктов алкилирования N-оксидов можно обьяснить изменением гибридизации атома кислорода в тех случаях, когда это приводит к менее напряженному состоянию молекулы. По-видимому, образование связи O-C при алкилировании N-оксида 2-метилпиридина осуществляется за счет sp2–гибридных орбиталей атома кислорода, приводя к равновесной смеси, в которой доля конформации с максимальным расстоянием между алкильными группами возрастает с увеличением размера радикала в алкилгалогениде (рис.8а ). При этом важно учитывать, что распад солей происходит только из ионной пары, в которой увеличение размера галогенид-иона при введении заместителей в положения 2 и 6 пиридинового кольца создает все большее напряжение в соли. В случае алкилирования N-оксида 2,6-диметилпиридина конформации с атомом кислорода в состоянии sp2-гибридизации становятся столь напряженными, что O-C связь (в плоскости перпендикулярной пиридиновому кольцу) образуется за счет sp3-гибридной орбитали атома кислорода (рис.8б), тем самым уменьшая электростатическое отталкивание между электронными облаками алкильных групп и повышая устойчивость соли.
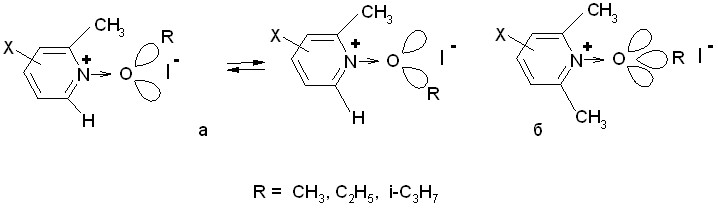 Рис.8. Конформации продуктов взаимодействия N-оксидов 2-метил- и 2,6-диметилпиридинов с алкил иодидами.
Рис.8. Конформации продуктов взаимодействия N-оксидов 2-метил- и 2,6-диметилпиридинов с алкил иодидами.
Следует отметить, что при взаимодействии N-оксидов пиридинов с субстратами, содержащими реакционный центр, способный к сопряжению с атомом кислорода группы NO, существует дополнительный фактор, позволяющий, не меняя состояние гибридизации атома кислорода, свободное вращение относительно связи N – O. Этот эффект заключается в том, что p-орбиталь атома кислорода в переходном состоянии, частично перекрывающаяся с p-орбиталями атома азота и реакционного центра, может выйти из сопряжения с пиридиновым кольцом, но стать частью цепи сопряжения в молекуле субстрата.
В твердом состоянии (подобно молекулярным комплексам N-оксидов пиридинов с BF3), все 6 известных в литературе солей N-алкокси-, N-арилокси- и N-гетерилоксипиридиния, для которых расшифрована структура методом РСА, содержат атом кислорода в состоянии sp3-гибридизации.
Однако, несмотря на то, что, в отличие от реакций нуклеофильного замещения, при комплексообразовании N-оксидов пиридинов с Zn-ТФП в переходном состоянии маловероятно (практически невозможно) сопряжение лиганда с атомом цинка, они остаются несколько более сильными нуклеофилами ( lgKPy = 0.23pKa + 2.41, lgKPyO = 0.32 pKa + 2.77), чем пиридины с той же основностью. Не исключено, что при комплексообразовании Zn-ТФП c N-оксидами пиридинов таким дополнительным стабилизирующим переходное состояние фактором, приводящим к их супернуклеофильности, может быть - взаимодействие между ароматическими системами участников процесса (невозможное в случае пиридинов ориентированных перпендикулярно молекуле МП).
1.3. Реакции нуклеофильного замещения с участием
молекулярных комплексов
1.3.1. Реакции N-оксидов хинолинов
Реакции нуклеофильного замещения в ряду N-оксидов пиридинов и хинолинов со слабыми нуклеофилами (галогенид-ионами) обычно требуют кипячения с концентрированными водными растворами HCl или HBr, либо использования галогенангидридов уксусной кислоты или фосфорилгалогенидов и в ряде случаев сопровождаются побочными процессами, например, образованием продуктов дезоксидирования.
Известно, что реакция между N–оксидом 4-нитрохинолина и триэтилбензиламмоний хлоридом (ТЭБАХ) в присутствии тетрацианоэтилена (ТЦЭ), способного образовывать комплексы с переносом заряда,-типа, довольно легко протекает при комнатной температуре, давая N-оксид 4-хлорхинолина, однако этот метод малопригоден для получения продукта реакции в препаративных количествах.
Нами обнаружено, что при пропускании газообразных сухих HCl и HBr через насыщенный раствор N-оксида 4-нитрохинолина в хлороформе превращение заканчивается при комнатной температуре с близким к количественному выходом за 15-30 мин. Гидрогалогениды N-оксидов в виде бледно-желтых кристаллов с количественными выходами получали простым испарением хлороформа, а свободные N-оксиды - обработкой солей водным раствором K2CO3 с последующей экстракцией хлороформом. При пропускании газообразных HF и HI через раствор N-оксида (IIг) в CHCl3 реакция замещения нитрогруппы не идет:

в первом случае образуется гидрофторид исходного соединения, а во втором осуществляются окислительно-восстановительные реакции с участием иодид-иона.
При добавлении BF3·Et2O в реакционную среду, содержащую N-оксид 4-нитрохинолина (или использовании твердого аддукта N-оксида с BF3) и, ТЭБАХ в безводном ацетонитриле реакция замещения нитрогруппы на атом хлора и в первом и во втором случаях заканчивается за одно и то же время (при комнатной температуре за 1ч, при 65°С за 30 мин). Это указывает на участие в нуклеофильном замещении молекулярного комплекса Iг·BF3 (IIг·HCl при использовании HCl), в котором за счет связывания с v-акцептором увеличивается электрофильность N-оксида. В хлороформе за 6 часов образуется только 50% продукта замещения, т.е. BF3 является менее эффективным активатором реакции, чем протон генерируемый хлороводородом.
При использовании HClO4 и CF3COOH в качестве активатора реакции скорость замещения в апротонных ацетонитриле и диоксане практически одинакова, а при использовании 96% этанола, способного к специфическим взаимодействиям с хлорид-ионом, значительно ниже. Так как хлористый водород одновременно является источником протона и нуклеофила (Cl-), мы сравнили скорость реакции замещения нитрогруппы в апротонном растворителе ацетонитриле и в конц. HCl. Оказалось, что в первом случае превращение заканчивается за 30 мин при 65°С или за 1 сутки при комнатной температуре, а во втором, несмотря на большую концентрацию HCl, даже при 100°С только за 1 час. Обе системы являются гомогенными, и поэтому мы склонны обьяснить этот факт меньшей нуклеофильностью хлорид-иона в концентрированной водной соляной кислоте по сравнению с апротонным ацетонитрилом. В случае использования соединений - источников бромид-иона - отмеченные выше закономерности в общем сохраняются, но реакция идет с меньшей скоростью.
Оказалось, что AlCl3 одновременно выступает в роли не только мощного v-акцептора, но и достаточно эффективного источника хлорид-ионов. Согласно данным ВЭЖХ нагревание эквимольных количеств N-оксида (IIг) и AlCl3 в ацетонитриле в течение 15 мин при 65°C или выдерживание реакционной смеси при комнатной температуре в течение суток приводит к образованию N-оксида (IIд) с количественным выходом. Такие галогенсодержащие кислоты Льюиса, как SbF3, BF3, ZnCl2 и CuCl2 в отличие от AlCl3 в описанных условиях являются плохими источниками галогенид-ионов (BF3), либо акцепторами электронов гетероцикла (ZnCl2 и CuCl2), либо тем и другим (SbF3).
Мы проверили возможность использования для активации реакции N-оксида (IIг) с ТЭБАХ таких -акцепторов как 2,4-дихлор-5,6-дицианобензохинон (ДДХ), 2,3,5,6-тетрахлорбензохинон (хлоранил- ХА) и 7,7,8,8-тетрацианохинодиметан (ТЦХМ). Оказалось, что первые два соединения довольно эффективно ускоряют замещение нитрогруппы на атом хлора (реакция заканчивается с хлоранилом за 1 ч., а с ДДХ за 2 ч.), однако значительно проигрывая таким v-акцепторам, как H+, BF3 и AlCl3. В то же время в присутствии ТЦХМ за 3 часа превращение осуществляется только на 40%, а с ТЦЭ за 15 мин образуется 37% N-оксида (IIд), количество которого не меняется при более длительном нагревании реакционной смеси и повторном добавлении акцептора.
Таким образом, v-акцепторы (H+, BF3, AlCl3) в случае реакции замещения нитрогруппы на атом хлора в N-оксиде 4-нитрохинолина, являются более эффективными активаторами чем -акцепторы.
1.3.2. Реакции N-оксидов пиридинов
Известно, что с N-оксидом 4-нитропиридина реакции нуклеофильного замещения протекают значительно хуже, чем с N-оксидом 4-нитрохинолина. Нами обнаружено, что в CH3CN реакционная способность N-оксидов 4-нитропиридинов с HCl, AlCl3 и ТЭБАХ/BF3 в зависимости от положения CH3-группы изменяется в следующем порядке: Iп >Iг >>Iс > Iр. Повышенная активность N-оксида (Iп), по-видимому, обусловлена эффектом “выворачивания” нитрогруппы из плоскости сопряжения с пиридиновым кольцом расположенной в орто-положении метильной группой. В случае N-оксидов (Iс) и (Iр) данные реакции практически не идут. По-видимому, это связано со стерическими эффектами метильных групп, препятствующих взаимодействию электроноакцептора по N-оксидной группе.
Как и при взаимодействии с N-оксидом (IIг), AlCl3 в реакциях с (Iг,п-с) выступает в роли v-акцептора и источника хлорид-иона.
Следует отметить, что ТЦЭ ускоряет реакцию N–оксидов (Iг,п-с) с ТЭБАХ почти в одинаковой степени. Этот феномен требует особого исследования, принимая во внимание тот факт, что акцепторные свойства ТЦЭ существенно ниже, чем у ДДХ, в присутствии которого реакция N-оксидов (Iс) и (Iр) с ТЭБАХ не идет.
1.3.3. Активация v–акцепторами реакции нуклеофильного замещения нитрогруппы и атомов галогена в хинолиновом кольце
Нами показано, что в 4-нитрохинолине реакция замещения нитрогруппы на хлор при активации протоном (HCl (газ) в CHCl3, конц. HCl), BF3 (ТЭБАХ в ацетонитриле) и AlCl3 (в CH3CN) протекает практически с той же скоростью, что и с N-оксидом 4-нитрохинолина. Это указывает на доминирующую роль кислот Бренстеда-Лоури и Льюиса в увеличении положительного заряда в гетероцикле (в их присутствии наличие
NO группы мало влияет на скорость реакции). В той же степени ускоряет реакцию и ДДХ. Однако при использовании в качестве акцептора ТЦЭ через 15 мин образуется равновесная смесь, содержащая 10% 4-хлорхинолина и 90% исходного соединения. Нам не удалось выделить гидрохлорид 4-нитрохинолина в индивидуальном состоянии, так как в нем довольно быстро протекает реакция замещения нитрогруппы на атом хлора. Осадок, выделяющийся после кратковременного пропускания хлороводорода через раствор 4-нитрохинолина в диэтиловом эфире (или гексане), содержит около 50 % 4-хлорхинолина. Реакция продолжает идти в твердой фазе даже без растворителя и через сутки проходит на 100 %.
Нами также обнаружено, что, используя в качестве исходного соединения 2,4-дибромхинолин и варьируя условия взаимодействия с HCl (полярность растворителя, температура и время), можно количественно получить гидрохлорид исходного соединения, а также продукты замещения одного или двух атомов брома (табл. 1). Так, взаимодействие 2,4-дибромхинолина с соляной кислотой в CH3CN при 65°С в течение 30 мин приводит к продукту замещения обоих атомов брома — 2,4-дихлорхинолину. При пропускании газообразного HCl через раствор 2,4-дибромхинолина в CH3CN через несколько минут образуется 4-бром-2-хлорхинолин, который затем медленно превращается (за 1 сутки на 100%) в 2,4-дихлорхинолин, в то время как реакция в хлороформе за 1 час приводит к образованию только 4-бром-2-хлорхинолина. При пропускании хлороводорода через раствор 2,4-дибромхинолина в гексане в течение нескольких секунд в осадок выпадает гидрохлорид 2,4-дибромхинолина.
При длительном нагревании (65°С, 3 суток или 80°С, 10 часов) в CH3CN 2,4-дибромхинолина в присутствии HClO4 происходит замещение атома брома на группу OH с образованием 4-бромхинолона-2. В
Таблица 1. Реакция 2,4-дибромхинолина с HCl и HClO4
| № | Кислота | t, oC | Раство-ритель | Продукт | Выход, % | Время |
| 1 | HCl газ | 20 | гексан | 2,4-дибромхинолинHCl | 70 | 15 с |
| 2 | HCl конц. | 65 | CH3CN | 2,4-дихлорхинолин | 98 | 0.5 ч |
| 3 | HCl конц. | 65 | CH3CN | 4-хлорхинолон-2 | 98 | 72 ч |
| 4 | HCl конц. | 20 | CH3CN | 2,4-дихлорхинолин | 94 | 20 ч |
| 5 | HCl газ | 20 | CHCl3 | 4-бром-2-хлорхинолин | 94 | 1 ч |
| 6 7 | HCl газ HCl газ | 20 20 | CH3CN CH3CN | 2-хлор-4-бромхинолин 2,4-дихлорхинолин | 98 96 | 5 мин 24 ч |
| 8 | HClO4 | 65 | CH3CN | 4-бромхинолон-2 | 81 | 72 ч |
аналогичных условиях продуктом взаимодействия 2,4-дихлорхинолина с HCl или HClO4 является 4-хлорхинолон-2. Последний также образуется при длительном нагревании раствора 2,4-дибромхинолина в CH3CN с конц. HCl (при 65°С в воде реакция не идёт, а в растворе KOH в смеси CH3CN-H2O (1:1) при 65°С проходит за 3 ч).
Нами обнаружено, что такие кислоты Льюиса как BF3 и AlCl3 (v-акцепторы), ДДХ и ТЦЭ (-акцепторы) также являются активаторами реакции нуклеофильного замещения атомов брома в 2,4-дибромхинолине на хлор. Однако в отличие от реакций с использованием кислот Брёнстеда-Лоури в этих условиях не удаётся заместить один или два атома брома с количественным выходом. При соотношении 2,4-дибромхинолин - нуклеофил 1:1 за 15–30 мин (с ДДХ около 1 ч) образуется равновесная смесь, содержащая исходное соединение (35%) и продукты замещения одного (50%) и двух (15%) атомов брома на хлор.
В ходе реакции 2,4-дихлорхинолина и 2-хлор-4-бромхинолина с конц. HBr в CH3N при 65 oC происходит замещение атомов хлора на бром, но этот процесс сопровождается быстрым гидролизом образующихся соединений, приводящий к 4-галогенхинолонам-2. Интересно, что в случае 4-бром-2-хлорхинолина, несмотря на большой избыток HBr, наряду с 2,4-дибромхинолином образуется также значительное количество 2,4-дихлорхинолина, что указывает на взаимодействие высвободившихся ионов хлора с исходным 2-хлор-4-бромхинолином.
На примере взаимодействия 2,4-дибромхинолина с ТЭБАХ и 2,4-дихлорхинолина с триметилцетиламмоний бромидом в CH3CN нами обнаружено, что, как и кислоты Бренстеда-Лоури, такие кислоты Льюиса как BF3, AlCl3, ДДХ и ТЦЭ также являются активаторами реакций нуклеофильного замещения атомов галогена на галоген в 2,4-дигалогенхинолинах.
Таким образом, принцип активации реакций SN электроноакцепторами может быть реализован в случае нуклеофильного замещения нитрогруппы и атомов галогена в неокисленных гетероциклах. По-видимому, этот принцип можно распространить и на другие типы процессов, для осуществления которых требуется увеличение положительного заряда в молекулах, способных к образованию n,v-комплексов.
2. Ацетиленовые амины и ЧАС как основания и нуклеофилы
2.1. Синтез исходных соединенй
Третичные - ацетиленовые амины синтезированы N-алкилированием вторичных аминов,
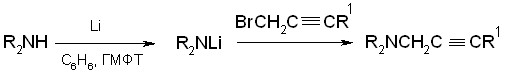
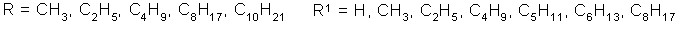
а третичные - и - ацетиленовые амины получены С- алкилированием ацетиленовых углеводородов с терминальной тройной связью бифункциональными соединениями – (диалкиламино)алкилхлоридами

R = CH3, C2H5, C4H9 n = 2, 3 R1 = C3H7, C4H9, C5H11, C6H13
Структура ранее неизвестных - и - ацетиленовых аминов подтверждена элементным анализом и спектроскопическими методами.
Для - и - ацетиленовых аминов с дизамещенной тройной связью были сняты спектры комбинационного рассеяния, которые подтверждают ее наличие поглощением в области 2225 см-1. Положение тройной связи по отношению к атому азота доказано химическим методом – окислением аминов перманганатом калия с последующей идентификацией образующихся кислот со стандартами методом ТСХ. Анализ спектров ЯМР 13С третичных -, - и -ацетиленовых аминов позволил сделать вывод о возможности использования этого метода для определения положения дизамещенной тройной связи.
2.2. Исследование основности и нуклеофильности ацетиленовых аминов
Для получения информации о состоянии свободной электронной пары на атоме азота мы определили константы основности третичных - и - ацетиленовых аминов в метаноле (табл.2) методом потенциометрического титрования. Полученные значения pKa показывают, что третичные -ацетиленовые амины в метаноле более сильные основания, чем - и - ацетиленовые амины, но более слабые, чем предельные третичные амины: pKa < pKa < pKa < pKa пред.
Таблица 2. Константы основности в метаноле, константы скорости для реакции R2 N R1 + EtI [ R2 N R1Et]+ I – (1) и константы скорости и параметры активации для реакции R2 N R1 + BrCH2CCR2 [ R2 N R1 CH2CCR2 ]+ Br – (2) в ацетофеноне.
| R2 N R1 | pKa 20°С | k50°104 л/моль· сек (1) | R2 | k20°104 л/моль· сек (2) | H ккал/моль | S э.ед. |
| (C4H9)2NCH2CCC4H9 | 8.73 | 1.70 | C4H9 | 25.3 | 8.8 | -40 |
| C6H13 | 24.5 | 8.8 | -40 | |||
| C8H17 | 24.0 | 8.6 | -41 | |||
| (CH3)2N(CH2)2CCC4H9 | 9.09 | 25.0 | C4H9 | 278 | 8.8 | -36 |
| (C2H5)2N(CH2)2CCC4H9 | 9.64 | 1.20 | 16.1 | 9.9 | -37 | |
| (C4H9)2N(CH2)2CCC4H9 | 9.47 | 0.71 | 6.59 | 12.3 | -31 | |
| (CH3)2N(CH2)3CCC4H9 | 9.51 | 9.51 | 335 | 8.3 | -37 | |
| (C2H5)2N(CH2)3CCC4H9 | 10.03 | 10.03 | 24.0 | 9.3 | -39 | |
| (C4H9)2N(CH2)3CCC4H9 | 9.76 | 9.76 | 9.3 | 12.0 | -32 |
Для изучения нуклеофильной реакционной способности третичных ацетиленовых аминов с различным положением тройной связи нами проведены кинетические исследования реакции кватернизации этих соединений иодистым этилом и бромидами пропаргильного типа в ацетофеноне в температурном интервале 20-40°С (табл.2). Как следует из кинетических данных - ацетиленовые амины опережают по нуклеофильности более сильные основания - и - ацетиленовые амины. Однако, если бы действовали только полярные факторы, то нуклеофильность аминов изменялась бы в той же последовательности, что и основность. Поэтому аномально высокая реакционная способность - ацетиленовых аминов должна быть связана с большей доступностью реакционного центра атома азота (четыре атома –С-СС-С- лежат на одной прямой) в этом случае, т.е. стерическими причинами.
Термодинамические параметры подтверждают особое положение - ацетиленовых аминов - низкие значения Еакт и H свидетельствуют о меньших стерических препятствиях в этих аминах по сравнению с - и - ацетиленовыми аналогами. Высокие отрицательные значения величин S характерны для таких реакций нуклеофильного замещения, которые протекают с образованием очень полярного переходного состояния, что относится и к реакции Меншуткина. При переходе от метильных к бутильным аналогам в - и - ацетиленовых аминах константа скорости реакции уменьшается, что объясняется увеличением стерических препятствий у атома азота в этом ряду. Это также подтверждается соответствующим увеличением H приблизительно на 3.5 ккал/моль.
Проведенные нами кинетические исследования, показавшие не зависящую от длины цепи высокую реакционную способность галогенидов пропаргильного типа, позволили нам разработать препаративный метод синтеза высших диацетиленовых ЧАС. Реакция проводилась при эквимолярном соотношении реагентов при комнатной температуре в полярных растворителях типа ацетонитрила и ацетофенона (время реакции 2-3 часа) и в пентане (время реакции несколько дней) и заканчивалась с высокими выходами. Индивидуальность полученных солей показана с помощью разработанного нами метода тонкослойной хроматографии в виде ионных пар на слоях силикагеля модифицированных NaBr. Строение ЧАС подтверждено элементным анализом (бромид-ион определен методом меркурометрии) и спектральными методами.
Используя литературные и наши данные для EN предельных и - ацетиленовых аминов и константы реакции кватернизации третичных предельных, -, - и - ацетиленовых аминов иодистым этилом мы с помощью расширенного уравнения Тафта рассчитали стерические константы (EN) для -, - и - ацетиленовых аминов. Оказалось, что они у третичных - и - ацетиленовых аминов близки к значениям EN предельных аналогов, но выше по абсолютной величине примерно на единицу, чем для третичных - ацетиленовых аминов.
Вторичные - ацетиленовые амины являются труднодоступными соединениями, а методы синтеза третичных - ацетиленовых аминов обладают рядом существенных недостатков. Проведенные нами кинетические исследования показали высокую реакционную способность галогенидов пропаргильного типа в реакции кватернизации, что позволило разработать новые методы синтеза вторичных и третичных - ацетиленовых аминов. В предложенном нами методе алкилирование первичных и вторичных аминов проводится в различных органических растворителях, полярность которых находится в обратной зависимости от основности аминов.
2 R1R2NH + BrCH2CCR3 R1R2NCH2CCR3 + [R1R2NH2]+ Br –
R1R2NCH2CCR3 + BrCH2CCR3 [ R1R2N(CH2CCR3)2]+ Br –
R1 = R2 – C2H5, R3 – H (VIIа); R1 = R2 – C2H5, R3 – C4H9 (VIIб); R1 = R2 = R3 - C4H9 (VIIв); R1 = R2 – C7H15, R3 – C4H9 (VIIг); R1 – C6H5, R2 –CH3, R3 – H (VIIд); R1 – C6H5, R2 – CH3, R3 – C4H9 (VIIе); R1 = R2 – C3H7, R3 – C4H9 (VIIж); R1 = R2 - C4H9, R3 - C2H5 (VIIз); R1 = R2 – C7H15, R3 - C2H5 (VIIи) Выходы 65 – 85 %
Было показано, что с увеличением кинетической активности растворителя количество ЧАС увеличивается. С целью подавления образования ЧАС реакция с сильными основаниями предельными аминами проводилась в пентане. В случае более слабых оснований ароматических аминов использовался хлороформ.
Соотношения исходных реагентов были нами установлены на основании кривых конверсии, построенных при исследовании реакционной смеси методом ГЖХ. Наиболее благоприятное соотношение молярных концентраций вторичный амин : пропаргилгалогенид – 2 : 1.
Нами разработан также эффективный метод синтеза вторичных - ацетиленовых аминов, на который получено авторское свидетельство.
2 R1NH2 + BrCH2CCR2 R1NHCH2CCR2 + [R1NH3]+ Br –
R1NHCH2CCR2 + BrCH2CCR2 R1N(CH2CCR2)2
R1 – (CH3)2CH, R2 – H (VIIIа); R1 – (CH3)2CH, R2 – C4H9 (VIIIб); R1 – C4H9, R2 – H (VIIIв); R1 = R2 - C4H9 (VIIIг); R1 – C4H9, R2 – C6H13 (VIIIд); R1 - C6H13, R2 – H (VIIIе); R1 - C6H13, R2 - C4H9 (VIIIж); R1 - C6H5, R2 – H (VIIIз); R1 - C6H5, R2 - C4H9 (VIIIи); R1 – O2NC6H4, R2 - C4H9 (VIIIк); R1 – H2NCH2CH2, R2 – H (VIIIл); R1 – H2NCH2 CH2, R2 - C4H9 (VIIIм); R1 – HOCH2CH2, R2 – H (VIIIн) Выходы 55 – 75 %
Выбор растворителя и в этом случае определялся основностью исходного амина. Для сильных предельных аминов использовался пентан, для более слабых ароматических аминов – хлороформ, а в очень полярном растворителе ацетонитриле нами впервые была проведена реакция пропаргилирования такого слабого амина, как пара-нитроанилин. Алкилирование первичных аминов осуществляли при комнатной температуре при соотношении первичный амин – ацетиленовый бромид 3 : 1.
Структура ранее неизвестных вторичных и третичных - ацетиленовых аминов подтверждена элементным анализом и методами ИК и ПМР спектроскопии, для вторичных - ацетиленовых аминов определены константы основности в метаноле методом потенциометрического титрования.
2.3. Прототропная изомеризация третичных - ацетиленовых аминов
Ацетиленовые амины с -, - и более удаленной от азота тройной связью труднодоступны. Третичные же -производные могут быть легко получены алкилированием вторичных аминов бромидами пропаргильного типа в предложенных выше условиях. Поэтому нами изучена изомеризация этих соединений в присутствии суперсильного основания 3-аминопропиламида натрия (рядом авторов показано, что с ацетиленовыми углеводородами, спиртами и борпроизводными смещение тройной связи в терминальное положение осуществляется даже на семь углеродных атомов за несколько минут в мягких условиях с количественными выходами). В качестве объектов нами были выбраны 1-дибутиламино- и 1- дигептиламинопент-2-ин, которые в результате реакции могли давать небольшое количество изомеров, упрощая идентификацию и выделение продуктов. Для контроля за ходом изомеризации нами был предварительно разработан хроматографический метод разделения -, - и - ацетиленовых аминов на кислой окиси алюминия фирмы Woelm в системе растворителей хлороформ : диэтиловый эфир = 3 : 1 или хлористый метилен : диэтиловый эфир = 5 : 1.
Реакция проводилась при комнатной температуре в присутствии 3-аминопропиламида натрия (NAPA), который получали по методу Брандсма взаимодействием амида натрия с 1,3-диаминопропаном.
В качестве основного продукта при изомеризации 1-дибутиламино-2-пентина был выделен диеновый изомер, а при изомеризации 1-дигептиламино-2-пентина - ацетиленовый амин с терминальным положением тройной связи. Специальными опытами нами было показано, что в условиях эксперимента диеновый и с терминальной тройной связью амины не претерпевают изменений по крайней мере в течение 48 часов.

Индивидуальность полученных соединений была показана с помощью ТСХ на кислой окиси алюминия и полиамиде, строение подтверждено элементным анализом и методами ИК, УФ, ПМР спектроскопии и масс-спектрометрии.
Позднее группой под руководством профессора Фаворской И.А. было обнаружено, что повышение температуры до 50-80°С позволяет из 1-дибутиламинопент-2-ина и гепт-2-ина, а также 1-диэтиламиноундец-2-ина получить соответствующие соединения с терминальной тройной связью с выходом 70-90%. Таким образом, третичные амины и ЧАС с любым количеством метиленовых групп между атомом азота и тройной связью стали легкодоступными (благодаря возможности повторного алкилирования терминального фрагмента C CH).
3. Практическое использование комплексообразующих свойств оснований с пространственно доступными реакционными центрами
Некоторые из полученных нами -ацетиленовых аминов прошли испытания в качестве ингибиторов кислотной коррозии стали при высоких температурах в Саратовском НИИ геологии и геохимии. Нами получено авторское свидетельство по результатам этих исследований.
3.1. Комплексообразование N-оксидов и ЧАС в экстракционных процессах
3.1.1. Экстракция цинка (II) и меди (II) N-оксидами
Известно, что N-оксиды пиридинов, содержащих алкильные группы с числом атомов углерода от 5 до 9 и фосфорилированных метилпиридинов являются эффективными и селективными экстрагентами d- и f-элементов, в связи с чем мы сочли целесообразным исследовать возможность использования N-оксидов стирильных производных пиридина и хинолина для экстракции цинка (II) и меди (II) из водных растворов.
Билогарифмическим методом нами показано, что в исследуемых системах образуются комплексы N-оксид-MeX2 состава 2:1 и коэффициенты распределения цинка (II) и меди (II) при экстракции гетероароматическими N-оксидами зависят от природы самого металла, фонового электролита (катиона и особенно аниона), растворителя и лиганда (электронные и стерические факторы заместителей в гетероцикле), а также от соотношения растворимостей образующихся молекулярных комплексов в водной и органической фазах. Обнаружено, что максимальной экстракционной способностью обладают N-оксиды пиридинов, содержащие стирильный фрагмент в 4- положении, что обусловлено стерическими препятствиями, т.к. в координации участвует атом кислорода группы NO, а N-оксид (VIи) является наиболее перспективным экстрагентом меди (II) и особенно цинка (II), причем более эффективным, чем классически используемый в этих целях трибутилфосфат
3.1.2. Экстракция цинка (II), меди (II), РЗМ (III) и Y (III) моно- и диацетиленовыми ЧАС.
Экстракция солями четвертичных аммониевых оснований (ЧАС) широко применяется в химической технологии для извлечения многих редких и радиоактивных элементов. В то же время соли с непредельными заместителями (особенно содержащими тройные связи), которые могут образовывать с v-акцепторами принципиально иные типы молекулярных комплексов, остаются практически неисследованными.
Нами в качестве объектов исследования были выбраны соединения (IXа-д) и (X), принципиальное отличие которых от описанных в литературе заключается в большей пространственной доступности атома
[ R3NCH2CCR’]+X- [ (C8H17)2N(CH2CCC4H9)2 ]+Br - [(C8H17)3NCH3]+ I-
IXа - д X XI
R - C8H17, R’– H, X– Br (а); R- C8H17, R’– C4H9, X– Br (б); R- C8H17, R’– C4H9, X – I (в); R – C10H21, R’ – C4H9, X – Br (г); R – C10H21, R’ – C6H13, X – Br (д)
азота вследствие линейного строения фрагмента CH2-CC-CH2. Этот факт чрезвычайно важен, т.к. в комплексах, образующихся в процессе экстракции, между анионом четвертичной аммониевой соли (Х-) и катионом металла (Me) возникает донорно-акцепторная связь R4N+Х-: MeХn. Экстракционная способность ЧАС исследовалась нами на примере извлечения Zn(II) и Cu(II) из галогенидных сред.
Оказалось, что зависимость коэффициентов распределения металлов от концентрации HCl в исходном водном растворе носит сложный характер: при использовании ЧАС (IXа) и (IXб) наблюдаются два локальных максимума при концентрациях HCl в областях 2 - 4 и 5 - 7 моль/л, тогда как при экстракции соединением (XI), не содержащим -связей, имеет куполообразный характер лишь с одним широким максимумом при концентрации соляной кислоты 3 - 5 моль/л.
С целью получения информации о составе комплексов Zn и Cu, экстрагируемых солью (IXб) был использован метод сдвига равновесия и показано, что зависимость коэффициента распределения металлов от концентрации экстрагента (IXб) является монотонно возрастающей, а в логарифмических координатах описывается прямой с тангенсом угла наклона, близким к единице, свидетельствуя о том, что в органическую фазу извлекаются комплексы состава металл/ЧАС = 1:1. Однако при наличии по крайней мере 3-4 кратного избытка экстрагента с ионами цинка образуются комплексы состава 1:2 (тангенс угла наклона прямой близок к двум). Следует подчеркнуть, что при экстракции указанных металлов солями предельного характера аддукты состава 1:1 в литературе не описаны. По-видимому, исследуемые нами экстрагенты в указанных условиях способны к образованию комплексов, в которых донорно-акцепторная связь с катионом металла образуется с одновременным участием галогенид-иона (связанного с аммонийным азотом) и тройной связью, а не обычных двойных солей типа [R4N+ X- Me2+ X- N+R4 ]X-2.
Оказалось, что в хлороформе для всех ацетиленовых ЧАС коэффициенты распределения цинка растут с увеличением длины заместителей при азоте и тройной связи и значительно выше, чем для насыщенного аналога: IXд > IXб > X > IX a > XI. Особо следует отметить необычно высокую экстракционную способность соли (X). При наличии двух электроноакцепторных заместителей она является более эффективным экстрагентом цинка, чем (IXа), а в случае меди уступает лишь соли (IXб). Очевидно, это обусловлено пространственной доступностью двух тройных связей в ЧАС (X).
Нами было установлено, что при экстракции редкоземельных металлов (РЗМ) ацетиленовыми ЧАС (IX-X) очень быстро устанавливается равновесие между водной и органической фазами, происходит быстрое расслоение жидкостей, и для процесса экстракции из растворов HNO3 требуется значительно меньшее количество соли, чем XI.
Полученные в Санкт-Петербургском государственном техническом университете данные по экстракции из азотной кислоты четырнадцати РЗМ (III) и Y(III) раствором предоставленного нами нитрата ЧАС (IXa) в толуоле позволяют предполагать, что при насыщении органической фазы во всех случаях образуется соединение состава (R4N)[(Ln)(NO3)4], тогда как согласно литературным данным при использовании нитратов триалкилметиламмония и триалкилбензиламмония в толуоле образуются молекулярные ассоциаты [(R4N)2Ln(NO3)5]·R4N(NO3) или соединения состава [(R4N)2Ln(NO3)5, соответственно. Таким образом наши данные свидетельствуют о перспективности ацетиленовых ЧАС для экстракционного разделения и концентрирования не только Zn(II), Cu(II) и РЗМ (III), но и других d- и f- элементов периодической таблицы Д.И. Менделеева.
3.2. Биологическая активность некоторых эндо- и экзогенных аминов и их производных
3.2.1. Модификация активности Na,K-АТФазы
Воздействие гетероароматических N-оксидов на Na,K-АТФазу ранее не исследовалось. Поэтому мы изучили влияние 32 соединений этого класса в 10-4 – 10-10 М на активность фермента из мозга крупного рогатого скота. Обнаружено, что 16 из них являются ингибиторами Na,K-АТФазы (на 20 - 67% ) даже при концентрациях 10-8 М, что сопоставимо или превышает эффективность используемого в настоящее время лекарственного препарата строфантина К. Особо следует отметить активирующий (на 80 – 90%) эффект соединения (VIIм), так как в настоящее время неизвестны вещества обладающие подобным действием на фермент.
Исследование влияния таких эндогенных нейромедиаторов как ацетилхолин (АХ) и норадреналин (НА) на биосинтетические процессы позволило нам впервые обнаружить, что in vitro и in vivo существует очень сложная система медиаторной регуляции уровня Na,K-АТФазной активности нервных клеток: при активации синтеза энзима (в случае НА) параллельно синтезируется низкомолекулярный фактор-ингибитор, и наоборот – при угнетении синтеза Na,K-АТФазы (АХ) образуется фактор-активатор. Очевидно, что эти разнонаправленные процессы являются звеньями единой саморегулирующейся системы поддержания активности фермента на оптимальном функционально обусловленном уровне. Разработана методика выделения неизвестного ранее ингибитора Na,K-АТФазы из мозга животных.
Указанные выше соединения могут быть рекомендованы для разработки на их основе фармакологически активных препаратов, используемых при лечении заболеваний связанных с нарушениями функционирования Na,K-АТФазы.
3.2.2. Биологические эффекты N-оксидов пиридинов и хинолинов на клетки опухолевых линий in vitro
Известно, что многие цитостатические агенты, используемые в химиотерапии опухолей человека, способны индуцировать дифференцировку клеток опухолей in vivo и опухолевых линий in vitro, в ряде случаев сопровождающуюся запуском в них апоптотических процессов. С другой стороны, использование дифференцирующих агентов в клинической практике может приводить к индукции у опухолевых клеток фенотипа множественной лекарственной устойчивости (МЛУ), что в свою очередь является основной причиной неэффективности применения многих цитостатиков. В связи с этим представляется весьма актуальным поиск таких соединений, которые способны существенно усилить дифференцировку резистентных опухолевых клеток, что может стать альтернативным терапевтическим подходом к преодолению фенотипа МЛУ.
Показано, что некоторые производные N-оксидов хинолина обладают в своих нетоксических дозах апоптогенной активностью, но не способны ингибировать эритроидную дифференцировку клеток К562, в частности, (IIIл). Другие, например, N-оксид хинолина, в нетоксичных концентрациях ингибируют эритроидную дифференцировку указанных клеток, но не влияют на апоптоз опухолевых клеток. И, наконец, такие соединения как (IIг) ингибируют в одних и тех же условиях инкубации эритроидную дифференцировку и индуцируют апоптоз клеток К562. Установлено, что наиболее сильный апоптогенный эффект в опухолевых клетках имеет место при обработке реагентами, способными к наибольшему связыванию с ДНК.
ВЫВОДЫ
- Впервые с использованием физико-химических (ИК, электронная, ЯМР 1H спектроскопия, рентгеноструктурный анализ) и экстракционных методов проведено систематическое исследование молекулярных комплексов N-оксидов ряда пиридина, хинолина и акридина с v-акцепторами различной жёсткости по Пирсону и найдены особенности строения определяющие специфику их реакционной способности.
- Впервые установлено, что при взаимодействии гетероциклических N-оксидов с v-акцепторами может происходить перегибридизация атома кислорода в составе N-оксидной группы. Методами РСА и ПМР доказано, что она зависит от природы донорно-акцепторных компонентов, растворителя и агрегатного состояния. sp3-Гибридизации благоприятствуют увеличение основности N-оксида, кислотных свойств v–акцептора, стерических затруднений образованию связи с кислородом и процессы кристаллизации.
- Впервые показано что Zn-тетрафенилпорфин в хлороформе образует с N–оксидами пиридинов, хинолинов и акридинов комплексы состава 1:1, для которых в отсутствие стерических эффектов наблюдаются линейные зависимости между логарифмами констант устойчивости (K), положением максимумов полос поглощения () в электронных спектрах комплексов по отношению к Zn-ТФП, –константами Гаммета и pKa лигандов в различных растворителях. Предлагается новая шкала основности и нуклеофильности, основанная на параметрах (lgK, ), характеризующих образование аксиальных (n,v-типа) комплексов Zn-ТФП с лигандами (основаниями/нуклеофилами).
4. Впервые предложено теоретическое обоснование супернуклеофильности N-оксидов пиридинов в реакциях переноса ацильных групп. В отличие от пиридинов переходное состояние реакции с их участием стабилизируется образованием системы с прямым резонансным сопряжением между нуклеофильным и электрофильным компонентами.
5. Установлена способность v-акцепторов к активации процессов нуклеофильного замещения в ряду гетероароматических N-оксидов. Комплексы n,v-типа лежат на координате реакции нуклеофильного замещения, а v-акцепторы выступают в роли более эффективных, чем -акцепторы активаторов. Показано, что принцип активации нуклеофильного замещения v- и -акцепторами может быть распространён на неокисленные гетероциклы.
6. Разработаны новые условия и усовершенствованы методы синтеза галогенопроизводных хинолинов, хинолонов, N-оксидов хинолинов и стирильных производных N-оксидов хинолинового ряда.
7. Исследованы кинетические и термодинамические закономерности кватернизации третичных -, -, -ацетиленовых аминов высшими галогенидами пропаргильного типа и иодистым этилом. Установлено, что необычно высокая нуклеофильность -ацетиленовых аминов и электрофильность пропаргилгалогенидов обусловлены пространственной доступностью реакционных центров.
8. Разработаны методы синтеза диацетиленовых четвертичных аммониевых солей, третичных и вторичных -ацетиленовых аминов пропаргилированием соответствующих аминов.
9. Впервые исследованы экстракционные свойства ацетиленовых ЧАС и гетероароматических N-оксидов в зависимости от электронных и стерических факторов. Данные соединения предложены в качестве эффективных экстрагентов d- и f-элементов в различных средах.
10. Впервые исследована изомеризация третичных -ацетиленовых аминов под влиянием суперсильного основания 3-аминопропиламида натрия. Установлено, что в этих условиях могут быть получены ацетиленовый амин с терминальным положением тройной связи и диеновый амин, соотношение которых определяется растворимостью ацетиленидов в пропилендиамине.
11. Исследован механизм действия эндогенных ацетилхолина и норадреналина и экзогенных гетероароматических N-оксидов пиридинового, хинолинового и акридинового ряда на активность Na,K-АТФазы. Впервые установлена индуцирующая роль нейромедиаторов на биосинтез низкомолекулярных регуляторов активности фермента. Выявлено активирующее и ингибирующее действие гетероароматических N-оксидов на функционирование Na,K-АТФазы, что позволяет рекомендовать разработку на их основе фармакологически активных препаратов. Впервые изучено дифференцирующее и апоптогенное действие ряда производных пиридина и хинолина и установлено, что наиболее сильный апоптогенный эффект в опухолевых клетках имеет место при обработке реагентами, способными к наибольшему связыванию с ДНК.
Основные работы, опубликованные по теме диссертации
1. Андреев В.П., Рыжаков А.В., Морозов А.К., Алексеева О.О., Родина Л.Л. Донорно-акцепторные комплексы гетероароматических N-оксидов (обзорная статья) // ХГС.- 1995. - N 6. - C. 760-773.
2. Ермилова Е.В., Ремизова Л.А., Андреев В.П., Абдулганеева С.А., Фаворская И.А. Основность и нуклеофильность высших третичных ацетиленовых аминов // ЖОрХ. - 1977. - Т. 13. - Вып. 6. - С. 1150-1153.
3. Андреев В.П., Вукс Е.М., Кочеткова Е.В., Ремизова Л.А., Фаворская И.А. Кватернизация ацетиленовых аминов 2-пропинил- и алкилгалогенидами // ЖОрХ. -1979. - Т. 15. - Вып. 3. - С. 464-467.
4. Андреев В.П., Ремизова Л.А., Утсаль О.Г., Фаворская И.А. Пропаргилирование первичных и вторичных аминов // ЖОрХ.- 1979.- Т. 15. - Вып. 3. - С.467-471.
5. Ремизова Л.А., Андреев В.П., Гиндин В.А., Балашов Ю.Г., Фаворская И.А. Изомеризация третичных -ацетиленовых аминов под влиянием 3-аминопропиламида натрия // ЖОрХ. - 1980. - Т. 16. - Вып. 4. - С. 726-730.
6. Елаев Н.Р., Андреев В.П., Шаврина Н.В. Эндогенные ингибиторы и активаторы Na,K-АТФазы // Бюлл. эксперим. биологии и медицины. - 1983. - Т. 95. - № 2. - С. 40-42.
7. Андреев В.П., Елаев Н.Р., Унжаков А.Р. Регуляция норадреналином биосинтеза Na,K-АТФазы и ее низкомолекулярного ингибитора // Нейрохимия. - 1984. - Т. 3. - № 4. - С. 443.
8. Андреев В.П., Рыжаков А.В. Исследование процессов таутомерии и внутримолекулярного переноса заряда в ряду ароматических N-оксидов методом электронной спектроскопии // ХГС. - 1993. - № 12. - C. 1662-1669.
9. Андреев В.П., Рыжаков А.В. Донорно-акцепторные комплексы N-оксидов хинолинов с трифторидом бора // ХГС. - 1994. - № 8. - C. 1087-1092.
10. Андреев В.П., Рыжаков А.В., Теканова С.Г. Стирильные производные N-оксида хинолина. // ХГС. - 1995. - N 4. - C. 518-521.
11. Андреев В.П., Калистратова Е.Г., Рыжаков А.В. Новый способ получения гидрогалогенидов N-оксидов 4-галогенохинолинов из N-оксида 4-нитрохинолина // ХГС. - 1996. - № 4. - C. 516-518.
12. Рыжаков А.В., Андреев В.П., Родина Л.Л. Молекулярные комплексы N-оксидов хинолинов и изохинолина с бромом // ЖОрХ. - 1996. - Т.32. - Вып.1. - C. 128-131.
13. Андреев В.П., Платонов А.В. Выделение и характеристика нового эндогенного низкомолекулярного ингибитора Na,K-ATPaзы из мозга крупного рогатого скота // Деп. ВИНИТИ, N1066-В97 от 02.04.97
14. Рыжаков А.В., Андреев В.П., Родина Л.Л. Молекулярные комплексы N-оксидов хинолинов, изохинолина и акридина с иодом // ЖОрХ. - 1998. - Т.34. - Вып.4. - C. 583-585.
15. Андреев В.П., Батоцыренова Е. Г., Рыжаков А.В., Родина Л.Л. Процессы внутримолекулярного переноса заряда в ряду стирильных производных N-оксидов пиридина и хинолина // ХГС. - 1998. - № 8.- C. 1093-1102.
16. Андреев В.П., Рыжаков А.В. Активация v-акцепторами реакций нуклеофильного замещения в N-оксиде 4-нитрохинолина // ХГС. - 1999. - № 11.- C. 1523-1527.
17. Андреев В.П., Тунина С.Г. Экстракция меди (II) и цинка (II) стирильными производными N-оксидов пиридина и хинолина // ЖОХ.- 2000. - Т.70.- Вып.4.- С.600-603.
18. Анисимов А.Г., Волкова Т.О., Чекмасова А.А., Андреев В.П. Взаимосвязь между апоптогенной активностью ряда производных хинолина и пиридина и их способностью ингибировать эритроидную дифференцировку клеток линии К 562 // Цитология. - 2000. - Т.42. - № 3. - С.258.
19. Рыжаков А.В., Нижник Я.П., Андреев В.П. Молекулярные комплексы N-оксида акридина // ЖОрХ.- 2000. - Т.36. - Вып.6. - C.918-920.
20. Тунина С.Г., Андреев В.П., Ершова Н.Ю., Нижник Я.П. Влияние природы катиона фонового электролита на экстракцию цинка N-оксидом хинолина из растворов бромидов щелочных металлов // ЖОХ. - 2000. - Т.70. - Вып.12. - С.1985 – 1989.
21. Андреев В.П., Нижник Я.П. Реакция N-оксида 4-нитрохинолина с хлоридом алюминия // ЖОрХ. - 2001. - Т.37. - Вып.1. - С.148 – 150.
22. Андреев В.П., Нижник Я.П. Взаимодействие 2,4-дибромхинолина с HCl // ЖОрХ. - 2002. - Т.38. Вып.1. - С.143-144.
23. Андреев В.П., Нижник Я.П., Тунина С.Г., Белашев Б.З. Донорно-акцепторные комплексы гетероароматических N-оксидов с хлоридами меди и цинка // ХГС. - 2002. - № 5. - C. 634-641.
24. Ivashevskaja S.N., Aleshina L.A., Andreev V.P., Nizhnik Y.P., Chernyshev V.V., Schenk H. Dichlorobis (2-methylquinoline N-oxide-O)zink (II) from powder data // Acta Cryst. - 2002. - C.58. - P.300-301.
25. Ivashevskaja S.N., Aleshina L.A., Andreev V.P., Nizhnik Y.P., Chernyshev V.V. Quinoline N-oxide dihydrate from powder data // Acta Cryst. - 2002. - E.58. - P.920-922.
26. Ivashevskaja S.N., Aleshina L.A., Andreev V.P., Nizhnik Y.P., Chernyshev V.V. Bis (-quinoline N-oxide-2O:O )bis[dichlorocopper (II) ], a power diffraction study // Acta Cryst. - 2002. - E.58. - P.721-723.
27. Ryzhakov A.V., Andreev V.P., Rodina L.L. Molecular complexes of heteroaromatic N-oxides and their reactions with nucleophiles // Heterocycles. - 2003. - V.60. - № 2. - P.419-435.
28. Андреев В.П., Тунина С.Г., Усов В.В., Ремизова Л.А. Экстракция цинка бромидом гепт-2-инилтриоктиламмония // ЖОХ. - 2003. - Т.73. - Вып.7. - С.1094-1098.
29. Ivashevskaja S.N., Aleshina L.A., Andreev V.P., Nizhnik Y.P., Chernyshev V.V., Schenk H. 4-(4’-Dimethylaminostyryl)pyridine N-oxide from powder data // Acta Cryst. - 2003. - E.59. - P.1006-1008.
30. Андреев В.П., Батоцыренова Е.Г., Данилова Л.А. Новые регуляторы активности Na+,K+-АТФазы природного и синтетического происхождения // Вестник Педиатрической Академии. СПб, вып.2. – 2004. С.71-74.
31. Rybakov V.B., Semenova T.A., Aleshina L.A., Andreev V.P., Nizhnik Y.P., Chernyshev V.V. Dichlorobis (2-methylquinoline N-oxide –O )-copper (II) // Acta Cryst. - 2004. - E.60. - P.901 - 903.
32. Рыжаков А.В., Андреев В.П. Координация N-оксидов пиридинов с катионами щелочных и щелочноземельных металлов в водной среде // ЖОХ. - 2005. - Т.75. -Вып.1.- С.133 – 136.
33. Андреев В.П., Тунина С.Г., Ремизова Л.А. Экстракция цинка и меди ацетиленовыми четвертичными аммониевыми основаниями // ЖОХ. - 2005. - Т.75. – Вып.5. - С.712 – 718.
34. Андреев В.П, Нижник Я.П., Безручко Д.Г., Морозов А.К. Экстракоординация Zn-тетрафенилпорфина с N-оксидами ряда пиридина, хинолина и акридина // ЖОХ. – 2005. - Т.75. – Вып.8. – С.1379 – 1387.
35. Андреев В.П., Корвачева Е.Г., Нижник Я.П. О влиянии N-оксидов пиридина и хинолина на активность Na,K-АТФазы микросом мозга крупного рогатого скота // Хим. Фарм. Ж. – 2006. – Т.40. – № 6. – С.96 – 97.
36. Фаворская И.А., Ремизова Л.А Андреев В.П., Гончаров В.П., Бабаян А.И., Маркина М.П. Ацетиленовые диамины в качестве ингибиторов кислотной коррозии стали // Авт. св. 1982. № 999479.
37. Фаворская И.А., Ремизова Л.А., Андреев В.П. Способ получения вторичных -ацетиленовых аминов // Авт. св. 1980. № 739065.
38. Ремизова Л.А., Андреев В.П., Фаворская И.А. Ацетиленовые амины // Тез. докл. IV Всероссийской конференции по химии ацетилена и его производных. Баку. 1979. С.86.
39. Ремизова Л.А., Андреев В.П., Фаворская И.А. Изомеризация третичных -ацетиленовых аминов под влиянием 3-аминопропиламида натрия. // Тез. докл. Всесоюзной конференции по развитию органического cинтеза. Ленинград. 1980. - С.133.
40. Andreev V.P., Korvachyova E.G., Rodina L.L. The activation of the nucleophilic substitution reaction by Bronsted and Lewis acids in the range of heteroaromatic N-oxides. // Book of abstracts. 11th International Conference of Organic synthesis ( ICOS-11 ). Amsterdam. The Netherlands. 1996. - P.452.
41. Anisimov A.G., Andreev V.P. Biological activity of some heteroaromatic N-oxide derivatives. // Book of Abstracts. International Workshop “ Results of Fundamental Research for Investments”. Third International Workshop “ Russian Technologies for Industrial Applications”. IWRFRI ‘ 99. St. Petersburg. 1999. - P.117-118.
42. Андреев В.П., Нижник Я.П. Активация нуклеофильного замещения в хинолиновом кольце v- и -акцепторами // Тез. докл. 1-ой Всероссийской конференции по химии гетероциклов памяти А.Н. Коста. Суздаль. 2000. - С.84.
43. Пяртман А.К., Андреев В.П., Кескинов В.А., Лищук В.В. Экстракция нитратов лантаноидов (III) и иттрия нитратом триоктил-2-гептиниламмония // Тез. докл. XIII Российской конференции по экстракции “Экстракция в гидрометаллургии, радиохимии, технологии неорганических веществ.“. Москва. 2004. Ч.1. - С.167
44. Yakubov S.P., Andreev V.P., Lebedeva N. Sh. Studing of blood croup metalloporphyrine interaction with heterocyclic N-oxide with the purpose of creation of the capable to inhibit erythroidal a differentiation of cells of line 562 medical products // European conference on calorimetry and thermal analysis for inviroment. Zakopane. Poland. 2005. - P.82.
45. Nizhnik Y.P., Andreev V.P. Molecular complexes of pyridine, quinoline and acridine N-oxides with electron acceptors (stable adducts and intermediates in SNAr reactions // Abstracts of International Conference on Organic Chemistry “Organic Chemistry since Butlerov and Belstein until present” Saint-Petersburg. 2006. P.616-617.
46. Андреев В.П., Нижник Я.П. N-Оксиды пиридинов, хинолинов и акридинов как потенциальные лекарственные препараты для нормализации активности Na,K-АТФазы // Тез. Межд. конф. по органической химии “Органическая химия от Бутлерова и Бельштейна до современности“. Санкт-Петербург. 2006. С.400-401.
47. Андреев В.П., Нижник Я.П. Основность и нуклеофильность стирильных производных N-оксидов пиридина и хинолина // Тез. Межд. конф. по органической химии “Органическая химия от Бутлерова и Бельштейна до современности“. Санкт-Петербург. 2006. С.402-403.
Рентгеноструктурные исследования проведены совместно с Л.А. Алёшиной (Петрозаводский государственный университет), В.В. Чернышёвым, В.Б. Рыбаковым, В.А. Тафеенко (Московский государственный университет имени М.В. Ломоносова), A. Szemik-Hojniak, L. Jerzykiewicz (Вроцлавский университет) и H. Schenk (Амстердамский университет), за что автор выражает им глубокую признательность.

