Определение некоторых биологически-активных веществ, основанное на эффекте сенсибилизированной флуоресценции в организованных средах
На правах рукописи
Неврюева Наталия Владимировна
Определение некоторых биологически-активных веществ, основанное на эффекте сенсибилизированной флуоресценции в организованных средах
02.00.02- аналитическая химия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата химических наук
Саратов – 2008
Работа выполнена в Саратовском государственно университете им. Н.Г. Чернышевского
Научный руководитель Доктор химических наук,
профессор Штыков С.Н.
Официальные оппоненты д.х.н., профессор Проскурнин М.А.
к.х.н., профессор Ястребова Н.И.
Ведущая организация Уральский государственный
Университет им. А.М. Горького
Защита состоится «2» июля 2008г в 1300 часов на заседании диссертационного совета Д 212.243.07 при Саратовском государственном университете им. Н.Г. Чернышевского по адресу:
410012, г. Саратов, ул. Астраханская, 83, СГУ, корп.1, химический факультет
С диссертацией можно ознакомиться в Научной библиотеке Саратовского государственного университета им Н.Г. Чернышевского
Автореферат разослан « » 2008г.
Ученый секретарь диссертационного совета Сорокин В.В.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Соединения, обладающие биологической активностью, например, различного рода антибиотики, аминокислоты, антикоагулянты и пестициды широко применяют в клинической практике и животноводстве в качестве лекарственных препаратов и добавок к кормам, а также в сельском хозяйстве для уничтожения вредителей. В связи с этим их содержание необходимо контролировать в биологических жидкостях, пищевых продуктах и объектах окружающей среды.
Одним из распространенных методов определения веществ данных классов является высокоэффективная жидкостная хроматография (ВЭЖХ). Её основные недостатки - относительно высокая стоимость аппаратуры, сложность её обслуживания и, вследствие этого, пока еще недостаточная распространенность метода в практике работы рядовых аналитических лабораторий.
Флуориметрическая аппаратура более проста в обращении, а флуоресцентный метод существенно более чувствителен. Однако количество интенсивно флуоресцирующих органических соединений невелико, в связи с чем необходимо развитие подходов, позволяющих увеличивать квантовый выход флуоресценции. Одним из таких подходов является метод сенсибилизированной флуоресценции с использованием некоторых лантаноидов. Он основан на переносе энергии электронного возбуждения с триплетного уровня органического лиганда (донор) на резонансный излучательный уровень иона лантаноида (акцептор), испускающего характерную для него флуоресценцию. Такой прием позволяет увеличить интенсивность аналитического сигнала и снизить предел обнаружения органических соединений.
Наличие в составе хелата с лантаноидом нескольких лигандов приводит к реализации эффекта «антенны», состоящего в одновременной передаче одному иону металла энергии электронного возбуждения нескольких доноров, а в ряде случаев и энергии других лигандов, входящих в состав смешаннолигандного комплекса. Дополнительным фактором, усиливающим эффект антенны, может быть солюбилизация хелата в наноразмерном объеме организованной системы, что способствует концентрированию компонентов реакции, повышению устойчивости хелатов и увеличению эффективности переноса энергии электронного возбуждения. Еще одним достоинством сенсибилизированной флуоресценции является возможность улучшения избирательности определений, поскольку перенос триплетной энергии может происходить только с триплетных уровней тех лигандов, энергия которых больше энергии излучательного уровня лантаноида.
Автор выражает благодарность к.х.н., доценту кафедры аналитической химии и химической экологии Саратовского государственного университета Т.Д.Смирновой за участие в обсуждении результатов и синтез реактивов.
Данная работа является частью плановых госбюджетных исследований кафедры аналитической химии и химической экологии, а также выполнялась в соответствии с проектами РФФИ № 04-03-32946а, 08-03-00725а и Госконтрактом 02.513.11.3028 Агентства по науке и инновациям.
Целью работы явилось применение эффектов переноса энергии и сенсибилизированной флуоресценции лантаноидов в организованных средах для разработки методов определения некоторых биологически-активных веществ в пищевых, биологических и природных объектах.
Для достижения цели необходимо было решить следующие задачи:
выявить системы лантаноид – лиганд, для которых реализуются эффекты переноса энергии и сенсибилизированной флуоресценции;
оценить влияние второго лиганда на сенсибилизированную флуоресценцию изучаемых систем;
изучить влияние организованных сред на собственную и сенсибилизированную флуоресценцию некоторых антибиотиков, антикоагулянтов и аминокислот и выбрать подход, обеспечивающий максимальный аналитический эффект;
изучить влияние природы и концентрации ПАВ, а также циклодекстринов на хроматографическое определение фторхинолонов;
разработать методики флуоресцентного определения антибиотиков, антикоагулянтов и аминокислот, основанные на сенсибилизированной флуоресценции лантаноидов в лекарственных формах, биологических, пищевых объектах и в почве.
Научная новизна
• получены данные о флуоресценции европия, тербия и гадолиния, сенсибилизированной представителями хинолонов, фторхинолонов, тетрациклинов, кумариновых антикоагулянтов, аминокислот, и влиянии на сенсибилизацию мицелл различных поверхностно-активных веществ (ПАВ);
• изучено влияние вторых лигандов на сенсибилизированную флуоресценцию указанных лантаноидов и установлено, что наибольший рост интенсивности флуоресценции наблюдается для второго лиганда, способного участвовать в переносе энергии к иону лантаноида;
• выяснено влияние природы и концентрации мицелл ПАВ и микроэмульсий на интенсивность сенсибилизированной флуоресценции европия, тербия и гадолиния в присутствии вторых лигандов, выбраны оптимальные условия её реализации и показана возможность применения эффектов для флуориметрического определения некоторых хинолонов, фторхинолонов, тетрациклинов, антикоагулянтов и аминокислот в виде смешаннолигандных хелатов c указанными лантаноидами;
• изучено влияние мицелл ПАВ на собственную флуоресценцию некоторых антибиотиков и антикоагулянтов, не способных сенсибилизировать лантаноиды, и найдены оптимальные условия их флуориметрического определения;
• проведено сравнение влияния организованных сред на основе мицелл ПАВ и циклодекстринов на определение флюмеквина методом жидкостной хроматографии и выявлены условия получения максимального аналитического сигнала.
Практическая значимость работы.
• Разработан подход, основанный на переносе энергии электронного возбуждения и эффекте антенны в системе хромофорный лиганд – ион лантаноида, вызывающий явление сенсибилизированной флуоресценции и позволяющий значительно уменьшить предел обнаружения веществ;
• разработаны методики флуориметрического определения оксолиниевой кислоты и доксициклина в плазме крови, флюмеквина – в плазме крови и мышечных тканях кур;
• проанализировано содержание норфлоксацина в лекарственных препаратах, доксициклина в лекарственной форме, разработанной в ЗАО «НИТА-ФАРМ»;
• разработана методика определения варфарина в почвах.
На защиту автор выносит:
• Результаты изучения сенсибилизированной флуоресценции европия, тербия и гадолиния с различными классами биологически-активных веществ;
• влияние второго лиганда на сенсибилизированную флуоресценцию в системе лантаноид- БАВ;
• влияние организованных сред на собственную флуоресценцию БАВ и сенсибилизированную флуоресценцию лантаноидов;
• методики определения антибиотиков хинолонового, фторхинолонового, тетрациклинового рядов и антикоагулянтов в биологических, фармацевтических, пищевых объектах и почве.
Апробация работы. Основные результаты работы должны на IV, V Всероссийских конференциях молодых ученых «Современные проблемы теоретической и экспериментальной химии» (Саратов, 2003, 2005); международной конференции молодых ученых и студентов в области оптики, лазерной физики и биофизики «Saratov Fall Meеting» (Саратов, 2005, 2006); VI Всероссийской конференции по анализу объектов окружающей среды «Экоаналитика-2006», (Самара, 2006); международной конференции по аналитической химии «IСAS-2006» (Москва, 2006), Всероссийских конференциях с международным участием «Аналитика России», (Краснодар, 2004, 2007); XVIII Менделеевском съезде по общей и прикладной химии (Москва, 2007); Российско-Украинско-Германском симпозиуме по аналитической химии «ARGUS'2007- Nanoanalytics», (Саратов, 2007).
Публикации. По материалам диссертации опубликована 21 работа, в том числе 4 статьи в журналах, из них 2 статьи в изданиях, рекомендованных ВАК, 6 статей в сборниках, 11 тезисов докладов
Объем и структура диссертации. Диссертационная работа изложена на 193 стр. машинописного текста, содержит 44 таблицы, 53 рисунка. Диссертация состоит из введения, 7 глав, выводов, списка использованной литературы и приложения. Библиография включает 191 источник.
КРАТКОЕ СОДЕРЖАНИЕ ДИССЕРТАЦИИ
Во введении обоснована актуальность темы, сформулированы цель и задачи исследования, изложены новизна, практическая значимость полученных результатов и основные положения, выносимые на защиту.
В главе 1 дано обобщение и систематизация литературных данных по современным методам определения антибиотиков, аминокислот и антикоагулянтов в лекарственных препаратах, биологических жидкостях, тканях и объектах окружающей среды, проанализированы их достоинства и недостатки.
В главе 2 описаны использованные в работе реактивы и оборудование. Объектами исследования явились биологически-активные вещества (БАВ) следующих классов: хинолоны, фторхинолоны, тетрациклины, кумарины, аминокислоты, а также соли редкоземельных элементов: нитраты европия, тербия, гадолиния.
Хинолоны
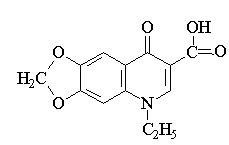 Оксолиниевая кислота (ОК) Оксолиниевая кислота (ОК) | 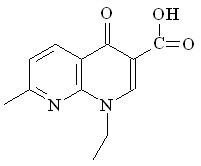 Налидиксовая кислота (НК) Налидиксовая кислота (НК) |
Фторхинолоны
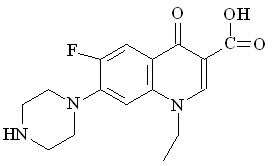 Норфлоксацин (НОР) Норфлоксацин (НОР) | 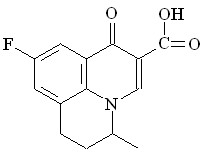 Флюмеквин (ФЛ) Флюмеквин (ФЛ) |
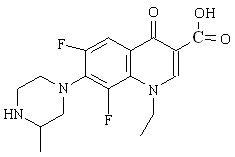 Ломефлоксацин (ЛФ) Ломефлоксацин (ЛФ) | 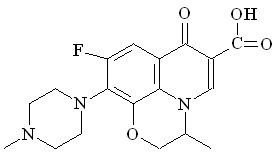 Офлоксацин (ОФ) Офлоксацин (ОФ) |
Тетрациклины

Доксициклин (ДЦ)
Аминокислоты
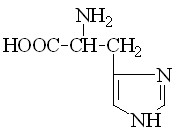 Гистидин (His) Гистидин (His) |  Пролин (Pro) Пролин (Pro) |
Антикоагулянты
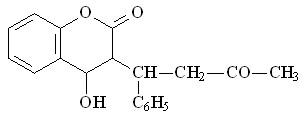 Варфарин (ВФ) Варфарин (ВФ) | 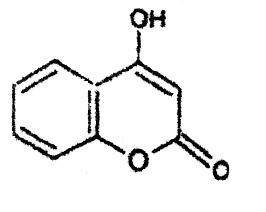 Оксикумарин (ОКМ) Оксикумарин (ОКМ) |
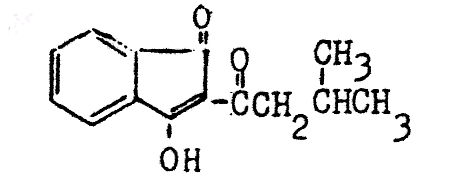 Куматетралил (КУМ) Куматетралил (КУМ) |
Содержание основного вещества БАВ составляло более 99 %.
В роли второго лиганда использовали 1,10-фенантролин (Фен), теноилтрифторацетон (ТТА), триоктилфосфиноксид (ТОФО), 2,9-диметил-дифенил-1,10-фенантролин (ДМДФФен), этилендиаминтетраксусной кислоты динатриевую соль (ЭДТА). Исследовали влияние анионных (додецилсульфат натрия (ДДС), додецилбензолсульфонат натрия (ДДБС)), катионных (бромид цетилтриметиламмония (ЦТАБ), хлорид цетилпиридиния (ЦПХ)) и 3 типов неионных (Тритон Х-100, Тритон Х-305, Твин-80, Бридж-35) ПАВ. В работе использовали молекулы-рецепторы -, - и - циклодекстрины.
Спектры флуоресценции регистрировали на флуориметре ФЛ-УХЛ-4 с источником возбуждения - галогенной лампой КГМ-12-100-2, при полностью открытой диафрагме в кварцевой кювете с толщиной слоя 1 см, а также на флуориметре «ФЛЮОРАТ–02-ПАНОРАМА», («ЛЮМЭКС», г. С.-Петербург) с импульсной лампой и на спектрометре СДЛ-1, («ЛОМО», г. С.–Петербург), с ксеноновой лампой. Сигнал регистрировали под углом 900 к возбуждающему свету. Оптическую плотность растворов и спектры поглощения получали на спектрофотометре СФ-46, («ЛОМО» г. С.-Петербург). Использовали кварцевые кюветы с длиной оптического пути 1 см (“Perkin-Elmer”).
Хроматографические исследования проводили на жидкостном хроматографе «Стайер» («Аквилон», Москва) с УФ- и флуориметрическим детекторами. Использовали колонки с обращенной фазой С18. Подвижные фазы содержали ацетатно-аммиачный буферный раствор и ацетонитрил.
В главах 3-7 приведены экспериментальные результаты.
Флуоресценция лантаноидов, сенсибилизированная БАВ
Показано (табл. 1), что все антибиотики и кумарины флуоресцируют. Из 20-ти аминокислот незначительной собственной флуоресценцией обладают только гистидин, пролин, тирозин, триптофан и фенилаланин. Все указанные лантаноиды образуют комплексы с БАВ, что подтверждается батохромным смещением на 10-15 нм максимумов их спектров поглощения.
Перенос энергии в комплексах европия и тербия с хинолонами, фторхинолонами, тетрациклинами, кумаринами и указанными аминокислотами наблюдается практически во всех случаях. Он сопровождается несколькими явлениями: перекрыванием спектра излучения донора со спектром поглощения акцептора (рис. 1); снижением интенсивности флуоресценции донора (лиганда) в присутствии акцептора (лантаноида); возникновением одновременно с тушением донора сенсибилизированной флуоресценции акцептора, что видно на примере системы альбумин (донор) – варфарин (акцептор) (рис. 2); соответствием величины убыли интенсивности флуоресценции донора и её роста для акцептора, а также условием ЕД > ЕА.
Сенсибилизированная флуоресценция, обусловленная переносом энергии, наблюдается не всегда и возможна, как правило, когда ЕД > ЕА и величина энергетической щели не очень велика (табл. 1). В соответствии с этим, сенсибилизация флуоресценции тербия обнаружена для всех видов антибиотиков. Для европия она характерна только для антикоагулянтов, норфлоксацина и доксициклина, причем для последнего эффект увеличения интенсивности флуоресценции существенно сильнее, поскольку триплетный уровень ДЦ (18100 см-1) расположен ближе к излучательному уровню европия (17260 см-1, 5D0 - 7F2 переход).
Для аминокислот сенсибилизированная флуоресценция свойственна только комплексам пролина и гистидина с Eu3+, Tb3+ и Gd3+. Интенсивность флуоресценции комплекса лантаноида с Pro возрастает по сравнению с собственной флуоресценцией аминокислоты в присутствии Tb3+ - в 9.0 раз, Eu3+ - в 1.8 раза.
Таблица 1. Кратность увеличения флуоресценции некоторых антибиотиков в присутствии ионов европия и тербия (в скобках значение энергии в см-1)
| Лантаноид | Антибиотики | Антикоагулянты | ||||||
| ФЛ | НОР | ОК | НК | ДЦ | ВФ | ОКМ | КУМ | |
| Tb3+ 20500 см-1 | 2 (21275) | 2 (21275) | 4 (20620) | 3.5 (22420) | 3 (18100) | 4.4 | 3 | 4 |
| Eu3+ 17260 см-1 | 2 | 1.3 | 6 | 5 | 5 | 2.5 | 1.5 | 1.7 |
кратность уменьшения флуоресценции лигандов
 | Рис.1. Нормированные спектры поглощения (1,3) и флуоресценции (2) Tb3+ (1), доксициклина (2), Eu3+ (3) (СДЦ=1.0·10-5 М, СEu3+=8.0·10-3 М, СTb3+ =2.0·10-3 М, рН 6.2) |
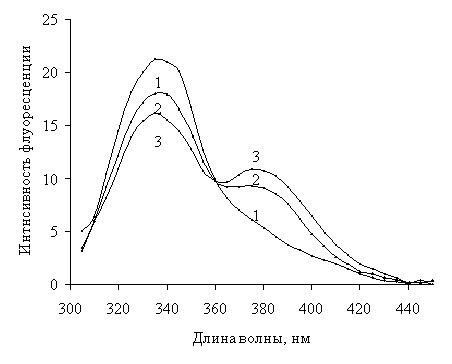 | Рис.2. Спектр флуоресцен-ции АБ в присутствии ВФ. САБ=5.0·10-5М 1.СВФ=1.0·10-7М, 2. СВФ=5.0·10-7М, 3. СВФ=1.0·10-6М |
Сенсибилизированная флуоресценция не обнаружена для антибиотиков ломефлоксацина и офлоксацина и, в случае тербия, для кумаринов. Таким образом, эффективность сенсибилизированной флуоресценции зависит от природы антибиотика, иона лантаноида, числа координированных лигандов и соотношения энергий триплетного уровня органического лиганда и излучательного уровня иона лантаноида.
Влияние второго лиганда на сенсибилизированную флуоресценцию лантаноидов
Введение второго лиганда в бинарные системы лантаноид – БАВ во многих случаях увеличивает интенсивность флуоресценции комплексов, т.е. сопровождается синергетическим эффектом. Этот эффект может быть результатом двух процессов: 1) замещения остаточных молекул воды (тушителей флуоресценции) в первой координационной сфере иона металла; 2) дополнительного переноса энергии возбуждения со второго лиганда на лантаноид (эффект «антенны»).
Антибиотики. Установлено, что наиболее эффективными вторыми лигандами для исследованных антибиотиков являются Фен и ТТА, которые дополнительно сенсибилизируют флуоресценцию лантаноидов (табл. 2). В присутствии ДМДФен, и ТОФО во всех системах выпадают осадки.
Из табл. 2 видно, что флуоресценция хелата Eu3+- ДЦ в присутствии ТТА выше, чем в присутствии Фен. Однако, диапазон определяемых концентраций ДЦ в системе Eu3+-ТТА меньше, что можно объяснить возможной конкуренцией ТТА по отношению к ДЦ при образовании хелата с ионом лантаноида. Отсутствие сенсибилизации теноилтрифторацетоном флуоресценции тербия объясняется близостью энергетических уровней лиганда (20660 см-1) и иона металла (20500 см-1), способствующей обратному переносу энергии возбуждения с акцептора на донор.
Таблица 2. Кратность увеличения интенсивности сенсибилизированной флуоресценции хелатов при добавлении второго лиганда
| Второй лиганд | I/I0 | ||||
| Eu3+- ДЦ | Tb3+- хинолон | Tb3+-фторхинолон | |||
| ОК | НК | НОР | ФЛ | ||
| Фен | 4 | 2 | 2 | 1.5 | 1.6 |
| ТТА | 5 | 1 | 1 | 1 | 1 |
| ЭДТА | 3 | 1.3 | 1.2 | 1 | 1 |
| Альбумин | 5 | - | - | - | - |
Известно, что роль синергетического агента в хелатах Eu3+ может выполнять биополимер - альбумин, содержащий в молекуле фрагмент триптофана, способного к комплексообразованию и передаче энергии возбуждения иону металла. Установлено, что флуоресценция хелата Eu3+-ДЦ в присутствии альбумина возрастает в 5 раз. Вклад в её увеличение может вносить также уменьшение доли безызлучательных потерь энергии при солюбилизации хелата Eu3+- ДЦ и изменение полярности его микроокружения в глобуле белка.
Антикоагулянты. Установлено, что для комплексов ВФ, ОКМ и КУМ с Eu3+ максимальное увеличение интенсивности флуоресценции в 20, 24 и 19 раз происходит в присутствии ТТА, а с Tb3+ – в 10, 4 и 2 раза, соответственно, в присутствии Фен (табл. 3). Влияние ЭДТА, роль которой сводится только к вытеснению остаточных молекул воды их координационной сферы металла, не столь значительно.
Таблица 3. Кратность увеличения интенсивности сенсибилизированной флуоресценции комплексов кумаринов при добавлении второго лиганда
| Комплекс | Второй лиганд | |||
| Фен | ТТА | ЭДТА | Аlb | |
| Eu3+-ВФ | 2 | 20 | 1.5 | 1.5 |
| Тb3+-ВФ | 10 | 1.5 | 2 | 1 |
| Eu3+-ОКМ | 2 | 24 | 2 | 1 |
| Тb3+-ОКМ | 4 | 1 | 1 | 1 |
| Eu3+- КУМ | 1 | 19 | 1 | 1 |
| Тb3+-КУМ | 2 | 1 | 2 | 1 |
Наиболее яркие эффекты сенсибилизированной флуоресценции получены на примере ВФ. В таблице 4 представлены метрологические характеристики флуориметрических методик определения ВФ по собственной флуоресценции, в присутствии АБ или ТТА, а также с помощью систем Tb3+–Фен и Eu3+–ТТА, из которой видно, что использование сенсибилизированной флуоресценции позволяют понизить предел обнаружения в 4, 28, 83 и 3800 раз, соответственно. В последнем случае предел обнаружения ВФ снижается до величины 5.210-10М. Такое поведение согласуется с ростом квантового выхода () флуоресценции системы.
Таблица 4. Пределы обнаружения и диапазоны линейности определения ВФ
| Система | I/I0 | Диапазон определяемых концентраций, М | Предел обнаружения, М | R2 | а | б | |
| ВФ | 1 | 5.010-6-5.010-4 | 2.010-6 | 0.943 | 0.25 | 2.37 | 0.32 |
| ВФ-ТТА | 2 | 1.010-7-1.010-4 | 7.210-8 | 0.976 | 0.28 | 3.09 | - |
| ВФ-АБ | 7 | 1.010-6 -1.010-4 | 5.110-7 | 0.983 | 0.33 | 4.26 | 0.56 |
| Tb3+-ВФ- Фен | 15 | 5.010-8-5.010-6 | 2.410-8 | 0.995 | 0.45 | 6.30 | 0.66 |
| Eu3+-ВФ- ТТА | 25 | 1.010-9-1.010-7 | 5.210-10 | 0.998 | 0.73 | 8.32 | 0.75 |
Аминокислоты. Для бинарного комплекса Eu3+ с Pro максимальная флуоресценция наблюдается в присутствии ТТА, который превышает собственную флуоресценцию аминокислоты в 18 раз и флуоресценцию бинарного хелата Eu3+-Pro в 5.5 раза. Интенсивность флуоресценции системы Tb3+ - Pro изменяется в присутствии добавок ТТА и Фен в 1.5 и 2 раза, соответственно. Сигнал сенсибилизированной флуоресценции в комплексе Gd3+-His-ТТА превышает флуоресценцию систем Eu3+-His-ТТА и Tb3+- His-Фен в 15.2 и 14.6 раз соответственно.
Можно предположить, что синергетический рост флуоресценции при добавлении таких вторых лигандов как ТТА и Фен связан с эффектом «антенны», вызывающим дополнительную сенсибилизацию флуоресценции лантаноида.
Влияние организованных сред на собственную флуоресценцию БАВ и сенсибилизированную флуоресценцию лантаноидов
Мицеллы ПАВ – смешаннолигандные комплексы. Основным типом исследованных организованных систем были мицеллы катионных, анионных и неионных ПАВ. Как видно из табл. 5, при их действии на сенсибилизированную флуоресценцию смешаннолигандных комплексов антибиотиков наблюдается дифференцирующий эффект. Так мицеллы анионных ПАВ тушат флуоресценцию хелатов Eu3+-ДЦ-Фен и Tb3+-ОК-Фен, а мицеллы катионных – наоборот, увеличивают её. Мицеллы неионных ПАВ сильно увеличивают флуоресценцию первого комплекса и не изменяют – второго. Влияние мицелл АПАВ может быть связано с разрушением хелатов в результате связывания иона металла отрицательно заряженной поверхностью анионной мицеллы, которая к тому же не связывает лиганды, имеющие тоже отрицательный заряд. В то же время ориентация солюбилизированных хелатов в мицеллах катионных ПАВ видимо такова, что положительно заряженная поверхность не разрушает хелаты. Хелат тербия с оксолиниевой кислотой и Фен, по-видимому, не солюбилизируется мицеллами неионных ПАВ.
Таблица 5. Влияние мицелл ПАВ на интенсивность флуоресценции смешаннолигандных хелатов европия и тербия с антибиотиками
| ПАВ | I/I0 | ||||
| Eu3+- ДЦ-Фен | Tb3+- НОР- Фен | Tb3+-ФЛ Фен | Tb3+-ОК-Фен | Tb3+-НК-Фен | |
| ДДС | тушение | 2.5 | 3.0 | тушение | 2.0 |
| ДДБС | тушение | 4 | 2.1 | тушение | 1.2 |
| ЦПХ | тушение | тушение | 2.4 | 1.4 | тушение |
| ЦТАБ | 2.5 | тушение | 1.2 | 4.2 | тушение |
| Тритон Х-100 | 7 | тушение | тушение | 1.0 | 1.0 |
| Бридж-35 | 6 | тушение | тушение | 1.0 | 1.2 |
| Твин -80 | 6 | тушение | тушение | 1.0 | 1.0 |
Интересно, что дифференцирование наблюдается даже для хелатов тербия с Фен и лигандами одного класса фторхинолонов – норфлоксацином и флюмеквином (табл. 5). Если мицеллы анионных ПАВ увеличивают флуоресценцию обоих хелатов, а мицеллы неионных тушат её, то катионные ПАВ действуют по-разному. Поскольку строение НОР и ФЛ отличается, можно предположить, что именно селективная солюбилизация лигандов является причиной разного влияния мицелл КПАВ. Особенностями солюбилизации можно объяснить и влияние мицелл на хелат тербия с налидиксовой кислотой и Фен, флуоресценция которого тушится мицеллами только катионных ПАВ, в отличие от хелата другого хинолона – оксолиниевой кислоты.
Метрологические характеристики определения хинолонов и фторхинолонов методом сенсибилизированной флуоресценции при проведении реакции в мицеллярных средах приведены в таблице 6. Видно, что интервал определяемых концентраций составляет от трех до пяти порядков, а пределы обнаружения находятся на уровне 10-8 –10-9 моля.
Изучено влияние мицелл ПАВ на флуоресценцию комплексов аминокислот в системах Gd3+–ТТА–His и Eu3+-Pro-ТТА. Установлено, что в мицеллярных растворах катионных ПАВ (ЦПХ, ЦТАБ) интенсивность флуоресценции смешаннолигандных комплексов Gd3+–ТТА–His и Eu3+-Pro-ТТА уменьшается соответственно в 1.8 и 2.3 раза. Анионный ПАВ - ДДС не оказывает влияния на флуоресценцию. Неионные ПАВ Тритон Х–100 и Бридж–35 увеличивают её интенсивность для Gd3+-His-ТТА и Eu3—Pro-ТТА в 2.2 и 25 раз и в 8.7 и 3.5 раз, соответственно. В связи с этим лучшим ПАВ для системы Gd3+-His-ТТА оказался Бридж-35 (рН 6.8-7.5), для Eu3—Pro-ТТА – Тритон Х-100 (рН 6.3-6.5).
Мицеллы ПАВ – собственная флуоресценция БАВ. Как упоминалось выше, для двух фторхинолонов – ломефлоксацина и офлоксацина, сенсибилизированная флуоресценция с лантаноидами не наблюдалась. В связи с этим нами исследовано влияние мицелл ПАВ на собственную флуоресценцию этих соединений. Установлено, что максимальное увеличение флуоресценции ЛФ наблюдается в присутствии ДДС, а ОФ - ЦПХ в 2.5 и 4 раза, соответственно, что может быть использовано для улучшения их флуориметрического определения. Таким образом, и для самих антибиотиков обнаружен дифференцирующий эффект.
Таблица 6. Метрологические характеристики определения хинолонов и фторхинолонов (pI=a·pC+b)
| Антиби-отик | Аналитическая система | Линейность градуировочного графика, М | а | b | ПрО, М |
| ФЛ | Tb3+-Фен-ДДС | 1.0·10-8 –1.0·10-3 | 0.39 | 7.07 | 6.2·10-9 |
| НОР | Tb3+-Фен -ДДБС | 1.010-8–1.010-3 | 0.35 | 3.54 | 3.110-9 |
| ОК | Tb3+-Фен- ЦТАБ | 1.010-7–1.010-4 | 1.20 | 9.42 | 7.010-8 |
| НК | Tb3+-Фен- ДДС | 5.0·10-8 – 8.0·10-5 | 0.8 | 4.4 | 2.8·10-8 |
| ДЦ | Eu3+-Фен-Тритон-Х-100 | 5.0·10-8 -5.0·10-5 | 0.47 | 5.4 | 2.2·10-8 |
| ЛФ | ЛФ-ЦПХ | 1.010-8-1.010-4 | 0.72 | 6.95 | 8.810-9 |
| ОФ | OФ-ДДС | 1.010-7-5.010-4 | 0.87 | 7.91 | 5.210-8 |
Установлено, что интенсивность собственной флуоресценции кумаринов возрастает в присутствии мицелл неионных, катионных и анионных ПАВ. Её максимальное увеличение (в 4-5 раз) наблюдается в мицеллярных растворах Тритона Х-100, однако диапазон определяемых содержаний уменьшается до одного порядка 5.010-5-5.010-4М. Установлено, что при добавлении АБ к водному раствору ВФ интенсивность флуоресценции возрастает в 7 раз.
Микроэмульсии. Влияние других представителей организованных систем – микроэмульсий изучали на примере системы Tb3+–ФЛ–ДМДФФен в микроэмульсиях состава ДДС/н-пентанол/н-октан/вода при переходе от структуры «масло в воде» к структуре «вода в масле». Установлено два эффекта:
- рост флуоресценции в обратной микроэмульсии масло/вода 80/20;
- высокая солюбилизирующая способность микроэмульсий, позволившая использовать в качестве второго лиганда такое гидрофобное соединение как ДМДФФен, добавки которого даже в мицеллярных растворах приводили к образованию осадков. Такое поведение микроэмульсий может быть связано с особенностью ее микрогетерогенной структуры и большой солюбилизирующей емкостью, что соответствует общим представлениям о свойствах микроэмульсий. Для хелата Tb3+–ФЛ–ДМДФФен подобраны оптимальные условия комплексообразования. Как видно из рисунка, в присутствии ДМДФФен интенсивность флуоресценции системы ФЛ– Tb3+ возросла в 1.7 раз по отношению к мицеллярному раствору, содержащему тот же анионный ПАВ – додецилсульфат натрия.
Циклодекстрины. Попытки использовать циклодекстрины для увеличения интенсивности собственной и сенсибилизированной флуоресценции рассмотренных ранее биологически-активных веществ не привели к успеху. Однако оказалось, что использование -ЦД при хроматографировании самих антибиотиков приводит к увеличению площади хроматографического пика в 2.3 раза и селективности хроматографирования, что положено в основу разработки более высокочувствительного метода определения флюмеквина. Применение других мицелл ПАВ оказалось менее эффективно, только для Тритона Х-100 площадь пика увеличилась практически в 2 раза. Использование -ЦД позволило снизить предел обнаружения ФЛ в 4.2 раза и значительно расширить интервал определяемых концентраций (табл. 7).
Таблица 7. Метрологические характеристики хроматографического определения ФЛ в отсутствии и присутствии в подвижной фазе –ЦД
| Организо- ванная среда | Диапазон определяемых концентраций, мкг/мл | ПрО, мкг/мл | Уравнение регрессии | R2 |
| - | 2.5 - 650 | 1.35 | y=3.90x+61.4 | 0.997 |
| -ЦД | 0.65 - 2500 | 0.32 | y=3.54x+201 | 0.999 |
Аналогичные зависимости установлены для кумаринов ОКМ и КУМ. Лучшей системой для их определения оказалась система Eu3+–ТТА, однако диапазон определяемых концентраций составляет лишь два порядка.
Определение биологически-активных веществ методом сенсибилизированной флуоресценции лантаноидов в мицеллярных растворах ПАВ
На основе проведенных исследований разработаны методики флуоресцентного определения антибиотиков, антикоагулянтов и аминокислот, основанные на сенсибилизированной флуоресценции лантаноидов в лекарственных формах, биологических, пищевых объектах и в почве.
Одной из таких методик явилось определение флюмеквина в плазме крови и мышечных тканях кур. Флюмеквин входит в лекарственные формы, разрабатываемые в ЗАО «НИТА-ФАРМ» (г. Саратов) для применения в птицеводстве. Флуориметрическое определение ФЛ по градуировочному графику в мясе курицы проводилось в присутствии мицеллярных и микроэмульсионных сред. Результаты определения ФЛ в мышечных тканях куриц после их трехдневного кормления представлены в таблице 8. Правильность определения в плазме крови контролировали методом «введено-найдено», а в тканях - методом ВЭЖХ с УФ- детектором по известной методике.
Таблица 8. Результаты определения флюмеквина в курином мясе (n = 3, P=0.95, tтабл = 4.30, Fтабл = 19.0)
| Образец | Найдено, мкг/мл | Sr | F | tэксп | ||||
| Флуориметрич. метод | ВЭЖХ | Флуориметрич. метод | ВЭЖХ | |||||
| 1 | 5.37±0.12 | 5.57±0.18 | 0.048 | 0.072 | 1.5 | 1.0 | ||
| 2 | 8.63±0.18 | 8.74±0.15 | 0.072 | 0.060 | 1.2 | 0.5 | ||
| 3 | 6.53±0.09 | 6.65±0.07 | 0.036 | 0.028 | 1.3 | 0.8 | ||
В лекарственных препаратах «Ренор», «Норбактин» и «Нолицин», с использованием сенсибилизированной флуоресценции тербия в присутствии второго лиганда Фен и мицелл ДДБС определено содержание норфлоксацина. Правильность контролировали методом добавок.
Разработаны методики флуориметрического определения ОКМ и ДЦ в плазме крови человека. Правильность контролировали методом «введено-найдено».
С целью изучения фармакокинетики доксициклина в ЗАО «НИТА-ФАРМ» проводили опытное вскармливание кур данным антибиотиком. Через определенное время, указанное в таблице 9, у подопытных отбирали пробы крови, в плазме которой определяли флуориметрическим методом содержание антибиотика по предложенной нами методике.
Таблица 9. Результаты определения доксициклина в плазме крови кур
| Однократно введенная концентрация ДЦ, мг/мл | |||
| 40мг/мл | 20мг/мл | 5мг/мл | |
| Время, мин | Найденная концентрация ДЦ, x ± х, мкг/мл | ||
| 30 | 0.07±0.01 | 0.06±0.01 | 0.16±0.01 |
| 60 | 3.77±0.47 | 0.23±0.03 | 0.60±0.02 |
| 180 | 1.13±0.06 | 1.34±0.08 | 0.41±0.05 |
| 240 | 0.47±0.02 | 0.39±0.02 | 0.34±0.02 |
| 360 | 0.24±0.01 | 0.32±0.01 | 0.20±0.05 |
| 480 | 0.19±0.01 | 0.24±0.01 | 0.12±0.01 |
Для подтверждения правильности результатов использовали известную методику определения методом ВЭЖХ с УФ-детектированием. Сопоставление результатов определения по F- и t- критериям (табл. 10) позволило установить отсутствие систематической погрешности в предлагаемой флуориметрической методике.
Таблица 10. Результаты определения доксициклина в плазме курицы
(Fтабл=19,2 при р=0.95; tтабл=4.30, n=3)
| Метод | Х± X, мкг/мл | Sr | Fэксп | tэксп |
| ВЭЖХ | 2.50±0.01 | 0.007 | 2.5 | 0.77 |
| Флуоримет-рический | 2.50±0.02 | 0.01 |
Актуальна также проблема определения ВФ в водах и почвах, поскольку это соединение может легко аккумулироваться в сельскохозяйственных культурах. Легко адсорбируемый почвой, богатой глиной и органическими остатками, ВФ может накапливаться в ней. Пробоподготовку почвы осуществляли по известной методике. Разработанная нами методика флуориметрического определения основана на использовании смешаннолигандного хелата Eu3+-ВФ-ТТА. Градуировочный график линеен в диапазоне концентраций 0.3-30 мкг/л. Стандартное отклонение определения Sr не превышало 0.025.
Выводы
- На примере биологически-активных веществ четырех классов органических соединений изучены условия реализации переноса энергии электронного возбуждения в системе лиганд-лантаноид, варфарин-альбумин и сенсибилизации флуоресценции европия, тербия и гадолиния, а также варфарина. Показано, что в указанных системах присутствуют основные признаки переноса энергии, такие как уменьшение флуоресценции донора и соответствующий ему рост флуоресценции акцептора, перекрывание спектра флуоресценции донора и спектра поглощения акцептора, бльшая величина энергии триплетного уровня донора по отношению к излучающему уровню акцептора. Выявлены соединения, не сенсибилизирующие флуоресценцию лантаноидов.
- Установлено, что в присутствии второго лиганда интенсивность флуоресценции бинарных хелатов лантаноидов с антибиотиками, антикоагулянтами, аминокислотами возрастает в 1.5 - 24 раз. Максимальный эффект увеличения флуоресценции наблюдается в присутствии лиганда, который способствует не только удалению из первой координационной сферы иона комплексообразователя остаточных молекул воды, но и участвует в процессе сенсибилизации иона металла. Указанный факт является следствием эффекта «антенны», состоящего в одновременной передаче энергии электронного возбуждения со всех лигандов на один излучающий ион лантаноида.
- Обнаружено дифференцирующее действие природы мицелл ПАВ на сенсибилизированную смешанными лигандами флуоресценцию лантаноидов, имеющее место даже внутри одного класса биологически-активных лигандов. Такое действие может быть связано с селективной солюбилизацией компонентов комплекса в мицелле, способствующей либо увеличению устойчивости комплекса, либо его разрушению. Мицеллы ПАВ существенно увеличивают интенсивность собственной флуоресценции ломефлоксацина и офлоксацина, которые не сенсибилизировали флуоресценцию лантаноидов. Показано, что бльшая солюбилизирующая способность микроэмульсий позволяет переводить в раствор и использовать в анализе высокогидрофобные системы, образующие осадки даже в мицеллярных растворах ПАВ.
- Выявлены условия проведения реакций и получены метрологические характеристики определения всех исследованных классов биологически-активных веществ, из которых следует, что метод сенсибилизированной флуоресценции позволил снизить пределы обнаружения веществ в десятки раз до уровня 10-8–10-10 М. Обнаружен уникальный эффект 3800-кратного снижения предела обнаружения варфарина по его сенсибилизированной флуоресценции в системе европий-варфарин-ТТА.
- Изучено влияние мицелл ПАВ и циклодекстринов на определение антибиотиков группы фторхинолонов и тетрациклинов методом ВЭЖХ с флуориметрическим детектором. Показано, что в ряде случаев при применении -циклодекстрина возможно двукратное увеличение площади хроматографического пика, позволяющее уменьшить предел обнаружения веществ в 3-4 раза и на несколько порядков увеличить интервал линейности градуировочного графика.
6. Разработаны методики флуориметрического определения флюмеквина – в плазме крови и тканях кур; доксициклина в плазме крови кур и лекарственной форме, разработанной в ЗАО «НИТА-ФАРМ»; оксолиниевой кислоты в плазме крови человека, найдено содержание норфлоксацина в трех лекарственных препаратах, предложена методика определения варфарина в почвах.
Основные публикации по теме диссертации
1. Штыков С.Н., Смирнова Т.Д., Былинкин Ю.Г., Калашникова (Неврюева) Н.В., Жемеричкин Д.А. Определение ципрофлоксацина и энрофлоксацина методом сенсибилизированной флуоресценции европия в присутствии второго лиганда и мицелл анионных ПАВ // Журн. аналит. химии. 2007. Т.62. №2. С.153-157.
2. Штыков С.Н., Калашникова (Неврюева) Н.В., Смирнова Т.Д., Жемеричкин Д.А. Флуориметрический метод определения норфлоксацина, основанный на явлении переноса энергии // Изв. вузов. Химия и хим. технол. 2006. Т.49. №7. С.27-30.
3. Штыков С.Н., Калашникова (Неврюева) Н.В., Смирнова Т.Д., Конюхова Ю.Г. Комплексы с переносом энергии в возбужденном состоянии в организованных средах для флуориметрического определения биологически активных веществ // Биомед. технол. и радиоэлектроника. 2006. № 12. С.4-9.
4. Shtykov S.N., Smirnova T.D., Kalashnikova (Nevrjueva) N.V., Bylinkin Y.G, Zhemerichkin D.A. Fluorescence in the system Eu(III) – oxytetracycline – co-ligand – sodium dodecylbenzene sulphonate micelles and its analytical application // Proс. SPIE. 2006. V.6165. P.61650Q1-6165Q6.
5. Неврюева Н.В., Штыков С.Н., Смирнова Т.Д., Криволапова Л.Ю., Ханина О.М. Флуориметрическое определение некоторых хинолонов с помощью хелатов тербия в организованных средах // Межвуз. сб. науч. трудов «Современные проблемы теорет. и эксперим. химии». Саратов, 2007. C.213-217.
6. Неврюева Н.В., Штыков С.Н., Смирнова Т.Д., Астахова Н.А. Сенсибилизированная флуоресценция хелатов лантанидов с пролином в мицеллярных растворах ПАВ // Межвуз. сб. науч. трудов «Современные проблемы теорет. и эксперим. химии». Саратов, 2007. С.217-219.
7. Неврюева Н.В., Штыков С.Н., Смирнова Т.Д., Фаррахова Л.В. Определение ломефлоксацина и офлоксацина флуориметрическим методом в присутствии мицелл поверхностно-активных веществ // Межвуз. сб. науч. трудов «Современные проблемы теорет. и эксперим. химии». Саратов, 2007. С.219-222.
8. Smirnova T.D., Nevrjueva N.V., Shtykov S.N. Effect of micelles and second ligands on Eu3+ and Tb3+ sensitized fluorescence determination of tetracycline and fluoroquinolone antibiotics based on energy transfer and antennа phenomenon // Proc. «Argus’2007-Nanoanalytics». Saratov, 2007. P.122-124.
9. Неврюева Н.В., Смирнова Т.Д., Штыков С.Н. Флуориметрическое определение биологически-активных веществ с помощью хелатов с переносом энергии в организованных средах // Тез. докл. «Аналитические методы и приборы для химического анализа». Санкт-Петербург, 2007. С.37-42.
10. Калашникова (Неврюева) Н.В., Богомолова И.В., Штыков С.Н., Смирнова Т.Д. Флуоресцентное определение флюмеквина в курином мясе // Межвуз. сб. науч. трудов «Современные проблемы теорет. и эксперим. химии». Саратов, 2005.С.161-164.
11. Былинкин Ю.Г., Калашникова (Неврюева) Н.В. Флуоресцентный метод определения норфлоксацина с использованием хелата Tb3+ в мицеллярных растворах ПАВ // Сб. науч. статей молодых ученых, посвященный 75-летию химического факультета «Современные проблемы теоретической и эксперим. химии». Саратов, 2004. С.115-119.
12. Хрячкова Е.С., Неврюева Н.В., Смирнова Т.Д., Штыков С.Н. Определение норфлоксацина методом сенсибилизированной флуоресценции РЗЭ в лекарственном препарате // Матер. XV Международ. конф. студентов, аспирантов и молодых ученых по фундам. наукам «Ломоносов-2008». Химия: Москва, 2008. С.78.
13. Shtykov S.N., Smirnova T.D., Kalashnikova (Nevrjueva) N.V. Fluorimetric determination of some 4-fluoroquinolone and tetracycline antibacterials based on the energy-transfer in micelles of surfactants // Intern. сonf. «Modern Physical Chemistry for Advanced Materials». Kharkiv, Ukraine, 2007. P.224-225.
14. Штыков С.Н., Неврюева Н.В., Смирнова Т.Д., Ханина О.М. Определение доксициклина флуоресцентным методом и ВЭЖХ с флуориметрическим детектором в организованных средах // XVIII Менделеевский съезд по общей и прикладной химии. Москва, 2007. Т.1. С.623.
15. Штыков С.Н., Смирнова Т.Д., Неврюева Н.В. Влияние организованных сред на эффективность переноса энергии в хелатах биологически активных веществ // XVIII Менделеевский съезд по общей и прикладной химии. Москва, 2007. Т.2. С.624.
16. Штыков С.Н., Неврюева Н.В., Смирнова Т.Д. Флуориметрический метод определения некоторых аминокислот с помощью хелатов лантанидов в организованных средах // Материалы II Всерос. конф. с междунар. участием «Аналитика России». Краснодар, 2007. С.484.
17. Штыков С.Н., Смирнова Т.Д., Неврюева Н.В. Комплексы с переносом энергии для определения биологически-активных веществ флуориметрическим методом // Материалы II Всерос. конф. с междунар. участием «Аналитика России». Краснодар, 2007. С. 177.
18. Shtykov S.N., Kalashnikova (Nevjueva) N.V., Smirnova T.D., Shishinina E. Flurorimertic determination of tetracycline based on the energy- transfer in micelles of surfactants // Intern. Congress Anal. Sci. “ICAS 2006”, Moscow, 2006. P.514.
19. Shtykov S.N., Smirnova T.D., Kalashnikova (Nevrjueva) N.V., E. Shishinina E. Lanthanide-sensitized spectrofluorimetric determination of some 4-fluoroquinolone antibacterials using organized media // Intern. Congress Anal. Sci. “ICAS 2006”, Moscow, 2006. P.514-515.
20. Штыков С.Н., Смирнова Т.Д., Калашникова (Неврюева) Н.В. Определение оксолиниевой кислоты с помощью сенсибилизированной флуоресценции в организованных средах в биологических жидкостях // VI Всерос. конф. по анализу объектов окруж. среды «Экоаналитика-2006». Самара, 2006. С.304.
21. Былинкин Ю.Г., Штыков С.Н., Смирнова Т.Д., Жемеричкин Д.А., Калашникова (Неврюева) Н.В. Определение производных фторхинолонов методом сенсибилизированной флуоресценции // Всерос. конф. по аналит. химии «Аналитика России». Москва, 2004. С.137-138.

