Синтез новых производных 4- и 5-аминоизоксазолов
На правах рукописи
СЕМЕНЫЧЕВ
Евгений Вадимович
СИНТЕЗ НОВЫХ ПРОИЗВОДНЫХ 4- И 5-АМИНОИЗОКСАЗОЛОВ
Специальность 02.00.03 – Органическая химия
А В Т О Р Е Ф Е Р А Т
диссертации на соискание ученой степени
кандидата химических наук
Иваново
2011
Работа выполнена в Научно-образовательном центре «Инновационные исследования» Государственного образовательного учреждения высшего профессионального образования «Ярославский государственный педагогический университет им. К.Д. Ушинского»
| Научный руководитель: | доктор химических наук, профессор Ясинский Олег Анатольевич |
| Официальные оппоненты: | доктор химических наук, профессор Клюев Михаил Васильевич доктор химических наук, доцент Герасимова Нина Петровна |
| Ведущая организация: | ГОУ ВПО «Тульский государственный педагогический университет им. Л.Н. Толстого» |
Защита состоится « » 2011 года в часов на заседании диссертационного совета Д 212.063.01 при Ивановском государственном химико-технологическом университете по адресу: 153000, г. Иваново, пр. Ф. Энгельса, д. 7.
Тел. 8 (4932) 32-54-33. Факс: 8 (4932) 32-54-33. E-mail: [email protected]
С диссертацией можно ознакомиться в информационном центре Государственного образовательного учреждения высшего профессионального образования «Ивановский государственный химико-технологический университет» по адресу: 153000, г. Иваново, пр. Ф. Энгельса, д. 10.
Автореферат разослан « » 2011 г.
| Ученый секретарь диссертационного совета |  | Е.М. Кувшинова |
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Развитие теоретических представлений и накопление прикладных знаний о химии гетероциклических соединений является важной задачей современной органической химии в связи с динамичным развитием индустриальных технологий получения разнообразных синтетических продуктов, имеющих большой потенциал практического применения. Использование гетероцикических соединений в прикладных исследованиях обусловлено огромным количеством возможностей структурного разнообразия и высокой статистической вероятностью проявления биологической активности. В частности, производные изоксазола с каждым годом находят всё более широкое применение в качестве объектов для фармакологических исследований и, как результат, в качестве коммерчески доступных лекарственных препаратов.
С этой точки зрения весьма интересным представляется дальнейшее развитие химии производных изоксазола, в частности, синтез новых соединений, содержащих карбоксамидные и сульфамидные фрагменты. Из литературы известно, что амиды являются перспективными биологически активными веществами – антиметаболитами, перенацеливающими на себя атаки бактерий при заболеваниях. Очевидно, что все новые вещества, сочетающие в своей структуре изоксазольный цикл и амидные фрагменты, имеют терапевтическую актуальность, потому их синтез является важной задачей органической химии.
Данная работа является частью исследований, проведенных в Научно-образовательном центре «Инновационные исследования» ГОУ ВПО «Ярославский государственный педагогический университет им. К.Д. Ушинского» в период с 2007-2010 годов в рамках двух Государственных контрактов: № 02.527.11.9002 «Разработка серии высокоэффективных клинических кандидатов для лечения инфекционных заболеваний на основе новых механизмов действия с применением технологий комбинаторного синтеза и высокопроизводительного скрининга» (Заказчик – Министерство образования и науки РФ) и № 02.740.11.0092 «Проведение комплексных научных исследований по разработке методов синтеза и получению новых органических соединений, обладающих потенциальной биологической активностью и являющихся перспективными кандидатами для создания лекарственных средств» (Заказчик – Министерство образования и науки РФ).
Цель работы. Разработка методов синтеза новых гетероциклических соединений – производных аминоизоксазола, отличающихся большим химическим разнообразием и рассматривающихся в качестве потенциальных объектов для дальнейших биомедицинских исследований.
Научная новизна. Разработка подходов к синтезу и последующим превращениям новых двуядерных соединений, содержащих 5-аминоизоксазольный фрагмент, а именно 3-гетерил-5-аминоизоксазолов, 4-арил-5-аминоизоксазолов. Установление факта диацилирования производных 4-арил-5-аминоизоксазолов с образованием соответствующих N,N-дизамещенных карбоксамидов в ходе реакции ацилирования и последующего селективного гидролиза одной из ацетильной групп. Разработка нового подхода активации дезактивированной аминогруппы в 3-гетерил-5-аминоизоксазолах с последующей карбоксамидной и сульфамидной функционализацией данной системы. Получение неизвестных ранее 3-метил-4-амино-5-винилизоксазолов конденсацией соответствующих 4-нитропроизводных 3,5-диметилизоксазола с ароматическими и гетероциклическими альдегидами с последующим восстановлением нитрогруппы. Амидная сульфофункционализация производных 4-арил-5-аминоизоксазолов и 3-метил-4-амино-5-винилизоксазолов с установлением точного положения сульфогруппы. Установление факта перегруппировки диметил-[2-(3-метил-4-нитроизоксазол-5-ил)-винил]-амина в 3-амино-2-метил-1Н-пиридин-4-он в условиях каталитического восстановления и доказательство структуры образующегося продукта. Сделан прогноз возможной биологической активности синтезированных соединений.
Практическая значимость работы. В ходе проведенных исследований нами были разработаны новые подходы к синтезу производных аминоизоксазолов, применены новые методики активирования аминогруппы в 3-гетерил-5-аминоизоксазолах, а также проведена функционализация полученных систем до соответствующих амидов.
Апробация работы и публикации. По материалам диссертации опубликованы 4 научные статьи и 6 тезисов докладов научных конференций. Результаты работы были доложены на международной конференции «Основные тенденции развития химии в начале XXI-ого века», посвященной 175-летию со дня рождения Д.И. Менделеева и 80-летию создания химического факультета Санкт-Петербургского университета, Санкт-Петербург, на III Международной конференции по химии гетероциклических соединений, посвященной 95-летию со дня рождения профессора А.Н. Коста, Москва, 17-21 октября 2010 г и других конференциях.
Положения, выносимые на защиту.
Синтез 3-гетерил- и 4-арил-5-аминоизоксазолов, способность данных соединений к последующей амидной и сульфамидной функционализации.
Синтез 3-метил-4-амино-5-винилизоксазолов из соответствующих нитропроизводных, содержащие разнообразные производные при винильном фрагменте и реализация возможностей структурного разнообразия данных соединений.
Применение нового метода функционализации дезактивированной системы 3-гетерил-5-аминоизоксазолов.
Теоретическое определение способности синтезированных соединений проникать через гематоэнцефалический барьер.
Структура работы. Диссертация состоит из введения, литературного обзора, химической и экспериментальной частей, выводов и списка литературы. Работа изложена на 135 страницах и включает 67 схем, 18 рисунков и 1 таблицу. Список литературы насчитывает 171 источник.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
В литературном обзоре рассмотрены химические свойства изоксазольного цикла, а именно реакции нуклеофильного и электрофильного замещения, трансформации изоксазола в другие гетероциклические системы. Литературный обзор включает также ссылки на литературу о применении производных изоксазола. Приведены сведения о принципах нейронно-сетевого моделирования и построения карт Кохонена.
1. Синтез молекулярных систем, содержащих структурный фрагмент 5-аминоизоксазол, и их функционализация
Синтез 4-арил-5-аминозамещенных производных изоксазола является одним из менее изученных направлений химии изоксазола. При этом, благодаря наличию нескольких реакционных центров, данная система обладает большим потенциалом для различной функционализации. В связи с повышенным в последние годы интересом со стороны фармакологической индустрии к сульфамидным соединениям разработан подход к синтезу новых амидных и сульфамидных производных 4-арил-5-аминоизоксазолов.
При проведении последовательных реакций сложноэфирной конденсации с участием различных бензилцианидов 1 и эфиров карбоновых кислот в присутствии гидрида натрия, и циклоконденсации кетонитрилов 2 при взаимодействии с гидроксиламином были получены соответствующие 3-алкил-4-арил-5-аминоизоксазолы 3 с выходами более 85 % (схема 1).
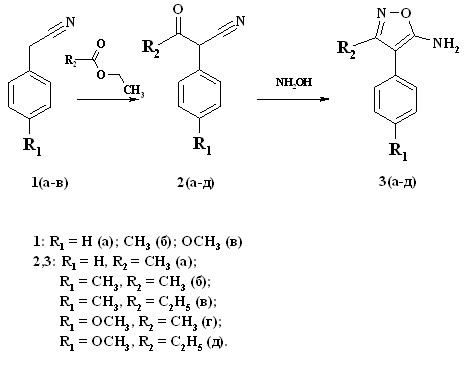
Схема 1
Обнаружено, что в соединениях 3 аминогруппа активна по отношению к ацилирующим агентам. Так, при взаимодействии аминов 3 с ацетилхлоридом при комнатной температуре в течение 12 ч были получены амиды 4. Кроме того, установлено, что при проведении аналогичной реакции при более высокой температуре единственным продуктом реакции был диацилированный продукт 5. Также было выявлено, что при нагревании соединения 5 в 10 %-ном растворе щелочи за 30 мин происходит отщепление одной ацетильной группы (схема 2).
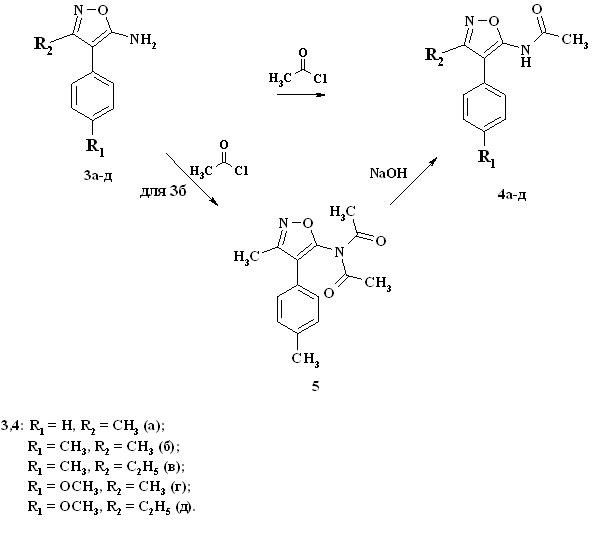
Схема 2
При нагревании соединений 4 в смеси хлорсульфоновой кислоты и хлористого тионила были получены соответствующие сульфохлориды 6, которые активно взаимодействовали с различными первичными и вторичными ароматическими и гетероциклическими и алифатическими аминами при нагревании в ацетонитриле в присутствии избытка пиридина, с образованием соответствующих сульфамидов 7 (схема 3 и 4).
С помощью метода 1Н ЯМР-спектроскопии было изучено положение электрофильной атаки при сульфохлорировании. В случае соединений 4а замещение протекало в пара-положение по отношению к изоксазольному гетероциклу (схема 3). Так, на ЯМР-спектрах в области 7-8 м.д. характерно наличие двух дублетов с КССВ 8.2 Гц, что соответствует нахождению сульфогруппы в пара-положении.

Схема 3
В случае нахождения в пара-положении к изоксазольному циклу алкильного или алкоксильного заместителя сульфохлорирование протекало в орто-положение к этому заместителю (схема 4).
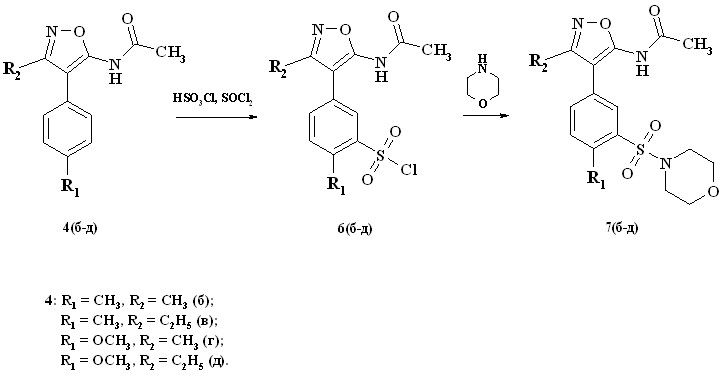
Схема 4
На ЯМР-спектрах соединений 6(б-д) и 7(б-д) в области 7.06-7.94 м.д. характерно наличие АВХ-системы взаимодействия протонов (двух дублетов и одного синглета), что соответствует двум протонам, находящимся в орто-взаимодействии друг с другом и одному протону, находящемуся в мета-взаимодействии с одним из них.
Для синтеза 3-гетерил-5-амиизоксазолов 10 был использован метод, аналогичный методу синтеза 4-арил-5-аминозамещенных производных изоксазола. В качестве исходных продуктов для данного синтеза использовали эфиры пиридин-, тиофен-, и фуранкарбоновых кислот 8 (схема 5).
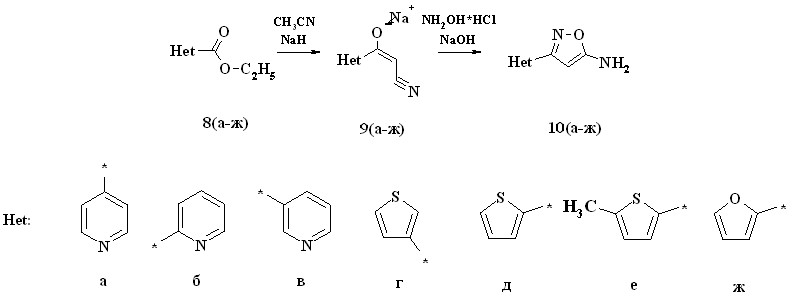
]
Схема 5
Наличие аминогруппы в соединениях 10 определяло направление их дальнейшей сульфамидной и карбоксамидной функционализации. Соответствующие сульфамиды 11 получали путем взаимодействия продуктов 10 с сульфохлоридами различного строения (схема 6).
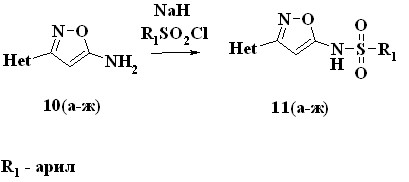
Схема 6
Получить карбоксамиды 12 путем взаимодействия 10 по известным методикам с хлорангидридами или имидазолидами ароматических карбоновых кислот не удалось. Для их получения был применен метод, являющийся вариацией методики получения карбоксамидов через N,N-карбодиимидазол (КДИ), и заключающийся во взаимодействии соединений 10 с имдазолидами карбоновых кислот в диоксане в присутствии эквивалентного количества гидрида натрия (схема 7).

Схема 7
Очевидно, что аминогруппа в данном случае является недостаточно основной для ацилирования имидазолидами кислот и, в этой связи, роль гидрида натрия сводится к повышению нуклеофильности азотного реакционного центра аминогруппы.
2. Синтез 3-метил-4-амино-5-винилизоксазолов и их амидная и сульфамидная функционализация
Получение соответствующих 3,5-диметил-4-нитроизоксазола 14 осуществляли путем нагревания 3,5-диметилизоксазола в смеси концентрированных серной и азотной кислот до 130 °C. Вследствие сильно выраженных электорноакцепторных свойств нитрогруппы, активируется 5-метильный заместитель в реакциях конденсации с ароматическими и гетероциклическими альдегидами (схема 8). Несмотря на возможность образования двух изомерных продуктов по 3- и 5- метильной группе, согласно данным ЯМР-спектроскопии, реакция протекала селективно. Это обусловлено тем, что при резонансной стабилизации промежуточный 5-карбанион более стабилен, чем 3-карбанион (рис. 1), исходя из чего, можно сделать вывод, что 15(а-г) являются соответствующими 5-винилзамещенныи производными.
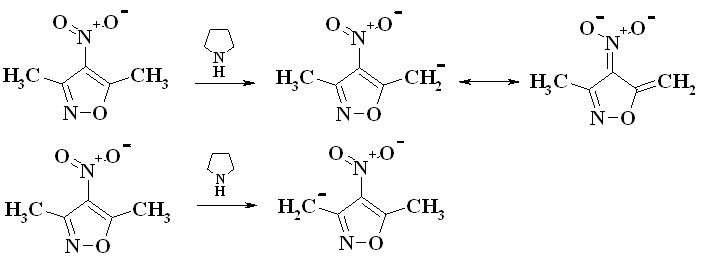
Рисунок 1 - Резонансная стабилизация 3,5-диметил-4-нитроизоксазола
Получение нитровинилизоксазолов 15(а-г) проводили в этаноле с добавлением каталитического количества пирролидина.
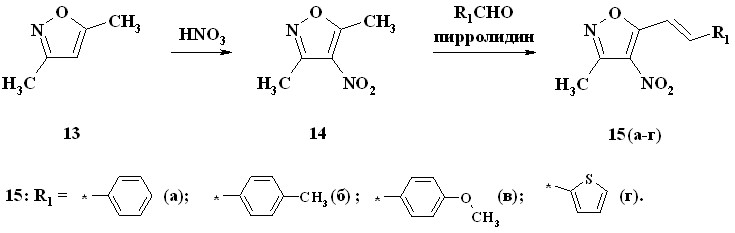
Схема 8
Восстановление нитрогруппы соединений 15 осуществляли хлоридом олова (II) в смеси ДМФА и концентрированной соляной кислоты при температуре 80 °С, после чего смесь выливали в воду и подщелачивали раствор до выпадения осадка нужного амина (схема 9).
Также для восстановления нитрогруппы нами было опробовано несколько других восстановительных систем, таких как: цинк-уксусная кислота, циклогексен-Pd/C, гидразин гидрат-никель Ренея. Данные системы себя не оправдали вследствие низких выходов целевых продуктов (не больше 10-15 %), а в случае с гидразин гидратом происходило раскрытие изоксазольного цикла.
Для ацилирования аминогруппы применяли ангидриды и хлорангидриды карбоновых кислот с образованием соответствующих карбоксамидов 17.
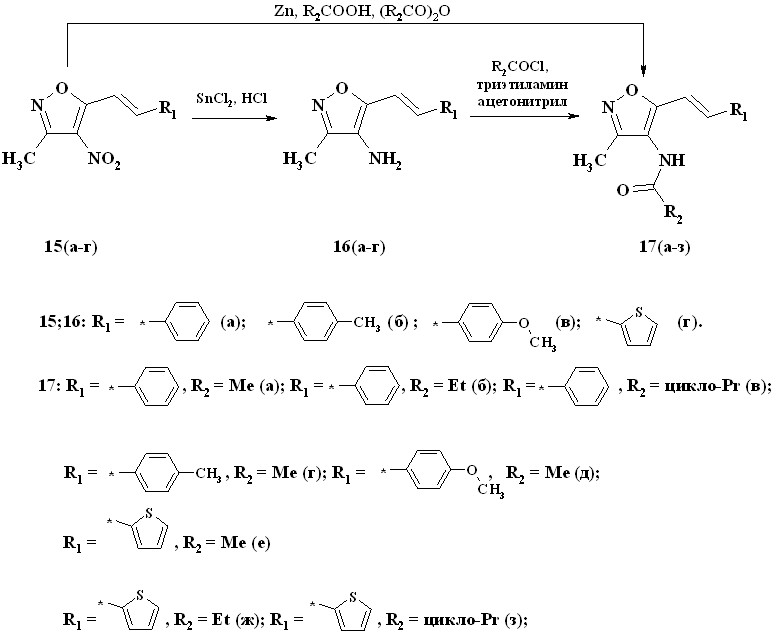
Схема 9
При взаимодействии аминов 16 с арилсульфохлоридами в условиях реакции Шоттена-Баумана при использовании в качестве основания пиридина, были получены ожидаемые сульфамиды 18. В случае же использования триэтиламина, реакция приводила к селективному образованию продуктов дизамещения 19 (схема 10).
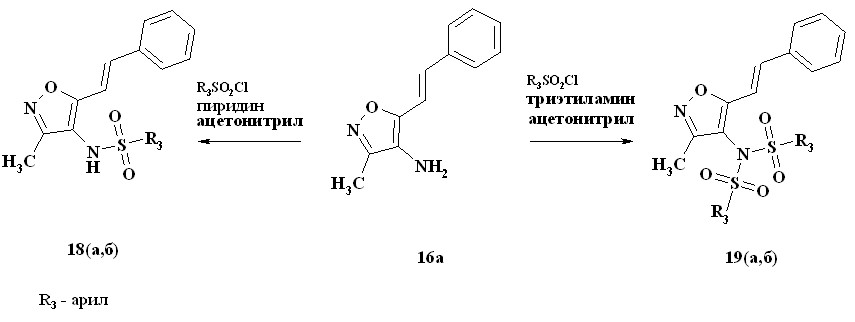
Схема 10
Другой вариант сульфамидной функционализации был осуществлен путем сульфохлорирования соединений 17 и последующего сульфамидирования с морфолином в присутствии пиридина с образованием соответствующих сульфамидов 21, 23, 25 (схема 11,12,13).

Схема 11
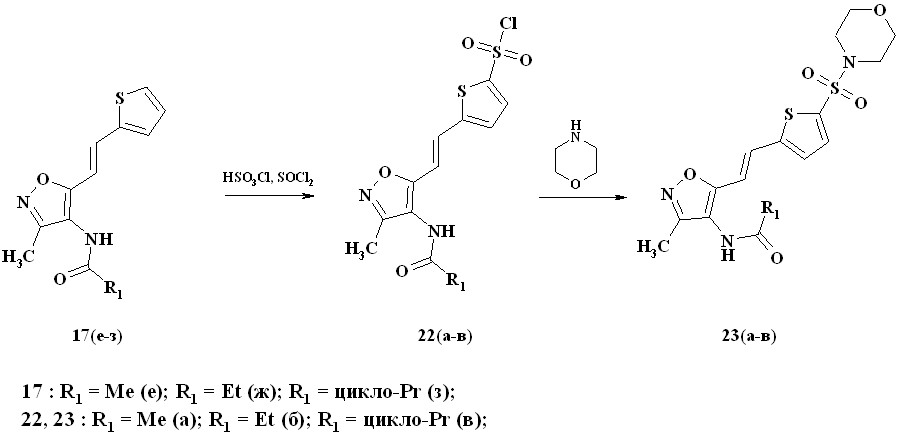
Схема 12
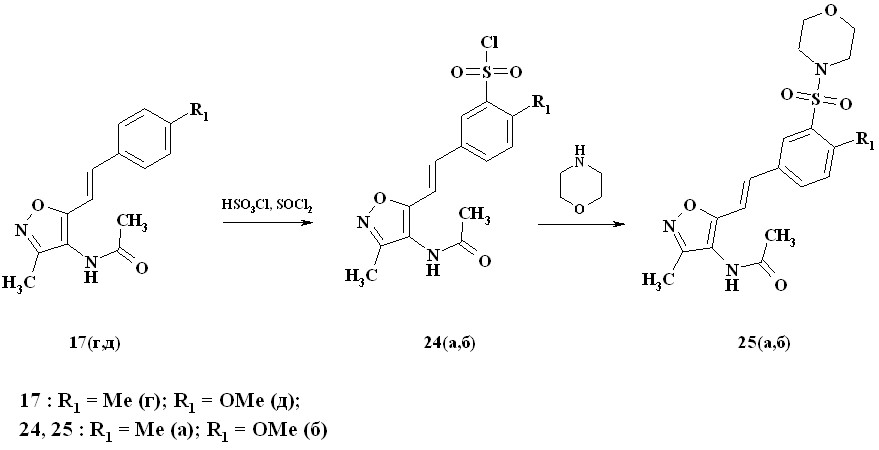
Схема 13
Во всех трех случаях сульфохлорирование протекает региоселективно, без образования других возможных изомеров. Строение полученных соединений подтверждено данными 1Н ЯМР-спектроскопии, масс-спектрометрии и данными элементного анализа.
При взаимодействии соединения 14 с диметилацеталем диметилформамида в ДМФА был выделен 5-енаминзамещенный изоксазол 26. После его восстановления водородом на палладиевом катализаторе вместо ожидаемого продукта 27 было выделено индивидуальное, по данным жидкостной хроматографии, соединение. На ПМР-спектре данного соединения наблюдается исчезновение двух дуплетов с КССВ 13,7 Гц. Вместо них в области 5,96 и 7,19 м.д. появляются два дуплета с КССВ 6,4 Гц. Так же на спектре характерно наличие двух уширенных синглетов – в области 4,18 м.д., соответствующий двум протонам, и в области 11,3 м.д., соответствующий одному протону. На 13С ЯМР-спектре в области 168,4 м.д. характерно наличие сигнала карбонильного углерода. Из совокупности данных анализа для выделенного продукта было предложено строение соединения 28 (схема 14).
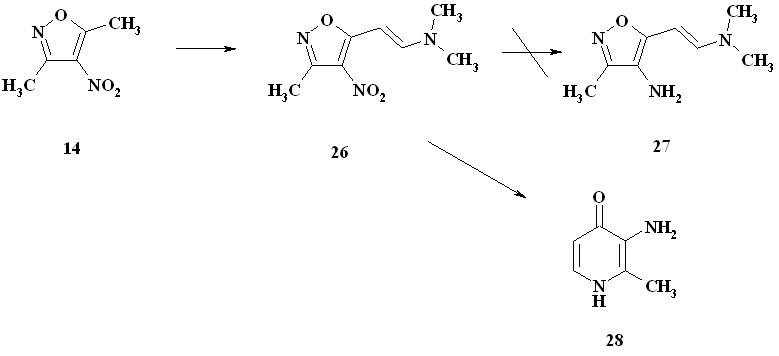
Схема 14
Для проверки достоверности предположенной структуры были сделаны анализы ЯМР-спектроскопии с использованием двухмерных гомоядерных (Н,Н) и гетероядерных (Н,С) методик. Предположенная структура продукта 28 подтвердилась совокупностью данных 1H-ЯМР, 13С-1H-ЯМР и NOESY спектроскопий, а также данными элементного анализа.
3. Прогнозирование потенциальной биоактивности производных аминоизоксазолов.
На основе принципов нейронно-сетевого моделирования и построения карт Кохонена с использованием программы Smart Mining v1.01 было проведено прогностическое исследование для выявления значимых фармакокинетичских свойств широкого спектра производных аминоизоксазолов, синтез которых может быть реализован на основании подходов, изложенных в разделах 1,2. Анализ карт Кохонена позволил выявить конкретные соединения из генерированных виртуальных библиотек А-Г (рис.2), проявляющих высокую степень проникаемости через гематоэнцефалический барьер.
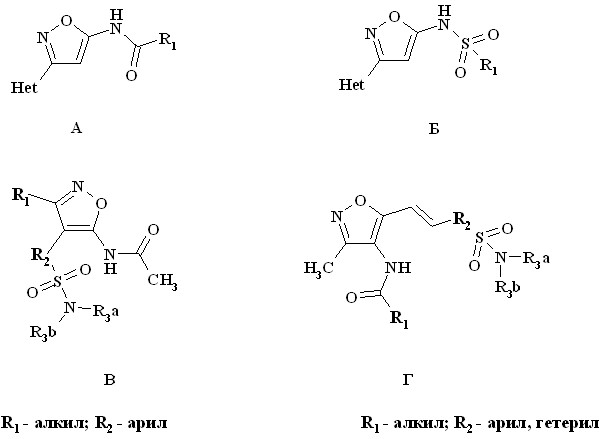
Рисунок 2 – Общие формулы виртуальных комбинаторных библиотек карбоксамидных и сульфамидных производных изоксазола
Для каждого соединения каждой комбинаторной библиотеки были рассчитаны значения основных молекулярных дескрипторов, после чего объекты библиотек А-Г наносились на карту Кохонена тренирующих выборок. Из полученных данных установлено, что абсолютной проникаемостью через ГЭБ обладают 527 из 966 соединений комбинаторной библиотеки А, 74 из 510 соединеий комбинаторной библиотеки Б, а в комбинаторных библиотеках В и Г ни одно из веществ не обладает абсолютной проникающей способностью через гематоэнцефалический барьер.
Исходя из полученных результатов, можно сделать вывод о том, что наиболее подходящими кандидатами для создания препаратов, воздействующих на ЦНС, являются карбоксамидные и сульфамидные производные 3-гетерил-5-аминоизоксазолов. Производные 4- и 5-аминоизоксазолов, а также производные 3-гетерил-5-аминоизоксазолов, не показавшие высокой проникающей способности, могут быть рекомендованы для исследований других типов биологической активности, например, антиинфекционной, так как удовлетворяют всем современным требованиям, предъявляемым к потенциальным биологически активным веществам.
ВЫВОДЫ
- На основе реакции циклоприсоединения гидроксиламина с различными кетонитрилами синтезированы двуядерные соединения, содержащие 5-аминоизоксазольный фрагмент и различные ароматические и гетероциклические фрагменты в положении 3- изоксазольного цикла (3-гетерил-5-аминоизоксазолы), в положении 4- изоксазольного цикла (4-арил-5-аминоизоксазолов).
- Разработан метод синтеза 3-алкил-4-амино-5-винилизоксазолов, основанный на реакции нитрования 3,5-диметилизоксазола, региоселективной конденсации 4-нитро-3,5-диметилизоксазолов с ароматическими и гетероциклическими альдегидами, с последующим восстановлением нитрогруппы до аминогруппы.
- Обнаружено, что при взаимодействии 3-метил-4-п-толилизоксазол-5-иламина с избытком ацетилхлорида единственным продуктом является N-ацетил-N-(3-метил-4-п-толилизоксазол-5-ил)-ацетамид. Установлено, что при нагревании N-ацетил-N-(3-метил-4-п-толилизоксазол-5-ил)-ацетамида в растворе щелочи протекает селективный гидролиз одной ацетильной группы с образованием N-(3-метил-4-п-толилизоксазол-5-ил)-ацетамида.
- Разработан новый метод синтеза амидных производных 3-гетерил-5-аминоизоксазолов через имидазолиды кислот в присутствии эквивалентного количества гидрида натрия.
- На основе полученных 4-арил-5-аминоизоксазолов, 3-метил-4-амино-5-винилизоксазолов были получены соответствующие карбоксамиды, а также синтезирован ряд ранее не известных сульфохлоридов и соответствующих сульфамидных производных. Положение сульфогруппы установлено с помощью с помощью метода спектроскопии 1Н ЯМР.
- Совокупностью данных физико-химического анализа доказан факт перегруппировки диметил-[2-(3-метил-4-нитроизоксазол-5-ил)-винил]-амина в 3-амино-2-метил-1Н-пиридин-4-он в условиях каталитического восстановления.
- В результате исследования проникаемости веществ через гематоэнцефалический барьер с помощью карт Кохонена, составлен прогноз потенциальных типов биологической активности для изучаемых производных аминоизоксазолов.
ПУБЛИКАЦИИ, ОТРАЖАЮЩИЕ ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ:
- Новожилов Ю.В. Синтез сульфамидов, содержащих структурный фрагмент 5-винилизоксазола / Новожилов Ю.В., Корсаков М.К., Семенычев Е.В. и др. // Изв. вузов. Химия и химическая технология. – 2009. – Т. 52. Вып. 5. – С. 19-25.
- Семенычев Е.В. Синтез сульфамидных производных 4-арилизоксазола / Семенычев Е.В., Корсаков М.К., Новожилов Ю.В. и др. // Изв. вузов. Химия и химическая технология. – 2009. – Т. 52. Вып. 5. – С. 61-66.
- Семенычев Е.В. Синтез 3-гетерил-5-аминоизоксазолов и их амидных и сульфамидных производных / Семенычев Е.В., Корсаков М.К., Ясинский О.А. и др. // Химическая технология. – 2010. №8. – С. 484-489.
- Семенычев Е.В. Синтез новых производных изоксазола на основе реакции переаминирования и изучение ее кинетических особенностей / Семенычев Е.В., Корсаков М.К., Дорогов М.В. и др. // Ярославский педагогический вестник. – 2010. №4. С. 121-127.
- Семенычев Е.В., Корсаков М.К., Ясинский О.А. Синтез новых сульфамидных производных 5-амино-4-арилизоксазолов // Тез. докл. Международной конференции по химии «Основные тенденции развития химии в начале XXI века», посвященной 175-летию со дня рождения Д.И. Менделеева и 80-летию создания химического факультета Санкт-Петербургского университета. – Россия, Санкт-Петербург, 21-24 апреля 2009. – С. 440.
- Семенычев Е.В., Корсаков М.К., Ясинский О.А. Разработка методов синтеза новых амидных производных 3-арил-5-аминоизоксазолов // Тез. докл. Всероссийской научно-практической конференции «Принципы зеленой химии и органический синтез». – Россия, Ярославль, 9-10 октября 2009. – С. 57.
- Семенычев Е.В., Корсаков М.К., Ясинский О.А. Синтез и амидная функционализация 3-(3изоксазол-5-ил-бензилсульфонил)-пропионовых кислот // Тез. докл. Всероссийской конференции по органической химии, посвященной 75-летию со дня основания Института органической химии им. Н.Д. Зелинского РАН. – Россия, Москва, 25-30 октября 2009. – С. 383.
- Семенычев Е.В., Корсаков М.К., Ясинский О.А. Синтез 4-фенил-5-иламинизоксазолов // Тез. докл. XLVI Всероссийской конференции по проблемам математики, информатики, физики и химии. Секция химии. – Москва, 19-23 апреля 2010. – С. 133.
- Семенычев Е.В., Корсаков М.К., Новожилов Ю.В. и др. Перегруппировка изоксазола под действием гидразина // Тез. докл. Всероссийской конференции с элементами научной школы для молодежи «Актуальные проблемы органической химии». – Россия, Казань, 6-8 октября 2010. – С. 119.
- Семенычев Е.В., Корсаков М.К., Ясинский О.А. Синтез и амидная функционализация 5-фенилизоксазолов-4-карбоновых кислот // Тез. докл. III Международной конференции «Химия гетероциклических соединений», посвященной 95-летию со дня рождения профессора Алексея Николаевича Коста. – Россия, Москва, 18-21 октября 2010. – У. 53.

