Конформационный анализ молекул азометинов с жидкокристаллическими свойствами и исследование их реакционной способности при гидрировании в дмфа на палладиевом катализаторе
На правах рукописи
Усанова Надежда Николаевна
Конформационный анализ молекул азометинов с жидкокристаллическими свойствами и исследование их реакционной способности при гидрировании в ДМФА на палладиевом катализаторе
02.00.03 – органическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Иваново – 2008
Работа выполнена на кафедре органической и биологической химии в ГОУ ВПО «Ивановский государственный университет».
Научный руководитель
доктор химических наук, профессор Клюев Михаил Васильевич
Официальные оппоненты:
доктор химических наук, профессор Лефедова Ольга Валентиновна
доктор химических наук, доцент Котов Александр Дмитриевич
Ведущая организация: Институт проблем химической физики РАН (г. Черноголовка).
Защита состоится «1» декабря 2008 г в 1000 часов на заседании совета по защите докторских и кандидатских диссертаций Д 212.063.01 при ГОУ ВПО «Ивановский государственный химико-технологический университет» (153000, г.Иваново, пр. Ф. Энгельса, 7).
С диссертацией можно ознакомиться в информационном центре ГОУ ВПО «Ивановский государственный химико-технологический университет» (153000, г.Иваново, пр. Ф. Энгельса, 10)
Автореферат разослан «28» октября 2008 года
Ученый секретарь
совета по защите докторских
и кандидатских диссертаций Хелевина О.Г.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Основания Шиффа или азометины с момента их открытия, и особенно в последние годы, являются объектами пристального внимания исследователей. Азометины широко используются в органическом синтезе для получения гетероциклических соединений и вторичных аминов несимметричного строения; применяются в электронике для создания жидкокристаллических мониторов, датчиков и индикаторов; в резиновой, текстильной промышленностях; служат исходным сырьем для производства ценных лекарственных препаратов и т.д. На наш взгляд, особый интерес вызывает использование жидкокристаллических свойств, которыми обладают некоторые молекулы азометинов. Кроме того, азометины могут быть использованы как исходные соединения в синтезе вторичных аминов несимметричного строения – соединений с большим потенциалом практического использования.
Однако причины проявления жидкокристаллических свойств азометинов и особенности жидкофазного каталитического гидрирования данных соединений в литературе практически не обсуждаются. Данные положения определили актуальность работы и ее практическое значение.
Работа выполнена в рамках Программы Министерства образования и науки РФ «Развитие научного потенциала высшей школы», проект РНП.2.2.1.1.7181, а также поддержана внутренним грантом Ивановского государственного университета «Развитие научно-исследовательской и инновационной деятельности молодых преподавателей, сотрудников, аспирантов и студентов на 2007-2008 гг.».
Цель работы состояла в определении структуры молекул азометинов, проявляющих жидкокристаллические свойства, с помощью квантово-химических методов исследования, а также в установлении взаимосвязи между электронными, структурными и энергетическими характеристиками молекул азометинов, и их реакционной способностью в жидкофазном каталитическом гидрировании. Для достижения поставленной цели в работе решены следующие задачи:
1. Обоснование выбора метода для проведения квантово-химических расчетов молекул азометинов.
2. Конформационный анализ некоторых молекул азометинов и определение их структуры при температурах существования кристаллического состояния вещества (C), нематической фазы (N) и изотропной жидкости (I), а также при температурах фазовых переходов: кристаллическое состояние нематическая фаза (CN), нематическая фаза изотропная жидкость (NI).
3. Исследование реакционной способности азометинов в каталитическом гидрировании в ДМФА на Pd/C.
4. Определение взаимосвязи между строением оснований Шиффа и их реакционной способностью в жидкофазном каталитическом гидрировании.
5. Установление последовательности восстановления >C=N- связи в молекулах азометинов с привлечением результатов квантово-химических расчетов.
Научная новизна. Впервые проведены квантово-химические расчеты 27 молекул азометинов различного строения с применением метода PBE/sbk (DFT) (Priroda) и полуэмпирического метода АМ1 (HyperChem 7.5). Анализ полученных результатов определил выбор молекулярных дескрипторов (величины сродства к электрону (СЭ) и суммарного эффективного заряда на реакционном центре молекулы - >С=N- связи (q)) всех исследуемых соединений.
Впервые проведен конформационный анализ пяти молекул азометинов, обладающих жидкокристаллическими свойствами: п-н-бутилоксибензилиден-п'-толуидина (БОБТ), п-н-пентилоксибензилиден-п'-толуидина (ПОБТ), п-н-гексил-оксибензилиден-п'-толуидина (ГОБТ 1), п-н-бутилоксибензилиден-п'-пропионилок-сиамина (ББПОА), п-пропилокси-о-гидроксибензилиден-п'-бутиланилина (ПОГББА) при температурах существования кристаллического состояния, нематической фазы, изотропной жидкости, и температурах фазовых переходов: кристаллическое состояние нематическая фаза, нематическая фаза изотропная жидкость. Показано, что фазовые переходы сопровождаются изменением конформации и длины молекулы. Смена конформаций молекулы в основном происходит благодаря концевым фрагментам – алкильной и алкилоксигруппам, жесткая часть молекул остается практически без изменения.
Впервые проведено жидкофазное каталитическое гидрирование п-н-этил-оксибензилиден-п'-толуидина (ЭОБТ), БОБТ, п-н-гептилоксибензилиден-п'-толуидина (ГОБТ 2), п-н-метилоксибензилиден-п'-бутиланилина, ПОГББА, ББПОА, п-н-нонил-оксибензилиден-п'-амилового эфира аминокоричной кислоты (НОБАЭАКК) в ДМФА на Pd/C в мягких условиях. Получены эффективные константы скорости реакции (kэф). Показана возможность использования двух дескрипторов (СЭ и q) для предсказания реакционной способности азометинов в жидкофазном каталитическом гидрировании.
Впервые предложены модели аддуктов, отражающие специфическое взаимодействие ДМФА с четырьмя азометинами.
На основании проведенных квантово-химических расчетов и анализа изменения зарядов на атомах входящих в азометиновую группу (>С=N-) предложена трехстадийная схема восстановления >С=N- связи, включающая двухэлектронный перенос и последовательное присоединение протонов к дианион-радикалу.
Практическая значимость работы. Гидрированием соответствующих азометинов на Pd/C в мягких условиях (298-318 К; PH2=0.1 МПа, ДМФА) получены вторичные амины несимметричного строения (N-(4-этилоксибензил)-4'-толуидин, N-(4-бутилокси-бензил)-4'-толуидин, N-(4-гептилоксибензил)-4'-толуидин, N-(2-ок-си,4-гептилоксибензил)-4'-бутиланилин, N-(4-бутилоксибензил)-4'-пропионилокси-анилин, N-(4-нонилоксибензил)-4'-(3''-пентилпропеноатил)анилин), обладающие боль-шим потенциалом практического использования.
Предложены корреляционные уравнения, описывающие взаимосвязь между скоростью гидрирования и значениями дескрипторов, позволяющие предсказывать реакционную способность азометинов в жидкофазном каталитическом гидрировании. Показано, что скорость восстановления >С=N- связи линейно зависит от величин значений СЭ и q.
Полученные значения длин связей, торсионных углов, заряды на атомах, СЭ и др. могут быть использованы в соответствующих справочных изданиях.
Апробация работы. Основные результаты проведенных исследований были представлены в виде устных и стендовых докладов на: Научной конференции фестиваля студентов, аспирантов и молодых ученых «Молодая наука в классическом университете» (Иваново, 2006, 2007, 2008); IX Научной школе-конференции по органической химии (Москва, 2006); I и II Региональных конференциях молодых ученых «Теоретическая и экспериментальная химия жидкофазных систем» (Крестовские чтения) (Иваново, 2006, 2007); III школе-семинаре «Квантово-химические расчеты: структура и реакционная способность органических и неорганических молекул» (Иваново, 2007); 5-ой Всероссийской конференции «Молекулярное моделирование» (Москва, 2007); XVI International Conference on Chemical Thermodynamics in Russia (RCCT 2007). X International Conference on the Problems of Solvation and Complex Formation in Solutions (Suzdal, 2007); VIII Всероссийской выставке научно-технического творчества молодежи (Москва, 2008).
Публикации. По результатам работы опубликовано 4 статьи, 3 из которых входят в список, рекомендуемый ВАК, и 8 тезисов докладов.
Личный вклад автора. Экспериментальные исследования и обработка полученных данных проведена лично автором. Постановка задачи, планирование эксперимента, анализ результатов исследования, формулирование основных выводов диссертации выполнены совместно с научным руководителем доктором химических наук, профессором Клюевым М.В.
Объем и структура диссертации. Работа (объемом 130 страниц, включая 31 рисунок, 25 таблиц, 35 схем и 20 уравнений) состоит из введения, обзора литературы, экспериментальной части, двух глав, посвященных обсуждению полученных результатов, выводов и списка цитируемой литературы (170 наименований).
Основное содержание работы
во введении обоснована актуальность выполненных исследований, сформулированы цели и задачи работы, ее научная новизна и практическая значимость.
В первой главе рассмотрены данные литературы по методам синтеза азометинов, жидкофазному каталитическому гидрированию, конформационному анализу, применению квантово-химических методов для определения реакционной способности органических соединений.
Во второй главе описаны экспериментальные методики получения исследуемых азометинов, проведения жидкофазного каталитического гидрирования, и методики проведения конформационного анализа и квантово-химических расчетов.
В третьей главе обоснован выбор метода квантово-химических расчетов и проведен конформационный анализ молекул некоторых азометинов, проявляющих свойства жидких кристаллов, при температурах существования С, N, I и температурах фазовых переходов: CN, NI.
Проверка адекватности полученных геометрических характеристик исследуемых азометинов проведена путем сравнения полученных результатов с данными литературы по рентгеноструктурному анализу и рентгенодифракционному эксперименту некоторых соединений, имеющих в своем составе азометиновую группу, а также с результатами квантово-химических расчетов родственных молекул.
На рис. 1 приведена структура азометинов ряда п-н-алкилоксибензилиден-п'-толуидина, для которых были выполнены квантово-химические расчеты. В качестве критерия адекватности, выбора метода для проведения квантово-химических расчетов, использовали величину дипольного момента молекулы, так как она определяется симметрией взаимной ориентации полярных групп и позволяет характеризовать соединение в целом.
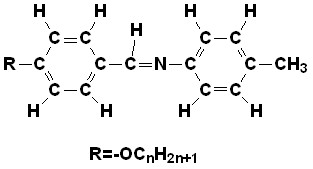
где n = 1…12
Рис.1. Общая структурная формула азометинов ряда п-н-алкилоксибензилиден-п'-толуидина
Таблица 1
Значения торсионных углов (град.) СAr-СAr-С-N, C-C-N-CAr
азометинов ряда п-н-алкилоксибензилиден-п'-толуидина
| угол | СAr-СAr-С-N | C-C-N-CAr | ||||||
| № соединения | АМ1 | РМ3 | MNDO | PBE /sbk | АМ1 | РМ3 | MNDO | PBE /sbk |
| 1 | 4.81 | 3.03 | -62.19 | -4.58 | 34.09 | 43.93 | 103.41 | -33.93 |
| 2 | 4.52 | 2.43 | -84.29 | -4.44 | 33.99 | 43.74 | 98.45 | -34.03 |
| 3 | 4.59 | 3.14 | 94.56 | -4.14 | 34.03 | 44.06 | -89.29 | -33.87 |
| 4 | 4.59 | 3.06 | -84.58 | -4.48 | 34.03 | 43.99 | 98.21 | -34.03 |
| 5 | 4.52 | 2.47 | 96.06 | -4.39 | 33.99 | 43.69 | -88.57 | -33.97 |
| 6 | 4.57 | 2.75 | -82.84 | -4.31 | 34.02 | 43.77 | 100.2 | -33.92 |
| 7 | 4.58 | 3.01 | -85.29 | -4.58 | 34.06 | 43.90 | 92.22 | -34.06 |
| 8 | 4.59 | 2.97 | 98.22 | -4.38 | 34.05 | 43.86 | -87.19 | -33.93 |
| 9 | 4.38 | 2.92 | -82.58 | -4.42 | 33.93 | 43.85 | 100.53 | -33.96 |
| 10 | 4.88 | 2.91 | 97.61 | -4.31 | 34.12 | 43.80 | -86.75 | -33.90 |
| 11 | 4.52 | 2.91 | 99.43 | 4.32 | 34.01 | 43.82 | -85.32 | 33.91 |
| 12 | 4.47 | 2.91 | 98.22 | -4.47 | 33.99 | 43.81 | -86.49 | -33.99 |
Таблица 2
Значения дипольных моментов (D) молекул азометинов ряда п-н-алкил-оксибензилиден-п'-толуидина
| № соединения | АМ1 | PM3 | MNDO | PBE/sbk | µэксп.* |
| 1 | 0.31 | 0.22 | 1.31 | 1.81 | |
| 2 | 0.60 | 0.30 | 0.56 | 2.14 | |
| 3 | 0.65 | 0.31 | 0.56 | 2.33 | |
| 4 | 0.68 | 0.33 | 0.56 | 2.41 | 2.29 |
| 5 | 0.70 | 0.33 | 0.56 | 2.47 | 2.13 |
| 6 | 0.71 | 0.33 | 0.58 | 2.48 | 2.07 |
| 7 | 0.71 | 0.34 | 0.57 | 2.55 | 2.16 |
| 8 | 0.72 | 0.34 | 0.57 | 2.55 | 2.04 |
| 9 | 0.72 | 0.34 | 0.58 | 2.59 | 2.03 |
| 10 | 0.73 | 0.34 | 0.57 | 2.57 | |
| 11 | 0.72 | 0.34 | 0.59 | 2.60 | |
| 12 | 0.73 | 0.34 | 0.58 | 2.58 |
* Сырбу С.А. Влияние межмолекулярных взаимодействий на физико-химические свойства жидкристаллических систем нематического типа. Дис.... докт. хим. наук.: Иваново, 2003. - 308 с.
Результаты проведенных квантово-химических расчетов показали, что из использованных методов, АМ1 и PBE (DFT) достаточно хорошо описывают геометрические характеристики азометинов ряда п-н-алкилоксибензилиден-п'-толуидина (табл. 1). Однако, полуэмпирические методы АМ1, РМ3, MNDO су-щественно занижают значения электронных характеристик, в частности, величины дипольных моментов исследуемых азометинов (табл. 2). Напротив, метод PBE (DFT) завышает дипольные моменты, но их значения ближе к эксперименту. Поэтому для проведения конформационного анализа в дальнейшем использовали полуэмпирический метод АМ1, а для анализа электронных (дипольный момент, заряды на атомах) и энергетических (СЭ) характеристик исследуемых молекул нематических ЖК ряда п-н-алкилоксибензилиден-п'-толуидина - PBE (DFT).
Конформационный анализ некоторых оснований Шиффа
В данном разделе приведены результаты конформационного анализа пяти молекул азометинов – ПОГОББА, ББПОА, БОБТ, ПОБТ, ГОБТ 1 – обладающих жидкокристаллическими свойствами.
Схема фазовых превращений исследуемых соединений представлена на рис. 2. Расчет квантово-химических параметров проведен при температурах фазовых переходов, которые представлены в табл. 3.
![]()
Рис. 2. Схема фазовых превращений исследуемых соединений
Таблица 3
Температуры фазовых переходов CN, NI
| ПОГОББА | ББПОА | БОБТ | ПОБТ | ГОБТ 1 | |||||
| t10C | t20C | t10C | t20C | t10C | t20C | t10C | t20C | t10C | t20C |
| 52.3 | 61.8 | 85 | 119 | 65 | 70 | 59 | 63.5 | 57 | 73.5 |
В результате проведенного конформационного анализа были установлены конформации и молекулярная структура приведенных выше молекул производных бензилиденанилина при температуре 25°С (соответствует C), в температурном интервале, при котором молекула находится в N и I, и при температурах фазовых переходов: CN, NI. Выяснено, что исследуемые основания Шиффа могут иметь при каждой температуре несколько конформаций. Были проанализированы только первые конформации, поскольку они имеют минимальную энергию, и, следовательно, являются наиболее устойчивыми.
В качестве примера ниже подробно рассмотрен конформационный анализ молекулы п-н-бутилоксибензилиден-п'-толуидина (БОБТ). Конформационный анализ остальных исследуемых молекул проводился аналогичным образом.
Оптимизированная структура и нумерация атомов молекулы п-н-бутилокси-бензилиден-п'-толуидина представлена на рис. 3.
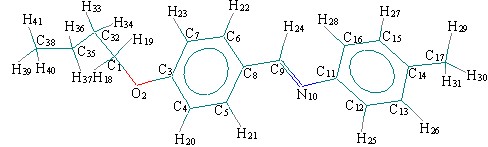
Рис. 3. Оптимизированная структура и нумерация атомов молекулы БОБТ
Выбор торсионных углов для конформационного анализа сделан по результатам анализа потенциальных функций внутреннего вращения для 9 торсионных углов: Н40-C38-С35-Н37, Н36-C35-С32-Н33, Н34-C32-С1-Н19, Н18-С1-О2-С3, C1-O2-C3-С4, С6-C8-C9-Н24, Н24-С9-N10-С11, С9-N10-С11-C12, C15-C14-С17-Н30 (рис. 3). Расчеты проводились с шагом 5. В табл. 4 представлены значения торсионных углов в молекуле БОБТ при температурах существования фаз С, N, I и температурах фазовых переходов: CN, NI.
Таблица 4
Значения торсионных углов БОБТ при температурах существования фаз: С, N, I и температурах фазовых переходов: CN, NI
| торсионные углы, град. | фазовые состояния, фазовые переходы | ||||
| С | С N | N | N I | I | |
| Н40-C38-С35-Н37 | 61.30 | -59.32 | -58.16 | 60.57 | -58.52 |
| Н36-C35-С32-Н33 | -179.53 | 76.75 | -175.77 | 76.72 | -179.33 |
| Н34-C32-С1-Н19 | 177.28 | -168.19 | 72.64 | -168.02 | 178.39 |
| Н18-С1-О2-С3 | -59.89 | -162.98 | -59.16 | -162.98 | -61.32 |
| C1-O2-C3-С4 | -0.35 | 179.27 | 179.36 | 179.23 | 1.74 |
| С6-C8-C9-Н24 | 175.59 | -3.64 | -4.64 | -3.65 | 156.61 |
| Н24-С9-N10-С11 | -1.44 | -1.44 | -1.44 | -1.44 | 178.83 |
| С9-N10-С11-C12 | 149.18 | 149.32 | 149.32 | 149.31 | 103.19 |
| C15-C14-С17-Н30 | 147.68 | 148.01 | -24.25 | 148.24 | 28.28 |
При температуре фазового перехода СN неизменными остаются только три торсионных угла Н24-С9-N10-С11, С9-N10-С11-C12 и C15-C14-С17-Н30. Первые два из них относятся к «жесткому» центру молекулы (связи С9=N10, N10-С11), последний к метильной группе (связь C14-С17). Основной вклад в изменение конформации молекулы БОБТ вносит внутреннее вращение в бутилоксигруппе.
Конформация, полученная для N, отличается значениями торсионных углов бутилоксигруппы (Н36-C35-С32-Н33, Н34-C32-С1-Н19, Н18-С1-О2-С3) и метильной группы (Н15-C14-С17-Н30) молекулы. При температуре существования I изменяется угол поворота вокруг связи C38-С35, О2-С3, C8-С9, С9=N10, N10-С11, C14-С17. При температуре фазового перехода NI изменяется угол поворота вокруг связей C38-С35, C35-С32, C32-С1, С1-О2, C14-С17. Конформационное изменение в этом случае также определяется внутренним вращением в алкильных фрагментах исследуемой молекулы (Н36-C35-С32-Н33, Н34-C32-С1-Н19, Н18-С1-О2-С3, Н15-C14-С17-Н30).
Структура конформаций молекулы БОБТ при фазовых состояниях (С, N, I) и фазовых переходах (CN, NI) представлены в табл. 5.
В табл. 6 представлены значения длин молекул всех исследуемых соединений при температурах существования фаз (C, N, I) и температурах фазовых переходов (СN, NI).
Таблица 5
Структура молекулы БОБТ при фазовых состояниях и соответствующих им переходам
| температура существова- ния фазы, фазового перехода | структура | длина молекул, |
| С, Т<640С | 17.31 | |
| С N, Т=650С | 14.91 | |
| N, Т=66-690С | 17.48 | |
| N I, Т=700С | 16.98 | |
| I, Т=720С | 11.67 |
Таблица 6
Длины исследуемых молекул при различных фазовых состояниях (С, N, I) и соответствующих им фазовых переходов (СN, NI)
| фазовые состояния, фазовые переходы* | Длина молекулы, | ||||
| ПОГББА | ББПОА | БОБТ | ПОБТ | ГОБТ 1 | |
| С | 20.42 | 21.51 | 17.31 | 16.11 | 19.06 |
| СN | 18.95 | 14.91 | 17.88 | ||
| N | 18.41 | 17.48 | 17.56 | ||
| NI | 18.72 | 11.4 | 16.98 | 18.02 | 16.12 |
| I | 19.96 | 21.51 | 11.67 | 14.18 | |
*температура фазового состояния и фазовых переходов для каждого азометина представлена в табл. 3.
Результаты расчета показывают, что фазовые переходы (рис. 2) сопровождаются сменой конформаций. Молекулы БОБТ, ПОБТ, ГОБТ 1, ББПОА, ПОГББА остаются акопланарными при всех конформационных изменениях. Наибольшие изменения претерпевают торсионные углы в алкильных и метильных группах, и этот факт согласуется с данными литературы по ИК-спектроскопии термотропных ЖК. Углы «жесткой» части молекул также способны менять свои величины. Как следует из данных табл. 6, при смене конформаций исследуемых молекул ЖК в большинстве случаев длина молекулы изменяется. Это согласуется с литературными данными рентгеноструктурного анализа некоторых молекул ряда п-н-алкилоксибензилиден-п'-этиланилина. Таким образом, подтверждена гипотеза проф. Клопова В.И. о том, что молекулы ЖК в зависимости от агрегатного состояния вещества находятся в виде различных конформеров.
В четвертой главе приведены результаты экспериментального и теоретического исследования процесса жидкофазного каталитического гидрирования некоторых азометинов, обладающих свойствами ЖК, в ДМФА.
Впервые проведено жидкофазное каталитическое гидрирование ЭОБТ, ГОБТ 2, п-н-метилоксибензилиден-п'-бутиланилина, ПОГОББА, ББПОА, НОБАЭАКК в ДМФА на Pd/C в мягких условиях. Реакции имеют нулевой порядок по субстрату и первый порядок по катализатору и водороду. В табл. 7 приведены значения kэф. гидрирования изученных соединений. Азометины ряда п-н-алкилосибензилиден-п'-толуидина имеют примерно одинаковые значения kэф., следовательно, она не зависит от увеличения объема заместителя в пара-положении. Наибольшую скорость гидрирования наблюдали у НОБАЭАКК.
Таблица 7
Значения эффективных констант скорости жидкофазного каталитического гидрирования исследуемых азометинов в ДМФА
| № п/п | названия вещества | kэф, л/с*г-ат.Pd | |
| Т=298К | Т=318К | ||
| 1 | ЭОБТ | 3.85 | 4.33 |
| 2 | ГОБТ 2 | 3.90 | 4.38 |
| 3 | ПОГОББА | 3.63 | 4.54 |
| 4 | ББПОА | 4.05 | 4.97 |
| 5 | НОБАЭАКК | 4.74 | 5.62 |
Условия: 0.3 г субстрата; 10мл ДМФА, Т=298К или 318К; 0,1 МПа Н2 ; 0.2 г Pd/C (содержание палладия 1 мас.%).
Для прогнозирования реакционной способности соединений без проведения эксперимента, можно использовать различные дескрипторы (заряды на атомах, порядки связи, энергии граничных молекулярных орбиталей и др.). В данной работе в качестве дескрипторов использовали значения СЭ и q.
Методом PBE/sbk проведены расчеты СЭ для 27 молекул азометинов разнообразного строения. В пределах одного ряда значения СЭ изменяются незначительно: у соединений ряда п-н-алкилоксибендена-п'-толуидина величина СЭ составляет 0.571 - 0.599 эВ, а у соединений ряда п-н-алкилоксибендена-п'-метоксианилина - 0.518 - 0.544 эВ. Наибольшее значение СЭ получено в случае НОБАЭАКК (1.442 эВ). Наименьшее значение СЭ у азометинов ряда. В настоящее время принято считать, что гидрирование ненасыщенных соединений в общем виде представляет собой последовательный процесс переноса электронов с восстановителя на субстрат с последующим присоединением протонов к образующимся анион-радикалам. Таким образом, исходя из общих теоретических представлений, чем меньше СЭ, тем легче образуется анион-радикал. Следует ожидать, что если стадия переноса электрона с образованием анион-радикала протекает быстро, то с увеличением СЭ логарифм kэф. гидрирования уменьшится. Если же стадия образования анион-радикала является лимитирующей, то зависимость должна быть обратной.
Сопоставление результатов гидрирования с данными, полученными с использованием квантово-химических расчетов, показало, что с ростом значения СЭ, значение kэф. увеличивается (рис. 4), следовательно, при гидрировании исследуемых субстратов стадия переноса электрона и образование анион-радикала является лимитирующей. Зависимость близка к линейной (r=0.984±0.007) и описывается уравнением 1:
lgkэф.=(0.517±0.008)+(0.112±0.009)СЭ (1)
Проведено моделирование (метод PBE/sbk (DFT) c использованием программы Priroda) влияния растворителя на процесс восстановления азометинов, для чего рассчитаны аддукты ЭОБТ, ГОБТ 2, ПОГОББА, ББПОА с одной и двумя молекулами ДМФА. Моделирование аддуктов проводили, учитывая распределение электронной плотности в молекулах азометинов, которое свидетельствует о том, что имеется только один реакционный центр, т. к. максимум электронной плотности сосредоточен в области двойной связи >С=N- (рис. 5).
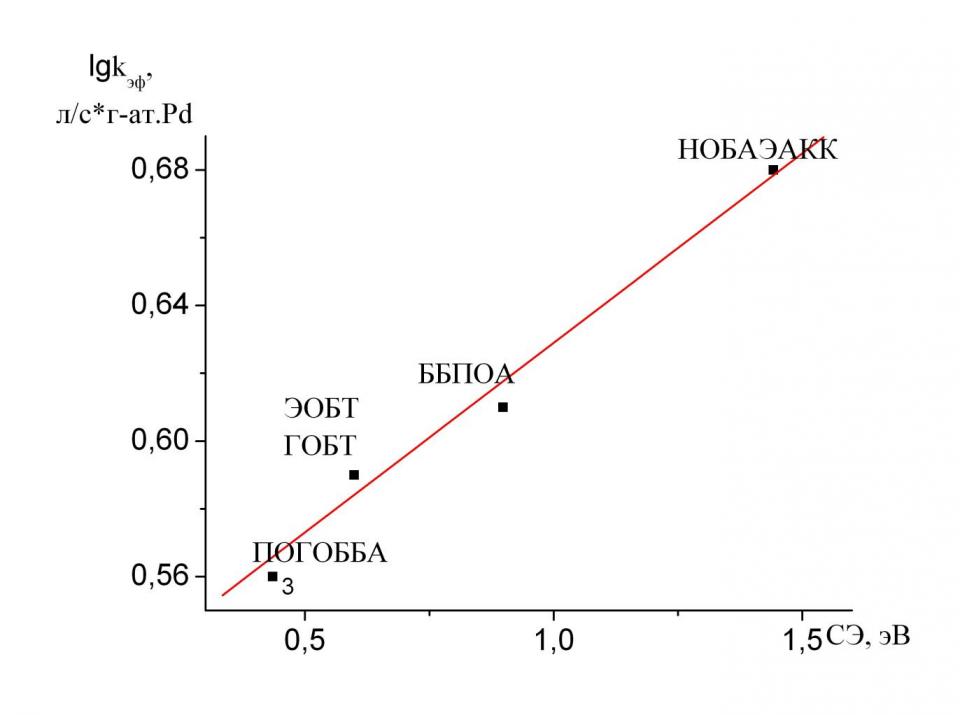
Рис. 4. Зависимость логарифма эффективных констант скорости от СЭ изученных молекул
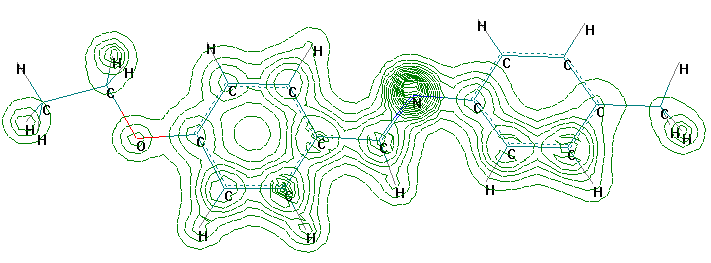
Рис. 5. Распределение электронной плотности в молекуле ЭОБТ
Молекулы растворителя помещали в моделируемую систему так, чтобы они были ориентированы относительно реакционного центра. Результаты расчетов представлены в табл. 8. Задавали ориентацию с учетом распределения электронной плотности в молекуле азометина. Максимум ее приходится на кратную связь (>С=N-). В результате оптимизации геометрии аддукта, получена молекулярная система, в которой координация наиболее положительного атома водорода в молекуле ДМФА происходит по неподеленной электронной паре атома азота азометина.
С увеличением количества молекул ДМФА в сольватной оболочке азометинов, геометрические характеристики последних мало изменяются, в частности это относится к значениям длин связи СAr–С, С=N, N-CAr (1.46, 1.29, 1.41 соответственно). Отметим, что при переходе от молекулы к аддуктам суммарный отрицательный заряд на >С=N- связи последовательно уменьшается.
Таблица 8
Значения зарядов на атомах входящих в азометиновую группу >C=N- и их сумма (ед.зар.)
| название соединений | Priroda | ||||||||
| молекула субстрата без растворителя | молекула субстрата с 1 молекулой ДМФА | молекула субстрата с 2 молекулами ДМФА | |||||||
| q(C) | q(N) | q(-C=N) | q(C) | q(N) | q(-C=N) | q(C) | q(N) | q(-C=N) | |
| ЭОБТ | 0.033 | -0.137 | -0.104 | 0.033 | -0.129 | -0.096 | 0.037 | -0.131 | -0.094 |
| ГОБТ 2 | 0.033 | -0.137 | -0.104 | 0.033 | -0.129 | -0.096 | 0.037 | -0.131 | -0.094 |
| ПОГОББА | 0.034 | -0.141 | -0.107 | 0.029 | -0.134 | -0.105 | 0.027 | -0.121 | -0.094 |
| ББПОА | 0.035 | -0.137 | -0.102 | 0.039 | -0.132 | -0.093 | 0.042 | -0.131 | -0.089 |
Оказалось, что в среде ДМФА скорость гидрирования увеличивается при уменьшении q. Зависимость (рис. 6) близка к линейной (r=0.993±0.006) и описывается уравнением 2:
lgkэф.=(1.341±0.049)+(7.232±0.481)q (2)
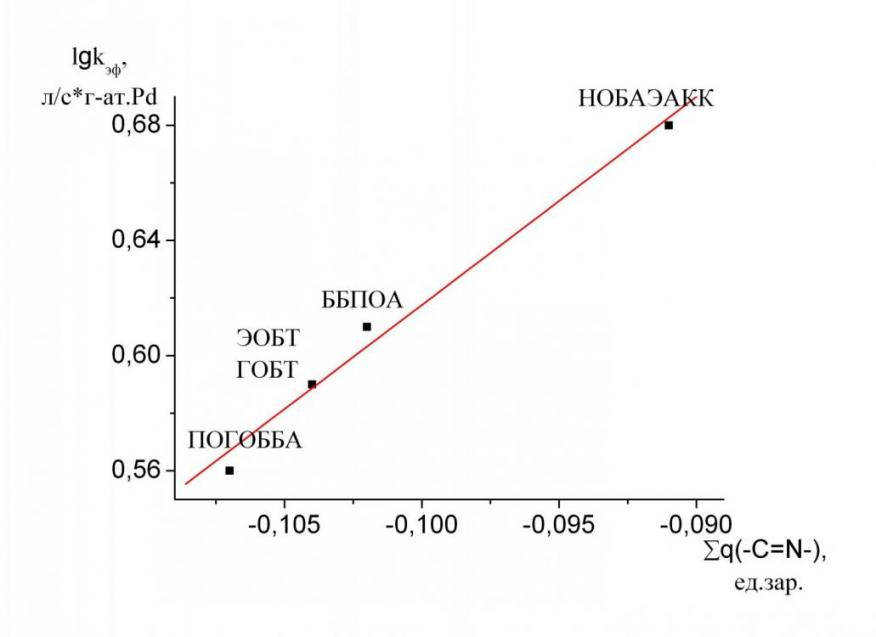
Рис. 6. Зависимость логарифма эффективных констант скорости от суммарного заряда на реакционном центре изученных молекул
Для проверки применимости предложенных уравнений, с их использованием проведен расчет эффективной константы скорости гидрирования. БОБТ и п-н-ме-тилоксибензилиден-п'-бутиланилина. Согласно расчету величина эффективной конс-танты скорости гидрирования у БОБТ составила 3.81 л/с*г-ат.Pd (по уравнению 1) и 3.89 л/с*г-ат.Pd (по уравнению 2). Экспериментально (в условиях аналогичных табл. 7) получено значение 3.72 л/с*г-ат.Pd. В свою очередь, эффективная константа скорости гидрирования п-н-метилоксибензилиден-п'-бутиланилина, согласно расчету по уравнениям 1 и 2, составила 3.87 л/с*г-ат.Pd и 3.88 л/с*г-ат.Pd соответственно. Экспериментальное значение - 3.98 л/с*г-ат.Pd. Таким образом, предложенные уравнения позволяют достаточно точно предсказать скорость реакции гидрирования азометинов на Pd/C в ДМФА.
Моделирование схемы жидкофазного каталитического
гидрирования азометинов
C помощью квантово-химических расчетов методом PBE/sbk (Priroda) проведено моделирование гидрирования азометиновой группы на примере ЭОБТ. Рассмотрены возможные схемы реакции.
Первая из них заключается в последовательном присоединении электронов и протонов к исследуемой молекуле поочередно (4 стадии) (рис. 7.) (здесь и далее на рис. 8, 9 приведены заряды на атомах входящих в азометиновую группу (>С=N-), полученные с помощью программы Priroda методом PBE/sbk).

Рис. 7. Четырехстадийная схема гидрирования >С=N- связи
Вторая (рис. 8) схема заключается в последовательном присоединение сразу двух электронов, а затем сразу двух протонов (2 стадии).

Рис. 8. Двухстадийная схема гидрирования >С=N- связи
Суть третей схемы заключается в том, что сначала в систему добавляются два электрона, а потом поочередно два протона (рис. 9).

Рис. 9. Трехстадийная схема гидрирования >С=N- связи
Согласно полученным результатам, присоединение электронов приводит к увеличению отрицательного заряда на реакционном центре, а присоединение протонов - к его снижению. С точки зрения симметрии при восстановлении >С=N- связи выгоден двухэлектронный перенос, т.е. схема 2 или 3. В этом случае суммарный отрицательный заряд на реакционном центре выше. Присоединение протонов к дианионрадикалу, скорее всего, проходит последовательно, поскольку вероятность бимолекулярных реакций существенно выше, чем тримолекулярных. Таким образом, наиболее вероятно, что гидрирование азометинов протекает по схеме 3 (рис. 9).
Основные выводы
1. С помощью квантово-химических методов PBE /sbk (DFT) (Priroda) и АМ1 (HyperChem 7.5) рассчитаны структурные, электронные и энергетические характеристики 27 оснований Шиффа. Полученные результаты стали основой для определения молекулярных дескрипторов (величины сродства к электрону (СЭ) и суммарного эффективного заряда на реакционном центре молекулы - >С=N- связи (q)) всех исследуемых соединений.
2. Впервые проведен конформационный анализ пяти молекул азометинов, обладающих жидкокристаллическими свойствами: ПОГОББА, ББПОА, БОБТ, ПОБТ, ГОБТ 1 при температурах существования С, N, I, и температурах фазовых переходов: CN, NI. Показано, что фазовые переходы сопровождаются изменением конформации и длины молекулы. Смена конформаций молекулы в основном происходит благодаря концевым фрагментам – алкильной и алкилоксигруппам, жесткая часть молекул остается практически без изменения.
3. Впервые проведено жидкофазное каталитическое гидрирование ЭОБТ, ГОБТ 2, п-н-метилоксибензилиден-п'-бутиланилина, ПОГББА, ББПОА, НОБАЭАКК в ДМФА на Pd/C в мягких условиях. Получены эффективные константы скорости реакции. Показана возможность использования двух дескрипторов (СЭ и q) для предсказания реакционной способности азометинов в жидкофазном каталитическом гидрировании: с ростом q на реакционном центре субстрата, значение эффективной константы скорости реакции уменьшается, а с ростом значения СЭ – увеличивается. Обе зависимости близки к линейным.
4. Получены уравнения, адекватно описывающие взаимосвязь реакционной способности и рассчитанных дескрипторов исследуемых азометинов. Проверка уравнений показала, что рассчитанное и экспериментальное значение эффективной константы скорости близки по своей величине.
5. Впервые предложены модели аддуктов, отражающие специфическое взаимодействие ДМФА с четырьмя азометинами. Показано, что с увеличением числа молекул ДМФА в аддукте, величина q уменьшается.
6. Проведено моделирование схемы жидкофазного каталитического гидрирования >C=N- связи в молекулах азометинов. Показано, что наиболее вероятной является трехстадийная схема восстановления азометиновой группы, заключающаяся в двухэлектронном переносе от восстановителя к субстрату с образованием дианион-радикала, и последовательном присоединении протонов к дианион-радикалу.
Список публикаций
1. Усанова Н.Н., Клюев М.В., Волкова Т.Г. Квантовохимические расчеты молекул азометинов ряда п-н-алкилоксибензилиден-п'-толуидинов. // Известия высших учебных заведений. Серия «Химия и химическая технология». 2007. Т.50. Вып.10. - С.13-17.
2. Усанова Н.Н. Волкова Т.Г., Клюев М.В. Конформационный анализ структуры п-пропилокси-о-гидроксибензилиден-п'-бутиланилина при температурах фазовых переходов. // Жидкие кристаллы и их практическое использование. 2008. Вып. 2 (12). – С. 64-71.
3. Волкова Т.Г., Небукина Е.Г., Усанова Н.Н, Клюев М.В. Конформационный анализ структуры п-н-бутилоксибензилиден-п'-пропионилоксиамина при температурах фазовых переходов: кристаллнематик, нематикизотропная жидкость. // ЖОХ. 2008. Т.78. №7. – С. 1173-1176.
4. Усанова Н.Н., Волкова Т.Г., Майдаченко Г.Г., Клюев М.В. Квантово-химическое моделирование структуры п-н-пентилоксибензилиден-п'-толуидина: выбор метода. // В кн. «Квантово-химические расчеты: структура и реакционная способность органических и неорганических молекул». 2007. - С.210 -214.
5. Усанова Н.Н. Квантово-химическое изучение молекул азометинов, обладающих свойствами жидких кристаллов // Тез. докл. научн. конф. «Молодая наука в классическом университете». - Иваново, 2006. - С.26.
6. Усанова Н.Н., Волкова Т.Г., Стерликова И.О., Клюев М.В. Квантовохимическая оценка сродства к электрону у ряда азометинов // Тез. докл. IX научной школы-конференции по органической химии. - Москва, 2006. – С.371.
7. Усанова Н.Н., Волкова Т.Г., Клюев М.В. Геометрические, энергетические и электронные характеристики некоторых азометинов, обладающих свойствами жидких кристаллов // Тез. докл. I Региональной конференции молодых ученых «Теоретическая и экспериментальная химия жидкофазных систем» (Крестовские чтения). – Иваново. - 2006. – С.82.
8. Усанова Н.Н. Моделирование структуры п-н-гексилоксибензилиден-п'-толуидина // Тез. докл. научн. конф. «Молодая наука в классическом университете». – Иваново, 2007. - С.46.
9. Волкова Т.Г., Стерликова И.О., Усанова Н.Н., Клюев М.В. Молекулярное моделирование п-н-алкилоксибензилиден-п'-толуидинов: нейтральная и анионная форма молекулы // Тез. докл. 5-ой Всероссийской конференции «Молекулярное моделирование». – Москва, 2007. http//www.geokhi.ru/lmms/Cmm-5/cmm5-theses/Volkova.htm.
10. Volkova T.G., Nebykina E.G., Sterlikova I.O., Klyuev M.V., Usanova N.N. Computer analysis of structural changes of para-n-alkoxybenzilidene-para'-toluidines at phase transitions temperatures // XVI International Conference on Chemical Termodynamics in Russia (RCCT 2007). X International Conference on the Problems of Solvation and Complex Formation in Solutions. - Suzdal, 2007. – Р.510.
11. Усанова Н.Н., Волкова Т.Г., Клюев М.В. Конформационный анализ структуры п-н-пропилокси-о-гидроксибензилиден-п'-бутиланилина при температурах фазовых переходов // Тез. докл. II Региональной конференции молодых ученых «Теоретическая и экспериментальная химия жидкофазных систем» (Крестовские чтения). – Иваново, 2007. – С.139.
12. Усанова Н.Н. Квантовохимическое исследование молекул азометинов и их реакционной способности в жидкофазном каталитическом гидрировании // Тез. докл. научн. конф. «Молодая наука в классическом университете». - Иваново, 2008. - С.91.
Усанова Надежда Николаевна
Конформационный анализ молекул азометинов с жидкокристаллическими свойствами и исследование их реакционной способности при гидрировании в ДМФА на палладиевом катализаторе
Специальность 02.00.03 – органическая химия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Подписано в печать 22.09.2008.
Формат 60![]() 84 1/16. Бумага писчая.
84 1/16. Бумага писчая.
Печать плоская. Усл. печ. л. 0.93. Уч.-изд. Л. 1.0. Тираж 100 экз.
Издательство «Ивановский государственный университет»
153025 Иваново, ул. Ермака, 39
(4932) 93-43-41

