Кинетические закономерности электроосаждения сплавов и композиционных электрохимических покрытий на основе цинка, полученных из малоконцентрированных кислых электролитов
На правах рукописи
Гусев Михаил Станиславович
Кинетические закономерности электроосаждения сплавов и Композиционных Электрохимических Покрытий на основе цинка, полученных из малоконцентрированных кислых электролитов
Специальность 02.00.05- Электрохимия
Автореферат
диссертации на соискание ученой степени
кандидата химических наук
Саратов 2008
Диссертация выполнена в ГОУ ВПО «Саратовский государственный
технический университет»
| Научный руководитель: | доктор технических наук, профессор Соловьева Нина Дмитриевна |
| Официальные оппоненты: | доктор технических наук, профессор Фомичев Валерий Тарасович кандидат химических наук Иванова Светлана Борисовна |
| Ведущая организация: | Ивановский государственный химико-технологический университет |
Защита состоится 19 декабря 2008г. в 16 часов на заседании диссертационного совета Д 212.242.09 при Саратовском государственном техническом университете по адресу: 413100, г.Энгельс, пл.Свободы, 17, Энгельсский технологический институт, (филиал) ГОУ ВПО «Саратовский государственный технический университет», ауд. 237.
С диссертацией можно ознакомиться в научно-технической библиотеке Саратовского государственного технического университета, по адресу: 410054, Саратов, ул. Политехническая, 77.
Автореферат разослан « 19 » ноября 2008г.
Учебный секретарь
диссертационного совета В.В. Ефанова
Общая характеристика работы
Актуальность темы. Интерес к сплаву цинка и никеля обусловлен хорошей коррозионной стойкостью покрытия, возможностью уменьшения числа технологических операций при нанесении покрытий, экологичностью производства. Цинковое покрытие обеспечивает электрохимическую защиту стальных изделий от коррозии в обычных атмосферных условиях, однако его коррозионная устойчивость не всегда бывает достаточной. Одним из перспективных направлений повышения срока службы цинковых покрытий является его рациональное легирование металлами группы железа. Работами Н.Т. Кудрявцева, В.Г. Роева, Ф.И. Данилова и др. показано, что электролитические сплавы Zn-Ni, содержащие 10-15% Ni, представляют интерес как возможная альтернатива кадмиевым покрытиям, могут быть использованы для защиты стали от коррозии при сохранении хорошей способности к формовке, свариваемости, окрашиванию.
Несмотря на большое внимание к сплаву Zn-Ni, его использование ограничено. Одной из причин этого является отсутствие четкого представления о механизме электроосаждения данного сплава, а, следовательно, трудность в управлении составом и свойствами Zn-Ni покрытия. Дальнейшее развитие представлений о кинетике и механизме процесса электроосаждения сплава Zn-Ni из малоконцентрированного кислого электролита, установление влияния режима электролиза на физико-химические свойства сплава представляет собой весьма актуальную проблему.
Диссертационная работа выполнена в рамках плановых научных исследований кафедры «Технология электрохимических производств» в соответствии с тематикой НИР по направлению 09В.05, а также в рамках НИР по заданию федерального агентства по образованию, финансируемой из средств федерального бюджета (№ государственной регистрации 01200703461).
Цель работы состояла в изучении кинетических закономерностей электроосаждения сплава Zn-Ni и КЭП Zn-Ni-коллоидный графит (Сколл) из кислых хлористых электролитов, в выявлении взаимосвязи структурных превращений в хлористых электролитах сплавообразования со скоростью электрохимических процессов, влияния режима электролиза на физико-химические свойства покрытия. Для достижения поставленной цели необходимо было решить следующие задачи:
- изучить физико-химические и термодинамические свойства водных растворов, содержащих основные компоненты электролитов осаждения сплава цинк-никель, и установить взаимосвязь кинетики электродных процессов со структурными превращениями в растворах;
- исследовать кинетику совместного осаждения цинка и никеля из хлористых электролитов сплавообразования;
- изучить влияние режима электролиза на свойства сплава цинк-никель (микротвердость, адгезию, коррозионную стойкость);
- установить влияние коллоидного графита в составе гальванического осадка Zn-Ni-Сколл на физико-механические свойства покрытия.
Научная новизна работы.
Впервые представлены экспериментальные данные по электропроводности одно- и многокомпонентных водных растворов, электролитных суспензий с Сколл., используемых для электроосаждения сплава Zn-Ni и композиции Zn-Ni-Сколл. В рамках теории Эйринга рассчитаны термодинамические характеристики вязкого течения (G, H), значения которых указывают на структурные изменения в водных растворах, содержащих хлористые соли цинка и никеля. Получены новые данные по кинетике совместного осаждения цинка и никеля из хлористых электролитов, электроосаждения композиционного электрохимического покрытия (КЭП) Zn-Ni-Сколл.. Получены данные по влиянию режима электролиза на состав и свойства сплава цинк-никель, осажденного из хлористых растворов.
Практическая значимость результатов работы. Полученные данные по электропроводности водных растворов отдельных компонентов и электролита для электроосаждения сплава Zn-Ni представляют интерес как справочный материал. Разработаны технологические рекомендации по составу хлористого электролита, обеспечивающего при выбранном режиме электролиза (i=1,5-1,7 А/дм2, 18-200С) получение коррозионно-стойкого, равномерного, мелкозернистого цинк-никелевого покрытия с выходом по току 82-85%, обладающего хорошей адгезией.
На защиту выносятся следующие основные положения:
- Результаты исследования концентрационных и температурных зависимостей вязкости, плотности, электропроводности одно- двух- и более компонентных водных растворов ZnCl2, NiCl2, ZnCl2+ NiCl2, ZnCl2+ Сколл, ZnCl2+ NiCl2+ Сколл.
- Кинетические закономерности электроосаждения сплава цинк-никель из хлористых электролитов во взаимосвязи с процессами в объёме раствора.
- Кинетические закономерности электроосаждения КЭП цинк-никель-коллоидный графит из суспензий на основе хлористых электролитов.
- Влияние плотности тока процесса электроосаждения на эксплуатационные свойства сплава цинк-никель (микротвердость, адгезию, коррозионную стойкость).
Апробация результатов работы.
Основные результаты работы докладывались на Международной конференции «Композит–2007», Вестник Саратовского государственного технического университета Саратов-2007, Защитные и специальные покрытия, обработка поверхности в машиностроении и приборостроении на IV Всероссийской научно- практической конференции Пенза–2007г.; 5-ой Международной конференции Москва – 2008 г.; Всеросс. конф. Новочеркасск – 2008г.; 1 Международной научной конференции г. Плес, Ивановская обл. 2008 г.; Всероссийской конференции молодых ученых « Актуальные проблемы электрохимической технологии» Саратов 2008г.;
Публикации. По материалам диссертации опубликовано 7 работ, в том числе 1 статья в журнале, рекомендуемом ВАК, 3 статьи в реферируемых сборниках научных трудов.
Структура диссертации. Диссертационная работа состоит из введения, четырёх глав, выводов и списка использованной литературы из наименований. Она изложена на страницах машинописного текста, содержит рисунков и таблиц.
Содержание Работы
Во введении дано обоснование актуальности темы, рассмотрены цели и задачи исследования, научная новизна и практическая значимость работы.
Глава 1. Литературный обзор
В обзоре литературы приведены материалы работ, в которых представлены точки зрения исследователей на кинетику и механизм электроосаждения сплава Zn-Ni. Отмечается, что единого представления не выработано вследствие сложности протекающих процессов. Показано влияние состава электролита, режима электролиза на соотношение компонентов в сплаве, на структуру формирующихся осадков. Установлено, что свойства электроосаждаемого сплава Zn-Ni во многом определяются качественным составом электролита. Отражены особенности электрохимического осаждения КЭП, рассмотрено изменение физико-механических и химических свойств композиционного покрытия по сравнению с металлическим покрытием.
Глава 2. Методика эксперимента
Объектами исследования являлись электроды из стали 10 кп, хлористые электролиты осаждения сплава цинк-никель и КЭП Zn-Сколл: ZnCl2, ZnCl2+NiCl2, ZnCl2+NiCl2+Н3ВО3, ZnCl2+Скол, ZnCl2+Сколл+Н3ВО3, ZnCl2+NiCl2+Сколл, ZnCl2+NiCl2+Сколл+Н3ВО3. Растворы готовили на основе дистиллированной воды и реактивов марки «х.ч.». Физико-химические свойства растворов исследовали в области температур 2050 0С (t=50С). Для измерения плотности использовали набор денсиметров (Гост 1300-74), для определения вязкости – вискозиметр ВПЖ-2 (ГОСТ 33-66), электропроводность измеряли кондуктометром с датчиком наливного типа УЭП-Н-С.
Сплав цинк-никель осаждали на сталь 10 кп в стеклянной ячейке при 250С. Толщина покрытий составляла 5-25 мкм. В качестве нерастворимого противоэлектрода использовали спектральный графит. Состав сплава определяли на установке лазерного эмиссионного микроспектрального анализа «Спектр-2000» и на магнитном масс-спектрометре МИ-1305 (ВИМС). Микротвердость осадков сплава цинк-никель измеряли на приборе ПМТ-3 (ГОСТ 9450-76) методом статического вдавливания алмазной пирамиды. Адгезию полученных осадков оценивали путем нанесения сетки царапин (ГОСТ 9.302-79). Коррозионная стойкость покрытия оценивалась гравиметрически, после выдержки стальных образцов покрытых сплавом Zn-Ni, в 3%-ном растворе NaCl. Электрохимические исследования проводили на потенциостате П-5848 с помощью методов вольтамперометрии, хроноамперометрии, хронопотенциометрии. Для регистрации тока и потенциала во времени использовали самопишущий потенциометр КСП-4 и цифровой вольтметр В7–27. Потенциалы регистрировали относительно стандартного 1н хлорсеребряного электрода сравнения. рН растворов определялся на рН-метре марки рН-340. Измерение рН приэлектродного слоя (рНs) проводилось с помощью микросурмяного электрода (МСЭ), при использовании калибровочной кривой в координатах Е, рН. Состояние поверхности оценивалось с помощью микроскопа CARL ZELSS JENA (IP-20) при увеличении в 50-500 раз.
Воспроизводимость полученных экспериментальных результатов оценивалась с помощью критерия Кохрена.
Глава 3. Физико-химические и термодинамические характеристики водных растворов электроосаждения покрытий Zn-Ni, Zn-Ni-Cколл
3.1. Физико-химические свойства растворов, моделирующих электролит электроосаждения покрытий Zn-Ni, Zn-Ni-Cколл
Изучение таких физико-химических свойств растворов, как электропроводность, вязкость и плотность, позволяет выделить область концентраций, в которой процесс электроосаждения будет протекать с меньшими энергетическими затратами, получить информацию о структурных превращениях в растворах электролитов, связанных с процессами гидратации, ассоциации, комплексообразования, происходящими при изменении состава раствора, концентрации компонентов и температуры.
Для выявления воздействия каждого компонента, входящего в состав электролита электроосаждения сплава Zn-Ni, на растворитель (воду) исследовались однокомпонентные водные растворы, а затем более сложные: двухкомпонентные водные электролиты.
Для электроосаждения сплава Zn-Ni наибольшее применение получили растворы на основе сульфатных и хлоридных солей цинка и никеля. Систематические данные по концентрационному и температурному изменению вязкости, плотности, электропроводности водных растворов солей хлорида цинка и никеля в диапазоне концентраций от 0,183 до 0,462 моль/л, а также их смеси отсутствуют. Указанный концентрационный интервал солей представляет интерес, т.к. в нем нет сведений по скорости электроосаждения сплава Zn-Ni, по составу и свойствам образующихся покрытий.
Полученные экспериментальные результаты анализировались при использовании модельных представлений О. Я. Самойлова, Г. А. Крестова, А. К. Лященко и др. о влиянии растворяющихся ионов на развитую сетку водородных связей в структуре воды, о строении сольватированного комплекса. Для ионов Zn2+, Ni2+, являющихся d-элементами, ярко выражена способность взаимодействовать с неподеленной парой электронов молекул воды, вследствие чего образуется связь, близкая к ковалентной, и аквакомплексы характеризуются повышенной устойчивостью.
Ион цинка гидратирован октаэдрически и первая гидратная сфера Zn2+ состоит из 6 молекул воды. Во второй координационной сфере количество молекул растворителя зависит от концентрации раствора. В присутствии Cl- ионы цинка могут образовывать комплексные соединения типа [Zn(H2O)2Cl2], [Zn(H2O)2Cl3]-, а также небольшое количество комплексов ZnCl42-. В гидратированном ионе никеля [Ni(H2O)n]2+ число «n» может принимать значения от 7 до 2. При близких ионных радиусах Ni2+ и Zn2+ (![]() = 0,074 нм,
= 0,074 нм, ![]() = 0,083) для катионов Ni2+ наблюдается усиление взаимодействия с водой по сравнению с ионами Zn2+ вследствие – взаимодействия. Соединения Ni2+ и Zn2+ с Н2О, образующиеся за счет возникновения кластеров воды вокруг ионов и в результате гидролиза, обладают разнообразием форм, структуры, устойчивости. Необходимо учитывать, что одновременно с ионами Zn2+ Ni2+ в электролите присутствуют ионы хлора, которые оказывают разрушающее действие на структуру воды.
= 0,083) для катионов Ni2+ наблюдается усиление взаимодействия с водой по сравнению с ионами Zn2+ вследствие – взаимодействия. Соединения Ni2+ и Zn2+ с Н2О, образующиеся за счет возникновения кластеров воды вокруг ионов и в результате гидролиза, обладают разнообразием форм, структуры, устойчивости. Необходимо учитывать, что одновременно с ионами Zn2+ Ni2+ в электролите присутствуют ионы хлора, которые оказывают разрушающее действие на структуру воды.
Конкурирующее действие ионов Zn2+и Cl- на структуру растворителя проявляется в нелинейной концентрационной и температурной зависимости вязкости, плотности и электропроводности растворов хлорида цинка (табл. 1), в росте кажущегося мольного объема (табл. 2) для изучаемого диапазона концентраций и температур.
Нелинейность концентрационного изменения вязкости и электропроводности в изучаемом интервале температур сохраняется и в двухкомпонентных электролитах ZnCl2 + NiCl2 (рис. 1, 2). Образование сольватов с большим числом молекул воды, а также гидратных комплексов цинка с ионами хлора снижает скорость роста электропроводности при увеличении концентрации солей, о чем свидетельствует уменьшение /С в растворах солей хлоридов никеля и цинка с 8,83 в электролите ZnCl2 0,183 М + NiCl2 от 0,308 до 0,462 М до 5,45 в электролите ZnCl2 0,44 М + NiCl2 от 0,308 до 0,462 М.
Таблица 1
Динамическая вязкость (), плотность (d), электропроводность ()
водных растворов ZnCl2
| t, c | d,г/см3 | ,сПз | , См·м-1 | |
| 0,183 | 25 | 1,019 | 1,224 | 2,86 |
| 30 | 1,018 | 1,128 | 3,2 | |
| 35 | 1,016 | 1,074 | 3,6 | |
| 40 | 1,014 | 0,978 | 3,97 | |
| 45 | 1,013 | 0,954 | 4,25 | |
| 50 | 1,010 | 0,902 | 4,5 | |
| 0,366 | 25 | 1,044 | 1,264 | 5,3 |
| 30 | 1,043 | 1,188 | 5,77 | |
| 35 | 1,040 | 1,131 | 6,5 | |
| 40 | 1,038 | 1,055 | 6,8 | |
| 45 | 1,036 | 0,999 | 7,08 | |
| 50 | 1,035 | 0,935 | 7,52 | |
| 0,440 | 25 | 1,047 | 1,289 | 5,58 |
| 30 | 1,045 | 1,223 | 6,4 | |
| 35 | 1,044 | 1,168 | 6,6 | |
| 40 | 1,043 | 1,070 | 7,3 | |
| 45 | 1,038 | 1,033 | 7,55 | |
| 50 | 1,036 | 0,978 | 8,0 |
Таблица 2
Кажущийся мольный объем (Фv) раствора ZnCl2
| Фv, см3 моль-1 | |||
| t,0С | |||
| 0,183 | 0,3669 | 0,440 | |
| 30 | - | - | 12,735 |
| 40 | - | - | 9,225 |
| 50 | 22,716 | 10,833 | 30,075 |
а б
Рис. 1. Влияние ![]() на растворов солей ZnCl2 + NiCl2.
на растворов солей ZnCl2 + NiCl2.
Содержание ZnCl2, моль/л.:1 - 0,183; 2 - 0,366; 3 – 0,440, при t0C: а) 25; б) 50
Дальнейшее увеличение концентрации солей нецелесообразно, так как возрастает вязкость электролита. Кроме того, концентрирование раствора по одному из компонентов приведет к уменьшению растворимости солей. Поэтому для электроосаждения сплава Zn-Ni рекомендуется электролит, содержащий 0,44 моль/л ZnCl2 и 0,308-0,385 моль/л NiCl2, как обладающий высокой стабильной электропроводностью.
а б
Рис. 2. Влияние ![]() на растворов солей ZnCl2 + NiCl2.
на растворов солей ZnCl2 + NiCl2.
Содержание ZnCl2, моль/л.: 1 - 0,183; 2 - 0,366; 3 - 0,440, при t0C: а) 25; б) 50.
3.2. Термодинамические свойства растворов электроосаждения сплава Zn-Ni
Влияние растворяющихся компонентов на структуру растворителя можно проанализировать, изучая термодинамические характеристики вязкого течения и переноса в электролитах. Была использована теория Эйринга, позволяющая оценить влияние природы электролита, его концентрации и температуры раствора на свободную энергию активации вязкого течения ![]() , энтальпию активации вязкого течения
, энтальпию активации вязкого течения ![]() . Расчет
. Расчет ![]() и
и ![]() для изучаемых растворов проводился в соответствии с уравнениями:
для изучаемых растворов проводился в соответствии с уравнениями:
![]() , (1)
, (1)
![]() , (2)
, (2)
где ![]() - кинематическая вязкость исследуемых водных растворов; R – универсальная газовая постоянная; Т – абсолютная температура;
- кинематическая вязкость исследуемых водных растворов; R – универсальная газовая постоянная; Т – абсолютная температура; ![]() - средняя масса (
- средняя масса (![]() ,
, ![]() и Ni –молекулярные массы и массовые молярные доли компонентов раствора); h – постоянная Планка; NА – число Авогадро.
и Ni –молекулярные массы и массовые молярные доли компонентов раствора); h – постоянная Планка; NА – число Авогадро.
Установлено, что уравновешивание структуроразрушающего (Сl-) и структурообразующего (Zn+2, Ni+2) воздействия ионов электролита приводит к незначительному изменению термодинамических характеристик вязкого течения: ![]() для водных растворов ZnCl2 (
для водных растворов ZnCl2 (![]() от 0,183 до 0,44 М) лежит в пределах от 15,6 до 16,4 кДж/моль, для растворов ZnCl2+NiCl2 (
от 0,183 до 0,44 М) лежит в пределах от 15,6 до 16,4 кДж/моль, для растворов ZnCl2+NiCl2 (![]() от 0,192 до 0,462 М) – от 15,6 до 16,5 кДж/моль.
от 0,192 до 0,462 М) – от 15,6 до 16,5 кДж/моль.
Результаты расчёта ![]() подтверждают факт конкурирующего воздействия катионов Zn+2, Ni+2 и анионов Cl- на структуру воды. Следует отметить, что значение
подтверждают факт конкурирующего воздействия катионов Zn+2, Ni+2 и анионов Cl- на структуру воды. Следует отметить, что значение ![]() водных растворов хлорида цинка (от 7,2 до 9,76 кДж/моль) и ZnCl2+NiCl2 (от 5,26 до 13,38 кДж/моль) для указанных выше диапазонов концентраций меньше энтальпии активации вязкого течения воды (
водных растворов хлорида цинка (от 7,2 до 9,76 кДж/моль) и ZnCl2+NiCl2 (от 5,26 до 13,38 кДж/моль) для указанных выше диапазонов концентраций меньше энтальпии активации вязкого течения воды (![]() воды составляет 16,26 кДж/моль), что свидетельствует о разупорядоченности в структуре раствора.
воды составляет 16,26 кДж/моль), что свидетельствует о разупорядоченности в структуре раствора.
Анализ термодинамических характеристик показывает, что в выбранном интервале концентраций компонентов не должно возникать затруднений для переноса и диффузии ионов, участвующих в электрохимическом процессе.
3.3. Электропроводность суспензии ZnCl2 + NiCl2 + Сколл
Для выявления воздействия коллоидного графита на электропроводность электролитной системы исследовались одно- и двухкомпонентные водные растворы. Диапазон изменения концентраций хлористых солей Zn и Ni от 0,183 до 0,462 моль/л. Выбор концентрационного интервала обусловлен разработкой малоконцентрированного электролита электроосаждения КЭП Zn-Ni-коллоидный графит.
С введением в изучаемые электролиты коллоидного графита происходит некоторое снижение проводимости во всем интервале температур и концентрации солей. Например, проводимость суспензии 0,44 М ZnCl2 + Сколл 50 мл/л при 25С – 5,1 Смм-1, а 0,44 М раствора ZnCl2 – 5,58 Смм-1; проводимость суспензии ZnCl2 0,44 М + NiCl2 0,38 М + 50 мл/л Сколл при 25С – 7,1 Смм-1, а раствора 0,44 М ZnCl2 + 0,38 М NiCl2 – 8,9 Смм-1. Данное явление можно связать с адсорбционной способностью частиц графита, в результате которой уменьшается количество подвижных ионов.
Глава 4. Исследование кинетики электроосаждения сплава Zn-Ni, покрытия Zn-Ni-Сколл и свойств получаемых осадков
- 4.1. Потенциодинамическое исследование электроосаждения
Zn и Ni из растворов хлористых солей
Для определения области тока, в которой становится возможным совместное осаждение ионов цинка и никеля, были получены потенциодинамические кривые (ПДК) электровосстановления сплава Zn-Ni на стальном электроде при скорости развёртки потенциала (Vр) 4 мВ/с (рис. 3).
i, мА/см2 i, мА/см2
-Е, В -Е, В
а б
Рис. 3. ПДК электровосстановления сплава Zn-Ni из электролита состава 0,44 М ZnCl2+ХМ NiCl2 на на сталь 10кп, при t=250С, Vp=4 мВ/с.
Концентрация NiCl2, моль/л: 1-0,31, 2-0,38, 3-0,39.
Установлено, что увеличение концентрации соли никеля способствует росту i в интервале потенциалов от -0,5 до -0,85 В. При смещении потенциала электрода в область более отрицательных значений происходит резкий подъём i за счёт электровосстановления ионов цинка. Следует отметить: рост тока наблюдается при более положительных значениях потенциала, чем стандартный электродный потенциал цинка, это может свидетельствовать о деполяризующем действии ионов Ni2+ на электровосстановление Zn2+.
Анализ ПДК электровосстановления сплава Zn-Ni из растворов хлористых солей позволяет выделить диапазон потенциалов и соответствующий им интервал плотностей тока, при которых следует проводить электроосаждение сплава: этот диапазон потенциалов от – 0,90 до -1,1 В и плотности тока от 7 10-3 до 25 10-3, А/см2.
4.2. Кинетические закономерности электроосаждения сплава Zn-Ni
Кинетические закономерности электроосаждения Zn и сплава Zn-Ni из хлористых электролитов на стальную основу изучались гальваностатическим методом.
Колебания потенциала электрода на первых секундах процесса свидетельствуют о сложности протекающих процессов: электровосстановлении гидратированных ионов цинка, ионов водорода, адсорбции гидроксидов цинка (рис.4).
-Е, В -Е, В
t, с t, с
а б
Рис. 4(а,б). Е, t кривые электроосаждения Zn на сталь 10кп, в 0,44 М ZnCl2, при i10-3, А/см2: 1-12,5 (1), 2-17,0 (2) и в 0,44 М ZnCl2 + 0,32 М Н3ВО3
при i=1710-3, А/см2 (3), при 250С
С ростом поляризующего тока увеличивается скорость электровосстановления Zn и Н2, сокращается время выхода потенциала на стационарное значение. Это может быть связано с образованием более плотной пассивной плёнки при адсорбции на поверхности электрода гидроксида цинка. О возможности данного процесса свидетельствует изменение рН приэлектродного слоя (табл. 3). Перенапряжение кристаллизации цинка с ростом тока увеличивается от 0,4 до 0,5 В.
С введением Н3ВО3 в 0,44 М раствор ZnCl2 уменьшается рН электролита (табл. 3), а потенциал погружения стального электрода становится более электроположительным, вероятно, за счёт того, что уменьшается депассивирующее действие ионов хлора в результате образования комплексов ионами Zn2+, борной кислотой и водой, (потенциал стали в 0,336 М ZnCl2 на 10-й секунде – -0,488 В, в растворе 0,366 М ZnCl2 + 0,323 М Н3ВО3 – -0,407 В).
Таблица 3
Изменение рНS во времени при катодной поляризации стального электрода в электролитах хлорида цинка, t=25 С
| Состав раствора, моль/л | iк10-3, А/см2 | рНS | ||||||||
| t, С | ||||||||||
| 0 | 5 | 15 | 30 | 45 | 60 | 90 | 120 | 150 | ||
| ZnCl2 0,44 | 15 | 4,80 | 7,80 | 6,85 | 6,8 | 6,8 | 6,8 | 6,8 | 6,81 | 6,81 |
| 17 | 4,80 | 6,60 | 6,81 | 6,85 | 6,12 | 6,10 | 6,01 | 6,01 | 6,01 | |
| ZnCl2 0,44 М+Н3ВО3 0,323 | 17 | 4,20 | 7,20 | 7,27 | 7,25 | 7,02 | 6,95 | 6,82 | 6,80 | 6,80 |
| 25 | 4,20 | 6,58 | 6,42 | 5,95 | 5,92 | 5,90 | 5,90 | 5,80 | 5,80 | |
Пассивная плёнка, образующаяся на поверхности электрода при электровосстановлении Zn, в присутствии Н3ВО3 более плотная, чем в электролите 0,44 М ZnCl2 (рис.4). Перенапряжение кристаллизации (кр) при электроосаждении Zn из электролита с Н3ВО3, уменьшается с ростом тока от 0,5 В при i = 1510-3 А/см2 до 0,22 В при 2510-3 А/см2.
Е, В Е, В
2
1
3 4
5
t, c t, c
| Рис. 5. Е, t кривые электроосаждения Zn-Ni на сталь 10 кп, при i = 12,5 ·10-3, А/см2, t=250С из электролита состава 0,44 М ZnCl2 + ХМ NiCl2 Х, моль/л: 1-0,33 (1), | Рис. 6. Е, t кривые электроосаждения Zn-Ni на сталь 10 кп, из электролита состава: 0,44 М ZnCl2 + 0,38 М NiCl2 при плотности тока i ·10-3, А/см2: 1-20 (1), |
| 2-0,35 (2), 3-0,38 (3), 4-0,39 (4) | 2-17 (2), 3-15 (3), 3-13 (4), 5-11,5 (5). |
При совместном электровосстановлении ионов цинка и никеля на Е, t кривых появляются два наклона: наклон в первые доли секунды, вероятно связан с преимущественным электроосаждением никеля. С увеличением времени поляризации и смещении потенциала в область отрицательных значений становится возможным совместное осаждение цинка и никеля, чему соответствует второй наклон на Е, t кривых.
О возможности включения в состав гальванического осадка гидроксидов Zn свидетельствует изменение рНs в течение первых 15 секунд до 6,4.
Используя начальные участки гальваностатических кривых, рассчитывалась поляризационная емкость Спол:
![]() . (3)
. (3)
Из полученных результатов следует, что увеличение концентрации соли NiCl2 до 0,39, приводящее, согласно данным по вязкости и электропроводности растворов (раздел 3.1), к укрупнению разряжающихся частиц, вызывает снижение Спол: Спол в растворе состава ZnCl2 0,44 М + NiCl2 0,35 М составляет 0,0086 Ф/см2, а в электролите ZnCl2 0,44 М + NiCl2 0,39 М – 0,0060 Ф/см2. Аналогичное действие оказывает влияние борной кислоты, способной образовывать комплексы как с ионами цинка, так и с ионами никеля.
Потенциостатическое исследование электроосаждения сплава Zn-Ni на сталь 10 кп (рис.7) позволило установить зависимость скорости процесса от потенциала и показать, что в первые секунды поляризации на поверхности электрода происходит адсорбция реагирующих частиц. Величина адсорбции (ГЕ), рассчитанная при использовании уравнения:
![]() , (4)
, (4)
лежит в пределах от 0,6·10-6 до 13,0·10-6 моль/л. Увеличение ГЕ связано с возрастающим участием в электродном процессе гидроксидов цинка при смещении потенциала в область отрицательных значений.
i10-3, А/см2 t2,c
t,c lg(i/t2)
| Рис. 7. i, t кривые электроосаждения сплава Zn-Ni на сталь 10кп, из электролита состава: 0,44 М ZnCl2 + 0,38 М NiCl2 +Н3ВО3 0,32 М, при –Е, В: 1-1,10 (1), 2-1,07 (2), 3-1,05 (3), 4-1,03 (4), 5-1,02 (5), 6-1,0 (6), 7-0,98 (7) | Рис. 8. Зависимости lg(i/t), t2, электроосаждения сплава Zn-Ni на сталь 10кп, из электролита состава: 0,44 М ZnCl2 + 0,38 М NiCl2 +Н3ВО3 0,32 М, при – Е, В: 1-1,05 (1), 2-1,03 (2), 3-1,02 (3), 4-1,0 (4). |
Анализ i, t кривых электровосстановления сплава Zn-Ni на стальном электроде в координатах lg(i/t), t2 (рис. 8) показал, что кристаллизация осадка протекает с образованием двухмерных зародышей.
4.3. Влияние режима электролиза на структуру и свойства
цинк-никелевых сплавов
При электроосаждении сплава Zn–Ni из электролита, содержащего 0,44М ZnCl2 и 0,38М NiCl2, количество никеля в осадке в изучаемом диапазоне плотностей тока согласно лазерному масс–спектральному анализу, колеблется от 68 до 81% (табл.4).
Таблица 4
Содержание цинка и никеля (%) в сплавах Zn-Ni, электроосажденных из электролита состава: ZnCl2 0,44М +NiCl2 0,38 М, при различных плотностях тока, t=250C
| Компоненты сплава | Катодная плотность тока, i ·10-3,А/см2 | |||
| 7 | 13 | 15 | 17 | |
| Ni, % | 81 | 70 | 71 | 68 |
| Zn, % | 19 | 30 | 29 | 32 |
С увеличением катодной плотности тока наблюдается тенденция к росту содержания Zn в покрытии. Анализ полученных экспериментальных результатов в координатах ![]() ,
, ![]() согласно уравнению:
согласно уравнению:
![]() , (5)
, (5)
где М1,М2 – соответственно содержание более электроотрицательного и более электроположительного компонентов в покрытии, показал, что для изучаемого сплава указанная зависимость соблюдается. Использование уравнения (5) позволит спрогнозировать содержание элементов в сплаве в зависимости от тока поляризации (коэффициенты уравнения А и B для изучаемого состава электролита и температуры 250С равны, соответственно, 1,135 и 0,8).
Методом ВИМС установлено, что поверхностные слои сплава содержат большое количество Zn и при перемещении вглубь на 1,5 мкм содержание Zn и Ni несколько меняется (табл. 5).
Таблица 5
Содержание Zn и Ni на поверхности сплава Zn-Ni и на глубине 1,5мкм при электроосаждении из электролита состава: Zn-Ni 0,44М + NiCl2 0,38М + Н3ВО3 0,32М
| Компоненты сплава | Содержание компонентов, % | |||
| iк=15·10-3, А/см2 | iк=17·10-3, А/см2 | |||
| =0 мкм | =1,5 мкм | =0 мкм | =1,5 мкм | |
| Ni | 8,96 | 18,63 | 9,05 | 12,03 |
| Zn | 65,05 | 75,43 | 71,78 | 75,43 |
Меньшее содержание никеля в сплаве Zn-Ni по результатам ВИМС по сравнению с данными масс-спектрального анализа можно объяснить тем, что основное количество Ni осаждается в начальный момент электролиза, а также затрудненностью электровосстановления комплексных соединений никеля с Н3ВО3. О включении продуктов взаимодействия Н3ВО3 с компонентами электролита в состав осадка свидетельствуют спектр соединений, присутствующих в покрытии (рис. 9). Проведенным анализом подтверждено наличие в сплаве гидроксида цинка.
Для покрытий сплавом Zn-Ni, получаемых из хлористых электролитов в изучаемом диапазоне плотностей тока, характерны адгезия, соответствующая ГОСТ 9.302-79, и равномерность осадка (рис. 10). Массовый показатель коррозии для сплавов, электроосажденных в диапазоне плотностей тока от 13·10-3 до 17·10-3 А/см2 лежит в пределах от 0,83·10-4 до 1,16·10-4 г/см2·ч для толщины покрытия 10 мкм и от 0,66·10-4 г/см2·ч до 0,25·10-4 г/см2·ч для 15 мкм, что в 2-3 раза меньше Кмасс для электролитического никеля, осажденного из сернокислого электролита. Выход по току для электроосажденного сплава возрастает при увеличении iк до 17·10-3 А/см2 до 82,6-85,2%. Микротвердость сплава зависит от плотности поляризующего тока (табл. 6).

Рис.9. Концентрационные профили компонентов сплава Zn-Ni, полученного из электролита состава Zn-Ni 0,44М + NiCl2 0,38М + Н3ВО3 0,32М, при iк=17·10-3, А/см2

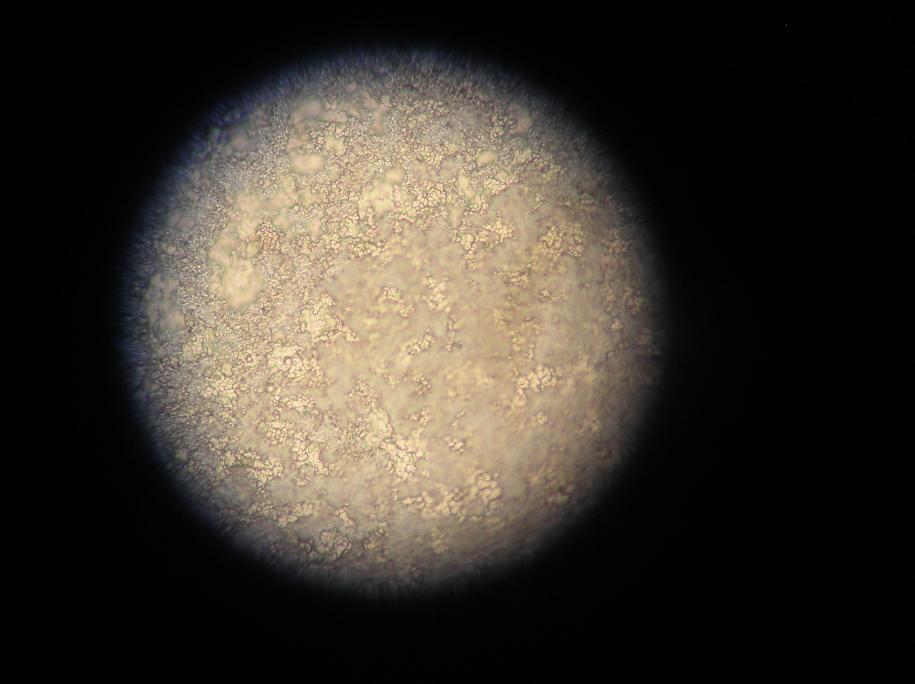
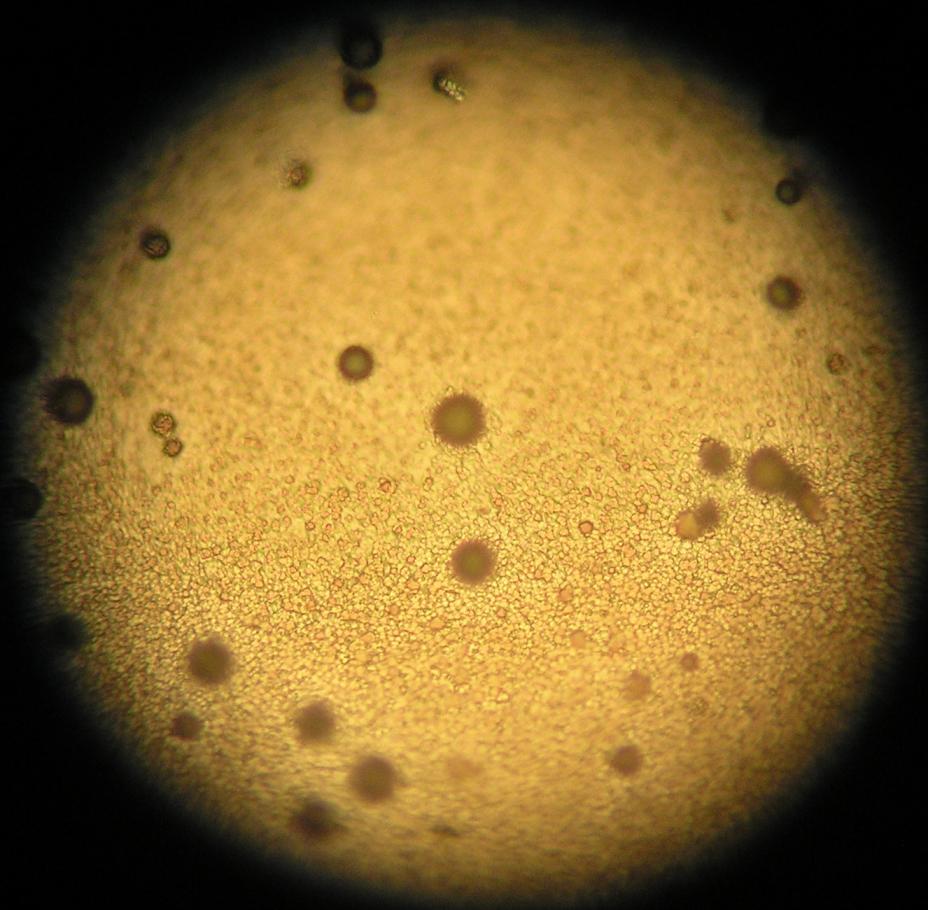
а б в
Рис. 10. Микрофотографии поверхности стального образца с нанесенным покрытием цинк-никель толщиной 15 мкм, при i·10-3, А/см2: 13 (а); 15 (б); 17 (в) из электролитов состава: ZnCl2 0,44 M + ZnCl2 0,38 М ( 500)
Таблица 6
Микротвердость (Н) сплавов Zn–Ni, электроосажденных из хлористых электролитов при 250С.
| Состав электролита | Н, кг/мм2 | ||
| 15·10-3, А/см2 | 17·10-3, А/см2 | 25·10-3, А/см2 | |
| ZnCl2 0,44 М + NiCl2 0,38 М | 123,6 | 116,8 | 99,5 |
| ZnCl2 0,44 М+NiCl2 0,38 М + Н3ВО3 0,32 М | 119,5 | 113,6 | 95,8 |
4.5. Электроосаждение КЭП на основе Zn с коллоидным графитом.
Известно, что КЭП электроосаждаются в широком диапазоне рН. Возможность получения равномерных с хорошей адсорбцией покрытий во многом зависит от способности ионов электролита взаимодействовать с частицами дисперсной фазы.
Гальваностатические исследования электроосаждения КЭП Zn+Сколл на стальную основу из электролита, содержащего хлорид цинка и борную кислоту, показало, что характер зависимости Е, t в присутствии коллоидного графита не меняется (рис. 11, 12, 4).
-Е, В -Е, В
1 1
2
2 3
t, c t, c
| Рис.11. Е, t кривые электроосаждения Zn на сталь 10 кп, при i = 17·10-3 А/см2, t=250С из электролитов состава: 1- 0,44 М ZnCl2 + 0,32 М Н3ВО3; 2-0,44 М ZnCl2 + 0,32 М Н3ВО3 + Сколл 10 мл/л. | Рис.12. Е, t кривые электроосаждения Zn на сталь 10 кп, при i = 17·10-3 А/см2, t=250С из электролитов состава: ХМ ZnCl2 + 0,32 М Н3ВО3 + 10 мл/л Сколл моль/л: 1- 0,36 (1), 2-0,44 (2), 3-0,183 (3). |
Однако потенциал максимума становится более положительным сглаживается его скачкообразное изменение во времени. Используя представления о том, что коллоидный графит в хлористом электролите способен взаимодействовать с ионами Сl- и приобретать дополнительный отрицательный заряд, можно предположить укрупнение его размеров за счёт дополнительной адсорбции ионов Zn 2+. При электроосаждении покрытия в стадии разряда будут участвовать ионы цинка и частицы коллоидного графита с адсорбированными ионами электролита Zn 2+ и Сl-. Включение Сколл в гальванический осадок экранирует часть поверхности, уменьшает скорость выделения водорода, и, соответственно, снижает содержание гидроксидных соединений цинка в покрытии, о чём свидетельствует смещение стационарного потенциала в область более отрицательных значений. При изменении концентрации ZnCl2 от 0,183 до 0,44 М быстрее происходит достижение стационарного потенциала (рис.12).
Перенапряжение кристаллизации электроосаждения КЭП Zn-Сколл лежит в пределах 0,400,42 В, что меньше данной характеристики для электролита ZnCl2 без добавки Сколл (кр=0,5 В). Следовательно, облегчается процесс формирования осадка.
Поляризационная ёмкость процесса электроосаждения КЭП Zn-Сколл, при катодной плотности тока 1710-3 А/см2 составляет 0,0051 Ф/см2. Эта величина меньше Сколл для электроосаждения цинка из электролита состава ZnCl2 0,44 М + Н3ВО3 0,32 М (Сколл – 0,056 Ф/см2), что может служить подтверждением участия частиц коллоидного графита в электрохимическом процессе. Покрытия Zn-Сколл, полученные на стали 10 кп из электролита состава ZnCl2 0,44 М + Н3ВО3 0,32 М + Сколл 10 мл/л при i=1710-3 А/см2, тёмно-серого цвета, с явно выраженной шероховатостью. Они легко механически полируются, образуя покрытия, прочно сцепленные с основой.
Введение соли никеля (0,38 М) в электролит ZnCl2 0,44 М + Н3ВО3 0,32 М + Сколл 10 мл/л приводит к уменьшению Спол, что связано с участием в электрохимическом процессе соединений никеля и коллоидного графита с адсорбированными ионами никеля. Электроосажденный сплав серого цвета. С ростом толщины покрытия увеличивается количество Сколл на поверхности электрода, что также требует полировки поверхности.
Полученные покрытия Zn-Ni-Сколл обладают большей коррозионной стойкостью, чем сплав Zn-Ni, осажденный при тех же условиях (табл.7), и меньшим (~ в 2 раза) коэффициентом трения.
Таблица 7
Значения массового коэффициента коррозии покрытий полученных из электролитов ZnCl2 0,44 + NiCl2 0,31 и ZnCl2 0,44 + NiCl2 0,31 + Сколл, при i=15·10-3 А/см2, =15 мкм
| С Сколл, мл/л | Кмасс10 -4, г/чсм2 |
| 3 | 0,3 |
| 0 | 0,7 |
Выводы
- Изучение физико-химических и термодинамических свойств одно- и двухкомпонентных электролитов, содержащих ZnCl2 и NiCl2, показало, что в изучаемом интервале концентраций компонентов устанавливается равновесие между структуроразрушающим и структуроупорядочивающим воздействием ионов Cl- и Zn2+, Ni2+ на структуру воды. Это проявляется в незначительном уменьшении электропроводимости растворов и термодинамических характеристик вязкого течения в наиболее концентрированных растворах. Установлено, что снижение электропроводности суспензии ZnCl2 + NiCl2 + Сколл. по сравнению с раствором ZnCl2 + NiCl2 связано со способностью частиц Сколл. адсорбировать на своей поверхности ионы. Выделен диапазон концентраций солей, представляющих интерес для практического применения: (ZnCl2 0,44 М, NiCl2 0,308 – 0, 385 М).
- Установлено, что электроосаждение сплава Zn-Ni из хлористого электролита протекает через стадию адсорбции разряжающихся частиц (ГЕ лежит в пределах от 0,6·10-6 до 13·10-6 моль/см2), в результате которой поляризационная ёмкость процесса изменяется от 0,0086 до 0,060 Ф/см2. Сплав Zn-Ni формируется через стадию образования двухмерных зародышей.
- Показана взаимосвязь процессов, происходящих в объёме раствора с процессами на границе раздела фаз: установлена зависимость поляризационной ёмкости процесса электроосаждения сплава Zn-Ni от концентрации соли никеля в электролите.
- Методами лазерной масс-спектроскопии, ВИМС проведён анализ качественного и количественного состава сплава Zn-Ni. Установлено наличие в сплаве Zn-Ni, гидроксидов цинка, продуктов взаимодействия Н3ВО3 с компонентами электролита. Установлено, что наблюдается прямо пропорциональная зависимость между количеством электроотрицательного компонента (Zn) и плотностью поляризующего тока. Это позволяет спрогнозировать содержание компонентов в сплаве в зависимости от плотности тока.
- Впервые получены КЭП Zn-Сколл, Zn-Ni- Сколл, обладающие большей коррозионной стойкостью по сравнению с покрытиями Zn и Zn-Ni, осажденных из исследуемых хлористых электролитов при соответствующих им режимах.
- Установлен режим (15-1710-3А/см2) осаждения сплава Zn-Ni из хлористого электролита состава: ZnCl2 0,44 М + NiCl2 0,38 М+ Н3ВО3 0,32 М, при котором возможно получить равномерное, коррозионно-стойкое, с хорошей адгезией матовое покрытие.
Основные положения диссертации отражены в следующих работах:
В изданиях рекомендованном ВАК РФ
- Гусев М. С. Физико-химические свойства растворов электроосаждения сплава Zn-Ni / М. С. Гусев, Н. Д. Соловьёва // Вестник Саратовского государственного технического университета. 2007. №2 (2). Вып. 2. С. 84-88.
В других изданиях
- Гусев М. С. Выбор малоконцентрированного электролита для электроосаждения сплава цинк-никель. / М. С. Гусев, Н. Д. Соловьёва // Перспективные полимерные композиционные материалы. Альтернативные технологии. Переработка. Применение. Экология: докл. Междунар. конф. «Композит–2007», Саратов: СГТУ, 2007. C. 88-91.
- Гусев М. С. Электроосаждение сплава Zn-Ni из хлористых электролитов / М. С. Гусев, Н. Д. Соловьёва // Защитные и специальные покрытия, обработка поверхности в машиностроении и приборостроении: сб. статей IV Всерос. науч.-практ. конф. Пенза 2007. C. 33-35.
- Гусев М. С.Соловьева Н. Д., Попова Н. Е. Влияние режима электролиза на свойства цинк-никелевых сплавов // Покрытия и обработка поверхности: сб. тез. докл. 5-ой Междунар. конф. Москва. 9-11 апреля 2008 г. - М., 2008. - C. 39-41.
- Гусев М. С., Соловьева Н. Д., Краснов В. В. Процессы в электролитной системе, используемой для электроосаждения КЭП Zn-Ni-коллоидный графит // Электрохимия и экология: материалы Всеросс. конф. Новочеркасск. 17-20 сентября 2008г. - Новочеркасск: ЮРГТУ, 2008. - C. 29.
- Гусев М. С., Соловьева Н. Д. Электроосаждение сплава цинк-никель из малоконцентрированного хлористого электролита // Современные методы в теоретической и экспериментальной электрохимии: тез. докл. 1 Междунар. науч. конф. г. Плес, Ивановская обл. 23-27 июня 2008 г. - Иваново: ИГХТУ, 2008 - C. 43
- Гусев М. С., Соловьева Н. Д., Краснов В. В. Электропроводность электролитной системы для электроосаждения КЭП Zn-Ni-коллоидный графит // Актуальные проблемы электрохимической технологи: сб. статей молодых ученых. - Саратов: Сарат. гос. техн. ун-т, 2008. - С. 234-236.
Гусев Михаил Станиславович
Кинетические закономерности электроосаждения сплавов и Композиционных Электрохимических Покрытий на основе цинка, полученных из малоконцентрированных кислых электролитов
Автореферат
Корректор О.А. Панина
| Подписано в печать ________08г | Формат 60х84 1/16 |
| Бум.тип. Усл. печ. л. 1.0 | Уч.-изд.л. 1.0 |
| Тираж 100 экз. Заказ ___ | Бесплатно |
| Саратовский государственный технический университет 410054, г. Саратов, ул.Политехническая, 77 | |
| Отпечатано в РИЦ СГТУ, 410054, г.Саратов, ул. Политехническая, 77 | |

