ӯ ров ӯ на дипреноидные спирты, альдегиды и имины в реакциях фосфорили ӯ рования
На правах рукописи
Большакова Ольга Владимиӯровӯна
дипреноидные спирты, альдегиды и имины
в реакциях фосфорилиӯрования
02.00.08 - химия элементоӯоргаӯнических соединеӯний
А в т о р е ф е р а т
диссертации на соискание ученой степени
кандидата химических наук
Казань - 2010
Работа выполнена на кафедре химии ГОУ ВПО «Татарский государственный гуманитарно-педагогический университет» и кафедре высокомолекулярных и элементооорганических соединений ГОУ ВПО "Казанский государственный университет им. В.И. Ульянова-Ленина".
Научный руководитель: доктор химических наук Низамов Ильяс Саидович
Официальные оппоненты: доктор химических наук,
профессор Катаев Владимир Евгеньевич
доктор химических наук, профессор Никитина Лилия Евгеньевна
Ведущая организация: Казанский государственный технологический университет
Защита состоится 1 июля 2010 г. в 1200 ч на заседании диссертационного совета Д 212.081.03 по защите диссертаций на соискание ученой степени доктора и кандидата наук в Казанском государственном университете им. В.И. Ульянова-Ленина по адресу: 420008, г. Казань, ул. Кремлевская, 18, КГУ, Бутлеровская аудитория.
С диссертацией можно ознакомиться в научной библиотеке им. Н.И. Лобачевского Казанского государственного университета.
Электронный вариант автореферата размещен на сайте Казанского государственного университета www.ksu.ru
Отзывы на автореферат, заверенные печатью, просим направлять по адресу: 420008, г. Казань, ул. Кремлевская, 18, Казанский государственный университет, научная часть.
Автореферат разослан 25 мая 2010 г.
Ученый секретарь диссертационного
совета, кандидат химических наук, доцент Казымова М.А.
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность работы. Одной из фундаментальных проӯблем химии приӯродных соединений является созӯдаӯние новых типов фосформодиӯфициӯрованных производных изопреноидов. Эти соединения явӯляӯются персӯпекӯтивными биореӯгуляӯторами, играюӯщими важную роль в продуцировании живыми организмами углеводсодерӯжаӯщих биопоӯлиӯмеров ряда (липо)полиӯсахаӯридов, гликопротеинов и пептиӯдогликанов. Между тем в настоящее время ветеӯринария и медицина исӯпытывают потӯребӯӯность в новых лекарӯстӯвенных средствах биорегуӯляторӯноӯго типа. Среди природных преноидов найдены вещества, проявляющие протиӯвоӯязвенную, ранозаживляющую, гипотенӯзивӯную, антитромӯбозӯную, протиӯвоопуӯхолевую, антигипертензивную, анӯдренергическую, антиульӯцеӯрогенӯную, гиперпротекторную и антигиперӯхолестеӯринеӯмическую активность, а также участвующие в норӯмализации иммунӯной функции, в восстановлении функций печени, являющиеся растӯворителями желчӯных камней. В то же вреӯмя недостаточное внимание уделено синтетическим фосфорилироӯванӯным ӯпреӯноӯидам. Между тем введение фосфорсодержащих фрагментов в молекулу преноидов может привести к созданию биологически активных веществ различного действия, являющихся базой для полуӯчения лекарственных средств нового поколения, что составляет актуальную задачу.
Целью работы является синтез новых фосфорилированных произӯводӯных дипренӯоиӯдов путем введения фосфорсодержащих фрагментов в молекулы дипреноидных диенильных спиртов, альдегидов и иминов и выявление среди полученных продуктов соединений с биологической активностью.
Научная новизна работы. Синтеӯзиӯрованы ранее неизвестные непреӯдельӯные дипреноидные фосфиты, имеӯюӯӯщие структурный фрагмент O-PO2, с различной геоӯметрической конӯфиӯгуӯрацией диенильных фрагментов на основе нерола и гераниола (Е- и Z-изомеров 3,7-диметил-2,6-октадиен-1-ола) и (R,S)-линалоола. В отличие от известных ранее,-ненасыщенных фосфитов полуӯченные в работе непредельные фосфиты и фосфиниты вторичных скелетных перегруппировок не претерпевают.
Впервые установлено региоспецифическое образоӯвание продуктов 1-алкилӯамииӯноӯӯфосӯфоӯнатӯного строӯения в реакции диалкилфосӯфитов с E,Z-циӯтӯралем, (R,S)-циӯтӯроӯнелӯлалем и (1R)-(–)-миртеналем в присутствии первичного алиӯфатического амина с учасӯтием карбонильной группы непредельного дипреноидного альӯдеӯгида по схеме реакции Кабачника-Филдса. При этом реакция Пудовика с приӯсоеӯдиӯнеӯнием фосӯфорӯсоӯдерӯжащих фрагӯментов по двойным связям неӯпреӯдельного дипреноидного альдегида в выбранных мягких условиях не реалиӯзуется.
Впеӯрӯвые получены непредельные дипреноидные имины с испольӯзоӯванием E,Z-цитӯраля и (R,S)-цитронеллаля и первичных аминов, в том числе оптически активных, в качестве промежуточных продуктов получения коӯнечӯных 1-аминофосфонатов в реакӯции Каӯбачӯӯника-Филдса. Найдено, что при обӯразовании иминов из перӯвичных аминов и E,Z-цитраля соотӯношение Z- и E-изоӯмеров меняется от 1:1 в исӯходном цитрале до 1:2 для соотӯветӯстӯвуюӯщих имиӯнов. При иминиӯровании (R,S)-цитронеллаля алкилӯамиӯнаӯми обраӯзуӯется рацемическая смесь изоӯмеров.
Реакция Пудовика иминов E,Z-цитраля с диалкилфосфитами протекает по схеме 1,2-присоединения с образованием 1-алкиламинофосфонатов. В этих реакциях в мягких усӯлоӯвиӯях обраӯзоӯвания проӯдуктов 1,4- и 3,4-присоедиӯнения по схеме реакӯции Пудовика не происходит.
В отличие от известных реакций,-ненаӯсыӯщенных иминов с диалкилӯтриӯӯметилӯсилилфосфитами, приводящих после обработки водой к 1,3-дифосӯфоӯнатам через тандемное двухкратное 1,4- и 1,2-приӯсоедиӯнение, впервые устаӯновлено, что реакции имиӯнов E,Z-циӯтӯраля с диалкилӯтриӯӯметилӯсилилӯфосӯфитами в присутствии воды или диэтиламина протекают региоспецифически с участием связи C=N и образованием 1-алкилӯаминоӯфосӯфонатов.
Практическая значимость работы. Ряд новых фосфорӯмодифиӯциӯроваӯнных непреӯдеӯльӯных дипреноидов с фрагӯментом C-O-P(III) получен на основе реакций дипреноидных диӯеӯниӯльӯных спиртов с хлорӯфоӯсӯӯфиӯтами, хлорӯфосӯфиӯнами и циклиӯческими амидофосфитами, содержащими лаӯбильӯные свяӯзи P-Cl и P-N. Модифицирован способ получения непреӯдеӯльных дипреӯноӯидӯных 1-гидӯроксиӯфосӯфоӯнатов с использованием реакции диалкилӯфосӯфиӯтов с E,Z-циӯтӯралем в присутствии триэтилӯамина при большом разӯбавӯлении в соотӯветӯстӯвуюӯщих спиртах, что позволило повысить выходы и чистоту целевых проӯдуктов. Неизвестные ранее непреӯдельӯные дипреӯноӯидӯные 1-алкилӯамиӯноӯӯфосӯфоӯнаты сиӯнӯтеӯзированы при введении E,Z-циӯтӯраля, (R,S)-циӯтӯронеллаля и (1R)-(–)-мирӯтеӯнаӯля) во взаимоӯдействие с диалӯкилӯӯфосӯфитами в присутствии перӯвичӯных алиӯфаӯӯтиӯческих амиӯнов в мягких условиях.
Среди дипреноидных иминов и 1-алкиламинофосфонатов с дипреноӯидӯными заместителями найдены веӯщеӯсӯӯтва, обладающие бакӯтериоӯстаӯтиӯчесӯкой и фунӯгистатиӯчесӯкой активностью. Наиболее эффективно подавляют рост бакӯтерӯий Staӯphyӯlococcus aureus и Bacillus cereus оптически активные левоӯвраӯщаюӯщие непредельные дипреӯноӯидӯные имины, содержащие хиӯраӯльӯные центры в алкилӯарильном фрагменте у атома азота. 1-Алкиламинофосфонаты окаӯзались наиболее активными по отношению к Staӯphyӯlococcus aureus и Bacillus cereus.
Апробация работы. Основные результаты работы докладывались и обӯсуӯжӯӯдались на итоговых научных конференциях Каӯзанӯсӯкоӯго наӯучӯноӯго центра РАН (Казань, 2005-2008 гг.); XIV-ой и XV-ой международных конференциях по химии соединений фосфора (г. Казань, 2005 г., г. С.-Петербург, 2008 г.); VIII-ой молодежной научной школе-конференции по органической химии (г. Казань, 2005 г.); четвертой международной конференции молодых ученых “Современные тенденции в органическом синтезе и проблемы химического образования” (г. С.-Петербург, 2005 г.); IV-ой Всероссийской научной конференции “Химия и технология растительных веществ” (г. Сыктывкар, 2006 г.); V-ой и VI-ой научных конференциях молодых ученых, аспирантов и студентов научно-образовательного центра Казанского государственного университета "Материалы и технологии XXI века" (г. Казань, 2005 г., 2006 г.); IV-ой Всероссийской научной конференции “Химия и технология растительных веществ” (г. Сыктывкар, 2006 г.), XV-ой международной конференции по химии соединений фосфора (г. С.-Петербург, 2008 г.).
Публикации. Основное содержание диссертации изложено в 16 пуӯбӯӯлиӯкаӯциях, в том числе в 5 статьях, тезисах 11 докладов на международных и Всероссийских конференций.
Объем и структура диссертации. Диссертация состоит из введения, трех глав, списка литературы и приложения; включает 2 таблицы, 26 риӯсунков и биӯбӯлиографию из 125 литературных ссылок. В первой главе приӯведен литеӯраӯтурӯный обзор, посвященный синтетическим фосӯформоӯдиӯфицированным изопреӯноӯидам. Во второй главе обсуждаются реӯзультаты исследования автора. В третьей главе приводится описание экспеӯриӯменӯтов. В приложении содерӯжатся рисунки спектров полученных продуктов.
Диссертационная работа поддержана грантами РФФИ-Татарстан № 03-03-96208, № 07-03-00617-а, академии наук Республики Татарстан № 07-7.2-182/2003(Ф) и молодежӯным грантом Reg. 007 научно-образовательного центра (CRDF) Казанского государственного университета (2004-2005 гг.) «Фосфорилирование 1,5-полиенов и их низкоӯмолекуӯлярӯных анаӯлоӯгов».
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Реакции дипреноидных диенильных спиртов с хлорфосфитами,
хлорфосфинами и амидофосфитами
Среди природных ациклических изопреноидов ряда дипреноидов с числом атомов углерода С10 в качестве субстратов для фосфорилирования нами выбраны доступные диӯеӯниӯльные спирты такие, как гераниол (E-изомер 3,7-диметил-2,6-октадиен-1-ола) 1, неӯрол (Z-изомер 3,7-диметил-2,6-окӯтаӯдиен-1-ола) 2 и линалоол (рацемическая смесь (+)-коӯриӯандрола и (-)-ликареола) 3 под действием хлоридов и амидов трехӯкоорӯдиниӯроӯванноӯго фосфора. Показано, что реакӯция диэтилӯхлорӯфосфита 4 с нероӯлом 2 протекает в теӯчение 1 ч в приӯсутӯстӯвии триӯэтиламина в бензоле с экзотерӯмиӯческим эфӯфектом и обраӯзованием 1-(Z-3,7-диӯметил-2,6-октаӯдиеӯнил)ӯдиэтилфосфита 5 (реакция 1). Для синӯтеза E-изомера 6 использована реакция диэтилӯхлорӯфосӯфита 4 с геӯраниолом 1 в приӯсутствии триэтиламина в растворе бенӯзола (реакция 2).
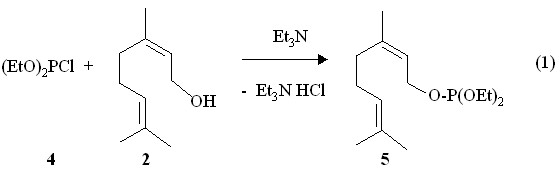

Продукты реакций (1) и (2) выӯдеӯлены с помощью приӯбора для молекулярно-пленочӯной пеӯреӯгонӯки. В спектрах ЯМР 31Р химический сдвиг ядра атома фосфора Z-изоӯмеӯра 5 расположен в более сильном поле (Р 138.3 м.д.) по сравнению с E-изоӯмеӯром 6 (Р 138.9 м.д.). Характерным структурным признаком полученных 3,7-диметил-2,6-октадиеӯнил)ӯдиӯэтилӯфосӯфиӯтов 5 и 6 являӯется наличие фрагмента CH2OP по соседству с непредельным фрагментом С=CH. В спектре ЯМР 1Н в растворе СDCl3 исходного нерола 2 метиленовые протоны у атома кислорода CH2O проявляются в виде дуӯбӯлета при 4.0 м.д. В спектре ЯМР 1Н Z-изоӯмеӯрного фосфита 5 сигналы проӯтонов метиленоксильной группы у атома фосфора С=CH-CH2OP принимают вид дублета дублетов при 4.45 м.д. (3JHH 6.9 Гц, 3JРH 9.0 Гц). В спектре ЯМР 1Н метиленовые протоны у атома кислорода CH2O исходного гераниола 1 дают дублет при 4.1 м.д. В спектре ЯМР 1Н E-изомерного фосфита 6 сигналы метиленовых протонов у атомов кислорода С=CH-CH2OP также смещены в сторону слабого поля (3JHH 7.5 Гц, 3JРH 9.0 Гц).
Нами показано, что реакция рацемического линалоола 3 с диэтилӯхлорӯӯфосӯфитом 4 в приӯсутӯствии триӯэтилӯамина в растворе бензола сопроӯвожӯдается неӯбольӯшим экзоӯӯтерӯӯмиӯческим эффектом и заверӯшается обраӯзованием 3-(3,7-диметил-1,6-октадиӯенил)ӯдиӯэтилӯфосӯфиӯта 7 в виде смеси R,S-изомеров, выделеных на приӯборе для молекулярно-плеӯночӯной пеӯрегонки (реакция 3).
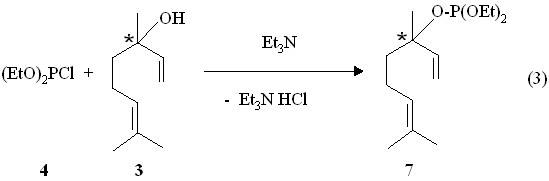
Сигнал ядра атома фосфора соединения 7 в спектре ЯМР 31Р в бенӯзольном растворе находится в более высоком поле (Р 134.3 м.д.), чем Z- и E-изомеры 3,7-диӯмеӯтил-2,6-октадиенил)диэтилӯфосӯфиӯта 5 и 6. Для соединения 7 характерно присутствие метильной группы у атома С3 (фрагмент СН3C=CH), протоны которых в спектре ЯМР 1Н проявляются в виде уширенного синглетного сигнала при 1.48 м.д. В масс-спектрах элекӯтронӯного удара непреӯдельӯных дипреноидных фосфитов 5, 6 и 7 имеются массовые пики m/z 274 их молекуӯлярных ионов [M]+. (выӯчислено М: 274.2).
Для получения преноидных производных, содержащих связи P-C, можӯно использовать диорганилхлорфосфины. Дифенилхлорфосфин 8 фосфорилирует с экзоӯтерӯӯмическим эффектом гераниол 1 в бензоле в приӯсутӯствии триӯэтилӯамина при 20 оС (4 ч) с образованием О-(E-3,7-диметил-2,6-октадиен-1-ил)дифеӯнилӯфосфинита 9 (реакция 4).

В спектре ЯМР 31Р О-геранилӯдифенилфосфинита 9 в растворе бензоӯӯла содержится синглетный сигнал при Р 111.8 м.д., что согласуется с трехкоординированным атомом фосфора с окружением Ph2POR. В спектре ЯМР 1Н в растворе СDCl3 фосфинита 9 наӯряду с сигналами протонов гераӯниӯльного замеӯстителя содержатся два муӯльӯтиплета при 7.28-7.58 и 7.67-7.70 м.д. протонов двух фенильных групп. В масс-спектре элекӯтронного удара ӯфосӯфинита 9 присутствует масӯсовый пик m/z 338, который соответӯствует его моӯлеӯкуӯлярӯному иону [M]+. (вычислено М: 338.2).
Впервые установлено, что в отличие от,-ненасыщенных фосфитов полученные дипреӯноӯидные диенильные фосфиты вторичных скелетных перегруппировок не преӯтерпевают (подобно [2,3]-сигматропной перегруппировки при кипячении в течение 5 ч толуольӯноӯго раствора аллилдиэтилфосфита с образованием 2-пропенилӯдиӯэтилӯфосфоната (Христов В.Ч., 1998 г.).
Биологическая акӯтивӯность зачастую обусловлена фармакофорными циклическими структурами. В связи с этим в качесӯтве фосфорилирующих агентов со связью P-N, нами использованы цикӯлиӯческие амидоӯфосӯфиты. Найдено, что при нагревании смеӯси нерола 2 и O,O-пропилен-N,N-диэтилӯамиӯдофосфита 10 до 140 оС с отгонкой диэтилӯамина обраӯзуӯется О-1-(Z-3,7-диметилокӯтаӯ-2,6-диӯенил)-1,3,2-диоксаӯфосӯфоӯӯриӯнан 11, выӯӯӯӯӯделенӯный на приборе для молекулярно-пленочӯной перегонки (реакция 5).
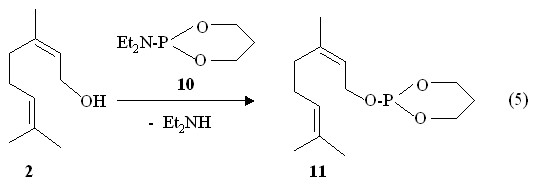
В спекӯтӯре ЯМР 31Р 1,3,2-диоксаӯфосӯфоринана 11 содержится синӯглетӯный сигӯнал при Р 129.4 м.д., в обӯласти, характерной для фосӯфиӯтов, что отличается от сигӯнала исӯходӯного амидоӯфосфита 10 (Р 145 м.д.). В спектре ЯМР 1Н 1,3,2-диоксаӯфосӯфоринана 11 при 3.47 и 3.48 м.д. имеются два дублета метильных протонов фрагмента C=C-CH2OP (3JPH 9.5 Гц). Массовый пик m/z 259.2, обнаӯруӯженӯный в масс-спектре химиӯческой ионизации 1,3,2-диоксафосӯфоӯриӯнаӯна 11, соответствует его молекулярному иону [M + Н]+.
Таким образом, реакции дипреноидных диӯеӯниӯльӯных спирӯтов с хлорӯфоӯсӯӯфитами, хлорфосфинами и амидофосфитами, содержащими лаӯбиӯльӯӯные свяӯзи P-Cl и P-N, открывают доступные подходы к фосформодифиӯциӯроваӯнным преноидам с фрагментом C-O-P(III).
1-Гидроксифосфонаты на основе E,Z-цитраля.
Модифицирование метода синтеза
Преноидные производные со связью C-P(IV), обладащие достаточно высокой гидролитической и термической стаӯбильностью, могут быть получены на основе реакций эфиров кислот трехӯвалентного фосфора с дипреноидными альдегидами. В молекулах непредельных дипреноидных альдегидов содерӯжитӯся неӯсӯколько реакционных центров (одна или две двойные связи и карбонильная группа). Поэтому структура продуктов их реакций с диалкилфосфитами не очеӯвидна, поӯсӯкольӯку возможно конкурентное приӯсоединение фосфорильных фрагӯменӯтов по карбоӯнильной группе цитраля (реакция Абраӯмоӯва), нукӯлеоӯфильное присоединение по 2,3-двойной связи С=С по схеме реакции Пуӯдовика и радикальное присоединение по 6,7-двойной свяӯзи С=С по реакции Пудовика в зависимости от выбранных условий реакции и строения реагентов.
В работах французских химиков (Kamal M., Montero J.-L. с сотр, 1999 г.) было показано, в условиях реакции Абрамова,-непредельные дипреноидные каӯрӯӯбоӯниӯльӯные соединения такие как цитраль и -ионон с диалкилфосфитом дают 1-гидроксиӯфосӯфонаты. Отметим, что 1-гидроксиӯфосӯфоӯнатам особенно с хиральными центраӯми в последнее вреӯмя уделяется большое внимание как биологически активным соединениям. В связи с умеренным выходом 1-гидроксиӯфосӯфоӯнатов на основе цитраля и их невысокой чистотой метод синтеза целевых продуктов модифицирован нами путем проведения реакции диалкилфосфитов 12а,б с E,Z-циӯтӯралем 13 в присутствии триэтиламина в моӯлярном соотӯноӯшении 2:1:4 при большом разбавлении в растворе соответстӯвуюӯщих спиртов при 40-55 оС в течение 16-17.5 ч с образованием О,О-диалкил-E,Z-1-гидрокси-3,7-диӯмеӯтилокӯтаӯ-2,6-диӯенилӯфоӯсӯӯфонатов 14а,б (выходы 87-88 %), выделенных с поӯмощью прибора для молекуӯлярно-пленочной перегонки (реакция 6).

О,О-Диӯ-изо-проӯпил-E,Z-1-гидрокси-3,7-диметилокӯтаӯ-2,6-диӯенилӯӯфоӯсӯфонаты 14б очиӯщены колоночной хроӯматоӯграфией. Их чистота подтверждена данными ГЖХ, которые показӯывает присутстӯвие двух изомеров соединения 14б. На хроматограмме имеӯютӯся 2 пика с временами удержиӯвания в толуоле 7.94 и 8.48 мин в соотношении 1:2. В спектре ЯМР 31Р смеси изомеровӯӯ ӯӯӯфоӯсӯфонатов 14б присуӯтӯствуют два синглетӯных сигӯнала при P 21.9 и 24.2 м.д. В спектре ЯМР 1Н О,О-диӯметил-E,Z-1-гидрокси-3,7-диӯметилокӯтаӯ-2,6-диӯеӯнилӯфоӯсӯфонатов 14а два мульӯтиӯплета при 5.02 и 5.27 м.д. относятся к винильным протонам фрагментов Me2C=CH и C=CH-CP соответственно. В ИК спектре О,О-диӯ-изо-проӯпил-E,Z-1-гидрокси-3,7-диметилокӯтаӯ-2,6-диӯенилӯӯфоӯсӯфонатов 14б содержатся полосы поӯгӯлощения при 3330 и 1665 см-1 валентных колебаний связей ОН и С=С соответственно. Двойные связи С=С E,Z-циӯтӯраля в реакции с диӯалкилфосфитами, таким образом, не затрагиваются. В масс-спектре элеӯкӯӯтронного удара О,О-диӯметил-E,Z-1-гидрокси-3,7-диӯметилокӯтаӯ-2,6-диӯеӯнилӯфоӯсӯфонатов 14а содерӯжиӯтӯся массовый пик m/z 262 [М+.], соотӯветӯстӯвующий его молекулярному иону. О,О-Диӯ-изо-проӯпил-E,Z-1-гидрокси-3,7-диметилокӯтаӯ-2,6-диӯенилӯӯфоӯсӯфонаты 14б в масс-спектре электронного удара дают массовый пик m/z 318 [M]+. их молекулярных ионов.
Следует отметить, что в отсутствие триэтиламина реакция (6) протекает медленно и с низким выходом продуктов 14а,б. Таким образом, нами модифицирован способ получения непредельных дипреноидных 1-гидӯрокӯсиӯфосӯфонатов на основе реакций E,Z-цитраля с диалкилфосӯфитами в основной среде путем большого разбавления соответствующими спиртами. Этот синтетический прием позволил повысить выходы и чистоту 1-гидроксиӯфосӯфоӯнатов. Присоединение диалкилфосфитов по связи С=О E,Z-цитраля происходит региоспецифически. Проӯдуктов присоединения по двойным связям С=С не обнаружено.
Фосфорилирование дипреноидных альдегидов
в условиях реакции Кабачника-Филдса
Перспективным направлением синтеза фосфорилиӯроӯваннӯных дипреӯноӯидов с фрагӯментом C-P(IV) может служить реакция дипреноидных альӯдеӯгидов с кислыми фосфитами в присутствии аминов со связями N-H (реӯакция Кабачника-Филдса). Нами найдено, что диэтилфосфит 13в реагирует с E,Z-цитралем 12 в приӯсутӯствии эквимольного количества изо-бутиламина 15а при 10-15 оС с обӯраӯзоӯваӯнием О,О-диӯэтил-1-(N-изо-бутилӯамино)-3,7-диметилокӯтаӯ-2,6-диӯенилӯӯфоӯсӯӯфоӯнаӯӯтов 16а в виде смеси E,Z-изоӯмеӯров (выход 95 %), очищенных перегонкой в вакууме (реакция 7).
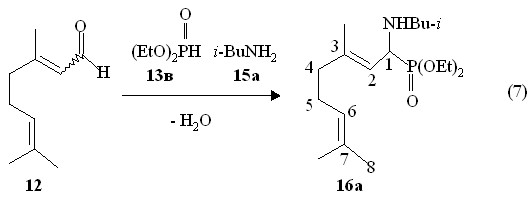
Спектр ЯМР 31Рӯӯ продуктов 16а содержит уширенный сигнал при P 24.6 м.д., что соответствует фосфонатам. В ИК спектре соединений 16а имеются две полосы поглощения при 3430 и 3306 см-1, характерные для валентных колебаний связи N-H. Масс-спектр элекӯтронного удара фосфоӯнаӯӯтов 16а содержит массоӯвый пик m/z 345.3, относящийся к их молекулярным ионам [М]+. . В спектре ЯМР 1Н двух изомерных проӯдукӯтов 16а метиновые протоны у атома фосфора (фрагмент PCH) дают два дублета дублетов при 3.74 м.д. (3JHH 9.9 Гц, 3JРH 12.5 Гц, 3JHH 2.9 Гц). При 4.18 м.д. и 5.11 м.д. находятся сигналы винильных протонов фрагӯменӯтов PCH-CH=C и (СН3)2C=CH, соответственно, что свидетельствует о сохранении двойных связей С=С в молекулах продукӯтов реакции (7). Таким образом, при взаимодействии диэтилфосфита с E,Z-цитралем в присутствии изо-бутиламина в мягких условиях происходит региоӯспеӯцифическое присоединение по связи С=О с образоӯванием продуктов 1-алкиламиноӯфосӯфоӯнатӯого строения. При этом реакция Пудовика с приӯсоедиӯнением фосӯфорӯсоӯдерӯжащих фрагментов по двойным связям С=С непредельного дипреноидного альдегида в выбранных мягких условиях реӯакции (7) не реалиӯзуется.
В случае (R,S)-цитронеллаля, который можно предӯстаӯӯвить в виде цитраля, гидрированного по 2,3-двойной связи, 6,7-двойная связь практически нереакционӯноӯспоӯсобна по отношению к присоединению фосфоӯрильных фрагӯменӯтов. Нами показано, что диэтилфосфит 13в в реакции с (R,S)-цитронеллалем 17 в приӯсутӯстӯвии изо-проӯпилӯамиӯна 15б или изо-буӯтилӯамина 15а дает О,О-диӯэтил-1-(N-алкиламино)-3,7-диметилокӯтаӯ-6-ӯенилфосӯфоӯнаӯты 18а,б с высокими выходами (до 98 %), выдеӯленные перегонками в вакууме (реӯакция 8). При использовании диэтилфосфита 13в реакция (8) сопровожӯдаӯется экӯзоӯтермическим эффектом.
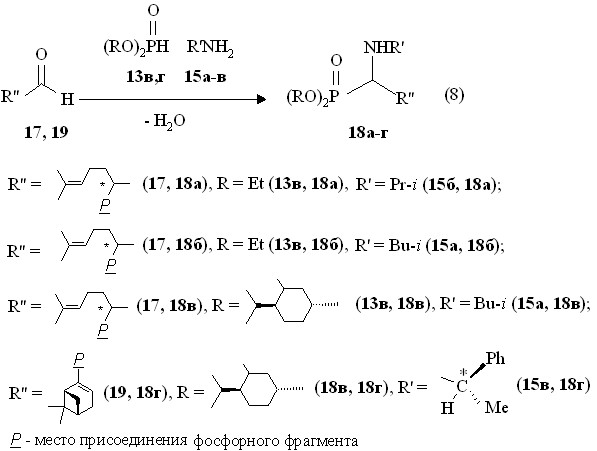
Предложенный подход к синтезу неӯпӯреӯдельных дипреноидных 1-амиӯнофосӯфоӯнатов (реакция 8) позволил ввести в эту реакцию диӯ[(–)-(1R,2S,5R)мент-2-ил]фосфит 13г с хиральным ӯпреӯноӯидными заместителями. Полученный на его основе О,О-ди[(–)-(1R,ӯ2Sӯ,5R)ӯӯмент-2-ил]-1-(N-изо-бутиламино)-3,7-диметилокӯтаӯ-6-ӯенилӯфосӯфонат 18в очиӯӯӯщен хроӯӯӯӯмаӯӯтоӯграфироӯваӯнием на коӯлонӯке. Масс-спектр электронного удара соединения 18в содержит массовый пик m/z 567.6, соответствующий его молекулярному иону [М]+.. Фосӯфонат 18в в спектре ЯМР 31Рӯӯ имеет синглептный сигнал при р 26.4 м.д. Спектры ЯМР 31Рӯӯ О,О-диэтил-1-(N-изо-проӯпиламино)-3,7-диӯмеӯтиӯлӯокӯӯтаӯ-6-ӯенил- фоӯсӯфонатов 18а и О,О-диӯэтилӯ-1-(N-изо-бутилӯамино)-3,7-диӯмеӯӯтилӯӯӯокӯӯтаӯ-6-енилӯфосӯфоӯнаӯтов 18б содержат по два сигӯнала при р 29.1 и 31.4 м.д. в соотноӯшении 14:1 и р 29.0 и 29.2 м.д. в соотӯношении ~1:1 соответственно. Эти сигналы относятся к двум диӯасӯтереомерам О,О-диӯэтил-1-(N-алӯкилӯамино)-3,7-диметилокӯтаӯ-6-ӯенилӯфоӯсӯфоӯӯнатов благодаря наличию двух асиӯмӯӯӯметрических центров - атомов углеродов C1 и С3. В спектре ЯМР 1Н О,О-диӯэтил-1-(N-изо-бутиламино)-3,7-димеӯтилӯокӯтаӯ-6-ӯеӯнӯилӯфосфонатов 18б метиновые протоны фрагмента Р-СН-СН2 проӯявӯляӯютӯся в виде двух дублетов триплетов при 3.72 и 3.90 м.д. (3JHH 7.0-7.3 Гц, 2JРH 15.4 Гц).
В развиӯтие этого подхода представляет интерес получить хиральные 1-аминоӯалӯкилфосфонаты при введении в реӯакӯцию Каӯбачӯӯника-Филдса трех опӯтически активных реагентов. С этой целью нами изуӯчеӯна реакӯция ди[(–)-(1R,2S,5R)мент-2-ил]фосфита 13г со смесью (1R)-(–)-миртеналя 19 и L-(–)--феӯнилэтиламина 15в, которая при кипячении реагентов в течение 14 ч в растворе безӯводӯного беӯнӯзола с использованием прибора Дина-Старка привела к образованию ди-O,O-(1R,2S,5R)-мент-2-ил[1-L-мирӯтеӯнил)-(N-1(L)-фенилӯэтилӯамиӯно)меӯтил]ӯфосӯфоӯнаӯта 18г (реакция 8). Продукт 18г является оптиӯчески активным ([]D22 -40.3о, c 1.0, C6H6), что согласуется со знаком угла оптиӯчесӯкоӯго враӯщеӯния исходных L-(–)--фенилэтиламина 15в ([]D20 -39о) и (1R)-(–)-миртеналя 19 ([]D20 -15о). В спектре ЯМР 31Рӯӯ ӯфосфоната 18г имеется сигнал при р 22.1 м.д. В спектре ЯМР 1Н соединения 18г метиӯновый проӯтон фрагмента PCH проявляется в виде дуӯбӯлета квартетов при 4.38 м.д. (3JHH 6.7 Гц, 3JРH 13.3 Гц). Соединение 18г в масс-спектре электронного удара дает молеӯкуӯлярный ион с массовым пиком m/z 611.8 [M]+.
Таким образом, реӯакӯция Каӯбачӯӯника-Филдса при использовании непредельных дипреноидных альдегидов позволяет получать 1-аминоӯфосӯфонаты, в том числе опӯтиӯчески активные, в одну стадию.
Имины на основе дипреноидных альдегидов
Учитывая, что одним из направлений полуӯчеӯния 1-амиӯнофосфонатов в реакции Каӯбачӯӯника-Филдса является образование проӯмежуточных иминов, нами изучены реакции непредельных дипреӯноидных альӯдегидов с первичӯныӯми амиӯнами, в том числе с хиральными. В этот вариант реакции Пудовика нами вовлечены те же E,Z-цитраль, (R,S)-цитронеллаль и (1R)-(–)-миртеналь, исӯпоӯльӯзоӯваннӯные выше в реакции Каӯбачӯӯника-Филдса (см. реакции 9 и 11). Установлено, что реакция E,Z-цитраля с этиламином (15г) (в виде хлоргидрата), изо-пропил- (15б), изоӯбутил- (15б) и н-бутиламинами (15д) в присутствии гидроксида калия при охлаждении до -20 оС приводит к 3,7-диметилокӯтаӯ-2,6-диӯенил-N-алкилӯиминам 20а-г в виде смеси E,Z-изомеров с выӯсокими выходами (84-87 %), очиӯщеӯнные перегонками в вакууме. Алкиламины вводилсь в реакции в 1.2-кратном избытке.
В ИК спектрах E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-бутилиминов 20а-г имеется сиӯльная полоса поглощения при 1651-1652 см-1 валенӯтных колеӯбаний связи С=N. В спектре ЯМР 1Н E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-диӯэтилиминов 20в соотношение меӯжӯду сигӯнаӯлами протона группы N=CH при 1 8.13 м.д. и 2 8.19 м.д. сосӯтавляет 1:2 (3JHH 9.5 Гц и 3JHH 9.2 Гц, соответственно).
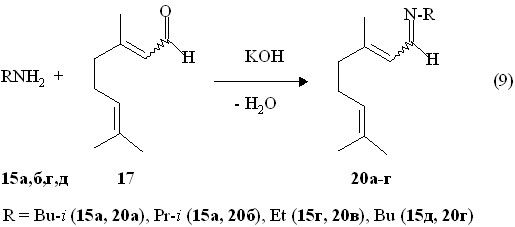
Таким образом, нами впервые установлено, что в проӯцесӯсе иминирования соотӯношение Z- и E-изомеров меняется от 1:1 в исӯходном цитрале до 1:2 для соответствующих иминов. Винильный протон (фрагмент C=CH-C=N) в спектре ЯМР 1Н E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-изо-буӯтиӯлӯӯиминов 20а проявляется в виде двух дублетов при 1 5.77 м.д. (3JHH 9.2 Гц) и 2 6.04 м.д. (3JHH 9.5 Гц). Масс-спектр химической ионизации E,Z-3,7-димеӯтилӯокӯтаӯ-2,6-диӯенил-N-изо-буӯтиӯлӯӯиминов 20а дает массовый пик m/z 208.3 их молекулярных ионов [M + Н]+. В масс-спектре электронного удара E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-изо-проӯпилӯимиӯнов 20б содержится массовый пик m/z 193.1, соответстӯвуӯюӯщий их молекулярным ионам [M]+..
В реакции (R,S)-цитроӯнелӯлаля 17 с изо-бутиламином 15а и изо-пропиламином 15б при охлаждении до -20 оС в присутствии КОН получены (R,S),E,Z-3,7-димеӯтилӯ-6-ӯенил-N-алкилӯимины 21а,б, выделенные перегонками в вакууме (реакция 10).

В ИК спектрах (R,S),E,Z-3,7-диметилокӯтаӯ-6-ӯенил-N-изо-бутилимиӯнов 21а имӯеӯӯется характерный набор полос поглощения валентных колеӯбаӯӯний свяӯзей С=N и C=С соответственно при 1669-1666 и 1637-1638 см-1. В спектре ЯМР 1Н (R,S),E,Z-3,7-диметилӯ-6-ӯенил-N-изо-ӯпроӯпилиминов 21б винильные протоны фрагмента N=CH дают два дублета при 1 7.64 и 2 7.65 м.д. (3JHH 5.1 Гц и 3JHH 5.2 Гц соответственно) в соотношении 1:1. В спектре ЯМР 1Н (R,S),E,Z-3,7-диметилокӯтаӯ-6-ӯенил-N-изо-бутилимиӯнов 21а соотношение дублетных сигналов проӯтонов у связи N=CH при 1 7.59 м.д. (3JHH 5.0 Гц) и 2 7.61 м.д. (3JHH 5.1 Гц) также равно 1:1. Таким образом, в реакӯции (R,S)-цитроӯнелӯлаля 17 с алкиламинами образуется смесь 1:1 изомеров.
При введении оптически активного L-(–)--фенил(этил)амина 15в во взаимодействие с (R,S)-цитроӯнелӯлалем 17 (-20 оС, КОН) получен оптически активный 3,7-димеӯтил-6-ӯенил-N-1-L--фенилӯ(этиӯл)ӯимин 21в ([]D22 -0.8 о, c 1.0, C6H6), выделенный пеӯреӯгонӯкой в вакууме (реӯакӯция 10). В спектре ЯМР 1Н ӯимина 21в при 1 7.77 м.д. (3JHH 5.1 Гц) и 2 7.79 м.д. (3JHH 4.4 Гц) содержится два дублета винильного протона группы CH=N в соӯотӯноӯшении 1:1
Представляет интерес ввести в реакцию имиӯниӯрования оба реагента в оптически активной форме. Установлено, что в реакӯции L-(–)--фенил(этил)амина 15в с (1R)-(–)-миртеналем 19 в присутствии КОН при -20 оС образуется оптически активный (1R),E,Z-(–)-миртенил-N-1-L-(–)--фенилӯ(этил)ӯимин 21г ([]D22 -17.8 о, c 1.0, C6H6) (реакция 10). Масс-спектр электронного удара имина 21г содержит массовый пик m/z 253.2, соотӯветствуюӯщий его молекулярному иону [M]+.. В спекӯтре ЯМР 1Н соединения 21г синглетный сигнал при 7.92 м.д. отнесен к винильному протону связи N=CH. При этом втоӯрого сигнала протона группы N=CH от другого вероятного изомера в спектре ЯМР 1Н не наблюдается. Полуӯченӯные имины могут служить в качестве исходных соединений реакциях фосфорилирования.
Реакции иминов дипреноидных альдегидов с диалкилфосфитами
В реакциях кислых фосфитов с непредельными иминами на основе E,Z-циӯтӯраля можно предположить следующие маршруты: 1) присоединение по связи C=N; 2) присоединение по 2,3-двойной связи); 1)+2) тандемное присоединение по связи C=N и 2,3-двойной связи С=С; 3) присоединение по 6,7-двойной связи. Направӯлеӯние 1 может служить модельной реакӯцией образования 1-аминофосфонатов по реакции Кабачника-Филдса E,Z-циӯтӯраля с диалкилфосфитами в присутствии первичных амиӯнов. Нами установлено, что в реакции E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-изо-буӯтилӯӯимиӯна 20а с диэтилфосфитом 13в при 20 оС образуются О,О-диэтил-E,Z-1-(N-изобутиламино)-3,7-диӯмеӯтилокӯтаӯ-2,6-диӯенилфосфонаты 16а (выход 90 %), выделенные перегонкой в ваӯкуӯуме (реакция 11).
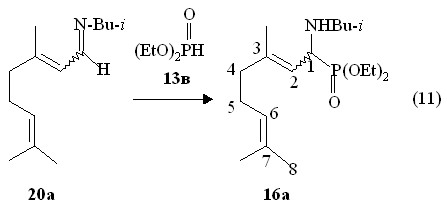
Параметры ИК спектров, спектров ЯМР 31Рӯӯ и 1Н и масс-спектров О,О-диэтил-E,Z-1-(N-изобутиламино)-3,7-диӯмеӯтилокӯтаӯ-2,6-диӯенилфосфонатов 16а, полученных во встречных синтезах (реакции 7 и 11), идентичны. Таким образом, в реакции иминов E,Z-циӯтӯраля с диалкилфосфитами реализуется направление, связанное с образованием 1-аминофосфонатов. Двухкомпонентная реакӯция дипреноидных иминов с диалкилфоӯсӯфитами дает возможӯность получать 1-алкилӯамиӯноӯӯфосӯфонаты более чистыми по сравӯнению с проӯдукӯтами реакции Кабачӯника-Филдса. В реакции Пудовика иминов цитраля с диалкилфосфитами образования продуктов с участием двойных связей С=С не происходит.
Реакции иминов E,Z-циӯтӯраля с диалкилcилилфосфитами
Известно, что при введении диалкилтриметилсилилфосфитов в реакции с,-ненаӯсыӯщенными иминами происходит тандемное двухкратное 1,4- и 1,2-приӯсоедиӯнеӯние с последующим образованием 1,3-дифосфонатов после обработки водой промежуточных продуктов (Стивенс С.В. с сотр., 2005 г.). В отличие от этого нами найдено, что в реакции (12) E,Z-3,7-диӯмеӯтиӯлокӯтаӯ-2,6-диӯенил-N-этилӯимиӯнов 20в и E,Z-3,7-диметилокӯтаӯ-2,6-диӯенил-N-буӯтиӯӯлӯимином 20г с диалкилтриметилсилилфосфитами 22а,б в присутствии конӯтроӯлируемых количеств воды или диэтиламина (20-70 оС, 1 ч) образуются О,О-диалкил-E,Z-1-(N-этил)-3,7-диӯмеӯтилокӯтаӯ-2,6-диӯенилфосфонаты 16в-г.
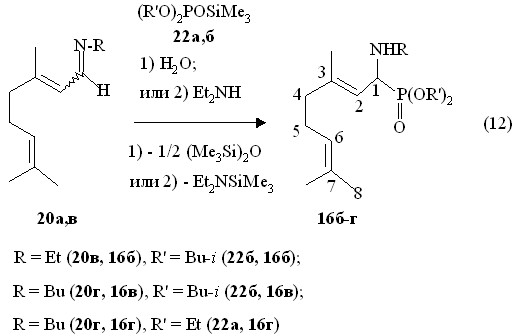
Соединения 16в-г имеют химические сдвиги в спектрах ЯМР 31Р при р 24.3-24.6 м.д., то есть в области, хаӯракӯтерной для 1-алкилӯаминоӯфосӯфонатов, полученных в реакциях (7) и (11). В спектре ЯМР 1Н О,О-ди-ӯизо-ӯбуӯтил-E,Z-1-(N-этил)-3,7-диӯмеӯтилӯокӯтаӯ-2,6-диӯенилӯфосфонатов 16б дублет дублетов при 3.60 м.д. относится к метиновому протону у атома фосфора (фрагмент PCH, 3JHH 6.6 Гц, 3JРH 14.0 Гц). Сохранение двойных связей С=С в молекулах продуктов реакции (12) подӯтӯверждается также присутствием сигналов при 5.08 м.д. и 5.93 м.д. в виде узких мультиплетов, характерных для винильных протонов (фрагӯменӯты PCH-CH=C и (СН3)2C=CH, соответственно). В масс-спектре элекӯтронного удара О,О-ди-ӯизо-ӯбуӯтил-E,Z-1-(N-этил)-3,7-диӯмеӯтилӯокӯтаӯ-2,6-диӯенилӯфосфонатов 16б имеется массовый пик m/z 373.4 их молекулярных ионов [М]+.. Массовый пик m/z 401.4, найденный в масс-спеӯкӯтре химической ионизации О,О-ди-изо-ӯбуӯтил-E,Z-1-(N-бутиламино)-3,7-диметилокӯтаӯ-2,6-ӯдиенилфосфонатов 16в, соответствует их молеӯкулярӯным ионам [M + Н]+.
Таким образом, параметры спектров продуктов 16в-г свидетельствуют о протекании реакӯции (12) с участием связи C=N непредельных диреноидных иминов. При этом двойӯные связи С=С не затрагиваются. Реакция иминов E,Z-циӯтӯраля с диалӯкилӯcилилфосфитами представляет собой еще один подход к синтезу непреӯдельных дипреноидных 1-алкилӯаминоӯфосӯфонатов.
Бактериостатическая и фунгистатическая активность
иминов цитраля и дипреноидных 1-алкиламинофосфонатов
Разработанные нами меӯтоӯды синтеза иминов цитраля и 1-алкилӯаминоӯфосӯфоӯнаӯтов, полученных на основе цитраля и цитронеллаля, предоӯсӯтавили возможность провести среди них поиск веществ, обладающих биологически активными свойӯстӯвами. Среди песӯтицидов знаӯчительӯный практический интерес представляют бактерицидные и фунӯгицидные препараты. В этой связи исследования по разработке средств заӯщиӯты проӯдуктов питания, кормов от токсикогенных бактерий и микроскопических грибов, лечению болезней, свяӯзанных с грибной этиоӯлогией, являются актуӯальӯными. Препаӯратов отеӯчественного производства для этих целей недосӯтаточно. С целью поиска бактирицидов и фунгицидов полученные имины цитӯраля и 1-алкиламинофосфонаты проӯшли испытания по отношению к патогенным бакӯтеӯриям и грибам Staӯphyӯlococcus aureus, Bacillus cereus, Escherichia coli и Aspergillus niger в лабоӯраӯтоӯрии химико-биологических исследований Учреждения РАН ИОФХ им. А.Е. Арбузова КазНЦ РАН. Установлено, что наибоӯльшую бактеӯриоӯстаӯтическую активность по отношению к Staӯphyӯlococcus aureus и Bacillus cereus проявляют (R,S),E,Z-3,7-диметил-6-ӯенил-N-1-L--фенилӯ(этил)имины (6.25 и 7.80 мг/л в ДМСО, соответственно). Им немного уступают (1R),E,Z-(–)-миртенил-N-1-L-(–)--фенил(этил)имины (125 и 250 мг/л, соответственно). Таким обӯраӯзом, наиболее эффективно подавляют рост грампоӯлоӯжиӯтеӯльӯных бакӯтерӯий оптически активные левовращающие непредельные дипреноидные имины, содержащие хиӯраӯльӯные центры в алкиларильном фрагменте у атома азота. 1-Алӯкилӯаминофосфонаты окаӯзались наиболее активными по отношению к Staӯphyӯlococcus aureus и Bacillus cereus и малӯоакӯтивӯными в отношении Escherichia coli и Aspergillus niger. Среди испытанных бактерий наиболее эффективно задерӯжиӯвается рост колоний зоӯлоӯтистого стафилококка (15.6-62.5 мг/л). По отношению Staӯphyӯlococcus aureus E,Z-1-(N-изо-бутилӯамино)-3,7-диметилокӯтаӯ-2,6-диӯенил-О,О-диэтилӯфоӯӯсӯӯфонаты, (R,S)-1-(N-изо-бутилӯамииӯно)ӯ-3,7-димеӯтилӯокӯӯтаӯ-6-ӯенил-О,О-диӯэтиӯлӯӯфосфоӯнаӯты и (R,S)-1-(N-изо-буӯтилӯамино)-3,7-диметилокӯтаӯ-6-ӯенил-О,О-диӯӯэтиӯлӯӯфосфоӯнаӯты проявляют фунгистатичсӯкое дейӯствие в конӯценӯтраӯции 15.6 мг/л. Полуӯченӯные результаты предӯставляют интерес для дальӯнейӯшего поиска биологически активных соединений в ряду фосфоӯриӯлиӯроӯванных дипреӯноӯидов.
выводы
1. Впервые установлено, что в отличие от,-ненасыщенных фосфитов новые непредельные фосфиты и фосфиниты c различной геометрической конфигурацией диенильных фрагментов, полученные на основе реакций Е- и Z-изомеров 3,7-диметил-2,6-октадиен-1-ола и (R,S)-линалоола с хлорфосфитами, хлорфосфинами и циклическими амидофосфитами, вторичных скелетных перегруппировок не претерпевают.
2. Модифицированный способ получения непредельных дипреноидных 1-гидӯрокӯсифосфонатов на основе реакции диалкилфосфитов с E,Z-цитралем в присутствии триэтиламина при большом разбавлении в соответствующих спиртах повышает чистоту целевых продуктов.
3. Реакции E,Z-цитраля, (R,S)-цитронеллаля и (1R)-(–)-миртеналя) с диалкилфосфитами в присутствии алкиламинов протекают региоспецифически с участием карӯбонильной группы по схеме реакции Кабачника-Филдса с образованием непредельных дипреноидных 1-алкиламинофосфонатов. Продуктов реакции Пудовика с участием двойных связей непредельных дипреноидных альдегидов не образуется.
4. В процессе образовании иминов из алкиламинов и E,Z-цитраля соотношение Z- и E-изомеров меняется от 1:1 в исходном цитрале до 1:2 для соответствующих иминов. При иминировании (R,S)-цитронеллаля алкиламинами образуется смесь 1:1 (R,S),E,Z-изомеров.
5. Реакция Пудовика иминов E,Z-цитраля с диалкилфосфитами протекают с участием связи C=N и образованием 1-алкиламинофосфонатов, при этом образования проӯдуктов с участием двойных связей С=С не происходит.
6. Впервые установлено, что в отличие от,-ненасыщенных иминов реакции иминов E,Z-цитраля с диалкилтриметилсилилфосфитами в присутствии воды или диэтиламина протекают с участием связи C=N и образованием 1-алкиламиноӯфосӯфоӯнатов.
7. Синтезированные дипреноидные имины и 1-алкиламинофосфонаты с непредельными дипреноидными заместителями обладают бактериостатической и фунгистатической активностью.
Основные результаты работы изложены в следующих публикациях
Публикации в изданиях, рекомендованных ВАК РФ,
для размещения материалов кандидатских диссертаций:
1. Низамов И.С., Большакова О.В., Низамов И.Д., Сергеенко Г.Г., Ямбушев Ф.Д., Батыева Э.С. Нерил- и геранил(диэтил)фосфиты // Журн. oбщ. химии. 2006. Т. 76, № 12. С. 2055-2056.
2. Низамов И.С., Большакова О.В., Низамов И.Д., Ямбушев Ф.Д., Сергеенко Г.Г., Батыева Э.С. 1-Гидрокси-3,7-диметилокта-2,6-диенил-О,О-диметилӯфосӯфонат. Разработка методов синтеза // Журн. oрг. химии. 2005. Т. 41, № 3. С. 472-473.
Другие статьи по теме диссертации
3. Nizamov I.S., Bolshakova O.V., Nizamov I.D., Sergeenko G.G., Mironov V.F., Yambushev F.D., Batyeva E.S., Alfonsov V.A. Development of methods of phosphorylation of citral by medial and acidic phosphites // Res. J. Chem. Envir. 2007. V. 11, N 3. P. 36-41.
4. Низамов И.С., Большакова О.В., Низамов И.Д., Ямбушев Ф.Д. Фосфорилирование диӯеӯнильных спиртов // Вест. Казанск. гос. педагог. ун-та. 2005. № 4. С. 172-176.
5. Низамов И.С., Ямбушев Ф.Д. Низамов И.Д., Больӯшакова О.В. Диенильные 1-гидроксифосфонаты // Вест. Казанск. гос. педагог. ун-та. 2005. № 4. С. 176-181.
Тезисы докладов
6. Низамов И.С., Большакова О.В., Низамов И.Д., Батыева Э.С., Миронов В.Ф. Фосформодифицирование низкомолекулярных аналогов полиӯпреӯноӯидов // IV Всеросс. науч. конф. “Химия и технология растительных веществ”: Тез. докл. Сыктывкар, 2006. С. 140.
7. Большакова О.В., Низамов И.С., Сергеенко Г.Г., Низамов И.Д., Василенко Г.И., Ямбушев Ф.Д., Батыева Э.С. Фосфорилирование диенильных кислот и спиртов // VI науч. конф. молодых ученых, аспирантов и студентов научно-образовательного центра Казанского госун-та “Материалы и технологии XXI века”: Тез. докл. Казань, 2006. С. 19.
8. Nizamov I.D., Nizamov I.S., Bolshakova O.V., Popovich Ya.E., Sergeenko G.G., Mironov V.F., Yambushev F.D., Batyeva E.S. Higher dienyl alcohols in phosphorylation reactions // XIV Intern. conf. on the chemistry of phosphorus compounds: Book of abstracts. Kazan, Russia, 2005. P103.
9. Nizamov I.S., Bolshakova O.V., Nizamov I.D., Mironov V.F., Batyeva E.S. Phosphorylated low-molecular weight analogues of native polyprenoides // XIV Intern. conf. on the chemistry of phosphorus compounds: Book of abstracts. Kazan, Russia, 2005. OP29.
10. Большакова О.В., Ахметзянова Л.Р., Низамов И.Д., Низамов И.С. Реакции фосфорилирования диенильных спиртов // VIII Молод. науч. школа-конф. по органической химии: Тез. докл. Казань, 2005. С. 103 (С1-60).
11. Ахметзянова Л.Р., Большакова О.В., Низамов И.С., Низамов И.Д. Цитраль в реакциях с фосфорорганическими соединениями // VIII Молод. науч. школа-конф. по органической химии: Тез. докл. Казань, 2005. С. 99 (С1-56).
12. Низамов И.Д., Большакова О.В., Ахметзянова Л.Р., Сергеенко Г.Г., Низамов И.С. Фосформодифицирование низкомолекулярных аналогов 1,5-полиенов // VIII Молод. науч. школа-конф. по органической химии: Тез. докл. Казань, 2005. С. 71 (С1-28).
13. Ахметзянова Л.Р., Низамов И.С., Большакова О.В., Низамов И.Д., Ерӯмолаев Е.С., Попович Я.Е., Миронов В.Ф., Батыева Э.С. Фосфоӯриӯлиӯрованные низкомолекулярные аналоги полипреноидов // Четвертая междунар. конф. молод. ученых “Современные тенденции в органическом синтезе и проблемы химического образования”: Тез. докл. С.-Петербург, 2005. С. 267-268.
14. Низамов И.Д., Большакова О.В., Ахметзянова Л.Р., Хайбуллин Р.Н., Низамов И.С., Миронов В.Ф. Моделирование процессов фосӯфоӯрилиӯроӯваӯния полиизопренилальдегидов // V Науч. конф. молодых ученых, аспирантов и студентов научно-образоӯваӯтельного центра Казанского госун-та "Материалы и технологии XXI века": Тез. докл. Казань: Казанский госун-т, 2005. С. 66.
15. Большакова О.В., Низамов И.Д., Попович Я.Е., Хайбуллин Р.Н., Ахӯметӯзянова Л.Р., Низамов И.С. Диенильные спирты в реакциях фосӯфориӯлиӯрования // V Науч. конӯф. молодых ученых, аспирантов и студентов наӯучӯно-образовательного центра Казанского госун-та "Материалы и техӯнологии XXI века": Тез. докл. Казань: Казанский госун-т, 2005. С. 17.
16. Bolshakova O.V., Nizamov I.D., Sergeenko G.G., Nizamov I.S., Batyeva E.S., Alfonsov V.A. Phosphorylation of citral, citronellal and (-)-myrtenal imines // XV-th Intern. conf. on the chemistry of phosphorus compounds: Book of abstracts. Saint-Petersburg, Russia, 2008. P. 117. (P-23).

