Иммунобиологические свойства термолабильного энтеротоксина бактерий рода enterobacter в системе взаимодействия “патоген - хозяин”
На правах рукописи
Ахтариева
Айгуль Атласовна
ИММУНОБИОЛОГИЧЕСКИЕ СВОЙСТВА
ТЕРМОЛАБИЛЬНОГО ЭНТЕРОТОКСИНА
БАКТЕРИЙ РОДА ENTEROBACTER
В СИСТЕМЕ ВЗАИМОДЕЙСТВИЯ “ПАТОГЕН - ХОЗЯИН”
03.02.03 – микробиология
14.03.09 – клиническая иммунология, аллергология
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук
Челябинск 2010
Работа выполнена на кафедре микробиологии, вирусологии и иммунологии ГОУ ВПО «Башкирский государственный медицинский университет Росздрава» и на кафедре микробиологии, вирусологии, иммунологии ГОУ ВПО «Челябинская государственная медицинская академия Росздрава».
Научные консультанты:
Заслуженный деятель науки РФ,
доктор медицинских наук,
профессор Габидуллин Зайнулла Гайнулинович
Заслуженный деятель науки РФ,
член–корреспондент РАМН,
доктор медицинских наук,
профессор Долгушин Илья Ильич
Официальные оппоненты:
Заслуженный деятель науки РФ,
член–корреспондент РАН, академик РАМН,
доктор медицинских наук,
профессор Бухарин Олег Валерьевич
доктор медицинских наук,
профессор Бурмистрова Александра Леонидовна
доктор медицинских наук,
профессор Симбирцев Андрей Семенович
Ведущая организация: Институт экологии и генетики микроорганизмов УроРАН,
г. Пермь
Защита диссертации состоится ____________________2010 года в _______ часов на заседании Диссертационного Совета Д 208.117.03 при ГОУ ВПО «Челябинская государственная медицинская академия Росздрава» по адресу: 454092, г. Челябинск, ул. Воровского, 64.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО «Челябинская государственная медицинская академия Росздрава».
Автореферат разослан « » 2010 года
Ученый секретарь
Диссертационного Совета,
доктор медицинских наук,
профессор Л.Ф. Телешева
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
В настоящее время пристальное внимание уделяется проблеме инфекционных заболеваний, вызываемых условно-патогенными энтеробактериями (УПЭ), патогенез которых недостаточно изучен. В развитии инфекционного процесса, ассоциируемого с УПЭ, безусловно, основополагающую роль играют токсины возбудителя, среди которых особый интерес представляет термолабильный (LT) энтеротоксин бактерий рода Enterobacter.
Известно, что LT-энтеротоксины УПЭ имеют сходный механизм токсического эффекта на желудочно-кишечный тракт как человека, так и животных, к разряду основных клинических проявлений которого относят диарейный симптомокомплекс на фоне выраженной интоксикации организма (A.L. Horstman, M.J. Kuehn, 2000; A.M. Al-Majali et al., 2000; C. Khursigara et al., 2001; M. Field, 2003; R. Mundy et al., 2005; J. Weckamp et al., 2005). Их местное воздействие способствует закреплению инфекта и повышает вероятность инвазии; они инициируют системные реaкции, достаточно удаленные от зоны первичной локализации (F. Qadri et al., 2005; P.A. Kenneth et al., 2006; D. Borenshtein et al., 2008; A. Masuda et al., 2008). Кроме того, выявлено, что LT-энтеротоксины УПЭ иммунологически схожи, в частности, определены сходства LT-энтеротоксинов E. cloacae и Escherichia coli (F.A. Klipstein, R.F.Engert, 1977; S.F. Jiwa et al., 1981; F. A. Klipstein et al., 1983; F. J. Pagotto et al., 2003; Hajishengallis G. et al., 2004; 2005). Вместе с тем, комплексный анализ иммунобиологических характеристик в системе «патоген-хозяин» LT- энтеротоксина Enterobacter spp. не проводился.
Течение любого инфекционного процесса тесным образом взаимосвязано с факторами и механизмами иммунной реактивности, поэтому понимание глубины патогенеза заболевания невозможно без раскрытия иммунологического контекста этой проблемы.
В преодолении защитной функции системы иммунореактивности при инфекционных процессах важную роль играют особенности реагирования клеточных факторов врожденного иммунитета в ответ на возбудителя. Одними из главных клеток врожденного иммунитета, осуществляющих первую линию защиты организма от инфекции, являются фагоциты – макрофаги, нейтрофилы, натуральные киллеры, дендритные клетки и др. (А. А. Тотолян, И.С. Фрейдлин, 2000; И.С. Фрейдлин, 2008; Н.К. Ахматова, М.В. Киселевский, 2008; И.И. Долгушин и др., 2009; S. Pasare, R. Medzhitov, 2005; M. Hausmann et al., 2005; O. Levy, 2005; C.B. Kenneth et al., 2006; A.N. Kopitar et al., 2006; S. Uematsu et al., 2006; A.J. Talati et al., 2008). В основе защитной функции указанных эффекторов лежит фагоцитарный процесс, заключающийся в их способности поглощать и уничтожать чужеродный материал (В.А. Ляшенко, 1995; C.A. Кетлинский, Н.М. Калинина, 1995; А. А. Тотолян, И.С. Фрейдлин, 2000; 2008; И.И. Долгушин и др., 2009; C.A. Jr. Janeway, R. Medzhitov, 2002).
Функциональные возможности фагоцитов могут меняться при действии разных объектов фагоцитоза (В.А. Ляшенко, 1995; И.И.Долгушин, О.В. Бухарин, 2001; М.В. Пащенков, Б.В. Пинегин, 2006; Н.Г. Плехова, 2006; Б.В. Пинегин, А.Н. Маянский, 2007; Б.В. Пинегин, М.И. Кирсанов, 2009; A.Sing et al., 2000; M.G. Paraje et.al., 2005; Л.М. Сомова, 2006; А.Н. Ильинская и др., 2007; М.И. Карсонова и др., 2007; D. Heumann et al., 2006; S.C. Eisenbarth, R.A. Flavell, 2006; T. Kawai, S. Akira 2006; S. Park et al., 2009).
Кроме того, чрезмерное воспаление, сопровождающееся избыточной продукцией и секрецией агрессивных молекул и радикалов, может привести к массивным повреждениям клеток и тканей организма (G.A. Stunczuk et al., 2003; D. Borenshtein et al., 2008).
Процесс взаимодействия патогена с клеткой хозяина вызывает развитие каскада иммунологических реакций, сопровождающихся продукцией цитокинов, спектр секреции которых зависит не только от вида бактерий, но и от их факторов патогенности (A.C. Симбирцев, 2004; Л.В. Ковальчук и др., 2005; А.Н. Маянский и др., 2007; Л.В. Ковальчук и др., 2008; C. Meserli et al., 1981; P.L. Meroni et al., 1987; G. R. Comelis, F. Van Gijsegem, 2000; S.W. Chensue et al., 2001; E.R. Kandimalla et al., 2003; O. Levy, 2005; A.J. Talati et al., 2008). Бактерии, со своей стороны, также используют разные возможности манипулирования цитокинами для своей выгоды (О.В. Бухарин и др., 2005; D.S. Merrell, S.Folkow, 2004).
В настоящее время существуют убедительные доказательства о том, что клинический исход заболевания во многом зависит от баланса секреции про- и противовоспалительных медиаторов (G.A. Stunczuk et al., 2003; S. Xanthoulea et al., 2004; D. Borenshtein et al., 2008; G. Mateolli et al., 2008).
Современное понимание особенностей иммунной реакции при инфекционных заболеваниях, вызванных энтеротоксигенными УПЭ, в частности, бактериями рода Enterobacter, невозможно без оценки функциональной активности Т- и В-лимфоцитов, так как направление дифференцировки Т-клеток в Т-хелпер – 1 (Th1)/ Т-супрессор – 1 (Тс1) или Т-хелпер – 2 (Th2)/ Т-супрессор – 2 (Tc2) тип, переключение В-клеток на продукцию классов иммуноглобулинов определяет характер и течение заболевания (А.С. Симбирцев, 2002; И.Н. Швыдченко и др., 2005; Г.Ф. Железникова, 2006; А.П. Суслов и др., 2006; Е.Г. Пономарева и др., 2007; А.Н. Маянский и др., 2007; J.M.A. Klapproth et al., 2000; B.S. Feng et al., 2008).
В настоящее время внимание исследователей привлекают вопросы изучения апопотоза эукариотических клеток, поскольку многие патогенные микроорганизмы выработали совершенные механизмы управления гибелью клеток хозяина в целях выживания (J. Moss et al., 1980; W. X. Ding et al., 2000; C. Arce et al., 2005; N. Kamado et al., 2008.). Вместе с тем, нарушение процессов инициации и реализации летальной программы клеток иммунной системы часто становится основополагающей в определении характера и тяжести течения патологического процесса. Поэтому изучение влияния LT-энтеротоксина Enterobacter spp. на апоптоз клеток иммунной системы хозяина также является актуальным.
Исходя из вышеизложенного, представляет научный и практический интерес изучение характеристики иммунобиологических возможностей LT-энтеротоксина Enterobacter spp. и сопряженных с ним иммунных реакций организма. Полученные данные помогут глубже проникнуть в фундаментальные механизмы патогенеза инфекционных заболеваний, вызываемых энтеротоксигенными Enterobacter spp., и откроют новые возможности управления ими.
На наш взгляд, представления о взаимоотношениях между паразитом и хозяином можно расширить, изучив морфологические особенности Enterobacter spp., характеристику факторов патогенности и генетические детерминанты патогенности.
Цель исследования
Дать комплексную характеристику иммунобиологическим свойствам термолабильного энтеротоксина бактерий рода Enterobacter в системе взаимодействия “патоген-хозяин”.
Задачи исследования
- Оценить фенотипические проявления факторов патогенности клинических штаммов Enterobacter spp., выделенных от больных с желудочно-кишечными, гнойно-воспалительными и урологическими инфекциями.
- Провести комплексное тестирование биологических свойств клинических штаммов Enterobacter spp. и определить штаммы, обладающие факторами патогенности и являющиеся суперпродуцентами термолабильного энтеротоксина.
- Изучить генотипическую характеристику «островков патогенности» Enterobacter spp., специфичных генам, входящим в состав патогенных кластеров E.coli и ответственных за разные этапы взаимодействия возбудителя с макроорганизмом.
- Определить особенности иммунного реагирования на разных этапах взаимодействия энтеротоксигенных представителей рода Enterobacter в системе “патоген-хозяин”.
- Изучить механизмы патогенного действия термолабильного энтеротоксина Enterobacter spp. на этапах формирования иммунного ответа организма хозяина.
- Определить влияние термолабильного энтеротоксина Enterobacter spp. на апоптоз перитонеальных фагоцитов мышей.
Научная новизна
Из коллекции культур Enterobacter spp. были выделены новые 3 штамма, обладающие комплексом факторов патогенности, в частности, продуцирующие термолабильный энтеротоксин: Enterobacter gergoviae ГИСК №259 (патент РФ №2161197 от 18.11.1999), Enterobacter cloacae ГИСК №258 (патент РФ №2164942 от 13.03.2000), Enterobacter agglomerans ГИСК №257 (патент РФ №2162485 от 13.03.2000).
Впервые получены данные, характеризующие фенотипические особенности бактерий рода Enterobacter, коррелирующие с их патогенностью. Установлены различия между клетками Enterobacter spp., образующими центр колоний и имеющими размеры 1,97±0,12 мкм в длину и 0,72±0,18 мкм в ширину, и формирующими на периферии колонии так называемые «швермеры» (бродяги). Эти высокоподвижные длинные клетки имеют избыточное количество жгутиков. У высокоадгезивных штаммов Enterobacter spp. обнаружены по периметру реснички длиной 297,8±152,8 нм и шириной 4,91±0,53 нм.
Впервые проведена молекулярно-биологическая характеристика клинических штаммов Enterobacter spp. в свете новых представлений о генетических основах патогенности микроорганизмов: обнаружены гены, аналогичные с “островками патогенности” E.coli.
На основе комплексного системного анализа выявлены особенности изменения иммунной системы животных, включая оценку феномена апоптоза клеток воспалительного экссудата.
Впервые выявлен эффект иммуносупрессивного влияния термолабильного энтеротоксина на антигенпрезентирующую и процессинговую функции перитонеальных макрофагов, расшифрованы молекулярные механизмы подавления указанных функций у макрофагов, опосредованных ложной индукцией трансформирующего фактора роста- (TGF-).
В патогенезе инфекционного процесса, связанного с термолабильным энтеротоксином, впервые определен характер модулирующего влияния токсина на макрофаги и нейтрофилы. Он способен несколько снижать продукцию интерферона- (IFN-). В то же время исследование состояния внутриклеточных механизмов микробиоцидной активности перитонеальных фагоцитов под влиянием термолабильного энтеротоксина Enterobacter spp. выявило негативное действие токсина на активность ферментов гексозомонофосфатного шунта фагоцитов, что характеризовалось резким снижением образования супероксидных анионов.
Теоретическая и практическая значимость работы
Полученные экспериментальные данные дополняют и углубляют представления о молекулярных механизмах действия термолабильного энтеротоксина бактерий рода Enterobacter на иммунную систему хозяина, раскрывают патогенез инфекционных процессов, обусловленных токсинпродуцирующими штаммами энтеробактерий, и создают основу для разработки этиопатогенетических принципов лечения и целенаправленной профилактики инфекционных заболеваний. Полученные данные будут полезны для своевременной коррекции иммунологических нарушений, связанных с энтеротоксинпродуцирующими штаммами условно-патогенных энтеробактерий.
Установлены маркеры вирулентности у штаммов Enterobacter spp., что позволит разработать пути целенаправленной профилактики и лечения инфекционных заболеваний, вызванных бактериями рода Enterobacter.
Отработаны оптимальные подходы для выяснения этиологической значимости бактерий рода Enterobacter, выделенных от больных с желудочно-кишечными, гнойно-воспалительными и урологическими заболеваниями.
Результаты работы расширяют экспериментальную базу для изучения патологических процессов, происходящих при острой энтеробактерной инфекции.
Основные положения, выносимые на защиту
- Патогенетические возможности клинических штаммов Enterobacter spp. определяются их способностью к адгезии, продукции цитолизинов, токсинообразованию и персистентными свойствами.
- Генотипическая характеристика «островков патогенности» бактерий рода Enterobacter детерминирована HlyA, HlyB, papAH, papC, sfaA, sfaG генами E.coli.
- Бактерии рода Enterobacter, выделенные из очагов поражения, включают генетически разнородные варианты, что имеет ценность для эпидемиологической оценки.
- Патогенетическое действие термолабильного энтеротоксина бактерий рода Enterobacter связано с его действием на различные этапы формирования иммунного ответа хозяина, в первую очередь, на антигенпрезентирующую функцию перитонеальных макрофагов и продукцию ими цитокинов TGF-, TNF- и IFN-.
Внедрение результатов исследования
Депонированные в ФГУН ГНИИСК имени Л.А. Тарасевича 3 штамма Enterobacter spp. (Патенты: №2161197 от 18.11.1999; №2164942 от 13.03.2000; №2162485 от 13.03.2000) используются в работе лаборатории анатоксинов «Иммунопрепарат» ФГУП «НПО «Микроген» МЗ и СР РФ в качестве токсигенных тест – культур.
Результаты исследования используются в бактериологических лабораториях Детской Республиканской клинической больницы и Республиканской клинической больницы им. Г.Г. Куватова г.Уфы.
Материалы исследования внедрены в учебный процесс на кафедрах микробиологии, вирусологии и иммунологии; эпидемиологии и детских инфекционных болезней ГОУ ВПО «БГМУ Росздрава»; на кафедре микробиологии, вирусологии, иммунологии ГОУ ВПО «ЧелГМА». Издано учебное пособие для врачей – бактериологов и клинических лаборантов «Условно-патогенные энтеробактерии» (Уфа, 2006; 2009).
Апробация работы
Материалы диссертации докладывались на VI конференции иммунологов Урала (Челябинск, 2005); конференции «Актуальные вопросы современной фармации и фармацевтическое образование» (Уфа, 2006); конференции, посвященной 25-летию ЦНИЛ ЧелГМА «Актуальные вопросы инфекционной патологии человека и прикладной иммунологии» (Челябинск, 2006); V Российской научной конференции «Персистенция микроорганизмов» (Оренбург, 2006), Республиканской конференции молодых ученых Республики Башкортостан «Медицинская наука – 2007» (Уфа, 2007); IX съезде Всероссийского общества эпидемиологов, микробиологов и паразитологов (Москва, 2007); Республиканской конференции молодых ученых Республики Башкортостан «Медицинская наука–2008» (Уфа, 2008); 73-й итоговой Республиканской Научной конференции студентов и молодых ученых БГМУ «Вопросы теоретической и практической медицины» (Уфа, 2008), X съезде Всероссийского общества эпидемиологов, микробиологов и паразитологов (Москва, 2008), VII Российской научной конференции «Персистенция микроорганизмов» (Оренбург, 2009); обсуждены на совместном заседании кафедры микробиологии, вирусологии и иммунологии ГОУ ВПО «Башкирский государственный медицинский университет Росздрава», кафедры микробиологии, вирусологии, иммунологии ГОУ ВПО «Челябинская государственная медицинская академия Росздрава», Башкирского отделения Всероссийского общества эпидемиологов, микробиологов и паразитологов и ведущих сотрудников уфимского филиала «Иммунопрепарат» ФГУП «НПО «Микроген» МЗ и СР РФ.
Публикации
По теме диссертации опубликованы 45 печатных работ.
Структура и объем диссертации
Диссертация изложена на 227 страницах, иллюстрирована 31 таблицами и 28 рисунками, состоит из введения, обзора литературы, материалов и методов исследования, 3 глав собственных исследований, заключения и выводов. Список литературы включает 95 отечественных и 320 иностранных источников.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
Клинический материал бактерий рода Enterobacter получали из бактериологических лабораторий Республиканской клинической больницы им. Куватова Г.Г., Городской клинической больницы №21, Детской Республиканской клинической больницы и Больницы скорой медицинской помощи №22 г. Уфы в период с 1998 по 2008 г.г.
В качестве эталонных штаммов использовали E.gergoviae ГИСК №259 (Патент РФ №2161197 от 18.11.1999), E.cloacae ГИСК №258 (Патент РФ №2164942 от 13.03.2000) и E.agglomerans ГИСК №257 (патент РФ №2162485 от 13.03.2000). В настоящее время Enterobacter agglomerans (Pantoeа agglomerans) выделен в новый род Pantoeа.
Эксперименты выполнены на 1130 беспородных белых мышах-самцах, 14 кроликах, 36 белых мышах – сосунках. Животные содержались в условиях вивария БГМУ с естественным световым режимом на стандартной диете лабораторных животных (ГОСТ Р50258-92) с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997), а также правил лабораторной практики при проведении доклинических исследований в РФ (ГОСТ З 51000.3-96 и 51000.4-96). Животные (мыши и кролики) получены из питомника лабораторных животных уфимского филиала «Иммунопрепарат» ФГУП «НПО «Микроген» МЗ и СР РФ и из питомника БГМУ.
В соответствии с целью диссертационной работы экспериментальная часть выполнялась в 3 этапа.
На первом этапе оценивались фенотипические признаки патогенности клинических штаммов Enterobacter spp. in vitro.
Объектом изучения служили 218 клинических штаммов бактерий рода Enterobacter, выделенных из проб клинического материала, полученного от больных с желудочно-кишечными, урологическими, гнойно-воспалительными заболеваниями – 132 штамма и здоровых лиц – 86 штаммов.
Биохимическую идентификацию культур осуществляли с использованием тест-систем «Enterotest» фирмы «Lachema» (Чехия) и компьютерной биохимической тест-системы типа API фирмы «BioMeruiox».
Изучение бактериальных колоний и особенностей клеточной структуры бактерий рода Enterobacter проводили с помощью оптического («Биолам», Россия) и электронного («JEM-100B», Япония) микроскопов.
Адгезивную активность изучали в реакции гемагглютинации с эритроцитами птиц (З.Г. Габидуллин и др., 1987) и I (0) группы АВО человека (В.И. Брилис и др., 1986). Продукцию -гемолизина, тиолзависимого и энтерогемолизина определяли по рекомендациям Г.З. Габидуллина (1978), J. Albesa et al. (1985) и L. Beutin et al. (1988) соответственно. Определение лецитиназной активности проводили на желточном агаре Ю.Н. Чистовича (1961), антилизоцимную активность (АЛА) определяли по методу О.В. Бухарина и др. (1984), антиинтерфероновую активность (АИА) - по методу Ю.В. Соколова (1990), антикомплементарную активность (АКА) - по методу О.В. Бухарина (2000), ДНК–азную активность - по C.D. Jeffries et al. (1957). Патогенность и вирулентность штаммов Enterobacter spp. оценивалась in vivo с определением протистоцидной активности на простейших - Paramecium caudatum (Х.Л. Галикеев, 1987), по способности вызывать гибель белых мышей (М.К.Войно-Ясенецкая, 1957), токсигенности бактериальных культур Enterobacter spp. на моделях лигированной петли тонкого кишечника кролика, на мышах–сосунках (R. Gianella et al., 1976) и в плантарном тесте (Ю.Н. Вартанян и др., 1978).
На втором этапе изучали генотипические признаки патогенности бактерий. Для этого выделяли бактериальную ДНК лизоцимом («Serva» США) с добавлением протеиназы, плазмидную ДНК по методу C.T. Каdо, S.T. Liu (1981), проводили избирательную амплификацию участков ДНК «островков патогенности» методом полимеразной цепной реакции (ПЦР). Для амплификации использовали специфические праймеры, подобранные на определенные участки генов для E.coli и ответственные за разные этапы взаимодействия патогена с клеткой хозяина (А.Р. Мавзютов, 2001; E.F. Boyd, 1998).
На третьем этапе изучали патогенетические механизмы термолабильного энтеротоксина бактерий рода Enterobacter в системе взаимодействия «патоген-хозяин» in vivo.
Модель острой энтеробактерной экспериментальной инфекции воспроизводили в 3 экспериментальных группах:
– экспериментальная 1: осуществляли внутрибрюшинным введением бульонной культуры E.cloacae, содержащей LT-энтеротоксин в дозе LD50 -5 1010КОЕ/мл.
– экспериментальная 2: осуществляли внутрибрюшинным введением бульонной культуры изогенной пары E.cloacae в дозе LD50-5 106 КОЕ/мл.
– экспериментальная 3: осуществляли внутрибрюшинным введением супернатанта бульонной культуры E.cloacae в дозе LD50-5 108 КОЕ/мл.
– контрольная: введение 0,9%-й физиологический раствор NaCl.
При введении дозы LD50 развивался инфекционный процесс, сопровождающийся выраженными изменениями активности животных, массы и состояния шерстяного покрова.
Оценку всех тестируемых параметров проводили на 1-е, 3-и, 5-е и15-е сутки.
Перитонеальные макрофаги (ПМ) мышей получали после внутрибрюшинного введения 2 мл пептонного бульона.
Селезенку после извлечения и взвешивания разрезали ножницами на несколько частей, размельчали в стеклянном гемогенизаторе Поттера и путем 2-3 тракций выдавливали клеточную массу в охлажденную среду 199.
Мононуклеарные клетки периферической крови выделяли на двойном градиенте плотности стерильных растворов фиколл - верографина. Плотность верхнего слоя градиента составляла 1,075-1,077, а нижнего – 1,093-1,095 (L.Wong, 1975).
На третьем этапе проводили: 1)оценку способности ПМ поглощать частицы полистирольного латекса (И.С.Фрейдлин и др., 1976); 2)изучение антигенпрезентирующей и процессинговой функции перитонеальных макрофагов (В.Г. Галактонов, Т.В.Анфалова, 1974); 3)НСТ - тест (А.Н.Маянский, М.Е.Виксман, 1979); 4)изучение уровня суммарного свечения лизосом в цитоплазме ПМ (И.С.Фрейдлин, 1984); 5)определение числа антителообразующих клеток (N.K. Jerne, 1963); 6)определение интерлейкинов макрофагов и нейтрофилов воспалительного перитонеального экссудата методом ПЦР; ДНК-гибридизации с праймерами и ДНК-зондом, подобранным по M.Takano (1998); 7)исследование апоптоза клеток воспалительного перитонеального экссудата в проточном цитофлюориметре (FL3, >600 нм) по структурным изменениям ядерной ДНК клеток, окрашенных йодистым пропидием (С.В. Сибиряк и др., 2008).
Методы статистической обработки
Для анализа данных использовали методы описательной статистики и дисперсионного анализа. При сравнении 2-х групп применяли парный критерий Стьюдента для независимых выборок; для множественных сравнений-критерий Стьюдента с поправкой Бонферрони, тест Ньюмена – Кейлса и метод Крускала – Уоллиса. При сравнении результатов опытов с альтернативной формой реакции использовался точный критерий Фишера для четырехпольных таблиц. Для сравнения категориальных переменных проводился анализ таблиц сопряженности с использованием критерия 2.
Для оценки степени (доли) влияния фактора проводился одно- и двухфакторный дисперсионный анализ, где были рассчитаны коэффициенты (2) и уровень их статистической значимости. Отличия считали статистически значимыми при р<0,05 (И.П. Ашмарин, 1962; О.Ю. Реброва, 2002; В.М. Зайцев и др., 2006).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Исследование проб клинического материала, полученного от больных с инфекционными процессами различной локализации, показали, что наиболее часто Enterobacter spp. обнаруживаются при желудочно-кишечных инфекциях – 49 шт. (39%) (рис.1).

Рис.1. Распределение штаммов Enterobacter spp.
по источникам выделения (%)
По видовому составу из 218 клинических штаммов Enterobacter spp. 63 шт. (28,9%) относились к E.cloacae, 59 шт. (27,1%) - E.aerogenes, 52 (23,9%) - E.gergoviaе, 39 шт. (17,8%) - E.sakazakii и 5 шт. (2,3%) – E. agglomerans.
Среди бактерий рода Enterobacter подавляющее большинство культур (86,2%) составляли прототрофы, а 13,8% – ауксотрофы. При сравнительном анализе частоты встречаемости прототрофов в зависимости от источника выделения было установлено, что в испражнениях больных с желудочно-кишечной патологией прототрофы обнаруживаются в 87,7% случаев против 91,3% контроля (2=0,62; р=0,365), в моче больных урологическими инфекциями в 81,9% против 91,3% контроля (2=0,08, р=0,78) и в раневом отделяемом больных с гнойно-воспалительными процессами - в 82,1% случаев против 83,3% контроля (2 =0,001; р=0,996)
Полученные результаты свидетельствуют о высокой экологической пластичности указанных бактерий, что позволяет адаптироваться им в различных полостях организма хозяина.
Электронно-микроскопические исследования показали, что колонии Enterobacter spp. способны к клеточной специализации и многоклеточной организации. У бактерий хорошо заметны различия между вегетативными клетками, образующими центр колонии и имеющими размеры длиной 1,97±0,12 мкм и шириной 0,72±0,18 мкм, и локализованными на периферии колонии высокоподвижными длинными клетками – «швермерами» (бродягами), имеющими избыточное количество жгутиков, среднее число которых колеблется от 7 до 60.


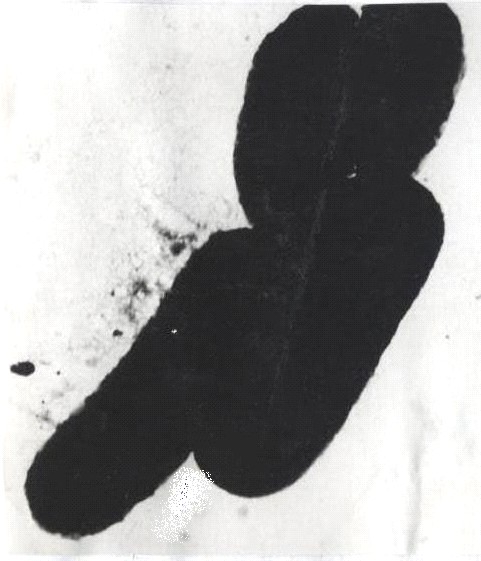
Электронограмма отпечатков колоний Enterobacter spp. убедительно показала наличие между клетками контактов двух типов: плотное слипание клеток между собой и контакты “конец в конец” (рис.2a).
Рис.2. Электронограмма снимков колоний бактерий Enterobacter spp.
а) 1 – плотное слипание клеток между собой “Байеровские зоны” (ув.х10000); 2 контакты “конец в конец”; б) клетки, формирующие «швермеры» (ув.х10000); в)внутриплазматические мостики и перемычки (ув.х20000).
По данным M.E.Bayer (1975), через липидные слои мембран проходят соприкасающиеся белковые структуры, часто называемые “Байеровскими зонами” (рис.2б). В результате соединения двух таких белковых структур образуется непрерывный водный канал, связывающий цитозоли двух взаимодействующих клеток. Это своего рода аналог примитивной “циркуляторной системы”, доставляющей питательные субстраты и убирающей продукты метаболизма (J.W. Costerton et al., 1995).
В колониях бактерий имеются перемычки, внутриплазматические мостики, поры и каналы (рис.2в), а также более специализированные структуры (“газовые баллоны”), окруженные своеобразной “мембраной” и содержащие внеклеточные гемопротеины. Предположительно, такие структуры способствуют транспорту О2 к клеткам в колониях (агрегатах) и являются аналогами дыхательной системы органов (В.И. Дуда и др., 1995).
В настоящее время сформировалась тенденция рассматривать межклеточные коммуникации у микроорганизмов с позиций кворума клеток в системе (О.В. Бухарин и др., 2005; К.Р. Allen et al., 2006; S. Towsend et al., 2006). Существующие сложные системы межклеточных контактов, способствуют распространению сигнальных молекул в популяции, особенно если речь идёт о недиффундирующих в среде факторах “коммуникации” (J.K. Crane et al., 1999). Вероятно, в эффектах кворума принимают участие все три канала коммуникации (химический, механический, опосредованный физическими полями), но наиболее изучена химическая сигнальная система, в которой внеклеточная концентрация ауторегуляторов отражает плотность микробных популяций. Например, показана способность штаммов E.sakazakii синтезировать сигнальные молекулы «чувства кворума» (quorum sensing), регулирующие экспрессию факторов патогенности. К ним относят молекулы N-гексаноил-L-гомосеринлактонов двух типов, выявленные методом тонкослойной хроматографии (A. Lehner et al., 2005; G.T. Gunduz, G. Tuncel, 2006).
Наличие определенных структур на внешней поверхности бактериальной клетки определяет их адгезивность к чувствительным клеткам хозяина, и обеспечивает быструю колонизацию самых разнообразных поверхностей, в том числе мембран клеток. Их фенотипическая экспрессия строго коррелирует с образованием пилей разных типов и обусловливает РГА (D.C. Old et al., 1983; 1984; Mange Jean-Philippe et al., 2006).
Анализ результатов показал, что из 218 клинических штаммов Enterobacter spp., 141 (64,7%) являются маннозочувствительными и 77 (35,3%) - маннозорезистентными.
При сравнительном анализе маннозорезистентных и маннозочувствительных клинических штаммов Enterobacter spp. в зависимости от источника выделения чаще обнаруживались маннозочувствительные штаммы Enterobacter spp. при гнойно-воспалительных процессах (87,2% против 29,2% в контроле; 2=19,53; р=0,001).
В следующей серии опытов мы провели оценку адгезивной активности – средний показатель адгезивности (СПА) штаммов Enterobacter spp. в реакции гемагглютинации с формалинизированными эритроцитами I (0) группы крови системы АВО.
Результаты исследования показали, что из 218 клинических штаммов Enterobacter spp. 132 (60,6%) обладали адгезивной активностью.
У штаммов Enterobacter spp., выделенных от больных с желудочно-кишечной патологией, адгезивные свойства встречались чаще и были выражены сильнее (рис.3).
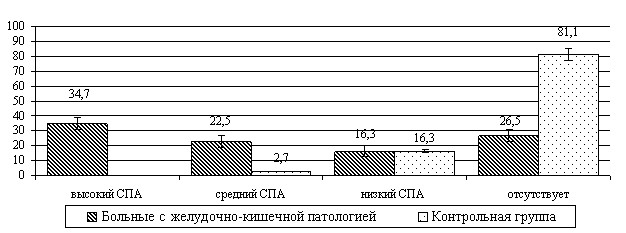
Рис.3. Распределение показателей адгезивности клинических штаммов Enterobacter spp., выделенных у больных с патологией желудочно-кишечного тракта и
в контрольной группе (%)
Результаты дисперсионного анализа показали, что коэффициент влияния экологического фактора на адгезивные свойства бактерий рода Enterobacter spp., выделенных при патологии желудочно-кишечного тракта, составил 2=14,9% (F=22,9; р<0,01). Этому способствует наличие развитого аппарата адгезии, обеспечивающего способность бактерий выдерживать воздействие перистальтической волны или тока мочи (T.G. Theander et al., 1998).
Наименьшей экологической зависимостью обладали культуры Enterobacter spp., изолированные при урологической патологии (2=9,1%; F=9,3; р<0,05), а у штаммов Enterobacter spp., выделенных при гнойно-воспалительных процессах, коэффициент влияния экологического фактора составил 14% (F=14,7; р<0,05).
Способность к адгезии, зависящей от условий экониш, позволяет расценивать адгезивность, как существенный детерминант, необходимый возбудителю для быстрого размножения и колонизации. Способность к адгезии обеспечивает выживаемость бактерий на разных этапах инфекционного процесса, особенно в начальной его фазе (T.G.Theander et al., 1998).
Изучение ультраструктуры внешней поверхности бактериальной клетки высокоадгезивных штаммов Enterobacter spp. показало наличие ресничек длиной 297,8±152,8 нм и шириной 4,91±0,53 нм.
Таким образом, адгезия бактерий рода Enterobacter spp. обусловлена наличием фимбриальных структур, с помощью которых происходит специфическое взаимодействие микроба с определенными рецепторами клеток хозяина.
В целях самосохранения бактериальные клетки обладают защитными механизмами дистанционного действия, которые благоприятствуют их выживанию. В этом отношении были изучены фенотипические признаки способности инактивировать лизоцим, лейкоцитарный интерферон и комплемент.
Фенотипический признак инактивации лизоцима был обнаружен у 87 (40%) клинических штаммов Enterobacter spp.
Штаммы АЛА были преимущественно представлены изолятами от больных с патологией желудочно-кишечного тракта - 33 (67,4%) против 3 (8,1%) контроля (2=12,33; р=0,001).
При этом результат дисперсионного анализа показал, что коэффициент влияния экологического фактора на АЛА штаммов Enterobacter spp., выделенных при патологии желудочно-кишечного тракта, был слабым и составил 2=0,6% (F=3,5; р>0,05), а для штаммов Enterobacter spp., изолированных при гнойно-воспалительных процессах и урологических заболеваниях, был 2=24,6% (F=43,1; р<0,001) и 2=4,4% (F=7,5; р<0,05) соответственно. Таким образом, существенное влияние на АЛА Enterobacter spp, изолированных при гнойно-воспалительных процессах, оказывает экологический фактор.
АИА обладали 56 (25,7%) клинических штаммов Enterobacter spp.
Наибольшую способность инактивировать интерферон проявляли штаммы Enterobacter spp., выделенные от больных с желудочно-кишечной патологией – 22 (44,6%), против 3 (8,1%) контроля (2=6,79; р=0,009) и с гнойно-воспалительными процессами 22 (56,4%) против 4 (16,7%) (2=3,4; р=0,065). При этом в большей зависимости от экологических условий по указанному признаку находились штаммы Enterobacter spp., изолированные при гнойно-воспалительных процессах (2=13,5%; F=15,3; р<0,001), а в меньшей - штаммы Enterobacter spp., выделенные при желудочно-кишечных заболеваниях (2=5,2%; F=12,8; р<0,05).
АКА была определена у 65 (29,8%) культур Enterobacter spp. Распространенность и экспрессия АКА варьировали. Наибольшей активностью обладали штаммы Enterobacter spp, выделенные при желудочно-кишечных заболеваниях – 38 ( 77,6%), против 5 (13,5%) контроля (2=11,48; р=0,001). Значения признака распределились следующим образом: штаммы Enterobacter spp. с высокой активностью составили 15 (30,6%) против 0 контроля, со средней активностью 16 (32,7%) против 0 контроля, с низкой активностью – 7 (14,3%) против 5 (13,5%) контролей (2=0,05; р=0,82), не активные – 11 (22,4%) против 32 (86,5%) контролей (2=10,1; р=0,001).
При этом коэффициент влияния экологического фактора на АКА культур Enterobacter spp., выделенных при патологии желудочно-кишечного тракта, составил 2 =20% (F=33; р<0,001).
Колонизация эпителиальных поверхностей бактериальными клетками параллельно сопровождается секрецией гемолизинов. Среди них наиболее известны -гемолизин, тиолзависимый гемолизин и энтерогемолизин.
Из 218 клинических штаммов Enterobacter spp. 35 (16,1%) продуцировали - гемолизин, 76 (34,9%) - тиолзависимый гемолизин и 20 (9,2%) - энтерогемолизин.
В зависимости от источника выделения штаммов Enterobacter spp. частота встречаемости -гемолитической активности была различной и колебалась в широких пределах. Штаммы Enterobacter spp. с -гемолитической активностью наиболее часто выделялись от больных с желудочно-кишечной патологией и составили 12 (24,5%) при 4 (10,8%) в контроле (р>0,11).
По степени активности преобладали штаммы с высокой активностью - 6 (12,3%) при 0 контроля. В контрольной группе обнаруживались штаммы Enterobacter spp. с низкой активностью - 4 (10,8%) и неактивные штаммы - 33 (89,2%) (рис.4).


Рис.4. Показатели -гемолитической активности штаммов Enterobacter spp., выделенных от больных с желудочно-кишечной патологией и в контрольной группе (%):
1 – отсутствует, 2 – низкая активность, 3 - средняя активность и 4 - высокая активность.
Среди штаммов Enterobacter spp., продуцирующих тиолзависимый гемолизин, преобладали культуры, изолированные при патологии желудочно-кишечного тракта, и составили 30 (61,3%) против 4 (10,8%) контроля (2=9,24; р=0,002). При этом штаммов с высокой активностью было 7 (14,3%), со средней – 11 (22,5%) и с низкой – 12 (25,5%), неактивные составили 19 (38,8%) против 37 (100%) контроля.
Аналогичные результаты были получены и при исследовании энтерогемолитической активности Enterobacter spp. Результаты согласуются с данными I. Beutin et al. (1988).
Проведенный сравнительный анализ гемолитической активности Enterobacter spp. выявил их своеобразие, по всей видимости, отражающее результат приспособления бактериальных популяций к специфическим условиям среды экониш.
Итоги дисперсионного анализа показали, что коэффициент влияния экологического фактора на тиолзависимую активность Enterobacter spp. был выше, чем на - и тиолзависимую гемолитическую активности. Данные влияния экологического фактора на тиолзависимую активность Enterobacter spp. представлены в табл. 1.
Таблица 1
Сила экологического влияния на тиолзависимую гемолитическую активность штаммов Enterobacter spp.
| Нозология | Сила влияния фактора, 2 (%) | F | р |
| Желудочно-кишечные заболевания | 16,5 | 35,5 | р<0,001 |
| Урологические заболевания | 5,1 | 8,1 | р<0,001 |
| Гнойно-воспалительные процессы | 11,4 | 13,8 | р<0,001 |
Изучение лецитиназной и ДНК-азной активностей Enterobacter spp. показали, что 59 (27,1%) и 22 (10,1%) штаммов, соответственно, обладают указанными свойствами.
Наиболее высокими значениями ДНК-азной активности характеризовались штаммы Enterobacter spp., изолированные от больных с желудочно-кишечной патологией. При этом высокая активность отмечалась у 13 (26,5%) штаммов против 0 контроля, средняя – у 10 (20,4%) против 1 (2,7%) контроля (р=0,0171), низкая – у 7 (14,3%) против 3 (8,1%) контроля (р=0,377) и неактивными были 19 (38,8%) против 33 (89,2%) (2=4,63; р<0,001). Полученные результаты согласуются с данными Н.А. Поликарпова и др. (1990).
Результаты дисперсионного анализа показали, что коэффициент влияния экологического фактора на ДНК-азную активность штаммов Enterobacter spp., выделенных от больных с патологией желудочно-кишечного тракта, составил 2=11,8% (F=19,5; р<0,001), а штаммов Enterobacter spp., изолированных при гнойно-воспалительных процессах, - 2=2,5% (F=5; р<0,05). Существенно ниже оказался коэффициент влияния экологического фактора на ДНК-азную активность штаммов Enterobacter spp., изолированных при патологии мочевыделительной системы (2=0,6%; F=1,2; р>0,05).
В зависимости от источника выделения, лецитиназная активность была выше среди культур Enterobacter spp., выделенных от больных с гнойно-воспалительными процессами. При этом культуры с высокой активностью составили 4 (10,3%) против 0 контроля, средней активностью - 3 (7,7%) против 0 контроля, низкой активностью - 2 (5,1%) против 0 контроля, неактивные - 30 (76,9%) против 24 (100%) контроля (р=0,013).
Изучение силы экологического влияния на лецитиназную активность Enterobacter spp. показало, что более подверженными экологической детерминации оказались штаммы Enterobacter spp., выделенные при патологии желудочно-кишечного тракта (2=22%, F=24,8; р<0,001). Это, возможно, отражает результат приспособления бактериальных популяций к специфическим условиям среды эндоэкониш.
Способность бактерий продуцировать токсин тесным образом связана с патогенетической значимостью возбудителя при развитии ряда инфекционных заболеваний. В литературе имеются сообщения об энтеротоксигенной способности Enterobacter spp. (И.Х. Мамоткулов и др., 1997), при этом исследования, направленные на выявление способности Enterobacter spp. вырабатывать токсины, немногочисленны и противоречивы (М.М. Баркус и др., 1986). Рутинным подходом к определению токсигенности и вирулентности служат биологические пробы, которые, однако, имеют ряд недостатков, связанных с необходимостью использования лабораторных животных, трудоемкостью, но, вместе с тем, достаточно полно отражают этиологическую значимость предполагаемого возбудителя. В связи с этим было проведено тестирование клинических штаммов Enterobacter spp. с использованием модели “плантарного теста” (Ю.Н. Вартанян и др., 1978), “интраназального инфицирования” беспородных белых мышей (М.К. Войно-Ясенецкая, 1957) и определение протистоцидной активности на токсигенность и вирулентность (Х.Л. Галикеев, 1987).
В результате постановки теста «отек лап» у мышей лишь 17 (7,8%) исследованных культур Enterobacter spp. давали положительный результат. Наибольшей активностью в этом тесте характеризовались 9 (18,4%) культур, выделенных от больных с желудочно-кишечными инфекциями. Показатели у культур Enterobacter spp., выделенных при урологических заболеваниях, были сопоставимы с результатами культур, изолированных при гнойно-воспалительных процессах, соответственно 4 (9,1%) и 4 (10,3%) (2=1,607; р=0,446). Ни один из штаммов Enterobacter spp., изолированных от здоровых людей, не вызывал появления визуально определяемой отечности лап.
Полученные результаты свидетельствуют о способности клинических штаммов Enterobacter spp. синтезировать термолабильное токсическое вещество, обусловливающее развитие “отека лапки” у белых мышей, что совпадает с вирулентностью, поэтому плантарный тест может быть использован в качестве биологической модели для выявления энтеротоксигенности бактерий рода Enterobacter.
Среди клинических штаммов Enterobacter spp., давших «отек лапки», центрифугат 3 штаммов оказался способным давать отек лапки мышей с разницей к интактной лапке до 80 мг. На основании полученных результатов 3 штамма Enterobacter spp. были депонированы в ФГУН ГНИИСК им. Л.А.Тарасевича, как продуценты LТ-энтеротоксина (патент РФ №2161197 от 18.11.1999, патент РФ №2164942 от 13.03.2000, патент РФ №2162485 от 13.03.2000).
В следующей серии опытов для подтверждения способности клинических штаммов Enterobacter spp. продуцировать LТ-энтеротоксин мы использовали метод «лигированная петля тонкого кишечника кролика» (R. Gianella et al., 1997). Результат опыта определялся по способности центрифугата 20-часовых бульонных культур Enterobacter spp. при введении в просвет тонкого кишечника кролика вызывать накопление экссудата, с последующим измерением отношения V/L (объема экссудата к длине лигированного участка). За положительную реакцию принимали показатель V/L=1,0-1,2.
Было выявлено 20 (9,2,6%) культур Enterobacter spp., вызывающих накопление экссудата в просвете тонкого кишечника кролика. При этом наибольшей активностью обладали штаммы Enterobacter spp., выделенные от больных с желудочно-кишечной патологией – 9 (18,4%). Так, у 1 (8,2%) штамма Enterobacter spp. против 0 в контроле V/L = 1,1-1,3, у 5 (10,2%) штаммов против 0 контроля V/L = 1,2, у 3 (6,1%) штаммов против 0 в контроле V/L = 1,0 и неактивные 37 (75,5%) штаммов против 37 (100%) в контроле.
Среди штаммов Enterobacter spp., выделенных при гнойных процессах, преобладали штаммы с V/L = 1,2. Так, 1 (2,7%) штамм против 0 контроля обладал V/L = 1,1-1,3; 3 (7,7%) штамма против 0 в контроле V/L = 1,2; 2 (5,1%) штамма против 0 контроля V/L = 1,0 и неактивные 33 (84,6%) штамма против 24 (100%) в контроле (р=0,151).
Штаммы Enterobacter spp., изолированные при патологии мочевыделительной системы, обладали наименьшей активностью. Так, 3 (6,8%) штамма против 0 контроля вызывали V/L = 1,2; 2 (4,6%) штамма против 0 контроля вызывали V/L = 1,0 и неактивными были 39 (88,6%) штаммов против 25 (100%) в контроле (р=0,074). Как показали результаты, ни один из штаммов, выделенных у лиц из группы контроля, указанным свойством не обладал.
Сила влияния экологического фактора на показатели V/L была низкой и не имела статистически значимых различий.
На легочной модели 54 (24,8%) клинических штамма Enterobacter spp. вызывали гибель экспериментальных мышей.
Патогенный потенциал был наиболее выражен среди культур, выделенных при патологии желудочно-кишечного тракта, поскольку больший процент указанных культур – 4 (8,2%) вызывал гибель животных в ранние сроки и 15 (30,8%) штаммов обусловливали летальную инфекцию. Среди культур Enterobacter spp., выделенных при заболеваниях мочевыделительной системы, 2 (4,6%) штамма вызывали раннюю гибель животных и 11 (25%) - летальную инфекцию. Штаммы Enterobacter spp., изолированные от больных с гнойно-воспалительными процессами, раннюю гибель животных обусловливали в 3-х (7,7%) случаях, а летальную инфекцию – в 4-х (10,2%). При этом показатели гибели в ранние сроки и летальной инфекции относительно штаммов Enterobacter spp., выделенных при патологии желудочно-кишечного тракта, не имели статистически значимых различий и составили соответственно 2=0,544; р=0,762 и 2=5,318; р=0,070.
При определении силы влияния экологического фактора на показатели интраназального теста обнаружено, что штаммы Enterobacter spp., выделенные от больных с желудочно-кишечными заболеваниями и гнойно-воспалительными процессами, находились в одинаковой зависимости от условий обитания, где сила влияния экологического фактора составила соответственно 8,6% (F=16,8; р<0,001) и 8,6% (F=13,5; р<0,001).
Проведенные нами исследования на различных биологических моделях экспериментальной инфекции показали, что интраназальное заражение и плантарный тест требуют значительного количества экспериментальных животных, поэтому не всегда выполнимы в условиях бактериологической лаборатории.
Метод, предложенный для выявления степени патогенности дизентерийных палочек на модели P.caudatum, вполне применим и для выявления патогенности УПЭ. Это связанно с тем, что P.caudatum относятся к эукариотическим клеткам, и могут быть чувствительны к действию токсических субстанций бактерий.
На модели P.caudatum был выявлен 61 (27,9%) клинический штамм Enterobacter spp., вызывающий гибель простейших.
Наибольшей активностью в этом тесте характеризовались штаммы Enterobacter spp., выделенные при патологии желудочно-кишечного тракта. Так, 1 (2,1%) штамм Enterobacter spp. против 0 контроля вызывал гибель P.caudatum в течение 0,5-14 мин, 6 (12,3%) штаммов против 0 контроля - в течение 1,5-3,4 мин, 16 (32,7%) штаммов против 3 (8,1%) в контроле - в течение 3,5-5,5 с (2=3,80; р=0,008), неактивными были 24 (52,9%) против 34 (91,9%) штамма контролей (р<0,001). Среди штаммов Enterobacter spp., выделенных от больных с патологией мочевыделительной системы, в течение 0,5-1,4 мин угнетали жизнедеятельность P.caudatum 4 (9,1%) штамма против 0 контроля, в течение 1,5-3,4 мин - 3 (6,8%) штамма против 0 контроля, в течение 3,5-5,5 мин – 7 (15,9%) штаммов против 6 (24%) контроля (2=0,256; р=0,613), неактивными были 30 (68,2%) штамма против 19 (76%) в контроле (2=0,17; р=0,680). Штаммы Enterobacter spp., изолированные от больных с гнойно-воспалительными процессами, характеризовались следующими значениями: 3 (7,7%) штамма против 0 контроля инактивировали P. caudatum в течение 0,5-1,4 мин, 4 (10,3%) штамма против 0 контроля - в течение 1,5-3,4 мин, 8 (20,5%) штаммов против 3 (12,5%) в контроле в течение 3,5-5,5 мин (р=0,193), неактивными были 24 (61,5%) штамма против 34 (87,5%) в контроле (р=0,003).
Гибель P.caudatum в ранние сроки вызывали культуры Enterobacter spp., одновременно показавшие высокую патогенность при интраназальном инфицировании мышей, а также продуцировавшие термолабильные токсические вещества, выявляемые в тесте «отек лап» на мышах.
Итоги дисперсионного анализа показали, что экологический фактор оказывал крайне слабое влияние на протистоцидный тест. Так, коэффициент влияния экологического фактора на протистоцидный тест штаммов Enterobacter spp., изолированных от больных с желудочно-кишечными заболеваниями, составил 2=0,2% (F=0,8; р<0,05), выделенных при урологических заболеваниях, - 2=0,8% (F=1,2; р<0,05), изолированных при гнойно-воспалительных процессах, - 2=2,9% (F=4,1; р<0,05).
Результаты исследований дают основание заключить, что время, в течение которого происходит гибель инфузорий, зависит от биологических свойств клинических штаммов Enterobacter spp., в частности, от их способности продуцировать токсические вещества, наличие которых у бактерий сочетается с их способностью вызывать гибель интраназально зараженных мышей. Протистоцидный тест на P.caudatum может быть рекомендован для выявления потенциально патогенных клинических штаммов Enterobacter spp.
Таким образом, изолируемые при инфекционных процессах различной локализации штаммы Enterobacter spp. характеризуются свойствами, определяющими их потенциальную способность выживать в условиях внутренней среды макроорганизма благодаря возможности противостоять факторам врожденного иммунитета.
Известно, что фенотипические проявления экспрессируемого фактора патогенности заложены в геноме бактериальной клетки. При этом гены, определяющие патогенность, могут входить в состав как хромосомы, так и плазмиды, а также могут быть фланкированы в состав IS-последовательностей и транспозонов.
В связи с этим перспективным является исследование плазмидного профиля ДНК для генотипической характеристики клинических штаммов бактерий рода Enterobacter. Наличие в бактериальной клетке плазмидной ДНК дает микроорганизму широкие адаптационные возможности в различных экологических нишах. Планируя проведение соответствующих опытов, мы основывались на том, что плазмиды различаются на: кодирующие устойчивость к лекарственным препаратам – R-плазмиды; отвечающие за фертильность бактериальной клетки – F-плазмиды, а также плазмиды бактериоциногении и патогенности. Вирулентные свойства энтеробактерий, чаще всего, контролируются плазмидой патогенности. В частности, F-, R-плазмиды и плазмиды бактериоциногении могут включать tox+-транспозоны, кодирующие токсинообразование. Нередко tox+-плазмиды кодируют синтез интактных протоксинов, активируемых клеточными протеазами, образование которых контролируют гены бактериальных хромосом (В.М. Бондаренко и др., 2001; А.Р. Мавзютов, 2002).
Анализ полученных данных позволил отобрать 132 клинических штаммов Enterobacter spp., обладающих Д-маннозочувствительной и Д-маннозорезистентной гемагглютинирующей активностью. Из 132 культур энтеробактеров 45 штаммов несли плазмиды, что составило 34,1%. При сравнительном анализе частоты встречаемости плазмидонесущих штаммов было установлено, что в 19 (42,2%) случаях относительно контроля плазмидонесущие штаммы были выделены от больных с желудочно-кишечной патологией (2=4,95; р=0,03), в 16 (35,6%) - урологической патологией (2=3,46;р=0,06), в 7 (15,6%) – гнойно-воспалительными процессами (2=0,10; р=0,75) и 3 (6,6%) - от здоровых людей.
Молекулярные массы плазмид значительно различались. Так, электрофоретически было установлено, что бактерии рода Enterobacter, вне зависимости от источника выделения, могут нести плазмиды с массами 120; 60; 38; 3,2; 1,4 МД и другие. При изучении плазмидного профиля штаммов с высокой адгезивностью было установлено, что они вообще не имели внехромосомной ДНК.
В следующей серии опытов у штаммов с адгезивной активностью провели элиминирование плазмид в бульоне Хоттингера, содержащем 5% додецилсульфата натрия. Тестирование изогенных пар на их способность давать MS- и MR-реакции гемагглютинации с эритроцитами цыпленка показало, что штаммы в одинаковой степени агглютинируют эритроциты. Результаты исследований дают основание полагать, что генетической детерминантой, контролирующей MS и MR реакцию гемагглютинации с эритроцитами цыпленка у Enterobacter spp., являются структурные элементы хромосомной природы.
Известно, что продукция LТ-энтеротоксина у E.coli детерминируется Ent плазмидами с мол.м. 55 - 61 МД (P.K. Lee et al.,1991; F.Qadri et al., 2005). В то же время энтеротоксин Vibrio cholerae является иммунологически родственным LT-энтеротоксину E.coli и C.freundii, контролируется структурными элементами хромосомной природы (M.I. Lesseva et al., 1995).
Из 17 культур энтеробактеров, продуцирующих LT-энтеротоксин, 13 штаммов оказались плазмидонесущими. В 8 случаях плазмидонесущие штаммы были выделены от больных с желудочно - кишечной патологией, в 2 – с урологической патологией, в 3 – гнойно-воспалительными процессами. Среди штаммов Enterobacter spp., выделенных от здоровых людей, LT-энтеротоксин продуцирующих штаммов не оказалось.
В связи с этим было проведено электрофоретическое исследование штаммов Enterobacter spp., продуцирующих LТ-энтеротоксин, на предмет обнаружения внехромосомных факторов наследственности. Для этого были выделены 2 группы штаммов: первую группу составили штаммы Enterobacter spp., суперпродуценты LT-энтеротоксина, способные вызывать “отек лап” мышей с разницей между контрольной лапкой 95 мг и более, вторую – культуры, не продуцирующие LT-энтеротоксин и дающие в опытах “отек лапки” разницу не более 35 мг. Все изученные 12 штаммов первой группы являлись носителями плазмиды мол.м. 60 МД. Среди 3 штаммов второй группы 2 культуры были бесплазмидными и 1 штамм нес плазмиды с мол.м.120; 38; 3,2 МД.
Элиминирование плазмид у штаммов, продуцирующих LT-энтеротоксин, показало, что бесплазмидные изогенные пары токсигенных штаммов не вызывали гибель P.caudatum.
Из 10 отобранных клонов каждого штамма Enterobacter spp., утративших свойство продуцировать LT-энтеротоксин, у двух на фореграмме просматривалась плазмида мол.м. 60 МД, остальные клоны оказались не несущими данной плазмиды и в биологических пробах не обладали активностью.
Опыты по фенотипическому определению гемолитической активности Enterobacter spp. указывают на то, что гемолизины являются одним из ведущих факторов патогенности клинических штаммов Enterobacter spp. В связи с этим было проведено электрофоретическое исследование гемолитически активных штаммов Enterobacter spp. для обнаружения природы детерминант.
Из 35 культур Enterobacter spp., способных гемолизировать эритроциты, 21 (60%) несли плазмиду мол.м. 120 МД. В 8 случаях плазмидонесущие штаммы были выделены от больных с желудочно-кишечной патологией, в 5 - урологической патологией, в 6 – гнойно-воспалительными процессами и в 2 - здоровых людей. Различия в частоте обнаружения указанных плазмид относительно контроля носили статистически не значимый характер (р>0,05).
Полученные результаты, таким образом, говорили в пользу плазмидной природы детерминирования гемолитической активности штаммов Enterobacter spp. Существование бесплазмидных вариантов гемолитических энтеробактеров не исключало этого предположения, так как при этом на результатах могло сказаться небольшое число копий этих плазмид, которые не обнаруживались исследуемым методом.
Для проверки этой рабочей гипотезы путем обработки акридиновым оранжевым были получены 2 генетически родственные изогенные пары штаммов Enterobacter spp., различающихся по наличию плазмиды с молекулярной массой 120 МД. При этом клоны 2 штаммов не продуцировали гемолизин, а клоны 2 штаммов - продолжали его продуцировать.
Эти данные, по нашему мнению, свидетельствуют в пользу хромосомной природы детерминирования указанного признака. Установление этого факта представляется существенным и, по нашему мнению, заслуживает самостоятельного изучения.
Проведенные нами опыты по изучению профиля плазмидной ДНК, элиминации и конъюгативной передачи плазмид не привели к выявлению новых плазмид, контролирующих синтез энтерогемолизина, ДНК-азную, лецитиназную, антилизоцимную и антиинтерфероновую активности клинических штаммов Enterobacter spp.
Следует отметить, что сила влияния экологического фактора во всех исследованиях была низкой и варьировала от 1 до 2,5 % (р>0,05).
Таким образом, результаты изучения плазмидного профиля дают основание полагать, что генетической детерминантой адгезивной активности бактерий рода Enterobacter, возможно, являются структурные элементы хромосомной природы, продукции LT-энтеротоксина плазмида мол.м. 60 МД, гемолизина - 120 МД.
Наличие у ряда клинических штаммов Enterobacter spp. генетических детерминант, контролирующих факторы патогенности, свидетельствует о том, что среди культур Enterobacter spp. встречаются штаммы, которые следует рассматривать не как условно-патогенные, а как конкретные патовары бактерий рода Enterobacter.
Учитывая, что штаммы легко могут терять плазмиду с утратой, соответственно, фенотипического признака, мы провели серию опытов по их конъюгативной передаче от доноров реципиентам. Причем реципиентами были представители как одного рода, так и других, в том числе был использован универсальный реципиент E.coli K12 G62 Rif®. В качестве доноров служили штаммы Enterobacter spp., имеющие плазмиды мол.м.м. 60 и 120 МД с выраженными фенотипическими признаками синтезировать высокоактивный LT-энтеротоксин и -гемолизин, соответственно. Опыты по скрещиванию родственных и неродственных представителей Enterobacteriaceae показали, что tox+ плазмида Enterobacter spp. может конъюгативно передаваться внутри рода Enterobacter, что объясняет трансформацию нетоксигенного реципиента в токсигенный патовар. Тогда как опыты по конъюгативной передаче tox+ плазмиды между неродственными представителями Enterobacteriaceae не увенчались успехом. Hly+ плазмида конъюгативно не перемещалась между штаммами, и это, на наш взгляд, может быть обусловлено большой мол.м. плазмиды (120 МД) или сложностью создания соответствующих условий для “интимных” процессов, либо же она является неконъюгативной.
Среди методов диагностики инфекционных заболеваний в последнее время все шире используется детекция генетических маркеров, ассоциируемых с патогенностью, к которым, в частности, относятся «островки патогенности».
В этой связи нами проведена амплификация с бактериальной ДНК Enterobacter spp. с праймерами к генам “островков патогенности” E.coli, контролирующими их способность к образованию фимбрий типа S (sfaA, sfaG), типа Р (рарС, рарАН), капсулообразованию (kpsMT), продукции гемолизинов (hlуА, hlуВ) и термолабильного энтеротоксина (Lth).
Удалось установить факт наличия у протестированных микроорганизмов фрагментов ДНК, специфичных известным генам кластеров патогенности E.coli. В частности, из 34 исследованных штаммов образование искомых ампликонов при использовании праймеров к hly A имело место в 7 случаях (20,5%), hly B – в 8 (23,5%), pap AH - в 4 (11,8%), pap C – в 5 (14,7%) случаях, sfa G и sfa A обнаружены у 2 (5,9%) и 8 (23,6%) штаммов соответственно (рис.5). Фрагменты, специфичные генам kps MT и Lth, обнаружены не были.

Рис.5. Частота обнаружения по результатам ПЦР фрагментов генов «островков патогенности» у клинических штаммов Enterobacter spp. (%)
Результаты исследования показали, что количество обнаруженных генов у штаммов, выделенных при желудочно-кишечной патологии, относительно здоровых людей составляет – 9 (2=4,38; р=0,04), у штаммов, изолированных при урологической патологии, – 7 (2=2,92; р=0,09), а у штаммов, выделенных при гнойно-воспалительных процессах, – 10 (2=7,64; р=0,01), т.е. имеются различия по источникам выделения в генах «островков патогенности».
Среди штаммов Enterobacter spp., изолированных от здоровых людей, встречались гены, специфичные только hlyA, hlyВ, papC и и sfaA.
Таким образом, среди штаммов Enterobacter spp., вне зависимости от источника их выделения, обнаруживаются гены hlyA, hlyB, papAH, papC, sfaG и sfaA. Это указывает на то, что между патогенными и непатогенными микроорганизмами постоянно осуществляется генетический обмен благодаря трансформации, трансдукции и конъюгации. Полученные результаты исследования дают основание полагать, что штаммы, относящиеся к разным видам и даже родам, содержат гены, кодирующие их токсигенность и вирулентность, фланкированные в состав кластеров “островков патогенности”. Это указывает на универсальный тип кодирования факторов патогенности и, соответственно, на схожий механизм развития патогенеза инфекционного процесса, обусловленного разными патоварами УПЭ.
Резюмируя выше изложенное, можно констатировать, что фенотипические признаки ряда факторов патогенности и наличие генетических детерминант, входящих в состав общих “островков патогенности”, позволяет клинические штаммы Enterobacter spp. рассматривать как конкретные патовары. Их богатый патогенный потенциал дает возможность Enterobacter spp. выживать в экологической нише, прикрепляться и колонизировать эпителиальные поверхности, способствуя противостоянию механизмам поддержания гомеостаза хозяина.
Изучение фенотипических проявлений факторов патогенности, экспрессируемых генетическими детерминантами хромосомной и нехромосомной природы, конечно, не исчерпывает всех аспектов, связанных с механизмами их патогенного действия, и констатирует факт только их этиологической значимости.
Как известно, возбудитель инфекционного процесса отличается значительной сложностью и неспецифичностью, что определяет многообразие клинических проявлений. Выяснение этих вопросов позволит определить наиболее уязвимые звенья иммунной системы хозяина и, возможно, связать их с локальными особенностями в цепи патогенеза заболевания и разработать наиболее рациональный этиопатогенетический принцип лечения инфекционных болезней и профилактики дизбиотических состояний, связываемых с УПЭ.
В качестве модели для изучения закономерностей функционирования системы “хозяин-патоген” мы использовали штамм E.cloacae №258, депонированный нами в ФГУН ГНИИСК имени Л.А. Тарасевича, обладающий продукцией термолабильного энтеротоксина. Выбор энтеротоксигенного штамма E.cloacae был обусловлен тем, что в патогенезе инфекционных заболеваний, вызванных УПЭ, ведущим фактором является его токсин.
Для выявления и характеристики дифференциального действия LT- энтеротоксина E.cloacae на клетки хозяина в инфекционном процессе был использован и липополисахарид клеточной стенки, который, наряду с термолабильным энтеротоксином, является мощным, но отличным по своей антигенной структуре иммуномодулятором.
Как известно, фагоцитоз является эффективным фактором специфической защиты организма.
Поэтому нами проведены исследования фагоцитарного звена иммунитета, позволившие констатировать факт нарушения функции макрофагов, которое сопровождалось снижением активности и интенсивности фагоцитоза в экспериментальных группах.
Результаты представлены на рис. 6.
Рис.6. Показатели активности (%) и интенсивности (усл.ед.) фагоцитоза перитонеальных макрофагов мышей в динамике
*-данные статистически достоверны по q-критерию Ньюмена-Кейлса при р<0,05.
Процесс фагоцитоза сопровождается активацией лизосомальных ферментов. Результаты наших исследований показали, что в I группе мышей, зараженной супернатантом токсигенной культуры E.cloacae, содержащей LT-энтеротоксин, прослеживается своеобразная динамика. Максимальная активация лизосомальных гранул происходит в 1 день, а быстрое “опустошение” ферментов лизосом - на 3 день исследования. Результаты отражены на рис.7.
Рис.7. Состояние лизосомальной активности перитонеальных макрофагов мышей в разные сроки исследования (усл.ед.)
*-данные статистически достоверны по q-критерию Ньюмена-Кейлса при р<0,05.
Как видно, термолабильный энтеротоксин E.cloacae уменьшает число лизосом в перитонеальных макрофагах, что приводит к снижению их переваривающей способности.
Фагоцитоз сопряжен с наработкой активных форм кислорода (АФК) с последующим внутриклеточным киллингом патогена (А.А. Тотолян и др., 2000; И.И. Долгушин, О.В. Бухарин, 2001; Н.С. Олиферук и др., 2005). Наиболее доступным и часто используемым подходом для оценки активности кислородзависимых систем бактерицидности фагоцитов является НСТ тест (спонтанный и индуцированный).
Так, исследование О2 - зависимого метаболизма фагоцитов в динамике показало активацию генерации АФК в 1 день и резкое снижение количества образования супероксиданиона в последующие дни исследования, особенно в клетках мышей I и III групп.
Показатели индуцированного латексом НСТ отражают резервные возможности фагоцитов к усиленной продукции АФК.
Установлено, что искусственная активация латексом приводит к снижению восстановления НСТ в клетках мышей, контактировавших с LT – энтеротоксином. Учитывая полученные результаты, можем констатировать факт о предельных возможностях работы ГМФШ-клеток под действием токсина, что, по-видимому, отражает недостаточность антиоксидантной системы фагоцитов, поскольку показатели количества образования свободных радикалов без индукции были намного выше. Близкие результаты были получены в работах Н.С. Олиферук и др. (2005), Ю.Н. Гончарук и др. (2006), Л.М. Сомовой и др. (2006). Результаты отражены в табл. 2.
Таблица 2
Динамика НСТ–редуцирующей способности перитонеальных макрофагов мышей в разные сроки исследования (М±m)
| Показатели | Группа животных (n=25) | Сроки исследования, сутки | |||
| 1 - е | 3 - и | 5 - е | 15 - е | ||
| Спонтанная НСТ-активность в % | I | 52,28±1,0* | 51,68±1,618* | 47,56±0,95* | 39,92±0,54* |
| II | 40,76±1,14* | 39,44±0,82* | 35,16±0,20 | 37,92±0,98* | |
| III | 55,32±0,69* | 30,64±1,04* | 33,16±1,05* | 26,32±0,49* | |
| Контроль | 36,20±0,25* | 36,40±0,25* | 35,88±0,33* | 33,44±1,85* | |
| Индуцированная НСТ–ак тивность в % | I | 64,60±2,03* | 53,76±0,78* | 42,44±0,62* | 45,44±0,22* |
| II | 58,60±2,13* | 52,44±0,49* | 50,04±1,08 | 45,76±0,28* | |
| III | 46,60±0,61* | 45,76±0,77* | 44,36±0,62* | 42,32±0,44 | |
| Контроль | 53,04±0,28 | 41,52±1,19 | 49,08±1,23 | 40,80 ±0,36 | |
*-различия статистически достоверны в сравнении с группой контрольных животных ( р<0,05).
Таким образом, у мышей, инфицированных LT-энтеротоксином E.cloacae, нарушалась способность перитонеальных макрофагов к восстановлению НСТ, что отражает дефекты кислородзависимых механизмов бактерицидности.
Исход фагоцитарной реакции, где участвуют фагоциты и бактерийные патогены, далеко не всегда заканчивается в пользу фагоцита. В ряде ситуаций микробной клетке удается, несмотря на ее поглощение фагоцитом, избежать последующего киллинга, что связано с различными приемами, выработанными патогеном в процессе микроэволюции. Как показывают приведенные данные, важным инструментом такой защиты от фагоцитов является LT-энтеротоксин E.cloacae.
Заключительным этапом функции антигенпредставляющих клеток является представление и определение направленности иммунного ответа (А.А. Тотолян и др., 2000; С.Н. Теплова и др., 2002; А.П. Топтыгина, 2008).
Исследования показали, что в селезенке I и III группы мышей выработка антителообразующих клеток (АОК) снижается, что может зависеть от подавления антигенпроцессинговой и антигенпрезентирующей функций фагоцитов на этапе фагоцитарного звена иммунитета. Различия с контролем в группе экспериментальных животных были статистически значимы (р<0,001). Результаты представлены на рис. 8.
Рис. 8. Антигенпредставляющая функция перитонеальных макрофагов мышей в разные сроки исследования (АОК102в селезенке)
*-данные статистически достоверны по q-критерию Ньюмена-Кейлса при р<0,05.
Данный факт послужил основанием к расшифровке механизма иммунной супрессии и проведению дальнейших опытов, характеризующих Т- и В- звено иммунитета.
Важнейшим показателем влияния стимулирующего агента на иммунную систему является пролиферативная активность лимфоцитов.
В результате проведенных исследований установлено, что LT-энтеротоксин E.cloacae обладает трансформирующим эффектом на Т-лимфоциты мышей. Следует отметить, что спонтанная пролиферативная активность лимфоцитов была выше, чем при стимуляции ФГА и КонА. Результаты отражены на рис. 9 и 10.
Рис. 9. Индуцированная митогенами (КонА, ФГА) пролиферативная активность Т-лимфоцитов мышей в динамике (%)
* р<0,05 по q-критерию Ньюмена-Кейлса.
Как видно из рисунка, LT-энтеротоксин E.cloacae стимулирует митотическую активность Т-лимфоцитов, подтверждением чему явились показатели индекса стимуляции.
Гуморальный иммунный ответ является специфической Th-2-зависимой формой реакции на внедрение чужеродных антигенов. Эффекторное звено такого отклика - это антигенспецифичные иммуноглобулины (А.П. Топтыгина, 2008).
Иммунный ответ организма имеет некоторые отличия, когда в роли патогена выступают внеклеточные или внутриклеточные паразиты. Поскольку ведущая роль в антиинфекционной защите организма от внеклеточной группы паразитов преимущественно принадлежит нейтрофилам, иммуноглобулинам и комплементу, в то время как в элиминации вторых - решающую роль играют Т-лимфоциты и макрофаги, хотя механизмы межклеточных коопераций в обоих случаях тесно взаимосвязаны друг с другом.
В связи с этим нами были проведены серии опытов по определению числа антителообразующих клеток к эритроцитам барана в селезенке, характеризующих гуморальный иммунный ответ хозяина.
Результаты исследований представлены на рис.11.
Рис.11. Динамика количества АОК-ЭБ в селезенке мышей
(АОК102 в селезенке), усл.ед.
*р<0,001по q-критерию Ньюмена-Кейлса;
**р<0,05 по q-критерию Ньюмена-Кейлса.
Как видно из рис.11, оценка В-звена иммунитета свидетельствует о снижении количества АОК в селезенке экспериментальных животных. Наиболее низкие показатели АОК отмечаются в I группе животных, зараженных LТ-энтеротоксином E.cloacae.
Таким образом, полученные результаты позволяют сделать вывод о том, что LТ-энтертоксин E. сloacae угнетает иммунный ответ мышей на ЭБ.
Кроме микробицидной и цитотоксической функции генерация супероксиданионрадикала способствует и иммунорегуляторному действию активированных фагоцитов, в частности, секреции цитокинов. Было установлено, что супероксидный анионрадикал участвует в выработке хемотаксических пептидов и индукции синтеза IL-1-подобного фактора (H.Schmidt et al., 2004), этому также свидетельствует большой спектр секретируемых макрофагами интерлейкинов, имеющих отношение к регуляции иммунного ответа (И.В. Дуда и др., 1978; С.А. Кетлинский и др., 1995; М.И. Карсонова и др., 2007). Функциональная активность цитокинов определяет направление дифференцировки T – клеток в Th1/Tc1, Th2/Tc2 тип, а также определяет класс иммуноглобулинов, на продукцию которого переключаются В-клетки (И.Н. Швыдченко и др., 2005).
В связи с этим было изучено влияние LT-энтеротоксина E. cloacae на уровень провоспалительных цитокинов (IL-6, IL-12, IFN-, TNF-), противовоспалительных цитокинов (TGF-, IL-10) и цитокинов, регулирующих специфические иммунные реакции (IL-2, IL - 4, IL - 15).
Изменения реактивности внутриклеточных механизмов макрофагов перитонеального экссудата подтвердили факт нарушения секреции интерлейкинов, регулирующих в последующем каскад иммуннологических реакций. В частности, в опытах по детекции посттранскрипционной экспрессии мРНК-интерлейкинов методом ПЦР с последующей амплификацией кДНК и дот-гибридизацией синтезированных ампликонов, удалось выявить существенные нарушения экспрессии отдельных цитокинов под влиянием LT-энтеротоксина E.cloacae.
В первой серии опытов мы изучали секрецию провоспалительных цитокинов, в частности, IL-6, IL-12, IFN- и TNF-.
Результаты экспериментов показали, что транскрипция мРНК IL - 6 в клетках отмечается лишь на 3-и сутки. Так, радиографические сигналы наблюдались в клетках нейтрофилов контрольной и I группы животных, тогда как макрофаги сигнализировали их только у животных II группы.
IL - 6 повышает бактерицидность нейтрофилов без достоверных изменений показателей фагоцитоза, так как действует в постактивационный период жизни гранулоцита, запуская внутриклеточные механизмы бактериолиза и продлевая жизнь гранулоцита. IL - 6 в синергизме с IL-2 участвует также в активации и индукции пролиферации Т-лимфоцитов, является индуктором синтеза острофазных белков (А.А.Тотолян, 2000).
В экспериментах IL-12 транскрибировался в клетках макрофагов и нейтрофилов во всех группах животных как на 1-е сутки, так и на 15-е сутки исследования.
Транскрипция TNF- отмечалась слабо на 5-е сутки исследования, как в опытных, так и в контрольной группе животных. У нейтрофилов сигнализировала радиографическая метка в контроле, а в макрофагах - только в опытных группах животных.
Существенные изменения наблюдались в транскрипции мРНК IFN-. Установлено, что транскрипция мРНК в нейтрофилах III группы животных происходила во все сроки исследования, но пик транскрипции мРНК приходился на 5-е сутки. В I группе животных радиометка сигнализировала только в 1-й день исследования. В остальных группах мышей радиографического сигнала не наблюдалось.
В макрофагах I группы животных экспрессия IFN- наблюдалась на 1-е сутки опытов и указывала на раннюю, возможно, ложную стимуляцию, поскольку в последующие дни экспериментов сигнала радиографической метки не наблюдалось. В I и II группах животных интенсивность радиографического сигнала усиливалась на 3- и сутки. В контрольной группе мышей транскрипция мРНК IFN- не обнаружена.
В следующей серии экспериментов была изучена транскрипция мРНК TGF- и IL-10.
Отличия в транскрипции мРНК отмечались в TGF-. Как показали исследования, экспрессия TGF- определялась макрофагальными клетками только в 1-е сутки опытов в I группе мышей. В контрольной группе животных наблюдались слабые сигналы.
В экспериментах транскрипция мРНК IL-2, IL-4 и IL-10 как у макрофагов, так и у нейтрофилов, не наблюдалась. Однако, важная роль в дифференцировке клеточного и гуморального типа иммунного ответа хозяина принадлежит именно IL-2 и IL-4 (S. Pasare, R. Medzhitov, 2004).
Изучение экспрессии мРНК IL-15 показало появление радиографического сигнала во всех изучаемых группах мышей на 1-й день опытов, как в нейтрофилах, так и в макрофагах. При этом интенсивность радиографического сигнала в макрофагах была выше в контроле и в I группе мышей.
Следует отметить, что, по литературным данным, IL-15 вырабатывается только макрофагами и по своему действию близок к IL-2. При участии IL-15 осуществляется пролиферация активированных Т-клеток и дифференцировка цитотоксических Т-лимфоцитов, а также активация NK-клеток (A.J. Talati et al., 2008), что противоречит полученным нами результатам.
Таким образом, можно заключить, что LT-энтеротоксин E.cloacae, способствуя повышенной экспрессии TGF-, подавляет в целом иммунологические реакции организма хозяина. Ранняя ложная индукция экспрессии IFN- макрофагами, возможно, имеет иммунокомпрометирующее значение, поскольку IFN- обладает плейотропным действием. Отсутствие в нейтрофилах транскрипции мРНК ключевых цитокинов указывает на то, что они как бы выключаются из цитокиновой регуляции иммунного ответа в инфекционном процессе.
Макрофаги определяют первую линию защиты организма и испытывают на себе влияние факторов как бактериальной природы, так и образующихся в процессе иммунного ответа, причем патогены способны индуцировать их апоптоз.
Представления о спектре механизмов бактерийного выживания при инфекции в последнее время расширились за счет установления способности микробных патогенов регулировать процесс апоптоза. В условиях инфекционной патологии обычно апоптоз выполняет функцию защиты макроорганизма, где гибель инфицированных клеток с последующей их элиминацией из организма предотвращает распространение инфекции. Однако некоторые патогены, в частности, облигатные внутриклеточные паразиты в условиях инфицированного организма «отменяют» клеточную гибель, поддерживая жизнь клеток хозяина, тем самым способствуя собственному выживанию и персистенции (D.W. McGee et al., 1992; S. Mathias et al., 1993; C.S. Reise et al., 1999).
В связи с этим, представлялось целесообразным изучить влияние LT-энтеротоксина E.cloacae на программированную клеточную гибель клеток хозяина.
Цитометрический анализ клеток перитонеального экссудата (КПЭ) с использованием двух видов светорассеяния (малого и под углом 90° С) показал, что КПЭ содержит две основные субпопуляции клеток, различающихся размерами и гранулярностью цитоплазмы.
Результаты исследования представлены на рис.12.
Рис.12. Уровень апоптоза клеток перитонеального экссудата мышей
в динамике (усл.ед.)
*р<0,001 по q-критерию Ньюмена-Кейлса;
**р<0,05 по q-критерию Ньюмена-Кейлса.
Из рис. 12 видно, что во всех опытных группах отмечается появление апоптотических клеток. Однако, статистически достоверные различия по сравнению с контролем наблюдались только в I группе мышей. Установлено, что в I группе мышей, зараженной LТ-энтеротоксином E.cloacae, количество ушедших в апоптоз клеток было значительно больше по сравнению с другими опытными группами. При этом количество апоптотических клеток в указанных группах были сопоставимы с показателями контрольной группы.
Данные B. Yankelevich и др. (1997) свидетельствуют о факте запуска программированной смерти CD4+ лимфоцитов, индуцируемого Ext В фрагментом термолабильного энтеротоксина E.coli и CD8+-холерогеном.
Таким образом, результаты изучения апоптоза клеток перитонеального экссудата, показывают, что термолабильный энтеротоксин E.cloacae может влиять на процесс апоптоза клеток перитонеального экссудата мышей.
Обобщая полученные результаты, можно заключить, что LT-энтеротоксин Enterobacter spp. является важным фактором патогенности, определяющим особенность развития инфекционного заболевания. Мишенями для его действия являются иммунокомпетентные клетки. Характеристика термолабильного энтеротоксина создает основу для разработки рациональных подходов в диагностике и лечении патологий, вызванных энтеротоксигенными Enterobacter spp.
ВЫВОДЫ
- Штаммы бактерий рода Enterobacter, выделенные при инфекционно-воспалительной патологии желудочно-кишечного тракта, мочевыделительной системы и гнойно-воспалительных процессах различной локализации, фенотипически характеризуются свойствами патогенности (способностью к адгезии, продукции цитолизинов, токсинообразованию и персистентными свойствами).
- Колониальная организация микроорганизмов Enterobacter spp. характеризуется морфологической гетерогенностью, входящих в её состав клеток: обнаружены активно делящиеся формы с образованием клеточных кластеров; покоящиеся; спонтанно аутолизирующиеся клетки. В концентрических зонах колоний микробы преимущественно представлены клетками, образующими «швермеры», с избыточным количеством жгутиков, не способных к делению. Адгезивная активность бактерий рода Enterobacter обусловлена наличием ресничек длиной 297,8±152,8 нм и шириной 4,91±0,53 нм, способных агглютинировать эритроциты птиц.
- Выявление у бактерий рода Enterobacter генетических фрагментов, определяющих их патогенность и токсигенность, идентичных с генами, входящими в состав “островков патогенности” E.coli, свидетельствует о едином генетическом механизме изменения патогенности и токсигенности.
- В основе патогенетического механизма инфекционных процессов, обусловленных энтеротоксинпродуцирующими штаммами бактерий рода Enterobacter, лежит иммуносупрессивное действие термолабильного энтеротоксина на антигенпрезентирующую и антигенпроцессинговую функцию макрофагов, которое отражается на развитии иммунных реакций как алло-, так и аутогенных антигенов снижением числа антителообразующих клеток.
- Механизм супрессивного действия термолабильного энтеротоксина может быть связан с ложной индукцией трансформирующего ростового фактора- макрофагами перитонеального экссудата, основная функция которого заключается в подавлении пролиферативной активности антигенспецифических клеток. Термолабильный энтеротоксин нарушает экспрессию интерферона- макрофагами и нейтрофилами, что может оказывать иммунокомпрометирующее плейотропное действие на развитие иммунных реакций хозяина.
- Термолабильный энтеротоксин Enterobacter spp. нарушает функцию ферментов гексозо-монофосфатного шунта фагоцитов, что проявляется снижением образования супероксиданионов, с последующим уменьшением микробиоцидной функции макрофагов и нейтрофилов.
- Термолабильный энтеротоксин Enterobacter spp. усиливает реакцию бласттрансформации лимфоцитов, в основе которой лежит нарушение проницаемости лизосомальных мембран, характеризующееся “опустошением” лизосомальных гранул клеток.
- В результате действия энтеротоксинпродуцирующего штамма Enterobacter spp. прекращется транскрипция мРНК фактора некроза опухоли- нейтрофилами. Это явление может служить причиной дизрегуляции запрограммированной клеточной смерти под влиянием фактора некроза опухоли-, секретируемого нейтрофилами.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Штаммы Enterobacter gergoviae ГИСК №259, Enterobacter cloacae ГИСК №258, Enterobacter agglomerans ГИСК №257 рекомендуется использовать в качестве эталонных культур при идентификации выделенных штаммов от больных и в биотехнологии в качестве суперпродуцентов термолабильного энтеротоксина.
2.Для установления этиологической значимости Enterobacter spp. при патологиях желудочно-кишечного тракта, мочевыделительной системы и гнойно-воспалительных процессах рекомендуется определение их факторов патогенности.
3.Для расшифровки инфекций, вызванных УПЭ, а также бактериями рода Enterobacter, рекомендуется определение генетических маркеров патогенности: HlyA, HlyB, papAH, papC, sfaA, sfa G.
4.Знания об иммуномодулирующих свойствах термолабильного энтеротоксина Enterobacter spp., рекомендуется использовать при подборе лечебно-профилактических препаратов в терапии инфекций, вызванных токсигенными условно-патогенными энтеробактериями, в частности, бактериями рода Enterobacter.
Список работ, опубликованных по теме диссертации
- О некоторых биологических свойствах бактерий рода Еnterobacter [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Д.Т. Гашимова, А.Р. Мавзютов // Идеи Пастера в борьбе с инфекциями: материалы второй международной конференции, посвященной 75-летию института им. Пастера. – СПб., 1998. С. 124.
- Об антибиотикорезистентности бактерий рода Enterobacter [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Д.Т. Гашимова, А.Р. Мавзютов // Вопросы теоретической и практической медицины: тезисы докладов Республиканской научной конференции молодых ученых. - Уфа, 1999. С. 13.
- Ахтариева, А.А. К вопросу о патогенном потенциале бактерий рода Enterobacter [Текст] / А.А. Ахтариева, Д.Т. Гашимова, М.М. Туйгунов // Вопросы теоретической и практической медицины: тезисы докладов Республиканской научной конференции молодых ученых. - Уфа, 1999. – С. 13.
- Ахтариева, А.А Продукция энтеробактерами энтеротоксина [Текст] / А.А. Ахтариева, Д.Т. Гашимова, М.М. Туйгунов // Вопросы теоретической и практической медицины: тезисы докладов Республиканской научной конференции молодых ученых. - Уфа, 1999. – С. 13.
- Ахтариева А.А. Адгезивная способность бактерий рода Enterobacter [Текст] / А.А. Ахтариева, А.А. Камалова // Вопросы теоретической и практической медицины: тезисы докладов Республиканской научной конференции молодых ученых. - Уфа, 1999. – С. 13.
- Пат. №2161197 Рос. Федерация Штамм бактерий Enterobacter gergoviae ГИСК №259, обладающий комплексом факторов патогенности / А.А. Ахтариева, М.М. Алсынбаев, З.Г. Габидуллин, Р.Х. Хананова, А.К. Булгаков, В.Ф, Кулагин, Р.З. Суфиярова, Ю.З. Габидуллин, М.М, Гафаров, Р.А. Очилова (Российская Федерация). - №99124328; заявл. 18.11.1999, опубл. 27.12.2000, Бюл. №36. - 6с.
- Пат. №2162485 Рос. Федерация Штамм бактерий Enterobacter agglomerans ГИСК №257, обладающий комплексом факторов патогенности / А.А. Ахтариева, З.Г. Габидуллин, М.М. Алсынбаев, В.Ф. Кулагин, О.В. Кунягина, В.В. Ленгесова, А.А.Гарифуллин, А.Р. Мавзютов, М.М. Гафаров, Р.С. Суфияров, Д.Т. Гашимова (Российская Федерация). - №2000106136; заявл. 13.03.2000, опубл. 27.01.2001, Бюл. №3. - 6с.
- Пат. №2164942 Рос. Федерация Штамм бактерий Enterobacter cloacae ГИСК №258, обладающий комплексом факторов патогенности / А.А. Ахтариева, З.Г. Габидуллин, М.М. Алсынбаев, В.Ф. Кулагин, В.В. Ленгесова, Р.Х. Хананова, А.К. Булгаков, А.А.Гарифуллин, Ю.З. Габидуллин, Р.З. Суфиярова,А.Б. Бакиров (Российская Федерация). - №2000106268; заявл. 13.03.2000, опубл. 10.04.2001, Бюл. №10. - 6с.
- Некоторые биологические свойства бактерий рода Enterobacter [Текст] / А.А. Ахтариева, В.В. Ленгесова, Р.К. Хананова, З.Г. Габидуллин, Ю.З. Габидуллин // Дерматовенерологической службе Республики Башкортостан – 80 лет: сборник трудов Республиканской конференции. - Уфа, 2000. С. 6768.
- Ахтариева, А.А. Ауксо- и прототрофность бактерий рода Enterobacter [Текст] / А.А. Ахтариева, А.А. Камалова, А.Н. Ишмухаметова // Вопросы теоретической и практической медицины: тезисы докладов 65й юбилейной научной конференции студентов и молодых ученых Башкирского государственного медицинского университета. - Уфа, 2000. Т. 1. - С. 16.
- Ахтариева, А.А. Антилизоцимная и антиинтерфероновая активность бактерий рода Enterobacter [Текст] / А.А. Ахтариева, А.А. Камалова, А.Н. Ишмухаметова // Вопросы теоретической и практической медицины: тезисы докладов 65й юбилейной научной конференции студентов и молодых ученых Башкирского государственного медицинского университета. - Уфа, 2000. Т. 1. - С. 1617.
- Ахтариева, А.А. Гемолитическая активность бактерий рода Enterobacter [Текст] / А.А. Ахтариева, А.А. Камалова, А.Н. Ишмухаметова // Вопросы теоретической и практической медицины: тезисы докладов 65й юбилейной научной конференции студентов и молодых ученых Башкирского государственного медицинского университета. - Уфа, 2000. Т. 1. - С. 17.
- Некоторые персистирующие свойства штаммов провиденция и энтеробактер [Текст] / А.Н. Ишмухаметова, А.А. Ахтариева // Вопросы теоретической и практической медицины: тезисы докладов 65й юбилейной научной конференции студентов и молодых ученых Башкирского государственного медицинского университета. - Уфа, 2000. Т. 1. - С. 19.
- Ахтариева, А.А. Некоторые персистентные свойства бактерий рода Enterobacter [Текст] / А.А. Ахтариева, А.А. Камалова // Здравоохранение Башкортостана. 2000. № 2: спец. вып. С. 1517.
- Ахтариева, А.А. Антибиотикорезистентность штаммов Enterobacter, выделенных в городе Уфе [Текст] / А.А. Ахтариева, Д.Т. Гашимова, А.А. Камалова // Вопросы теоретической и практической медицины: тезисы докладов научной конференции студентов и молодых ученых Башкирского государственного медицинского университета. – Уфа, 2001. С. 16.
- Ахтариева, А.А. Роль бактерий рода Enterobacter в патологии экстрагенитальных заболеваний [Текст] / А.А. Ахтариева, З.Г. Габидуллин, А.А. Камалова // Актуальные проблемы материнства в медицине труда: материалы докладов российской научно–практической конференции. – Уфа, 2001. С. 251253.
- Ахтариева, А.А. Распространенность бактерий рода Enterobacter в больничных стационарах г. Уфы [Текст] / А.А. Ахтариева, З.Г. Габидуллин, А.А. Камалова // Материалы VIII съезда Всероссийского общества эпидемиологов, микробиологов и паразитологов. – М., 2002. Т. 3. С. 137-138.
- Лекарственная устойчивость штаммов Enterobacter spр., выделенных на территории республики Башкортостан [Текст] / А.А. Ахтариева, З.Г. Габидуллин, А.А. Камалова, И.Ш. Хурамшина, А.Р. Мурзаганеева // Материалы VIII съезда Всероссийского общества эпидемиологов, микробиологов и паразитологов. – М., 2002. Т. 4. С. 78-80.
- Ахтариева, А.А. Изучение антибиотикорезистентности бактерий рода Enterobacter, выделенных на территории республики Башкортостан [Текст] / А.А. Ахтариева, Р.З. Саляхов, Т.А. Савченко // Здравоохранение Башкортостана. - 2002. № 3: спец. вып. С. 14-16.
- Ахтариева, А.А. Анализ распространенности бактерий рода Enterobacter в экологически неблагоприятных регионах Башкирии [Текст] / А.А. Ахтариева, З.Г. Габидуллин, А.А. Камалова // Наука-Образование-Производство в решении экологических проблем: материалы международной научно технической конференции. - Уфа, 2002. – Т. 2. С. 349351.
- Адгезивная активность клинических штаммов Enterobacter [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Т.А. Савченко, А.А. Камалова // Гомеостаз и инфекционный процесс: III общероссийская конференция с международным участием. - Сочи, 2002. С. 11.
- Показатели иммунного статуса у больных с гнойно-воспалительными заболеваниями [Текст] / Р.А. Нигматуллина, А.А. Ахтариева, М.М. Туйгунов, З.Г. Габидуллин, Т.А. Савченко, Р.З. Саляхов, А.А. Камалова // Иммунология Урала. – 2003. № 1 (3): Материалы III конференции иммунологов Урала. С. 67-68.
- Антибиотикочувствительность условно-патогенных энтеробактерий, выделенных при инфекциях мочевыводящих путей [Текст] / Р.З. Саляхов, З.Г. Габидуллин, В.З. Галимзянов, А.К. Булгаков, А.А. Ахтариева, М.М. Туйгунов // Иммунология Урала. – 2003. № 1 (3): Материалы III конференции иммунологов Урала. С. 109.
- Ахтариева, А.А. Гемолитическая активность бактериий рода Enterobacter [Текст] / А.А. Ахтариева, Т.А. Савченко, Р.З. Саляхов, А.А. Камалова // Успехи современного естествознания. – 2003. № 8: Гомеостаз и инфекционный процесс: материалы III общероссийской конференции с международным участием. – С. 72.
- Факторы патогенности клинических штаммов Enterobacter [Текст] / Ю.З. Габидуллин, А.А. Ахтариева, Т.А. Савченко Р.З. Саляхов, А.А. Камалова, Ю.З. Габидуллин // Современные проблемы диагностики и лечения дисбактериозов: материалы конференции, посвящ. 10-летию НПЦ лечения дисбактериозов НИИ иммунологии ЧелГМА и 60-летию ГОУ ВПО «Челябинская Государственная медицинская академия МЗ РФ». Челябинск, 2004. С. 10-11.
- Гемолитическая активность клинических штаммов бактерий рода Enterobacter, Citrobacter, Klebsiella, Proteus, E.coli, Shigella dуsenteriae, Serratia, St.aureus, Str. pneumoniae, выделенных в виде смешанных и монокультур [Текст] / З.Г. Габидуллин, А.К. Булгаков, Р.З. Саляхов, Ю.З. Габидуллин, М.М. Туйгунов, А.А. Ахтариева // Актуальные вопросы инфекционной патологии человека, клиники и прикладной медицины: материалы Всероссийской научной конференции молодых ученых. - Уфа, 2004. С. 43-44.
- Структура высеваемости и антибиотикорезистентность бактерий рода Enterobacter, выделенных от пациентов урологического отделения ГКБ №8 за 2003 год [Текст] / Р.Р. Нигматуллина, Д.В. Шемагонов, А.А. Ахтариева, Р.З. Саляхов, Ю.З. Габидуллин, Т.А. Савченко, А.А. Камалова // Материалы 69–ой межвузовской научной конференции. - Курск, 2004. – Ч. 1. С. 224-225.
- Влияние термолабильного энтеротоксина Enterobacter cloacae на отдельные звенья иммунной системы [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, А.А. Камалова // Иммунология Урала. – 2005. – Вып. 1, № 4: Материалы VI конференции иммунологов Урала. С. 2-3.
- Некоторые особенности факторов патогенности бактерий рода Enterobacter spр., Serratia spр. в виде моно – и ассоциированных культур [Текст] / Ю.З. Габидуллин, З.Г. Габидуллин, А.А. Ахтариева, А.К. Булгаков, М.М. Туйгунов, Р.З. Саляхов, Э.Ф. Мамбетова, Н.Н. Гибазов // Здравоохранение Башкортостана. - 2005. № 3: Актуальные вопросы урологии, заболевания предстательной железы. Новые технологии в урологии: материалы Респуб. науч. конф. С. 322-323.
- Ахтариева, А.А. Роль термолабильного энтеротоксина бактерий рода Enterobacter в системе «патоген - хозяин» [Текст] / А.А. Ахтариева, З.Г. Габидуллин, А.А Камалова // Медицинский вестник Башкортостана. - 2006. – № 1: Актуальные вопросы современной фармации и фармацевтического образования: сборник научных трудов юбилейной конференции, посвящ. 25-летию фармацевтического факультета Башкирского государственного медицинского университета. С. 218-220.
- Изучение влияния термолабильного энетротоксина бактерий рода Enterobacter spр. на функциональную активность перитонеальных макрофагов в эксперименте [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, Ю.З. Габидуллин, Н.Г. Насибуллин // Известия Челябинского научного центра: электронный журнал. – 2006. - Вып. 2, № 32. С. 120-122.
- Патогенетическое значение термолабильного энтеротоксина и антикомплементарной, антиинтерфероновой и антилизоцимной активности бактерий рода Enterobacter в условиях выживания в организме хозяина [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Ю.З. Габидуллин, Ф.С. Билалов, Э.Ф. Мамбетова, А.А. Камалова // Новые лабораторные технологии в диагностике и лечении заболеваний человека: материалы конференции, посвящ. 25-летию ЦНИЛ ЧГМА. - Челябинск, 2006. С. 98-100.
- Изучение влияния ЛТ – энтеротоксина некоторых представителей бактерий семейства Enterobacteriaceae на лизосомальную активность перитонеальных макрофагов в эксперименте [Текст] / А.А. Ахтариева, Э.Ф. Мамбетова, Ф.С. Билалов, З.Г. Габидуллин // Здоровье семьи – XXI века: материалы X международной научной конференции (Бангкок - Паттайя, Тайланд, 2006 г.). М., 2006. - С. 2526.
- Характеристика свойств, определяющих персистенцию моно–ассоциированных культур условно – патогенных энтеробактерий [Текст] / Ю.З. Габидуллин, А.А. Ахтариева, М.М. Алсынбаев, М.М. Туйгунов, Э.Т. Галимова, Ф.С. Билалов // Журн. микробиол., эпидемиол. и иммунобиол. 2006. № 4. С. 62-64.
- Функциональная активность перитонеальных фагоцитов и энтеротоксигенные бактерии рода Enterobacter [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Т.А. Савченко, Р.А. Кудакаева, Д.Н. Аскарова, Т.С. Корюкова, А.А. Камалова // Медицинская наука – 2007: материалы Респуб. конф. молодых ученых Республики Башкортостан, посвящ. году единства Башкортостана с Россией, 75–летию БГМУ, Дню медицинского работника. - Уфа, 2007. С. 6-7.
- Влияние термолабильного энтеротоксина бактерий рода Enterobacter cloacae на фагоцитарную активность перитонеальных макрофагов мышей [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, Ю.З. Габидуллин, А.А. Камалова // Журн. микробиол., эпидемиол. и иммунобиол. 2007. № 4. С. 58-61.
- Состояние некоторых звеньев иммунной системы мышей, инфицированных энтеротоксинпродуцирующими штаммами бактерий рода Enterоbacter [Текст] / А.А. Ахтариева, И.И. Долгушин, Ю.З. Габидуллин, З.Г. Габидуллин, Т.А. Савченко, Г.К Давлетшина // Журн. микробиол., эпидемиол. и иммунобиол. 2007. № 4. С. 84-87.
- Оценка влияния энтеротоксинпродуцирующих Enterоbacter cloacae на внутриклеточный кислородзависимый метаболизм перитонеальных макрофагов мышей [Текст] / Ю.З. Габидуллин, З.Г. Габидуллин, Т.А. Савченко, Ф.С. Билалов, Э.Ф. Мамбетова, А.А Камалова // Материалы IX съезда Всероссийского научно-практического общества эпидемиологов, микробиологов и паразитологов. – М., 2007. Т. 2. С. 209.
- Функциональная активность перитонеальных фагоцитов и энтеротоксигенные бактерии рода Enterobacter [Текст] / А.А. Ахтариева, З.Г. Габидуллин, Т.А. Савченко, Р.Х. Кудакаева, Д.Н. Аскарова, Т.С. Корюкова, А.А. Камалова // Медицинская наука – 2007: материалы Респуб. конф. молодых ученых Республики Башкортостан, посвящ. году единства Башкортостана с Россией, 75–летию БГМУ, Дню медицинского работника. - Уфа, 2007. С. 6-7.
- Влияние энтеротоксина Enterobacter на клеточное звено иммунитета [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, А.А. Камалова // Журн. микробиол., эпидемиол. и иммунобиол. 2008. № 3. – С. 96-98.
- Изучение действия термолабильного энтеротоксина Enterоbacter cloacae на экспрессию генов цитокинов мышей [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, Ю.З. Габидуллин, А.А. Камалова, Р.М. Ахмадеев // Журн. микробиол., эпидемиол. и иммунобиол. 2009. № 5. – С. 62-66.
- Влияние термолабильного энтеротоксина Enterоbacter cloacae на иммунную систему мышей [Текст] / А.А. Ахтариева, И.И. Долгушин, З.Г. Габидуллин, Ю.З. Габидуллин, А.А. Камалова, Р.Р. Суфияров // Журн. микробиол., эпидемиол. и иммунобиол. 2009. № 6. – С. 98-104.
- Взаимодействие бактерий семейства Enterobacteriaceae c антигенпрезентирующими клетками иммунной системы организма [Текст] / З.Г. Габидуллин, А.А. Ахтариева. М.М. Туйгунов, Р.С. Суфияров, В.Г. Туйгунова, Н.Х. Насибуллин. Р.Р. Суфияров, Ю.З. Габидуллин, Г.А. Идиатуллина, В.М. Изикаев // Медицинский вестник Башкортостана. – 2009. - Т. 4, № 5. – С. 78-86.
- Факторы патогенности бактерий семейства Enterobacteriacae, обеспечивающие выживание в организме хозяина [Текст] / З.Г. Габидуллин, А.А. Ахтариева, М.М. Туйгунов, Р.С.Суфияров, В.Г. Туйгунова, Р.Р. Суфияров, Ю.З. Габидуллин, В.М. Изикаев, Г.А. Идиатуллина // Медицинский вестник Башкортостана. – 2009. - Т. 4, № 5. – С. 86-94.
- Регуляция апоптоза бактериальными клетками семейства Enterobacteriacеae [Текст] / З.Г. Габидуллин, А.А. Ахтариева, М.М. Туйгунов, Р.С. Суфияров, В.Г. Туйгунова, Р.Р. Суфияров, Ю.З. Габидуллин, Г.А. Идиатуллина, В.М. Изикаев, А.А. Габдрахманова // Медицинский вестник Башкортостана. – 2009. - Т. 4, № 6. – С. 68-76.
На правах рукописи
Ахтариева
Айгуль Атласовна
ИММУНОБИОЛОГИЧЕСКИЕ СВОЙСТВА
ТЕРМОЛАБИЛЬНОГО ЭНТЕРОТОКСИНА
БАКТЕРИЙ РОДА ENTEROBACTER
В СИСТЕМЕ ВЗАИМОДЕЙСТВИЯ “ПАТОГЕН - ХОЗЯИН”
03.02.03 – микробиология
14.03.09 – клиническая иммунология, аллергология
Автореферат
диссертации на соискание ученой степени
доктора медицинских наук

