Концепция регуляции сердечно-сосудистой системы –
от управления функциями к согласованию возможностей (часть1 - физиологические предпосылки)
Л.А. Бокерия, В.А. Лищук
НЦССХ им. А.Н. Бакулева РАМН
Аннотация
Ключевые слова: сердечно-сосудистый (бульбарный) центр, центральная команда, продолговатый мозг, кровообращение, сердце, сосуды, регуляция, согласование, математическая модель, имитация, интенсивная терапия, УО, МОК, АД.
(Введение) Клинико-физиологическое обоснование регуляции сердечно-сосудистой системы - актуальная задача современной интенсивной терапии (Л.А. Бокерия, 2004). Её актуальность и сложность особенно значимы при лечении таких тяжёлых больных, которые преобладают в нашем Центре, вообще в кардиологической ИТ. Сравнительно простой пример. Снижая артериальное давление, чтобы разгрузить больное сердце (вводя в/в нитропруссид, арфонад или применяя закись азота и т.п.), мы ограничиваем возможности перераспределения кровотока, ставим под удар кровоснабжение почек, головного мозга, желез и других органов. Повышая артериальное давление (вводя капельно адреналин, мезатон, норадреналин и т.п.), чтобы поддержать кровоснабжение тканей и органов, увеличиваем нагрузку на больное сердце и, в результате, создаём предпосылку для последующего падения СИ. Эти наши меры изменяют естественную регуляцию сердечно-сосудистой системы. Поэтому они должны исходить не только из необходимости поддержания адекватного артериального давления, ресурсов миокарда и потребностей в кровоснабжении мозга, сердца, почек и др. органов, но и должны быть согласованы с естественной регуляцией кардио- и гемодинамики, которая в норме согласует эти запросы метаболизма, возможности сердца и артериальное давление. И при патологии регуляторные механизмы, как правило, изменяют функцию ССС адекватно. А если мы берём управление на себя, то должны учитывать ответ организма, его многоуровневой регуляции на наше вмешательство. Вы подумаете: «так оно и есть». Посмотрите «Российские рекомендации» по диагностике и лечению острой сердечной недостаточности [2]. Регуляция, если и отражена, то опосредованно, через нарушения функции сердца, сосудов, почек, лёгких, и др. органов. Или через такие обобщения, как кома, стресс, шок («кардиогенный шок — клинический синдром, характеризующийся гипоперфузией тканей из-за СН, которая сохраняется после коррекции преднагрузки», как видите, и здесь регуляция не отображается в явном виде [2]). Более того, игнорирование расстройств регуляции как причины заболевания принято сейчас на уровне методологии: «никакая болезнь не может начинаться с нарушений регуляции» [3]. Чуть далее в этом, несомненно, фундаментальном и одним из лучших учебников написано: «Придерживаться иной точки зрения, а именно: допустить, что болезнь может начинаться с нарушения регуляторных процессов …, - это значит отойти от материалистической позиции в учении о болезни и в противоречии с принципом единства структуры и функции утверждать, что инициальным звеном болезни может быть первичное повреждение той или иной функции» [3]. Но перегрузка функции, вызванная внешними причинами, часто вызывает повреждения органов. А нарушение регуляции, например, дезадаптация или, скажем, дисбаланс регуляции артериального давления (АД) и кровотока (сердечного выброса, СВ) порождает расстройства кровообращения и, соответственно, проблемы адекватной медикаментозной терапии, когда сердце не обеспечивает нозологическую норму, а естественная регуляция не поддерживает АД на гомеостатическом уровне. Поэтому независимо от того, что было вначале - яйцо или курица, изучение регуляции сердечно-сосудистой системы нам представляется актуальным и в клинической медицине недооцененным.
Основная функция, которую сердечно-сосудистая система выполняет, вне зависимости от других систем, - адекватное, в соответствии с потребностями метаболизма и другими запросами организма, снабжение кровью тканей и органов. Эта функция определяется способностью мышечных насосов сердца, вкладом скелетных мышц и тканевого интерстициального давления в продвижение крови по сосудам и через стенки капилляров, вязкостью и объёмом крови, структурой, эластичностью и тонусом сосудистых резервуаров, клапанами вен и сфинктерами артериол, включая саморегуляторные свойства большинства из этих компонентов сердечно-сосудистой системы, а также системами нейроэндокринной и гуморально-молекулярной регуляции кровообращения. Снабжая клетки тканей и органов кровью, сердечно-сосудистая система участвует в комплексе смежных функциональных систем (дыхания, производства энергии, выделения, теплообмена и др.), доставляющих кислород, глюкозу, питательные вещества, жирные кислоты, витамины, гормоны, стволовые клетки, тепло и т.п. Кроме того, эти системы обеспечивают вывод продуктов метаболизма, углекислоты, шлаков и т.п.
Многие авторы считают также важными функциями сердечно-сосудистой системы
генерацию волн, несущих как массажную, так и информационную функцию,
генерацию электрических потенциалов и полей,
эндотелиальную барьерную защиту крови и интерстиция,
кровенаполнение органов и тканей, определяющее давление в них и формообразование их полостей,
создание давления в сосудистых областях как предпосылку адекватного кровотока и как самостоятельную функцию, детерминирующую поставку кислорода, вывод углекислоты, фильтрацию и реабсорцию, наконец, может быть,
создание линейной скорости крови, участвующей через давление сдвига в и стабилизации градиента давлений и др.
Мы не претендуем на отражение в представляемой концепции всего этого многообразия явлений, связанных с кровообращением. Представляемая здесь гипотеза будет обобщать (и то со многими допущениями) регуляцию основной функции сердечно-сосудистой системы - снабжение организма человека, его клеток, тканей и органов кровью в нормальных условиях жизнедеятельности. В качестве примеров подтверждения этой гипотезы будут рассмотрены некоторые патологические состояния, имеющие значение для кардиологической интенсивной терапии. В основном, - это режимы гемодинамики, ограниченные интервалами времени от секунд до дней и нагрузками, свойственными кардиохирургическому лечению (гипо- и гиперволемия, введение катехоламинов, анестезия и т.п.; подробнее см. публикации Л.А. Бокерия и др., 2007; В.А. Лищук, 2008). Эти состояния столь разнообразны, что требуют отдельного обсуждения. Здесь мы ограничиваемся лишь примерами, а основное содержание посвящено собственно концепции. Концепция сориентирована на отображение основных законов и целей систем регуляции сердца и сосудов и отношений между этими системами регуляции. Для этого мы, естественно, были вынуждены абстрагироваться от биофизических и биохимических механизмов, реализующих те или другие контуры управления, и использовать термины и методы общей теории регулирования.
Классические представления о сердечно-сосудистом центре. Долгое время в руководствах и учебниках классическая концепция «вазомоторного центра» представлялась единственной, обобщающей факты и представления по регуляции сердца и сосудов (например, у Фолкова и Нила (стр. 248 - 251), Амосова Н.М., и др. (стр. 33 - 52); рис.1 [6,7,8]). Действительно, она удачно отображала реципрокные отношения между симпатическим и вагусным влиянием на миокард, барорецепторные рефлексы, эффекты раздражения прессорных и депрессорных точек продолговатого мозга, роль спинальных центров, афферентную импульсацию от хеморецепторов внутренних органов и кожи и т.п. Кора головного мозга, гипоталамус, гипофиз, как и нейроэндокринная регуляция в целом, по классическим представлениям также оказывают (прямые и/или опосредованные) как бы дополнительные возбуждающие и тормозящие влияния на вазомоторный центр. Причём эти влияния рассматривались как постоянные (фоновые), так и ситуационные (эмоциональное возбуждение, стресс и т.п.).

Рис.1. Схема, отображающая классические представления о регуляции сердечно-сосудистой системы. Она соответствует представлению Пейса о классическом бульбарном центре [28]. Пейс - наиболее последовательный и жёсткий критик классической гипотезы. Обращаем внимание читателей, что даже в его видении структуры бульбарного центра имеют место связи с гипоталамусом и корой. Многие авторы критикуют классическую гипотезу, ставя ей в вину отсутствие таких связей. Спинальные центры показаны не как проводники, а как звенья, обрабатывающие сигналы (см. схему). Это обстоятельство так же не замечают авторы новых гипотез (см. наш текст далее).
Сам центр представлялся автономным, т.е. способным выполнять свою функцию (в основном, поддерживать артериальное давление) самостоятельно при отсоединении от него вышележащих (супрабульбарных) нервных образований [9]. Последние в норме могут менять режим его работы, выполняя функции настройки. При этом нейроны медиальной области продолговатого мозга могут регулировать сердечно-сосудистую систему и самостоятельно, если организм находится в покое. В покое имеет место спонтанная нервная активность нейронов бульбарного центра (по преимуществу тормозящая). Последняя существенно зависит от местных биохимических условий (рН, рО2, рСО2 и др.).
Впервые зависимость работы сердца и тонуса сосудов от активности нейронов, принадлежащих каудальным отделам мозгового ствола выявил в экспериментах Ф.В. Овсянников (1871 г.) [9]. Он показал, что значимого падения артериального давления при последовательных пересечениях мозгового ствола до уровня каудальнее нижнего четверохолмия не происходит. Продолжение перерезок с переходом в область пентобульбарного отдела мозга даёт существенное падение артериального давления. Деструкция дорсальной, как и вентромедиальной частей продолговатого мозга не влияет на давление. В.Ф. Овсянников писал: «Самостоятельна ли сосудодвигательная система и где ее центр? Людвиг и Тири перерезывали продолговатый мозг в нижнем конце его и получали следующее: после перерезки сосуды расширялись, раздражение периферического его отрезка вызывало сужение; значит центр сосудодвигательной системы лежит выше. Исследования профессора Овсянникова доказали, что центр этот находится в продолговатом мозгу позади четыреххолмия и занимает пространство 3-4 мм. Так как, вследствие большого количества анастомозов, кровотечение в мозгу при перерезках очень сильно, что в высшей степени затрудняет исследования, то были приняты следующие меры: одна сонная артерия зажата, а другая соединена с кимографом. Для питания мозга оставались обе позвоночные артерии. Выпилка костей производилась трепаном (пила, нарезанная по краю цилиндрической трубки) так что они вынимались кусочками; самый разрез мозга вёлся тупым орудием, чтобы не поранить веточки артерии. Когда нож наталкивался на чувствительный нерв, то давление крови повышалось и через некоторое время приходило к норме; когда же разрез пришелся на 4 мм ниже четыреххолмия, то давление понизилось очень сильно, и после этого, раздражение какого бы то ни было чувствительного нерва не могло уже вызвать сужение сосудов» (текст восстановлен по рукописи «Овсянников Ф. Анатомия и физиология, 1880–1881 г., с. 194»).
Зависимость тонуса сосудов от состояния определённых отделов ствола мозга подтвердилась экспериментами, выявившими выраженное влияние на артериальное давление электрической и химической стимуляции нервных элементов внутри продолговатого мозга. Имели место эффекты как повышения, так и снижения величины давления. Всё же повторяющейся анатомической локализации прессорных и депрессорных зон установить не удалось. Возможная причина – эти области как в рострокаудальном, так и в дорсовентральном направлении локализованы диффузно и перекрывают друг друга. Коагуляция значительных объёмов продолговатого мозга и моста не вызывала значимого падения давления. Тогда как разрушение небольшого участка вентролатеральной поверхности продолговатого мозга вызывало падение давления, близкое по величине с его снижением при высокой перерезке. Сейчас считается, что вазомоторный центр простирается от каудальной части латерального ретикулярного ядра до верхней оливы. Подробное описание современных представлений можно найти в работе В. А. Цирлина [26].
Вернёмся к рис. 1. На нём дано упрощённое схематическое изображение бульбарного центра. Сосудистого по одним представлениям, сердечно-сосудистого по другим. Импульсация поступает на обе функционально-топографические области вазомоторного центра. Область ВК/КА называют «вазоконстрикторно-кардиоакселераторной», ВД/КИ – «вазодилататорно-кардиоингибиторной». Таким образом, в классической интерпретации выделяют область, которая ответственна за констрикцию сосудов, и она же - за активацию сердца. Считается, что рядом лежит область, ответственная за вазодилатацию и за снижение функции сердца. Как для сосудов, так и для сердца эти влияния противоположны. Сами области также находятся в реципрокных отношениях, т.е. взаимосвязаны так, что возбуждение одной подавляет активность другой и наоборот (сейчас считается, что вместе с тем они могут работать и однонаправлено). В результате получается двойное противоположное влияние на исполнительные органы. Как уже сказано, это влияние различно для сердца и сосудов. Сигналы, поступающие из «констрикторно-акселераторной» области, через симпатические нервные стволы активируют сердце и сосуды (посредством адреналина, норадреналина и дофамина), а из «ингибиторной», как через симпатические, так и парасимпатические, - оказывают тормозное действие (в основном, посредством ацетилхолина). Наряду с влиянием на давление, СВ, ОЦК, жизненно важной является нервная регуляция перфузии почек, печени, селезёнки и мозга, а также перераспределения кровоснабжения в соответствии с вегетативными и поведенческими нагрузками на организм.
Кроме непосредственного прямого влияния бульбарного центра на сердце и сосуды рассматривается другой путь – нейроэндокринный (подробно изложен в монографии Смирнова А.Н.[27]). Симпатический отдел вегетативной нервной системы влияет на уровень АД через медиаторы: адреналин и норадреналин. Основная их часть вырабатывается надпочечниками. Выброс медиаторов в кровь сопровождается учащением сердцебиений (вероятно, имеют место не только хронотропный, но и ино-, батмо-, дромотропные эффекты) и спазмом сосудов. Эмоциональные, психические и физические нагрузки способствуют активации прессорных систем и, вследствие этого, повышению АД. В ответ могут активироваться депрессорные системы, обуславливающие снижение АД. Это, в первую очередь, парасимпатическое влияние вегетативной нервной системы. Оно реализуется посредством ацетилхолина, который замедляет пульс и расширяет периферические сосуды, если его действие не блокируется симпатическими медиаторами.
Во второй части статьи мы перейдём к математическому описанию представляемой концепции. Но здесь мы должны изложить критику многими современными исследователями классической концепции бульбарного центра, или, более правильно будет сказать, попытки развития представлений о регуляции сердечно-сосудистой системы. До этого совсем кратко коснёмся представлений о «центральной команде». Это интереснейшая проблема, но она весьма далека от лечения больных в операционных или в БИТ-ах, которые находятся в лежачем положении или, тем более, под наркозом. В то же время гипотеза о «центральной команде» с более широких позиций освещает проблему взаимодействия коры мозга и сосудистой системы.
Представления о «центральной команде» (feedforward). Когда животное или человек реализует целенаправленное, детерминированное волей действие, то автономные системы, в том числе сердечно-сосудистая, обеспечивают его соответствующими ресурсами, иногда даже опережая потребности. Как задание соматическим функциям передаётся на вегетативный уровень? Ещё в конце позапрошлого века эту проблему поставили Geppert (1886) и Johansson (1895). Её сложность очевидна. Чрезвычайно многообразное поведение человека должно быть обеспечено и согласовано со столь же разнообразными реакциями автономных систем, как правило, нарушая их гомеостазис. В этот процесс всё время вовлекаются процессы регуляции: от коры мозга до спинальных рефлексов, от гипоталамуса до желез, от системы крови до систем саморегуляции. Эти возникающие в коре и лавинообразно спускающиеся к сердечно-сосудистой системе сигналы разной природы, но подчинённые одному целесообразному результату получили название «центральной команды» (feedforward). Это название ввёл Goodwin в 1972 году.
Считается, что представления о центральной команде хорошо изучены и обоснованы. Они относятся к классике физиологии. На рис. 2 представлена схема, отражающая регуляцию автономных систем в объёме, необходимом для понимания «центральной команды», в интерпретации Alexander с соавторами (2007) ; адаптация схемы Wyss et al. (2004).
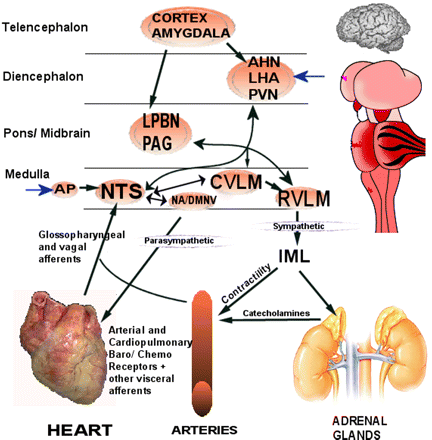
Рис. 2. Нервный контроль сердечно-сосудистой системы в объёме, необходимом для понимания «центральной команды», по Alexander с соавторами (2007); адаптация схемы Wyss et al. (2004) [19].
В последние годы вновь возникла дискуссия об определении и свойствах понятия «центральная команда» (см. следующий раздел). Сразу отметим, что эта дискуссия не касалась основного вопроса: как удаётся подстроить функции автономных систем (кровообращения, дыхания, теплообмена, выделения и т.п.) к мало предсказуемому целостному поведению организма. Обеспечить фантастически тонко согласованный результат взаимодействия мышечных систем в непрерывной взаимосвязи с сенсорными, вербальными, интеллектуальными и эмоциональными процессами. Многокомпонентными и многоплановыми.
Развитие классических представлений. За последние 50 лет высказаны многочисленные критические замечания и предприняты усилия по развитию представлений о регуляции сердечно-сосудистой системы.
Сердечно-сосудистый центр. Спинальные структуры предложено в соответствии с последними экспериментальными данными рассматривать не как передающие каналы, а как предбульбарные центры контроля сердечно-сосудистой системы.

Рис. 3. Схематическое представление гипотезы Пейса в интерпретации Н.М. Амосова (1977). Знак + и сплошные линии означают возбуждающие влияния. Знак – и пунктирные линии означают тормозные влияния.
Появились утверждения и веские факты участия в регуляции артериального давления переднего гипоталамуса и даже прямого влияния коры мозга на функции спинальных структур. В развитие этих данных получила распространение рабочая гипотеза, суть которой: вазомоторный центр - одна из рядовых супрамедуллярных структур. Эти воззрения наиболее полно воплощены в гипотезе Пейса, что хорошо видно из схемы, отражающей его представления (рис. 3, по Н.М. Амосову) [7].
Система регуляции рассматривается здесь как единый интегративный механизм, состоящий из четырёх равноправных частей: 1 - кожные и висцеральные афференты, а также прессо- и хеморецепторы; 2 - центральная связующая система (ЦНС); 3 - эфферентные выходы из ЦНС к спинному мозгу; 4. спиной мозг с выходом к сердцу и сосудам.
На основе этих представлений жёсткой критике подвергается сама идея автономности сердечно-сосудистого центра. Приводятся аргументы неотделимости регуляции процессов кровообращения от дыхания, метаболизма, других сопряжённых вегетативных и соматических систем (как, например, это имеет место в «центральной команде», см. далее). Эта точка зрения опирается на результаты исследований по раздражению структур лимбико-диэнцефалического уровня, показавшие, что сердечно-сосудистые реакции неразрывно связаны с сомато-висцеральными поведенческими приспособлениями организма.
Часть исследователей категорически отказываются от «длительно существовавшего представления о бульбарном вазомоторном центре». В то же время другие выполняют тщательные исследования его связей и структуры. Такие противоречивые мнения можно встретить в научно-клинических сборниках, где излагаются оба подхода и не обсуждается их разноречивая аргументация, высказываемая критиками классических представлений в особенно категорической форме. Действительно, показано, что после перерезки спинного мозга он по истечении определённого времени может восстанавливать рефлекторную деятельность. И супрабульбарные уровни, как уже отмечалось, способны модулировать функцию нижележащих уровней, притом даже независимо от стволовых структур.
Однако, кажется нелогичным, что для доказательства того, что бульбарный сердечно-сосудистый центр не существует, изучают не его роль в регуляции сердечно-сосудистой системы, а стараются выявить хоть какие-нибудь проявления других структур - спинальных и супрабульбарных - в изменении регуляции сердечно-сосудистой системы. Как будто их (других центров) участие в регуляции сердца и сосудов исключает возможность существования центра, ответственного за интеграцию основных (или достаточно многих) рефлекторных связей регуляции и функции кровообращения.
Ещё более странно, что основная суть любого центра регуляции - то, как он перерабатывает поступающую в него информацию в сигналы управления (алгоритм управления), совсем не рассматривается в большинстве исследований. Как будто словом «интегративная функция» (которым объясняется, что делает центр) всё сказано. И даже задача такая (как перерабатывается информация в центре или во многих центрах), как правило, не ставится. Ведь смысл не в том, что после перерезки давление падает, а рефлексы прекращаются (или возвращаются со временем; хотя это тоже важно и нельзя не отдать должное искусству поставленных здесь опытов). Смысл, на наш взгляд, в том, что опыты Ф.В. Овсянникова, вслед за ним Диттмара, Wang, Alexander и многих других показали, что имеются структуры, лежащие в стволе мозга, от которых существенно зависят функция и регуляция кровообращения (сердца и сосудов). Настолько существенно и многообразно, что их (эти структуры) вполне можно назвать центром регуляции (хотя дело, конечно, не в названии). И эта суть однозначно следует из исследований Ф.В. Овсянникова.
Всё же нужно подчеркнуть, что и сегодня в разрешении проблемы, каков алгоритм переработки афферентной информации в эфферентную, особых достижений не наблюдается. Для физиологии решение именно этой задачи определит, как формируется, изменяется и нарушается регуляция функции сердечно-сосудистой системы. И как можно бороться с этими нарушениями.
Вместе с тем важно подчеркнуть, что простые описания (несмотря на веру – «в природе всё просто») пока не помогли в понимании этих процессов. Сейчас признаётся: нервно-гормональные механизмы, регулирующие работу сердца и сосудов, имеют сложную саморегуляторную и иерархическую структуру. Г.И. Косицкий считал, что первый уровень этой иерархии расположен внутрисердечно, образован интрамуральными ганглиями и относящимися к ним нейронами. Этот уровень формирует внутрисердечные периферические рефлекторные механизмы. С нашей позиции формирования концепции регуляции сердечно сосудистой системы необходимо в качестве первого уровня признать саморегуляцию сердца, реализуемую для всех полостей законом Эрнста Старлинга. При этом должны быть учтены исправления и дополнения, сделанные Зонненбликом и Амосовым (Н.М. Амосов и др., 1971) [10], а также Капелько [30]. Эта система саморегуляции, включая обратную связь, регуляцию по возмущению, форсаж и интегрально-пропорциональный закон преобразования ошибки регулирования и линеаризацию сложного непрерывно-импульсного алгоритма функционирования, подробно описана в работе Лищука (В.А. Лищук, «Алгоритм функционирования левого желудочка сердца», 1967) [11, 12]. Саморегуляция, вероятно, является первым уровнем в иерархии всех функциональных систем живых организмов. Не нервная или гормональная регуляция, а биофизическая или даже молекулярная саморегуляция.
Вторым уровнем иерархии Г.И. Косицкий выделяет «этаж», который образуют нервные структуры, замыкающиеся на уровне экстраорганных периферических ганглиев вегетативной нервной системы. Низшие вегетативные центры спинного и продолговатого мозга выделяются как третий уровень (четвёртый, если учитывать саморегуляцию отдельных полостей сердца и сосудистых регионов). Кроме того, он выделяет нейроны межуточного мозга как четвёртую ступень, а нейроны коры больших полушарий головного мозга как пятый уровень нервных механизмов, регулирующих работу сердца. При этом он считает, что
внутрисердечная нервная система интегрирует функцию камер самого сердца (замечание авторов: скорее, учитывая нашу т.з. на саморегуляцию сердца, согласует системы саморегуляции его мышечных полостей),
спинальные центры совместно с бульбарным «регулируют не только сердце, но и движение крови во всех отделах сердечно-сосудистой системы» (замечание авторов: в нормальных режимах, может быть, более точно будет сказать - согласует, а не регулирует совместную функцию сердца и сосудов, к чему мы ещё вернёмся в дальнейшем изложении; хотя согласование можно, если строго не придерживаться теории управления, рассматривать как вид регуляции),
центры гипоталамуса обеспечивают приспособительные реакции сердечно-сосудистой системы при изменении вегетативного статуса, эмоциональных напряжениях и адаптации,
кора больших полушарий головного мозга обеспечивает изменения функций сердечно-сосудистой системы при поведенческих реакциях и целенаправленной деятельности.
Другой, активно развиваемой темой является дискуссия о «главной и выходной переменной сердечно-сосудистой системы». Часть авторов относят к ней сердечный выброс, другие – артериальное давление. Постулируется также главенство эндокринной системы (норадреналин, альдостерон и др. гормоны) и ЦНС (нервная импульсация, медиаторы), а также способность каждой из них генерировать управляющие сигналы и подчиняться влияниям другой. Остаётся без определения само понятие главенства той или другой функции, как и регуляторных факторов, молекул, клеток, электрических импульсов, участвующих в детерминации процессов регуляции. Эта неопределённость осложняет изучение и обсуждение механизмов перестройки регуляции бульбарного центра, в том числе под влиянием супрамедуллярных структур.
Многолетняя дискуссия о «главной переменной», о «главенстве» одних систем регуляции над другими представляется нам бессодержательной, даже вредной. О неопределённости этих понятий мы уже сказали. В организме человека та, либо другая функция становится ведущей в зависимости от его состояния, поведения, решаемых задач, заболевания. Для лечащего врача выбор контролируемых показателей и опорных нормативов зависит от заболевания, сопутствующих осложнений, общего состояния организма [24]. Очевидно, что различные показатели функции будут определять регуляцию сердечно-сосудистой системы больного в БИТ-е (СИ, АД [13]) и испытуемого на центрифуге (V – перераспределение объёмов) [13,14].
За последние десятилетия превалирующее развитие получили исследования нецентральных (можно сказать, молекулярных) механизмов регуляции сердечно-сосудистой системы. Многие биологически активные вещества, попадая с кровью к органам-мишеням, оказывают влияние на сердце и сосуды. В соответствии с представлениями В.А. Ткачука (2008) можно говорить об отдельных молекулах: «Функцией системы рецепции и внутриклеточной сигнализации является согласование всех процессов жизнедеятельности по скорости, времени и месту протекания». Некоторые из них могут быть исполнительными органами систем регуляции (Пальцев М.А., 2006 [29]). Так, например, общеизвестно, что в результате влияния катехоламинов и ренина запускается прессорный механизм, приводящий к образованию ангиотензина-2. Последний обладает выраженным сосудосуживающим эффектом, который может повышать общее периферическое сопротивление. Совместно ренин и ангиотензин-2 стимулируют синтез надпочечниками альдостерона. Альдостерон регулирует реабсорбцию натрия в почечных канальцах и повышает проницаемость клеточных мембран, что способствует проникновению кальция и натрия внутрь клеток из внеклеточного пространства. В противовес этому механизму, клетки мозгового слоя почек синтезируют кинины и простогландины, обладающие сосудорасширяющим эффектом, снижающим периферическое сопротивление. Подробно исследована не только роль почек, но и многих других органов и механизмов, влияющих на функцию и регуляцию кровообращения. Детально исследованы взаимовлияния структур мозга, их влияние на регуляцию сердца, артерий, вен, артериол, венул, капилляров и, с другой стороны, на гипофиз и др. железы, изучена регуляция коронарной системы, механизмы возбуждения миокарда, роль в регуляции интимы сосудов и их мышц, взаимовлияние нервной и эндокринной систем, роль рилизинг-факторов, тропных гормонов, статинов, АКТГ и т.п. Эти исследования свидетельствует о том, что нейроны, как и иные клетки, контролируются гуморальными (эндокринными) системами регуляции. В свою очередь нервная регуляция определяет состояние автономных систем, эндокринных органов, гуморальные среды и т.п. Таким образом, как правило, функциональные системы воспринимают управляющие воздействия и сами генерируют управляющие сигналы, т.е. являются управляемыми и управляющими. Часто из этих фактов делают вывод: « поэтому нельзя рассматривать каждую из систем в отдельности».
Действительно, множество систем регуляции сердечно-сосудистой системы имеют как прямые (управляющие), так и обратные (информационные) связи, как синергические, так и конкурентные отношения. Можно ли при такой сложности составить целостную концепцию регуляции сердечно-сосудистой системы, тем более построить модель? Мы вполне сознаём всю сложность микрокосма нашего организма и неадекватность современных знаний для его постижения. Примерно так, как если бы мы попытались описать каждую молекулу газов вместо обобщений термодинамики. Из этого опыта нужно сделать вывод: нельзя описать всё, нужно найти решение, адекватное уровню знаний и задачам практики. Сейчас имеют место детальные и глубокие экспериментальные исследования регуляции сердечно-сосудистой системы. В нашей стране много сделано работами В..М. Хаютина (например, [32]), Б.И. Ткаченко ([31]), К.В. Судакова ([17]) и многими другим физиологами, экспериментаторами и клиницистами. Известны попытки построить как общие, так и органно- и предметно-ориентированные концепции регуляции сердечно-сосудистой системы; например, [7, 13, 32, 17] и [14, 15, 31]. Какие есть возможности? Начнём с того, что в зависимости от состояния организма, целей и желаемых результатов некоторая часть связей, очевидно, не оказывает заметного влияния на другие системы и при их описании эти связи можно не учитывать. Чувствительность многих систем к воздействию других может быть пренебрежимо мала. С другой стороны, при рассмотрении очень больших интервалов времени взаимовлияние этих систем может стать значимым. Процессы, протекающие за доли секунды, могут определять функцию сердца. Для лёгких это уже секунды. Кровообращение в целом требует учесть минуты, и долями секунд и секундами можно, как правило, пренебречь. Если же мы захотим учесть все связи и процессы, то не сможем решить ни одной практической задачи. Поэтому как аналитический (выделение центра) так и синтетический (учёт целостности) подходы и методы вполне конструктивны и имеют право на жизнь. Утверждения о невозможности рассмотрения отдельных систем организма в стремлении к идеалу, может быть, не лишены оснований, но в практике и в ориентированной на практику теории они не конструктивны. Их несомненная польза – расширение горизонта и нашего мыслительного мира, его упорядочивание и очищение от гипотез, не оправдавших себя.
Многими исследованиями показано, что в ходе передачи управляющего сигнала он может усиливаться многократно, активизировать сигналы другой специфики и направленности и даже менять цели регуляции (так целенаправленная регуляция превращается в шок). Как усиление (ослабление), так и распространение активации на другие системы (и какие именно) зависят от состояния организма и его отдельных подсистем. В ходе этой лавинообразной передачи регулирующих сигналов и биовеществ некоторые из них оказывают общее организменное воздействие, другие – выборочное, специфическое и, наконец, третьи (особенно передающиеся нервами) – локальное, строго локализованное проявление. По крайней мере, некоторые функциональные системы могут решать определённые задачи, управляя своей функцией (или функциями) так, чтобы обеспечить эффективное качественное функционирование, достижение конечного полезного результата. В определённых ситуациях, по крайней мере, некоторые (большинство) функциональных систем могут подчиняться, изменять свои критерии управления в соответствии с общеорганизменными задачами, участвовать в достижении результата, полезного для всего организма, возможно, даже в ущерб своим локальным целям и критериям. Чёткое определение полезного результата (или критерия) и механизма его достижения крайне важно для понимания роли регуляторных процессов, причин расстройств и для выбора лечения нарушений кровообращения. Впервые этот акцент в физиологии был поставлен и развит П.К. Анохиным в общей теории функциональных систем [16]. Мы ещё вернёмся к его исследованию с этих позиций регуляции артериального давления. Сейчас же закончим этот раздел представлением схемы «поддержания оптимального для метаболизма артериального давления», разработанной К.В. Судаковым с позиций теории функциональных систем (рис. 4). Эта схема детальная (вместе с описанием) и общая, охватывала, на время её публикации, содержание большинства концепций и представлений, отобранных по критерию целесообразного полезного результата [17].
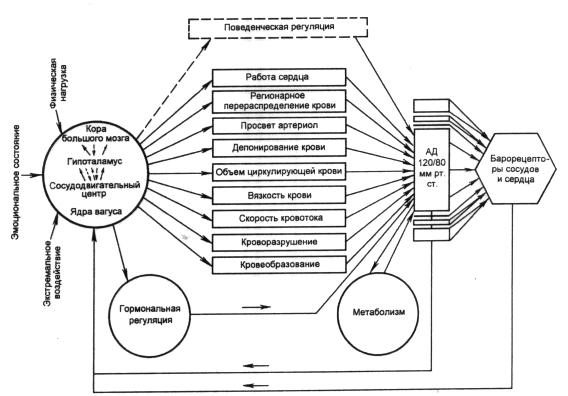
Рис.4. Функциональная схема, поддерживающая оптимальное для метаболизма артериальное давление (по К.В. Судакову).
Новые идеи о свойствах Feedforward. Ряд исследований показали, что активация «центральной моторной команды» не обязательно предполагает детерминацию и параллельное вовлечение в процесс «центральной сердечно-сосудистой команды». Последняя может развиваться независимо и даже опережать первую. Частично эти выводы следуют из исследований, например, Williamson (1999 - 2002), Nowak (1999 – 2005) и др.
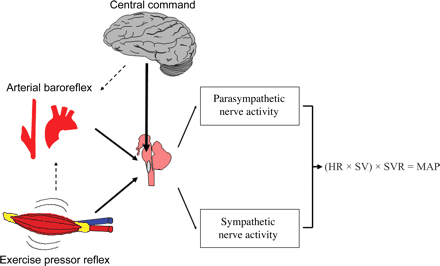
Рис. 5 показывает как эти отношения (mechanisms of neural cardiovascular control during exercise) видит Williamson (2006). Здесь HR – ЧСС, SV – ударный объем, SVR – общее периферическое системное сопротивление, MAP – среднее артериальное давление [18].
Williamson считает, что feedforward, как правило, работает без непрерывной отрицательной обратной связи. Эта характеристика основывается на ответе сердечно-сосудистой системы на само начало, даже только на ожидание посылки центростремительных сигналов к скелетной мускулатуре. Совпадение с началом и тем более опережение заставляет признать, что для формирования обратной связи нет достаточного времени. Нет, поскольку сигналам нужно пройти от периферийных мышечных образований к сердечно-сосудистым центрам в стволе мозга. Однако Williamson вместе с тем считает, что есть многочисленные свидетельства того, что эффекты центральной сердечно-сосудистой команды кореллируют с интенсивностью мышечного усилия. Таким образом, имеются данные за то, что центростремительная обратная связь от мышечной системы к сердечно-сосудистому центру не имеет места, как и за то, что она всё же может в каких-то ситуациях иметь место.
Ключевой пункт состоит в том, что увеличение интенсивности сокращения мышц или силы их сокращения ведёт к активации центростремительной обратной связи и вместе с тем само предвидение или восприятие предстоящего усилия, причём даже без изменений в мышцах может вызывать адекватные сердечно-сосудистые реакции. Таким образом, предвидение усилия и его значимости, вероятно, предопределяет генез «центральный сердечно-сосудистой команды».
Обобщение. Будем считать, что функционально связанные автономные системы (сердце, кровь, лёгкие, почки, мышцы и т.п.)
- имеют собственные системы регуляции (миогенные, биофизические и т.п.),
- взаимодействуют непосредственно через функции и
- через нейрогуморальные центры регуляции,
- совокупность нейрогуморальных центров многофункциональна и имеет иерархическую соподчинённость.
Многосвязная саморегуляция функциональных систем обеспечивает их автономность, а согласование их функций нейроэндокринными центрами порождает целостность и является следствием целостности организма. Из этих положений мы исходили при разработке концепции регуляции сердечно–сосудистой системы.
Математические модели сердечно-сосудистой регуляции. Большинство авторов публикаций с описанием сердечно-сосудистого центра излагают свои взгляды на регуляцию кровообращения, используя вербальные средства. Что касается не вербальных, а математических интерпретаций, то они включают простые одно- и двухконтурные регуляторы АД и/или МОК. Сама регуляция представлена в них традиционно в рамках теории автоматического регулирования (например, [7,11,12,20,21]).
y(t)=yб+к1*е(t)+к2*еd +к3*е`(t).
Здесь у – управление, е – ошибка регулирования, к - коэффициенты, б – символ базового значения.
Различия между системами регуляции первого уровня (саморегуляции), спинальной регуляции и бульбарной часто не отражаются. Первый уровень как бы распространён до бульбарного и выше (рис. 6).
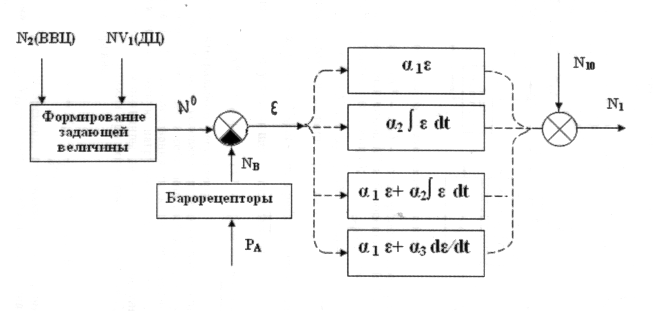
Рис. 6. Блок-схема сосудодвигательного центра по Н.М. Амосову. ВВЦ – высшие вегетативные центры, РА – артериальное давление, – ошибка регулирования), – коэффициенты, NV1 – влияние дыхательного центра (ДЦ), N1 выход, N2 – влияние высших вегетативных центров гипоталамуса (ВВЦ), N10 – базальная активность, NВ – барорецепция, N0 – «заданная величина».
Получили также распространение несколько развитых математических моделей, в которых системы регуляции кровообращения представлены подробно. Однако этим описаниям для оценки параметров не хватает, что естественно, экспериментальных данных и обоснованных наблюдений. Это особенно сказывается на центральных уровнях переработки информации.
Во всех моделях объектами регуляции принимаются сердце и сосуды. Почти всегда - без разделения на левое и правое сердце (предсердия и желудочки). В моделях, где такое разделение сделано, где отдельно моделируются правый и левый желудочки, и/или предсердие и желудочек, а также клапаны и коронарный кровоток, центральная регуляция не рассматривается, в лучшем случае описывается одна из составляющих функции сердца (ЧСС, как правило). Сосудистые локусы и резервуары, как и отдельные крупные сосуды, выделяются без обоснований. Это делается в соответствии с научными интересами авторов или спецификой задачи применения модели, что естественно для первоначального этапа моделирования. В то же время, не вредно вспомнить, что модели периода становления математической физиологии в шестидесятые годы прошлого века иногда состояли из 500 и даже больше сосудистых резервуаров (компартментов). Однако специфика сосудистого древа отражалась слабо. Это было скорее механическое подразделение сосудистого русла, чем его адекватное описание. Регуляция, соответственно, также носила скорее иллюстративный, чем конструктивный характер. При желании сохранить конструктивность модели (возможность имитации и интерпретации результатов) в модель включали ограниченное число сосудистых резервуаров. Почти всегда – аорту, артериальный сосудистый резервуар плечеголовной части и нижней части туловища, а также их капиллярные ложа, реже выделялись сосуды брюшной полости, печени, почек, кожи, мышц. Почти всегда отображался лёгочный круг – лёгочная артерия, капилляры лёгких, шунты и легочные вены. При ориентации модели на сердце включали коронарные сосуды. В тех моделях, где по преимуществу исследуется кровоснабжение мозга, выделяется краниальная сосудистая система.
Тогда и сейчас в качестве регулируемых функций принимают артериальное давление, ЧСС и/или кровоток (объёмы сосудистых резервуаров не рассматриваются). Отметим также, что, какие именно функции и параметры являются управляемыми (сократимость левого желудочка, правого сердца, тонус, ёмкость или резистивность сосудов и т.п.), часто не уточняется. Оценки и локализация артериального давления (среднее, диастолическое, мгновенное; в дуге аорте, в синокаротидных зонах и т.п.) и кровотока (СВ, МОК, УО правого желудочка, левого и т.п.) также не уточняются. Отчасти поэтому в качестве источников обратной афферентации (связи) принимается импульсация от баро- и хеморецепторов (влияние гормонов и водно-солевого состояния в большинстве исследований предполагается по умолчанию). Связь нервной импульсации и гормонального статуса с параметрами кардио- и гемодинамики трактуется по-разному, нередко упускается. Кроме рецепции непосредственно от сердца и сосудов имеет, по мнению некоторых исследователей, место афферентная импульсация от других органов и тканей (в большинстве случаев опосредованная), а также рецепция непосредственно окружающей нейроны среды.
Во второй половине прошлого века получили распространение модели Гродинза (1963 - 1967), Сагавы (1967, 1973), Н.М. Амосова (1962-1980), А. С. Гайтона (1964-1982), В.А. Лищука (1962 - 2008), (подробный список литературы дан в монографии Н.М. Амосова с соавторами «Теоретические исследования физиологических систем» [7]). В последние годы опубликованы близкие к ним модели с сосредоточенными параметрами, например, Heldt et al. (2001 - 2006) [14]. Практическая направленность следует из самого названия - «Вычислительные модели сердечно-сосудистой функции для анализа послеполетной ортостатической нетолерантности». В модели отражены сердце, артериолы, вены, синоатриальный узел (всего 13 компартментов) и свойства: ЧСС, сократимость, сопротивление, тонус, а также процессы регуляции: артериальный барорефлекс, сердечно-лёгочный рефлекс и индивидуальные механизмы регуляции (рис. 7).
Нам близок этот подход, так как индивидуализация моделей в ходе терапии - основное направление наших исследований и применения моделей в клинике в течение 40 последних лет (рис.8) [15, 22 - 25].
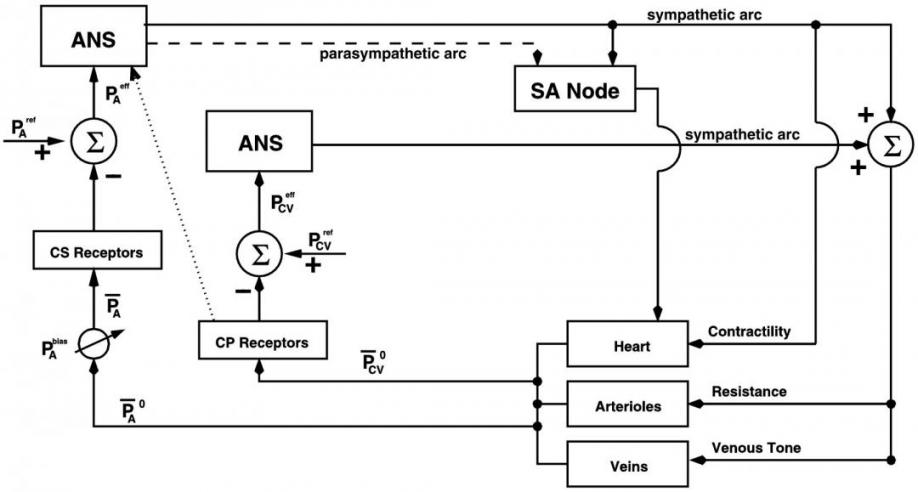

Рис. 7. Схема рефлексов модели Heldt T. et al. (2001). SA Node - синоатриальный узел. ANS – автономная нервная система [14].

Рис. 8. Автоматизированная система обеспечения решений врача ИССХ им. А.Н. Бакулева АМН (1975 - 2008). Дана структура с иллюстрацией содержания подсистем. В нижнем правом углу структура модели кровообращения, включая регуляцию (подробнее см. Л.А. Бокерия и др., 2007 [4] ), внизу в центре – математическое описание сердечно-сосудистой системы (В.А. Лищук, 1971 - 1991 [13]). Здесь: ССЦ – сердечно-сосудистый центр, СС – система саморегуляции, ВВЦ - высшие вегетативные центры, МКК – малый круг кровообращения, БКК – большой круг кровообращения, ЛП и ЛЖ – левое предсердие и левый желудочек, ПП и ПЖ - правое предсердие и правый желудочек, А – артериальный резервуар, АГ и АТ – артерии головы и, соответственно, туловища, ВГ и ВТ - вены головы и туловища, ТГ и ТТ – капилляры тканей головы и туловища, ЛА – лёгочная артерия, ЛВ – лёгочные вены, ЛК – капилляры лёгких.
В заключение этого раздела мы хотим обратить особое внимание на отсутствие в разработке моделей сердечно-сосудистой системы ориентации на диагностические и клинические задачи, на патологию как важнейшее возмущение, имеющее особо значимое практическое значение.
Клинические данные (преобладающие по объёму, нередко и по качеству перекрывающие другие наблюдения и исследования) используются редко. Это положение, т.е. отсутствие повторяющихся экспериментальных данных и слабое использование клинических, делает математические интерпретации мало отличимыми от вербальных. Они имеют скорее характер описания полуформальными средствами суммы знаний рассматриваемой области, чем гармоническое сочетание адекватности и конструктивности, присущее математическим методам. Но и этот аспект (обобщение суммы знаний формальными средствами) не даёт более ясного понимания функции и регуляции сердечно-сосудистой системы, если практическая направленность на задачи медицины, спорта и т.п. отсутствует.
В начале этого столетия вновь (после активного обсуждения в середине прошлого столетия) появились статьи, в которых некоторые авторы открывают для себя метод моделирования. В них развиваются темы «Полезности моделирования для анестезии и ИТ», «What is modeling?», «What does modeling have to offer the researcher?», «What new skills are required of researchers?» и т.п. К сожалению, опыт, полученный с помощью моделей в прошлом столетии, авторы последних разработок не учитывают (например, модели и их применения в клинике и физиологии В.И. Бураковским (1970-1990), Кирклиным (1970-1980) и др.; см. подробный список литературы к монографии Лищука «Математическая теория кровообращения» [13]).
Во второй части статьи дано вербальное и математическое описание концепции регуляции сердечно-сосудистой системы. Приведены тренды поведения модели в нормальных условиях при покоящемся состоянии организма человека. В третьей части работы выполнены имитации патофизиологических процессов и получены реакции сердечно-сосудистой системы на некоторые виды терапии в кардиохирургической клинике.
Литература.
- Бокерия Л.А. Клиническая физиология кровообращения // Клиническая физиология кровообращения. № 1. – 2004 г. – М.: Издательство НЦССХ им. А.Н. Бакулева РАМН. – С. 1 – 4.
- Диагностика и лечение острой сердечной недостаточности. Российские рекомендации. Разработаны комитетом экспертов Всероссийского научного общества кардиологов. Секция неотложной кардиологии. - М. – 2006. (www.cardiosite.ru).
- Саркисов Д.С. Пальцев М.А., Хитров Н.К. «Общая патология человека» (учебник), М., Медицина, 1995, с.115.
- Бокерия Л.А., Лищук В.А., Газизова Д.Ш., Горбач А.А., Сазыкина Л.В., Сокольская Н.О. Математическая модель регуляции сердечно-сосудистой системы, ориентированная на интенсивную терапию в кардиохирургии // Клиническая физиология кровообращения. № 3. – 2007 г. – М.: Издательство НЦССХ им. А.Н. Бакулева РАМН. – С. 5 – 18.
- Лищук В.А. Исследование гомеостазиса артериального давления на математической модели, идентифицированной с данными больных ИБС// Клиническая физиология кровообращения. № 1. – 2008. – М.: Издательство НЦССХ им. А.Н. Бакулева РАМН. – С. 24 – 54.
- Folkow B., Neil E, Circulation. New Yorc – London – Toronto, Oxford University Press, 1981/ 563 p.
- Амосов Н. М. и др. Теоретические исследования физиологических систем. К.: «Наук. Думка», 1977. 246 с.
- Физиология человека: Учебник/ Под ред. В.М. Покровского, Г.Ф. Коротько – М.: Медицина, 2003. – 656 с. (С. 322).
- Овсянников Ф. В. Избранные произведения. – М.: Изд. мед. литер. - 1955. – 400 с.
- Амосов Н.М., Лищук В.А., Пацкина С.А., Палец Б.Л., Лиссов И.Л. Саморегуляция сердца. – Киев: Наукова думка, 1971. – 157 с.
- Лищук В. А. Построение алгоритма функционирования сердца // Автоматика. — 1967. — №3. — С. 60—76.
- Listschuk W.A., Die Selbstreguliering des Herzens. // Der Mensch als Regler.-Berlin. VEB Verlag Technik Berlin 1970, p.43-68.
- Лищук В.А. Математическая теория кровообращения. – М.: Медицина, 1991. – 256 с.
- Heldt T., Shim E.B., Kamm R.D., Mark R.G. Computational models of cardiovascular function for analysis of post-flight orthostatic intolerance / Lecture. – Massachusetts Institute of Technology. – 2006.
- Лищук В.А. Бокерия Л.А., Математические модели и методы в интенсивной терапии: сорокалетний опыт. К 50-летию НЦССХ им. А.Н. Бакулева. Части 1-4. // Клиническая физиология кровообращения. – 2006–2007.
- П.К. Анохин, Принципиальные вопросы общей теории функциональных систем», М. АН СССР, 1971. – 298 с.
- Физиология. Курс лекций/Под ред. К.В. Судакова. – М.: Медицина, 2000. – 784 с. (страница 355).
- J. W. Williamson, P. J Fadel and J. H Mitchell New insights into central cardiovascular control during exercise in humans: a central command update Experimental Physiology 91.1 pp 51-58 DOI: 10.1113/expphysiol.2005.032037 © The Physiological Society 2006.
- Alexander L. Green and David J. Paterson Identification of neurocircuitry controlling cardiovascular function in humans using functional neurosurgery: implications for exercise control. Experimental Physiology 93.9 pp 1022-1028.
- Лищук В.А. Формализация системы стабилизации артериального давления. //ДАН СССР, 1972, т. 207, №6, с. 1497-1500.
- Лищук В.А. Формализация принципа перераспределения кровотока.// ДАН СССР, 1973, т. 210, № 3, с. 741-744.
- Лищук В.А. Опыт применения математических моделей в лечении больных после операций на сердце // Вестн. АМН СССР. – 1978. - №11. – С. 33-49.
- Лищук В.А. Специфика применения математических моделей в лечении больных после операции на сердце// В кн.: Применение математических моделей в клинике сердечно-сосудистой хирургии. М.: Машиностроение. – 1980. – С.155-170.
- Бураковский В.И., Бокерия Л.А., Газизова Д.Ш., Лищук В.А., Люде М.Н., Работников В.С., Соколов М. В., Цховребов С.В. Компьютерная технология интенсивного лечения: контроль, анализ, диагностика, лечение, обучение. – М., 1995. – 85 с.
- Бокерия Л.А., Лищук В.А., Спиридонов А.А. и др. Влияние пережатия аорты на гемодинамику при реконструкции грудной и брюшной аорты // Ангиология и сосудистая хирургия. – 2004. – том 10. - № 1. – С. 125-135.
- Цырлин В.А. Бульбарный вазомоторный центр – морфофункциональная и нейрохимическая организация //Артериальная гипертензия. - 2003.- том 9.- № 3. - 77–81 c.).
- Смирнов А.Н. Элементы эндокринной регуляции. Под.ред В.А.Ткачука. – М.: ГЭОТАР-Медиа. – 2008. – 352 с.
- Peiss C.N. Concepts of cardiovascular regulation: past, present and future // In.: Nervous control of the heart. – 1965/ P. 154-197.
- Пальцев М.А., Квитной И. Руководство по нейроиммуноэндокринологии. – М.: Медицина. – 2006. - …
- Капелько В.И. Биофизика кровообращения. – М., 2007. – 72 с.
- Ткаченко Б.И., Кульчицкий В.А., Вишневский А.А. Центральная регуляция органной гемодинамики. – Спб.: Наука. – 1992. – 242 с.
- Хаютин В.М. Основные принципы организации системы управления кровообращением. – В кн.: Болезни сердца и сосудов. Под ред. Е.И.Чазова. – 1992. - Том.1. – С. 172-211.

