Государственное образовательное учереждение высшего профессионального образования
Московская медицинская академия имени И.М. Сеченова
На правах рукописи
Мартиросян Наира Тариеловна
Дифференцированный подход к обследованию
и лечению женщин
с угрозой прерывания беременности
14.01.01 - Акушерство и гинекология
Диссертация на соискание
ученой степени
кандидата медицинских наук
Научный руководитель:
академик РАМН,
заслуженный деятель науки РФ,
профессор Стрижаков А.Н.
Москва – 2010
Работа выполнена в Московской медицинской академии имени И.М. Сеченова
Научный руководитель:
академик РАМН,
заслуженный деятель науки РФ,
профессор Александр Николаевич Стрижаков
Официальные оппоненты:
доктор медицинских наук
профессор Лали Григорьевна Сичинава
доктор медицинских наук
профессор Игорь Олегович Макаров
Ведущее учреждение – Московский государственный медико-стоматологический университет
Защита состоится «____» _______________ 2010 г. в 14 часов на заседании диссертационного совета Д208.040.03 при Московской медицинской академии имени И.М. Сеченова (119991, Москва, ул. Трубецкая, д. 8, стр. 2).
С диссертацией можно ознакомиться в ГЦНМБ ГОУВПО Московской медицинской академии имени И.М. Сеченова (117998, Москва, Нахимовский проспект, д. 49).
Автореферат разослан «____» _______________ 2010 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук,
профессор Александр Михайлович Шулутко
Актуальность темы. Несмотря на достигнутые в последние годы успехи в профилактике и лечении угрожающего прерывания беременности и привычной ее потери, частота самопроизвольных выкидышей остается стабильной и достаточно высокой. Так, по данным разных авторов она составляет от 2% до 55%, достигая в I триместре 50% (Кидралиева А.С.,1994; Сидельникова В.М., Дадальян Л.Г., 1996, 2004; Макаров И.О., 2009; Савельева Г.М., Сичинава Л.Г., 2007,2009; Торчинов А.М., 2006). Помимо частоты ранних репродуктивных потерь актуальность проблемы невынашивания беременности обусловлена высоким уровнем перинатальной заболеваемости и смертности (Boers G.N., 1997). По данным Ю.И. Барашнева (2001), Е.М. Бурцева и соавт. (1999), высокий уровень перинатальной и детской заболеваемости при угрозе прерывания определяется высокой частотой плацентарной недостаточности, которая развивается в 47,1% - 84,8%. Стремление снизить перинатальную заболеваемость и смертность при синдроме потери плода послужило поводом для поиска основных принципов ранней профилактики, своевременной диагностики и адекватной терапии осложнений беременности (Макаров И.О., 2009; Стрижаков А.Н., Серова О.Ф., 2000; Сидельникова В.М., 2002; Стрижаков А.Н., Игнатко И.В., 2007; Савельева Г.М., Сичинава Л.Г., 2007,2009; Торчинов А.М., 2006). Исходя из вышесказанного, вполне объяснимо, почему в последние годы сфера научных интересов в перинатальной охране плода сместилась к ранним срокам беременности - к первому триместру, так как именно в этот период происходит формирование фетоплацентарной системы, закладка органов и тканей плода, экстраэмбриональных структур, что в большинстве наблюдений определяет дальнейшее течение беременности (Стрижаков А.Н., Игнатко И.В. 2007). Благодаря внедрению высокоэффективных методов исследования, появилась возможность комплексной диагностики нарушений состояния плода с самых ранних сроков, определение их степени тяжести и патогенетических особенностей развития клинических проявлений плацентарной недостаточности (Савельева Г.М. 2000, 2009; Стрижаков А.Н. и соавт., 2003).
Цель исследования - разработать дифференцированный подход к ведению беременных с ретрохориальной гематомой на основании эхографической оценки особенностей развития плодного яйца, становления гемодинамики эмбриона/плода, гемостазиологического статуса беременной и продукции факторов роста.
Для достижения цели были поставлены следующие задачи:
1. определить эхографические параметры развития эмбриона и экстраэмбриональных структур в I триместре при наличии клиники угрожающего прерывания беременности с образованием ретрохориальной гематомы;
2.выявить особенности становления гемодинамики в системе мать-плацента-плод при наличии ретрохориальной гематомы, а также показать влияние гематомы на становление плодового и экстраэмбрионального кровотока;
3. установить взаимосвязь данных эхографического и допплерометрического исследований в I триместре с особенностями клинического течения беременности и исхода родов у пациенток с наличием ретрохориальной гематомы;
4. обосновать значимость исследования гемостазиологического статуса беременной (наличие врожденных и приобретенных нарушений гемостаза) в прогнозировании исходов первого триместра беременности и развития гестоза и плацентарной недостаточности;
5. изучить уровень сосудисто-эндотелиального фактора роста и фактора роста плаценты при угрожающем прерывании беременности и наличии ретрохориальной гематомы, определить их роль в патогенезе развития осложнений гестации и прогнозировании неблагоприятных исходов;
6. оценить эффективность дифференцированного подхода к терапии у беременных с ретрохориальной гематомой, основанного на оценке эхографических и допплерометрических особенностей эмбриоплацентарной системы, гемостазиологического статуса беременной, продукции факторов роста в снижении частоты репродуктивных потерь, плацентарной недостаточности, гестоза и неонатальной заболеваемости.
Научная новизна.
Впервые в акушерской практике проведена комплексная эхографическая оценка развития эмбриона и внезародышевых структур (хорионической и амнионической полостей, экзоцелома, желточного мешка и хориона) в I триместре у беременных с угрожающим прерыванием беременности и ретрохориальной гематомой. Установлена взаимосвязь эхографических параметров эмбриона и экстраэмбриональных структур с особенностями течения и исхода беременности при наличии ретрохориальной гематомы. Впервые проведено изучение гемостазиологического статуса женщин с угрожающим прерыванием беременности и ретрохориальной гематомой с определением значимости врожденных и приобретенных дефектов гемостаза в патогенезе ранних репродуктивных потерь и развития других осложнений гестации. Изучены особенности продукции факторов роста (СЭФР и ФРП) у беременных с угрожающим прерыванием и наличием отслоек хориальной ткани и определена их роль в прогнозе репродуктивных потерь, гестоза и плацентарной недостаточности. Впервые оценена эффективность дифференцированного подхода к терапии у беременных с ретрохориальной гематомой, основанного на оценке эхографических и допплерометрических особенностей эмбриоплацентарной системы, гемостазиологического статуса беременной, продукции факторов роста.
Практическая значимость работы.
Установлено, что оценка эхографических и допплерометрических особенностей формирования системы мать-плацента-плод в I триместре беременности при наличии ретрохориальной гематомы позволяет оценить не только рост и развитие плодного яйца, но также выявить прогностически неблагоприятные маркеры ранних репродуктивных потерь, развития гестоза и плацентарной недостаточности. Доказано, что у 64-68% пациенток с ретрохориальной гематомой имеет место генетическая или приобретенная тромбофилия. При этом частота длительной угрозы прерывания, ПН, СЗРП, гестозом, репродуктивными потерями в последующем напрямую определяется выраженностью нарушений гемостаза. При изучении факторов роста показано, что уже в I триместре (6-10 недель) при наличии ретрохориальной гематомы на фоне угрожающего прерывания беременности значения ФРП и СЭФР значительно изменяются. Так, средний уровень СЭФР выше значений при неосложненной беременности в 2,04 раза, а средний уровень ФРП – в 2,7 раза ниже. В результате проведенного исследования разработан дифференцированный подход к ведению беременных с угрожающим прерыванием беременности и ретрохориальной гематомой на основании данных эхографического, допплерометрического исследований в I триместре, изучения гемостаза и продукции факторов роста. Подобная тактика позволила повысить эффективность терапевтических мероприятий в 87,4% наблюдений.
Основные положения, выносимые на защиту.
1. комплексное эхографическое и допплерометрическое изучение особенностей развития системы мать-плацента-плод в I триместре гестации при наличии ретрохориальной гематомы позволяет своевременно выявить прогностически неблагоприятные маркеры ранних репродуктивных потерь, развития осложнений беременности во второй ее половине;
2. оценка данных ультразвукового обследования с учетом клинических особенностей течения беременности и нарушением системы гемостаза позволяет осуществлять своевременную коррекцию нарушений и повысить эффективность гравидопротективной терапии;
3. исследование уровня факторов роста (СЭФР и ФРП) дает возможность не только прогнозировать ранние репродуктивные потери, но и развитие гестоза и плацентарной недостаточности, а также осуществлять контроль за эффективностью проводимой терапии;
4. разработанные эхографические, допплерометрические, лабораторные критерии оценки состояния фетоплацентарной системы на ранних сроках гестации позволяют выделить группу риска в отношении неблагоприятного течения и исхода беременности при угрожающем прерывании беременности с формированием ретрохориальной гематомы.
Внедрение результатов исследования в практику.
Результаты исследования и практические рекомендации, вытекающие из них, внедрены в клиническую практику работы гинекологических отделений и родильного дома при ГКБ №7 г. Москвы. Материалы и результаты исследования широко используются в учебном процессе в виде лекций и практических занятий для студентов, интернов и клинических ординаторов Московской медицинской академии имени И.М. Сеченова.
Апробация материалов диссертации.
Материалы диссертации доложены на VIII и X Всероссийском форуме «Мать и дитя» (2007,2009), II Ежегодного конгресса специалистов перинатальной медицины «Новые технологии в перинатологии» (2007), XV Российского национального конгресса «Человек и лекарство»(2008), IV Международном конгрессе по репродуктивной медицине (2010). Апробация диссертации состоялась на конференции сотрудников кафедры акушерства, гинекологии и перинатологии лечебного факультета Московской медицинской академии имени И.М. Сеченова.
Структура и объем диссертации.
Диссертация состоит из введения, четырех глав, выводов, практических рекомендаций и указателя использованной литературы. Материалы диссертации изложены на 196 страницах машинописного текста, иллюстрированы 34 таблицами и 28 рисунками. Список литературы включает 265 публикацию: 121 отечественных и 144 зарубежных автора.
Публикации:
По теме диссертации опубликованы 6 печатных научных работ, из них 1в центральной печати, в которых изложены основные положения диссертации
СОДЕРЖАНИЕ РАБОТЫ
Клиническая характеристика и методы обследования беременных.
С целью разработки системы обследования и ведения беременных с угрозой прерывания и частичной отслойкой хориона в I триместре проведено проспективное обследование – 139 женщин. Из них 53 женщины с нормальным течением одноплодной беременности, с неотягощенным акушерско-гинекологическим и соматическим анамнезом составили контрольную группу. В основную группу включены 42 беременные с угрозой прерывания и отслойкой хориона в первом триместре беременности. В этой группе нами проведено ультразвуковое, допплерометрическое исследование, исследование гемостаза, уровня факторов роста, а также медикаментозная коррекция осложнений беременности. У всех женщин беременность и роды были проведены с использованием новых технологий оценки состояния плода с учетом этиопатогенеза угрозы прерывания беременности, и соблюдением принципов ранней диагностики и медикаментозной коррекции осложнений гестационного процесса. Группу сравнения составили 44 беременные с такой же патологией, не получавшие дифференцированной терапии на основе определения ведущих механизмов патогенеза. В данной группе мы проводили динамическое ультразвуковое и допплерометрическое исследование в определенные сроки беременности, исследование гемостаза, уровня факторов роста,
Все женщины контрольной группы имели неотягощенный соматический и акушерско-гинекологический анамнез, а также нормальный менструальный цикл. Настоящая беременность у данных пациенток была одноплодной и протекала без осложнений на всем ее протяжении по данным клинико-лабораторных и инструментальных методов исследования. Все беременности в контрольной группе обследуемых, закончились рождением живых доношенных детей массой 3450,56+240,59 г, ростом 51,45+2,01 см, с оценкой по шкале Апгар 8-9 баллов. Последующие неонатальный, послеродовый, послеоперационный периоды протекали без осложнений.
Основная группа была представлена 42 беременными, средний возраст которых составил 26,21+ 1,34 лет с индивидуальными колебаниями от 18 до 37 лет. Группу сравнения составили 44 беременные. В обеих группах количество первобеременных первородящих достоверно не отличалось и составило 26,7% (23 женщины). Повторнобеременных в обеих группах было 63 (73,3%), из них 28 (32,6%) - первородящие и 35 (40,7%) - повторнородящие. Из этих 35 повторнородящих женщин у 15 (42,9%) предыдущая беременность протекала на фоне угрозы прерывания, а у 11 (31,4%) была обнаружена ретрохориальная гематома в первом триместре. Особенности акушерского анамнеза характеризовались наличием искусственных абортов (от одного до трех) в 43,1% наблюдениях, наличием самопроизвольных выкидышей до 14 недель у 27,3% беременных. При изучении соматического статуса у женщин обеих подгрупп выявлено наличие экстрагенитальной патологии в 32,6% (28 пациенток). Тяжелых соматических заболеваний не было выявлено ни в одном наблюдении. Гинекологический анамнез был отягощен у 44 (51,16%) женщин обеих групп. В 24 (27,9%) наблюдениях ранее проводилось лечение по поводу наличия генитальных инфекций. Течение настоящей беременности в I триместре у всех женщин осложнилось угрозой прерывания беременности и отслойкой хориона. Жалобы на кровянистые выделения из половых путей предъявляли 60 (69,76%) женщин, тянущие боли внизу живота отмечались у 64 (74,41%). У 50 (58,14%) беременных выявлено сочетание вышеперечисленных симптомов, у 10 (11,63%) - только кровянистые выделения из половых путей, у 14 (16,28%) - боли внизу живота. У 12 (13,95%) беременных ретрохориальная гематома явилась находкой при ультразвуковом сканировании. За время наблюдения всем пациентам с осложненным течением беременности проводилась комплексная патогенетическая терапия, основанная на современных принципах лечения выявленной патологии.
В последующем, в основной группе во II и III триместрах с учетом 2 (4,76%) произошедших самопроизвольных выкидышей и 1(2,38%) прерывания беременности по медицинским показаниям под нашим наблюдением находилось 39 беременных. В данной группе плацентарная недостаточность диагностирована у 8 (20,0%): компенсированная - у 7(87,5%) беременных и субкомпенсированная - у 1 (12,50%). Декомпенсированная ПН не отмечалась ни в одном наблюдении. СЗРП был диагностирован у 5 (12,85%) беременных. Гипоксия плода - у 3(7,7%). У всех беременных с гестозом - 7(17,95%) - наблюдалась легкая форма данного осложнения. В этой группе преждевременные роды (на 37 неделе) произошли у 3(7,14%) беременных, своевременные роды - у 36 (85,71%). В группе сравнения самопроизвольное прерывание беременности произошло в 5 (11,36%) наблюдениях, искусственное прерывание по медицинским показаниям - у 1 (2,27%), преждевременные роды - у 4 (9,09%), своевременные роды - у 33 (75,0%) женщин. В данной группе плацентарная недостаточность диагностирована у 13 (34,21%): компенсированная - у 9 (69,23%), субкомпенсированная – у 3 (23,08%) беременных. Декомпенсированная ПН отмечалась в 1 наблюдении (2,63%). СЗРП был диагностирован в 11 (28,95%) наблюдениях. Гипоксия плода выявлена у 7 (18,42%) беременных. У 7 (70%) беременных с гестозом наблюдалась легкая форма, среднетяжелая - у 3 (30%).
У женщин обследуемых групп в целом родоразрешение путем операции кесарева сечения проводилось 17 (21,8%) беременным. Средняя оценка новорожденных по шкале Апгар в основной группе составила на 1 минуте после рождения 7,59+ 0,08, на 5 минуте - 8,59+0,08. Средняя масса новорожденных составила 3644,6+232 г, средний рост - 52,45+2,01 см.
Методы обследования.
Клиническая часть обследования включала детальное изучение анамнеза, объективное исследование, оценку лабораторных анализов, а также клинико-лабораторное обследование новорожденных в динамике.
Эхографическое обследование пациенток проводили на ультразвуковом приборе «Aloka SSD 2000», работающего в режиме импульсного и цветного допплеровского картирования. Эхографическое обследование в I триместре заключалось в определении ультразвуковых признаков угрозы прерывания беременности, отслойки хориона, ее размеров и месторасположения, особенностей развития эмбриона, экстраэмбриональных структур. Во II – III триместрах беременности ультразвуковое обследование включало фетометрию, тщательную оценку анатомии плода, поиск маркеров хромосомальных аномалий и внутриутробного инфицирования, плацентографию, оценку качества и количества околоплодных вод. С помощью импульсного режима и цветного допплерометрического картирования изучен внутриплацентарный, маточно-плацентарно-плодовой кровоток.
Исследование системы гемостаза проводили в лаборатории патологии гемостаза кафедры акушерства и гинекологии (заведующий кафедрой, профессор А. Д. Макацария) медико-профилактического факультета ММА им. И.М. Сеченова. Генетические формы тромбофилии диагностировали методом полимеразной цепной реакции. Проводили определение показателей плазменного звена гемостаза (АЧТВ, ПИ, МНО), тромбоэластограммы (ч+к, ма, ИТП, 2ТЭГ-К, проба переноса), исследовали агрегационную активность тромбоцитов с использованием различных индукторов агрегации (АДФ, ристомицин). Диагностику ДВС-синдрома осуществляли по уровню молекулярных маркеров тромбофилии: ТАТ, Pt Fl+2, РКМФ, Д-димер, ПДФФ. Определяли также волчаночный антикоагулянт, проводили ИФА-диагностику концентрации антифосфолипидных антител (IgG, IgM), кофакторов антифосфолипидных антител (антитела IgG, IgM к аннексину V, антитела IgG, IgM, IgА к 2гликопротеину I, антитела IgG, IgM, IgА к протромбину).
Сосудисто-эндотелиальный фактор роста и фактор роста плаценты определяли в лаборатории клинической биохимии НИИ клинической онкологии ГУ РОНЦ им. Н.Н.Блохина РАМН (заведующий - член-корр. РАМН, профессор Н.Е. Кушлинский). Определение СЭФР и ПФР в сыворотке крови основано на количественном иммуноферментном анализе (quantitative sandwich enzyme immunoassay technique) (R&D systems).
Кардиотокографическое исследование проводили всем женщинам при помощи приборов OXFORD Sonicaid Team (Великобритания) и Hewett Packard Virida Series 50 XM (США) по общепринятой методике с компьютерной обработкой данных (OXFORD System 8000, Великобритания).
Статистическая обработка результатов исследования.
Статистическая обработка материалов проводилась на персональном компьютере с процессором Intel Pentium-II, в среде Window’s 2000, с использованием прикладных статистических пакетов «Statistica 5.5», а также статистических функций прграммы MS Exel’2000.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ.
Для выявления особенностей роста и развития эмбриона, экстраэмбриональных структур при угрозе прерывания и ретрохориальной гематоме в I триместре беременности с помощью трансвагинальной эхографии обследовано 86 женщин. При проведении ультразвукового сканирования обращали внимание на расположение, объем, срок проявления гематомы.
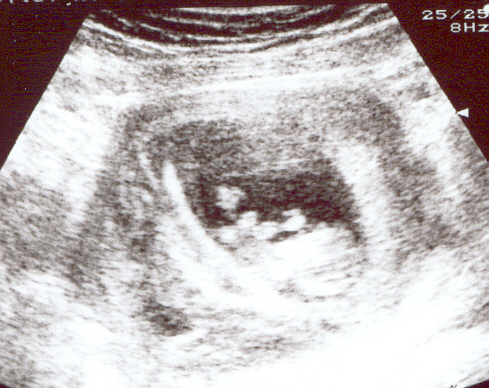
Рис.1. Эхограмма ретрохориальной гематомы большого объема с признаками активной организации (указано стрелкой).
В основной группе в 2(4,76%) наблюдениях беременность закончилась са- мопроизвольным прерыванием беременности, гематома локализовалась в области одной из стенок полости матки(рис.1). При супрацервикальном расположении гематомы ни в одном наблюдении прерывания беременности не было, а при корпоральном расположении гематомы у 4(12,1%) беременных в группе сравнения произошло самопроизвольное прерывание беременности. Следует отметить, что в основной группе у 33,33% с ретрохориальной гема-
томой, выявленной до 6 недель, в дальнейшем произошло самопроизвольное прерывание беременности. При проведении биометрии эмбриона выявлено, что отставание КТР >7 дней (7(8,14%)) в обеих группах привело: к самопроизвольному прерыванию у 5(71,4%) и неразвивающейся беременности у 2(28,6%) беременных. Оценка ЧСС эмбриона показала, что наиболее неблагоприятным является брадикардия. Урежение сердечного ритма до 90 уд/мин обнаружено у 3 (7,69%) пациенток группы сравнения и во всех наблюдениях привело к потере беременности. Среди беременных обеих групп с выраженной угрозой прерывания и ретрохориальной гематомой у 14 (16,28%) эмбрионов отмечена тахикардия. При этом только в 3 наблюдениях произошло самопроизвольное прерывание беременности (табл.1)
| Таблица 1. Эхографические особенности эмбриона при угрозе прерывания беременности и отслойке хориона. | |||
| Эхографический признак | Частота | Течение беременности | Исход беременности |
| Отставание КТР от срока >7 дней | 17 (19,77%) | Угроза прерывания, начавшийся самопроизвольный выкидыш – 7(41,17%) | Самопроизвольное прерывание – 5(29,41%) Неразвивающаяся беременность – 2(11,76%) |
| Брадикардия | 3 (3,45%) | Начавшийся самопроизвольный выкидыш (ретрохориальная гематома большого объема) – 100% | Самопроизвольное прерывание - 2(66,7%) Неразвивающаяся беременность - 1(33,3%) |
| Тахикардия | 14 (16,28%) | Угроза прерывания, ретрохориальная гематома большого объема – 41,18% | Самопроизвольное прерывание у 1(7,14%) Неразвивающаяся беременность у 2(14,3%) женщин группы сравнения |
Объем плодного яйца соответствовал параметрам, характерным для неосложненной беременности у 28 (32,56%) женщин в обеих группах. У 48,6% выявлено маловодие, у 18,6% - многоводие. Во всех наблюдениях маловодие сопровождалось клиническими признаками угрозы прерывания с кровянистыми выделениями из половых путей. Выраженное прогрессирующее уменьшение объема плодного яйца в группе сравнения отмечено у 5 (11,34%) пациенток с последующим самопроизвольным прерыванием беременности. У этих же беременных отмечалось отставание КТР от срока беременности и нарушение сердечной деятельности эмбриона. Раннее многоводие диагностировано у 16 (27,6%) беременных. Во всех наблюдениях при многоводии были выявлены возбудители заболеваний, передающихся половым путем. Эхографические отклонения в размере, форме, и структуре желточного мешка выявлены в 28 (32,56%) наблюдениях. Увеличение размера желточного мешка более 10 мм отмечено у 4 (14,3%). В 50% наблюдений увеличение размера желточного мешка сопровождалось отставанием КТР от гестационного срока на 2 недели, выраженным маловодием, что в дальнейшем привело к самопроизвольному прерыванию беременности на сроке 7-8 недель (группа сравнения).
Кровоток в межворсинчатом пространстве регистрировался с помощью цветового допплеровского картирования, начиная с 6 недель беременности. Анализ результатов допплерометрического исследования межворсинчатого кровотока выявил у 62 (72,09%) пациенток гемодинамические нарушения. При этом для 53 (85,48%) беременных обеих групп с небольшими гематомами (до 20 мл) явилось характерным снижение индексов сосудистого сопротивления (в сроке 8-13 недель ИР=0,36+0.03, ПИ=0,49+0,06). В то время как в 9 (14,52%) наблюдениях, где объем субхориальной гематомы превышал 20 мл, регистрировалось увеличение показателей сосудистой резистентности в межворсинчатом пространстве (в сроке 8-13 недель ИР=0,51+0,06, ПИ=0,72 +0,06). В результате данные беременности закончились самопроизвольным прерыванием. Увеличение периферического сопротивления в маточных артериях зафиксировано в 19 (24,36%) наблюдениях с выраженными признаками угрозы прерывания. Допплерометрическое исследование кровотока во всех наблюдениях установлено повышение сосудистого сопротивления (ПИ>0,67) в спиральных артериях, расположенных в области проекции ретрохориальной гематомы. У 6 (7,69%) беременных с большим объемом корпоральной гематомы соответственно зарегистрировано полное отсутствие диастолического компонента в области проекции гематомы (рис.2). Результаты допплерометрического исследования показывают, что первые цветовые сигналы кровотока в аорте и артерии пуповины плода начинают отчетливо регистрироваться с 7 недель беременности.
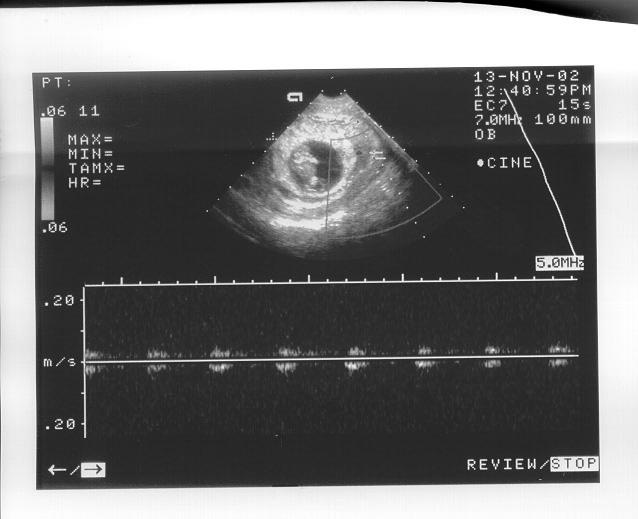
Рис. 2. Отсутствие диастолического компонента кровотока в спиральных артериях в области проекции ретрохориальной гематомы.
У 18(22,78%) плодов на сроке 10-11 недель установлены высокие значения пульсационного индекса (ПИ=3,48+0,16 в 10 недель и 3,3+0,11 в 11 недель). В дальнейшем на фоне проведения комплексной патогенетической терапии отмечена нормализация всех сосудистых нарушений к 18-20 неделям гестации. При последующем динамическом наблюдении у всех пациенток наблюдалось успешное прогрессирование и вынашивание беременности до доношенного срока. При исследовании кровотока в вене пуповины в первом триместре установлено, что сохранение пульсирующего спектра кровотока при наличии выраженных клинически симптомов угрожающего выкидыша в 42,8% является неблагоприятным признаком. Данные допплерометрического исследования кровотока в венозном протоке в I триместре в 46 (53,5%) наблюдениях не соответствовали нормативным значениям. Во всех случаях эти изменения сочетались с клиникой угрозы прерывания беременности и с кровянистыми выделениями из половых путей. Надо отметить, что у большинства (14(60,9%) и 17(73,9%) соответственно в основной группе и группе сравнения) из них изменения кровотока в венозном протоке сопровождалось симптомами угрозы прерывания и во II триместре.
Во II и III триместре нами проведено комплексное эхографическое и допплерометрическое обследование 78 беременных, из них 39 женщин из основной группы, 39 – из группы сравнения. При проведении эхографического обследования у 5 из 39 (12,8%) беременных основной группы был выявлен синдром задержки роста плода. У 3 (7,7%) беременных было выявлено маловодие, у 2 (5,1%) – многоводие (на фоне внутриутробного инфицирования, что потребовало проведения антибактериальной терапии). При проведении эхографического обследования у 11(28,21%) из 39 беременных группы сравнения был выявлен синдром задержки роста плода. Анализ фетометрических показателей позволил установить у 8 из 11 (72,73%) беременных СЗРП 1 степени с отставанием данных фетометрии на 1-2 недели от нормативных для данного срока гестации, у 3 (27,27%) – СЗРП II степени (с отставанием фетометрических показателей на 2-3 недели). Средний срок выявления СЗРП составил 30-32 недели. Следует отметить, что у всех беременных при этом отмечалась аномальная продукция факторов роста (СЭФР и ФРП) и нарушения гемостаза. При проведении допплерометрического обследования беременных обеих групп нами было выявлено, что в основной группе у 23 (57,5%) беременных и у 20 (51,28%) - в группе сравнения после организации ретрохориальной гематомы, обнаруженной в первом триместре, и нормализации показателей кровотока в спиральных и маточных артериях, выявлено постепенное снижение индексов сосудистого сопротивления на всем протяжении беременности. У остальных 16 (41%) беременных в основной группе и у 19 (48,72%) - в группе сравнения наблюдались нарушения кровотока в маточных и спиральных артериях.
Семейный тромботический анамнез оказался отягощенным у 24 (27,9%) из 86 обследованных беременных основной группы и группы сравнения. При наличии у беременных ретрохориальной гематомы суммарная доля тромбофилии составила 67,44% (58 беременных), в группе же пациенток с неосложненной беременностью – 1,89%. У женщин с ретрохориальной гематомой установлена высокая частота генетически обусловленной тромбофилии (44,2%). Наиболее часто встречались: гомозиготная и гетерозиготная мутация гена фермента метилентетрагидрофолатредуктазы (MTHFR), полиморфизм гена PAI-1, и полиморфизм рецептора ангиотензина II. Антифосфолипидные антитела были выявлены у 22,09% беременных. Циркуляция АФА в каждом четвертом наблюдении имела место в сочетании с генетической тромбофилией, и только у 16,28% была выявлена изолировано.
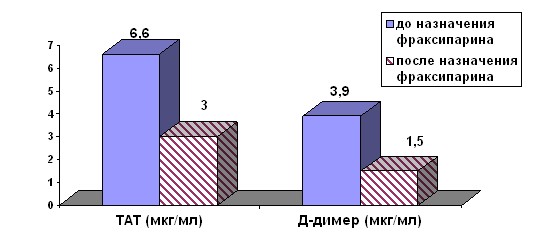
Рис. 3. Динамика снижения агрегационной активности тромбоцитов до и через 10 дней от начала терапии.
Первое исследование системы гемостаза проводилось пациенткам до назначения НМГ, а затем через 10 дней и далее ежемесячно. В результате терапии с использованием НМГ как базового препарата к 10 дню терапии по лабораторным данным отмечалось достоверное снижение уровня маркеров тромбофилии (ТАТ, Д-димер) и нормализация функции тромбоцитов (рис.3).
Нами был изучен уровень двух факторов роста ангиогенеза в сыворотке крови у беременных: 1) сосудисто-эндотелиальный фактор роста (СЭФР) и 2) фактор роста плаценты (ФРП). Уже в I триместре (6-10 недель) при наличии ретрохориальной гематомы на фоне угрожающего прерывания беременности значения ФРП и СЭФР значительно изменяются. Так, средний уровень СЭФР выше значений при неосложненной беременности в 2,04 раза, а средний уровень ФРП – в 2,7 раза ниже. Причем, в группе сравнения значения СЭФР были выше не только нормативных значений, но и значений, полученных в основной группе, а уровень ФРП – был ниже. Следует отметить, что у 2 (4,55%) беременных группы сравнения с диагностированной в последующем неразвивающейся беременностью отмечались значения ФРП равные 0. В последующем, у беременных с ретрохориальной гематомой отмечались следующие осложнения (табл.2).
| Таблица 2. Осложнения II и III триместров у беременных основной группы и группы сравнения. | ||
| Виды осложнений | Основная группа (n=39) | Группа сравнения (n=39) |
| Угроза прерывания во II и III триместрах | 19 (47,5%) | 22 (56,41%) |
| Гестоз | 7 (17,5%) | 10 (25,64%) |
| Плацентарная недостаточность (гипоксия плода+СЗРП) | 8 (20,0%) | 13 (34,21%) |
В основной группе, где женщины получали патогенетическое лечение, продукция ФРП во II триместре соответствовала нормативным значениям, а СЭФР - в 2,36 раза выше, чем при неосложненной беременности, что можно расценить как компенсаторную реакцию на локальную ишемию плацентарной ткани при повышении тонуса миометрия. В III триместре - продукция ФРП была 1,42 выше, чем при неосложненной беременности. В группе сравнения продукция ФРП во II триместре при наличии клиники угрозы прерывания также соответствовала нормативным параметрам, а при угрожающих преждевременных родах была в 1,33 раза ниже, чем при неосложненной беременности, и в 1,9 раза ниже, чем в основной группе. В этой группе беременных отмечались неблагоприятные исходы беременности (поздний самопроизвольный выкидыш в 24-25 нед, преждевременная отслойка нормально расположенной плаценты в 32-33 нед, преждевременные роды 36-37 нед, антенатальная гибель плода в 37-38 недель). Продукция СЭФР у беременных основной группы во II триместре была в 2,48 раза выше, чем при неосложненной беременности. В группе сравнения – в 3,63 раза выше. В III триместре продукция СЭФР была в 4,53 раза и в 6,33 раза выше, чем при неосложненной беременности, в обеих группах соответственно.
Использование разработанного дифференцированного подхода позволило снизить в 1,2 раза частоту развития угрозы прерывания во II и III триместрах, причем частота репродуктивных потерь в группе сравнения (без дифференцированного подхода к терапии) была в 2,87 раза выше, чем в основной группе. Частота преждевременных родов в основной группе была в 1,27 раза ниже, а сами роды происходили не ранее 36-37 нед, и новорожденные не потребовали проведения реанимационных мероприятий. Частоту СЗРП удалось снизить - в 2,25 раза, а сам СЗРП был 1 степени. Учитывая более благоприятное течение беременности, частота оперативного родоразрешения составила 16,67% в основной группе против 22,73% - в группе сравнения.
ВЫВОДЫ
1. Применение высокотехнологичных методов исследования (эхография, допплерометрия, кардиотокография) и современных лабораторных тестов (диагностика тромбофилий, определение уровня факторов роста) с учетом новых представлений о патогенезе угрозы прерывания беременности (с формированием ретрохориальной гематомы) позволяет оптимизировать акушерскую тактику при данном осложнении, снизить частоту репродуктивных потерь, перинатальную заболеваемость и смертность.
2. Обнаружение ретрохориальной гематомы до 6 недели гестации в 33,3-50% является маркером ранних репродуктивных потерь. При этом наиболее неблагоприятно сочетание ретрохориальной гематомы большого объема (более 20 мл) с корпоральным ее расположением и отставанием КТР от нормативных параметров на 10 и более дней.
3. Прогностически неблагоприятными ультразвуковыми критериями при угрозе прерывания беременности являются: отсутствие желточного мешка при СВДпя>10мм, отсутствие визуализации эмбриона при СВДпя>14 мм., отсутствие сердечной деятельности при КТР>16мм, отставание роста эмбриона более чем на 2 недели при КТР<18 мм., брадикардия (ЧСС90 уд/мин), прогрессирующее уменьшение объемов амниотической и хориальной полостей, ретрохориальная гематома в области проекции корня пуповины.
4. Эхографическими критериями патологического течения беременности (ранних репродуктивных потерь, плацентарной недостаточности и гестоза) при наличии ретрохориальной гематомы следует считать: позднюю визуализацию эмбриона (после 6 нед), уменьшение (d<2мм) и увеличение (d>7мм) диаметра желточного мешка на сроке 5-12 недель, нарушение сердечной деятельности плода, раннее маловодие плодного яйца, наличие корпорально расположенной ретрохориальной гематомы, нарушение кровотока в спиральных артериях и межворсинчатом пространстве. Сочетание двух вышеперечисленных признаков увеличивает риск самопроизвольного выкидыша в 4,5 раза, трех и более факторов – в 6,2 раза.
5. При наличии у беременных ретрохориальной гематомы суммарная доля тромбофилии составила 67,44%, в группе же пациенток с неосложненной беременностью -1,89%. У женщин с ретрохориальной гематомой установлена высокая частота генетически обусловленной тромбофилии(44,2%). У 8,14% беременных с ретрохориальной гематомой имела место мультигенная форма тромбофилии. У 64,29% беременных с ретрохориальной гематомой обнаружена гиперкоагуляция, повышения маркеров тромбофилии (Д-димер, РКМФ), у 62,7% - повышенная агрегация тромбоцитов. АФА обнаружены у 22%, циркуляция ВА -у 5,8%, антитела к 2-гликопротеину- у 16,25%, антитела к протромбину -у 3,6%, антитела к аннексину V -у 2,35% беременных, что является неблагоприятным патогенетическим фоном ранних репродуктивных потерь, плацентарной недостаточности и гестоза.
6. В первом триместре (6-10 недель) при наличии ретрохориальной гематомы на фоне угрожающего прерывания беременности значения ФРП и СЭФР значительно изменяются. Так, средний уровень СЭФР выше значений при неосложненной беременности в 2,04 раза, а средний уровень ФРП – в 2,7 раза ниже. У 4,55% беременных с диагностированной в последующем неразвивающейся беременностью отмечалось отсутствие ФРП. Повышенная выработка СЭФР отмечалась во всех наблюдениях при ретрохориальной гематоме в первом триместре, независимо от исхода беременности.
7. Использование разработанного дифференцированного подхода позволило снизить в 1,2 раза частоту развития угрозы прерывания во втором и третьем триместрах, причем частота репродуктивных потерь в группе сравнения (без дифференцированного подхода к терапии) была в 2,87 раза выше, чем в основной группе. Частоту СЗРП удалось снизить в - 2,25 раза, а гестоза -в 1,47.
8. Частота рождения детей в состоянии гипоксии с проведением реанимационных мероприятий и интенсивной терапии, была в 4,88 раз ниже в основной группе беременных. Почти в 5 раз реже диагностировалось гипоксически-ишемическое поражение ЦНС плода, в 2,66 раза реже – выявлялись признаки внутриутробного инфицирования. Перинатальная заболеваемость при дифференцированном подходе составила 7,68%, перинатальная смертность – 0. В группе сравнения перинатальная заболеваемость составила 22 %, перинатальная смертность – 2,63%.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- В обследование пациенток с угрозой прерывания беременности в I триместре гестации рекомендуется включить трансвагинальное ультразвуковое исследование с обязательной оценкой роста эмбриона, развития экстраэмбриональных структур плодного яйца, сердечной деятельноcти эмбриона, кровотока в спиральных артериях и венозном протоке плода. Обязательным является обследование беременной на врожденные и приобретенные тромбофилии, определение маркеров ДВС-синдрома, тромбоцитопатий, а также уровня ФРП и СЭФР.
- Дифференцированный подход к терапии зависит от полученных эхографических и клинико-лабораторных данных.
| Основные эхографические параметры и тактика ведения пациенток с ретрохориальной гематомой. | ||
| Эхографический признак | Дополнительные показатели | Терапия |
| Отставание КТР > 10 дней |
| - мониторный УЗ контроль (каждые 3-5 сут) из-за высокой вероятности неразвивающейся беременности; - гестагены (Дюфастон, Утрожестан); - Аспирин (до 100 мг/сут) - Метипред (при выявлении гиперандрогении, гематоме большого объема). |
| Уменьшение объемов амниотической и хориальной полостей |
| - гестагены (Дюфастон, Утрожестан); - Метипред (при выявлении гиперандрогении) - Актовегин !! - Магне В6 |
| Уменьшение объема амниотической полости | - повышение тонуса миометрия; - отсутствие признаков организации гематомы. | - спазмолитическая (Магне В6, Но-шпа и т.д.) терапия; - гестагены (беременным с ППБ) - Метипред до появления активной организации, далее – при гиперандрогении |
| Раннее многоводие + увеличение диаметра желточного мешка |
| - ранняя антибиотикотерапия (по показаниям), иммуностимулирующая терапия; - Дюфастон !! - Актовегин |
| Нарушения кровотока в спиральных артериях и межворсинчатом пространстве | - повышение агрегационной активности тромбоцитов - Снижение уровня прогестерона, - снижение продукции ФРП (более чем в 2 раза) или повышение уровня ФРП (более чем в 1,3 раза), повышение продукции СЭФР. | - антиагреганты (Курантил, Аспирин) - гестагены (Дюфастон, Утрожестан) до 24 нед !! - Магне В6 - Актовегин |
| Нарушения кровотока в венозном протоке с 10 недели | - отставание КТР > 10 дней; - изменение сердечной деятельности эмбриона (бради- или тахикардия); - увеличение ТВП | - мониторный УЗ контроль (каждые 3-5 сут) из-за высокой вероятности неразвивающейся беременности; - кариотипирование !! - антиагреганты (Курантил, Аспирин); - гестагены |
| Любые эхографические изменения при наличии врожденных и приобретенных тромбофилий | при наличии органицазации гематомы по УЗИ, после прекращения кровянистых выделений из половых путей | - антикоагулянтная терапия (низкомолекулярные гепарины) - антиагрегантная терапия (Аспирин, Курантил) - фолиевая кислота 1мг 3 р/сут - далее – Дюфастон |
- В 16-18 недель, учитывая высокую частоту нарушений становления системы мать-плацента-плод, длительной угрозы прерывания, нарушений маточно-плацентарного и плодово-плацентарного кровотока, для ранней диагностики и профилактики гестоза и плацентарной недостаточности, необходимо проводить динамическое эхографическое и допплеромпетрическое исследование маточно-плацентарного, плодового и внутриплацентарного кровотока. Необходим контроль за показателями гемостаза и их своевременная коррекция (антикоагулянты (низкомолекулярные гепарины) – фраксипарин 0,3-0,6 мл/сут, фрагмин – 0,2-0,6 мл/сут, клексан – 0,2-0,8 мл/сут под контролем показателей коагулограммы, антиагреганты - аспирин до 100 мг/сут, курантил – 75 мг/сут, трентал – 300 мг\сут). При нарушениях плодового кровотока показано применение Актовегина по 200 мг 3 р/сут курсами по 3 нед. В 20-22 недели следует проводить контрольное эхографическое обследование для исключения аномалий развития плода. В 28-32 недели беременности показано проведение эхографии, детального допплерометрического и кардиотокографического обследования для оценки состояния фетоплацентарного комплекса, гемодинамики и гемостаза матери. Для оценки степени тяжести плацентарной недостаточности необходимо определять уровень СЭФР и ФРП в сроки 28-30 недель.
- При появлении признаков угрозы прерывания беременности во II триместре, особенно с повторным формированием ретрохориальной (ретроплацентарной или заоболочечной) гематомы показана госпитализация и терапия в условиях акушерского стационара.
- Выявление признаков плацентарной недостаточности и гестоза также требует госпитализации в акушерский стационар и дальнейшее ведение беременности осуществляется по общепринятым стандартам с учетом данных эхографии, допплерометрии, определения гемостазиологического статуса беременной и уровня факторов роста.
Список работ, опубликованных по теме исследования
1 Игнатко И.В., Мартиросян Н.Т. Прогноз перинатальных исходов у женщин с угрозой прерывания и частичной отслойкой хориона в первом триместре. Материалы VIII Всероссийского форума «Мать и дитя», Москва, 2007, с. 88.
2. Стрижаков А.Н., Игнатко И.В., Мартиросян Н.Т. Прогноз перинатальных исходов беременности у женщин с угрозой прерывания и частичной отслойкой хориона в I триместре. Материалы II Ежегодного конгресса специалистов перинатальной медицины «Новые технологии в перинатологии», Москва, 2007, с.18.
3. Стрижаков А.Н., Игнатко И.В., Мартиросян Н.Т. Принципы комплексной терапии угрожающего прерывания беременности у женщин с привычным невынашиванием. «Вопросы гинекологии, акушерства и перинатологии», Москва, 2008, 2(7),с. 5-11.
4. Мартиросян Н.Т., Игнатко И.В. Эффективность лечения угрозы прерывания у женщин с частичной отслойкой хориона в I триместре. Материалы XV Российского национального конгресса «Человек и лекарство»,2008, с.463
5. Стрижаков А.Н., Игнатко И.В., Мартиросян Н.Т. Эхографические особенности эмбриона, экстраэмбриональных структур и становление маточно-плацентарного кровотока в I триместре у женщин с отслойкой хориона. Материалы X Всероссийского форума «Мать и дитя», Москва, 2009, с.74-75.
6. Игнатко И.В., Мартиросян Н.Т. Сравнительная оценка медикаментозной коррекции осложнений беременности у женщин с угрозой прерывания и отслойкой хориона в первом триместре. Материалы X Всероссийского форума «Мать и дитя», Москва, 2009, с.75-76.

