Поиск веществ с противомикробной активностью среди производных антраниловой кислоты, полиоксосоединений и гетероциклических азотсодержащих соединений
На правах рукописи
Дубровина Светлана Сергеевна
ПОИСК ВЕЩЕСТВ С ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ СРЕДИ ПРОИЗВОДНЫХ АНТРАНИЛОВОЙ КИСЛОТЫ, ПОЛИОКСОСОЕДИНЕНИЙ И ГЕТЕРОЦИКЛИЧЕСКИХ АЗОТСОДЕРЖАЩИХ СОЕДИНЕНИЙ
15.00.02 – фармацевтическая химия, фармакогнозия
Автореферат диссертации на соискание ученой степени
кандидата фармацевтических наук
Пермь-2009
Диссертационная работа выполнена в ГОУ ВПО «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию»
Научный руководитель : доктор фармацевтических наук, профессор
Одегова Татьяна Федоровна
Научный консультант : доктор химических наук, профессор
Шкляев Юрий Владимирович,
Институт технической химии УрО РАН, г. Пермь
Официальные оппоненты : доктор фармацевтических наук, профессор
Куклин Владимир Николаевич,
ГОУ ВПО «Санкт-Петербургская государственная
химико-фармацевтическая академия Федерального
агентства по здравоохранению и социальному развитию»
доктор химических наук, профессор
Гейн Владимир Леонидович,
ГОУ ВПО «Пермская государственная фармацевтическая
академия Федерального агентства по здравоохранению и
социальному развитию»
Ведущая организация: ГОУ ВПО «Пятигорская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию»
Защита диссертационной работы состоится «22» декабря 2009 г. в 1300 час. на заседании диссертационного совета Д 208.068.01 при ГОУ ВПО «Пермская государственная фармацевтическая академия Федерального агентства по здравоохранению и социальному развитию» по адресу : 614990, г. Пермь, ГСП-277, ул. Ленина, 48.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО «Пермская госу-дарственная фармацевтическая академия Федерального агентства по здравоохра-нению и социальному развитию» по адресу : 614070, г. Пермь, ул. Крупской, 46.
Дата размещения объявления о защите диссертации на сайте ПГФА
http://www.pfa.ru « 20 » ноября 2009 г.
Автореферат разослан « » ноября 2009 г.
Ученый секретарь диссертационного
совета, кандидат фармацевтических наук И.А. Липатникова
Общая характеристика работы
Актуальность темы
Важнейшей задачей фармацевтической науки является поиск, изучение и внедрение в клиническую практику относительно безвредных препаратов с высокой биологической активностью. Весьма актуален поиск новых противомик-робных соединений, что связано с лидирующим положением инфекционных забо-леваний среди причин нетрудоспособности, инвалидности и преждевременной смертности на Земле. Анализ литературы показывает, что применяемые в медицин-ской практике антибиотические, антисептические и дезинфицирующие средства со временем теряют свою терапевтическую ценность, что обусловлено формирова-нием микроорганизмами резистентных форм. Открытие новых видов возбудителей с неустановленной устойчивостью к современным препаратам, а также прецеденты биотерроризма повышают потребности здравоохранения в эффективных, более совершенных, экологически безопасных и экономически выгодных биоцидных средствах.
Поиск новых соединений, обладающих антимикробным действием, ведется по нескольким направлениям, одним из которых является целенаправленный синтез химических веществ с заданными биологическими свойствами. Имеющиеся в научной литературе сведения позволяют сделать вывод, что поиск потен-циальных противомикробных средств следует вести среди рядов антраниловой и ацилпировиноградных кислот, производных пиридина. Высокая реакционная спо-собность и широкий круг химических превращений производных ацилпирови-ноградных кислот дают возможность использовать их для конструирования разно-образных нециклических и гетероциклических систем, которые обладают противо-микробным, противоопухолевым, противовоспалительным и другими видами действия при низкой токсичности. Многообразие гетероциклических систем позво-ляет синтезировать соединения с широким спектром фармакологической актив-ности. В частности, производные пиридина обладают противотуберкулезным, ноотропным, гипотензивным, бактерицидным и другими действиями. Кватер-низованные соли пиридина нашли практическое применение в качестве кожных антисептиков. Таким образом, производные данных классов химических веществ перспективны для поиска новых противомикробных средств, а оценка их биологической активности является актуальной.
Цель и задачи исследования
Целью настоящей работы является поиск соединений с противомикробным действием среди производных антраниловой кислоты, полиоксосоединений : 2-ариламино-1,4-диарил-2-бутен-1,4-дионов и производных ацилпировиноградных кислот, гетероциклических азотсодержащих соединений и отбор активных ве-ществ, перспективных для внедрения в медицинскую практику в качестве лекарст-венных средств.
Для достижения поставленной цели были сформулированы следующие задачи:
1. Провести скрининговые исследования новых производных антраниловой и ацилпировиноградных кислот, гетероциклических азотсодержащих соединений по отношению к штаммам грамположительных кокков Staphylococcus aureus АТСС 6538-Р и грамотрицательных палочек Escherichia coli АТСС 25922 на наличие среди них веществ, обладающих противомикробной активностью.
2. Выявить наиболее активные соединения для дальнейших исследований.
3. Определить спектр противомикробного действия активных соединений по отношению к другим тест-штаммам микроорганизмов, как к музейным (Staphylococcus epidermidis АТСС 14990, Bacillus subtilis АТСС 6633, Bacillus cereus АТСС 8035, Pseudomonas aeruginosa АТСС 9027, Candida albicans АТСС 24433), так и к клиническим резистентным штаммам. Оценить острую токсичность актив-ных соединений.
4. Установить качественную зависимость противомикробной активности соединений от химической структуры, параметров квантово-химического расчета.
Научная новизна
Впервые изучено противомикробное действие 270 неописанных ранее в ли-тературе производных антраниловой и ацилпировиноградных кислот, гетеро-циклических азотсодержащих соединений по отношению к тест-штаммам - S. aureus АТСС 6538-Р, E. сoli АТСС 25922. Проведенный анализ результатов скри-нинга позволил выявить 32 соединения, обладающие умеренной и высокой проти-вомикробной активностью по отношению к грамположительному микроорга-низму, и 27 веществ – по отношению к грамотрицательному. Проведены углуб-ленные исследования 9 активных соединений, не уступающих по силе действия известным препаратам, по отношению к грамположительным коагулазонегативным коккам, аэробным грамотрицательным неферментирующим палочкам, споро-образующим грамположительным палочкам рода Bacillus, грибам рода Candida. Показана перспективность поиска соединений с выраженным противомикробным действием среди рядов амидов ацилпировиноградной кислоты, монокватерни-зованных 1,2-ди-3(4)-пиридилэтиленов.
Установлена некоторая связь химической структуры изученных веществ с данным видом активности. Впервые проведен расчет величины дипольного момента молекул 40 соединений.
Практическая значимость
Обнаружено, что перспективными для дальнейшего изучения являются енаминопроизводные ацилпировиноградных кислот и их амиды и монокватер-низованные 1,2-ди-3(4)-пиридилэтилены, обладающие противомикробной актив-ностью. Они имеют потенциальную возможность использования в практической медицине. Среди производных данных рядов отобраны 9 соединений, которые по степени выраженности бактериостатического эффекта в отношении тест-штаммов S. aureus и E. сoli превосходят препараты сравнения. Установлен спектр противо-микробного действия и класс опасности данных веществ. По результатам углуб-ленных исследований два соединения : N-(2,4,6-триметилфенил)амид 2-(-N,N-диэтиламиноэтиламино)-4-оксо-4-(4-хлорфенил)-2-бутеновой кислоты и хлорид 1-[N-цетил-4-пиридиний]-2-(4-пиридил)этилена рекомендованы для проведения доклинических испытаний с целью внедрения в медицинскую практику в качестве лекарственных средств. Результаты научных исследований внедрены в научно-исследовательский процесс кафедр фармацевтической технологии, органической химии ГОУ ВПО «ПГФА Росздрава», кафедры общей и биоорганической химии ГОУ ВПО «ПГМА Росздрава».
Апробация работы. Результаты исследований докладывались на конфе-ренциях и конгрессах различного уровня : межвузовской научно-практической конференции «Вузы и регион» (Пермь, 2003), Российской научно-практической конференции «Рациональное использование лекарств» (Пермь, 2004), Всероссий-ской научно-практической конференции «Разработка, исследование и маркетинг новой фармацевтической продукции», (Пятигорск, 2005), XIV Российском нацио-нальном конгрессе «Человек и лекарство» (Москва,2007), международной научно-практической конференции «Здоровье и образование», (Палермо - Пермь, 2007), региональной конференции молодых ученых с международным участием «Совре-менные проблемы экологии, микробиологии и иммунологии» (Екатеринбург-Пермь, 2007), российской научно-практической конференции, посвященной 70-летию ПГФА «Достижения и перспективы в области создания новых лекарст-венных средств» (Пермь, 2007), международной конференции «Техническая химия. От теории к практике» (Пермь, 2008), научно-практической конференции «Совре-менное состояние и пути оптимизации лекарственного обеспечения населения» (Пермь, 2008).
Публикации. По материалам диссертационной работы опубликовано 12 на-учных работ : 1 статья в издании, рекомендуемом ВАК, 6 статей и 5 тезисов докла-дов конференций различного уровня. Подана 1 заявка на выдачу патента РФ.
Связь задач исследования с проблемным планом фармацевтических наук. Диссертационная работа выполнена в соответствии с планом научных ис-следований Пермской государственной фармацевтической академии Федерального агентства по здравоохранению и социальному развитию (номер государственной регистрации 01.9.10018875).
Объем и структура диссертации. Содержание работы изложено на 147 страницах машинописного текста и состоит из введения, четырех глав, выводов, списка литературы, приложения. Содержит 35 таблиц и 5 рисунков. Библиография включает 155 источников отечественных и зарубежных авторов.
В первой главе (обзор литературы) освещена проблема резистентности микро-организмов к противомикробным средствам. Обобщены данные о поиске новых соединений, обладающих противомикробной и другими видами активности, среди производных антраниловой кислоты, полиоксосоединений и гетероциклических азотсодержащих соединений. Рассмотрены подходы изучения количественных соотношений «структура–активность» в данных рядах.
Во второй главе описываются объекты и методы, использованные в работе.
В третьей главе представлены результаты скрининговых исследований соеди-нений указанных рядов, и рассмотрена связь «структура–противомикробная ак-тивность».
Глава 4 посвящена углубленному изучению широты спектра противомикроб-ного действия активных соединений.
В приложение включены акты внедрения научных исследований.
На защиту выносятся
1. Результаты микробиологических испытаний производных антраниловой, ацилпировиноградных кислот, гетероциклических азотсодержащих соединений, которые выявили 9 соединений, обладающих выраженной противомикробной ак-тивностью в отношении грамположительных и грамотрицательных микроор-ганизмов.
2. Закономерности качественной зависимости противомикробного действия иссле-дованных соединений от их химической структуры.
3. Рекомендации для углубленных доклинических испытаний двух перспективных соединений : N-(2,4,6-триметилфенил)амида 2-(-N,N-диэтиламиноэтиламино)-4-оксо-4-(4-хлорфенил)-2-бутеновой кислоты и хлорида 1-[N-цетил-4-пиридиний]-2-(4-пиридил)этилена, не уступающих препаратам сравнения по степени выра-женности антибактериальной и противогрибковой активности.
Основное содержание диссертации
Анализ противомикробной активности изученных соединений
Исследована противомикробная активность (ПМА) 270 соединений, синте-зированных сотрудниками ПГФА на кафедрах органической химии, физической и коллоидной химии, фармацевтической химии очного факультета; в лаборатории медицинской химии Научно-образовательного центра ПГФА, в лаборатории «Окислительного катализа в расплавленных электролитах» Института технической химии УрО РАН, г. Пермь.
Изучение бактериостатического действия по отношению к тест-штаммам микроорганизмов проведено стандартным методом серийных разведений в жидкой питательной среде. Критерием отбора соединений для углублённого изучения являются значения минимальных подавляющих концентраций (МПК) ис-пользуемых в настоящее время и аналогичных по антимикробному эффекту препа-ратов. В качестве препаратов сравнения использованы диоксидин, хлоргексидин, флуконазол.
Изученные соединения по химическому строению распределены на 18 рядов и объединены по базовой структуре на 6 групп (таблица 1).
Таблица 1
Результаты скрининга противомикробной активности соединений
| Объекты изучения | Общая формула | Кол-во изучен-ных соеди-нений | Кол-во активных соединений | |||
| с низкой ПМА, (%) по отнош. к S. aureus и E. coli | с умерен-ной ПМА, (%) по отнош. к S. aur. и E. coli | с высокой ПМА, (%) по отнош. к S. aureus, E. coli | ||||
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 1. Производные 5-галогенантраниловой кислоты | 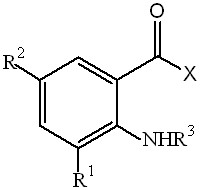 | 26 | 13 (50,0)/ 10 (38,5) | 2 (7,7)/ 2 (7,7) | 0 | |
| 2. 2-Ариламино-1,4-диарил-2-бутен-1,4-дионы | 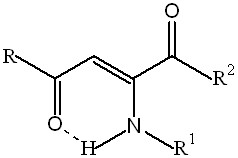 | 7 | 6 (85,7)/ 6 (85,7) | 0 | 1 (14,3)/ 1 (14,3) | |
| 3. Производные ацилпировиноградных кислот | 144 | 117 (81)/ 114 (79) | 13 (9,0)/ 14 (9,7) | 5 (3,4)/ 2 (1,4) | ||
| 3.1. 4-арил-2-гидрокси-4-оксо-2-бутеноаты гетериламмония | 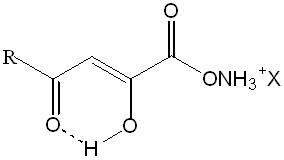 | 22 | 22 (100)/ 22 (100) | 0 | 0 | |
| 3.2. Енамино- и енгидразинопроизвод-ные ацилпировино-градных кислот | 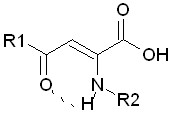 | 40 | 27 (67,5)/ 25 (62,5) | 7 (17,5)/ 6 (15,0) | 1 (2,5)/ 1 (2,5) | |
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 3.3. Енамино-производные метиловых эфиров ацилпировиноградных кислот | 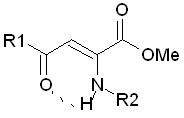 | 33 | 32 (97,0)/ 32 (97,0) | 1 (3,0)/ 1 (3,0) | 0 | |
| 3.4. Хелатные соли гетериламидов ацилпировиноградных кислот с ионами металлов | 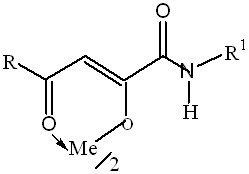 | 5 | 2 (40,0)/ 2 (40,0) | 2 (40,0)/ 2 (40,0) | 0 | |
| 3.5. Енаминоамиды ацилпировиноградных кислот | 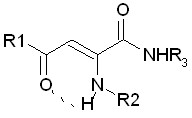 | 40 | 31 (77,5)/ 31 (77,5) | 3 (7,5)/ 5 (12,5) | 4 (10,0)/ 1 (2,5) | |
| 3.6. Енамино- и енгидразиногидразиды ацилпировиноградных кислот | 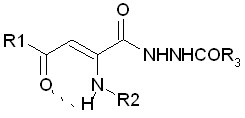 | 4 | 3 (75,0)/ 2 (50,0) | 0 | 0 | |
| 4. Гетероциклы с одним атомом азота | 64 | 51 (79,7)/ 39 (59,3) | 3 (5,1)/ 2 (3,4) | 2 (3,4)/ 2 (3,4) | ||
| 4.1. 1-Арил-4-ацил-3,5-дигидрокси-5-метокси-карбонил-2,5-дигидро-пиррол-2-оны | 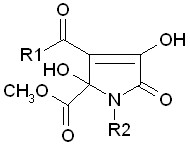 | 19 | 18 (94,7)/ 13 (68,4) | 0 | 0 | |
| 4.2. 5-Арил-4-ацил-1-гетерилэтил-3-гидрок-си-3-пирролин-2-оны | 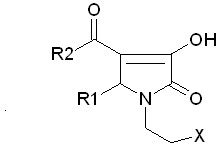 | 22 | 19 (86,4)/ 15 (68,2) | 0 | 0 | |
| 4.3. Моно- и диква-тернизованные производные 1,2-ди-3(4)-пиридилэта-нов(этиленов) | 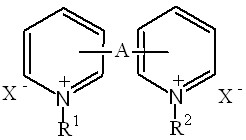 | 9 | 2 (22,2)/ 2 (22,2) | 2 (22,2)/ 2 (22,2) | 2 (22,2)/ 2 (22,2) | |
| 4.4. Производные изоиндоло-2,3,4-три-гидрохинолина | 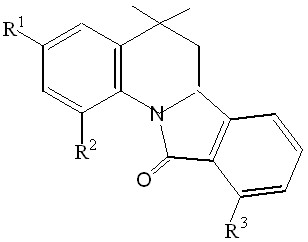 | 14 | 12 (85,7)/ 9 (64,3) | 1 (7,1)/ 0 | 0 | |
| 5. Гетероциклы с двумя гетероатомами | 25 | 18 (72,0)/ 16 (64,0) | 4 (16,0)/ 2 (8,0) | 1 (4,0)/ 1 (4,0) | ||
| 5.1. Производные 6-нитробензимидазола | 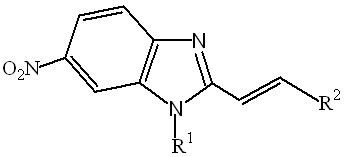 | 10 | 8 (80,0)/ 6 (60,0) | 0/ 1 (10,0) | 0/ 1 (10,0) | |
| 5.2. Производные 3-замещенных 3,4-дигидро-2Н-1,4-бензоксазин-2-онов и 3,4-дигидро-2Н-1,4-бензотиазин-2-онов | 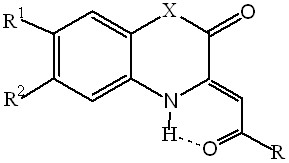 | 15 | 10 (66,6)/ 10 (66,6) | 4 (26,7)/ 1 (6,7) | 1 (6,7)/ 0 | |
| 1 | 2 | 3 | 4 | 5 | 6 | |
| 6. Гетероциклы с тремя атомами азота | 4 | 3 (75,0)/ 3 (75,0) | 1 (25,0)/ 1 (25,0) | 0 | ||
| 6.1. Производные 5-гетерилэтилпирро-ло[3,4-с]пиразола | 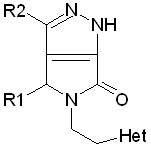 | 4 | 3 (75,0)/ 3 (75,0) | 1 (25,0)/ 1 (25,0) | 0 | |
| Всего : 6 групп, 18 рядов | 270 | 208 (77)/ 188 (69) | 23 (8,5)/ 21(7,7) | 9 (3,3)/ 6 (2,2) | ||
Результаты скрининговых исследований представлены в таблице 1, из которой видно, что из общего количества соединений 240 угнетают в той или иной степени рост S. аureus, что составляет 88,8 %. Не оказывают влияния на данный микроорганизм 30 (11,2 %) соединений. По отношению к E. сoli эти показатели составляют 215 (79,6 %) и 55 (20,4 %) веществ соответственно. Малоактивны (МПК находится в интервале 1000-125 мкг/мл) в отношении грамположительного микроорганизма 208 и в отношении грамотрицательного - 188 соединений, что со-ставляет 77% и 69% соответственно. Умеренно активны (МПК находится в диапа-зоне 62,5-15,6 мкг/мл) по отношению к S. aureus 23 соединения (8,5%) и по отно-шению к E. сoli - 21 соединение (7,7%). Высокую ПМА (МПК составляет 7,8 мкг/мл и менее) в отношении S. aureus проявляют 9 соединений (3,3%) и в отноше-нии E. coli - 6 соединений (2,2%).
Оценка полученных результатов показывает, что наибольшее количество активных веществ из всех групп содержат вторая и пятая, что составляет 14,3% и 4% соответственно. Несколько меньший процент активных соединений (3,4% веществ в группе) имеют третья и четвертая группы. Наибольший вклад в этот показатель вносят ряды 2-ариламино-1,4-диарил-2-бутен-1,4-дионов (соединение 2ё), енаминопроизводных ацилпировиноградных кислот (АПК) и их амидов (соединения 4ё, 8аг-8аё), монокватернизованных 1,2-ди-3(4)-пиридилэтиленов (соединения 13ж и 13д), 3,4-дигидро-2Н-1,4-бензоксазин-2-онов (соединение 16г). Таким образом, активные соединения из указанных рядов можно рассматривать в качестве потенциальных противомикробных средств, в связи с чем они исследова-ны более подробно.
Изучение зависимости противомикробного действия
исследованных соединений от их структуры
Установление связи биологической активности веществ с их строением является актуальным как для теоретических основ органической химии, так и для конструирования лекарственных средств, обладающих высокой эффективностью и избирательностью действия. Известно, что на проявление химическим веществом биологического действия оказывают влияние фармакофорные группы в молекуле, стерические особенности структуры, электронные эффекты, влияющие на иони-зацию и полярность молекулы. Основную роль при взаимодействии химического вещества с рецептором играют ван-дер-ваальсовы силы, а также электростатиче-ское притяжение противоположно заряженных ионогенных групп, водородные связи и гидрофобные взаимодействия. Гидрофобность связана с полярностью молекулы и пространственным распределением заряда. Мерой распределения зарядов в молекуле является дипольный момент.
Для поиска зависимости «структура-активность» нами проведен квантово-химический расчет молекул. Методом АМ1 с полной оптимизацией геометрии мо-лекулы по программе HyperChem 7.0 исследованы сорок соединений, принадле-жащих к производным 5-галогенантраниловой кислоты, ацилпировиноградных кислот, гетероциклических соединений с двумя и тремя гетероатомами. Выбор соединений в каждом ряду определен наибольшими и наименьшими значениями МПК, найденными при скрининге по отношению к тест-штаммам S. aureus и E. сoli. В ходе изучения связи «структура-активность» нами установлено влияние дипольного момента молекул (µ) на проявление данными соединениями бакте-риостатического действия. Предположение о линейной связи между lg 1/МПК и дипольным моментом проверено расчетом коэффициента корреляции (r).
Исследование активности в рядах производных антраниловой кислоты, полиоксосоединений и гетероциклических азотсодержащих соединений позволило выявить некоторые закономерности связи их структуры с противомикробным действием.
В ряду амидов 5-галогенантраниловой кислоты обнаружено, что наличие га-логена (Br или J) в 5-м положении бензольного кольца не оказывает влияние на бактериостатическое действие. Как видно из таблицы 2, амиды 5-бромантрани-ловых кислот с незамещенной аминогруппой (1б, 1д, 1ж) в большей степени угне-тают рост обоих тест-штаммов, чем амиды N-замещенных 5-галогенантраниловых кислот, исследованных и описанных в литературе ранее, и в случае соединений 1о, 1у. Наиболее активен изопропиламид 5-бромантраниловой кислоты (1д), что мож-но объяснить стерическим ограничением свободного вращения связи и, как следст-вие, более прочным взаимодействием функциональной группы с рецептором.
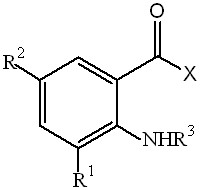
Таблица 2
Противомикробная активность и величина дипольного момента производных
амидов 5-бром(йод)антраниловой кислоты
| № | Шифр | R1 | R2 | R3 | Х | МПК, мкг/мл | µ, Д | |
| S. aureus | E. coli | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| 1б | КЛГ-516 | 1000 | н/а | 4,725 | ||||
| 1д | КЛГ-519 | 31 | 15,6 | 7,785 | ||||
| 1ж | КЛГ-523 | 62 | 62 | 5,331 | ||||
| 1о | КЛГ-511 | н/а | н/а | -* | ||||
| 1у | КЛВ-624 | н/а | н/а | 2,495 | ||||
| Диоксидин | 62-1000 | 3,9-62 | ||||||
| r | 0,79 | 0,99 | ||||||
* - расчеты не проводили
Квантово-химический расчет молекул в данном ряду показывает, что ПМА проявляется только для соединений 1б, 1д, 1ж, углы отклонения плоскости моле-кулы которых мало отличаются от 180°. Приведенные в таблице 2 результаты расчета показывают, что с возрастанием дипольного момента с 4,725 Д до 7,785 Д противомикробное действие усиливается в 64 раза.
Среди 2-ариламино-1,4-диарил-2-бутен-1,4-дионов нами установлено, что су-щественное влияние на проявление ПМА оказывает сочетание п-толильных замес-тителей в 1-м и 4-м положениях молекулы с 2,4-дихлорфенильным радикалом во
2-м положении (соединение 2ё) (таблица 3).
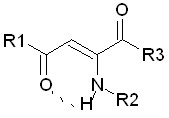
Таблица 3
Противомикробная активность 2-ариламино-1,4-диарил-2-бутен-1,4-дионов
| № | Шифр | R1 | R2 | R3 | МПК, мкг/мл | |
| S. aureus | E. coli | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 2г | НОЦ-147 | 2-Br-3,4-(СН3)2С6Н2 | 250 | 250 | ||
| 2д | НОЦ-141 | 125 | 125 | |||
| 2е | НОЦ-110 | 4-СН3С6Н4 | 4-СН3С6Н4 | 1000 | 1000 | |
| 2ё | НОЦ-109 | 4-СН3С6Н4 | 2,4-Cl2С6Н3 | 4-СН3С6Н4 | 2,0 | 2,0 |
| Диоксидин | 62-1000 | 3,9-62 | ||||
Среди производных ацилпировиноградных кислот наибольшее количество активных соединений выявлено в рядах енаминопроизводных АПК и их амидов (таблица 1).
Результаты проведенных нами исследований (таблица 4) показывают, что на проявление ПМА в ряду енаминопроизводных АПК влияет заместитель в енами-ногруппе : наличие тимольного радикала приводит к увеличению активности по отношению к тест-штаммам от 32 до 128 раз (соединения 4ё-л). Среди енгидразинопроизводных арилпировиноградных кислот наиболее активны соеди-нения 5р и 5с, содержащие в енгидразинной группе о-гидроксифенилкарбонильный фрагмент.
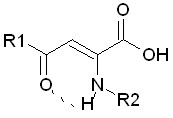
Таблица 4
Противомикробная активность и величина дипольного момента
енамино- и енгидразинопроизводных ацилпировиноградных кислот
| № | Шифр | R1 | R2 | МПК, мкг/мл | µ, Д | |
| S. aureus | E. coli | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 4в | И-13 | 1000 | 1000 | 4,103 | ||
| 4ё | И-119 | 3,9 | 3,9 | 6,950 | ||
| 4ж | И-149 | 31 | 15,6 | 4,414 | ||
| 4з | И-121 | 4-СН3С6Н4 | 15,6 | 15,6 | -* | |
| 4и | И-151 | 15,6 | 15,6 | -* | ||
| 4к | И-150 | 31 | 31 | -* | ||
| 4л | И-120 | 31 | 31 | -* | ||
| 5п | И-92 | 250 | 250 | -* | ||
| 5р | И-142 | 62 | 62 | -* | ||
| 5с | И-112 | 15,6 | 125 | 6,176 | ||
| 5ц | И-15 | 1000 | 1000 | 3,350 | ||
| Диоксидин | 62-1000 | 3,9-62 | ||||
| r | 0,88 | 0,69 | ||||
* - расчеты не проводили
Квантово-химический расчет соединений 4в, 4ё, 4ж, 5с, 5ц обнаружил неплоское строение молекул. Однако прослеживается аналогичная производным 5-галогенантраниловой кислоты зависимость активности от величины дипольного момента : наиболее активно соединение 4ё, для которого дипольный момент равен 6,950 Д (таблица 4).
Впервые проведенные исследования ПМА в ряду метиловых эфиров 4-арил-2-ариламино-4-оксо-2-бутеновых кислот (таблица 5) выявили одно соединение (6а), обладающее бактериостатическим действием по отношению к S. aureus, E. сoli на уровне диоксидина, что обусловлено сочетанием двух фенильных радикалов во 2-м и 4-м положениях молекулы. Наблюдается уменьшение активности в 2 раза соединений 6е, 6з, имеющих в енаминогруппе 4-хлор(фтор)фенильный радикал. Замена арильного заместителя R1 на гетерильный (6п, 6р) не влияет на проявление активности.
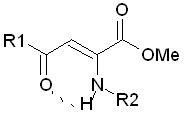
Таблица 5
Противомикробная активность и величина дипольного момента
енаминопроизводных метиловых эфиров ацилпировиноградных кислот
| № соед. | Шифр | R1 | R2 | МПК, мкг/мл | µ, Д | |
| S. aureus | E. coli | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 6а | НОЦ-119 | 62 | 62 | 5,531 | ||
| 6е | НОЦ-132 | 125 | 125 | 3,700 | ||
| 6з | НОЦ-120 | 4-С2Н5ОС6Н4 | 4-BrС6Н4 | 125 | 125 | -* |
| 6п | НОЦ-104 | -фурил | 4-BrС6Н4 | 500 | 1000 | -* |
| 6р | НОЦ-117 | -тиенил | | 1000 | 1000 | 3,730 |
| 6ш | НОЦ-111 | 3-СF3С6Н4 | 1000 | 1000 | 2,599 | |
| Диоксидин | 62-1000 | 3,9-62 | ||||
| r | 0,80 | 0,80 | ||||
* - расчеты не проводили
Данные квантово-химического расчета молекул в ряду метиловых эфиров 4-арил-2-ариламино-4-оксо-2-бутеновых кислот свидетельствуют, что соединения, имеющие плоское строение, малоактивны (6р, 6ш), а соединения, в которых плоскости ароматических колец расположены под некоторым углом (6а, 6е), проявляют более высокую ПМА. При этом с увеличением дипольного момента с 3,700 Д до 5,531 Д, соответственно, ПМА усиливается в 2 раза (таблица 5).
Среди комплексных солей гетериламидов АПК с ионами металлов установ-лено влияние на рост тест-штаммов S. аureus и E. сoli хелатов магния и марганца (II), которые обладают бактериостатическим действием на уровне диоксидина. Как следует из таблицы 6, проявлению ПМА способствует наличие тиазольного цикла в амидной группе молекул соединений 7а-7г. Полученные нами результаты согласуются с выявленной ранее и описанной в литературе связью ПМА металлохелатов гетериламидов АПК с характером гетероцикла.
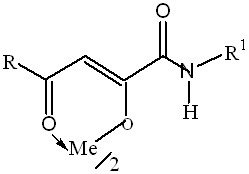
Таблица 6
Противомикробная активность хелатных солей гетериламидов
ацилпировиноградных кислот с ионами металлов
| № соед. | Шифр | R | Ме | R1 | МПК, мкг/мл | |
| S. aureus | E. coli | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 7а | ФС-11 | Mg | 62 | 62 | ||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 7б | ФС-28 | Mg | 250 | 500 | ||
| 7в | ФС-29 | Mn | 62 | 62 | ||
| 7г | ФС-30 | Co | н/а | н/а | ||
| 7д | ФС-181 | Cd | 1000 | 1000 | ||
| Диоксидин | 62-1000 | 3,9-62 | ||||
Представленные в таблице 7 данные по скринингу производных енамино-амидов 4-арил-2-енамино-4-оксо-2-бутеновых кислот (соединения 8аб-8аё) пока-зывают, что исследованные вещества превосходят по активности препарат сравнения. Установлено, что бактериостатическое действие указанных соединений обусловлено наличием N,N-диэтиламиноэтильного заместителя в енаминогруппе и фрагментов тимола, 2,6-ксилидина, мезитилена в амидном звене молекулы АПК (соединения 8аг-8аё), что, в свою очередь, делает их более активными, чем опи-санные ранее ариламиды бензоилпировиноградной кислоты. Нами впервые изучена противомикробная активность замещенных амидов 2-(2(4)-бром(хлор)фенилами-но)-5,5-диметил-4-оксо-2-гексеновых кислот. Обнаружено, что бактериостатиче-ское действие зависит от природы галогена в фениламиногруппе во 2-м положении углеродной цепи : более выраженную ПМА имеют соединения 8ы, 8ю с 2,4-ди-хлорфенильным радикалом в отличие от 2- и 4(2,4)-бром(дибром)фениламино-производных (8б, 8л, 8н, 8т, 8у).
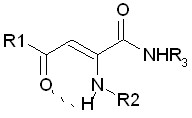
Таблица 7
Противомикробная активность и величина дипольного момента
енаминопроизводных амидов ацилпировиноградных кислот
| № | Шифр | R1 | R2 | R3 | МПК, мкг/мл | µ, Д | |
| S. aur. | E. coli | ||||||
| 8б | И-243 | 2-BrС6Н4 | 2-JС6Н4 | 1000 | 1000 | 7,238 | |
| 8л | И-175 | 4-BrС6Н4 | 4-О2NС6Н4 | 1000 | 1000 | -* | |
| 8н | И-174 | 4-BrС6Н4 | 500 | 500 | -* | ||
| 8т | И-220 | 4-BrС6Н4 | 1000 | 1000 | 7,419 | ||
| 8у | И-222 | 4-С2Н5ОСОС6Н4 | 1000 | 1000 | -* | ||
| 8ы | И-241 | 2-СН3-5-О2NС6Н3 | 15,6 | 15,6 | 5,717 | ||
| 8ю | И-240 | 125 | 250 | -* | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 8я | И-223 | 500 | 500 | 5,726 | |||
| 8аб | И-211 | 4-СН3С6Н4 | 2,6-(CH3)2C6H3 | 15,6 | 31 | 11,500 | |
| 8ав | И-212 | 2,6-(CH3)2C6H3 | 31 | 62 | 13,320 | ||
| 8аг | И-213 | 2,6-(CH3)2C6H3 | 7,8 | 15,6 | 13,910 | ||
| 8ад | И-214 | 2,4,6-(CH3)3C6H2 | 3,9-7,8 | 3,9-1000 | 14,120 | ||
| 8ае | И-251 | 4-СН3С6Н4 | 7,8 | 15,6 | -* | ||
| 8аё | И-249 | 3,9 | 7,8 | -* | |||
| Диоксидин | 62-1000 | 3,9-62 | |||||
| r | 0,71 | 0,59 | |||||
* - расчеты не проводили
Квантово-химический расчет молекул в ряду енаминопроизводных амидов АПК показывает неплоское строение молекул соединений 8б-8ад. Наиболее активно вещество 8ад, имеющее дипольный момент 14,120 Д и в пространственном строении угол между кольцами заместителей R1 и R2 в пределах 120° (таблица 7). В случае енаминопроизводных амидов АПК, имеющих третичный бутильный ради-кал в 4-м положении молекулы (8б, 8т, 8ы, 8я), картина меняется на противо-положную : противомикробная активность усиливается при уменьшении величины дипольного момента молекул соответственно от 7,419 Д до 5,717 Д. Вероятно, такая зависимость обусловлена разными механизмами бактериостатического действия на стенку микробной клетки ароматических и трет-бутильных енамино-производных амидов АПК.
Таким образом, результаты скрининговых исследований среди производных ацилпировиноградных кислот показывают, что наиболее активными по отношению к тест-штаммам S. aureus, E. сoli являются амиды 4-арил-2-енамино-4-оксо-2-бутеновых кислот, не уступающие активности препарата сравнения – диоксидина. Противомикробное действие исследовавнных соединений обусловлено наличием N,N-диэтиламиноэтильного заместителя в енаминогруппе и фрагментов тимола, 2,6-ксилидина, мезитилена в амидном звене молекулы. Превосходит действие диоксидина в отношении обоих тест-штаммов и 5,5-диметил-2-[N-(4'-гидрокси-2'-изопропил-5'-метилфенил)амино]-4-оксо-2-гексеновая кислота. По-видимому, ме-тильные группы, расположенные в заместителях при С2 и С4 атомах молекулы и в амидном звене 4-арил-2-енамино-4-оксо-2-бутеновых кислот, и образование внут-римолекулярной водородной связи между атомом водорода аминогруппы и атомом кислорода оксогруппы в 4-м положении молекулы способствуют более прочному взаимодействию функциональных групп данных соединений со стенкой микроб-ной клетки. Полученные нами результаты в целом согласуются с проведенными ранее исследованиями и свидетельствуют о перспективности поиска противомик-робных соединений среди производных ацилпировиноградных кислот.
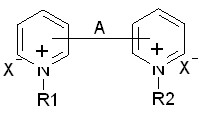
В группе гетероциклических соединений с одним атомом азота производные 1-, 4-, 5-замещенных 3-гидрокси-3-пиррол-2-онов обладают слабым бактериостати-ческим действием. Соединения, проявляющие выраженную ПМА, содержат ряды моно- и дикватернизованных производных 1,2-ди-3(4)-пиридилэтанов и 1,2-ди-3(4)-пиридилэтиленов (таблица 1). Результаты скрининговых исследований в дан-ных рядах представлены в таблице 8.
 цис-форма
цис-форма
Таблица 8
Противомикробная активность кватернизованных производных 1,2-ди-3(4)-пиридилэтанов и 1,2-ди-3(4)-пиридилэтиленов
| № соед | Шифр | R1 | R2 | А | Поло- жение кольца | Х | МПК, мкг/мл | |
| S. aureus | E. coli | |||||||
| 13а | Ч-124 | С12Н25 | - | СН2СН2 | 3 | Br | 15,6 | 15,6 |
| 13в | Н-15 | С16Н33 | С16Н33 | СН2СН2 | 3 | Cl | н/а | н/а |
| 13г | Н-8 | С12Н25 | - | СН=СН | 3 | Br | н/а | 1000 |
| 13д | Н-11 | С16Н33 | - | СН=СН | 3 | Cl | 3,9 | 7,8 |
| 13ё | Ч-121 | С12Н25 | - | СН=СН | 4 | Br | 15,6 | 15,6 |
| 13ж | Ч-34 | С16Н33 | - | СН=СН | 4 | Cl | 0,5 | 0,5 |
| 13з | Ч-54 | СН2=СНСН2 | СН2=СНСН2 | СН=СН | 4 | Br | 500 | 500 |
| Диоксидин | 62-1000 | 3,9-62 | ||||||
Обнаружено, что природа аниона солей не влияет на проявление ПМА. Монокватернизованные производные 1,2-ди-3(4)-пиридилэтанов(этиленов) в боль-шей степени угнетают рост тест-штаммов, чем дикватернизованные. Повышает активность наличие двойной связи в мостике, соединяющем пиридиновые циклы : наиболее активны 1,2-ди-3(4)-пиридилэтилены (13д-13ж). Кроме того, бактерио-статическое действие зависит от длины углеродной цепи алкильного радикала у атома азота : максимальную активность проявляют соединения, содержащие 12-16 атомов углерода в радикале (13а, 13д, 13ё, 13ж), что согласуется с результатами проведенных ранее исследований в рядах моно- и бисчетвертичных аммониевых солей. Таким образом, кватернизация одного пиридинового цикла алкильным заместителем, повышающим липофильность молекулы, способствует усилению противомикробного действия в отличие от описанных 2,4,6-замещенных фениль-ным радикалом солей N-N-алкиленбиспиридиния.
Среди гетероциклических соединений с двумя гетероатомами ряды произ-водных 3-замещенных 3,4-дигидро-2Н-1,4-бензоксазин-2-онов и 3,4-дигидро-2Н-1,4-бензотиазин-2-онов содержат соединения, обладающие выраженным бакте-риостатическим действием (таблица 1). Как показывают приведенные в таблице 9 данные наших исследований, в ряду 3-замещенных 3,4-дигидро-2Н-1,4-бензок-сазин-2-онов проявлению ПМА способствует наличие объемного -нафтильного фрагмента в 3-ем положении бензоксазинового цикла в отличие от менее активных 6-этилсульфонил-3-ацилметилен- и 3-ароилметилен-3,4-дигидро-2Н-1,4-бензокса-зин-2-онов, изученных и описанных ранее. Присутствие электроноакцепторной нитрогруппы в положениях 5 или 6 бензоксазина (соединения 16д-е) приводит к снижению бактериостатического действия. Уменьшение активности происходит при наличии в ацильном фрагменте бензоксазина арильного радикала (16б, 16в) или тиенильного и фурильного циклов (16ё, ж).
Представленные в таблице 9 результаты скрининга среди 3,4-дигидро-2Н-1,4-бензотиазин-2-онов выявили соединения 17а-б, 17д, угнетающие рост S. аureus на уровне диоксидина. Установлено, что наиболее активны соединения, имеющие фурильный (17д) и м-замещенный фенильный радикалы в положении 3 цикла бензотиазина (17а-б).
По результатам квантово-химического расчета молекул для 3-замещен-ных 3,4-дигидро-2Н-1,4-бензоксазин-2-онов сохраняется выявленная в других ря-дах соединений закономерность. Как видно из таблицы 9, для сравнимых по строению соединений 16б и 16в, 16д и 16е возрастание дипольного момента от 6,666 Д до 8,296 Д и от 3,732 Д до 6,710 Д соответственно приводит к усилению активности. Некоторое отличие соединения 16г объясняется отсутствием нитро-группы, положение которой существенно влияет на проявление действия. Однако, если сравнивать 16г и 16е, то связь ПМА с дипольным моментом молекул аналогична.
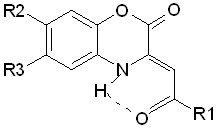
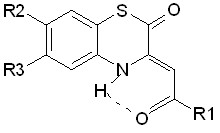
16б-ж 17а-д
Таблица 9
Противомикробная активность и величина дипольного момента производных
3,4-дигидро-2Н-1,4-бензоксазин-2-онов и 3,4-дигидро-2Н-1,4-бензотиазин-2-онов
| № соед | Шифр | R1 | R2 | R3 | МПК, мкг/мл | µ, Д | |
| S. aureus | E. coli | ||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 16б | СТД-4 | 3,4-(СН3О)2С6Н3 | 125 | 125 | 8,296 | ||
| 16в | СТД-2 | 3,4-(СН3О)2С6Н3 | 1000 | 1000 | 6,666 | ||
| 16г | И-100 | 7,8 | 31 | 5,760 | |||
| 16д | И-99 | 31 | 125 | 6,710 | |||
| 16е | И-98 | 250 | 250 | 3,732 | |||
| 16ё | СТД-6 | 125 | 1000 | -* | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 16ж | СТД-3 | 250 | 250 | -* | |||
| 17а | И-280 | 3-СН3ОС6Н4 | 62 | н/а | -* | ||
| 17б | И-281 | 3-BrС6Н4 | 62 | 1000 | -* | ||
| 17д | И-282 | 62 | 1000 | -* | |||
| Диоксидин | 62-1000 | 3,9-62 | |||||
| r | 0,22 | 0,21 | |||||
* - расчеты не проводили
В ряду производных 5-гетерилэтилпирроло[3,4-с]пиразола нами выявлено, что бактериостатическое действие указанных производных зависит от характера гетероцикла при атоме азота пиррольного кольца (таблица 10). Соединения 18а, 18в, содержащие 2-морфолилэтильный фрагмент, задерживают рост обоих тест-штаммов в концентрации 1000-125 мкг/мл. Замена морфолинового цикла на ин-дольный, реализованная в структуре 18г, приводит к усилению ПМА по отноше-нию к S. aureus и E. coli в 16 раз.
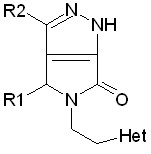
Таблица 10
Противомикробная активность и величина дипольного момента
производных 5-гетерилэтилпирроло[3,4-с]пиразола
| № соед | Шифр | R1 | R2 | Het | МПК, мкг/мл | µ, Д | |
| S. aureus | E. coli | ||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 18а | МС-44 | 1000 | 500 | 6,180 | |||
| 18в | МС-49 | 4-ClС6Н4 | 125 | 125 | 6,805 | ||
| 18г | МС-78 | 3-НОС6Н4 | 62 | 62 | 15,080 | ||
| Диоксидин | 62-1000 | 3,9-62 | |||||
| r | 0,74 | 0,79 | |||||
Проведенный квантово-химический расчет молекул соединений 18а, 18в, 18г показывает, что при увеличении дипольного момента с 6,180 Д до 15,080 Д бактериостатическое действие усиливается (таблица 10).
Таким образом, изучение качественной зависимости противомикробной ак-тивности соединений от их химической структуры позволило выявить следующие закономерности. Установлено, что в ряду замещенных амидов 4-арил-2-алкилами-но-4-оксо-2-бутеновых кислот значительное влияние на проявляемое действие оказывает сочетание диэтиламиноэтильного радикала в енаминогруппе и ароматических заместителей в амидном звене молекулы. В ряду ква-тернизованных 1,2-ди-3(4)-пиридилэтиленов противомикробная активность обус-ловлена одним ониевым центром в молекуле и определенным соотношением липо-фильных и липофобных частей их структуры. В ряду производных 3,4-дигидро-2Н-1,4-бензоксазин-2-онов наиболее выраженному проявлению бактериостатического действия способствует наличие в 3-ем положении бензоксазинового цикла объемного -нафтильного фрагмента.
Структура активных соединений представлена ниже.
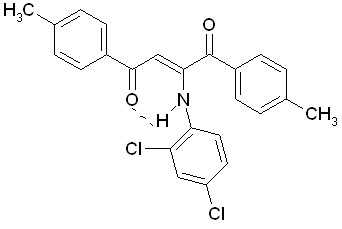
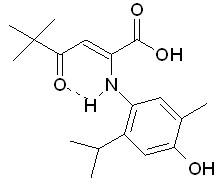
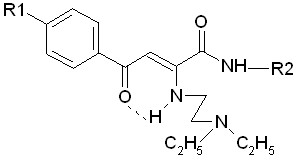
2ё 4ё 8 аг, ад, ае, аё
R1=Cl (8aг, 8aд, 8aё), СН3 (8ае)
R2= 2,6-(СН3)2С6Н3 (8aг), 2,4,6-(СН3)3С6Н2 (8aд), 4-НО-2-i-С3Н7-5-СН3С6Н2 (8aе, 8aё)
13д, 13ж 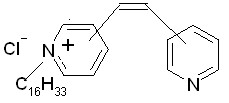 16г
16г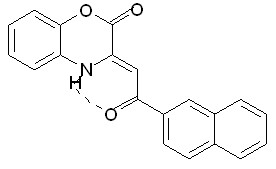
Анализ противомикробной активности исследованных соединений в рядах амидов 5-галогенантраниловой кислоты, эфиров и амидов АПК, гетероцикличе-ских азотсодержащих соединений и величин дипольных моментов молекул пока-зывает, что между ними имеется зависимость : с увеличением дипольного момента молекулы бактериостатическое действие изученных соединений усиливается, а для енаминопроизводных амидов ацилпировиноградных кислот, имеющих третичный бутильный радикал в 4-м положении молекулы, активность снижается. Установ-лено, что влияние дипольного момента молекул исследованных соединений на величину lg 1/МПК не имеет строго линейного характера. В целом, результаты наших исследований согласуются с данными других авторов о влиянии дипольного момента молекул химических веществ на их фармакологическую активность.
Исследования противомикробного действия активных соединений
Широта спектра противомикробного действия изучена по отношению к пяти музейным штаммам : S. epidermidis АТСС 14990, B. subtilis АТСС 6633, B. cereus АТСС 8035, P. aeruginosa АТСС 9027, C. albicans АТСС 24433 коллекции Всерос-сийского музея патогенных микроорганизмов. Как следует из полученных резуль-татов, представленных в таблице 11, более чувствительны к действию изученных соединений грамположительные микроорганизмы. Нами установлено, что наибо-лее активными в отношении грамположительных неспорообразующих бактерий являются : по отношению к S. aureus – все соединения (МПК составляет 0,5-7,8 мкг/мл); по отношению к S. epidermidis соответственно - 4ё, 8ад, 8ае, 13д, 13ж (МПК находится в диапазоне 2,0-7,8 мкг/мл). Тормозят рост грамположительных спорообразующих бактерий при МПК от 2,0 до 7,8 мкг/мл следующие субстанции : по отношению к B. cereus – 13д (МПК = 2,0-3,9 мкг/мл), 4ё, 8аё и 13ж (МПК составляет 3,9-7,8 мкг/мл), 8ад и 8ае (МПК = 7,8-15,6 мкг/мл); по отношению к B. subtilis – 13д (МПК 2,0-3,9 мкг/мл), 4ё (МПК = 3,9-7,8 мкг/мл), 8ад (МПК находится в интервале 7,8-15,6 мкг/мл). Наиболее активны по отношению к грамот-рицательному микроорганизму E. coli соединения 13ж (МПК составляет 0,5-2,0 мкг/мл), 2ё (МПК находится в диапазоне 2,0-3,9 мкг/мл), 4ё, 8аё и 13д (МПК составляет 7,8-15,6 мкг/мл). В отношении P. aeruginosa незначительную актив-ность проявляют соединения 8аё, 8ае, 13ж и 16г, что сравнимо с действием диоксидина. Рост C. albicans в концентрации 3,9-7,8 мкг/мл угнетают соединения 13д и 13ж. Более слабым противогрибковым действием обладают соединения 2ё и 8ад.
Таблица 11
Противомикробная активность соединений по отношению к музейным штаммам
| № | Шифр, ряд | МПК, мкг/мл | |||||||
| S. aureus | S. epid. | B. cereus | B. subtilis | E. coli | P. aerug. | C. albicans | |||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | |
| 1 | 2ё НОЦ109 | 2,0-3,9 | 125 | 31-62 | 250 | 2,0-3,9 | н/а | 31-62 | |
| 2 | 4ё И-119 | 3,9-7,8 | 3,9-7,8 | 3,9-7,8 | 3,9-7,8 | 3,9-7,8 | н/а | 500 | |
| 3 | 8аг И-213 | 7,8-15,6 | 15,6-31 | 15,6-31 | 31-62 | 15,6-31 | н/а | 500 | |
| 4 | 8ад И-214 | 3,9-15,6 | 3,9-1000 | 7,8-15,6 | 7,8-15,6 | 3,9-1000 | н/а | 62 | |
| 5 | 8аё И-249 | 3,9-7,8 | 15,6-31 | 3,9-7,8 | 15,6-31 | 7,8-15,6 | 1000 | н/а | |
| 6 | 8ае И-251 | 7,8-15,6 | 7,8-15,6 | 7,8-15,6 | 62 | 15,6-31 | 1000 | н/а | |
| 7 | 13д Н-11 | 3,9-7,8 | 2,0-3,9 | 2,0-3,9 | 2,0-3,9 | 7,8-15,6 | н/а | 3,9-7,8 | |
| 8 | 13ж Ч34 | 0,5-2,0 | 7,8-15,6 | 3,9-7,8 | 31-62 | 0,5-2,0 | 1000 | 3,9-7,8 | |
| 9 | 16г И100 | 7,8-15,6 | 15,6-31 | н/а | 500 | 31-62 | 1000 | 125 | |
| Диоксидин* | 62,5-1000 | 62,5-1000 | 125-1000 | 125-1000 | 3,9-62,5 | 125-1000 | - | ||
| Хлоргексидин** | 1,0-2,0 | - | - | 1,0-3,0 | 1,0-5,0 | 10-500 | 7,0-15 | ||
| Флуконазол*** | - | - | - | - | - | - | <8-32 | ||
* - Указаны пределы колебаний МПК [Пушкина Т.В., 1995]
** - Указаны пределы колебаний МПК [Галынкин В.А., 2003]
***- Указаны пределы колебаний МПК [Rex J.Y, Walsh T.J., 2000]
Таким образом, большинство соединений проявляет высокую активность по отношению к S. aureus, E. сoli и S. epidermidis, не уступая препаратам сравнения. Наиболее выраженным бактериостатическим действием к большинству изученных штаммов микроорганизмов обладают соединения 4ё, 8ад, 13д и 13ж. Соединение 4ё угнетает рост грамположительных и грамотрицательных микроорганизмов : S. aureus, E. сoli, S. epidermidis, B. сereus, B. subtilis в МПК от 3,9 до 7,8 мкг/мл, что превосходит активность диоксидина. Высокая активность соединения 8ад (енами-ноамид АПК) проявляется в отношении стафилококков (МПК = 3,9-15,6 мкг/мл) и бактерий рода Bacillus (МПК составляет 7,8-15,6 мкг/мл). Соединения 13д и 13ж (монокватернизованные 1,2-ди-3(4)-пиридилэтилены) угнетают рост изучаемых штаммов, за исключением P. aeruginosa (МПК = 1000 мкг/мл), в пределах 0,5-31 мкг/мл, что свидетельствует об их превосходстве над препаратами сравнения. При этом монокватернизованные 1,2-ди-3(4)-пиридилэтилены активны и в отношении штаммов грибов рода Candida в концентрации 3,9-7,8 мкг/мл, что превышает фун-гистатическое действие хлоргексидина и флуконазола и подчеркивает перспек-тивность применения данных соединений в качестве биоцидных агентов.
Несомненный интерес представляет оценка противомикробной активности соединений в отношении резистентных штаммов, обладающих большей виру-лентностью по сравнению с музейными. Клинические резистентные штаммы пре-доставлены бактериологической лабораторией ДГКБ №13 г. Екатеринбурга. Нами изучено бактериостатическое действие соединений по отношению к метицил-линчувствительным (MS) и метициллинрезистентным (MR) штаммам S. aureus и S. epidermidis, которые устойчивы к действию всех -лактамных антибиотиков, макролидов, тетрациклинов, линкозамидов, а также по отношению к двум штам-мам E.сoli : 1, устойчив к действию цефазолина, гентамицина, тобрамицина, и 2, устойчив к ампициллину, цефотаксиму. Результаты исследований представлены в таблице 12.
Таблица 12
Минимальные подавляющие концентрации соединений по отношению
к клиническим штаммам, мкг/мл
| № | Шифр | S. аureus MS | S. аureus МR | S. еpider. MS | S. еpider. МR | E. сoli-1 | E. сoli-2 |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 1 | 4ё И-119 | 15.6-31 | 250 | 3,9-7,8 | 7,8-15,6 | 500 | 500 |
| 2 | 8ад И-214 | 15,6-31 | 15,6-31 | 15,6-31 | 15,6-31 | н/а | н/а |
| 3 | 8аё И-249 | 15,6-31 | 15,6-31 | 31-62 | 31-62 | н/а | н/а |
| 4 | 13д Н-11 | 7,8-15,6 | 31-62 | 7,8-15,6 | 15,6-31 | 62-250 | 62-500 |
| 5 | 13ж Ч-34 | 3,9-7,8 | 31-62 | 7,8-15,6 | 7,8-15,6 | 62-125 | 62-125 |
Выявлено, что соединения активны по отношению к коагулазоположитель-ным и коагулазоотрицательным стафилококкам. Штаммы грамотрицательных микроорганизмов не чувствительны к действию данных соединений за исключе-нием монокватернизованных 1,2-ди-3(4)-пиридилэтиленов, МПК которых состав-ляет 62-500 мкг/мл. В отношении метициллинчувствительных штаммов S. аureus и S. epidermidis МПК соединений 4ё, 8ад и 8аё находится на уровне средних значе-ний (15,6-62 мкг/мл), а соединений 13д и 13ж – на высоком (3,9 - 7,8 мкг/мл). Соединение 4ё угнетает рост S. epidermidis в концентрации 3,9-7,8 мкг/мл. По отно-шению к MRSA енаминоамиды АПК (8ад, 8аё) и монокватернизованные 1,2-ди-3(4)-пиридилэтилены (13д и 13ж), как следовало ожидать, менее активны, при этом МПК находится в диапазоне от 15,6 до 62 мкг/мл соответственно. В отно-шении MR S. еpidermidis МПК, равную 7,8-15,6 мкг/мл, имеют соединения 4ё и 13ж; более слабым бактериостатическим действием обладают соединения 8ад, 8аё, 13д (МПК = 15,6-31 мкг/мл). Таким образом, наибольшее влияние на рост клини-ческих штаммов оказывают монокватернизованные 1,2-ди-3(4)-пиридилэтилены.
В целом, выраженным бактериостатическим действием против большинства изученных штаммов микроорганизмов обладают енаминопроизводные амидов ацилпировиноградных кислот и монокватернизованные 1,2-ди-3(4)-пиридилэти-лены, что свидетельствует о перспективности синтеза и поиска противомикробных соединений среди производных указанных рядов. Представители первого, угнетая рост грамположительных микроорганизмов, имеют высокий потенциал возмож-ного использования в качестве средств терапии инфекций, вызванных S. аureus. Соединения второго ряда проявляют одновременно антибактериальную и противо-грибковую активность и могут найти применение в медицинской практике в качестве кожных антисептиков или дезинфектантов. Для доклинического иссле-дования можно рекомендовать N-(2,4,6-триметилфенил)амид 2-(-N,N-ди-этиламиноэтиламино)-4-оксо-4-(4-хлорфенил)-2-бутеновой кислоты (8ад) и хлорид 1-[N-цетил-4-пиридиний]-2-(4-пиридил)этилена (13ж).
Изучение острой токсичности активных соединений
Острая токсичность соединений (LD50) определена на мышах при внутрибрюшинном введении на кафедре физиологии ПГФА. В таблице 13 приведены данные этой серии опытов. Установлено, что соединения 2ё, 4ё, 8аг-8аё имеют LD50 в интервале от 564 мг/кг до >2000 мг/кг, хлорид 1-[N-цетил-3-пири-диний]-2-(3-пиридил)этилена (13д) – 300 мг/кг, а 3-нафтилметилен-3,4-дигидро-1,4-бензоксазин-2-он (16г) - > 5000 мг/кг.
Таблица 13
Острая токсичность активных соединений, мг/кг
| Шифр | 2ё НОЦ109 | 4ё И-119 | 8аг И-213 | 8ад И-214 | 8ае И-251 | 8аё И-249 | 13д Н-11 | 16г И-100 |
| LD50 | > 2000,0 (2700-3800) | 564,0 (470-670) | > 2000,0 (2700-3800) | 708,0 (590-840) | 2820,0 (2300-3400) | > 2000,0 (2700-3800) | 300,0 (240-380) | > 5000,0 |
| Класс опасности | 3 | 3 | 3 | 3 | 3 | 3 | 3 | 4 |
Результаты изучения острой токсичности соединений свидетельствуют, что указанные соединения согласно ГОСТ 12.1.007-76 относятся к 3 классу умеренно опасных веществ, за исключением соединения 16г, которое является малоопас-ным.
Выводы
1. Скрининговые исследования 270 новых продуктов органического синтеза среди производных антраниловой кислоты, полиоксосоединений : 2-ариламино-1,4-диарил-2-бутен-1,4-дионов и производных ацилпировиноградных кислот, гетероциклических азотсодержащих соединений выявили 32 вещества, обла-дающие противомикробной активностью по отношению к S. aureus и 27 – по отно-шению к E. coli, что составляет соответственно 11,8% и 9,9% от общего количества соединений. Для дальнейшего изучения отобрано 9 активных соединений.
2. Проведенные углубленные исследования противомикробного действия 9 соединений по отношению к музейным штаммам : S. epidermidis АТСС 14990, B. subtilis АТСС 6633, B. cereus АТСС 8035, C. albicans АТСС 243244, P. aeruginosa АТСС 9027 и клиническим резистентным штаммам S. aureus, S. epidermidis, E. сoli позволяют выделить 2 соединения, которые по степени выраженности бактерио-статического действия превосходят препараты сравнения. По острой токсичности исследованные соединения относятся к умеренно и малоопасным веществам.
3. Выявлены некоторые закономерности качественной взаимосвязи химической структуры соединений с противомикробной активностью. Установлено, что в ряду замещенных амидов 4-арил-2-алкиламино-4-оксо-2-бутеновых кислот значи-тельное влияние на проявляемое действие оказывает сочетание диэтиламино-этильного радикала в енаминогруппе и ароматических заместителей в амидном звене молекулы. В ряду кватернизованных 1,2-ди-3(4)-пиридилэтиленов противо-микробная активность обусловлена одним ониевым центром в молекуле и опреде-ленным соотношением липофильных и липофобных частей их структуры. В ряду производных 3,4-дигидро-2Н-1,4-бензоксазин-2-онов наиболее выраженному про-явлению противомикробной ативности способствует наличие в 3-ем положении бензоксазинового цикла объемного -нафтильного фрагмента.
4. Проведен квантово-химический расчет молекул, который обнаружил зави-симость противомикробной активности от величины дипольного момента молекул в рядах производных 5-галогенантраниловой кислоты, эфиров и амидов арилпи-ровиноградных кислот, гетероциклических азотсодержащих соединений. Обнару-жено, что с увеличением дипольного момента молекул бактериостатическое дейст-вие изученных соединений усиливается, а для енаминопроизводных амидов ацил-пировиноградных кислот, имеющих третичный бутильный радикал в 4-м поло-жении молекулы, активность снижается.
5. Рекомендовано для доклинического исследования два соединения : N-(2,4,6-триметилфенил)амид 2-(-N,N-диэтиламиноэтиламино)-4-оксо-4-(4-хлорфенил)-2-бутеновой кислоты и хлорид 1-[N-цетил-4-пиридиний]-2-(4-пири-дил)этилена с наиболее выраженными бактериостатическими свойствами, пред-ставляющие интерес для дальнейшего изучения с целью создания новых эффек-тивных противомикробных средств.
Основное содержание диссертации опубликовано в работах
- Изучение антимикробной активности производных пивалоилпировиноград-ной кислоты / Е.В. Буканова, Э.В. Воронина, Е.В. Бажина, С.С. Швецова // Вузы и регион : материалы межвуз. науч.-практ. конф. - Пермь, 2003. - С.36.
- Одегова, Т.Ф. Исследования по рациональному применению антисептиче-ских средств в медицине / Т.Ф. Одегова, С.С. Швецова // Рациональное использование лекарств : материалы Рос. науч.-практ. конф. - Пермь, 2004. - С. 75.
- Поиск противомикробных лекарственных средств среди продуктов органического синтеза / Т. Ф. Одегова, М.В. Томилов, С.С. Швецова [и др.] // Разработка, исследование и маркетинг новой фармацевтической продукции : материалы Всерос. науч.-практ. конф. – Пятигорск, 2005. - С. 400-401.
- Исследования антимикробных свойств производных ацилпировиноградных кислот / С.С. Дубровина, Т.Ф. Одегова, С. Ю. Солодников, О.П. Красных // Человек и лекарство : материалы XIV Рос. нац. конгресса. – Москва, 2007. - С. 543.
- Антимикробная активность метиловых эфиров 2-(гет)ариламино-4-оксо-Z-2-бутеновых кислот / С.С. Дубровина, Т.Ф. Одегова, Н.А. Ботева, О.П. Крас-ных // Здоровье и образование : материалы Международ. науч.-практ. конф. – Палермо, Пермь / ПГМА. – Пермь, 2007. - С. 47-50.
- Дубровина, С.С. Изучение противомикробной активности производных 1,4-бензоксазин-2-онов / С.С. Дубровина, Н.М. Игидов // Современные проблемы экологии, микробиологии и иммунологии : материалы регионал. конф. молодых ученых с международ. участием. – Пермь, 2007.- С. 58-59.
- Поиск новых отечественных дезинфицирующих средств / С.С. Дубровина, Т.Ф. Одегова, Н.А. Ботева [и др.] // Достижения и перспективы в области создания новых ЛС : материалы науч.-практ. конф. – Пермь, 2007. - С. 328-330.
- Биологическая активность 4-арил-2-ариламино(ароилгидразино)-4-оксобут- и 2-арилаимно(ароилгидразино)-5,5-диметил-4-оксо-2-гексеновых кислот / А.Ю. Бородин, В.В. Залесов, С.С. Дубровина [и др.] // Техническая химия. От теории к практике : доклады Международ. конф. - Пермь, 2008. - С. 197-199.
- Синтез и противомикробная активность метиловых эфиров 2-(гет)арил-амино-4-оксо-Z-2-бутеновых кислот и продуктов их модификации / А.А. Ботева, О.П. Красных, С.С. Дубровина [и др.] // Хим.-фарм. журн. - 2008. - Т. 42, № 8. - С. 12-15.
- Биологическая активность N-замещенных амидов 2-(2-бромфениламино)- и 2-(4-бромфениламино)-5,5-диметил-4-оксо-2-гексеновых кислот / А.Ю. Бо-родин, Н.М. Игидов, С.С. Дубровина [и др.] // Современное состояние и пути оптимизации лекарственного обеспечения населения : материалы Рос. науч.-практ. конф. - Пермь, 2008.- С. 188-190.
- Синтез, биологическая активность 4-арил-2-гидрокси-4-оксо-2-бутеноатов 5-фенилоксадиазолил аммония / А.Ю. Бородин, Н.М. Игидов, С.С. Дубро-вина [и др.] // Современное состояние и пути оптимизации лекарственного обеспечения населения : материалы Рос. науч.-практ. конф. - Пермь, 2008. - С. 193-196.
- Синтез, свойства и биологическая активность 4-замещенных 2-[N-(4-гидрокси-3-изопропил-2-метилфенил)амино]-4-оксо-2-бутеновых кислот / И.Н. Чернов, Н.М. Игидов, С.С. Дубровина [и др.] // Современное состояние и пути оптимизации лекарственного обеспечения населения : материалы Рос. науч.-практ. конф. - Пермь, 2008. - С. 392-395.
Автор выражает благодарность сотрудникам кафедры микробиологии ПГФА за постоянное внимание к работе, ст. лаборанту кафедры Яковлевой О.С. за помощь в проведении исследований.

