Вклад ожирения в поражение почек у больных сахарным диабетом 2 типа
На правах рукописи
Савельева
Светлана Алексеевна
ВКЛАД ОЖИРЕНИЯ В ПОРАЖЕНИЕ ПОЧЕК У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ 2 ТИПА
14.01.29 – нефрология
14.01.02 – эндокринология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва 2010
Работа выполнена в ГОУ ВПО Первый Московский государственный медицинский университет имени И.М. Сеченова и в
ФГУ Эндокринологический научный центр
Научные руководители:
доктор медицинских наук, профессор Ирина Михайловна Кутырина
доктор медицинских наук, профессор Марина Владимировна Шестакова
Официальные оппоненты:
доктор медицинских наук, профессор Лидия Владимировна Козловская
доктор медицинских наук, профессор Ольга Михайловна Смирнова
Ведущее учреждение:
ГОУ ДПО «Российская медицинская академия последипломного образования» Росздрава
Защита диссертации состоится «___»___________2011г. в ___часов
на заседании диссертационного совета Д.208.040.05 при ГОУ ВПО Первый МГМУ им. И.М. Сеченова (119991, Москва, ул. Трубецкая, д.8, строение 2)
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО Первый МГМУ им. И.М. Сеченова (117998, Москва, Нахимовский проспект, д.49)
Автореферат разослан «___»_________2011г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор Елена Васильевна Волчкова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
В настоящее время во всех странах мира наблюдается стремительный рост популяции с избыточной массой тела и ожирением. Эпидемия ожирения неизбежно перерастает в эпидемию сахарного диабета (СД) 2 типа. Диабетическая нефропатия (ДН) наряду с заболеваниями сердечно-сосудистой системы являются наиболее частыми, тяжелыми и прогностически неблагоприятными осложнениями СД. В последние годы ДН заняла лидирующие позиции среди причин терминальной почечной недостаточности [Шестакова М.В., Дедов И.И., 2009; Томилина Н.А., 2009; Ritz Е., 2006]. Патогенез ДН наиболее изучен при СД 1 типа. Традиционно ведущую роль в формировании ДН отводят гипергликемии и обусловленным гипергликемией нарушениям метаболизма: неферментативному гликированию, дислипидемии, оксидативному стрессу, а также расстройствам внутрипочечной и системной гемодинимики [Дедов И.И., Шестакова М.В, 2000; Brenner B., 1982, 2002].
Несмотря на интенсивные исследования, многие аспекты формирования ДН и кардиоренального синдрома, особенно при СД 2 типа, недостаточно ясны. В частности, результаты ряда экспериментальных исследований свидетельствуют о том, что в патогенезе ДН при СД 2 типа, помимо гипергликемии, свой собственный вклад вносит ожирение [Кутырина И.М., Федорова Е.Ю., 2008; Masaomi N. et al., 2005]. В последние годы появляется все больше данных, доказывающих, что ожирение утяжеляет течение нефропатий разного генеза и способствует развитию ремоделирования миокарда [Мухин Н.А., Сагинова Е.А., 2006; Конради А.О., 2002; Turkbey E. et al., 2010].
Механизмы, предрасполагающие к поражению почек при ожирении, в настоящее время активно изучаются. Установлено, что жировая ткань обладает высокой гормональной активностью, секретируя биологически активные вещества, которые могут непосредственно участвовать в развитии поражения органов-мишеней независимо от наличия нарушений углеводного обмена [Wolf G., 2006; Osawa H., 2007; Eynatten М., 2009]. Однако патогенетические механизмы влияния этих гормонов на функцию почек при СД 2 типа недостаточно изучены. Требуют изучения взаимосвязи между особенностями нарушений метаболизма и гемодинамики с гормональной активностью жировой ткани, генетическими факторами, ремоделированием миокарда левого желудочка и поражением почек у больных СД 2 типа и ожирением.
Целью настоящего исследования явилось изучение роли ожирения в поражении почек у больных СД 2 типа.
Задачи исследования:
- Оценить частоту ранних стадий ДН у больных СД 2 типа в зависимости от степени ожирения.
- Выявить спектр метаболических факторов риска ДН у больных СД 2 типа и их взаимосвязь с ожирением.
- Оценить роль системной артериальной гипертензии в развитии ранних стадий ДН у больных СД 2 типа и взаимосвязь артериальной гипертензии с ожирением.
- Определить роль гормонов жировой ткани лептина и адипонектина в поражении почек у больных СД 2 типа.
- Изучить взаимосвязь полиморфного маркера Pro12Аlа гена PPARG2 с риском возникновения ДН при СД 2 типа.
- Оценить взаимосвязь процессов ремоделирования миокарда левого желудочка с ожирением и развитием ранних стадий ДН у больных СД 2 типа в рамках кардиоренального синдрома.
Научная новизна
Впервые определена роль ожирения в развитии ДН при СД 2 типа. Установлено, что частота поражения почек у больных СД 2 типа с ожирением превышает таковую у больных СД 2 типа без ожирения, как на начальных стадиях развития ДН – гиперфильтрации и микроальбуминурии, – так и при более выраженном повреждении почек – развитии протеинурии.
При СД2 типа с ожирением выявлены более выраженные и значимые расстройства липидного и пуринового обменов, расстройства системной гемодинамики, по сравнению с больными СД 2 типа без ожирения.
Впервые установлена взаимосвязь между гормональной активностью жировой ткани (влиянием лептина и адипонектина) и поражением почек у больных СД 2 типа. Нарастание лептина при увеличении степени ожирения сопровождалось увеличением частоты поражения почек у больных СД 2 типа. Нефропротективный гормон жировой ткани - адипонектин - на ранних стадиях поражения почек снижался, но возрастал при появлении протеинурии.
Впервые проведена оценка генетической предрасположенности к развитию поражения почек при СД 2 типа: исследована взаимосвязь полиморфного маркера Pro12Ala гена PPARG2 с риском возникновения ДН при СД 2 типа в российской популяции. Ассоциации данного полиморфного маркера с возникновением ДН в исследуемой выборке больных не выявлено.
Установлена взаимосвязь развития ранних стадий ДН и процессов ремоделирования миокарда. Факторами риска ремоделирования миокарда и развития ДН, помимо висцерального ожирения, значимыми оказались гликированный гемоглобин, и уровень мочевой кислоты в сыворотке крови, что отражает тесную взаимосвязь метаболических расстройств и расстройств углеводного обмена при ожирении с развитием кардиоренального синдрома.
Практическая значимость
Полученные результаты исследования позволяют рассматривать ожирение как фактор риска развития и прогрессирования ДН у больных СД 2 типа и раннего формирования кардиоренального синдрома. Данные проведенного исследования могут быть использованы в клинической практике для выделения групп больных СД 2 типа, имеющих высокий риск развития ДН и сердечно-сосудистых заболеваний, и проведения в этой группе больных профилактических мероприятий. Результаты работы обосновывают необходимость наряду со строгим контролем гликемии, коррекции системной и клубочковой гипертензии, дислипидемии, нарушений пуринового обмена у больных СД2 типа и ожирением для предупреждения развития ДН и кардиоренального синдрома. Разработаны прогностические модели, позволяющие оценить риск развития ДН.
Внедрение результатов работы в практику
Результаты настоящего исследования используются при обследовании и лечении больных в Университетской клинической больнице № 3 Первого МГМУ им. И.М.Сеченова, отделении диабетической нефропатии и гемодиализа ФГУ ЭНЦ, основные положения диссертации включены в лекционный курс на кафедре нефрологии и гемодиализа ФППОВ, на кафедре детской эндокринологии с курсами диабетологии и эндокринологии ФППОВ ГОУ ВПО Первый МГМУ им. И.М. Сеченова.
Публикации
По теме диссертации опубликовано 10 печатных работ.
Апробация работы
Апробация работы проведена 27 октября 2010 года (протокол №8) на совместном заседании кафедры нефрологии и гемодиализа ФППОВ, отдела нефрологии НИЦ, кафедры терапии и профессиональных заболеваний Первого МГМУ им. И.М. Сеченова, кафедры внутренних болезней факультета фундаментальной медицины МГУ им. М.В. Ломоносова, отделения диабетической нефропатии и гемодиализа ФГУ ЭНЦ. Материалы работы доложены и обсуждены на научной конференции молодых исследователей с международным участием «Татьянин день» (Москва, январь 2010 г.), XVII Международной конференции студентов, аспирантов и молодых ученых «Ломоносов» (Москва, апрель 2010 г.), XLVII Европейском конгрессе нефрологов (ERA – EDTA, Мюнхен, июнь 2010 г.), VII Съезде Научного общества нефрологов России (Москва, октябрь 2010 г.).
Основные положения, выносимые на защиту:
- У больных с ожирением частота развития ранних стадий ДН выше по сравнению с больными СД 2 типа без ожирения. Частота развития ДН у больных СД 2 типа зависит от степени ожирения.
- Развитие ранних стадий ДН у больных СД 2 типа с ожирением обусловлено сочетанным воздействием метаболических факторов и расстройствами системной и внутрипочечной гемодинамики - артериальной гипертензии и внутрипочечной гипертензии.
- У пациентов СД2 типа с ожирением развитию ДН способствует высокая гормональная активность жировой ткани: нефротоксические эффекты лептина и на начальных стадиях ДН снижение нефропротективного гормона адипонектина.
- У пациентов СД2 типа ожирение, наряду с влиянием на развитие ДН, способствует ремоделированию левого желудочка с формированием кардиоренального синдрома, что обусловлено общностью патогенетических факторов, лежащих в основе развития данных процессов.
Объем и структура диссертации
Диссертация состоит из введения, обзора литературы, глав с описанием материалов и методов исследования, результатов собственного исследования, обсуждения, выводов, практических рекомендаций. Текст изложен на 112 страницах машинописного текста, включает 20 таблиц, 24 рисунка. Библиографический указатель содержит 202 источника (60 отечественных и 142 зарубежных).
Автор выражает глубокую благодарность научным руководителям – д.м.н., профессору И.М. Кутыриной и д.м.н., профессору М.В. Шестаковой за помощь в работе над диссертацией, а также коллективам кафедры нефрологии и гемодиализа ФППОВ, кафедры терапии и профессиональных заболеваний МПФ, отдела нефрологии НИЦ Первого МГМУ им. И.М. Сеченова и отделений Института диабета ФГУ ЭНЦ.
СОДЕРЖАНИЕ ДИССЕРТАЦИИ
Материалы и методы исследования
В исследование включено 152 больных СД 2 типа, из них 61 мужчина и 91 женщина, в возрасте от 34 до 70 лет (средний возраст 57,3±7,1 лет). Диагноз СД 2 типа устанавливался в соответствии с рекомендациями ВОЗ (1998г).
Критериями исключения были выраженные стадии ДН (скорость клубочковой фильтрации (СКФ) < 60 мл/мин/1,73м2, протеинурия более 2 г/сутки), гематурия, гемодинамически значимые стенозы сосудов почек, первичное поражение почек в рамках системных заболеваний соединительной ткани, хронический гломерулонефрит, онкологические заболевания, острые сердечно-сосудистые события в течение последних 6 месяцев, возраст старше 70 лет.
У всех больных определяли антропометрические показатели: индекс массы тела (ИМТ), окружность талии (ОТ), окружность бедер (ОБ), соотношение ОТ/ОБ. В сыворотке крови, взятой натощак после 14-часового голодания, оценивали показатели липидного спектра - уровни общего холестерина (ХС), триглицеридов (ТГ), холестерина липопротеидов высокой плотности (ЛПВП) и низкой плотности (ЛПНП), - также оценивали уровни креатинина, мочевой кислоты. Гликированный гемоглобин (НвА1с) определяли методом высокоэффективной жидкостной хроматографии.
Уровень гормонов жировой ткани в сыворотке крови определяли иммуноферментным методом у 55 больных СД 2 типа: лептин – наборами фирмы Diagnostics Biochem (Канада), адипонектин – наборами фирмы Bio Vendor (Чехия). Группа контроля для сывороточных показателей состояла из 12 добровольцев без ожирения (ИМТ 23,6±3,8 кг/м2) и не страдающих СД, из них 4 мужчины, 8 женщин, в возрасте от 25 до 60 лет.
Исследование полиморфного маркера Pro12Ala гена PPARG2 выполнено 134 больным СД 2 типа. Амплификацию полиморфного участка гена PPARG2 проводили с помощью полимеразной цепной реакции.
Поражение почек оценивали по уровню СКФ и альбуминурии. Расчет СКФ осуществлялся по формуле Кокрофта-Голта с коррекцией на стандартную поверхность тела (1,73м2): CКФ к-г ст. (мл/мин/1,73м2)=[(140– возраст) x вес] х 88/(72xScrхBSA), где возраст – годы, вес – кг, Scr –концентрация креатинина в плазме – мкмоль/л. Для женщин результат умножали на 0,85. Для расчета площади поверхности тела (BSA) использовали формулу Дюбуа: BSA (м2)=0,007184 х вес0,425 х рост0,725, где вес-кг, рост-см.
СКФ>130 мл/мин/1,73м2 расценивали как гиперфильтрацию. При этом под гиперфильтрацией подразумевали превышение абсолютных значений СКФ по отношению к верхней границе нормы.
Определение уровня экскреции альбумина с мочой за сутки проводили методом иммунотурбидиметрии. В зависимости от уровня альбуминурии выделяли нормоальбуминурию (НАУ), микроальбуминурию (МАУ) и протеинурию (ПУ). Нормоальбуминурию диагностировали при уровне альбумина <30 мг в суточной моче, микроальбуминурию – при экскреции 30-299 мг альбумина за сутки, протеинурию – при уровне альбуминурии 300 мг/сут.
Для оценки параметров геометрии миокарда левого желудочка и установления типа ремоделирования использовали эхокардиографическое исследование (выполнено 89 больным СД 2 типа). Массу миокарда левого желудочка (ММЛЖ) рассчитывали по формуле, рекомендуемой Американским обществом эхокардиографии:
ММЛЖ (г)= 0,8х [1,04х(ТМЖП + ТЗСЛЖ+КДР)3- (КДР)3]+0,6, где ТМЖП (мм) - толщина межжелудочковой перегородки, ТЗСЛЖ (мм) - толщина задней стенки левого желудочка, КДР (мм) - конечно-диастолический размер.
Индекс массы миокарда левого желудочка (ИММЛЖ) определяли по формуле: ИММЛЖ (г/м2)=ММЛЖ/площадь поверхности тела (BSA).
Индекс относительной толщины стенки (ИОТ) левого желудочка рассчитывали по формуле: ИОТ=(ТМЖП+ТЗСЛЖ)/КДР.
Гипертрофию миокарда левого желудочка диагностировали при ИММЛЖ > 125 г/м2 у мужчин и > 110 г/м2 у женщин.
В зависимости от величины ИММЛЖ и ИОТ были выделены следующие модели геометрии левого желудочка сердца: нормальная геометрия (ИОТ <0,42; нормальный ИММЛЖ); концентрическое ремоделирование (ИОТ0,42; нормальный ИММЛЖ); концентрическая гипертрофия (ИОТ0,42; ИММЛЖ больше нормы); эксцентрическая гипертрофия (ИОТ<0,42; ИММЛЖ больше нормы).
Методы статистического анализа
Статистический анализ проводили с использованием пакета программ SPSS for Windows, 9 версия. Результаты представлены в виде средних значений ± стандартное отклонение исследуемых показателей в группе, медиан, 25 и 75 процентилей. Для изучения взаимосвязи между показателями применяли метод корреляции Спирмена. Достоверность различий оценивали с помощью методов непараметрической статистики: U-теста Манна-Уитни - для 2-х независимых выборок, H-критерия Краскела — Уоллиса– для сравнения 3-х и более выборок. Для проверки статистической значимости различий частотных показателей использовали критерий 2 по Пирсону. Достоверным считался уровень р<0,05, при 0,05 р< 0,1 говорили о наличии тенденции. Многофакторный анализ проводили с помощью метода линейной регрессии.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Учитывая, что точное начало развития СД 2 типа установить, как правило, не удается, и длительность СД является мощным фактором развития осложнений СД, в частности прогрессирования ДН, мы отдельно анализировали группы больных с длительностью СД менее 5 лет и с длительностью СД более 5 лет. В зависимости от ИМТ выделяли группы больных без ожирения - с ИМТ менее 30 кг/м2 - и с ожирением - с ИМТ более 30 кг/м2. Исследуемые группы с ожирением и без ожирения как при длительности СД менее 5 лет, так и при длительности СД более 5 лет были сопоставимы по возрасту, полу, длительности СД и степени компенсации углеводного обмена. (Табл. 1)
Таблица 1. Характеристика исследуемых групп больных без ожирения (ИМТ < 30 кг/м2) и с ожирением (ИМТ 30 кг/м2) при длительности СД 2 типа менее 5 лет и при длительности СД 2 типа более 5 лет
| Показатели | Группа 1 ИМТ < 30 кг/м2 | Группа 2 ИМТ 30 кг/м2 | р | |
| Длительность СД2 типа менее 5 лет | ||||
| (N=21) | (N=23) | |||
| Возраст (лет) | 55,5± 8,4 | 54,7± 7,1 | 0,501 | |
| Пол (м/ж,%) | 38/62 | 35/65 | 0,820 | |
| Длительность СД (годы) | 2,8 ±1,3 | 2,8±1,6 | 0,584 | |
| НвА1с (%) | 9,1±2,4 | 7,7±1,4 | 0,303 | |
| Длительность СД2 типа более 5 лет | ||||
| (N=39) | (N=69) | |||
| Возраст (лет) | 58,7± 5,4 | 58,95± 6,2 | 0,900 | |
| Пол (м/ж,%) | 43,6/56,4 | 40,6/59,4 | 0,762 | |
| Длительность СД (годы) | 12,7 ±5,5 | 14,2±6,3 | 0,240 | |
| НвА1с (%) | 9,2±1,6 | 9,2±2,0 | 0,731 | |
Частота ДН в зависимости от степени ожирения у больных СД 2 типа
В результате проведенного исследования установлена более высокая частота поражения почек у больных СД 2 типа с ожирением, по сравнению с больными без ожирения, при длительности СД более 5 лет: развитие МАУ и ПУ у больных с ожирением наблюдалось достоверно чаще. Частота МАУ у больных без ожирения составляла 7,9%, у больных с ожирением – 23,1%, частота ПУ – 5,3% и 11,5% соответственно. (Рис.1)
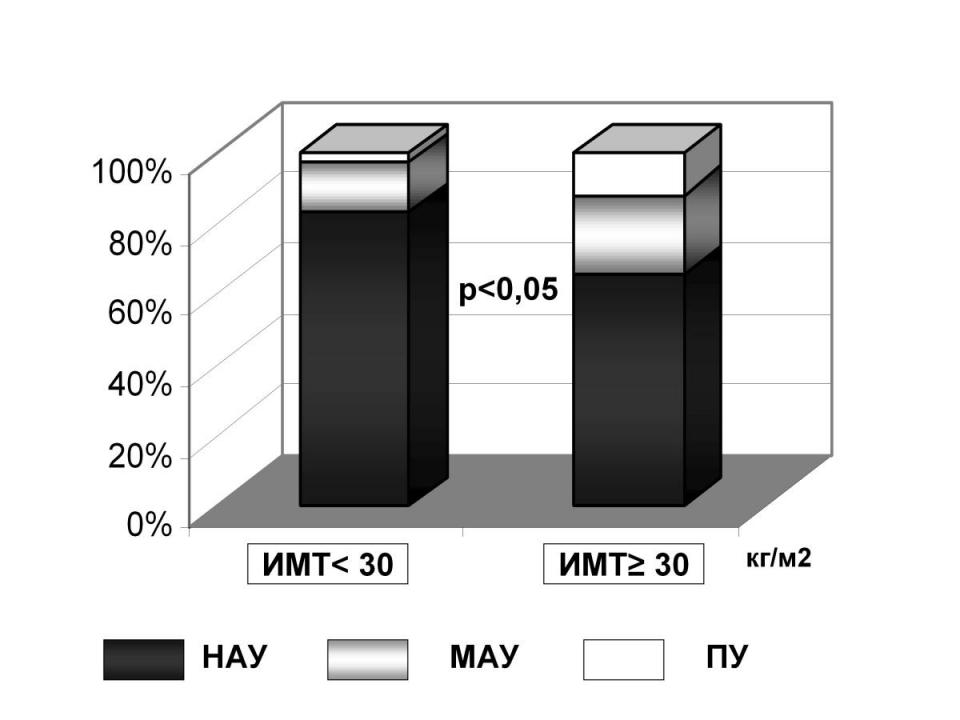
Рис.1 Частота нормоальбуминурии, микроальбуминурии и протеинурии в группах больных СД 2 типа без ожирения (ИМТ < 30 кг/м2) и с ожирением (ИМТ 30 кг/м2) при длительности СД более 5 лет
При длительности СД менее 5 лет частота развития МАУ, ПУ у больных СД с ожирением также была выше - составляла 20%, тогда как у больных СД без ожирения - 13,4%, хотя эти различия не являются достоверными.
Частота гиперфильтрации (маркера раннего поражения почек) также была выше в группе больных СД 2 типа с ожирением при длительности СД более 5 лет, составляла 13%, тогда как в группе больных без ожирения – 2,6%. (Рис.2)

Рис. 2 Частота гиперфильтрации в группах больных СД 2 типа без ожирения
(ИМТ < 30 кг/м2) и с ожирением (ИМТ 30 кг/м2) при длительности СД более 5 лет
Роль традиционных факторов риска в развитии ранних стадий ДН у больных СД 2 типа, их взаимосвязь с ожирением
При оценке традиционных факторов риска ДН, у больных СД 2 типа с ожирением при длительности СД более 5 лет выявлены более тяжелые системные гемодинамические расстройства: чаще определялась 3 степень артериальной гипертензии и в большем проценте случаев появлялась необходимость использования трех и более антигипертензивных препаратов. Кроме того, у больных с ожирением были более выражены расстройства пуринового и липидного обменов: был выше уровень мочевой кислоты в сыворотке крове, чаще определялось снижение ЛПВП. (Табл. 2)
Таблица 2. Традиционные факторы риска диабетической нефропатии в исследуемых группах больных СД 2 типа без ожирения (ИМТ<30 кг/м2) и с ожирением (ИМТ30 кг/м2) при длительности СД более 5 лет
| Показатели | Группа 1 ИМТ < 30 кг/м2 | Группа 2 ИМТ 30 кг/м2 |
| АГ 1 степени, % | 11,7 | 1,2* |
| АГ 2 степени, % | 38,3 | 23,5* |
| АГ 3 степени, % | 50 | 75,3* |
| Частота использования 3-х и более антигипертензивных препаратов, % | 20,4 | 43,6* |
| Мочевая кислота (мкмоль/л) | 285,8±94,8 | 360,1±114,6* |
| Частота снижения уровня ЛПВП1, % | 26,5 | 55,1* |
| Частота гипертриглицеридемии2, % | 43,6 | 52,5 |
Примечание: 1- Снижение уровня ЛПВП: у мужчин < 1,04 ммоль/л, у женщин<1,3 ммоль/л; 2- гипертриглицеридемия: ТГ >1,7 ммоль/л; * достоверность различий между группами 1 и 2 p < 0,05
При длительности СД менее 5 лет в группе больных с ожирением также были более выражены расстройства липидного и пуринового обменов, расстройства системной гемодинамики, однако различия не достигали уровня достоверности.
Результаты многофакторного анализа
При проведении многофакторного регрессионного анализа в исходную модель включали факторы, обладающие влиянием на риск развития МАУ и ПУ, - возраст, пол, длительность СД, НвА1с, антропометрические показатели (ИМТ, окружность талии, окружность бедер), АД (САД и ДАД), длительность артериальной гипертензии, уровень мочевой кислоты, показатели липидного спектра (ХС, ТГ, ЛПНП, ЛПВП), индекс курения. О высокой прогностической силе данной модели свидетельствуют результаты построения ROC-кривой (площадь под кривой составила 0,903). В конечную модель в качестве факторов, обладающих самостоятельным прогностическим значением, вошли 6 факторов - НвА1с, окружность талии, САД, пол, длительность АГ, ЛПВП. Однако наиболее значимыми оказались 3 фактора: гликированный гемоглобин (=0,389, В=0,08, р=0,001), окружность талии (=0,384, В=0,01,р=0,0027) и САД (=0,336, В=0,009,р=0,014), что, по-видимому, отражает тесную связь ожирения с декомпенсацией СД2 типа и развитием высокой систолической АГ. Учитывая, что окружность талии (показатель массы висцерального жира) является самостоятельным фактором риска развития МАУ, ПУ, можно предположить, что неблагоприятное влияние ожирения на функцию почек может реализовываться не только через нарушения углеводного обмена и гемодинамические механизмы, но, вероятно, существуют и иные факторы, ассоциированные с ожирением, способствующие развитию ДН.
Роль гормонов жировой ткани (лептина и адипонектина) в развитии ДН у больных СД 2 типа
Мы исследовали взаимосвязь гормональной активности жировой ткани и поражения почек у больных СД2 типа. Гиперлептинемия выявлена у 66% больных СД2 типа, уровень лептина нарастал с увеличением степени ожирения: при увеличении индекса массы тела, окружности талии, окружности бедер отмечено нарастание уровня лептина (r=0,517,р=0,0001; r=0,467,р=0,0001; r=0,494,р=0,0001 соответственно).
При оценке взаимосвязи уровня лептина и поражения почек, при наиболее выраженном повреждении почек (развитии протеинурии) уровень лептина был наиболее высоким. (Рис.3)
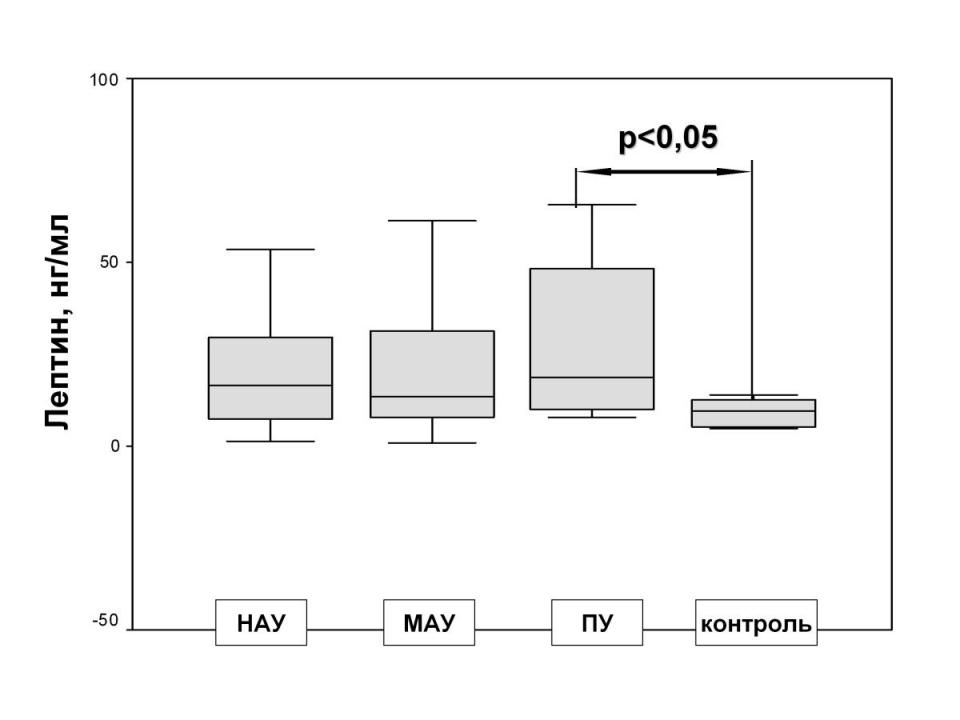
Рис. 3 Уровень лептина в зависимости от экскреции белка с мочой
Кроме того выявлены различия в уровнях лептина у мужчин и женщин: у женщин уровень лептина был выше. (Табл. 3)
Таблица 3. Взаимосвязь уровня лептина и альбуминурии в зависимости от пола
| Лептин, нг/мл | НАУ | МАУ | ПУ | Контроль |
| Мужчины | 7,3 [3,1;20,9] | 10,6[5,9;58,7] | 8,6[8,0;21,1]* | 5,3[5,0; 7,2] |
| Женщины | 26,3[14,9;37]* | 18,3[15,1;31,5] | 65,9[11,4;279,5] | 12,0[9,5;14,0] |
*р < 0,05 - по сравнению с группой контроля. Результаты представлены в виде медиан, 25, 75 процентилей
Помимо участия лептина в процессах нефросклероза, в последнее время обсуждается участие гиперлептинемии и в патогенезе АГ при ожирении. Так, по нашим данным, существуют корреляционные взаимосвязи уровня лептина с тяжестью АГ: при нарастании уровня лептина отмечено повышение уровня ДАД (r=0,270, p=0,046), также выявлена взаимосвязь уровня лептина со степенью АГ (r=0,401, p=0,003.) (Рис.4)
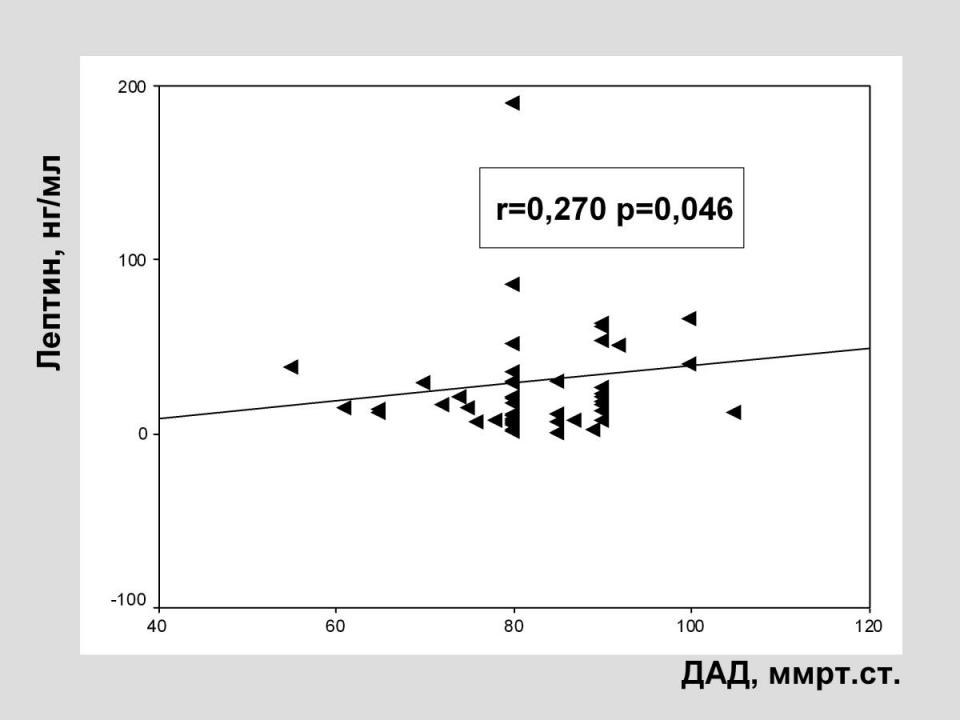
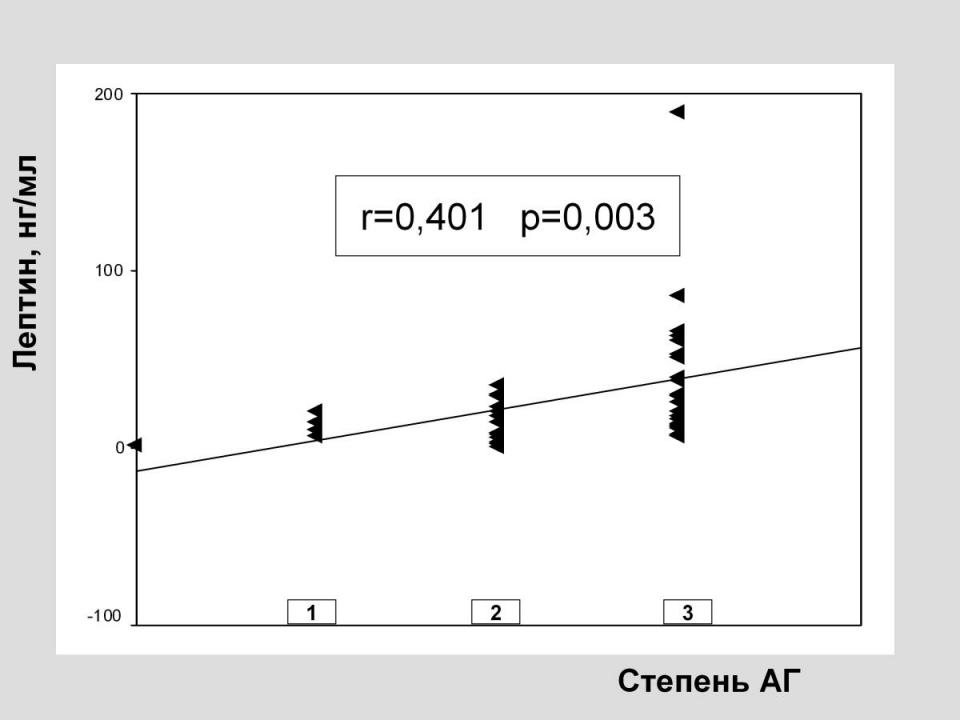
Рис. 4 Взаимосвязь уровня лептина и артериальной гипертензии
Уровень адипонектина - адипоцитокина, обладающего протективными свойствами, был снижен у большей части больных СД2 типа - гипоадипонектинемия обнаружена у 89% больных. Однако четкая зависимость степени снижения адипонектина от ИМТ в группе больных СД2 типа отсутствовала (Табл. 4).
Таблица 4. Уровни адипонектина в зависимости от степени ожирения
| Показатели | Группа контроля | Группа 1 (ИМТ<30 кг/м2) | Группа 2 (ИМТ 30-35 кг/м2) | Группа 3 (ИМТ 35 кг/м2) | Р |
| Адипонек- тин (нг/мл) | 10,62 [9,4;12,59] | 6,4 [4,8;9,5] | 6,7 [5,9; 7,9] | 6,6 [4,5;7,7] | р1=0,020 р2=0,001 р3=0,005 |
Примечание: р1 - достоверность различий между группой контроля и группой 1; р2 -достоверность различий между группой контроля и группой 2; р3 -достоверность различий между группой контроля и группой 3. Результаты представлены в виде медиан, 25,75 процентилей
В большей мере уровень адипонектина был связан с изменениями липидного обмена. По данным корреляционного анализа при снижении адипонектина отмечено снижение ЛПВП (r=0,398; р=0,012) и нарастание уровня триглицеридов (r= –0,452; р=0,001), что может свидетельствовать об антиатерогенной роли адипонектина. (Рис.5)
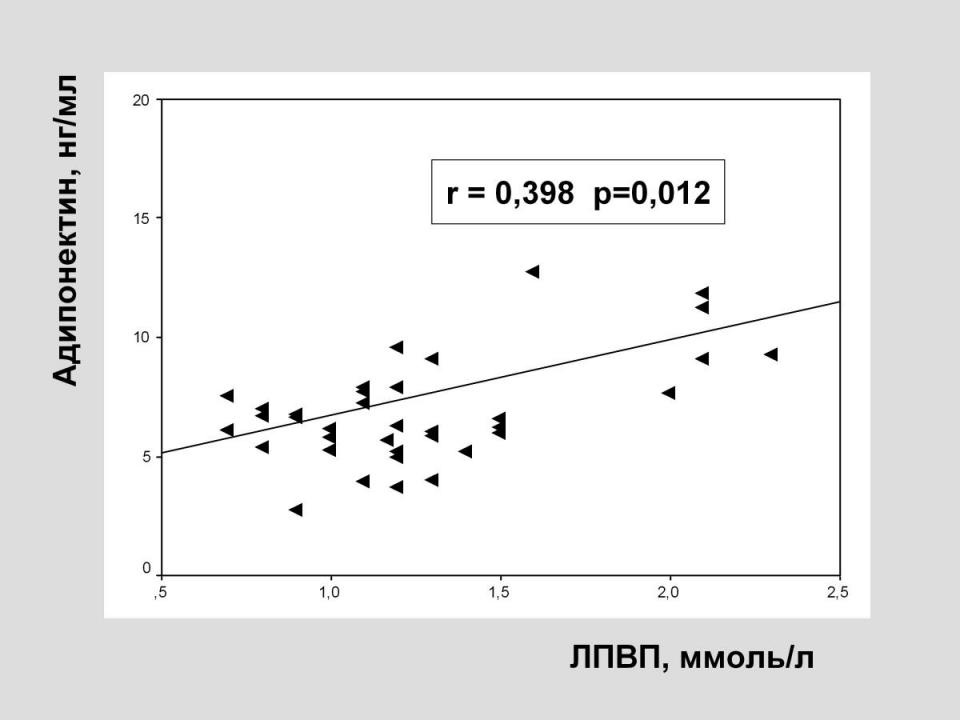
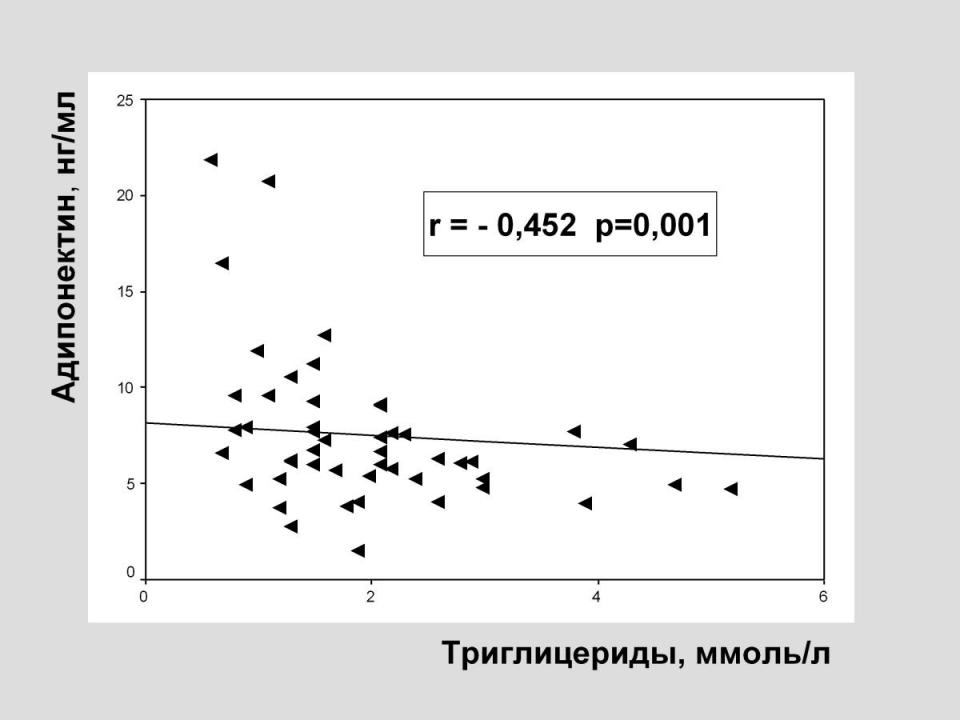
Рис. 5 Взаимосвязь уровня адипонектина и липидных изменений
При оценке взаимосвязи уровня адипонектина с поражением почек, у больных без признаков ДН и с начальными признаками ДН (микроальбуминурией) адипонектин был ниже, чем в группе контроля, при развитии необратимого повреждения почек – появлении протеинурии – отмечено нарастание адипонектина. (Рис.6)
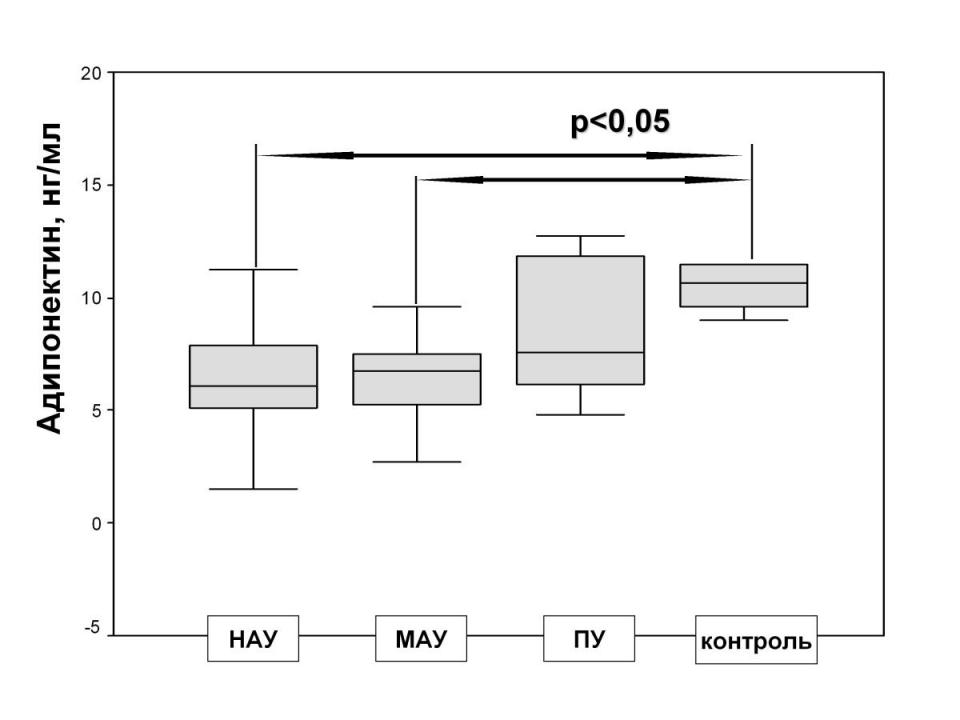
Рис. 6 Уровень адипонектина в зависимости от экскреции белка с мочой
Механизмы выявленных изменений остаются не ясными. В ряде экспериментальных исследований доказано, что адипонектин восстанавливает функцию поврежденных подоцитов [Sharma K. et al., 2008]. Можно обсуждать компенсаторное повышение адипонектина, направленное на усиление нефропротективного эффекта при повреждении почек. Однако необходимы дополнительные исследования, уточняющие механизм подобной динамики адипонектина.
У мужчин и женщин также выявлены различия в уровнях адипонектина: у женщин уровень адипонектина был выше. (Табл. 5)
Таблица 5. Взаимосвязь уровня адипонектина и альбуминурии
| Адипонектин нг/мл | НАУ | МАУ | ПУ | Контроль |
| Мужчины | 5,0 [4,0;6,6] | 5,6 [4,8;7,5] | 7,2 [5,2;9,1] | 8,2 [6,5; 9,8] |
| Женщины | 7,7 [5,8;9,6]* | 7,5 [7,1;8,6]* | 12,8 [6,2;20,7] | 10,9[9,7;14,8] |
Примечание: *р < 0,05 по сравнению с группой контроля. Результаты представлены в виде медиан, 25, 75 процентилей
Исследование взаимосвязи полиморфного маркера Pro12Аla гена -формы рецепторов, активируемых пролифераторами пероксисом (PPARG2), с риском развития ДН у больных СД 2 типа
При оценке роли генетических факторов в развитии ДН при СД 2 типа в качестве гена-кандидата с возможной сочетанной генетической предрасположенностью как к ожирению, так и к нефропатии, рассматривали ген PPARG2. Данный ген кодирует рецепторы, активаторы пролиферации пероксисом 2 типа, которые относятся к семейству ядерных рецепторов и участвуют в регуляции процессов энергообмена. По данным ряда исследований носительство аллеля Аlа полиморфного маркера Pro12Аlа гена PPARG2 играет протективную роль при развитии ожирения и инсулинорезистентности [Майоров А.Ю., 2009; Носиков В.В., 2010]. Мы исследовали взаимосвязь данного полиморфного маркера с риском возникновения ДН при СД 2 типа. Для оценки взаимосвязи полиморфного маркера Pro12Аlа гена PPARG2 с риском развития ДН пациенты с СД 2 типа (67 человек), были разделены на 2 группы в соответствии с неперекрывающимися критериями отбора (для исключения маскирующего влияния негенетических факторов). В группу «случай» («ДН+», n = 25) включены пациенты c выраженным фенотипом нефропатии: с протеинурией или микроальбуминурией при любой длительности СД. В группу «контроль» («ДН-», n=42) – пациенты с отсутствием клинических признаков ДН: нормоальбуминурией, несмотря на большую длительность СД (10 лет). Исследуемые группы были сопоставимы по возрасту, полу, длительности СД, степени компенсации углеводного обмена. (Табл.6)
Таблица 6 Клиническая характеристика исследуемых групп больных СД 2 типа «ДН+» и «ДН-»
| Показатели | Группа «ДН-» | Группа «ДН+» | р |
| Возраст (лет) | 60,5± 5,2 | 58,1± 6,4 | 0,106 |
| Пол (м/ж) | 17/25 | 13/12 | 0,363 |
| Длительность СД (годы) | 15,0 ±5,7 | 12,0±5,9 | 0,083 |
| НвА1с (%) | 9,2±1,6 | 9,9±2,1 | 0,150 |
Распределение аллелей и генотипов полиморфного маркера Pro12Ala гена PPARG2 групп больных СД 2 типа «ДН+» и «ДН-» приведено в Таблице 7.
Таблица 7. Частота аллелей и генотипов полиморфного маркера Rro12Ala гена PPARG2 в исследуемых группах больных СД 2 типа «ДН+» и «ДН-»
| Генотипы и аллели | Группа «ДН-» | Группа «ДН+» | р |
| Генотип Pro12Pro | 0,55 | 0,48 | нд |
| Генотип Pro12Ala | 0,43 | 0,48 | нд |
| Генотип Ala12Ala | 0,02 | 0,04 | нд |
| Аллель 12Pro | 0,77 | 0,72 | нд |
| Аллель 12Ala | 0,23 | 0,28 | нд |
Как следует из результатов, представленных в Таблице 7, достоверные различия в частоте аллелей и генотипов полиморфного маркера Pro12Ala гена PPARG2 в группах больных СД 2 типа «ДН+» и «ДН-» отсутствовали. Таким образом, в исследуемой выборке больных СД 2 типа мы не выявили ассоциации данного полиморфного маркера с генетической предрасположенностью к возникновению ДН.
Кардиоренальные взаимоотношения у больных СД 2 типа и ожирением
Мы оценивали взаимосвязь эхокардиографических признаков поражения миокарда левого желудочка – развития ремоделирования – с наличием ожирения и частотой ранних стадий ДН у больных СД 2 типа. При сравнении групп больных СД 2 типа с ожирением (ИМТ 30 кг/м2) и без ожирения (ИМТ < 30 кг/м2) при длительности СД более 5 лет признаки гипертрофии миокарда чаще присутствовали в группе больных с ожирением: 53% и 32% соответственно. (Рис.7) При длительности СД менее 5 лет различия не определялись.
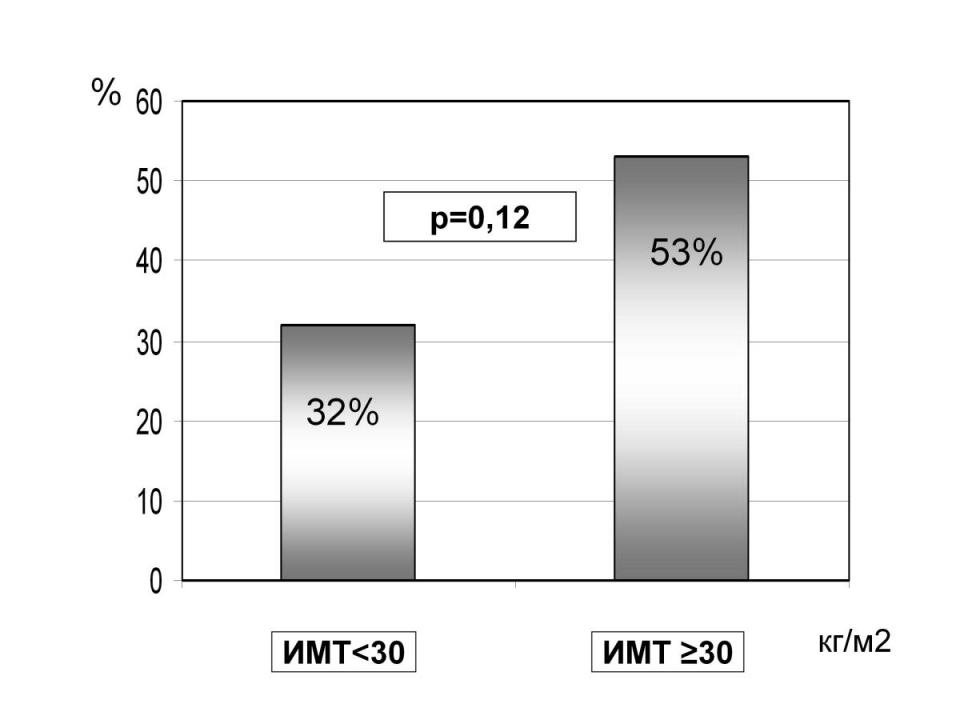
Рис.7 Частота гипертрофии миокарда левого желудочка в группах больных СД 2 типа с ожирением (ИМТ 30 кг/м2) и без ожирения (ИМТ < 30 кг/м2) при длительности СД более 5 лет
Частота гипертрофии левого желудочка при длительности СД более 5 лет зависела от степени ожирения, причем выявлены отличия у мужчин и женщин: у женщин гипертрофия миокарда развивалась чаще. (Рис.8)
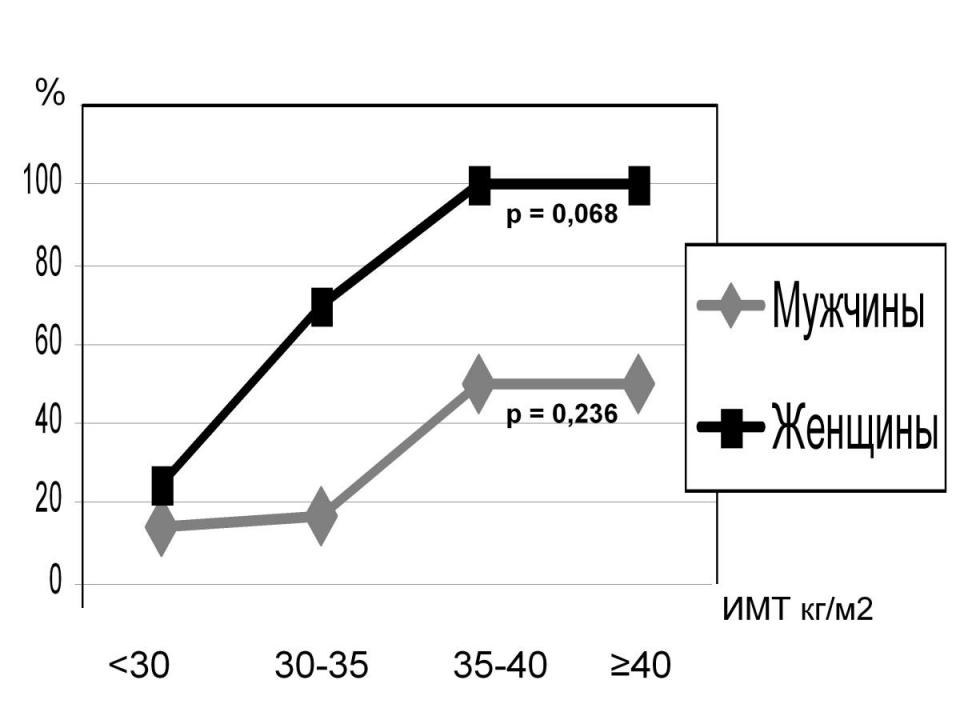
Рис.8 Частота гипертрофии миокарда левого желудочка в зависимости от пола и ИМТ при длительности СД более 5 лет
При оценке типа геометрии сердца в группе больных СД 2 типа с ожирением наиболее часто отмечено формирование концентрической гипертрофии миокарда – порядка 50 % и в 3 % случаев – эксцентрической гипертрофии. В группе больных без ожирения преимущественно развивалось концентрическое ремоделирование миокарда – в 63% случаев. (Рис. 9)

Рис. 9 Типы геометрии левого желудочка в группах больных СД 2 типа без ожирения (ИМТ<30 кг/м2) и с ожирением (ИМТ30 кг/м2)
При оценке взаимосвязи процессов ремоделирования миокарда левого желудочка с развитием поражения почек при длительности СД 2 типа более 5 лет по мере нарастания тяжести ДН, увеличивалась частота концентрической гипертрофии миокарда, при этом уменьшалась частота концентрического ремоделирования. Так в группе больных с НАУ – частота концентрического ремоделирования составляла 55%, концентрической гипертрофии – 37%, при появлении МАУ - частота концентрического ремоделирования составляла 45%, концентрической гипертрофии – 44%, при появлении ПУ – частота концентрического ремоделирования – 33% и гипертрофии - 50 %. (Рис. 10)
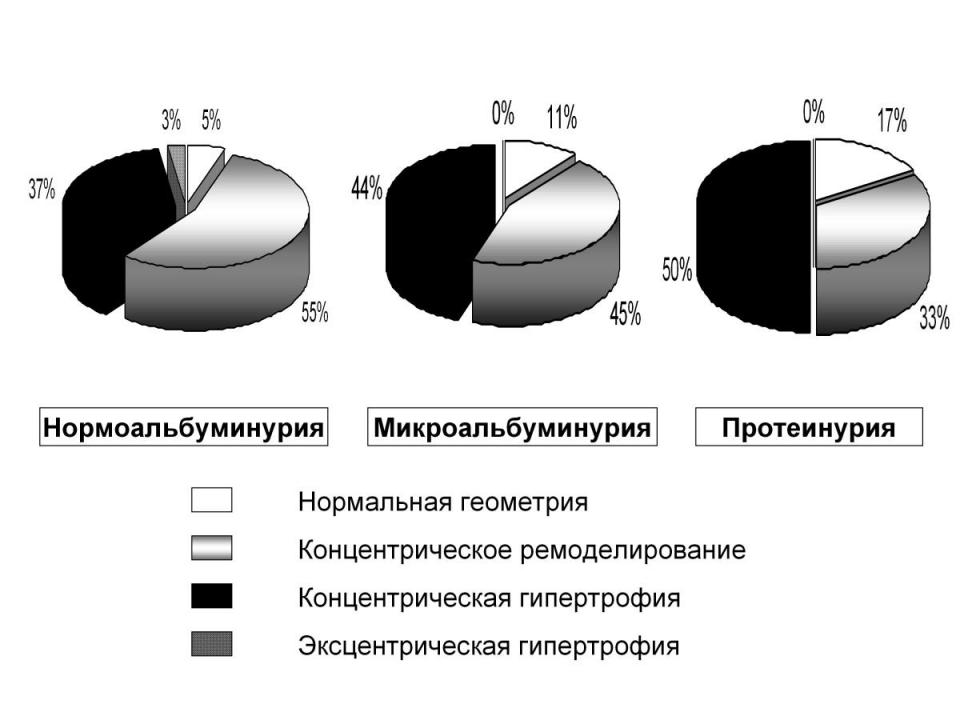
Рис. 10 Типы геометрии левого желудочка в зависимости от уровня альбуминурии при длительности СД более 5 лет
Данные корреляционного анализа также свидетельствуют о взаимосвязи гипертрофии миокарда с развитием ДН: установлена взаимосвязь индекса массы миокарда с уровнем альбуминурии (r=0,455 p=0,009).
При оценке факторов, связанных с развитием гипертрофии миокарда, помимо антропометрических показателей, значимыми оказались уровень мочевой кислоты в сыворотке крови и гликированный гемоглобин, что отражает тесную взаимосвязь расстройств пуринового и углеводного обменов с ожирением и процессами ремоделирования миокарда. Учитывая данные экспериментальных исследований, свидетельствующих о влиянии гормональной активности жировой ткани, в частности уровней лептина и адипонектина, на процессы ремоделирования миокарда, мы также анализировали данные показатели [Majane O. et al., 2009; Rajapurohitam V. et al., 2003]. Однако достоверные взаимосвязи уровней лептина и адипонектина с выраженностью гипертрофии миокарда нами не установлены. (Табл. 8)
Таблица 8. Взаимосвязь факторов риска ДН и индекса массы миокарда левого желудочка (ИММЛЖ) при длительности СД более 5 лет
| Показатели | ИММЛЖ | Показатели | ИММЛЖ |
| ИМТ, кг/м2 | r=0,304, p=0,023 | Липидный спектр | ns |
| ОТ, см | r=0,360, p=0,007 | САД, ммрт.ст. | ns |
| ОБ, см | r=0,293, p=0,030 | ДАД, ммрт.ст. | ns |
| ОТ/ОБ | r=0,261, p=0,054 | Длительность АГ, годы | ns |
| Мочевая кислота, мкмоль/л | r=0,446, p=0,010 | Лептин, нг/мл | ns |
| НвА1с, % | r=0,274, p=0,045 | Адипонектин, нг/мл | ns |
ВЫВОДЫ
- При СД 2 типа абдоминальное ожирение наряду с нарушениями углеводного обмена и систолической артериальной гипертензией является самостоятельным фактором риска поражения почек (окружность талии - =0,384, В=0,01, р=0,0027; гликированный гемоглобин - =0,389, В=0,08, р=0,001; САД - =0,336, В=0,009, р=0,014). В группе больных СД 2 типа с ожирением частота гиперфильтрации, микроальбуминурии и протеинурии выше, по сравнению с больными СД 2 типа без ожирения при равной длительности СД.
- Более частое поражение почек у больных СД 2 типа с ожирением обусловлено ассоциированными с ожирением нарушениями липидного и пуринового обменов, а также нарушениями системной гемодинамики (артериальной гипертензией) и внутрипочечной гемодинамики (гиперфильтрацией), дисбалансом гормонов жировой ткани (лептина и адипонектина).
- Гиперлептинемия сопряжена с развитием артериальной гипертензии, появлением протеинурии. Снижение протективного гормона жировой ткани – адипонектина - характерно для больных СД 2 типа без признаков ДН и с начальными проявлениями ДН (микроальбуминурией). При дальнейшем прогрессировании поражения почек и появлении протеинурии, уровень адипонектина нарастает, что связано с компенсаторными механизмами, направленными на усиление нефропротективного эффекта.
- Взаимосвязи полиморфного маркера Pro12Ala гена PPARG2 с риском развития диабетической нефропатии в исследуемой группе больных СД 2 типа не выявлено.
- Раннему формированию кардиоренального синдрома при СД 2 типа способствует наличие ожирения, за счет ассоциированных с ожирением гемодинамических и метаболических расстройств (ОТ и степень АГ - r=0,297; p=0,0001; ОТ и ЛПВП - r= -0,161; p=0,074; ОТ и мочевая кислота - r=0,443; p=0,0001). При увеличении степени ожирения нарастает выраженность гипертрофии миокарда (ИМТ и ИММЛЖ - r=0,304; p=0,023) и уровень альбуминурии (ИМТ и МАУ - r=0,331; p=0,016; ИММЛЖ и МАУ - r=0,455; p=0,009).
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- При СД 2 типа больных с ожирением следует относить к группе повышенного риска развития ДН, в связи с чем, в данной группе больных СД 2 типа необходимы постоянный контроль МАУ, ПУ и проведение профилактических мероприятий, направленных на снижение массы тела, в первую очередь за счет соблюдения диетических рекомендаций, активного образа жизни.
- Профилактика ДН у больных СД 2 типа с ожирением должна включать рекомендации по контролю гликемии, АД, коррекции клубочковой гипертензии, дислипидемии, нарушений пуринового обмена.
- При СД2 типа ожирение способствует ремоделированию миокарда и раннему формированию кардиоренального синдрома, в связи с чем рекомендуется включать в комплекс обследования больных СД 2 типа с начальными стадиями ДН эхокардиографическое исследование.
- Для профилактики развития ремоделирования миокарда и раннего формирования кардиоренального синдрома у больных СД 2 типа с ожирением, помимо контроля АД, уровня гликемии, необходимо проводить коррекцию нарушений липидного и пуринового обменов (за счет соблюдения диеты, при неэффективности - показан прием гиполипидемических препаратов, ингибитора ксантиноксидазы).
СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Савельева С.А., Крячкова А.А., Кутырина И.М., Шестакова М.В. Роль лептина и адипонектина в поражении почек у больных с метаболическим синдромом. Всероссийский конгресс нефрологов: материалы конгресса. Нефрология 2009; 3 (13): 79-80.
- Савельева С.А., Крячкова А.А., Кутырина И.М., Шестакова М.В. Роль лептина и адипонектина в поражении почек у больных сахарным диабетом 2 типа. Тезисы VI конференции РДО. Нефрология и диализ 2009; 4(11): 331.
- Савельева С.А., Крячкова А.А. Роль ожирения в поражении почек у больных сахарным диабетом 2 типа. Итоговая научная конференция молодых исследователей с международным участием «Татьянин день»: тезисы М., 2010; с. 154-155.
- Крячкова А.А., Савельева С.А., Галлямов М.Г. Инсулинорезистентность и функциональные параметры почек у больных с избыточной массой тела и ожирением. Итоговая научная конференция молодых исследователей с международным участием «Татьянин день»: тезисы М., 2010; с. 88-89.
- Крячкова А.А., Савельева С.А., Галлямов М.Г., Шестакова М.В., Кутырина И.М. Роль ожирения в поражении почек при метаболическом синдроме. Нефрология и диализ 2010; 1(12): 34-39.
- Савельева С.А., Крячкова А.А., Курумова К.О, Шамхалова М.Ш., Кутырина И.М., Шестакова М.В. Ожирение – фактор риска поражения почек у больных сахарным диабетом 2 типа. Сахарный диабет 2010; 2:45-50.
- Кутырина И.М., Савельева С.А., Крячкова А.А., Шестакова М.В. Вклад ожирения в поражение почек у больных сахарным диабетом 2 типа. Терапевтический архив 2010; N6: 21-25.
- Кутырина И.М., Крячкова А.А., Савельева С.А., Шестакова М.В. Роль альдостерона в поражении почек при метаболическом синдроме, ассоциированном с ожирением. Клиническая нефрология 2010; 4: 34-39.
- Савельева С.А., Крячкова А.А., Железнякова А.В., Курумова К.О., Викулова О.К., Шамхалова М.Ш., Кутырина И.М., Шестакова М.В. Исследование полиморфного маркера Pro12Ala гена формы рецепторов, активируемых пролифераторами пероксисом, у больных сахарным диабетом 2 типа с диабетической нефропатией. Сборник тезисов VII съезда Научного общества нефрологов России. М. 2010; с. 110-111.
- Kryachkova A., Savelieva S., Gallyamov M., Kutyrina I. Insulin resistance and renal injuri in patients with obesity and various polymorphism of gene PPAR. XLVII ERA-EDTA CONGRESS -II DGfN CONGRESS June 25-28, 2010, Munich, Germany. Nephrology Dialysis Transplantation Plus 2010- 3 (Supplement 3): iii 436.
СПИСОК СОКРАЩЕНИЙ
АГ – артериальная гипертензия
АД – артериальное давление
ДАД – диастолическое артериальное давление
ДН – диабетическая нефропатия
ИММЛЖ – индекс массы миокарда левого желудочка
ИМТ – индекс массы тела
ИОТ – индекс относительной толщины стенки левого желудочка
КДР - конечно-диастолический размер
ЛПВП – липопротеиды высокой плотности
ЛПНП – липопротеиды низкой плотности
МАУ – микроальбуминурия
ММЛЖ – масса миокарда левого желудочка
НАУ – нормоальбуминурия
ОБ – окружность бедер
ОТ – окружность талии
ОТ/ОБ – отношение окружности талии к окружности бедер
ПУ – протеинурия
САД – систолическое артериальное давление
СД – сахарный диабет
СКФ – скорость клубочковой фильтрации
ТГ– триглицериды
ТЗСЛЖ – толщина задней стенки левого желудочка
ТМЖП – толщина межжелудочковой перегородки
ХС – общий холестерин
НвА1с – гликированный гемоглобин
PPAR - -форма рецепторов, активируемых пролифераторами пероксисом

