Патогенетическое обоснование эрадикации h.pylori при осложненном течении язвенной болезни двенадцатиперстной кишки
На правах рукописи
ПОПОВ
Евгений Александрович
ПАТОГЕНЕТИЧЕСКОЕ ОБОСНОВАНИЕ ЭРАДИКАЦИИ H.PYLORI
ПРИ ОСЛОЖНЕННОМ ТЕЧЕНИИ ЯЗВЕННОЙ БОЛЕЗНИ
ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ
14.01.17 - хирургия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Санкт-Петербург
2010
Работа выполнена в Федеральном государственном образовательном учреждении высшего профессионального образования «Военно-медицинская академия им. С.М. Кирова» Министерства обороны РФ на кафедре военно-морской и госпитальной хирургии.
Научный руководитель:
доктор медицинских наук профессор Назаров Виталий Евгеньевич
Официальные оппоненты:
доктор медицинских наук профессор Плотников Юрий Владимирович
доктор медицинских наук профессор Синенченко Георгий Иванович
Ведущая организация:
ГОУВПО «Санкт-Петербургский государственный медицинский университет им. академика И.П. Павлова» Росздрава
Защита диссертации состоится 11 марта 2010 г. в «___» часов на заседании диссертационного совета Д 208.086.01. при Государственном образовательном учреждении высшего профессионального образования «Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова Федерального агентства по здравоохранению и социальному развитию» (195067, Санкт-Петербург, Пискаревский проспект, д. 47).
С диссертацией можно ознакомиться в библиотеке Государственного образовательного учреждения высшего профессионального образования «Санкт-Петербургская государственная медицинская академия им. И.И. Меч-никова Федерального агентства по здравоохранению и социальному развитию».
Автореферат разослан «___» ___________ 2010 г.
Ученый секретарь
диссертационного совета
доктор медицинских наук профессор Ю.П.Успенский
Введение
Актуальность проблемы.
В течение жизни язвенной болезнью страдают 10-15% населения (Барановский А.Ю., Назаренко Л.И., 2006; Краснов О. А., 2009; Маев И.В., Самсонов А.А., 2009). Открытие Helicobacter pylori заставило пересмотреть существующие концепции ульцерогенеза, существенно изменило стратегию и тактику лечения язвенной болезни (Поташев Л.В. и соавт., 1999; Goodwin C.S., 1988; Malfertheiner P. et al., 2007). Современная фармакотерапия, включающая эрадикацию H.pylori, сместила акцент хирургии язвенной болезни с плановых оперативных вмешательств в сторону ургентной хирургии язвенных осложнений (Власюк С.Б., 2005; Синенченко Г.И. и соавт., 2007). Вместе с тем, многочисленными исследованиями доказано, что противоязвенная и эрадикационная терапия являются основными факторами, улучшающими отдаленные результаты оперативных вмешательств. При эрадикации H.pylori частота рецидивов и осложнений существенно снижается и составляет не более 6 % и 2-4 % соответственно (Погосян Г.Э., 2007; Чекмасов Ю.С., 2007; Липницкий Е.М., Алекберадзе А.В., 2008; Хасанов А.Г. и соавт., 2009;Macri G.,1998; Powell K.U., 1994; el Nakeeb A. et al., 2009).
Однако, не смотря на все эти достижения последних 10 лет, число осложнений язвенной болезни, требующих хирургического лечения, не уменьшается, а по свидетельству некоторых авторов даже увеличивается (Синенченко Г.И. и соавт., 2007; Иванова Е.В., 2008; Краснов О. А., 2009). Одной из причин роста числа, как осложнений язвенной болезни, так и рецидивов после оперативного лечения, называется низкая эффективность эрадикационной терапии, проводимой стандартными схемами (Власюк С.Б., 2005; Барановский А.Ю., Назаренко Л.И., 2006; Погосян Г.Э., 2007).
Анализ отечественной и зарубежной литературы показывает, что этот вопрос при осложненных формах язвенной болезни на сегодняшний день практически не изучен: не решен вопрос выбора схем эрадикационной терапии (тройной или квадротерапии), ее места комплексной фармакотерапии язвенной болезни, длительности и времени ее назначения. До сих пор должным образом не освещена роль H.pylori в возникновении осложнений язвенной болезни ДПК. Неизвестно, есть ли какие-либо определенные специфические механизмы развития тяжелого течения язвенного процесса с вовлечением H.pylori (Поташев Л.В., 1999; Подчеко П.И., 2006).
Другой немаловажной причиной низкой эффективности эрадикационной терапии является проведение консервативного лечения при осложненной язвенной болезни врачами терапевтического профиля, которые не владеют в полном объеме знаниями патогенеза и течения осложненных форм (Синенченко Г.И. и соавт., 2007).
Все это настоятельно диктует необходимость изучения роли H.pylori в развитии осложненных форм язвенной болезни и разработки современных подходов к эрадикации H.pylori с учетом хирургической практики.
Цель исследования.
На основе изучения патогенетических механизмов взаимодействия H.pylori со слизистой оболочкой антрального отдела желудка и двенадцатиперстной кишки обосновать оптимальную тактику эрадикационной терапии H.pylori у больных с осложненным течением язвенной болезни двенадцатиперстной кишки.
Задачи исследования.
1. Оценить возможности, валидность иммунногистохимического и иммуноцитохимического методов окраски биоптатов и их значение для определения патогенетических механизмов взаимодействия H.pylori со слизистой оболочкой.
2. Определить особенности взаимодействия H.pylori со слизистой оболочкой антрального отдела желудка и двенадцатиперстной кишки в зависимости от патофизиологических изменений функции желудка, при различных осложнениях язвенной болезни двенадцатиперстной кишки, а так же в основные периоды течения заболевания.
3. Уточнить характер изменений в слизистой оболочке антрального отдела желудка и двенадцатиперстной кишки, возникающих в ответ на присутствие H.pylori и их роль в развитии осложнений при язвенной болезни двенадцатиперстной кишки.
4. Основываясь на выявленных патогенетических механизмах взаимодействия H.pylori со слизистой оболочкой антрального отдела желудка и двенадцатиперстной кишки, обосновать дифференцированный подход к проведению эрадикационной терапии при различных осложнениях язвенной болезни двенадцатиперстной кишки.
Научная новизна.
Впервые применены иммунные методы окраски для оценки взаимодействия H.pylori со слизистой оболочкой антрального отдела желудка и двенадцатиперстной кишки при осложненном течении язвенной болезни двенадцатиперстной кишки. Проведены ИГХ и ИЦХ параллели не только для диагностики, но и для трактовки механизмов взаимодействия H.pylori со слизистой оболочкой антрального отдела желудка и ДПК. Оценено распределение антигена H.pylori в слоях слизистой оболочки антрального отдела желудка и двенадцатиперстной кишки при различных осложнениях и в различные периоды течения язвенной болезни двенадцатиперстной кишки. Выявлены специфические фиксированные иммунные комплексы в слизистой оболочке антрального отдела желудка и ДПК и показана их роль в патогенезе язвенной болезни. Обоснован с точки зрения патогенеза дифференцированный подход к эрадикационной терапии H.pylori при различных осложнениях язвенной болезни двенадцатиперстной кишки.
Практическая значимость полученных результатов.
Изученные особенности течения инфекционного процесса, вызываемого H.pylori, выявленные особенности патогенеза осложненной язвенной болезни двенадцатиперстной кишки и некоторые механизмы возникновении рецидивов заболевания позволили обосновать дифференцированную тактику эрадикационной терапии у больных с осложненным течением язвенной болезни двенадцатиперстной кишки, а именно уточнить схемы и сроки проведения эрадикационной терапии, обосновать использование иммуннотропных препаратов в зависимости от формы осложнения, уточнить место эрадикации H.pylori в комплексной терапии язвенной болезни.
Положения, выносимые на защиту.
1. Иммуногистохимический и иммуноцитохимический методы окраски биоптатов являются высокоспецифичными, надежными и позволяют выявлять некоторые патогенетические механизмы взаимодействия H.pylori со слизистой оболочкой.
2. При осложненном течении язвенной болезни ДПК вследствие патофизиологических изменений функции желудка, нарушения барьерной функции слизистой оболочки H.pylori (или его разрушенные фрагменты) способны проникать субэпителиально, вызывая ответную воспалительную реакцию слизистой.
3. Возможным ключевым звеном в патогенезе развития язвенной деструкции слизистой двенадцатиперстной кишки может являться образование специфических фиксированных иммунных комплексов, содержащих в своем составе антиген H.pylori.
4. Комплексная противоязвенная терапия при осложненных формах язвенной болезни ДПК должна строиться с учетом особенностей патогенеза H.pylori инфекции и преследовать не только искоренение жизнеспособных форм H.pylori, но и снижение концентрации антигена H.pylori в слоях слизистой оболочки, что будет способствовать уменьшению локального воспалительного процесса, обрыву иммунопатологических процессов в слизистой и профилактике рецидивов.
Реализация и внедрение результатов исследований.
По теме диссертации опубликовано 9 научных работ (из них 1 монография, 3 статьи в журнале, рекомендованном ВАК). Результаты диссертационной работы внедрены в практику ГУ «СЗОМЦ Минздрава России», НИИ скорой помощи им. И.И.Джанелидзе, ГУЗ «Городской консультативно-диагностический центр №1» г. Санкт-Петербурга. Материалы диссертации используются в учебном процессе на кафедре военно-морской и госпитальной хирургии Военно-медицинской академии им. С.М.Кирова. По результатам диссертационной работы опубликованы методические рекомендации.
Апробация работы.
Основные материалы диссертации доложены на научно-практической конференции «Современные диагностические и лечебные технологии в многопрофильной клинике», посвященной 145-летию ФГУ «Северо-Западный окружной медицинский центр» Федерального агенства по здравоохранению и социальному развитию (Санкт-Петербург, 2006 г.), юбилейной конференции «Современные технологии в хирургии», посвященной 120-летию кафедры хирургии им. Н.Д.Монастырского СПб МАПО и 10-летию центра неотложной ЭВХ Александровской больницы (Санкт-Петербург, 2006 г.), VIII Всероссийской научно-практической конференции: «Актуальные вопросы диагностики и лечения в многопрофильном учреждении» (Санкт-Петербург, 2007 г.).
Структура и объем диссертации.
Диссертационная работа состоит из введения, 5 глав, заключения, выводов, практических рекомендаций и библиографического указателя. Работа изложена на 171 странице машинописного текста, содержит 17 таблиц и 32 рисунков. Список литературы включает 214 наименований работ (71 отечественных и 143 иностранных авторов).
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования
В работе использованы результаты обследования и лечения 248 больных, получавших лечение на кафедре военно-морской и госпитальной хирургии ВМА им. С.М.Кирова, НИИ скорой помощи им. И.И.Джанелидзе, Николаевской больнице г.Санкт-Петербург (в период с 2003 по 2008 гг.). Основную группу составили 150 больных с осложненной язвенной болезнью ДПК: 29 больных с перфоративной язвой, 39 – с кровотечением, 36 – с пилородуоденальным стенозом, 46 – с частым рецидивированием или длительным заживлением язвы.
Контрольную группу составили больные неосложненной язвенной болезнью двенадцатиперстной кишки (65 человек) и хроническим гастродуоденитом (33 человек). Больным контрольной группы проводилось традиционное противоязвенное лечение, принципы которого изложены в «Стандартах (протоколах) диагностики и лечения болезней органов пищеварения», утвержденных приказом Министерства здравоохранения Российской Федерации от 17.04.1998 № 125.
Среди лечившихся больных 172 (69,2%) человек были мужчины, а 76 (30,8%) – женщины. Средний возраст больных составил 43,8+1,23 года (от 17 до 80 лет). Основную группу исследуемого контингента составили пациенты трудоспособного возраста – от 24 до 60 лет (78,7%).
Пациентам проводили контроль эффективности эрадикационной терапии через 4 недели после ее окончания и повторные тесты на H.pylori через 3, 6 и 9 месяцев от завершения курса эрадикационной терапии. С этой целью выполнялась ФЭГДС по общепринятой методике с одновременной многозональной биопсией слизистой антрального отдела желудка и луковицы ДПК.
Функцию желудка исследовали методом внутрижелудочной многозональной реогастрографии. Определялись показатели секретообразования (ПС) и нейтрализации (ПН), а так же рН в теле (рНтела) и антральном отделе (рНантр.) желудка.
Выявление H.pylori осуществлялось с помощью уреазного теста и гистологически, в соответствие с методическими указаниями «Диагностика, лечение и профилактика обострений и осложнений кислотозависимых и хеликобактерзависимых заболеваний» (1997). Основными методами морфологической диагностики были иммуногистохимический (ИГХ) и иммуноцитохимический (ИЦХ). Материалом для исследования явились биоптаты слизистой оболочки желудка и ДПК, полученные интраоперационно, а так же при выполнении ФЭГДС. Объем и структура гистологических исследований представлены в табл. 1.
Таблица 1.
Объем и структура гистологических исследований
(количество изученных биоптатов).
| Варианты течения язвенной болезни | Периоды течения заболевания | Всего | |||
| Обострение | Рубцевание | 1 мес | 3 и более мес | ||
| Неосложненная | 8 | 7 | 5 | 6 | 26 |
| Часто рецидив. | 9 | 6 | 8 | 12 | 35 |
| Кровоточащая | 10 | 9 | 12 | 11 | 42 |
| Стеноз | 12 | 6 | 7 | 12 | 37 |
| Перфорация | 12 | 6 | 5 | 8 | 31 |
| Итого | 51 | 34 | 37 | 49 | 171 |
Полученные биоптаты использовались как для окраски гематоксилин-эозином, так и для ИГХ окраски. ИГХ окрашивание на выявление H.pylori проводили с применением поликлональных кроличьих антител (B0471, Dako) против CH-20 429 специфического антигена клеточной стенки бактерии и системы визуализации DAKO Envisionтм. ИЦХ исследованию подверглись 39 биоптатов от больных с различными формами ЯБ ДПК.
Одним из основных лабораторных методов исследования явилось определение специфических фиксированных на слизистой оболочке желудка и ДПК иммунных комплексов (СФИК), содержащих антиген H.pylori. Выделение иммунных комплексов и измерение их уровней проводили по методу, описанному Digeon M. (1977) в модификации Т.А.Рязанцевой (1984). Определение антигенов H.pylori в составе СФИК осуществляли методом реакции коагглютинации на стекле с использованием диагностикума производства НИИЭМ им. Н.Ф. Гамалеи (Москва).
Для статистической обработки наблюдений использовались непараметрические методы. Оценку значимости различий производили с помощью 2- критерия Пирсона, точного критерия Фишера, вычисления рангового коэффициента корреляции и расчетом коэффициента связи (коэффициент сопряженности).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Обоснование использования иммунных методов окраски при морфологическом исследовании биоптатов слизистой оболочки желудка и ДПК.
Выбор в пользу иммунных методов окраски (ИГХ и ИЦХ) был продиктован тем, что они позволяют выявлять не только спиралевидные и кокковые формы H.pylori, но и фрагменты разрушенных бактерий, сохранившие антигены клеточных стенок, и, тем самым, оценивать расположение антигенов клеточной стенки H.pylori относительно слоев слизистой оболочки. В подавляющем большинстве случаев при ИГХ выявлялась специфическая окраска в виде глыбок или комочков (ДАБ-позитивный коричневый субстрат), которую мы в дальнейшем определили как «антигены бактерий», подразумевая, что за этим стоит окраска фрагмента клеточной стенки H.pylori.
При анализе расположения специфически окрашенных участков (ИГХ) были выделены следующие категории: антигены бактерий, расположенные в слое слизи, а так же между эпителиоцитами. Впервые, применительно к осложненным вариантам ЯБ ДПК, обнаружен специфически окрашенный антиген в эпителиоцитах, в строме слизистой оболочки и среди клеток воспалительного инфильтрата (рис.1-2). Объяснение данных фактов может быть двояким: 1) H.pylori способен проникать в субэпителиальный слой в жизнеспособном или разрушенном состоянии; 2) имеет место неспецифическое окрашивание эпителиальных клеток. Поэтому для исключения неспецифического окрашивания материала мы выполнили ряд исследований:
1.Контрольную постановку ИГХ реакции без первичных антител. Из общей группы было отобрано 5 препаратов с верифицированным наличием H.pylori (с помощью уреазного и гистологического метода). При постановке реакции без первичных антител специфической окраски в препаратах ни в одном случае не наблюдалось.
2.Сравнение результатов диагностики H.pylori ИГХ и ИЦХ методами, используя в качестве материала один и тот же биоптат. Всего в параллельных опытах было изучено 39 биоптатов от больных с различными формами ЯБ ДПК. Совпадение результатов ИГХ и ИЦХ методов было в 38 из 39 случаев.
3. Сравнили результаты ИГХ метода с результатами быстрого уреазного теста и гистологического исследования. Результаты, полученные при применении ИГХ метода, не противоречили данным, полученным с помощью уреазного и гистологического тестов.
Проведенные исследования позволили заключить, что ИГХ метод, выполненный на высоком техническом уровне, является достоверным специфическим методом выявления антигена H.pylori. Специфическая окраска, наблюдаемая в слизи, между или в эпителиоцитах, а так же в клетках инфильтрата в строме обусловлена окрашиванием антигена H.pylori. Это относится и к случаям, когда в ИГХ препаратах морфология бактерий не определяется.

Рис.1. H.pylori и\или его антиген (окрашен в коричневый цвет) ИГХ с
поликлональными антителами против H.pylori., ДАБ, гематоксилин.
а – в слизи и внутри эпителиоцитов, х1000;
б – в просвете эпителиоцита, х1000;
в - в просвете пилорической железы, х 200;
г – в слизи и апикальной части эпителиоцитов (тот же препарат, что и
на рис. «в»), х1000.

Рис. 2. Специфически окрашенный антиген H.pylori. ИГХ с
поликлональными антителами против H.pylori., ДАБ, гематоксилин.
а – в строме слизистой, х 200;
б – субэпителиально (тот же препарат, что и на рисунке «а»), х 1000;
в – в строме слизистой, х 200;
г – среди клеток воспалительного инфильтрата, х 200.
Основные варианты взаимодействия H.pylori со слизистой оболочкой
Сравнение частоты внутриклеточной локализации антигена H.pylori при гастродуодените, неосложненном и осложненных вариантах язвенной болезни ДПК. Частота выявления специфически окрашенного антигена H.pylori внутри эпителиоцитов и субэпителиально в биоптатах, взятых от больных с язвенной болезнью, была достоверно (р < 0,001) выше (23-100%), чем в биоптатах, взятых от больных хроническим гастритом (0%) (табл.2).
Таблица 2.
Частота внутриэпителиального и субэпителиального
обнаружения антигена H.pylori
| Частота обнаружения антигена | Всего биоптатов | ||
| внутри эп-цитов | в к-ках инфильтрата | ||
| Хронический гастрит | - | - | 20 |
| Вариант течения язвенной болезни | |||
| Неосложненное течение | 6 (23%) | 6 (23%) | 26 |
| Перфорация | 31 (100%) | 9 (29%) | 31 |
| Часто рецидивирующее течение | 10 (28,6%) | 3 (8,6%) | 35 |
| Кровотечение | 11 (26,2%) | 2 (4,8%) | 42 |
| Стеноз | 10 (27%) | 3 (10 %) | 37 |
| Итого | 68 (35,6%) | 23 (12,0%) | 191 |
Таким образом, если в случае хронического гастрита проникновение бактерий H.pylori (или их фрагментов) внутрь эпителиоцитов и субэпителиально скорее исключение из правил, то при язвенной болезни, особенно при осложненном ее течении, – это распространенное явление, которое может являться важным звеном в патогенезе развития заболевания. Полученные данные заставили нас проанализировать факторы, влияющие на локализацию антигена H.pylori в различных слоях слизистой оболочки.
Варианты взаимодействия H.pylori со слизистой оболочкой в зависимости от патофизиологических изменений функции желудка, варианта и периода язвенной болезни. Выявлена прямая ранговая сильно выраженная корреляционная связь между увеличением концентрации антигена H.pylori в слизи и 1) гиперсекрецией в стадию обострения (мы связываем это с разрушением бактерий) (рис.3), 2) гипосекрецией спустя 3 месяца от рубцевания язвенного дефекта (возможное объяснение-размножение бактерий при данных условиях). Так же выявлена корреляционная связь между увеличением концентрации антигена H.pylori внутри эпителиоцитов и в клетках инфильтрата и такими факторами, как ослабление/потеря защитных свойств слизистой (рис.4), снижение рН антрального отдела желудка, повышение рН в теле желудка.

Рис. 3. Распределение антигена H.pylori в слоях слизистой в зависимости от показателя секреции, стадия обострения.

Рис. 4. Распределение антигена H.pylori в слоях слизистой в зависимости от показателя нейтрализации
Выявлено так же, что наибольшая частота обнаружения антигена H.pylori была характерна для перфоративной язвы ДПК, причем, как в целом в биоптатах, так и в разных слоях слизистой; наименьшая – для язвенных кровотечений (табл. 3). При послойном сравнении было выявлено, что наибольшая диспропорция между концентрацией антигена, расположенного внеклеточно (в слизи и между эпителиоцитов) и внутриклеточно (внутри эпителиоцитов и в клетках инфильтрата) ( в 2,5 раза) была характерна для часторецидивирующего течения язвенной болезни.
Таблица 3.
Частота обнаружения антигена H.pylori в биоптатах в зависимости от варианта течения ЯБ ДПК
| Вариант течения язвенной болезни | Количество биоптатов, в которых обнаружен специфически окрашенный антиген (абс.(%)) | ||||
| в целом в биоптатах | в слизи | между эпителиоцитов | внутри эпител-ов и в кл-х инфильтрата | Общее число бип-тов | |
| Перфорация | 31 (100%) | 21 (67,7%) | 0 | 31 (100%) | 31 |
| Неосложненная | 19 (73,1%) | 16 (61,5%) | 3 (11,5%) | 12 (46%) | 26 |
| Часто рецидивирующая | 25 (71,4%) | 22 (62,9%) | 10 (28,6%) | 13 (37,1%) | 35 |
| Кровотечение | 22 (52,4%) | 14 (33,3%) | 10 (23,8%) | 13 (31%) | 42 |
| Стеноз | 22 (59,4%) | 16 (43,2%) | 8 (21,6%) | 14 (37,8%) | 37 |
Аналогичная закономерность характерна для язвенного кровотечения (разница частоты встречаемости 2 раза), стеноза (разница частоты встречаемости 1,7 раза), неосложненной язвенной болезни (разница частоты встречаемости 1,5 раза). Принципиально отличается вариант перфоративной язвы. В этом случае, напротив, частота встречаемости антигенного материала внутри эпителиоцитов и в клетках инфильтрата была больше, чем в слизи и между эпителиоцитов ( в 1,5 раза).
При сопоставлении частоты выявления антигена H.pylori и периодов язвенной болезни прослеживалась четкая тенденция: увеличение частоты обнаружения антигена H.pylori в период рубцевания во всех слоях слизистой, с последующим снижением по мере заживления язвенного дефекта (табл.4). При безуспешной эрадикационной терапии представляет интерес падение концентрации антигена H.pylori в субэпителиальном слое (до 21,9%) при одновременном нарастании концентрации антигена в слизи (до 78,1%) через 3 месяца и более от момента заживления. Это можно объяснить восстановлением барьерной функции слизистой оболочки в указанные сроки.
При успешной эрадикационной терапии, наибольшая частота выявления антигена в биоптатах (в целом) была характерна для стадии рубцевания (в 63,2%), что в 3 раза больше, чем в фазу обострения (р=0,002), в 1,5 раза больше, чем спустя 1 мес от рубцеваниия и в 6 раз больше, чем спустя 3 мес (р=0,002), когда нарастания концентрации антигена в слизистой не происходило, а частота выявления антигена межэпителиально и субэпителиально равнялась нулю.
Таблица 4.
Частота обнаружения антигена H.pylori в биоптатах в зависимости от периода язвенной болезни (при безуспешной эрадикационной терапии)
| Период язвенной болезни | Частота обнаружения антигена H.pylori, абс (%) | ||||
| в целом в биоп-тах | в слизи | между эпи-тов | внутри- и субэпит-но | Общее число биоп-тов | |
| Обострение | 22 (91,6%) | 12 (50%) | 12 (50%) | 10 (41,7%) | 24 |
| Рубцевание | 15 (100%) | 13 (86,7%) | 7 (46,7%) | 10 (66,7%) | 15 |
| 1 месяц | 17 (100%) | 10 (58,8%) | 2 (11,8%) | 12 (70,6%) | 17 |
| > 3 месяцев | 25 (78,1%) | 25 (78,1%) | 12 (37,5%) | 7 (21,9%) | 32 |
При обострении концентрация антигена H.pylori в слизи (50%), между эпителиоцитами (50%) и в подслизистом слое (41,7%) приблизительно находится на одном уровне, что может говорить о несостоятельности барьерной функции слизистой оболочки (рис.5).

Рис. 5. Частота обнаружения антигена H.pylori (%) в биоптатах слизистой желудка и ДПК в зависимости от периода язвенной болезни (при успешной эрадикационной терапии).
В последующем, через 1 месяц после заживления, по мере нормализации функциональных показателей, снижается уровень антигена H.pylori в слизи (58,8%), между эпителиоцитов (11,8%), что говорит о постепенной нормализации барьерной функции слизистой. Концентрация антигена в подслизистом слое остается практически на прежнем уровне (70,6%), что и в период рубцевания. Это может свидетельствовать в пользу того, что процессы связывания антигена в субэпителиальном слое достаточно длительны и происходят медленней, чем нормализация функциональных показателей желудка. При достигнутой эрадикации, в эти сроки частота обнаружения антигена H.pylori между эпителиоцитов и субэпителиально равна нулю (р<0,05).
Полученные данные указывают на несостоятельность барьерной функции слизистой в период обострения и рубцевания и на связывание антигена H.pylori субэпителиальным слоем по мере заживления язвенного дефекта. В свою очередь, это заставило нас проанализировать зависимость морфологических изменений и воспалительной реакции от распределения антигена H.pylori в слоях слизистой оболочки.
Зависимость морфологических изменений и воспалительной реакции от распределения антигена H.pylori в слоях слизистой оболочки. Проведенное исследование показало, что по мере проникновения H.pylori и\или его антигена через слои слизистой оболочки меняется клеточный состав воспалительного инфильтрата (табл. 5).
Таблица 5.
Выраженность и характеристика воспалительного инфильтрата в зависимости от частоты обнаружения антигена H.pylori.
| Выраженность воспалительного инфильтрата | Частота обнаружения антигенного материала, % | ||||
| в слизи | между эпителиоцитов | внутри эпителиоцитов | в клетках инфильтрата | визуализация морфологии бактерий | |
| Инфильтрация эпителия полиморфноядерными лейкоцитами | |||||
| нет | 38,2 | 14,5 | 27,3 | 9,1 | 9,1 |
| есть | 73,3 | 46,7 | 40,0 | 13,3 | 53,3 |
| р | 0,02 | 0,007 | 0,35 | 0,64 | 0,0001 |
| Инфильтрация стромы | |||||
| нейтрофилами | |||||
| отсутствует | 39,5 | 10,5 | 23,7 | 10,5 | 5,3 |
| слабая | 45,0 | 30,0 | 35,0 | 10,0 | 20,0 |
| умер.и выраж. | 66,7 | 41,7 | 41,7 | 8,3 | 58,3 |
| р | 0,68 | 0,04 | 0,36 | 0,95 | 0,0002 |
| эозинофилами | |||||
| отсутствует | 38,6 | 20,5 | 25,0 | 4,5 | 18,2 |
| слабая | 50,0 | 22,2 | 22,2 | 11,1 | 11,1 |
| умер.и выраж. | 75,0 | 25,0 | 75,0 | 37,5 | 37,5 |
| р | 0,41 | 0,88 | 0,01 | 0,01 | 0,49 |
| плазмоцитами | |||||
| отсутствует | 75,0 | 25,0 | 50,0 | 0,0 | 0,0 |
| слабая | 32,0 | 8,0 | 16,0 | 0,0 | 4,0 |
| умер.и выраж. | 51,2 | 29,3 | 36,6 | 14,6 | 29,3 |
| р | 0,10 | 0,09 | 0,12 | 0,03 | 0,02 |
| лимфоцитами (имела место во всех изученных препаратах) | |||||
| слабая | 39,3 | 10,7 | 21,4 | 3,6 | 3,6 |
| умер.и выраж. | 50,0 | 28,6 | 35,7 | 14,3 | 28,6 |
| р | 0,38 | 0,07 | 0,20 | 0,14 | 0,008 |
Так, наличие H.pylori на поверхности эпителиального слоя в виде жизнеспособных форм или бактериальных фрагментов сочеталось с полиморфноядерной (нейтрофильной и эозинофильной) инфильтрацией эпителия, с выраженной нейтрофильной и лимфо-плазмоцитарной инфильтрацией стромы. Внутриклеточное расположение специфически окрашенного антигена сопровождалось умеренной и выраженной эозинофильной и плазмоцитарной инфильтрацией стромы слизистой оболочки гастродуоденальной зоны.
Определение фиксированных иммунных комплексов в биоптатах слизистой оболочки антрального отдела желудка и ДПК. В 29 из 93 исследованных биоптатов слизистой желудка и двенадцатиперстной кишки, взятых от больных с гастродуоденитом и различными формами ЯБ ДПК, было выявлено наличие специфических фиксированных иммунных комплексов, состоящих из иммуноглобулинов и антигенов H.pylori (табл. 6).
Таблица 6.
Частота обнаружения СФИК в биоптатах желудка и ДПК.
| Вид патологии | Частота обнаружения СФИК (абс.(%)) | Всего биоптатов в группе | |||
| Периоды течения заболевания | |||||
| Обострение | Рубцевание | Ремиссия | |||
| Гастродуоденит | 5 (17,9%) | - | 3 (10,7%) | 28 | |
| Вариант течения язвенной болезни | |||||
| Неосложненная | 7 (21,9%) | 1 (3,1%) | - | 32 | |
| Перфорация | 4 (40,0%) | 1 (10,0%) | - | 10 | |
| Кровотечение | 4 (33,3%) | - | - | 12 | |
| Стеноз | 4 (36,4%) | - | - | 11 | |
СФИК в стадии обострения при гастродуодените выявлялись реже, чем при язвенной болезни. Следует так же отметить более частое выявление СФИК при наличии язвенного дефекта, чем в стадию рубцевания и ремиссии. В то же время не было выявлено значимых различий в частоте обнаружения СФИК между неосложненным и осложненным вариантом ЯБ ДПК (в том числе отдельно в стадию обострения), попарно между осложнениями. Вместе с тем, СФИК достоверно чаще встречались в биоптатах, взятых из края язвенного дефекта, чем из антрального отдела и тела желудка (табл. 7).
Таблица 7.
Частота выявления СФИК в зависимости от зоны взятия биоптата
| Зона взятия биоптата | Частота обнаружения СФИК | Значимость различий (р) | Всего биоптатов |
| Край язвы | 9 (56,3%) | - | 16 |
| Антрум | 9 (26,5%) | 0,04 | 34 |
| Тело желудка | 7 (24,1%) | 0,03 | 29 |
| Интактная слизистая ДПК | 4 (28,6%) | 0,12 | 14 |
Полученные результаты позволяют считать, что образование язвенного дефекта связано, в первую очередь, с иммунопатологическими процессами, вызванными СФИК.
Особенности проведения эрадикационной терапии при осложненном течении язвенной болезни двенадцатиперстной кишки.
Нами в ходе проспективного исследования изучена частота рецидивирования инфекции, обусловленной H.pylori у 111 больных язвенной болезнью ДПК - неосложненной и при наличии осложнений. Пациентам проводили контроль эффективности эрадикационной терапии через 4 недели после ее окончания и повторные тесты на H.pylori через 3, 6 и 9 месяцев от завершения курса эрадикационной терапии. Из 59 больных основной группы через 4 недели, при контроле эффективности курса эрадикационной терапии, H.pylori выявили у 8 человек, а из 52 больных с неосложненной язвенной болезнью - у 4. Эти больные в дальнейшем были исключены из исследования. Сравнение частоты рецидивирования инфекции в группах показала, что она выше у больных с осложненной язвенной болезнью ДПК (рис. 6).

Рис. 6. Частота обнаружения H.pylori в различные сроки после антибактериальной терапии при осложненном и неосложненном течении язвенной болезни двенадцатиперстной кишки
Через 6 и более месяцев после антибактериальной терапии H.pylori выявлялась в два раза чаще при осложненном течении язвенной болезни (через 6 месяцев – у 29,0% и через 9 месяцев – у 34,5% пациентов), чем при неосложненном (13,1% и 15,8% пациентов, соответственно) (р=0,04).
Лекарственный патоморфоз H.pylori. При рассмотрении лекарственного патоморфоза H.pylori (при проведении эрадикационной терапии) было выявлено, что фрагменты разрушившихся бактерий проникают сквозь эпителиоциты в субэпителиальный слой; в дальнейшем, при успешной эрадикации H.pylori и нормализации функциональных сдвигов желудка, происходит полное очищение слизистой от антигена H.pylori (рис.7).

Рис. 7. Состояние слизистой пилорического отдела желудка (срез желудочной ямки), инфицированной H.pylori, до, во время и после проведения антибактериальной терапии. Антиген H.pylori окрашен в светло-коричневый цвет. ИГХ с поликлональными антителами против H.pylori, ДАБ, гематоксилин.
а – H.pylori в глубине желудочной ямки до проведения противоязвенного лечения, х 400;
б –во время текущей антибактериальной терапии (специфическая окраска эпителиоцитов, межэпителиального пространства, стромы), х 400;
в –во время текущей антибактериальной терапии (специфическая окраска слоя слизи, эпителиоцитов, стромы), х 600;
г – через 3 месяца после успешной эрадикационной терапии (полное отсутствие специфической окраски в препарате), х 400.
Схожие находки были сделаны и при ИЦХ методе исследования: при текущей терапии отмечалось появление «специфически окрашенного фона».
То, что проводимая антибактериальная терапия, направленная на уничтожение H.pylori, является фактором, многократно увеличивающим концентрацию антигена в слизи, подтверждает и количественный анализ частоты обнаружения антигена H.pylori в биоптатах в зависимости от времени проведения антибактериальной терапии (рис. 8).

Рис. 8. Частота обнаружения антигена H.pylori в целом в биоптатах в зависимости от времени проведения эрадикационной терапии
До начала лечения антиген H.pylori в клетках инфильтрата не обнаруживался, во время проведения эрадикационной терапии он выявлялся в 23,1% случаев, а спустя месяц и более после завершения курса терапии частота обнаружения антигена падала до 0-5,9% случаев (р=0,04). Уменьшение количества антигена в слоях слизистой происходило только по истечении нескольких месяцев, по мерее его утилизации.
Обоснование применения иммунных препаратов в составе комплексной антибактериальной терапии. Нами на примере циклоферона показано, что дополнение эрадикационной терапии иммуномодулятором повышает эффективность последней. У больных осложненной язвой ДПК при проведении эрадикационной терапии стандартными схемами, дополненной циклофероном, спустя более полугода после курса эрадикации H.pylori отсутствовал в 89,5% случаев, при проведении эрадикационной терапии только стандартными схемами H.pylori отсутствовал в 73,7,5% случаев (р=0,04). Более того, у больных осложненной язвой эффективность эрадикационной терапии с использованием стандартных схем, дополненной иммуномодулятором, приближалась к эффективности эрадикационной терапии с использованием только стандартных схем у больных без осложнений (р> 0,05).
Индивидуализация проведения эрадикационной терапии при разных формах осложненной ЯБ ДПК. Обобщение результатов проведенных исследований с учетом морфофункциональных нарушений, свойственных каждому виду осложнения язвенной болезни ДПК, и фармакологических свойств различных схем эрадикационной терапии позволило сформулировать следующие принципы дифференцированной эрадикационной терапии H.pylori при различных формах дуоденальной язвы. Комплексная противоязвенная терапия при осложненной язвенной болезни двенадцатиперстной кишки должна проводиться с учетом доминирующих патофизиологических нарушений, характерных для каждого вида осложнений. Задачами эрадикационной терапии являются не только искоренение H.pylori, но и снижение концентрации ее антигенов в слоях слизистой оболочки. Выбор схем и сроков проведения эрадикационной терапии должен быть дифференцированным с учетом вида осложнения, фазы течения заболевания, основанным на применении блокаторов протонной помпы и препаратов висмута, и дополняться применением иммуномодуляторов.
Результаты дифференцированной эрадикационной терапии при осложненной язвенной болезни ДПК. Обоснование принципов дифференцированной эрадикационной терапии позволило нам провести проспективное исследование, где больные были разделены на группу с индивидуальным подходом к проведению эрадикационной терапии и группу, где курс эрадикационной терапии проводился стандартными схемами.
Отдаленные результаты дифференцированной эрадикационной терапии (от 1 года до 3 лет) удалось проследить у 143 больных с осложненными формами язвы ДПК. 89 больным (основная группа) эрадикационная терапия проводилась согласно разработанным нами принципам. 54 больным (контрольная группа) курс эрадикационной терапии проводился стандартными схемами. Оценивалась частота рецидивов язвенной болезни и частота выявления H.pylori после проведения курса эрадикационной терапии (рис. 9-10).
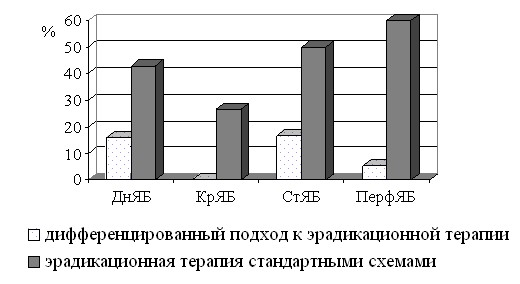
Рис. 9. Частота рецидивирования язвенной болезни ДПК (от 1 года до 3 лет).
ДнЯБ – язвенная болезнь с частым рецидивированием или длительным заживлением
КрЯБ – язвенная болезнь, осложненная кровотечением
СтЯБ – язвенный стеноз
ПерфЯБ – перфоративная язва

Рис. 8. Частота выявления H.pylori (от 1 года до 3 лет).
ДнЯБ – язвенная болезнь с частым рецидивированием или длительным заживлением
КрЯБ – язвенная болезнь, осложненная кровотечением
СтЯБ – язвенный стеноз
ПерфЯБ – перфоративная язва
В целом, как частота рецидивов язвенной болезни, так и частота выявления H.pylori при дифференцированной эрадикационной терапии были значительно меньше (10,1% и 6,7% соответственно), чем при использовании стандартных схем, без учета индивидуальных особенностей осложнений (53,7% и 59,3% соответственно), на протяжении всего периода наблюдения (р<0,00001).
Приведенные данные свидетельствуют о том, что индивидуальный подход к проведению эрадикационной терапии (в составе комплексной противоязвенной терапии) позволяет существенно повысить ее эффективность и добиться не только эрадикации H.pylori, но и стойкой ремиссии заболевания с хорошими отдаленными результатами. Достижение стойкой ремиссии стирает различия между больными неосложненной язвенной болезнью и теми, у которых развились ее осложнения.
Выводы
- Иммуногистохимический и иммуноцитохимический методы диагностики H.pylori являются достоверными высокоспецифичными методами выявления антигенов H.pylori, позволяют изучать процессы их проникновения в слои слизистой оболочки (в том числе субэпителиально) и процессы утилизации антигенов в слизистой оболочке, а так же интерпретировать ответную воспалительную реакцию.
- У больных с осложненным течением язвенной болезни двенадцатиперстной кишки проникновение H.pylori (жизнеспособных форм и\или фрагментов бактерий) внутрь эпителиоцитов встречается в 42,8%, а субэпителиально - в 11,7% случаев и сопровождается соответствующей воспалительной инфильтрацией. Концентрация антигена H.pylori в слоях слизистой зависит от кислотопродукции, ослабления барьерной функции слизистой оболочки, вида осложнения, стадии язвенной болезни и проводимого лечения.
- Специфические фиксированные иммунные комплексы, состоящие из антигена H.pylori и специфических антител, обнаруживаются чаще при различных формах язвенной болезни ДПК (21,9-40%), чем при гастродуодените (17,9%) и в крае язвенного дефекта (56,3%), чем в неповрежденной слизистой оболочке (24,1- 28,6%). Это позволяет считать причиной обострения язвенной болезни развитие реакции гиперчувствительности III типа в слизистой оболочке двенадцатиперстной кишки, разрешающейся в агрессивной среде образованием язвенного дефекта.
- Комплексная противоязвенная терапия при осложненной язвенной болезни двенадцатиперстной кишки должна проводиться с учетом доминирующих патофизиологических нарушений, характерных для каждого вида осложнений. При этом задачами эрадикационной терапии являются не только искоренение H.pylori, но и снижение концентрации ее антигенов в слоях слизистой оболочки. Поэтому выбор схем и сроков проведения эрадикационной терапии должен быть дифференцированным с учетом вида осложнения, фазы течения заболевания, основанным на применении блокаторов протонной помпы и препаратов висмута, и дополняться применением иммуномодуляторов. Индивидуальный подход к проведению эрадикационной терапии (в составе комплексной противоязвенной терапии) позволяет добиться эрадикации H.pylori в 93,3% и стойкой ремиссии заболевания в 89,9% случаев осложненных форм язвенной болезни двенадцатиперстной кишки.
Практические рекомендации
1.При частом рецидивировании заболевания предпочтение следует отдавать схемам тройной терапии на основе ингибиторов протонного насоса. Курс эрадикационной терапии может проводиться в период обострения, но только после использования средств, стойко подавляющих кислотопродукцию.
2. При дуоденальной язве, осложненной кровотечением, эрадикация H.pylori должна проводиться схемами тройной терапии на основе препаратов висмута. Курс эрадикационной терапии следует проводить после рубцевания язвенного дефекта и коррекции функциональных нарушений желудка и двенадцатиперстной кишки. Проводить эрадикационную терапию сразу после остановки кровотечения или, спустя несколько дней, нецелесообразно из-за усиления воспалительной реакции и увеличения риска рецидива кровотечения.
3. При язвенных стенозах курс эрадикационной терапии должен быть отложен до улучшения проходимости пилородуоденального канала, достигаемого в результате комплексной противоязвенной и противовоспалительной терапии. Предпочтение следует отдавать схемам на основе препаратов висмута.
4. В послеоперационном периоде (при перфоративной язве, оперативном вмешательстве при язвенном кровотечении, стенозе) антихеликобактерная терапия должна проводиться не ранее 1-1,5 месяцев после операции с предварительной диагностикой H.pylori. В случае перфоративной язвы основой курса «первой линии» эрадикационной терапии могут являться схемы тройной терапии на основе ингибиторов протонного насоса.
5. В случае частого рецидивирования язвенной болезни, при дуоденальной язве, осложненной кровотечением, а так же при язвенных стенозах курс эрадикационной терапии должен дополняться последующим применением иммуномодуляторов (циклоферона).
Публикации по теме диссертации
- Попов Е.А. Патогенез, диагностика и лечение инфекции, обусловленной Helicobacter pylori / Г.Я.Ценева, Н.В.Рухляда, В.Е.Назаров, Е.А.Попов, А.Б.Жебрун. – СПб.: Человек, 2003. – 96 с.
- Попов Е.А. Иммуногистохимическое исследование биоптатов желудка и двенадцатиперстной кишки, полученных от больных осложненной язвенной болезнью / Е.А.Попов, В.Е.Назаров // Вестник хирургической гастроэнтерологии. – 2006. – №1. – С.127.
- Попов Е.А. Иммуноцитохимические и иммуногистохимические исследования Helicobacter pylori в гастробиоптатах у пациентов с язвенной болезнью двенадцатиперстной кишки / В.Ю.Кравцов, Е.А.Попов, В.Е.Назаров, Ю.А.Еремин, А.Е.Носов, Д.М.Семов // Современные проблемы клинической цитоморфологии: Тезисы Всероссийской конференции с международным участием, научные чтения, посвященные памяти член-корреспондента РАМН, з.д.н. РФ, профессора О.К.Хмельницкого и 25-летию курса цитологии кафедры патологической анатомии СПбМАПО. – СПб, 2007 г. – С.58–59.
- Попов Е.А. Значение обнаружения антигенов H.pylori в слизистой оболочке желудка и двенадцатиперстной кишки при осложненном течении язвенной болезни двенадцатиперстной кишки / Н.В.Рухляда, Е.А.Попов, В.Е.Назаров, В.Ю.Кравцов, Ю.А.Еремин // Вестник Российской Военно-медицинской академии. – 2007. – №3(19). – С.9–13.
- Попов Е.А. Сравнение чувствительности и специфичности уреазного, гистологического и иммуногистохимического методов диагностики H.pylori-инфекции у больных с осложненным течением язвенной болезни двенадцатиперстной кишки / Попов Е.А. // Вестник Российской Военно-медицинской академии. – СПб, 2007.– прил. Часть II. № 1 (17). – С.706.
- Popov E. Immunocytochemistry and immunohistochemistry study of Helicobacter pylori in gastric biopsies from patients with duodenal ulcer / V. Kravtsov, E. Popov, V. Nazarov, S. Proshin, Y. Eremin, D. Semov, A Nosov // Cytopathology. – 2008. – Vol.19 (Suppl. 1). – P.47.
- Попов Е.А. Распределение антигена H.pylori в слоях слизистой оболочки при различных патофизиологических изменениях функции желудка / В.Е. Назаров, Г.Я. Ценева, Е.А. Попов // Актуальные вопросы военно-морской и клинической хирургии: Сб. научных трудов к всероссийской научно-практической конференции, посвященной 90-летию профессора М.А.Лущицкого. – СПб: «Морсар АВ», 2009. – С.44–45.
- Попов Е.А. Определение специфических фиксированных иммунных комплексов в биоптатах слизистой оболочки антрального отдела желудка и двенадцатиперстной кишки / В.Е. Назаров, Г.Я. Ценева, Е.А. Попов // Актуальные вопросы военно-морской и клинической хирургии: Сб. научных трудов к всероссийской научно-практической конференции, посвященной 90-летию профессора М.А.Лущицкого. – СПб: «Морсар АВ», 2009. – С.47.
- Попов Е.А. Дифференцированная эрадикационная терапия H.pylori при осложненном течении язвенной болезни двенадцатиперстной кишки: Методические рекомендации / В.Е. Назаров, Г.Я. Ценева, Е.А. Попов // Санкт-Петербургский НИИ скорой помощи им. И.И. Джанелидзе, СПб, 2010 – 10 с.

