Место эстрогенсодержащих препаратов, активных метаболитов витамина d и их комбинации в лечении постменопаузального остеопороза
На правах рукописи
МЕЛЬНИКОВА ЮЛИЯ НИКОЛАЕВНА
Место эстрогенсодержащих препаратов, активных метаболитов витамина D и их комбинации в лечении постменопаузального остеопороза
14.00.01 — Акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2007 г.
Работа выполнена в ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» Минздрава Московской области.
Научный руководитель:
член-корр. РАМН,
доктор медицинских наук,
профессор Краснопольский Владислав Иванович
Официальные оппоненты:
доктор медицинских наук,
профессор Сметник Вера Петровна
доктор медицинских наук,
профессор Буянова Светлана Николаевна
Ведущая организация:
ГОУ ВПО «Московский государственный медико-стоматологический университет».
Защита состоится « » 200__ года в часов на заседании диссертационного совета Д 208.048.01 при ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» (101000, Москва, ул. Покровка, д.22а).
С диссертацией можно ознакомиться в библиотеке ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии».
Автореферат разослан «___» _______ 200__ г.
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор О.Ф. Серова
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы.
По оценкам ВОЗ, остеопороз и его последствия рассматриваются как одна из главных причин заболеваемости, смертности и возрастания медицинских расходов среди лиц старше 50 лет (Сметник В.П., 2001; Риггз Б.Л., 2000). При этом, обусловливаемые остеопорозом проблемы, по своей социальной значимости, занимают 4-е место, уступая лишь онкологической патологии, сердечно-сосудистым заболеваниям и сахарному диабету (ВОЗ, 2000). Важнейшим последствием снижения костной плотности при остеопорозе является резкое возрастание риска переломов при минимальной травматизации, что нередко сопровождается стойкой инвалидизацией и может представлять угрозу для жизни (Торопцова Н.В., 2000; Akesson K., 2003; Cadarette S.M., 2000).
Среди существующих вариантов остеопороза в женской популяции наиболее распространен постменопаузальный остеопороз (ПМО), ассоциируемый с ослаблением защитного действия эстрогенов на костную ткань на фоне возрастного угасания функции яичников. ПМО диагностируется в среднем у 30-40% всех женщин в постменопаузе, причем частота его выявления возрастает пропорционально увеличению продолжительности постменопаузы (Baran D.T., 1998; Ettinger B., 1992; Hansen S.A., 2000).
Несмотря на проведение множества исследований (Байдак М.М., 1994; Белова А. Е., 2002; Болдырева Н.В., 1998; Краснопольская К. В., 1993; Писаревская М.А.,1998; Торопцова Н.В., 2000), посвященных различным аспектам ПМО, многие вопросы, касающиеся диагностики и терапии этого заболевания требует уточнения.
Таким образом, актуальность проблемы совершенствования диагностики и лечения ПМО является вполне очевидной, что явилось побудительным мотивом для проведения собственных прицельных исследований для решения ряда вышеперечисленных «открытых» вопросов.
Цель исследования:
Оптимизация тактики ведения больных с постменопаузальным остеопорозом.
Задачи исследования:
1. Сопоставить степень снижения костной плотности в лучевой и большеберцовой костях для уточнения корреляции между потерями костной ткани в разных участках скелета при ПМО.
2. Изучить корреляцию между выраженностью отклонений маркера костной резорбции CL и денситометрическими проявлениями ПМО с учетом их тяжести и распространенности.
3. Уточнить целесообразность определений общего и ионизированного кальция, неорганического фосфора, остеокальцина и щелочной фосфатазы для характеристики активности костнорезорбтивного процесса и чувствительности к костнопротективной терапии на основе сопоставлений с данными, получаемыми при параллельном тестировании уровня CL.
4. Оценить антирезорбтивный костнопротективный потенциал фемостона 1/5, -кальцидола и их комбинации при ПМО на основе динамических оценок (с 6- и 12-месячными интервалами) уровня CL и значений ПКТ.
5. Охарактеризовать сопутствующее действие костнопротективной терапии фемостоном, -кальцидолом и их комбинацией на факторы, влияющие на качество жизни пациенток в постменопаузе.
6. Уточнить частоту и характер побочных эффектов при использовании костнопротективной терапии на основе ЗГТ фемостоном (комбинируемой или нет с препаратом витамина D) или только -кальцидолом.
Научная новизна
Сопоставлен антирезорбтивный потенциал эстрогенсодержащего препарата фемостона и производного витамина D -кальцидола, а также проведено сравнительное изучение их корригирующего эффекта на важнейшие факторы, влияющие на качество жизни в постменопаузе.
Подтверждена необходимость одновременной оценки плотности костной ткани (ПКТ) в нескольких костях, подверженных наибольшему риску переломов.
Подтверждено, что динамическое определение маркера костной резорбции CL делает возможным проводить раннюю оценку эффективности терапии, что позволяет своевременно решать вопрос о сохранении или изменении тактики лечения. Одновременно показано, что использование динамической ультразвуковой денситометрии с теми же временными интервалами не обеспечивает получение объективной информации об эффективности антирезорбтивного лечения.
Разработан алгоритм ведения пациенток в постменопаузе с постменопаузальным остеопорозом.
Практическая значимость
Сформулированы показания к раздельному и сочетанному использованию -кальцидола и ЗГТ фемостоном при лечении ПМО.
Обоснована целесообразность одновременной денситометрической оценки ПКТ в лучевой и большеберцовой костях для более надежного выявления лиц с ПМО.
Уточнены диагностические процедуры, позволяющие получать оперативную информацию о выраженности процесса костной резорбции и чувствительности пациенток к используемому костнопротективному лечению.
Продемонстрирована непригодность определений маркеров фосфорно–кальциевого обмена и остеокальцина для получения достоверной информации об активности костнорезорбтивного процесса.
Положения, выносимые на защиту
1. Выбор фемостона, -кальцидола или их комбинации для костнопротективной (антирезорбтивной) терапии у больных с ПМО должен определяться степенью повышения биохимического маркера костной резорбции CL.
2. Повторные измерения CL позволяют оценить эффективность проводимой костнопротективной (антирезорбтивной) терапии уже через 6 месяцев после ее начала, тогда как динамические ультразвуковые измерения ПКТ с 6- и 12-месячными интервалами непригодны для этой цели.
3. При ПМО выраженность снижения ПКТ в лучевой и большеберцовой костях в большинстве случаев оказывается различной, что означает целесообразность одновременного определения костной плотности в этих костях для повышения надежности диагностики остеопороза у женщин в постменопаузе.
4. Костнопротективная (антирезорбтивная) терапия с использованием фемостона и -кальцидола обеспечивает позитивные сопутствующие эффекты в виде ослабления костно-суставных болей и снижения утомляемости при обычных бытовых нагрузках. Применение ЗГТ не только способствует большей выраженности указанных эффектов, но и сопровождается быстрым устранением нейро-вегетативных проявлений климактерического синдрома.
Внедрение результатов исследования в практику здравоохранения
Разработанная тактика ведения пациенток с ПМО внедрена в практику отделения гинекологической эндокринологии НКО МОНИИАГ, поликлиники 150-го Центрального военного госпиталя Космических войск (г.Краснознаменск Московской области).
Апробация работы
Апробация диссертации состоялась на заседании Ученого совета ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» 9 октября 2007г., протокол № 9.
Структура и объем диссертации
Диссертация изложена на 156 страницах компьютерного текста и состоит из введения, обзора литературы, материала и методов исследования, четырех глав, представляющих результаты собственных исследований, обсуждения, выводов, практических рекомендаций и списка использованной литературы. Иллюстративный материал представлен в виде 31 таблицы и 13 рисунков. Библиография включает 203 источника, из них 60 на русском и 143 на иностранном языках.
СОДЕРЖАНИЕ РАБОТЫ
Материалы и методы исследования.
Исходно в исследование были включены 90 пациенток в постменопаузе с диагностированным снижением ПКТ (остеопения/остеопороз) в возрасте 45-65 лет, с естественной менопаузой не менее 2-х лет и отсутствием эндокринной патологии и тяжелых соматических заболеваний, способных вызвать развитие вторичного остеопороза.
Пациентки трех групп были сопоставимы по среднему возрасту (55,3±0,8 лет), длительности менопаузы (до 5 лет - у 60 %), среднему возрасту наступления менопаузы - 53,1±0,6 лет. В становлении менструальной функции также не было различий, репродуктивная функция была реализована у 95% пациенток. Среди гинекологической патологии наиболее часто отмечались воспалительные процессы органов малого таза (29,1%), миомы матки (32,0%), гиперпластические процессы эндометрия (4,6%).
В структуре экстрагенитальной патологии мы акцентировали внимание на заболеваниях костно-мышечной системы, таких как остеохондроз позвоночника и грыжи межпозвонковых дисков, которые встречались примерно с одинаковой частотой – от 5,3% до 22,2%.
Методом слепой выборки и с учетом противопоказаний к использованию заместительной гормонотерапии (ЗГТ) пациентки были разделены на 3 группы. I группу составили 38 человек, которые получали фемостон 1/5 в непрерывном режиме, II – 20 человек, которые получали комбинированную терапию фемостоном и альфакальцидолом в дозировке 1 мкг/сут, III – 32 человека, получавших монотерапию альфакальцидолом.
Методы исследования.
В работе использованы стандартные методы обследования - сбор анамнеза, оценка общего и гинекологического статуса, ультразвуковое исследование органов малого таза («Siemens – Sequoia 512»), маммография, определение липидного спектра крови и показателей свертывающей системы с использованием рутинных методов.
Из специализированных методов мы применяли ультразвуковую остеоденситометрию (УЗД) с определением плотности костной ткани в двух точках скелета – средней трети лучевой и срединной части большеберцовой кости с помощью аппарата «Omnisens 7000S» Sunlight Medical Ltd (Израиль); определение маркеров костного ремоделирования - остеокальцина (ОК) и -cross laps на электрохемилюминесцентном анализаторе Elecsys 2010; определение маркеров фосфорно-кальциевого обмена – общего и ионизированного кальция, неорганического фосфора и общей щелочной фосфатазы - методом колориметрического УФ-анализа.
В качестве дополнительных оценочных критериев эффективности костнопротективной терапии использовали показатели, влияющие на качество жизни больных в менопаузе - климактерический синдром (по индексу Куппермана), костно-суставной болевой синдром (по 4-х балльной шкале) и утомляемость при обычных бытовых нагрузках (по 3-балльной шкале.
Статистическую обработку материала проводили с помощью программ «Microsoft Exel–2002» и «Biostat–1998». Достоверность различий оценивалась с помощью параметрических и непараметрических критериев статистики (описательная статистика, парный (t) и непарный критерии Стьюдента, Манна-Уитни, Уилкоксона, корреляционный метод).
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ
И ИХ ОБСУЖДЕНИЕ
Исходно всем пациенткам была проведена УЗД, при которой однонаправленные изменения костной плотности (остеопения/остеопороз) были зафиксированы лишь у 1/5 больных, тогда как у остальных 80% имелись расхождения между выраженностью указанных показателей (табл. 1). Корреляции между одновременным наличием остеопении или остеопороза в изучавшихся костях не получено. Это свидетельствует о необходимости одновременного определения костной плотности с помощью УЗД как минимум в двух костях для повышения надежности выявления остеопоротического процесса.
Таблица 1.
Изменения костной плотности по УЗД
| Число больных (n = 90) | ||||
| Лучевая кость | ||||
| Норма | Остеопения | Остеопороз | ||
| Большая берцовая кость | Норма | - | 25 27,8% | 7 7,8% |
| Остеопения | 17 18,9% | 16 17,8% | 4 4,4% | |
| Остеопороз | 9 10,0% | 8 8,9% | 4 4,4% | |
| r = от -0,188 до + 0,035 (р>0,05) между одновременным развитием остеопении/остеопороза в лучевой и большеберцовой костях. | ||||
В связи с тем, что маркер костной резорбции -cross-laps (CL) признан «золотым стандартом» в диагностике остеопороза, мы попытались выявить корреляцию данным маркером и показателями денситометрии. В табл. 2 указывается частота выявления случаев аномального повышения СL (>0,58 нг/мл) среди подгрупп пациенток, выделенных с учетом вариантов имевшихся отклонений костной плотности в лучевой и большеберцовой костях. Пациентки с СL выявлялись во всех подгруппах с частотой от 11,1% до 75%. Эти результаты позволяют констатировать, что среди больных с остеопорозом/остеопенией в одной или в двух изучавшихся костях встречаются лица как имеющие, так и не имеющие признак аномально ускоренного процесса костной резорбции.
Величина корреляции свидетельствует о полном отсутствии связи между этими признаками. Из этого следует, что остеопороз с одинаковой вероятностью может сопровождаться или не сопровождаться аномальным возрастанием СL.
Таблица 2.
Частота больных с повышенным уровнем СL
| Число и частота больных с повышенным уровнем СL n с изменениями костной плотности = 90 n с повышенным уровнем СL = 36 | ||||
| Лучевая кость | ||||
| Норма | Остеопения | Остеопороз | ||
| Большая берцовая кость | Норма | - | 25 | 7 |
| Остеопения | 17 | 16 | 4 | |
| Остеопороз | 9 | 8 | 4 | |
| - абс.число больных с повышенным СL и их % среди лиц с конкретным сочетанием отклонений костной плотности (r = + 0,009 (р>0,05)). | ||||
Заслуживает внимания то, что в 48 пробах с CL, лишь в 19 (39,6%) уровень ОК также оказывался повышенным (рис. 1). При этом корреляция между одновременным возрастанием этих двух маркеров составляет только +0,54 при р<0,001. Из этого можно заключить, что если ориентироваться при постановке диагноза остеопороза именно на уровень ОК, а не на CL, то можно «пропустить» почти 60% пациенток с аномально усиленной резорбцией костной ткани, подтверждаемой по уровню CL, но не ОК.
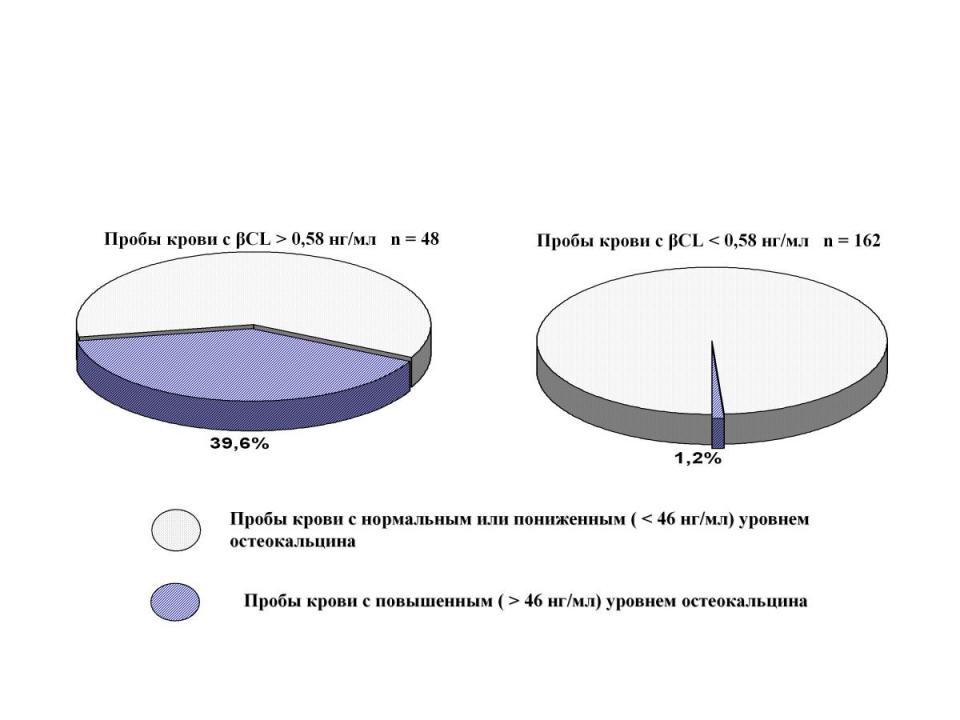
Рис. 1. Повышение ОК среди проб крови с повышенным CL.
Кроме того, 2(1,2%) случая повышения ОК, не сопровождавшихся одновременным возрастанием CL, могут стать причиной «гипердиагностики» в действительности несуществующего процесса.
Также не было получено корреляции между отклонениями уровня CL и маркеров фосфорно-кальциевого обмена, такими как общий кальций (рис.2):
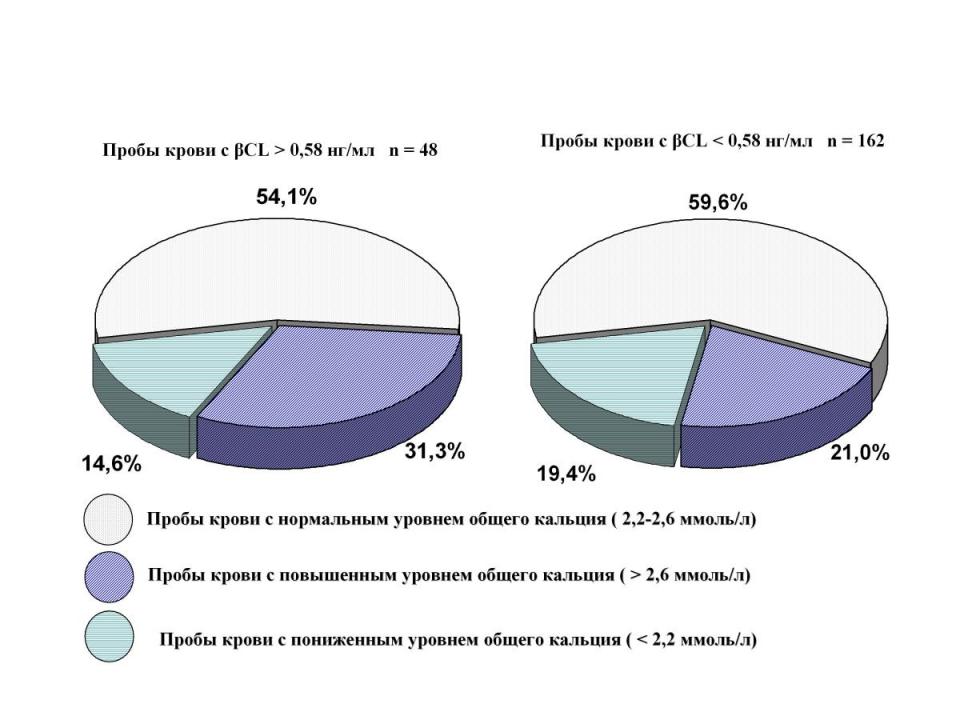
r = + 0,105 (р>0,05) – между повышением -cross laps и повышением общего кальция
r = + 0,101 (р>0,05) – между повышением -cross laps и понижением общего кальция
Рис. 2. Связь между отклонением CL и общим кальцием.
между отклонениями уровня CL и ионизированным кальцием (рис. 3):
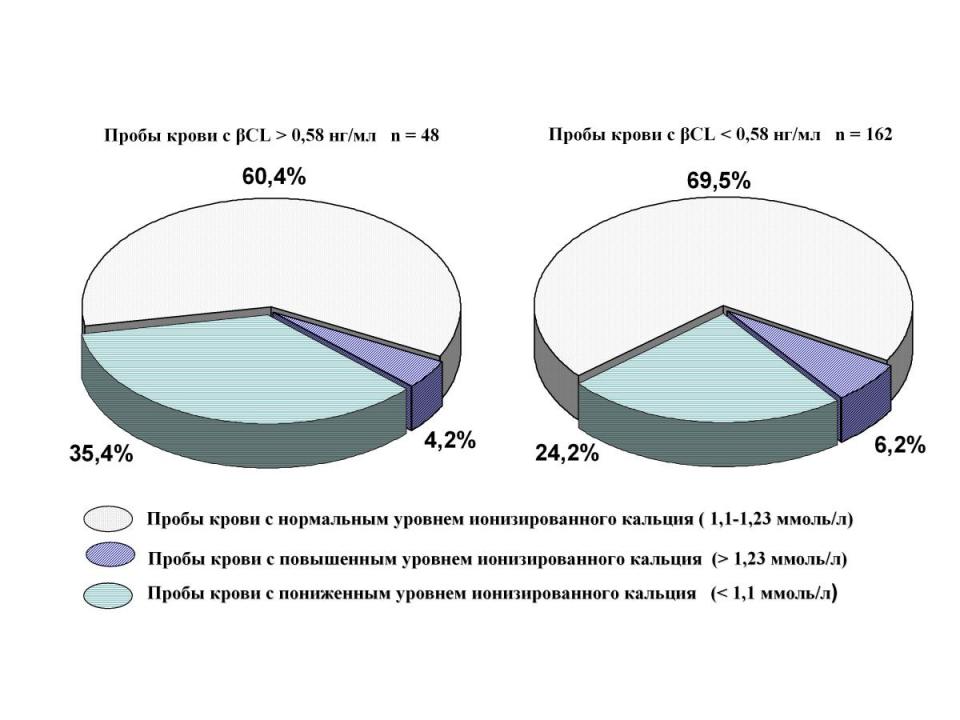
r = - 0,036 (р >0,036) между повышением уровня -cross laps и повышением уровня ионизированного кальция
r = + 0,1 (р>0,05) между повышением уровня -cross laps и понижением уровня ионизированного кальция
Рис. 3. Связь между отклонениями CL и ионизированным кальцием.
между отклонениями уровня CL и неорганическими фосфатами (рис. 4):
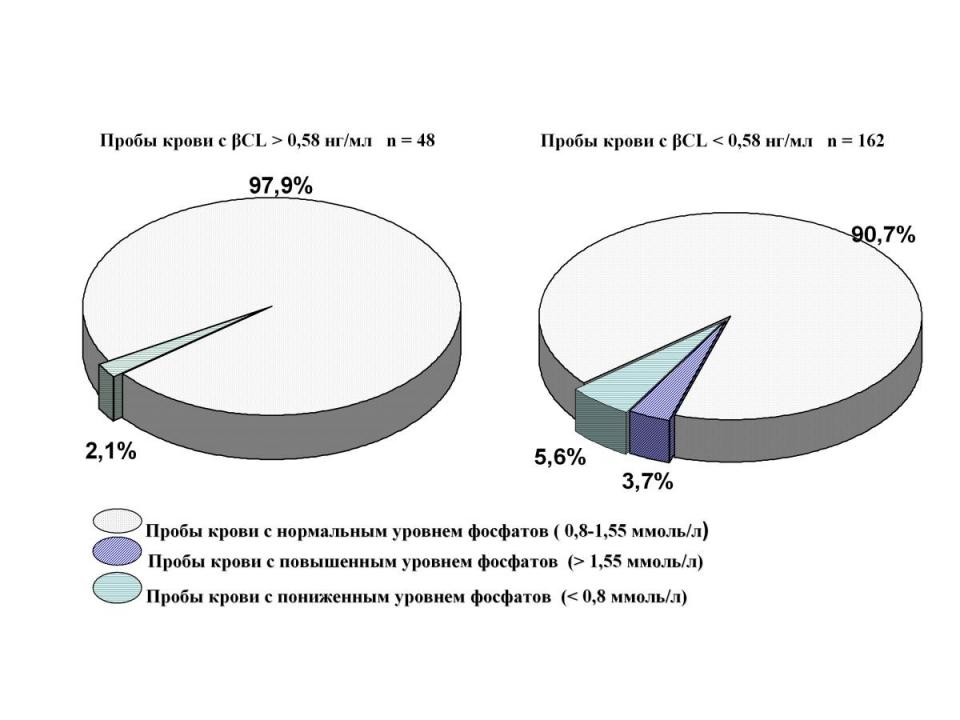
r = -0,068 (р>0,05) между повышением уровня -cross laps и понижением уровня фосфатов.
Рис. 4. Связь между отклонениями уровня CL и неорганическими фосфатами.
Также не получено корреляции между -cross laps и маркером костного формирования остеокальцином, щелочной фосфатазой.
В течение года из исследования выбыли 20 человек, по тем или иным причинам, о которых будет сказано ниже. Оценку эффективности терапии мы проводили у 70 больных, которые прошли все три исследования интересующих маркеров - исходное, через 6 и 12 месяцев терапии.
Все три назначавшихся варианта костнопротективной терапии обеспечивали снижение средних значений СL (рис. 5).
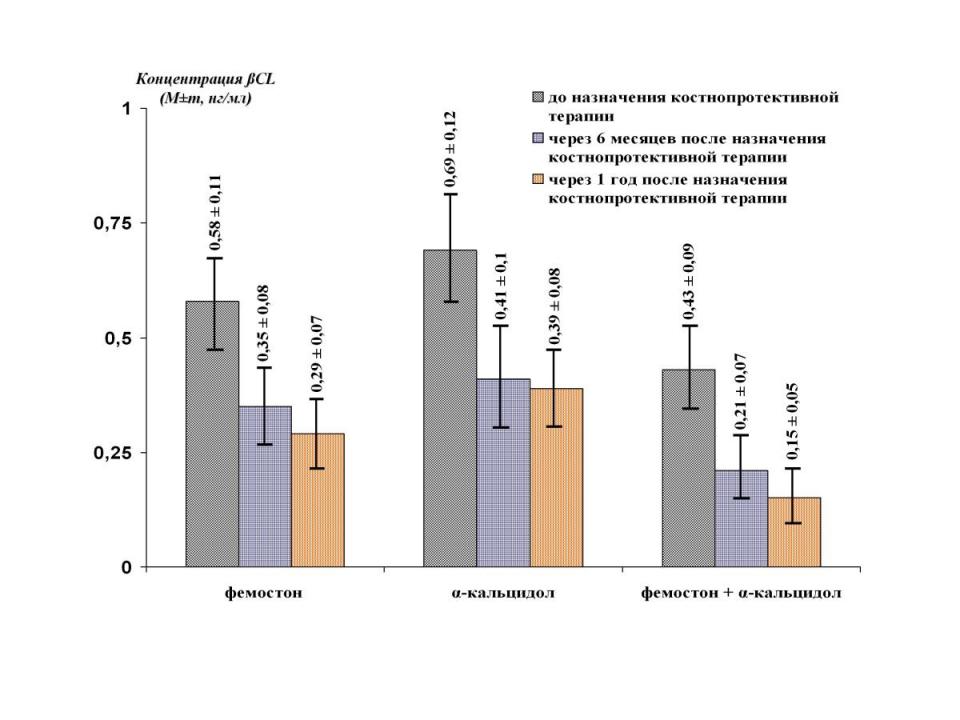
Рис. 5. Снижение СL под влиянием терапии (р от <0,05 до <0,01).
Так, в группе больных, получавших фемостон, уровень СL уменьшался с исходных 0,58+0,11 нг/мл до 0,35+0,08 нг/мл на шестом месяце терапии и до 0,29+0,07 нг/мл через 1 год после ее начала. Аналогичная картина наблюдалась и в других группах: на фоне применения -кальцидола уровень СL уменьшался к концу 6-го и 12-месяца терапии с исходных 0,69+0,12 нг/мл до, соответственно, 0,41+0,1 и 0,39+0,08 нг/мл, а при применении комбинации фемостон+-кальцидол на тех же сроках после начала лечения исходная концентрация СL, составлявшая 0,43+0,09 нг/мл, снижалась до 0,21+0,07 и 0,15+0,05 нг/мл.
По критерию нормализации аномально повышенного СL (>0,58 нг/мл) комбинация фемостон+-кальцидол оказывалась эффективной в 100% случаев, причем это наблюдалось уже к концу 6 месяца терапии (табл. 3).
Таблица 3.
Эффективность терапии по нормализации СL
| Вид терапии | Период определения СL | Результаты | ||
| Число больных c СL (>0,58 нг/мл) | Частота эффективной терапии по критерию нормализации исходно повышенного уровня СL | |||
| Абс. | % | % | ||
| Фемостон n=30 | 1 | 9 | 30,0 | - |
| 2 | 4 | 13,3 | 55,6 | |
| 3 | 2 | 6,7 | 77,8 | |
| -кальцидол n=28 | 1 | 16 | 57,1 | - |
| 2 | 7 | 25,0 | 56,3 | |
| 3 | 7 | 25,0 | 56,3 | |
| Фемостон+ -кальцидол n=12 | 1 | 3 | 25,0 | - |
| 2 | 0 | 0 | 100 | |
| 3 | 0 | 0 | 100 | |
Примечания:
1 – до начала терапии;
2- через 6 месяцев после начала терапии
3- через 12 месяцев после начала терапии
Менее эффективным было применение только фемостона, использование которого обеспечивало устранение аномального повышения СL на 6 месяце терапии лишь у 55,6% больных. Одногодичное применение этого препарата сумело повысить частоту лиц с нормализованным СL до 77,8%. Еще менее успешным было применение -кальцидола. К концу 6-го месяца использования этот препарат обеспечивал устранение биохимических признаков ускоренной резорбции у 56,3% пациенток, что было вполне сопоставимо с эффектом фемостона на том же сроке после начала костнопротективной терапии.
Анализ изменений средних значений остеокальцина под влиянием фемостона, -кальцидола и их комбинации (рис.6) позволяет отметить редуцирующий эффект всех трех вариантов терапии на средние значения этого маркера.
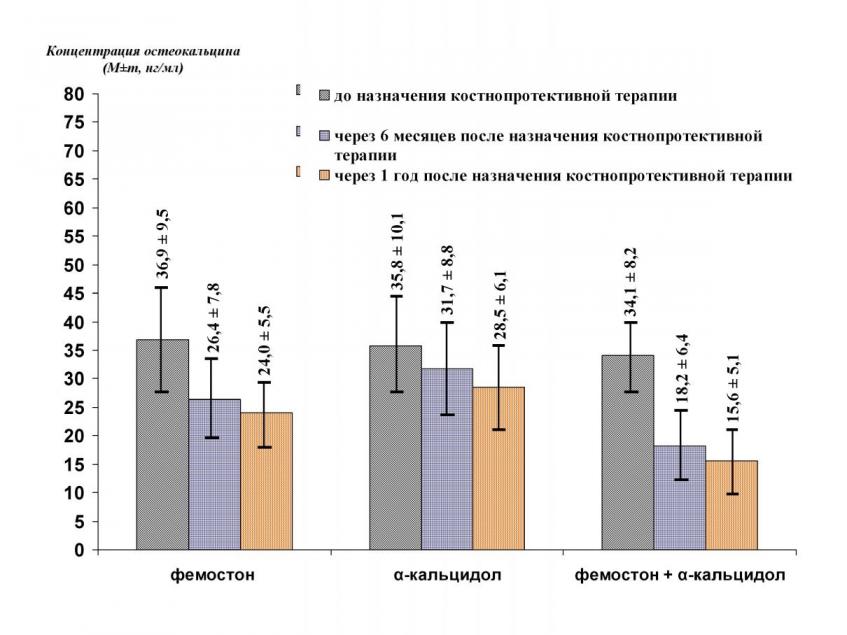
Рис. 6. Изменения значений остеокальцина под влиянием терапии.
Фемостон обеспечивал снижение ОК на 6-м и 12-м месяце терапии с исходных 36,9+9,5 нг/мл до, соответственно, 26,4+7,8 нг/мл и 24,0+5,5 нг/мл. Под влиянием лечения -кальцидолом в те же сроки происходило снижение ОК с 35,8+10,1 нг/мл до 31,7+8,8 и 28,5+6,1 нг/мл; применение комбинации фемостон+-кальцидол сопровождалось уменьшением ОК с 34,1+8,2 нг/мл до 18,2+6,4 и 15,6+5,1 нг/мл.
По критерию нормализации аномально повышенного ОК наиболее успешной оказывалась терапия комбинацией фемостон+-кальцидол, обеспечивавшая 100% эффективность лечения уже к концу 6 месяца после начала ее использования (табл. 4).
Таблица 4.
Эффективность терапии по нормализации ОК
| Вид терапии | Период определения остеокальцина | Результаты | ||
| Число больных c ОК (>46 нг/мл) | Частота эффективной терапии по критерию нормализации исходно повышенного уровня остеокальцина | |||
| Абс. | % | % | ||
| Фемостон n=30 | 1 | 6 | 20,0 | - |
| 2 | 4 | 13,3 | 33,3 | |
| 3 | 2 | 6,7 | 66,7 | |
| -кальцидол n=28 | 1 | 3 | 10,7 | - |
| 2 | 2 | 7,1 | 33,3 | |
| 3 | 2 | 7,1 | 33,3 | |
| Фемостон+ -кальцидол n=12 | 1 | 2 | 16,7 | - |
| 2 | 0 | 0 | 100 | |
| 3 | 0 | 0 | 100 | |
Примечания:
1 – до начала терапии;
2- через 6 месяцев после начала терапии
3- через 12 месяцев после начала терапии
Применение только фемостона обеспечивало нормализацию аномально повышенного ОК на 6 и 12-м месяце лечения у, соответственно, 33,3% и 66,7% больных. Как видно из этих данных, продолжавшееся использование фемостона на сроках от 6 до 12 месяцев позволяло преодолевать резистентность к его костнопротективному действию, установленному в конце 6-го месяца после начала лечения, только у части больных. Последнее указывает на то, что -кальцидол при более длительном применении (>6 месяцев) не наращивал свой костнопротективный потенциал.
Альфакальцидол обеспечивал нормализацию ОК и на 6-м и 12-м месяце лечения у 33,3% больных. Как видно из этих данных, продолжавшееся использование альфакальцидола на сроках от 6 до 12 месяцев не позволяло преодолевать резистентность к его костнопротективному действию, установленному в конце 6-го месяца после начала лечения.
Принято считать, что денситометрическим признаком эффективности антирезорбтивной терапии является «удерживание» показателя костной плотности в интервале, который складывается из величины «физиологической» потери КП и величины ошибки при исходном и повторном измерениях.
Согласно данным, получаемым с помощью ультразвукового денситометра Omnisense 7000S, величина «физиологического» годового снижения скорости ультразвуковой волны у здоровых женщин в возрасте 50-65 лет составляет 13 м/сек/год для лучевой кости и 9,5 м/сек/год для большеберцовой кости. Ошибка измерений ультразвукового денситометра может составлять 1%, что соответствует разнице () в 40 м/сек как для лучевой, так и для большеберцовой кости. Следовательно, достоверную разницу измерениями костной плотности можно констатировать лишь при разности СУВ более 93 м/сек (40 + 40 + 13 м/сек) для лучевой кости и более 89,5 м/сек (40 + 40 + 9,5 м/сек) для большеберцовой кости.
Для удобства измерений костной плотности перевели разность между определявшимися (исходным и последующим) показателями из м/сек в единицы Т-критерия. Следовательно, эффективной костнопротективной терапией можно считать такую, при которой разница костной плотности не превышает 0,95 ед Т-критерия для лучевой и 0,81 ед – для большеберцовой кости. Неэффективную терапию можно констатировать при превышении данных показателей.
Данные, полученные при динамической УЗ-денситометрии на первый взгляд свидетельствовали об успешности лечения у всех обследованных лиц (табл. 5). Так, не было выявлено ни одного случая неэффективности проводимой терапии ( разница между исходным и повторным измерениями костной плотности укладывалась в значения <0,95 ед Т-критерия (в лучевой кости) и <0,81 ед Т-критерия (в большеберцовой кости). Однако эти данные находились в явном противоречии с результатами определений СL – при исследовании уровня этого маркера на 6 и 12 месяце терапии были выявлены, соответственно, 11 и 9 больных с признаком ускоренной костной резорбции. По нашему мнению, это связано с недостаточной точностью динамической УЗ-денситометрии с использованными временными интервалами. Неудовлетворительная чувствительность УЗ-денситометрии объясняется величиной стандартной ошибки.
Таблица 5.
Эффективность терапии по УЗД и по уровню СL
| Число больных | Период определения | Результаты | |||
| Число больных c сохранением исходного СL | Число больных с Т | ||||
| Абс. | % в группе | % в группе | |||
| Фемостон n=30 | 1 | 4 | 13,3 | 0 | 0 |
| 2 | 2 | 6,7 | 0 | 0 | |
| -кальцидол n=28 | 1 | 7 | 25,0 | 0 | 0 |
| 2 | 7 | 25,0 | 0 | 0 | |
| Фемостон+ -кальцидол n=12 | 1 | 0 | 0 | 0 | 0 |
| 2 | 0 | 0 | 0 | 0 | |
| Всего | 1 | 1 | 15,7 | 0 | 0 |
| 2 | 9 | 15,7 | 0 | 0 | |
1 – через 6 месяцев после начала лечения;
2 – через 12 месяцев после начала лечения
Выраженность нейровегетативных проявлений климактерического синдрома (КС), оценивавшаяся по ИК, на фоне использования только фемостона снижалась с исходных 23,4+1,9 балла до 10,1+1,3 (к концу 6 месяца терапии) и до 8,2+1,4 (через 1 год после начала лечения) (рис.7). При применении комбинации фемостон+-кальцидол средние значения ИК составляли: 17,7+2,1 балла (исходное определение), 7,1+1,8 балла (через 6 месяцев лечения) и 5,7+1,9 балла (через 12 месяцев лечения). На фоне использования только -кальцидола также отмечалась редукция клинических проявлений КС с исходных 17,0+1,3 баллов до 12,3+1,4 (через 6 месяцев) и 11,6+1,5 (через 12 месяцев).
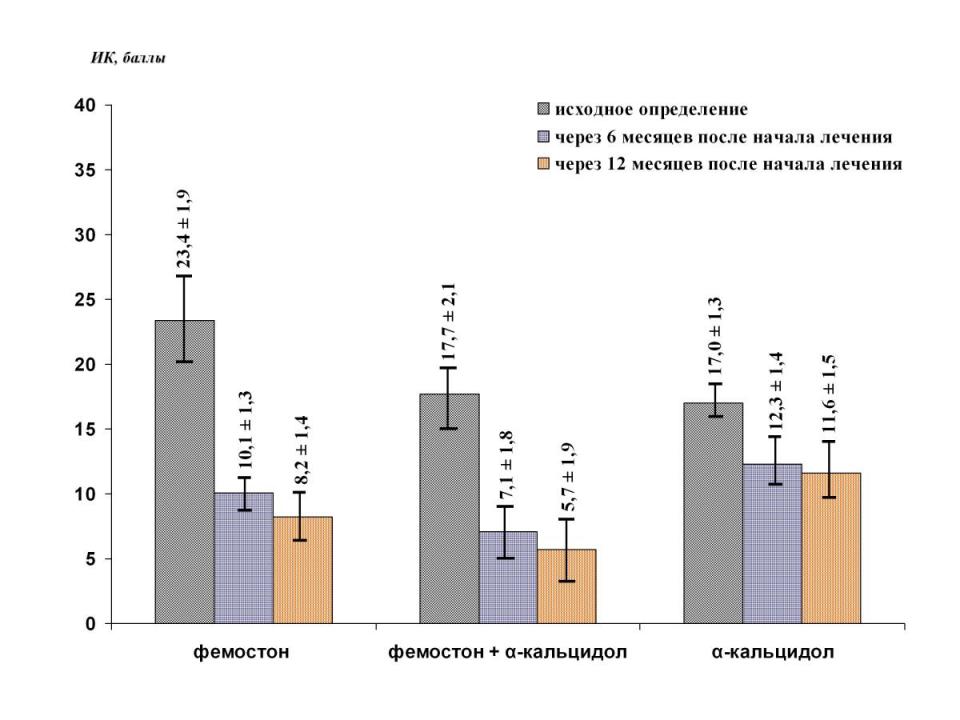
Рис. 7. Динамика ИК на фоне терапии (р<0,05).
Выраженность костно-суставных болей (КСБ) при использовании только фемостона снижалась в среднем с исходных 2,7+0,2 балла до 1,9+0,3 (к концу 6 месяца терапии) и до 1,4+0,2 (через 1 год после начала лечения) (рис. 8).
КСБ, баллы
Рис. 8. Динамика КСБ на фоне терапии ((р<0,05).
При применении комбинации фемостон+-кальцидол средние значения выраженности КСБ составляли: 3,3+0,4 балла (исходное определение), 1,4+0,2 балла (через 6 месяцев лечения), 0,8+0,3 балла (через 12 месяцев лечения). На фоне использования только -кальцидола выраженность КСБ уменьшалась в среднем с исходных 3,2+0,3 балла до 1,8+0,3 (через 6 месяцев) и 1,4+0,2 (через 12 месяцев). При этом во всех группах отмечалось достоверное (при парных сравнениях) уменьшение в процессе лечения доли больных со средними и тяжелыми проявлениями КСБ при одновременном возрастании доли пациенток с отсутствием или легкими проявлениями КСБ.
К концу 12-месячного лечения частота лиц с сохранением показателя утомляемости при обычных бытовых нагрузках (УБН) на исходном уровне на фоне использования фемостона составляла 46,7%, на фоне применения комбинации фемостон+-кальцидол – 41,7%, на фоне использования только -кальцидола – 75% (табл. 6). Заслуживает внимания, что среди пациенток, получавших только -кальцидол, в конце 12-месячного периода наблюдения у 7,1% отмечалось даже возрастание показателя УБН в сравнении с его значением до начала лечения.
Таблица 6.
Динамика показателя утомляемости на фоне терапии
| Вариант терапии | Число больных n=70 | |||||
| Уменьшение | Сохранение | Увеличение | ||||
| абс | % в группе | абс | % в группе | абс | % в группе | |
| фемостон n=30 | 16 | 53,3 | 14 | 46,7 | 0 | 0 |
| фемостон + -кальцидол n=12 | 7 | 58,3 | 5 | 41,7 | 0 | 0 |
| -кальцидол n=28 | 5 | 17,9 | 21 | 75,0 | 2 | 7,1 |
Монотерапия -кальцидолом была назначена 32 больным. За время наблюдения в течение 1 года из этой группы выбыло 4 (12,5%) больных, из которых лишь у одной пациентки (3,1%) лечение было прекращено из-за побочного эффекта в виде крапивницы. Остальные 3 женщины выбыли по разным причинам, не имевшим связи с проводимой терапией. Терапия препаратами женских половых стероидов (фемостоном) была назначена 58 женщинам, из которых 38 получали только ЗГТ, а 20 – ЗГТ в сочетании с -кальцидолом.
Из этих пациенток 16 (28,6%) женщин прервали лечение до завершения 1-годичного периода наблюдения, причем у 7 (12,8%) больных терапия была прекращена именно из-за осложнений ЗГТ. Таким образом, по выраженности перечисленных выше терапевтических эффектов ЗГТ превосходила -кальцидол, что указывает на более заметное позитивное влияние фемостона на качество жизни пациенток с ПМО. Однако, по критерию переносимости и безопасности ЗГТ значительно уступала -кальцидолу, что стало причиной отказа от дальнейшего лечения. Эти результаты приводят к заключению, что для обеспечения костнопротективного действия при терапии ПМО к ЗГТ целесообразно прибегать либо при резко-выраженных нейровегетативных проявлениях КС, либо при подтвержденной резистентности к альтернативным негормональным средствам, проявляющейся в сохранении показателей КСБ и УБН на исходном уровне.
Таблица 7.
Структура побочных эффектов.
| Определявшиеся параметры | варианты лечения ПМО | ||
| ЗГТ фемостоном n = 58 | -кальцидол n = 32 | ||
| Число выбывших больных | Причины, связанные с побочными эффектами использованного лечения | 12,1% | 3,1% |
| Причины, не связанные с побочными эффектами использованного лечения | 15,5% | 9,4% | |
| Характеристика побочных эффектов | Кожная аллергическая реакция | - | 3,1% |
| Учащение приливов | 1,7% | - | |
| Тромбоз глубоких вен голени, тромбофлебит | 3,4% | - | |
| Гиперплазия эндометрия | 3,4% | - | |
| Мастодиния | 1,7% | - | |
| Ухудшение зрения | 1,7% | - | |
ВЫВОДЫ
1. Комбинация фемостон+альфакальцидол оказывает более выраженный антирезорбтивный эффект в сравнении с монотерапией каждым из препаратов.
2. Использование ЗГТ фемостоном (комбинируемой или нет с альфакальцидолом) оказывает более выраженные эффекты на:
- подавление симптомов климактерического синдрома;
- уменьшение выраженности костно-суставных болей;
- выраженность утомляемости.
3. Такие маркеры, как общий и ионизированный кальций, фосфаты, остеокальцин и щелочная фосфатаза непригодны для характеристики активности процесса костной резорбции.
4. При ПМО выраженность процесса костной резорбции (характеризуемая по уровню -cross laps) не коррелирует ни с распространенностью процесса, ни со степенью снижения ПКТ (по данным УЗД); также не получено достоверной корреляции между степенью снижения ПКТ в лучевой и большеберцовой костях.
5. Динамические определения -cross laps дают достоверную информацию об изменениях активности костной резорбции под влиянием проводимой терапии.
6. Динамическая УЗД с интервалами в 6 и 12 месяцев непригодная для оценки эффективности костнопротективной терапии.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. У женщин в постменопаузе с подозрением на остеопороз следует прицельно оценивать состояние костной ткани. Для этого денсито-метрическое исследование ПКТ необходимо сочетать с определением CL. Показания к назначению антирезорбтивной терапии должны определять: 1) низкая ПКТ; 2) высокие показатели CL (>0,58 нг/мл) независимо от наличия или отсутствия отклонений ПКТ в исследуемых костях.
2. При проведении костнопротективной терапии необходимо контроли-ровать ее эффективность по динамике изменений уровня CL через 6 месяцев после начала лечения. Эффективной антирезорбтивной терапией следует считать: а) у пациенток с любыми значениями ПКТ и исходным CL >0,58 нг/мл - снижение уровня этого маркера до нормативных значений (цель лечения - торможение аномально ускоренной костной резорбции); б) у пациенток с денситометрическими признаками остеопении / остеопороза и исходным CL<0,58 нг/мл - снижение уровня этого маркера не менее чем на 20% от его исходного значения (цель лечения - уменьшение скорости костной резорбции для редукции величины ежегодной физиологической потери костной ткани). При недостижении указанных целей назначенная костнопротективная терапия должна быть признана неэффективной, что требует пересмотра тактики проводимого лечения. Спустя 6 месяцев после такой коррекции в лечении следует вновь оценить его эффективность для определения последующей тактики.
3. В процессе контроля эффективности антирезорбтивной терапии при ПМО следует ориентироваться на изменения уровня CL. Использование для этой цели определений оСа+2, иСа+2, кФ и ОК неоправданно.
Не рекомендуется использование динамической ультразвуковой денситометрии с интервалами в 6 и 12 месяцев в связи с отсутствием достоверности получаемых результатов.
4. Костнопротективная терапия должна проводиться длительное время и оцениваться по уровню CL через 6 месяцев, далее – 1 раз в 2 года. Если при этом обнаруживается возрастание значений указанного маркера на 20% от уровня, зарегистрированного при последней проверке, это должно служить показанием к пересмотру тактики лечения.
5. При выборе конкретных препаратов для костнопротективной терапии ПМО следует руководствоваться следующим алгоритмом:
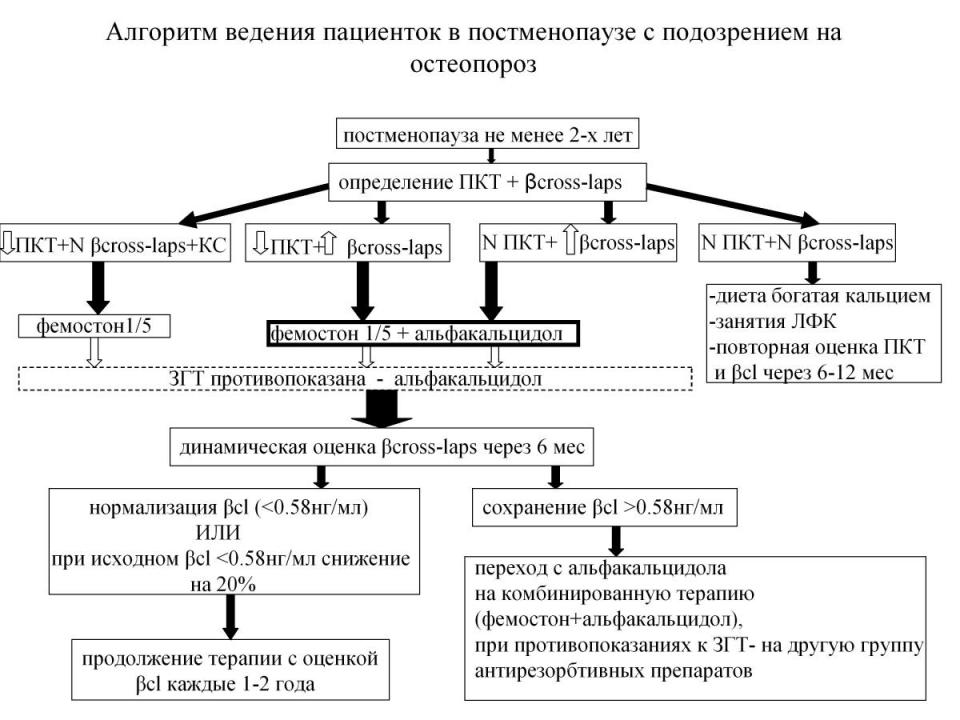
Список работ, опубликованных по теме диссертации:
- Краснопольский В.И., Гаспарян Н.Д., Бабунашвили Е.Л., Мельникова Ю.Н., Склянкина И.В. Состояние эндо- и миометрия при лечении фемостоном 1/5 и альфакальцидолом постменопаузального остеопороза. // Материалы XIII Национального конгресса «Человек и лекарство». – М., 2006. – С.180.
- Краснопольский В.И., Гаспарян Н.Д., Бабунашвили Е.Л., Мельникова Ю.Н., Титченко Ю.П. Состояние эндометрия в постменопаузе при лечении остеопороза фемостоном 1/5. // Материалы VIII Всероссийского Форума «Мать и дитя». — М., 2006. — С. 420—421.
- Краснопольский В.И., Гаспарян Н.Д., Бабунашвили Е.Л., Мельникова Ю.Н. Влияние лечения женщин с постменопаузальным остеопорозом на качество их жизни. // Российский вестник акушера-гинеколога. — М., 2006. — Т. 6. — №6. — С. 34—36.
- Краснопольский В.И., Гаспарян Н.Д., Мельникова Ю.Н. Бабунашвили Е.Л. Оценка качества жизни женщин при лечении постменопаузального остеопороза. // Материалы I регионального научного форума «Мать и дитя». — Казань, 2007. — С. 274—275.
- Краснопольский В.И., Гаспарян Н.Д., Мельникова Ю.Н., Горенкова О.С. Влияние фемостона 1/5 на плотность костной ткани у женщин в постменопаузе. // Материалы XIV Российского национального конгресса «Человек и лекарство». — М., 2007. — С. 127.

