Прогнозирование перинатальных исходов при синдроме поликистозных яичников в зависимости от метода восстановления фертильности
На правах рукописи
ЖУРАВЛЕВА
Юлия Александровна
ПРОГНОЗИРОВАНИЕ ПЕРИНАТАЛЬНЫХ ИСХОДОВ
ПРИ СИНДРОМЕ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ В ЗАВИСИМОСТИ ОТ МЕТОДА ВОССТАНОВЛЕНИЯ ФЕРТИЛЬНОСТИ
14.01.01 – акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Волгоград – 2011
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Уральская государственная медицинская академия Минздоавсоцразвития России».
Научный руководитель: доктор медицинских наук, профессор
Зильбер Марина Юрьевна
Официальные оппоненты:
доктор медицинский наук, профессор
Геворкян Марьям Арамовна
доктор медицинский наук
Андреева Маргарита Викторовна
Ведущее учреждение: Московский областной научно-исследовательский институт акушерства и гинекологии
Защита диссертации состоится «24» июня 2011 года в _____ часов на заседании диссертационного совета Д 208.008.05 при Волгоградском Государственном медицинском университете (400131, г. Волгоград, пл. Павших борцов, 1).
С диссертацией можно ознакомиться в библиотеке Волгоградского Государственного медицинского университета.
Автореферат разослан «24» мая 2011 г.
Ученый секретарь
диссертационного совета:
доктор медицинских наук, профессор Селихова
Марина Сергеевна
СПИСОК СОКРАЩЕНИЙ
АФП - альфа-фетопротеин
ВА - волчаночный антикоагулянт
ВРТ – вспомогательные репродуктивные технологии
ГА - гиперандрогения
ДГЭАс – дэгидроэпиандростерона сульфат
Е2 - эстриол
ЗВУР – задержка внутриутробного развития
КВАЗАР – комплекс вычислительных алгоритмов для задач распознавания
КТГ - кардиотокография
ПГ – прогестерон
ПЛ – плацентарный лактоген
СГЯ – синдром гиперстимуляции яичников
СПКЯ – синдром поликистозных яичников
ТБГ – трофобластический гамма – глобулин
Т – тестостерон общий
Т св. - тестостерон свободный
ТТГ – тиреотропный гормон
ТЭСГ – тестостеронэстрадиолсвязывающий глобулин
ФПН – фетоплацентарная недостаточность
ЭКО и ПЭ – экстракорпоральное оплодотворение и перенос эмбриона
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы. Одной из наиболее актуальных проблем акушерско – гинекологической эндокринологии, определяющей патологию репродуктивной функции (Манухин И.Б. 2007, Boosma C. 2006, Legro R. 2007) - является синдром поликистозных яичников (СПКЯ). Среди женского населения, по данным различных авторов, частота встречаемости СПКЯ колеблется от 3 до 11% (Андреева Е.Н. 2005, Геворкян М.А. 2006, Глухова С.В. 2008, Дедов И.И. 2009, Kumar A. 2005,Mesinis I. 2005, Aziz R. 2006, Chang J. 2007, Hirschberg A. L. 2009), а среди женщин репродуктивного возраста, этот показатель составляет – 15%. (Глухова С.В. 2008, Артымук Н.В. 2009, Манухин И.Б. 2010, Franks S. 2006, Norman R.J. 2007).
Однако, высокая распространенность бесплодия среди данной патологии и прогрессивное развитие высоких репродуктивных технологий (ВРТ), перевели изучение проблемы в иное русло, связанное с материнством (Сидельникова В.М. 2007, 59). Доказано, что частота наступления беременности после ЭКО и ПЭ (экстракорпоральное оплодотворение и перенос эмбриона) в значительной степени зависит от формы и клинической картины заболевания, длительности предварительного его лечения и степени проявления гормональных нарушений. Варианты течения СПКЯ (с менархе или с ожирением) отражаются на эффективности методов стимуляции яичников (Калинина Е.А. 2005, Назаренко Т.А. 2010, Homburg R. 2008), а широкое внедрение методов ВРТ, предусматривающих индукцию суперовуляции и применение современных стимуляторов овуляции при лечении, усугубляют нарушения стероидогенеза у больных с гиперандрогенией (Дедов И.И. 2009).
Следует особо подчеркнуть, что при беременности на фоне гиперандрогении формируются гестационные осложнения до 48% (F.Orio 2008, K.I.Cheang 2009). Это – в 30% невынашивание беременности (Бородин Ю.И. и соавт., 2006; Haakova L. 2003, Evan R. 2005), истмико-цервикальная недостаточность (ИЦН), плацентарная недостаточность (ПН) (Милованов А.П., 2000; Абдурахманова Р.А., 2002; Качалина Т.С. 2004, Агаркова Л.А., Диш О.Г. 2007). Не исключается и внутриутробная гибель плода (Подзолкова Н.М. 2004, Olson C.K. 2005; Lindn А. 2009; Tang T. 2009)..
В то же время, исследователей продолжает волновать вопрос, в какой мере, используемая репродуктивная технология безопасна для здоровья матери и будущего потомства (Кулаков В.И. 2005, Барашнев В.И. 2005, Пшеничникова Т.Б. 2006, Bowdin S. 2007, Neveu N 2007). Несмотря на многочисленные исследования, на сегодняшний день до конца не определены подходы к ведению беременности и перинатальному прогнозированию у пациенток в зависимости от методов восстановления фертильности при СПКЯ, что является целью нашего исследования.
Цель работы. Улучшить перинатальные исходы у беременных с СПКЯ при различных методах восстановления фертильности на основании разработки прогностических критериев ведения беременности.
Данная цель реализуется в решении следующих научных задач:
1. Изучить особенности течения беременности, родов, послеродового периода у пациенток с СПКЯ, индуцированной различными методами.
2. Проанализировать состояние фетоплацентарного комплекса и перинатальные исходы при СПКЯ в зависимости от метода восстановления фертильности.
3. Выделить факторы риска развития перинатальных осложнений при беременности, индуцированной различными методами у пациенток с СПКЯ, реализованные в решающем правиле прогноза перинатального благополучия.
4. Разработать и внедрить в акушерскую практику дифференцированный алгоритм прогнозирования перинатальных исходов для пациенток с СПКЯ при различных методах восстановления фертильности.
5. Оценить эффективность и приемлемость предложенного прогностического алгоритма для усовершенствования ведения беременности при СПКЯ и улучшения перинатальных исходов.
Научная новизна исследования. В данной работе нами уточнены особенности течения беременности и родов и определены наиболее частые осложнения гестационного периода у пациенток с СПКЯ в зависимости от метода восстановления фертильности. В работе показаны различия в состоянии маточно-плодово-плацентарного кровотока, гормонов плацентарного комплекса и свёртывающей системы крови по триместрам у пациенток с СПКЯ в зависимости от метода восстановления фертильности. Впервые, на основании выделения факторов риска развития перинатальных осложнений, применен метод математического прогнозирования развития перинатальных исходов у пациенток с СПКЯ в зависимости от метода восстановления фертильности. Оптимизированы практические рекомендации по ведению беременности у пациенток с СПКЯ, в зависимости от метода восстановления фертильности и доказана их эффективность.
Практическая значимость работы. Применение метода многофакторного анализа прогнозирования перинатальных исходов позволило на практике разделить беременных на группы по тяжести предполагаемых перинатальных осложнений у пациенток с СПКЯ при различных методах восстановления фертильности. Оптимизированные и предложенные в клиническую практику рекомендации ведения беременных с СПКЯ явились резервом для улучшения перинатальных исходов. Использование, предложенного нами лечебно- профилактического комплекса привело к снижению частоты невынашивания беременности в 1,6 раза, уменьшению на 40% развития гипотрофии плода, улучшению неонатальной адаптации на 33%, к снижению развития неонатальной инфекции в 2 раза.
Основные положения диссертации, выносимые на защиту:
1. При беременности с СПКЯ имеются разноплановые гестационные осложнения, зависящие от метода восстановления фертильности и влияющие на исходы родов.
2. Оценка состояния фетоплацентарного комплекса определила корреляционную зависимость между его функционированием и тяжестью перинатальных исходов, позволила выделить факторы риска перинатальных осложнений, реализованных в составлении решающего правила математического прогнозирования.
3. Оптимизированный комплекс лечебно-профилактических мероприятий ведения беременных с СПКЯ с учётом метода восстановления фертильности позволил снизить тяжёлые перинатальные исходы и улучшить раннюю адаптацию новорождённых.
Внедрение результатов исследований в практику. Разработанные нами методы прогнозирования, внедрены в практику работы амбулаторно – поликлинического звена и круглосуточных стационаров патологии беременности многопрофильных клинических больниц №6, № 24, № 40 г. Екатеринбурга, в ряде других лечебно – профилактических учреждений Свердловской области. Материалы исследований используются в лекциях, практических занятиях со студентами 6 курса, клиническими интернами и ординаторами лечебно – профилактического факультета ГОУ ВПО УГМА.
Апробация работы. Основные положения диссертации доложены и обсуждены на заседаниях проблемной комиссии и Ученого Совета ГОУ ВПО «Уральская государственная медицинская академия» Россздрава (г. Екатеринбург, 2006), городской научно-практической конференции, посвященной юбилею МУ ЦГКБ № 24 г. Екатеринбурга (г. Екатеринбург, 2007г.), в работе I съезда акушеров-гинекологов Урала 2009 года, региональной конференции «Мать и дитя» 28-30 июня 2010 года.
По теме диссертации опубликовано 8 научных работ: журнальные статьи – 3 (в том числе 3 – в журналах, входящих в рекомендованный ВАК Минобрнауки России перечень научных изданий).
Объём и структура диссертации. Диссертация изложена на 174 страницах компьютерного текста в текстовом редакторе Microsoft Word и состоит из введения, обзора литературы, описания материала и методов исследования, 3 глав собственных исследований, обсуждения полученных результатов, выводов, практических рекомендаций и указателя литературы. Библиография включает 203 источника, в том числе – 82 отечественных и 121 зарубежных авторов. Работа проиллюстрирована 30 таблицами и 23 рисунками.
СОДЕРЖАНИЕ РАБОТЫ
Материал и методы исследования. Для достижения поставленной цели и решения задач исследования, в период с января 2000 года по январь 2010 года нами было проведено комплексное клинико-лабораторное обследование 189 беременных и их новорожденных.
I группа – группа сравнения - 69 беременных с СПКЯ в анамнезе, беременность у которых была достигнута проведением различных вариантов лапароскопических операций на яичниках в сочетании с индукцией овуляции, которая проводилась с использованием гонадотропинов.
II группа – основная группа - 70 беременных с СПКЯ в анамнезе, беременность у которых наступила после применения вспомогательных репродуктивных технологий (ВРТ);
III группа – контрольная - 50 здоровых беременных без клинических и лабораторных признаков СПКЯ.
Критериями включения пациенток в исследование явилось наличие в анамнезе бесплодия, обусловленного СПКЯ по критериям The Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group 2004, возраст беременных до 35 лет, фертильность мужа, использование гонадотропинов в качестве индукторов созревания фолликулов и одноплодная беременность, срок беременности до 7 недель.
Критериями исключения стали: гиперандрогения неуточнённого или надпочечникового генеза, наличие доброкачественных опухолей яичников, трубно-перитонеальный фактор бесплодия, многоплодная беременность, мужской фактор бесплодия.
На каждую беременную была заполнена специально разработанная статистическая карта наблюдения. Обследуемые группы беременных были сходны по основным характеристикам: возрасту, акушерскому, гинекологическому анамнезу, частоте и характеру экстрагенитальной патологии и длительности бесплодия.
Все беременные были обследованы в соответствии с Приказом МЗ РФ №50, от 10.02 2003 года, № 808 от 02.10.09 г. и региональными стандартами ведения беременных. В работе использовались следующие методы диагностики: клинические, лабораторные (биохимические, гемостазиологические, гормональные, иммунологические), инструментальные, статистические. Помимо общеклинических анализов крови, мочи и мазка применялись и специфические. Для обследования углеводного обмена определялись: гликемический профиль, глюкозотолерантный тест (ГТТ), ацетон мочи, суточная глюкозурия. Белковый обмен оценивался с помощью определения концентрации общего белка плазмы крови, а показатели гемостаза по времени свертывания крови, времени кровотечения, концентрации фибриногена, АЧТВ, протромбина, плазминогена «Д» - димера, волчаночного антикоагулянта. Гормональная функция плацентарного комплекса оценивалась по уровню альфафетопротеина (АФП), плацентарного лактогена (ПЛ), трофобластического глобулина (ТБГ) и эстриола (Е 3 ) в плазме крови иммунохемолюминисцентным методом. Определение уровня эстриола проводилось с использованием иммуноферментных наборов «VEDA.LAB”. Урогенитальные инфекции диагностировались с помощью культурального метода, полимеразной цепной реакцией (ПЦР), иммуноферментным анализом (ИФА) определяли в крови антитела анализаторами «Hofmann – La Rochec» (Швейцария) и «Medac» (Германия). Состояние плода и плацентарного комплекса исследовалось при помощи аппарата "GL Logic - 5000", "Aloka SSD - 1200" Кардиотокографию (КТГ) проводили на аппаратах Colometrics – 145 (США), Analogic Fetalgard – 2000 (США), Air Shields 1200.
Эффективность программы ЭКО оценивали по частоте наступления беременности на цикл стимуляции овуляции и с учётом общепризнанного показателя «take home baby rate» (THBR).У новорожденных изучался ранний адаптационный период. Определялось наличие асфиксии и её степень с помощью шкалы Апгар, зрелость и доношенность ребенка.
Полученные в процессе исследования данные были обработаны с помощью пакета прикладных статистических программ MS Excel для Windows ХР, «Statistica 6.0». Для определения информативности показателей расчет коэффициентов проводили с помощью методов многофакторного статистического анализа, реализованного в пакете «КВАЗАР». Статистически значимыми считали отличия при р<0,05 (95%-й уровень значимости) и при р<0,01 (99%-й уровень значимости).
Результаты исследования и их обсуждение. Возраст обследованных беременных колебался от 22 до 35 лет и составил в группе сравнения 28,6±0,4, в основной группе 29,2±0,5 года (р1,2>0,05), а в группе контроля средний возраст беременных был 27,1±0,6 года (р1,3 < 0,02; р2,3< 0,001).
Изучение экстрагенитальной патологии в группах показало, что в обеих группах исследования ведущее место занимают заболевания сердечно-сосудистой системы, эндокринные нарушения и патология жирового обмена (р1,2>0,05, р1,3<0,001; р2,3 < 0,001).
Для большинства пациенток с СПКЯ характерно первичное бесплодие. Общая длительность бесплодия колебалась от 1 до 16 лет, и составила в группе сравнения 4,25±0,3 года по сравнению с основной группой 4,96±0,2 года
(р1,2 >0,05). Анализ гинекологической заболеваемости свидетельствовал о высокой частоте воспалительной патологии гениталий в группе сравнения у 36,2% против 44,3% в основной группе, эндокринных нарушений (миома матки, эндометриоз, доброкачественные кисты яичников) у пациенток групп исследования, что не имело статистически значимых различий
При обобщении результатов течения I триместра беременности у пациенток с СПКЯ при различных методах восстановления фертильности, была выявлена высокая частота акушерских осложнений, таких как синдром гиперстимуляции яичников (СГЯ) в группе сравнения был диагностирован у 2 (2,9%) пациенток только лёгкой степени, а у беременных основной группы у 12 (17,1%) всех степеней тяжести (р1,2< 0,01). Наиболее частым осложнением беременности I триместра в обеих группах являлся угрожающий выкидыш, который диагностирован у 40 (63,4%) vs 45 (71,4%) беременных (р1,2>0,05), превышая показатель группы контроля 7 (14%) (р2,,3< 0,001; р1,3< 0,001). Высока и частота перманентной угрозы прерывания. Среди пациенток группы сравнения этот показатель составил 5 (7%), а в основной группе 12 (17%) случаев, в группе контроля данная патология не встречалась (р1,2< 0,05, р2,3 <0,001, р1,3 <0,02). Кровотечение из половых путей, обусловленное отслойкой хориона и образованием ретрохориальной гематомы достоверно реже регистрировалось в группе сравнения 17 (25%), чем в основной группе 29 (41%) (р1,2< 0,05, р2,3 <0,001,
р1,3 <0,001). Развитие угрозы невынашивания при всех видах индуцированной беременности может быть обусловлено нарушением секреторной трансформации эндометрия на фоне гиперсекреции половых гормонов. При оценке показателей системы гемостаза частота выявления приобретенных тромбофилических состояний составляла: в группе сравнения 7(10,1%), в основной группе 19 (27,1%), а в группе контроля только у 1(2%), (р1,2<0,001; р2,3< 0,001, p1,3< 0,05).
Ранний токсикоз различной степени тяжести был у 19 (28%) беременных группы сравнения, у 24 (35%) беременных основной группы и у 8 (16%) в группе контроля, что не отличалось от среднестатистических показателей. Тяжёлая степень раннего токсикоза беременных (рвота 8 – 10 раз в сутки, выраженная гиперсаливация, потеря веса на 3 – 5 кг лабораторные признаки метаболического ацидоза) была диагностирована только у 4 (6%) пациенток основной группы, что коррелировало с развитием СГЯ средней и тяжёлой степени (r=0,681, р=0,005).
ОРВИ в I триместре беременности перенесли 2 (3%) беременных группы сравнения, 7 (10%) беременных основной группы, а в группе контроля 1(2%), что составило (р1,2<0,05, р2,3 < 0,05, р 1,3 > 0,05), что по данным различных исследователей может обуславливать аномалии развития плаценты (бочкообразная плацента, краевое прикрепление пуповины, дольчатость плаценты и.т.д.) и увеличивать риск преждевременных родов. Активация вирусной и\или бактериальной инфекции у беременных группы сравнения была выявлена в 3 (4,8%) случаях, в основной же группе достоверно чаще и составило 8 (11,4%) случаев, а в группе контроля 1 (2%), что имело статистически значимые отличия (р1,2<0,05; р2,3< 0,05, p1,3> 0,05), что коррелировало с развитием хронической гипоксии плода (r=0,542, р=0,020).
Как следствие ранних осложнений гестации у больных с СПКЯ, репродуктивные потери I триместра беременности при различных методах восстановления фертильности составили в группе сравнения 4 (5,6%), а в группе контроля 6 (8,6%) (р1,2 > 0,05).
Во II триместре мы увидели снижение частоты угрожающего выкидыша в обеих группах исследования на 31% в группе сравнения и на 10% в основной группе по сравнению с показателями I триместра, однако достоверно реже угрожающий выкидыш продолжает регистрироваться у беременных группы сравнения 21 (32,3%) против 39 (60,9%) основной группы (р1,2 <0,05). Не зависимо от метода восстановления фертильности, для пациенток исследуемых групп было характерно развитие ИЦН. Всем пациенткам была проведена хирургическая коррекция ИЦН в сроке 16-24 недели 12 (17,4%) беременным группы сравнения и 15 (21,4%) в основной группе.
Ко II триместру нормализовались показатели свёртывающей системы крови и хронический ДВС – синдром был диагностирован только у 2 (3,1%)беременных группы сравнения и у 7(10,9%) в основной группе (р1,2 <0,05). Раннее начало гестоза было диагностировано у 5 (7,7%) беременных группы сравнения, у 10 (15,6 %) беременных основной группы и только у 2 (4%) в группе контроля (р1,2> 0,05, р1,3 <0,001, р2,3 <0,001), что проявлялось в большей степени развитием отёков и патологической прибавкой массы тел.
Гестационный диабет во II триместре был диагностирован у 2 (1,5 %) беременных группы сравнения и у 5 (7,8%) беременных основной группы
(р1,2 < 0,05), что незначительно превышало средне популяционные показатели (2-6%).
Наличие факторов риска у пациенток с СПКЯ является причинной раннего формирования фетоплацентарной недостаточности и синдрома задержки развития плода со II триместре беременности. Плацентарная недостаточность достоверно реже встречалась у беременных в группе сравнения 8 (11,6%), по сравнению с показателями в основной группе у 16 (22,9%) и только у 2 (4%) группы контроля (р1,2 <0,05, р2,3 <0,001, р1,3<0,01). Несмотря на осложнённое течение II триместра беременности, частота репродуктивных потерь составила в группе сравнения 2 (3,1%), а в группе контроля 1 (1,7%). Факторами, определившими репродуктивные потери II триместра, стала ИЦН и преждевременное излитие околоплодных вод на фоне обострения вирусно-бактериальной инфекции.
Течение III триместра беременности характеризовалось развитием гестоза различной степени тяжести с преобладанием гипертензии у беременных группы сравнения у 22 (34,9 %), в основной группе в 30 (47,6 %) случаев и в группе контроля у 4 (8%) (р1,2 <0,05, р2,3 <0,001, р1,3<0,01), что можно объяснить снижением адаптационных механизмов в организме наблюдаемых беременных, изменениями в свёртывающей системе крови после ЭКО. В основе формирования плацентарной недостаточности, которая диагностировалась у 12 (19%) беременных группы сравнения, а в основной группе у 21 (33,3%) и у 3 (6%) беременных группы контроля (р1,2 <0,05, р2,3 < 0,001, р1,3 <0,05), лежат нарушения плацентарного микроциркуляторного кровообращения, обменных процессов, как реакция плаценты на различные патологические состояния матери на предыдущих этапах гестационного процесса.
Известно, что индуцированная беременность развивается на фоне нарушения соотношений между эндогенными и экзогенными гормонами. Согласно нашему исследованию, концентрация прогестерона у беременных с СПКЯ в группе сравнения в 3 раза, а в контрольной группе в 5,4 раза была меньше, чем в основной группе (p1.2< 0,001, p2,3 < 0,05, р1,3< 0,001). При исследовании уровня эстрадиола в сроке 6 недель у пациенток после программы ЭКО, мы увидели превышение нормативных показателей в 2,5 раза по сравнению с индуцированной беременностью и здоровыми беременными: в группе сравнения 4850±1742 пмоль/л, в основной группе 11876±2547 пмоль/л, в группе контроля 4720 ±921 пмоль/л (при норме для этого срока 4700±700 пмоль/л. Учитывая исходную гиперандрогению, мы решили проследить динамику уровня тестостерона в период гестации у беременных с СПКЯ при различных методах восстановления фертильности и было выявлено, что концентрация общего тестостерона в период беременности при СПКЯ имеет прямую корреляционную связь со сроком беременности (r=0,682; p=0,0001) и индексом периферического сосудистого сопротивления в сосудах пуповины плода по доплерометрическому исследованию (r=0,673; p=0,003). Динамика уровней общего тестостерона в период беременности представлена на рисунке 1.
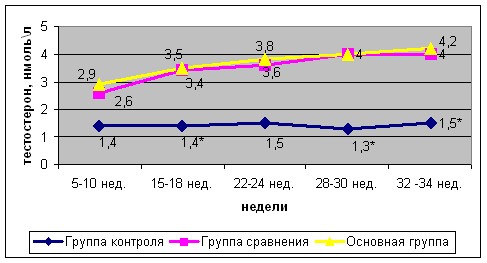
* - статистическая значимость р<0,01 в сравнении с контрольной группой
Рис. 1. Уровень содержания тестостерона (нмоль/л) в течение беременности
Более высокие показатели ТБГ у беременных группы контроля и сравнения в течение всей беременности, чем у беременных основной группы может быть обусловлено дистрофическими изменениями в плаценте, сформировавшимися ещё в I триместре. Нами выявлено, что уровни ТБГ и ПЛ имеют прямую положительную корреляционную связь с состоянием плода (r =0,61, p=0,01 и r =0,56, р=0,02) и обратную зависимость с состоянием плодово-плацентарного кровотока (r =-0,55, p=0,03 и r=-0,49, р=0,04), то есть увеличение ТБГ и ПЛ свидетельствует об улучшении внутриутробного состояния плода (повышение оценки по Фишеру), а так же об улучшении маточно-плацентарного кровотока и снижении ИР в артерии пуповины. Данные динамики уровня ТБГ и плацентарного лактогена представлены на рисунках 2 и 3.
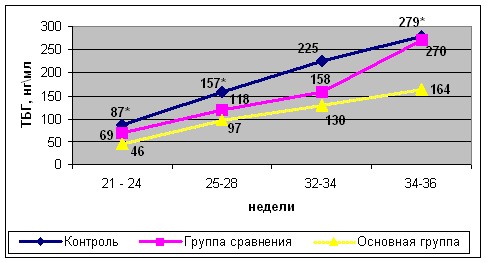
*- статистическая значимость р<0,05 в сравнении между I и II группами и группой контроля
Рис. 2. Уровни трофобластического глобулина (ТБГ) (нг/мл) в сыворотке крови у беременных
Показатели ПЛ в обеих группах исследования с СПКЯ были несколько ниже значений, полученных для здоровых беременных, и в основной группе отмечался более медленный прирост этих показателей, что отражено на рисунке3.
Исследования гормональных показателей функционирования плаценты позволило нам определить тип гормональной регуляции плаценты. Так, сниженный тип регуляции преобладал у беременных основной группы в 5 (7,9%), у беременных группы сравнения – у 2 (3%), что было признаком истощения плацентарного комплекса.
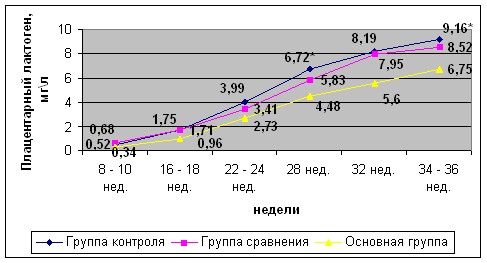
*- статистическая значимость р<0,05 в сравнении между IIгруппой и группой контроля
Рис. 3. Уровни плацентарного лактогена (ПЛ) (мг/л) в сыворотке крови у
беременных исследуемых групп в различные сроки беременности
Неустойчивый тип регуляции был выявлен у 3 (4,8%) беременных группы сравнения, у 7 (11,1%) беременных основной группы, в группе контроля не встречалось. Повышенный тип гормональной регуляции был диагностирован одинаково часто в обеих группах с СПКЯ у 5 (7,9%) беременных соответственно и у 1 (2 %) в группе контроля. У остальных пациенток функционирование плацентарной системы было расценено, как удовлетворительное. Особое внимание заслуживает группа пациенток с СПКЯ, у которой в начале беременности по УЗИ выявляется полное предлежание хориона (плаценты), что составило в группе сравнения 3 (4,3%), в основной группе 9 (17,1%) во много раз превышая показатели группы контроля (р1,2< 0,05, р2,3 < 0,001, р1,3< 0,05), гипоплазия хориона в группе сравнения составила 3 (4,3%), а в основной группе встречалась достоверно чаще, в 7 (10%) случаев, и это может обуславливать высокую частоту перинатальных осложнений у данной группы пациенток. Характеристика локализации плаценты по данным УЗИ представлены в таблице 1.
При осложнённом течении беременности для ранней диагностики нарушений маточно-плацентарного кровообращения большое значение приобретает доплерометрическое исследование кровотока.
Таблица 1
Особенности локализации плаценты и признаков угрожающего выкидыша у беременных с СПКЯ по данным УЗИ
| Вид патологии | Группа контроля | Группа сравнения | Основная группа | |||
| Абс. | % | Абс. | % | Абс. | % | |
| I триместр | n=50 | n=69 | n=70 | |||
| Полное предлежание хориона | 1 | 2 | 3 | 4,3*^ | 9 | 17,1** |
| Краевое прикрепление | 2 | 4 | 10 | 14,5 | 8 | 11,4 |
| Отслойка хориона (ретрохориальная гематома) | 1 | 2 | 5 | 7^ | 13 | 19^** |
* - статистическая значимость р<0,05 в сравнении с контрольной группой
** - статистическая значимость р<0,001 в сравнении с контрольной группой
^ - статистическая значимость р<0,05 в сравнении между 1 и 2 группами
По данным исследования нарушения маточно-плацентарного (МПК) и плодово-плацентарного кровотока (ППК) в 22 – 24 недели зарегистрировано у 4 (6,2%) группы сравнения, у 9 (12,9%) в основной группе (р1,2>0,05, р2,3 < 0,001, р1,3< 0,05). В 32 – 34 недели в группе сравнения у 6 (9%) беременных, у 17 (27%) в основной группе и у 2 (4%) в группе контроля. (р1,2< 0,05, р1,3< 0,05). Изменения плодово-плацентарного кровотока характеризовалось повышением индекса резистентности в артерии пуповины, а характерным признаком нарушения маточно-плацентарного кровотока было увеличение сосудистого сопротивления в маточных артериях.
Основным способом родоразрешения у пациенток исследуемых групп была операция кесарева сечения и проводилась она чаще всего по сочетанным показаниям, в плановом порядке группе сравнения у 43 (68,3%), в основной группе у 52 (82,5%) беременных, и в группе контроля у 7 (14%), (р1,2 < 0,02, р1,3 < 0,001, р2,3 < 0,001). Роды произошли в срок у всех беременных контрольной группы, у 58 (92,1%) беременных группы сравнения и у 54 (85,7%) в основной группе соответственно и только у 5 (7,9%) и 9 (14,3%) беременных группы сравнения и основной группы произошли преждевременные роды.
Всего родилось 176 детей. Средняя оценка на 1 и 5 минуте различалась и составила в группе сравнения 6,81±0,1, на 5 минуте 7,82±0,1, в основной группе – 6,54±0,2, на 5 минуте – 7,48±0,1 балла, а в группе контроля 7,4±0,1 и 8,18±0,1 (р1,2< 0,02, р1,3< 0,001 р2,3< 0,001).Средняя масса тела детей, рождённых при контролируемой индукции овуляции у пациенток группы сравнения составила 3274,1±64,3 г, длина 50,9±0,3 см, у женщин основной группы - 3030±72,6 г, 49,5±0,5 см. (р1,2= 0,002), а в группе контроля 3538,5±57 гр. и 51,9±0,2 ( р1,3 < 0,001; р 2,3 <0,001).
Перинатальных проблемы, характеризовались высоким процентом рождения детей в состоянии асфиксии тяжелой степени в группе сравнения 2 (3,2%) против 6 (9,5%) в основной группе, гипоксически-ишемическим поражениями ЦНС в группе сравнения 12 (14,3%) против 20 (31,7 %) в основной группе, МФН (в группе сравнения 4 (6,3 %) против 10 (15,9%) в основной группе), ЗВУР (у 5 (7,9%) группы сравнения против 12 (19 %) в основной группе). Врождённые пороки развития были диагностированы только у 4 (6,3 %) детей основной группы Патологические состояния новорождённых представлены в таблице 2.
Таблица 2
Патологические состояния новорожденных, выявленных в неонатальном
периоде у пациенток с СПКЯ
| Состояние новорожденных | Контрольная группа(n=50) | Группа сравнения (n=63) | Основная группа (n=63) | |||
| Абс. | % | Абс. | % | Абс. | % | |
| Недоношенность | - | - | 5 | 7,9** | 9 | 14,3** |
| Асфиксия при рождении | - | - | 2 | 3,2 | 6 | 9,5* |
| Гипоксически-ишемические поражения ЦНС | 1 | 2 | 12 | 14,3^** | 20 | 31,7^** |
| Инфекционно-воспалительные заболевания неонатального периода | 2 | 4 | 10 | 15,9^* | 18 | 28,6^** |
| Синдром дыхательных расстройств | - | - | 4 | 6,3^* | 10 | 15,9^** |
| ЗВУР (гипотрофический вариант) | - | - | 5 | 7,9^* | 12 | 19^** |
| Транзиторные неврологические изменения (синдром гипервозбудимости, синдром угнетения, синдром мышечной дистонии) | 3 | 6 | 10 | 15,9^* | 18 | 28,6^** |
| Морфо-функциональная незрелость | 1 | 2 | 4 | 6,3^ | 10 | 15,9^* |
* - статистическая значимость р<0,05 в сравнении с контрольной группой
** - статистическая значимость р<0,001 в сравнении с контрольной группой
^ - статистическая значимость р<0,05 в сравнении между 1 и 2 группами
Для выявления и оценки факторов риска развития перинатальных осложнений определяющих исход для новорожденных нами был использован специальный диагностический алгоритм. С этой целью мы применили специфический анализ с построением решающего правила на основе реализованных в программе КВАЗАР (комплекс вычислительных алгоритмов для задач распознавания). Все новорожденные от матерей с СПКЯ были разделены на три группы по перинатальному исходу: I группа - с низкой степенью вероятности развития осложнений, II группа - группа пограничного состояния, III группа - группа с высокой степенью вероятности развития осложнений.
Под ситуацией неблагоприятного перинатального исхода мы подразумевали - ЗВУР, хроническую гипоксию плода, рождение ребенка в асфиксии, с аномалиями развития, с гипотрофией, морфофункциональной незрелостью, отклонениями в неврологическом статусе, нарушения ранней постнатальной адаптации, необходимость перевода ребёнка на второй этап реабилитации.
Итоговый алгоритм прогноза благоприятного (неблагоприятного) исхода конкретного пациента для беременных группы сравнения выглядит следующим образом:
![]()
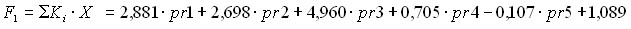 (1),
(1),
где F1 – прогноз по развитию перинатальных осложнений в группе сравнения;
Ki - дискриминантный коэффициент или вес, Xi- предиктор или независимая переменная;
pr1 – проявления тромбофилии в любом сроке беременности;
pr2 - уменьшение концентрации эстриола в крови беременной;
pr3 – активация вирусно-бактериальной инфекции внастоящую беременность
pr4 – неадекватная поддерживающая гормональная терапия в начале беременности;
pr5 –перманентная угроза прерывания беременности.
Если F1< - 0,56, исход благоприятен, Если F1 > 0, исход неблагоприятен, значение F1 находится в интервале от - 0,56 до 0, пациент относится к группе риска (группе пограничного состояния). Чувствительность алгоритма неблагоприятного исхода 90,1%, специфичность 100%, эффективность 96%.
Итоговый алгоритм прогноза благоприятного (неблагоприятного) исхода конкретного пациента для беременных основной группы выглядит следующим образом:
![]()
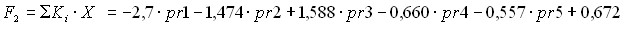 (2),
(2),
где F2 – прогноз по развитию перинатальных осложнений в основной группе;
pr1 – монотонный прирост ХГЧ при завышенном уровне прогестерона;
pr2 – снижение (пороговые) концентрации ТБГ в крови беременной;
pr3 – нарушение маточно-плацентарного кровотока по данным доплерометрии любой степени тяжести в 24 – 32 недели;
pr4 – попытки ЭКО более 5;
pr5 - угрожающий выкидыш с образованием ретрохориальной гематомы.
Если F2 >0,78, то исход должен быть благоприятным. Если F2 < -0,44, высокая вероятность неблагоприятного исхода, F2 в интервале от -0,44 до 0,78, пациент относится к группе пограничного состояния. Чувствительность алгоритма неблагоприятного исхода 93,3%, специфичность 87,9%, эффективность 90%. Уровень значимости отличий совокупности признаков, по которым оценивается исход: р<0,0001.
Разработанная методика пренатального прогноза состояния новорожденных от женщин с СПКЯ в зависимости от метода восстановления фертильности позволила составить прогностический алгоритм наблюдения беременных с СПКЯ и оптимизировать лечебно-профилактические мероприятия по ведению беременности у таких пациенток. Алгоритм представлен на рисунке 4.
Для оценки эффективности разработанного акушерского алгоритма нами был проведен анализ перинатальных исходов у 66 беременных после ЭКО распределенных в 2 группы. Основная группа 1а представлена 33 беременными с СПКЯ. В группе проведен полный комплекс прегравидарной подготовки, клинико–лабораторного обследования и лечения в зависимости от перинатального прогноза, определённого по предложенной формуле. Группа 2а (сравнения) – 33 беременные с рассматриваемой патологией и не прошедших полного курса поэтапной реабилитации без выявления факторов риска перинатальных осложнений и составления прогноза.
Рис. 4. Прогностический алгоритм наблюдения беременных с СПКЯ в пренатальном периоде
При анализе прогностических факторов группа Iа была разделена по прогнозируемым исходам: низкий риск перинатальных осложнений имели 6 (18,8%) беременных, пограничное состояние 18 (54,5%), высокий риск перинатальных осложнений был выявлен у 9 (27,3%) беременных. После проведения беременности по предложенному алгоритму, большинство детей Iа группы родилось в удовлетворительном состоянии 75,8%, в то время, как во IIа группе нормальную оценку по шкале Апгар имели 63,6% детей. Недоношенными родилось 2 (6,1 %) детей Iа группы и 3 (9,1 %) во IIа группе, то есть снижение показателя было в 1,5 раза. Можно отметить, что признаки дизадаптации: патологическая потеря массы тела, нарушения микроциркуляции в 2 и в 2,8 раза реже встречались в Iа группе, неполноценность системы гомеостаза в 2,4 раза реже, а общие симптомы в 1,8 раза. Частота гипотрофии новорождённых в Iа группе была ниже в 1,7 раза, чем во IIа группе. Неонатальная инфекция в Iа группе была представлена только малыми формами, а во II группе малые формы и пневмонии диагностировались одинаково.
Таким образом, анализ полученных нами данных позволяет предполагать, что предложенный нами прогностический алгоритм ведения беременных с СПКЯ и различными видами восстановления фертильности, позволяет улучшить перинатальные исходы в обеих группах примерно одинаково: невынашивания беременности в 1,5 - 2 раза, улучшению неонатальной адаптации и качество здоровья новорожденных, за счет уменьшения выраженности симптомов дизадаптации в 2,2 раза, снизить гипотрофию новорожденных в 1,7 раза.
ВЫВОДЫ
- В результате изучения особенностей течения беременности у пациенток с СПКЯ, выявлен высокий процент осложнений гестации во всех триместрах беременности, среди которых доминируют невынашивание в 63,4%у беременных группы сравнения против 71,4% основной группы (р>0,05), синдром гиперстимуляции яичников в группе сравнения 2,9% против 12 17,7% основной группы (р<0,05), гиперкоагуляция в группе сравнения у 10,1% против 27,1% в основной группе (р<0,05) и раннее развитие плацентарной недостаточности в основной группе в 11,6% против 22,9% в основной группе.
- Исследование состояния фетоплацентарного комплекса выявило: нарушение структуры и расположения плаценты: полное предлежание хориона (плаценты) в групппе сравнения 3 (4,3%), в основной группе 9 (17,1%) (р1,2< 0,05), гипоплазия хориона в группе сравнения составила 4,3%, а в основной группе в 10% случаев (р1,2< 0,05). Установлена прямая корреляционная связь между уровнем ТБГ в материнской крови и внутриутробным состоянием плода в обеих группах (r =0,61, p=0,01), и обратная зависимость между уровнем ТБГ и ИР в артерии пуповины (r =-0,55, p=0,03). Недоношенные дети в основной группе встречались в 1,8 раза чаще, чем в группе сравнения. Рождение детей в состоянии асфиксии тяжелой степени регистрировалось в группе сравнения 3,2% против 9,5% основной группы, гипоксически-ишемическое поражение ЦНС в группе сравнения 14,3% против 31,7 % основной группы.
3. Факторами риска в развитии антенатальных и интранатальных осложнений у беременных группы сравнения явились: проявления тромбофилии в любом сроке беременности (Xi1=0.861); уменьшение концентрации эстриола в крови беременной (Xi2=0.796); активация вирусно-бактериальной инфекции во время настоящей беременности (Xi3=0.620); неадекватная поддерживающая гормональная терапия в начале беременности (Xi4=0.291), перманентная угроза прерывания беременности (Xi4=0.227). Для беременных основной группы факторами риска по развитию перинатальных осложнений стали: монотонный прирост ХГЧ при завышенном уровне прогестерона (Xii1=0.913); уменьшение концентрации ТБГ в крови беременной (Xii2=0.578); нарушение маточно-плацентарного кровотока по данным доплерометрии любой степени тяжести в 24 – 32 недели (Xii3=0.525), попытки ЭКО более 5 (Xii4 =0.232), угрожающий выкидыш с образованием ретрохориальной гематомы (Xii5=0.179). Факторы риска реализованы в решающем правиле прогноза для каждой группы исследования.
4. Факторы риска оказывают неодинаковое влияние на уровень перинатальной смертности и заболеваемости. Это влияние интегративно, т.е. их воздействие не является результатом простого суммирования. На основании выделения факторов перинатального прогнозирования нами предложен дифференцированный прогностический алгоритм наблюдения беременности при СПКЯ.
5. Предложенный нами алгоритм ведения беременности при СПКЯ позволил уменьшить на 40% развитие гипотрофии плода, улучшить неонатальную адаптацию новорожденных на 33%, снизить развитие неонатальной инфекции в 2 раза.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
1. Предложенный прогностический алгоритм ведения беременности у пациенток с СПКЯ, основанный на выделении факторов риска, эффективен в использовании с ранних сроков беременности и рекомендуется для сплошного скрининга беременных с СПКЯ.
2. В комплекс диагностических и лечебных мероприятий при наличии признаков угрожающего выкидыша и нарушения прикрепления хориона включать с ранних сроков необходимо обследование на наличие маркеров генетической тромборфилии, раннее выявление нарушений в свёртывающей системе крови, гормональных маркёров состояния плацентарного комплекса.
3. Для контроля за состоянием защитно-приспособительных механизмов в течение беременности целесообразно контролировать гормональный и инфекционный фон в течении всей беременности с интервалом 2 – 3 недели.
4. Мониторинг по развитию у женщин с СПКЯ гестационного диабета осуществляется совместно акушером-гинекологом и эндокринологом в I половине беременности 1 раз и во II половине 1 раз. При выявлении признаков гестационного диабета 1 раз в 1 – 2 недели.
5. Плановая госпитализация в гинекологическое отделение для пациенток с СПКЯ после ЭКО необходима с момента переноса эмбриона, а лечение в стационаре дневного пребывания рекомендуется в I триместре беременным обеих групп для решения вопроса о тактике ведения беременности, в 16 -18 недель, 20 -24 недели, в 28–30 недель для коррекции плацентарной недостаточности, гестоза, а так же для диагностики, профилактики и лечения осложнений беременности, в 34-36 недель проводится оценка состояния плода и определяется срок и метод родоразрешения.
Список работ, опубликованных по теме
диссертации
- Журавлева Ю.А. Оценка эффективности медикаментозного прерывания неразвивающейся беременности у пациенток с синдромом поликистозных яичников/ Ю.А. Журавлева, М.Ю. Зильбер // Уральский медицинский журнал. Перинатология. – Вып. 10. – Екатеринбург, 2009. – С.175 – 180.
- Журавлева Ю.А. Особенности течения и оценка перинатальных исходов у беременных с синдромом поликистозных яичников в зависимости от методов лечения бесплодия/ Ю.А. Журавлева, М.Ю. Зильбер // Уральский медицинский журнал. Акушерство и гинекология – Вып. 03. – Екатеринбург, 2010. – С.33 – 38.
- Зильбер М.Ю. Превентивная диагностика опухолей и опухолевидных образований яичников в программе ЭКО / М.Ю. Зильбер, С.В. Цыганенко, Ю.А. Журавлёва, Ю.Е. Буев // Уральский медицинский журнал. Онкология. – Вып. 10. – Екатеринбург, 2010
- Журавлева Ю.А. Особенности ведения беременных с овариальной гиперандрогенией неопухолевого генеза (СПКЯ) и генитальной инфекцией в условиях женской консультации/ Ю.А. Журавлева, М.Ю. Зильбер // Материалы III регионального научного форума «Мать и дитя» – Саратов, 2009. – С.100 – 101.
- Журавлева Ю.А. Эффективность оказания амбулаторной помощи беременным с бесплодием в анамнезе в условиях дневного стационара женской консультации./ Л.В. Бунеева, Ю.А. Журавлева, С.С. Анищенко// Сборник тезисов к Всероссийскому конгрессу «Амбулаторно-поликлиническая практика – новые горизонты». – Москва, 2010. – С.56 - 57
- Журавлева Ю.А. Пренатальная диагностика врождённых пороков развития у беременных с синдромом поликистозных яичников./ М.Ю. Зильбер, Ю.А. Журавлева // Сборник тезисов к Всероссийскому конгрессу «Амбулаторно-поликлиническая практика – новые горизонты». – Москва, 2010. – С.115 – 117.
- Журавлева Ю.А. Характеристика течения I триместра беременности у пациенток с синдромом поликистозных яичников// Ю.А. Журавлева, М.Ю. Зильбер// Сборник тезисов к Всероссийскому конгрессу «Амбулаторно-поликлиническая практика – новые горизонты». – Москва, 2010. – С.108 – 109.
- Журавлева Ю.А. Возможности использования медикаментозного прерывания беременности у пациенток с синдромом поликистозных яичников// Ю.А. Журавлева, М.Ю. Зильбер// Сборник тезисов к Всероссийскому конгрессу «Амбулаторно-поликлиническая практика – новые горизонты». – Москва, 2010. – С.109 – 111.
ЖУРАВЛЕВА
Юлия Александровна
ПРОГНОЗИРОВАНИЕ ПЕРИНАТАЛЬНЫХ ИСХОДОВ
ПРИ СИНДРОМЕ ПОЛИКИСТОЗНЫХ ЯИЧНИКОВ В ЗАВИСИМОСТИ ОТ МЕТОДА ВОССТАНОВЛЕНИЯ ФЕРТИЛЬНОСТИ
14.01.01 – акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
_______________________________________________________________________________
Подписано в печать 23.05.2011 г. Формат 60х84 1/16 Усл. печ. л. 1,0. Тираж 100 экз.
Заказ №_52_. Отпечатано в типографии ГОУ ВПО УГМА Росздрава,
г. Екатеринбург, ул. Репина, д. 3.

