Диагностика синдрома множественной эндокринной неоплазии первого типа у больных с органическим гиперинсулинизмом
на правах рукописи
Васильев Иван Алексеевич
Диагностика синдрома множественной эндокринной неоплазии первого типа у больных с органическим гиперинсулинизмом
14.01.17. – хирургия
Автореферат диссертации на соискание ученой степени
кандидата медицинских наук
Москва
2010 г.
Работа выполнена в ГОУ ВПО Первый Московский государственный медицинский университет имени И. М. Сеченова
Научный руководитель:
доктор медицинских наук, профессор Егоров Алексей Викторович
Официальные оппоненты:
доктор медицинских наук, профессор,
член-корреспондент РАМН Кубышкин Валерий Алексеевич
доктор медицинских наук, профессор Дюжева Татьяна Геннадьевна
Ведущая организация
Институт хирургии имени А.В. Вишневского РАМН
Защита диссертации состоится «____»________________2010г.
В 14 часов на заседании Диссертационного совета Д.208.040.03 в ГОУ ВПО Первый Московский государственный медицинский университет имени
И. М. Сеченова (119991, Москва, ул. Трубецкая, д. 8, стр.2).
С диссертацией можно ознакомиться в ГЦНМБ
(117998, Москва, Нахимовский проспект, д. 49).
Автореферат разослан «____»________________2010г.
Ученый секретарь Диссертационного совета,
доктор медицинских наук,
профессор Шулутко Александр Михайлович
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность темы
Органический гиперинсулинизм является нечастым заболеванием и встречается в 2-4 наблюдениях на один миллион населения в год. Чаще всего его причиной является B-клеточная опухоль (инсулинома) поджелудочной железы, которая составляет до 70% всех гормонально-активных опухолей этого органа [Lvy-Bohbot N et al., 2004; Mullan MH et al., 2002; Thakker RV, 2001; Triponez F et al., 2006]. Кроме того, причиной болезни могут быть микроаденоматоз или гиперплазия B-клеток поджелудочной железы (незидиобластоз). Это заболевание в течение 3-5 лет от его начала приводит к тяжелым и часто необратимым изменениям в организме человека, являясь причиной выраженной энцефалопатии и потери трудоспособности. Примерно 15-25% инсулином поджелудочной железы диагностируются в рамках синдрома множественной эндокринной неоплазии 1 типа (МЭН-1 или синдром Вермера) [Кузин Н. М. и соавт., 2000; Doherty GM et al., 2003; Larsson C et al., 1988].
При синдроме МЭН-1 обычно синхронно или последовательно развиваются эндокринно-клеточные гиперпластические процессы и опухоли паращитовидных желез, поджелудочной железы, передней доли гипофиза, гастроинтестинального тракта, реже – тимуса, легких, щитовидной железы, надпочечников, яичников. Выявление МЭН-1 очень важно, так как наличие данного синдрома коренным образом влияет на дальнейшую тактику лечения и прогноз заболевания.
Диагностика синдрома МЭН-1 представляет значительные трудности, что, прежде всего, связано с множественным поражением и частым развитием микроаденом и гиперплазии эндокринной ткани органов мишеней по сравнению со спорадическими опухолями.
Комплексное дооперационное обследование поджелудочной железы позволяет точно локализовать опухоль или зону гиперпродукции инсулина не более чем в 90% наблюдений [Кузин Н. М. и соавт., 1998; Brandi ML, 2000; Gollini P et al., 2004; Langer P et al., 2004].
Лечение больных с синдромом МЭН-1 представляет значительные трудности и обусловлены они, прежде всего, сложностью установления причины того или иного синдрома, вызываемого довольно часто не солитарной опухолью, а микроаденомами и диффузной гиперплазией различных эндокринных желез. Вышеперечисленные особенности поражения эндокринных органов приводят к более высокой частоте развития рецидивов заболевания по сравнению со спорадическими НЭО.
Количество публикаций, посвященных проблеме комплексной диагностики синдрома МЭН-1 в русскоязычной литературе крайне мало [Ильичев В.А., 1997; Казанцева И.А. и соавт., 1999; Кузнецов Н.С. и соавт., 2002], а заболевания органов мишеней этого синдрома зачастую рассматриваются изолировано друг от друга. Развитие нейроэндокринных опухолей в рамках синдрома МЭН-1 требует выполнения более радикальных операций, таких как тотальная паратиреоидэктомия, панкреатэктомия, субтотальная резекция поджелудочной железы и т.д., что в свою очередь может приводить к тяжелым и порою пожизненным осложнениям.
Таким образом, представляется актуальным, разработать наиболее рациональный алгоритм диагностики синдрома МЭН-1 у больных с органическим гиперинсулинизмом, что позволит найти оптимальный вариант лечения этих больных.
Целью работы являлось улучшение диагностики и, как следствия, результатов лечения больных с органическим гиперинсулинизмом в рамках синдрома множественной эндокринной неоплазии первого типа.
Для этого нами были поставлены следующие задачи:
- Оценить особенности клинической картины у больных с органическим гиперинсулинизмом в рамках синдрома МЭН-1.
- Определить возможности лабораторной диагностики поражения поджелудочной железы, паращитовидных желез и гипофиза у пациентов с синдромом МЭН-1.
- Оценить возможности различных способов топической диагностики поражения поджелудочной железы, паращитовидных желез и гипофиза у пациентов с синдромом МЭН-1.
- Определить порядок проведения интраоперационной ревизии у пациентов с органическим гиперинсулинизмом в рамках синдрома МЭН-1.
- Разработать алгоритм диагностического поиска у больных с органическим гиперинсулинизмом в рамках синдрома множественной эндокринной неоплазии первого типа.
Научная новизна.
- Оценены различия в клиническом течении гипогликемической болезни при синдроме множественной эндокринной неоплазии первого типа и спорадических инсулиномах.
- Определена чувствительность методов лабораторной диагностики при поражении поджелудочной, паращитовидных желез и гипофиза в рамках синдрома множественной эндокринной неоплазии первого типа.
- Определена чувствительность методов топической диагностики при поражении поджелудочной, паращитовидных желез и гипофиза в рамках синдрома множественной эндокринной неоплазии первого типа.
- Обоснован и разработан алгоритм диагностики синдрома множественной эндокринной неоплазии первого типа у пациентов с органическим гиперинсулинизмом.
- Выявлены особенности интраоперационной ревизии у пациентов с органическим гиперинсулинизмом в рамках синдрома МЭН-1, влияющие на объем оперативного вмешательства.
Практическая значимость.
Оценка клинических проявлений, определение и сравнительный анализ чувствительности различных методов лабораторной и топической диагностики позволили разработать алгоритм диагностики синдрома МЭН-1 у больных с органическим гиперинсулинизмом. Применение данного алгоритма позволило значительно увеличить выявляемость синдрома множественной эндокринной неоплазии среди пациентов с органическим гиперинсулинизмом и определить последовательность и объем хирургического лечения.
Основные положения, выносимые на защиту.
- Существенных клинических отличий гипогликемической болезни при синдроме МЭН-1 и при спорадических инсулиномах нет. В ряде наблюдений при множественной эндокринной неоплазии возможны жалобы со стороны других эндокринных органов, вовлеченных в патологический процесс, что может существенно облегчить выявление синдрома МЭН-1.
- Повышение в периферической крови уровня ИРИ и С-пептида среди больных с синдромом МЭН-1 и без него сопоставимо между собой. В связи с преобладанием нефункционирующих опухолей гипофиза чувствительность исследования гормонального профиля низка. В случае развития первичного гиперпаратиреоза у подавляющего большинства пациентов определяется нормокальциемия.
- При топической диагностике инсулином чувствительность наиболее ценного неинвазивного метода – ЭндоУЗИ ниже при синдроме МЭН-1 в сравнении со спорадическими опухолями. Сочетанное ангиографическое исследование – это единственный метод дооперационной диагностики, позволяющий выявить не только опухоли, но и очаги микроаденоматоза и незидиобластоза. При интраоперационной ревизии обязательным является использование ИОУЗИ.
- Для топической диагностики поражения паращитовидных желез в рамках синдрома МЭН-1 наиболее простым методом является УЗИ, а сочетание со сцинтиграфией позволяет в большинстве случаев выявить изменения со стороны паращитовидных желез.
- Для топической диагностики опухолей гипофиза наиболее информативным методом диагностики, учитывая высокую частоту гормонально-неактивных аденом, является МРТ с внутривенным контрастированием.
- Диагностический алгоритм синдрома МЭН-1 у больных с органическим гиперинсулинизмом должен включать в себя изучение семейного анамнеза, гормональные и топические методы диагностики поджелудочной и паращитовидных желез и гипофиза.
Реализация результатов работы. Основные положения работы внедрены, используются и развиваются в клинике факультетской хирургии им. Н. Н. Бурденко ММА имени И.М. Сеченова.
Апробация работы. Материалы диссертации были представлены и обсуждены на заседании научной конференции кафедры факультетской хирургии N 1 лечебного факультета ММА им. И. М. Сеченова; на XVI Российском симпозиуме по хирургической эндокринологии «Современные аспекты хирургической эндокринологии» (Саранск, 2007г.); на 5-ой ежегодной конференции Европейского общества по диагностике и лечению нейроэндокринных опухолей (5th Annual ENETS Conference for the Diagnosis and Treatment of Neuroendocrine Tumor Disease, Paris 2008).
Публикации. По теме работы опубликовано 14 печатных работ, 4 из них – в центральной печати.
Объем и структура работы. Работа изложена на 112 страницах машинописного текста, состоит из введения, 5 глав, выводов, практических рекомендаций, списка литературы, в котором 45 отечественных и 71 зарубежный источник, иллюстрирована 5 таблицами, 18 рисунками.
ОБЩАЯ ХАРАКТЕРИСТИКА ПАЦИЕНТОВ И МЕТОДОВ ИССЛЕДОВАНИЯ
В основу работы положены данные о 130 больных с органическим гиперинсулинизмом, обследованных в клинике факультетской хирургии им. Н.Н. Бурденко за период с 1994 по 2009 год. Среди 130 пациентов женщин было 93 (72%) и 37 мужчин (28%). Все больные были оперированы и диагноз подтвержден при интраоперационной ревизии, включающей в себя ИОУЗИ и пальпацию поджелудочной железы, а также при морфологическом исследовании удаленного макропрепарата. У 33 из этих пациентов был выявлен синдром множественной эндокринной неоплазии первого типа. По этому критерию пациенты были разделены на две группы:
- больные со спорадическим синдромом органического гиперинсулинизма;
- пациенты с инсулиномой в рамках синдрома множественной эндокринной неоплазии первого типа.
В первой группе было 97 больных, среди которых 68 женщин (70%) и 29 мужчин (30%). Среди больных с синдромом МЭН-1 было 8 мужчин (24%) и 25 женщин (76%). Средний возраст в обеих группах сопоставим и составил 45±14 лет. Частота поражения эндокринных желез в группе больных с синдромом МЭН-1 представлена в таблице №1. Также у 4 пациентов из данной группы диагностирована аденома надпочечника, у одной пациентки – карциноидная опухоль сигмовидной кишки. В 3 наблюдениях синдром МЭН-1 сочетался с аденокарциномой желудочно-кишечного тракта различной локализации.
Таблица №1 Частота поражения эндокринных желез в группе пациентов с синдромом МЭН-1.
| Частота поражения | Гипофиз | Паращитовидные железы | Поджелудочная железа |
| Относительная | 61% | 70% | 100% |
| Абсолютная | 20 | 23 | 33 |
Среди 20 больных с новообразованиями гипофиза у 13 выявлена нефункционирующая микроаденома, у 4 – пролактинома и у 3 – АКТГ-секретирующая опухоль.
В 23 наблюдениях был диагностирован первичный гиперпаратиреоз, причиной которого у 18 человек являлись аденомы, а у 5 – гиперплазия паращитовидных желез. Множественные поражения встречались у 7 пациентов (30%).
У пациентов с синдромом МЭН-1 в поджелудочной железе наряду с инсулиномами наблюдались и другие нейроэндокринные опухоли. Так у 130 больных было выявлено 163 опухоли, из них – 147 инсулином, 6 опухолей со смешанной секрецией инсулина и гастрина, 5 глюкагоном и 5 нефункционирующих опухолей поджелудочной железы.
Локализация нейроэндокринных опухолей поджелудочной железы при спорадических случаях и синдроме МЭН-1 не имела существенных отличий и представлена в таблице № 2. В то время как множественные опухоли при синдроме МЭН-1 (24%) обнаруживались значительно чаще, чем при спорадических инсулиномах (5%). При множественном поражении поджелудочной железы в рамках синдрома МЭН-1 выявляли от 2 до 6 опухолей, в случае спорадического органического гиперинсулинизма более 2 опухолей выявлено не было. Частота незидиобластоза среди пациентов со спорадическими опухолями составила 6%. В то время как изолированный незидиобластоз во второй группе больных выявлен в 30% наблюдений, а в сочетании с аденомами – у всех пациентов второй группы. Средние размеры спорадических инсулином составили 16,2±5 мм в диаметре, что существенно не отличалось от таковых у пациентов с синдромом МЭН-1 (15,4±5 мм в диаметре). Согласно данным литературы для синдрома МЭН-1 характерно образование микроаденом, среди обследованных нами больных у четырех пациентов (12%) имелись микроаденомы поджелудочной железы. В группе пациентов со спорадическими инсулиномами микроаденомы поджелудочной железы выявлены только в трех случаях (3%), что достоверно ниже, чем при синдроме МЭН-1.
Таблица №2 Локализация НЭО при МЭН-1 и спорадических опухолях.
| N | головка | тело | хвост | |
| Спорадическая инсулинома | 103 | 36% (37) | 32% (33) | 32% (33) |
| МЭН-1 | 60 | 30% (18) | 28% (17) | 42% (25) |
Обследование больных с органическим гиперинсулинизмом включало в себя: клиническое обследование пациента; проведение пробы с голоданием; исследование гормонального профиля (АКТГ, пролактин, паратгормон, ИРИ, С-пептид, гастрин). Также использовали следующие инструментальные методы исследования: ультразвуковое исследование, компьютерная томография органов брюшной полости, ангиографическое исследование в сочетании с забором проб крови после внутриартериальной стимуляции (АСЗК); сцинтиграфию паращитовидных желез, МРТ головного мозга.
Интраоперационная ревизия поджелудочной железы. Интраоперационно в обязательном порядке проводили визуальную и пальпаторную ревизию поджелудочной железы, а также ИОУЗИ. Целью УЗИ явилось определение опухоли в ткани поджелудочной железы, а при подозрении на гиперплазию -клеток или микроаденоматоз наоборот – исключение очагового образования поджелудочной железы. При обнаружении инсулиномы определяли глубину ее расположения, расстояние от передней и задней поверхности поджелудочной железы, соотношение с панкреатическим протоком, крупными артериями и венами.
Ревизию выполняли в следующем порядке:
1. Для доступа к поджелудочной железе широко вскрывали сальниковую сумку путем пересечения и перевязывания желудочно-ободочной связки вплоть до коротких желудочных артерий (а при необходимости с пересечением одной или двух из них).
2. Производили визуальную и пальпаторную оценку передней поверхности поджелудочной железы. Если опухоль не удавалось обнаружить, а при дооперационном обследовании было подозрение на ее локализацию в области хвоста и тела, то переходили к третьему этапу.
3. Рассекали заднюю париетальную брюшину, частично мобилизовали тело и хвост поджелудочной железы. При одновременной пальпации как передней, так и задней ее поверхности, возможно определить образования, находящиеся в толще ткани железы.
4. Выполняли пальпацию и осмотр головки поджелудочной железы после ее мобилизации по Кохеру для выявления новообразований. Если на основании ревизии и предоперационного обследования не было данных за опухоль в головке поджелудочной железы, а в дистальном отделе обнаруживалась инсулинома, то на этом ревизию заканчивали.
5. В противном случае полностью мобилизовали двенадцатиперстную кишку с головкой поджелудочной железы путем отделения головки поджелудочной железы от полой вены и мобилизации нижней горизонтальной ветви кишки до дуоденоеюнального перехода. Проводили пальпацию поджелудочной железы.
По нашему мнению, такой порядок проведения ревизии органов брюшной полости с наибольшей вероятностью позволяет выявить инсулиному. В настоящее время при отсутствии данных за синдром МЭН-1 и четком топическом диагнозе, установленном на дооперационном этапе ревизию производили по короткой схеме. Отличие от вышеуказанного алгоритма заключается в том, что для снижения операционной травмы мы ограничивались мобилизацией того участка поджелудочной железы, где при дооперационном обследовании выявлялась опухоль, а остальные отделы осматривались при ИОУЗИ с расположением датчика на передней поверхности поджелудочной железы.
Визуальная и пальпаторная ревизия паращитовидных желез
Оперировано 7 больных, интраоперационно в обязательном порядке проводили визуальную и пальпаторную ревизию щитовидной железы, а также ИОУЗИ.
У всех оперированных в качестве операционного доступа мы использовали воротникообразный разрез по Кохеру в нижней трети шеи. Претиреоидные мышцы отводили тупым способом, после чего мобилизовали обе доли щитовидной железы с последующей их ревизией и пальпацией. Для выявления верхних паращитовидных желез выполняли ревизию верхней и средней трети щитовидной железы, ее заднемедиальной поверхности и щитовидно-трахеальной борозды, выше места проникновения возвратного нерва в гортань. В случае атипичного расположения верхних паращитовидных желез проводили ревизию ткани щитовидной железы, заднего средостения, по ходу верхних щитовидных артерий, или латерально и сзади от пищевода. Для выявления нижних паращитовидных желез выполняли ревизию боковой и задней поверхности нижнего полюса щитовидной железы, яремной ямки, по ходу сонной артерии в области каротидной бифуркации, перед трахеей, тиротимической связки.
Ревизию и пальпацию сочетали с ИОУЗИ, которое выполняли до полной мобилизации с целью уменьшения травматизации. Учитывая множественный характер поражения, проводили ревизию всех паращитовидных желез. К сожалению, срочное гистологическое исследование и экспресс определение уровня паратгормона крови мы не могли выполнить по техническим причинам.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Среди всех больных с органическим гиперинсулинизмом первым этапом, как правило, диагностировали поражение поджелудочной железы, далее считали необходимым проведение обследования на предмет синдрома МЭН-1.
К сожалению, до последнего времени в России проведение кариотипирования не было возможно, в связи с этим основная роль в диагностике должна отводиться исследованию гормонального профиля и различным видам лучевой диагностики. Для выявления синдрома МЭН-1 необходимо изучение клинической картины, анамнеза, комплексное лабораторное и топическое обследование паращитовидных желез, гипофиза и поджелудочной железы на предмет выявления неоплазии. Также морфологическое изучение операционного материала позволяет выявить такие признаки как микроаденоматоз и незидиобластоз окружающей ткани, что позволяет ретроспективно заподозрить синдром МЭН-1 у больного.
Изучение семейного анамнеза позволило лишь у двух пациентов заподозрить синдром МЭН-1. Тем не менее, мы считаем тщательное изучение семейного анамнеза обязательным компонентом расспроса любого больного с нейроэндокринными опухолями.
При сравнении клинических проявлений органического гиперинсулинизма в двух группах следует отметить, что энцефалопатический синдром встречался чаще на 10%, а ожирение III-IV степени – на 20%, что связано с более поздней диагностикой заболевания и, как следствие, длительным анамнезом заболевания (в 1,5 раза) среди этих больных.
При множественной эндокринной неоплазии возможны жалобы со стороны других эндокринных органов, вовлеченных в патологический процесс, что может существенно облегчить диагностику данного синдрома. В обследованной группе больных с синдромом МЭН-1 при комплексном обследовании удалось выявить изменения, связанные с поражением паращитовидных желез и гипофиза только у 6 пациентов (18%). То есть поражения органов мишеней данного синдрома в большинстве наблюдений протекали субклинически, либо развивалось метахронно, что усложняло диагностику синдрома МЭН-1 и требовало длительного динамического наблюдения после хирургического лечения, во время которого выявляли признаки синдрома МЭН-1.
При подозрении на органический гиперинсулинизм всем больным проводили пробу с голоданием для исключения других причин гипогликемических состояний. Информативность этой функциональной пробы составила 98,5%, что подтверждает данные других авторов [Майстренко Н.А. 2004, Modlin IM et al. 2007]. Параллельно с проведением пробы для установления органического гиперинсулинизма, мы исследовали гормональный профиль для выявления поражения органов мишеней синдрома МЭН-1.
Низкую чувствительность лабораторной диагностики, которая составила лишь 35%, обусловило преобладание нефункционирующих микроаденом гипофиза среди обследованных нами больных.
У подавляющего большинства пациентов с первичным гиперпаратиреозом отмечалась нормокальциемия и как следствие этого – субклиническое течение заболевания. Данная группа больных является наиболее трудной для выявления и неоднозначной в плане тактики лечения первичного гиперпаратиреоза [Clerichi T. et al. 2004, Lee CH et al., 2006].
Среди обследованных пациентов с НЭО поджелудочной железы повышение уровня ИРИ в периферической крови выявлено в 55%, а С-пептида – в 71% наблюдений, что достоверно не отличалось в обеих группах больных. Полученные данные соответствуют литературным, согласно которым чувствительность определения гормонального профиля составляет 60-90% [Кузин Н.М. и соавт., 2001; Майстренко Н.А. 2004; Nesje LB et al., 2002; Oberg K et al., 1998].
Повышение хромогранина А определяется практически при всех нейроэндокринных новообразованиях и более чем в 75 % случаев послеоперационных рецидивов, также важным свойством хромогранина А является корреляция повышения его уровня с ростом опухоли [Barakat MT et al., 2004; Brandi ML et al., 2001; Modlin IM et al. 2007]. Следует подчеркнуть значение этого маркера нейроэндокринных опухолей, несмотря на небольшое количество измерений (2 наблюдения).
Таким образом, общей чертой поражения эндокринных желез при синдроме МЭН-1 является преобладание бессимптомных или субклинических форм заболевания.
В большинстве случаев на первый план в лечении пациентов с нейроэндокринными заболеваниями выходит хирургическое удаление опухоли или участка гиперплазии ткани железы. В связи с этим значительную роль в определении хирургической тактики лечения играет топическая диагностика.
Чувствительность сцинтиграфии и УЗИ паращитовидных желез, по нашим данным, составила соответственно 61 и 79%, что соответствует литературным данным, согласно которым информативность сцинтиграфии паращитовидных желез составляет 55-65%, а УЗИ – 55-85% [Черенько С.М. и соавт., 2003; Шидловский В.А., 2003]. Комплексное применение этих исследований позволило повысить частоту выявления изменений со стороны паращитовидных желез до 87%. В связи преобладанием гиперплазии и неполным выявлением аденом на дооперационном этапе, значительную роль приобретает интраоперационная ревизия, которая включает не только осмотр и пальпацию, но и выполнение ИОУЗИ. Применение ИОУЗИ позволяет облегчить поиск паращитовидных желез и их аденом во время операции, сокращая время вмешательства, травму в связи с излишней мобилизацией и, как следствие, частоту интраоперационных осложнений, связанных с повреждением возвратного гортанного нерва. В связи с этим пальпаторную ревизию мы выполняли после ИОУЗИ.
Наиболее чувствительным методом топической диагностики аденом гипофиза по литературным данным является МРТ с контрастным усилением [Brandi ML et al., 2001; Vergs B et al., 2002]. С помощью МРТ мы выявили аденому гипофиза у 18 из 20 пациентов с поражением гипофиза, у остальных диагноз был поставлен на основании выполненной КТ, МРТ этим пациентом не выполнили по техническим причинам. У 19 больных была выявлена микроаденома и лишь у одного пациента – аденома гипофиза размерами до 2,5 см.
Таким образом, учитывая высокую частоту бессимптомных микроаденом гипофиза, основная роль при диагностике должна отводиться инструментальным методам.
Не меньше трудностей, несмотря на яркую клиническую симптоматику, возникало при топической диагностике нейроэндокринных опухолей поджелудочной железы в рамках синдрома МЭН-1. Чувствительность инструментальных методов диагностики НЭО поджелудочной железы среди обеих групп пациентов в сравнении с данными литературы представлена в таблице №3.
Таблица №3. Чувствительность инструментальных методов диагностики НЭО поджелудочной железы.
| Вид исследования | Синдром МЭН-1 | Данные литературы* | |
| есть | нет | ||
| УЗИ | 45,5% | 62% | 40-60% |
| КТ с в/в контр. | 48% | 58% | 50-80% |
| ЭндоУЗИ | 68% | 85% | 80-90% |
| Ангиография | 81% | 80% | 70-85% |
| АСЗК | 97% | 87% | 85-95% |
| Ангиография+ АСЗК | 97% | 91% | 90-96% |
| Пальпация | 91% | 90% | 40-85% |
| ИОУЗИ | 91% | 97% | 95-100% |
* Jensen RT, 2006; Karges W et al., 2002; Langer P et al., 2004; Chen X et al., 2002.
Наиболее информативным неинвазивным методом топической диагностики НЭО поджелудочной железы является ЭндоУЗИ. Этот метод позволяет выявить опухоли в головке и теле поджелудочной железы размером менее 10 мм. Сочетанное ангиографическое исследование является высокочувствительным методом, диагностические возможности которого зависят не от размеров опухоли, а от ее гормональной активности. Данное преимущество трудно переоценить, учитывая частоту микроаденом и незидиобластоза при синдроме МЭН-1. Комплексное применение интраоперационной пальпации и ИОУЗИ позволило повысить чувствительность интраоперационной ревизии до 94%.
В заключение следует отметить, что клиническая картина органического гиперинсулинизма не позволяет дифференцировать спорадический случай от инсулиномы в рамках синдрома МЭН-1. В связи с этим наиболее рациональным является алгоритм диагностики синдрома множественной эндокринной неоплазии 1 типа у пациентов с органическим гиперинсулинизмом, представленный на рисунке 1.
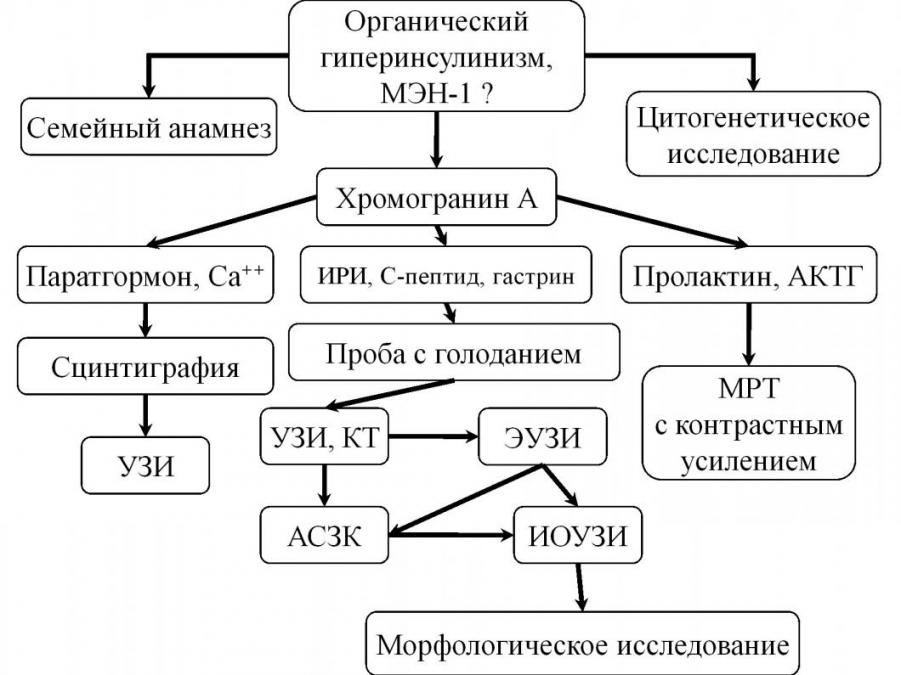
Рисунок 1. Алгоритм диагностики синдрома МЭН-1 у больных с органическим гиперинсулинизмом.
Таким образом, комплексное обследование пациентов с НЭО поджелудочной железы с целью выявления синдрома МЭН-1 позволяет диагностировать на более раннем этапе и, следовательно, своевременно выполнять оперативные вмешательства, когда клинические проявления гормональной гиперпродукции не успели развиться и вызвать характерные осложнения. Основным методом лечения нейроэндокринных опухолей является хирургический, причем подходы к определению оперативной тактики отличаются в зависимости от того является новообразование спорадическим или развилось в рамках синдрома МЭН-1. Так как для МЭН характерно возникновение множественных опухолей и незидиобластоза поджелудочной железы, предпочтение отдается обширным резекционным вмешательствам.
Однако при точной дооперационном топическом диагнозе возможно выполнение органосберегающих операций (энуклеаций и экономных резекций). Данный факт справедлив и в плане поражения паращитовидных желез. Если при спорадической аденоме ее удаление является адекватным объемом операции, то высокая частота рецидива в случае синдрома МЭН-1 вынуждает выполнять субтотальное удаление паращитовидных желез или тотальное удаление с аутотрансплантацией. В связи с длительным течением и медленным развитием заболевания специалисты имеют больше времени для установления диагноза и лечения, что обуславливает более благоприятный прогноз при синдроме МЭН-1, однако, частота развития рецидивов заболевания выше у больных с наследственной этиологией заболевания [Barakat MT et al., 2004; Busygina V et al., 2006; Jensen RT et al., 2008].
Применение вышеописанного алгоритма выявления синдрома МЭН-1 у пациентов с органическим гиперинсулинизмом, позволило увеличить выявляемость синдрома множественной эндокринной неоплазии среди пациентов с органическим гиперинсулинизмом с 2% до 25% за период с 1994 по 2009 годы.
Выводы:
- Существенных клинических отличий гипогликемической болезни в рамках синдрома МЭН-1 и спорадической инсулиномы не выявлено. Однако при синдроме МЭН-1 гипогликемическая болезнь чаще сопровождалась развитием энцефалопатии и ожирения III-IV степени (на 10 и 20% соответственно).
- Чувствительность определения ИРИ и С-пептида при органическом гиперинсулинизме в рамках синдрома МЭН-1 и при спорадической форме заболевания существенно не отличалось, и составила 55% и 71% соответственно.
- Заподозрить аденому гипофиза на основании исследования пролактина и АКТГ крови удалось лишь в 35%.
- Для синдрома МЭН-1 при гиперпаратиреозе характерна в 96% нормокальциемия.
- В дооперационной топической диагностике инсулином наиболее ценным методом является сочетанное ангиографическое исследование, чувствительность которого составляет 97%. Чувствительность ЭндоУЗИ и ИОУЗИ ниже при синдроме МЭН-1 и составляет соответственно 68% и 91%.
- Сочетание УЗИ (чувствительность 61%) и сцинтиграфии паращитовидных желез (чувствительность 79%) позволяет выявить опухоль или гиперплазию в 87% наблюдений.
- Для топической диагностики опухолей гипофиза наиболее информативным методом диагностики является МРТ с внутривенным контрастированием.
- Алгоритм диагностики синдрома МЭН-1 у больных с органическим гиперинсулинизмом, включающий изучение семейного анамнеза, гормональные и топические методы диагностики, позволил увеличить выявляемость синдрома множественной эндокринной неоплазии среди пациентов с органическим гиперинсулинизмом с 2% до 25%.
- Интраоперационная ревизия поджелудочной железы у пациентов с синдромом МЭН-1, включающая обязательную полную мобилизацию органа до выполнения ИОУЗИ, повысила ее чувствительность с 91% до 94%.
Практические рекомендации:
- Для диагностики синдрома множественной эндокринной неоплазии 1 типа у больных с органическим гиперинсулинизмом необходимо использование диагностического алгоритма, включающего в себя изучение семейного анамнеза, клинической картины и методов гормональной и топической диагностики.
- При оценке клинической картины необходимо учитывать заболевания эндокринных органов у родственников и степень выраженности энцефалопатии и ожирения.
- Из гормональных методов исследования необходимо изучать уровень иммунореактивного инсулина, С-пептида, гастрина, паратгормона, АКТГ и пролактина.
- Топическую диагностику опухолей поджелудочной железы необходимо начинать с ультразвукового исследования (УЗИ, ЭндоУЗИ), при подозрении на синдром МЭН-1 целесообразно проведение сочетанного ангиографического исследования.
- Для топической диагностики опухолей и гиперплазии паращитовидных желез целесообразно использование сочетания УЗИ и сцинтиграфии паращитовидных желез.
- МРТ с внутривенным контрастированием является методом выбора в диагностике опухолей гипофиза.
- Во время интраоперационной ревизии паращитовидных желез обязательно обследование всех паращитовидных желез, верхних рогов тимуса с интраоперационным УЗИ.
- При синдроме множественной эндокринной неоплазии 1 типа во время операции на поджелудочной железе перед интраоперационным УЗИ необходим тщательный осмотр и пальпация всех ее отделов.
- Разработанный алгоритм рекомендован к применению в специализированных стационарах хирургического профиля.
Список печатных работ по теме диссертации
- Васильев И.А. Диагностика синдрома множественной эндокринной неоплазии первого типа у больных с органическим гиперинсулинизмом. Анналы ФПНПК, т. XII. – М., 2006г., С 10.
- Егоров А.В., Кузин Н.М., Кондрашин С.А., Лотов А.Н., Гуревич Л.Е., Васильев И.А., Майорова Е.М., Анисимова О.В. Лечение синдрома множественной эндокринной неоплазии 1 типа (синдром Вермера). Материалы XVI российского симпозиума по хирургической эндокринологии «Современные аспекты хирургической эндокринологии». – Саранск, 2007г., С 84-86.
- Егоров А.В., Кашеваров С.Б., Лотов А.Н., Гузнов И.Г., Гуревич Л.Е., Парнова В.А., Васильев И.А., Вычужанин Д.В. Клиническое наблюдение: первый опыт лапароскопической энуклеации инсулиномы поджелудочной железы в России. Материалы XVI российского симпозиума по хирургической эндокринологии «Современные аспекты хирургической эндокринологии». – Саранск, 2007г., С 82-84.
- Кондрашин С.А., Егоров А.В., Ипполитов Л.И., Волков Р.Ю., Рабинович Э.З., Васильев И.А. Использование аналогов соматостатина для диагностики и лечения нейроэндокринных опухолей. Материалы XVI российского симпозиума по хирургической эндокринологии «Современные аспекты хирургической эндокринологии». – Саранск, 2007г., С 118-120.
- Черноусов А.Ф., Егоров А.В., Кондрашин С.А., Лотов А.Н., Васильев И.А., Парнова В.А., Гуревич Л.Е. Диагностика и лечение гастринпродуцирующих опухолей и синдрома Золлингера-Эллисона. Вестник хирургической гастроэнтерологии №3, 2007г., С 17-26.
- Егоров А.В., Кузнецов Н.С., Кондрашин С.А., Лотов А.Н., Силина Т.Ю., Анисимова О.В., Васильев И.А. Современные подходы к диагностике нейроэндокринных опухолей поджелудочной железы. Вестник хирургической гастроэнтерологии №3, 2007г., С 60.
- Egorov A.V., Kuzin N.M., Kondrashin S.A., Lotov A.N., Gurevich L.E., Vasiliev I.A., Majorova E.M., Anisimova O.V. Treatment of patients with multiple endocrine neoplasia type I. Abstracts of the 5th annual ENETS conference for the diagnosis and treatment of neuroendocrine tumor disease, Paris 2008.
- Егоров А.В., Кондрашин С.А., Лотов А.Н., Мусаев Г.Х., Орлов С.Ю., Силина Т.Ю., Васильев И.А., Майорова Е.М. Диагностика синдрома множественной эндокринной неоплазии 1 типа у пациентов с нейроэндокринными опухолями поджелудочной железы. Анналы хирургии 2009 г., №1, С. 44-48.
- Егоров А.В., Васильев И.А. Диагностика и лечение нейроэндокринных опухолей органов брюшной полости и забрюшинного пространства (обзор литературы). Фарматека 2009, №2, С.23-27.
- Трошина Е.А., Юкина М.Ю., Егоров А.В., Васильев И.А., Кривко А.А., Васильева А.Г. Злокачественная инсулинома. Проблемы эндокринологии 2009, №5 Т. 55, С. 10-14.
- Егоров А.В., Кондрашин С.А., Фоминых Е.В., Мусаев Г.Х., Гитель Е.П., Гуревич Л.Е., Парнова В.А., Васильев И.А., Рабинович Э.З., Волков Р.Ю. Аналоги соматостатина в диагностике и лечении нейроэндокринных опухолей. Анналы хирургической гепатологии, 2009 г., том 14 № 4, С. 71-78.
- A.V.Egorov, S.A.Kondrashin, G.H.Musaev, L.E.Gurevich, I.A.Vasilev, O.V.Anisimova, V.A.Parnova, E.A.Askenderova 20-years experience in diagnosis and treatment of insulinoma in Burdenko Surgery Clinic. Abstracts of the 7th Annual ENETS Conference for the Diagnosis and Treatment of Neuroendocrine Tumor Disease, Berlin 2010. P. 16.
- Guervich LE, Egorov A.V., Askenderova E.O., Kubyshkin V.A., Kochatkov A.V., Vasiliev I.A., Kondrashin S.A. Multiple tumours in patients with pancreatic neuroendocrine tumours: morphological and immunohistochemical characteristics. Abstracts of the 7th Annual ENETS Conference for the Diagnosis and Treatment of Neuroendocrine Tumor Disease, Berlin 2010. P. 18.
- Silina T, Gurevich L, Britvin T, Eyznetcov N, Krivko A, Melikian M, Vasiliev I, Orlov S, Stepanov A, Averianova J. Endoscopic ultrasound of 66 insulinomas. Abstracts of the 7th Annual ENETS Conference for the Diagnosis and Treatment of Neuroendocrine Tumor Disease, Berlin 2010. P. 132.
Для заметок

